Année : 2020 Thèse N° : 36
CANCER EN OFFICINE
PRISE EN CHARGE DES PATIENTS SOUS
THERAPIES CIBLEES
Thèse
PAR
Madame Meriem BAYOUMI
Docteur en Pharmacie
MOTS CLES : Cancer, Thérapies ciblées, Expertise pharmaceutique, Observance
RABAT
Monsieur Abdelkader BELMEKKI Président
Professeur d’Hématologie biologique
Monsieur Mohammed CHAKOUR Rapporteur
Professeur d’hématologie
Monsieur Abdellah DAMI Juge
Professeur de biochimie
Monsieur Anass JEAÏDI Juge
Professeur d’Hématologie Biologique
* Enseignants Militaires
ET DE PHARMACIE DOYENS HONORAIRES :
1962 - 1969 : Professeur_Abdelmalek FARAJ 1969 - 1974 : Professeur Abdellatif BERBICH 1974 - 1981 : Professeur Bachir LAZRAK 1981 - 1989 : Professeur Taieb CHKILI
1989 - 1997 : Professeur Mohamed Tahar ALAOUI 1997 - 2003 : Professeur Abdelmajid BELMAHI 2003 - 2013 : Professeur Najia HAJJAJ - HASSOUNI
ADMINISTRATION : Doyen
Professeur Mohamed ADNAOUI
Vice Doyen chargé des Affaires Académiques et estudiantines Professeur Brahim LEKEHAL
Vice Doyen charge de la Recherche et de la Coopé ration Professeur Toufiq DAKKA
Vice-Doyen chargé des Affaires Spécifiques à la Pharmacie Professeur Younes RAHALI
Secrétaire Général : Mr. Mohamed KARRA
Décembre 1984
Pr. MAAOUNI Abdelaziz Médecine Interne - Clinique Royale Pr. MAAZOUZI Ahmed Wajdi Anesthésie –Réanimation
Pr. SETTAF Abdellatif Pathologie Chirurgicale
Janvier, Février et Décembre 1987
Pr. LACHKAR Hassan Médecine Interne
Décembre 1988
Pr. DAFIRI Rachida Radiologie
Décembre 1989
Pr. ADNAOUI Mohamed Médecine Interne -Doyen de la FMPR Pr. OUAZZANI Taibi Mohamed Réda Neurologie
Janvier et Novembre 1990
Pr. KHARBACH Aicha Gynécologie Obstétrique
Pr. TAZI Saoud Anas Anesthésie Réanimation
Février Avril Juillet et Décembre 1991
Pr. AZZOUZI Abderrahim Anesthésie Réanimation- Doyen de FMPO
Pr. BAYAHIA Rabéa Néphrologie
Pr. BELKOUCHI Abdelkader Chirurgie Générale
Pr. BENCHEKROUN Belabbes Abdellatif Chirurgie Générale
Pr. BENSOUDA Yahia Pharmacie galénique
Pr. BERRAHO Amina Ophtalmologie
Pr. BEZAD Rachid Gynécologie Obstétrique Méd. Chef Maternité des Orangers
Pr. CHERRAH Yahia Pharmacologie
Pr. CHOKAIRI Omar Histologie Embryologie
Pr. KHATTAB Mohamed Pédiatrie
Pr. SOULAYMANI Rachida Pharmacologie- Dir. du Centre National PV Rabat
Pr. TAOUFIK Jamal Chimie thérapeutique
Décembre 1992
Pr. AHALLAT Mohamed Chirurgie Générale Doyen de FMPT
Pr. BENSOUDA Adil Anesthésie Réanimation
Pr. CHAHED OUAZZANI Laaziza Gastro-Entérologie
Pr. CHRAIBI Chafiq Gynécologie Obstétrique
Pr. EL OUAHABI Abdessamad Neurochirurgie
Pr. FELLAT Rokaya Cardiologie
Pr. JIDDANE Mohamed Anatomie
Pr. TAGHY Ahmed Chirurgie Générale
Pr. ZOUHDI Mimoun Microbiologie
ue
* Enseignants Militaires
FMPA
Pr. EL AMRANI Sabah Gynécologie Obstétrique Pr. EL BARDOUNI Ahmed Traumato-Orthopédie Pr. EL HASSANI My Rachid Radiologie
Pr. ERROUGANI Abdelkader Chirurgie Générale - Directeur du CHIS
Pr. ESSAKALI Malika Immunologie
Pr. ETTAYEBI Fouad Chirurgie Pédiatrique
Pr. IFRINE Lahssan Chirurgie Générale
Pr. MAHFOUD Mustapha Traumatologie - Orthopédie
Pr. RHRAB Brahim Gynécologie -Obstétrique
Pr. ŞENOUCI Karima Dermatologie
Mars 1994
Pr. ABBAR Mohamed* Urologie Inspecteur du SSM
Pr. BENTAHILA Abdelali Pédiatrie
Pr. BERRADA Mohamed Saleh Traumatologie - Orthopédie Pr. CHERKAOUI Lalla Ouafae Ophtalmologie
Pr. LAKHDAR Amina Gynécologie Obstétrique
Pr. MOUANE Nezha Pédiatrie
Mars 1995
Pr. ABOUQUAL Redouane Réanimation Médicale
Pr. AMRAOUI Mohamed Chirurgie Générale
Pr. BAIDADA Abdelaziz Gynécologie Obstétrique
Pr. BARGACH Samir Gynécologie Obstétrique
Pr. EL MESNAOUI Abbes Chirurgie Générale Pr. ESSAKALI HOUSSYNI Leila Oto-Rhino-Laryngologie Pr. IBEN ATTYA ANDALOUSSI Ahmed Urologie
Pr. OUAZZANI CHAHDI Bahia Ophtalmologie
Pr. SEFIANI Abdelaziz Génétique
Pr. ZEGGWAGH Amine Ali Réanimation Médicale
Décembre 1996
Pr. BELKACEM Rachid Chirurgie Pédiatrie Pr. BOULANOUAR Abdelkrim Ophtalmologie Pr. EL ALAMI EL FARICHA EL Hassan Chirurgie Générale
Pr. GAOUZI Ahmed Pédiatrie
Pr. OUZEDDOUN Naima Néphrologie
Pr. ZBIR EL Mehdi* Cardiologie Directeur HMI Mohammed V
Novembre 1997
Pr. ALAMI Mohamed Hassan Gynécologie-Obstétriq
Pr. BEN SLIMANE Lounis Urologie
Pr. BIROUK Nazha Neurologie
Pr. ERREIMI Naima Pédiatrie
Pr. TOUFIQ Jallal Psychiatrie Directeur Hôp.Arrazi Salé Pr. YOUSFI MALKI Mounia Gynécologie Obstétrique
Novembre 1998
Pr. BENOMAR ALI Neurologie Doyen de la FMP Abulcassis
Pr. BOUGTAB Abdesslam Chirurgie Générale Pr. ER RIHANI Hassan Oncologie Médicale
Pr. BENKIRANE Majid* Hématologie
Janvier 2000
Pr. ABID Ahmed* Pneumo-phtisiologie
Pr. AIT OUAMAR Hassan Pédiatrie
Pr. BENJELLOUN Dakhama Badr.Sououd Pédiatrie
Pr. BOURKADI Jamal-Eddine Pneumo-phtisiologie Directeur Hộp. My Youssef
Pr. CHARIF CHEFCHAOUNI Al Montacer Chirurgie Générale Pr. ECHARRAB El Mahjoub Chirurgie Générale Pr. EL FTOUH Mustapha Pneumophtisiologie Pr. EL MOSTARCHID Brahim* Neurochirurgie
Pr. TACHINANTE Rajae Anesthésie-Réanimation Pr. TAZI MEZALEK Zoubida Médecine Interne
Novembre 2000
Pr. AIDI Saadia Neurologie
Pr, AJANA Fatima Zohra Gastro-Entérologie
Pr. BENAMR Said Chirurgie Générale
Pr. CHERTI Mohammed Cardiologie
Pr. ECH-CHERIF EL KETTANI Selma Anesthésie Réanimation
Pr. EL HASSANI Amine Pédiatrie - Directeur Hôp.Cheikh Zaid
Pr. EL KHADER Khalid Urologie
Pr. GHARBI Mohamed El Hassan Endocrinologie et Maladies Métaboliques Pr. MDAGHRI ALAOUI Asmae Pédiatrie
Décembre 2001
Pr. BALKHI Hicham* Anesthésie-Réanimation
Pr. BENABDELJLIL Maria Neurologie
Pr. BENAMAR Loubna Néphrologie
Pr. BENAMOR Jouda Pneumo-phtisiologie
Pr. BENELBARHDADI Imane Gastro-Entérologie
Pr. BENNANI Rajae Cardiologie
Pr. BENOUACHANE Thami Pédiatrie
Pr. BEZZA Ahmed* Rhumatologie
Pr. BOUCHIKHI IDRISSI Med Larbi Anatomie Pr. BOUMDIN El Hassane* Radiologie
Pr. CHAT Latifa Radiologie
Pr. ETTAIR Said Pédiatrie - Directeur Hôp. d'Enfants Rabat
Pr. GAZZAZ Miloudi* Neuro-Chirurgie
Pr. HRORA Abdelmalek Chirurgie Générale Directeur Hôpital Ibn Sina Pr. KABIRI EL Hassane* Chirurgie Thoracique
Pr. LAMRANI Moulay Omar Traumatologie Orthopédie
Pr. LEKEHAL Brahim Chirurgie Vasculaire Périphérique V-D chargé Aff Acad. Est.
Pr. MEDARHRI Jalil Chirurgie Générale
Pr. MIKDAME Mohammed* Hématologie Clinique
Pr. MOHSINE Raouf Chirurgie Générale
Pr. NOUINI Yassine Urologie
Pr. SABBAH Farid Chirurgie Générale
Pr. SEFIANI Yasser Chirurgie Vasculaire Périphérique Pr. TAOUFIQ BENCHEKROUN Soumia Pédiatrie
Décembre 2002
Pr. AL BOUZIDI Abderrahmane* Anatomie Pathologique
Pr. AMEUR Ahmed * Urologie
Pr. AMRI Rachida Cardiologie
Pr. AOURARH Aziz* Gastro-Entérologie
Pr. BAMOU Youssef * Biochimie-Chimie
Pr. BELMEJDOUB Ghizlene* Endocrinologie et Maladies Métaboliques
Pr. BENZEKRI Laila Dermatologie
Pr. BENZZOUBEIR Nadia Gastro-Entérologie Pr. BERNOUSSI Zakiya Anatomie Pathologique Pr. CHOHO Abdelkrim * Chirurgie Générale
Pr. CHKIRATE Bouchra Pédiatrie
Pr. EL ALAMI EL Fellous Sidi Zouhair Chirurgie Pédiatrique Pr. EL HAQURI Mohamed * Dermatologie
Pr. FILALI ADIB Abdelhai Gynécologie Obstétrique
Pr. HAJJI Zakia Ophtalmologie
Pr. JAAFAR Abdeloihab* Traumatologie Orthopédie
Pr. KRIOUILE Yamina Pédiatrie
Pr. MOUSSAOUI RAHALI Driss* Gynécologie Obstétrique Pr. OUJILAL Abdelilah Oto-Rhino-Laryngologie
Pr. RAISS Mohamed Chirurgie Générale
Pr. SIAH Samir * Anesthésie Réanimation
Pr. THIMOU Amal Pédiatrie
Pr. ZENTAR Aziz* Chirurgie Générale
Janvier 2004
Pr. ABDELLAH El Hassan Ophtalmologie
Pr. AMRANI Mariam Anatomie Pathologique
Pr. BENBOUZID Mohammed Anas Oto-Rhino-Laryngologie Pr. BENKIRANE Ahmed* Gastro-Entérologie
Pr. EL HANCHI ZAKI Gynécologie Obstétrique Pr. EL KHORASSANI Mohamed Pédiatrie
Pr. HACHI Hafid Chirurgie Générale
Pr. JABOUIRIK Fatima Pédiatrie
Pr. KHARMAZ Mohamed Traumatologie Orthopédie
Pr. MOUGHIL Said Chirurgie Cardio-Vasculaire
Pr. OUBAAZ Abdelbarre * Ophtalmologie Pr. TARIB Abdelilah* Pharmacie Clinique
Pr. TIJAMI Fouad Chirurgie Générale
Pr. ZARZUR Jamila Cardiologie
Janvier 2005
Pr. ABBASSI Abdellah Chirurgie Réparatrice et Plastique Pr. AL KANDRY Sif Eddine* Chirurgie Générale
Pr. ALLALI Fadoua Rhumatologie
Pr. AMAZOUZI Abdellah Ophtalmologie
Pr. BAHIRI Rachid Rhumatologie Directeur Hôp. Al Ayachi Salé
Pr. BARKAT Amina Pédiatrie
Pr. BENYASS Aatif Cardiologie
Pr. DOUDOUH Abderrahim* Biophysique
Pr. HAJJI Leila Cardiologie (mise en disponibilité)
Pr. HESSISSEN Leila Pédiatrie
Pr. JIDAL Mohamed* Radiologie
Pr. LAAROUSSI Mohamed Chirurgie Cardio-vasculaire
Pr. LYAGOUBI Mohammed Parasitologie
Pr. SBIHI Souad Histo-Embryologie Cytogénétique
Pr. ZERAIDI Najia Gynécologie Obstétrique
AVRIL 2006
Pr. ACHEMLAL Lahsen* Rhumatologie
Pr. BELMEKKI Abdelkader* Hématologie
Pr. BENCHEIKH Razika O.R.L
Pr. BIYI Abdelhamid* Biophysique
Pr. BOUHAFS Mohamed El Amine Chirurgie - Pédiatrique
Pr. BOULAHYA Abdellatif* Chirurgie Cardio - Vasculaire. Directeur Hôpital Ibn Sina Mé
Pr. CHENGUETI ANSARI Anas Gynécologie Obstétrique
Pr. DOGHMI Nawal Cardiologie
Pr. FELLAT Ibtissam Cardiologie
Pr. FAROUDY Mamoun Anesthésie Réanimation
Pr. HARMOUCHE Hicham Médecine Interne
Pr. IDRISS LAHLOU Amine* Microbiologie
Pr. JROUNDI Laila Radiologie
Pr. KARMOUNI Tariq Urologie
Pr. KILI Amina Pédiatrie
* Enseignants Militaires
Pr. OUANASS Abderrazzak Psychiatrie
Pr. SAFI Soumaya* Endocrinologie
Pr. SEKKAT Fatima Zahra Psychiatrie
Pr. SOUALHI Mouna Pneumo - Phtisiologie
Pr. TELLAL Saida* Biochimie
Pr. ZAHRAOUI Rachida Pneumo - Phtisiologie
Octobre 2007
Pr. ABIDI Khalid Réanimation médicale
Pr. ACHACHI Leila Pneumo phtisiologie
Pr, ACHOUR Abdessamad* Chirurgie générale
Pr. AIT HOUSSA Mahdi * Chirurgie cardio vasculaire Pr. AMHAJJI Larbi * Traumatologie orthopédie
Pr. AOUFI Sarra Parasitologie
Pr. BAITE Abdelouahed * Anesthésie réanimation Pr. BALOUCH Lhousaine * Biochimie-chimie Pr. BENZIANE Hamid * Pharmacie clinique Pr. BOUTIMZINE Nourdine Ophtalmologie Pr. CHERKAOUI Naoual * Pharmacie galénique Pr. EHIRCHIOU Abdelkader * Chirurgie générale Pr. EL BEKKALI Youssef * Chirurgie cardio-vasculaire
Pr. EL ABSI Mohamed Chirurgie générale
Pr. EL MOUSSAOUI Rachid Anesthésie réanimation
Pr. EL OMARI Fatima Psychiatrie
Pr. GHARIB Noureddine Chirurgie plastique et réparatrice
Pr. HADADI Khalid * Radiothérapie
Pr. ICHOU Mohamed * Oncologie médicale
Pr. ISMAILI Nadia Dermatologie
Pr. KEBDANI Tayeb Radiothérapie
Pr. LOUZI Lhoussain * Microbiologie
Pr. MADANI Naoufel Réanimation médicale
Pr. MAHI Mohamed * Radiologie
Pr. MARC Karima Pneumo phtisiologie
Pr. MASRAR Azlarab Hématologie biologique
Pr. MRANI Saad * Virologie
Pr. OUZZIF Ez zohra Biochimie chimie
Pr. RABHI Monsef* Médecine interne
Pr. RADOUANE Bouchaib* Radiologie
Pr. SEFFAR Myriame Microbiologie
Pr. SEKHSOKH Yessine * Microbiologie
Pr. SIFAT Hassan * Radiothérapie
Pr. TABERKANET Mustafa * Chirurgie vasculaire périphérique
Pr. TACHFOUTI Samira Ophtalmologie
Pr. TAJDINE Mohammed Tariq* Chirurgie générale
Pr. TANANE Mansour * Traumatologie-orthopédie
Pr. AGADR Aomar * Pédiatrie
Pr. AIT ALI Abdelmounaim * Chirurgie Générale Pr. AIT BENHADDOU El Hachmia Neurologie
Pr. AKHADDAR Ali * Neuro-chirurgie
Pr. ALLALI Nazik Radiologie
Pr. AMINE Bouchra Rhumatologie
Pr. ARKHA Yassir Neuro-chirurgie Directeur Hôp.des Spécialités Pr. BELYAMANI Lahcen Anesthésie Réanimation
Pr. BJIJOU Younes Anatomie
Pr. BOUHSAIN Sanae * Biochimie-chimie
Pr. BOUI Mohammed * Dermatologie
Pr. BOUNAIM Ahmed * Chirurgie Générale
Pr. BOUSSOUGA Mostapha * Traumatologie-orthopédie
Pr. CHTATA Hassan Toufik * Chirurgie Vasculaire Périphérique
Pr. DOGHMI Kamal * Hématologie clinique
Pr. EL MALKI Hadj Omar Chirurgie Générale Pr. EL OUENNASS Mostapha* Microbiologie
Pr. ENNIBI Khalid * Médecine interne
Pr. FATHI Khalid Gynécologie obstétrique
Pr. HASSIKOU Hasna * Rhumatologie
Pr. KABBAJ Nawal Gastro-entérologie
Pr. KABIRI Meryem Pédiatrie
Pr. KARBOUBI Lamya Pédiatrie
Pr. LAMSAOURI Jamal * Chimie Thérapeutique Pr. MARMADE Lahcen Chirurgie Cardio-vasculaire
Pr. MESKINI Toufik Pédiatrie
Pr. MESSAOUDI Nezha * Hématologie biologique
Pr. MSSROURI Rahal Chirurgie Générale
Pr. NASSAR Ittimade Radiologie
Pr. OUKERRAJ Latifa Cardiologie
Pr. RHORFI Ismail Abderrahmani * Pneumo-Phtisiologie
Octobre 2010
Pr. ALILOU Mustapha Anesthésie réanimation
Pr. AMEZIANE Taoufiq* Médecine Interne Directeur ERSSM
Pr. BELAGUID Abdelaziz Physiologie
Pr. CHADLI Mariama* Microbiologie
Pr. CHEMSI Mohamed* Médecine Aéronautique
Pr. DAMI Abdellah* Biochimie-Chimie
Pr. DARBI Abdellatif* Radiologie
Pr. DENDANE Mohammed Anouar Chirurgie Pédiatrique
Pr. EL HAFIDI Naima Pédiatrie
Pr. EL KHARRAS Abdennasser* Radiologie
Pr. EL MAZOUZ Samir Chirurgie Plastique et Réparatrice
Pr. EL SAYEGH Hachem Urologie
* Enseignants Militaires
Pr. ZOUAIDIA Fouad Anatomie Pathologique
Décembre 2010
Pr.ZNATI Kaoutar
Mai 2012
Pr. AMRANI Abdelouahed Chirurgie pédiatrique Pr. ABOUELALAA Khalil * Anesthésie Réanimation Pr. BENCHEBBA Driss * Traumatologie-orthopédie Pr. DRIŞSI Mohamed * Anesthésie Réanimation Pr. EL ALAOUI MHAMDI Mouna Chirurgie Générale Pr. EL KHATTABI Abdessadek * Médecine Interne Pr. EL OUAZZANI Hanane * Pneumophtisiologie
Pr. ER-RAJI Mounir Chirurgie Pédiatrique
Pr. JAHID Ahmed Anatomie Pathologique
Pr. RAISSOUNI Maha* Cardiologie
Février 2013
Pr. AHID Samir Pharmacologie
Pr. AIT EL CADI Mina Toxicologie
Pr. AMRANI HANCHI Laila Gastro-Entérologie
Pr. AMOR Mourad Anesthésie Réanimation
Pr. AWAB Almahdi Anesthésie Réanimation
Pr. BELAYACHI Jihane Réanimation Médicale Pr. BELKHADIR Zakaria Houssain Anesthésie Réanimation Pr. BENCHEKROUN Laila Biochimie-Chimie
Pr. BENKIRANE Souad Hématologie
Pr. BENNANA Ahmed* Informatique Pharmaceutique Pr. BENSGHIR Mustapha * Anesthésie Réanimation
Pr. BENYAHIA Mohammed * Néphrologie
Pr. BOUATIA Mustapha Chimie Analytique et Bromatologie Pr. BOUABID Ahmed Salim* Traumatologie orthopédie
Pr BOUTARBOUCH Mahjouba Anatomie
Pr. CHAIB Ali * Cardiologie
Pr. DENDANE Tarek Réanimation Médicale
Pr. DINI Nouzha * Pédiatrie
Pr. ECH-CHERIF EL KETTANI Mohamed Ali Anesthésie Réanimation Pr. ECH-CHERIF EL KETTANI Najwa Radiologie
Pr. ELFATEMI NIZARE Neuro-chirurgie
Pr. EL GUERROUJ Hasnae Médecine Nucléaire
Pr. EL HARTI Jaouad Chimie Thérapeutique
Pr. EL JAOUDI Rachid * Toxicologie
Pr. EL KABABRI Maria Pédiatrie
Pr. EL KHANNOUSSI Basma Anatomie Pathologique
Pr. EL KHLOUFI Samir Anatomie
Pr. IMANE Zineb Pédiatrie
Pr. IRAQI Hind Endocrinologie et maladies métaboliques
Pr. KABBAJ Hakima Microbiologie
Pr. KADIRI Mohamed * Psychiatrie
Pr. LATIB Rachida Radiologie
Pr. MAAMAR Mouna Fatima Zahra Médecine Interne
Pr. MEDDAH Bouchra Pharmacologie
Pr. MELHAOUI Adyl Neuro-chirurgie
Pr. MRABTI Hind Oncologie Médicale
Pr. NEJJARI Rachid Pharmacognosie
Pr. OUBEJJA Houda Chirugie Pédiatrique
Pr. OUKABLI Mohamed Anatomie Pathologique
Pr. RAHALI Younes Pharmacie Galénique Vice-Doyen à la Pharmacie
Pr. RATBI Ilham Génétique
Pr. RAHMANI Mounia Neurologie
Pr. REDA Karim * Ophtalmologie
Pr. REGRAGUI Wafa Neurologie
Pr. RKAIN Hanan Physiologie
Pr. ROSTOM Samira Rhumatologie
Pr. ROUAS Lamiaa Anatomie Pathologique
Pr. ROUIBAA Fedoua * Gastro-Entérologie
Pr SALIHOUN Mouna Gastro-Entérologie
Pr. SAYAH Rochde Chirurgie Cardio-Vasculaire
Pr. SEDDIK Hassan * Gastro-Entérologie
Pr. ZERHOUNI Hicham Chirurgie Pédiatrique
Pr. ZINE Ali * Traumatologie Orthopédie
AVRIL 2013
Pr. EL KHATIB MOHAMED KARIM* Stomatologie et Chirurgie Maxillo-faciale
MARS 2014
Pr. ACHIR Abdellah Chirurgie Thoracique
Pr. BENCHAKROUN Mohammed Traumatologie-Orthopédie Pr. BOUCHIKH Mohammed Chirurgie Thoracique
Pr. EL KABBAJ Driss * Néphrologie
Pr. EL MACHTANI IDRISSI Samira * Biochimie-Chimie
Pr. HARDIZI Houyam Histologie- Embryologie-Cytogénétique
Pr. HASSANI Amale * Pédiatrie
Pr. HERRAK Laila Pneumologie
Pr. JANANE Abdellah Urologie
Pr. JEAIDI Anass * Hématologie Biologique
Pr. KOUACH Jaouad* Génycologie-Obstétrique
Pr. LEMNOUER Abdelhay* Microbiologie
Pr. MAKRAM Sanaa * Pharmacologie
Pr. OULAHYANE Rachid* Chirurgie Pédiatrique Pr. RHISSASSI Mohamed Jaafar CCV
Pr. ABILKACEM Rachid* Pédiatrie
Pr. AIT BOUGHIMA Fadila Médecine Légale
Pr. BEKKALI Hicham * Anesthésie-Réanimation Pr. BENAZZOU Salma Chirurgie Maxillo-Faciale
Pr. BOUABDELLAH Mounya Biochimie-Chimie
Pr. BOUCHRIK Mourad* Parasitologie
Pr. DERRAJI Soufiane* Pharmacie Clinique
Pr. DOBLALI Taoufik Microbiologie
Pr. EL AYOUBI EL IDRISSI Ali Anatomie
Pr. EL GHADBANE Abdedaim Hatim* Anesthésie-Réanimation Pr. EL MARJANY Mohammed* Radiothérapie
Pr. FEJJAL Nawfal Chirurgie Réparatrice et Plastique
Pr. JAHIDI Mohamed* O.R.L
Pr. LAKHAL Zouhair* Cardiologie
Pr. OUDGHIRI NEZHA Anesthésie-Réanimation
Pr. RAMI Mohamed Chirurgie Pédiatrique
Pr. SABIR Maria Psychiatrie
Pr. SBAI IDRISSI Karim* Médecine préventive, santé publique et Hyg.
AOUT 2015
Pr. MEZIANE Meryem Dermatologie
Pr. TAHIRI Latifa Rhumatologie
PROFESSEURS AGREGES: JANVIER 2016
Pr. BENKABBOU Amine Chirurgie Générale
Pr. EL ASRI Fouad* Ophtalmologie
Pr. ERRAMI Noureddine* O.R.L
Pr. NITASSI Sophia O.R.L
JUIN 2017
Pr. ABI Rachid* Microbiologie
Pr. ASFALOU Ilyasse* Cardiologie
Pr. BOUAYTI El Arbi* Médecine préventive, santé publique et Hyg.
Pr. BOUTAYEB Saber Oncologie Médicale
Pr. EL GHISSASSI Ibrahim Oncologie Médicale
Pr. HAFIDI Jawad Anatomie
Pr. OURAINI Saloua* O.R.L
Pr. RAZINE Rachid Médecine préventive, santé publique et Hyg.
Pr. ZRARA Abdelhamid* Immunologie
NOVEMBRE 2018
Pr. AMELLAL Mina Anatomie
Pr. SOULY Karim Microbiologie
Pr. ABOUDRAR Saadia Physiologie Pr. ALAMI OUHABI Naima Biochimie chimie
Pr. ALAOUI KATIM Pharmacologie
Pr. ALAOUI SLIMANI Lalla Naima Histologie-Embryologie
Pr. ANSAR M'hammed Chimie Organique et Pharmacie Chimique Pr .BARKIYOU Malika Histologie-Embryologie
Pr. BOUHOUCHE Ahmed Génétique
Humaine Pr. BOUKLOUZE Abdelaziz Applications Pharmaceut iques Pr. CHAHED OUAZZANI Lalla Chadia Biochimie chimie Pr. DAKKA Taoufiq Physiologie
Pr. FAOUZI Moulay El Abbes Pharmacologie
Pr. IBRAHIMI Azeddine Biologie moléculaire/Biotechnologie Pr. KHANFRI Jamal Eddine Biologie
Pr. OULAD BOUYAHYA IDRISSI Med Chimie Organique Pr. REDHA Ahlam Chimie
Pr. TOUATI Driss Pharmacognosie
Pr. ZAHIDI Ahmed Pharmacologie
Mise à jour le 04/02/2020 Khaled Abdellah
ABL Abelson murine leukemia viral oncogene homolog
ADC adénocarcinome
ADP Adénosine Diphosphate
AINS Anti Inflammatoire Non Stéroïdien
Ag Antigen
AKT Protein Kinase B
ALK anaplastic lymphoma kinase
APC Antigen-Presenting Cell
ARA II Antagoniste des Récepteurs a
l'Angiotensine II
ATP Adénosine triphosphate
AUC Area Under the curver -Aire sous la courbe (des concentrations
plasmatiques)
BCRP Breast Cancer Resistance Proteine BRCA1 Breast Cancer gene 1
BRCA2 Breast Cancer gene 2
CAM Complementary and Altarnative Medecine - Médecines
complémentaires et alternatives
CAR Constitutive Androstane Receptor
CBNPC Cancer Bronchique Non à Petites
Cellules
CCRm Cancer Colorectal métastatique Cl Clairance rénale d'élimination
CLL Chronic lymphocytic leukemia
Cmax Concentration maximale CMH complexe majeur
d'histocompatibilité
CpG Cytosine-phosphate-Guanine
CPPC : Cancer de Poumon à Petites cellules CTL Cytotoxic T lymphocytes
CTLA-4 Cytotoxic T-Lymphocyte Antigen 4 CYP Cytochrome
EGF Epidermal Growth Factor
EGFR epidermal growth factor receptor ER+ Récepteur aux œstrogènes positif
FEVG Fraction d’Ejection du Ventricule
Gauche
FAK Focal adhesion kinase
FGF Fibroblast Growth Factor
Flt-1 Fms-Like-Tyrosine kinase - 1
Flt-3 Fms-Like-Tyrosine kinase – 3
GIST Gastro-Intestinal Stromal tumor
GM-CSF Granulocyte-Macrophage
Colony-Stimulating Factor
HER Human Epidermal growth factor Receptor
HGF hepatocyte growth factor
HIF Hypoxia Inducible Factor
HTA Hypertension Artérielle
IC Insuffisance Cardiaque
IGF insulin growth factor
IGF-1R insulin-like growth factor-1
receptor IL-2 Interleukine 2 IND inducteur INH Inhibiteur IPDE-5 Inhibiteurs de la Phosphodiestérase de type 5
ITK Inhibiteur de Tyrosine Kinase
JAK Janus Kinase
MAP-ERK Mitogen Activated Protein kinase -
extracellular signal-regulated kinase
mTOR mechanistic target of rapamycin mTORC1 mammalian target of rapamycin
complex 1
NCCAM National Center for Complementary
and Alternative Medicine
NCI-CTCAE National Cancer
Institute-Commun Terminology Criteria for Adverse Events
NFS Numeration Formule Sanguine
NK Natural Killer
NGF Nerve growth factor
NGS Next Generation Sequencing
NRP Neuropiline
NRTK Non-receptor tyrosine kinase NSCLC non-small-cell lung cancer OMIT Observatoire inter-régional des
Médicaments et de l’Innovation Thérapeutique
OMS Organisation Mondiale de la Sante OATP Organic-Anion-Transporting
Polypeptide
OAT1 Organic Anion Transporter 1 OCT Organic Cation Transporter
PA Pression Artérielle
PARP poly ADP-ribose polymerase PD-1 Programmed cell Death 1
PDGFR platelet-derived growth factor
PDGF Platelet Derivated Growth Factor PGI-2 Prostaglandin I2
P-gp P- Glycoproteine
PI3K Phosphatidyl-Inositol-3-Kinase
PIGF Placenta Growth Factor
PIP3 Phophatidylinositol-3-Phosphate
PR+ Récepteur aux progestérone positif
PTEN Phosphatase and Tensin
Homologue Gene
PXR Pregnane X Receptor
RAPTOR Regulatory-Associated Protein of
mTOR
RCC Renal Cell Carcinoma - Cancer à Cellules Rénales
RCCcc Cancer Rénal à Cellules Claires RICTOR Rapamycine Insensitive Companion
of mTOR
RTK Recepteur Tyrosine Kinase
S6K ribosomal S6 kinase
SCLC Small-Cell lung Cancer SUB Substrat
TGF Tumor Growth Factor
TGF-β Transforming Growth Factor β TK Tyrosine Kinase
TME Tumor Microenvironment
TRK Tropomyosin receptor kinase
UGT UDP Glucuronosyl-Transferases
UGT1A1 UDP-glucuronosyltransferase 1A1 VEGF Vascular Endothelial Growth Factor VEGF-R Vascular Endothelial Growth Factor
Liste des
Illustrations
Liste des figures
FIGURE 1 : Chronologie des traitements classiques et innovants du cancer ... 7
FIGURE 2 : Théorie des mutations somatiques ... 8
FIGURE 3 : Les trois phases de la cancérogenèse : initiation, promotion,
progression ... 10
FIGURE 4 : Six caractéristiques clés de la cellule maligne ... 11
FIGURE 5 : Poinçons et caractéristiques habilitantes émergents 2011 ... 12
FIGURE 6 : Schéma simplifié des différents composants du microenvironnement
tumoral et les différentes interactions entre eux ... 13
FIGURE 7 : Passage de la tumeur de la phase latente à la phase invasive « SWITCH
» angiogénique ... 15
FIGURE 8 : Déséquilibre de l’expression des facteurs pro-angiogéniques et
anti-angiogéniques ... 16
FIGURE 9 : Différentes étapes de l’angiogénèse dans la vascularisation de la
tumeur ... 17
FIGURE 10 : Réseau vasculaire tumoral sous l’effet de VEGF visionné sous
microscopie optique avec coloration immunohistochimique par un anticorps
anti-CD31 fluorescent ... 17
FIGURE 11 : Hétérogénéité intra-tumorale ... 18
FIGURE 12 : Modèle stochastique et modèle des cellules souches cancéreuses . 19
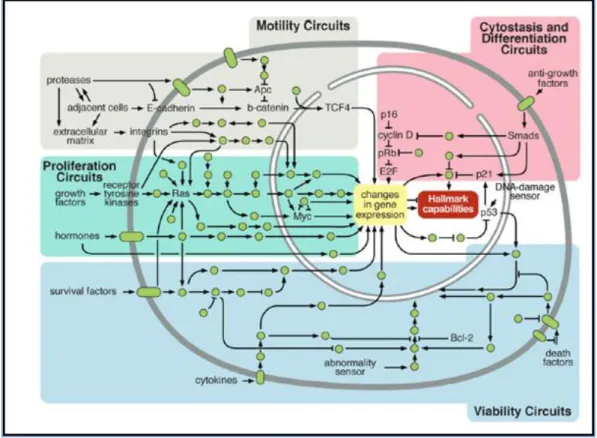
FIGURE 13 : Schéma simplifié d’un réseau de signalisation intracellulaire régulant
le fonctionnement des cellules cancéreuses. ... 20
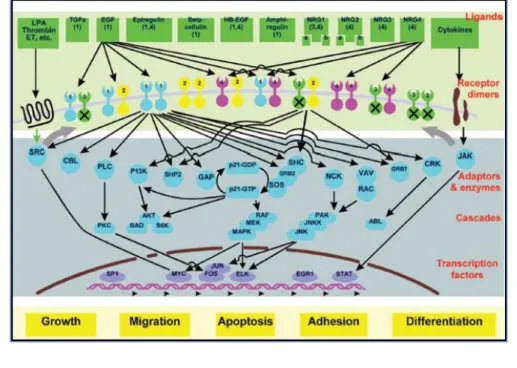
FIGURE 14 : Cibles thérapeutiques des biothérapies. ... 22
FIGURE 15 : Schéma représentatif de RTK et les différentes voies de signalisation
FIGURE 16 : Différentes sous-familles ou prototypes de récepteurs de tyrosine
kinases ... 24
FIGURE 17 : Mécanisme d’activation des RTK ... 25
FIGURE 18 : EGFR et ses ligands ... 26
FIGURE 19 : Signalisation du récepteur ERBB conduit à une grande variété de
voies et de résultats de signalisation... 26
Figure 20 : Différentes voies de signalisation en aval médiées par le VEGFR ... 27
FIGURE 21 : Récepteur VEGF et ses ligands ... 28
FIGURE 22 : Protéines-tyrosine kinases cytoplasmiques ... 29
FIGURE 23 : Mode d’action des inhibiteurs de tyrosine kinases ... 31
FIGURE 24 : Structure générale de l’anticorps... 32
FIGURE 25 : Mécanismes de blocage d’EGFR par les anticorps monoclonaux ... 33
FIGURE 26 : Différentes générations d’anticorps thérapeutiques ... 34
FIGURE 27 : Classification des tumeurs malignes ... 36
FIGURE 28 : Symptômes généraux du cancer du sein ... 37
FIGURE 29 : Cancer du sein fongateur, la tumeur primitive s'est développée
localement et a finalement envahi la peau provoquant une fongation locale (photo
à droite). Caractéristique typique de la peau d’orange (photo à gauche). ... 38
FIGURE 30 : Classification du cancer du sein basée sur son origine tissulaire 38
FIGURE 31 : Signatures moléculaires du cancer du sein détectées lors de
séquençage de génome ... 39
FIGURE 32 : Voie de signalisation PI3KT/AKT/mTOR et les molécules inhibitrices
de mTOR ... 43
FIGURE 34 : Mécanisme d’inhibiteurs de CDK4/6 ... 45
FIGURE 35 : Mécanisme d’action des inhibiteurs de PARP sur les cellules
normales et sur les cellules malignes ... 47
FIGURE 36 : Classification histologique du cancer du poumon ... 51
FIGURE 37 : Stratification des patients atteints d'un cancer du poumon par
mutation ou surexpression de divers oncogènes ... 52
FIGURE 38 : Réarrangement au niveau de chromosome 2p et formation de
protéine de fusion ALK-EML4 dans les NSCLC ... 53
FIGURE 39 : Fusions ROS1 dans les adénocarcinomes ... 54
FIGURE 40 : Illustration de la voie de signalisation de la kinase RAS – RAF – MEK
– ERK MAPK et les inhibiteurs actuels ciblant BRAF, MEK et ERK ... 56
FIGURE 41 : Séquences de progression tumorale adénome carcinome. ... 60
FIGURE 42 : Mécanisme moléculaire du CCR. La mise en place et la progression
du CCR ... 61
FIGURE 43 : Différents types d’instabilité génomique dans le cancer colorectal et
leur répartition dans la population. ... 64
FIGURE 44 : Ciblage d’EGFR par les anticorps monoclonaux le cetuximab et le
panitumumab ... 67
FIGURE 45 : Tumeur mésenchymateuse gastrique type GIST ... 70
FIGURE 46 : Exemples de morphologies des tumeurs stromales
gastro-intestinales ... 72
FIGURE 47 : Principales voies de signalisation médiées par KIT ... 73
FIGURE 48 : Les mutations de KIT et PDGFRA sont représentées en rouge pour les
mutations primaires et en bleu pour les mutations secondaires. Leur fréquence est
proportionnelle à la largeur du rectangle ... 75
FIGURE 49 : Classification moléculaire des GIST ... 76
FIGURE 50 : Histologie des sous-types de RCC les plus fréquents ... 80
FIGURE 51 : Différentes voies de signalisation ciblées par le traitement du cancer
du rein ... 84
FIGURE 52 : Différentes méthodes d’immunothérapie ... 87
FIGURE 53 : Mécanisme des inhibiteurs de points de contrôle dans le cas de
cancer du poumon ... 88
FIGURE 54 : Exemples d’interactions impliquant la P-GP et BCRP ... 100
FIGURE 55 : Expression de la P-GP dans différents tissus ... 101
FIGURE 56 : Médicaments pour lesquels un risque d’allongement de l’intervalle QT
est bien connu ... 111
FIGURE 57 : Mécanisme d’induction enzymatique de CYP3A4 par millepertuis . 112
FIGURE 58 : A : éruption acnéiforme induite par cetuximab, B : 1 semaine après le
traitement par (hydrocortisone / tararotène) ... 119
FIGURE 59 : Contrôle cellulaire de l'hyperglycémie. ... 139
FIGURE 60 : Résumé des lignes directrices pour la gestion de l'hyperglycémie
proposée par Busaidy et al. Et Villadolid et al ... 141
FIGURE 61 : Algorithme de gestion de l'hypertriglycéridémie. ... 144
FIGURE 62 : Schéma de la distribution des différentes voies de signalisation dans
l’œil et les agents ciblés spécifiques ... 148
FIGURE 63 : Vue externe des structures anatomiques de l’œil et différents types
d’atteintes oculaires induites par les thérapies ciblées ... 149
FIGURE 64 : Diagramme de la prise en charge pharmaceutique des patients sous
FIGURE 66 : Echelle d’évaluation de l’observance de Girerd. ... 172
FIGURE 67 : Fonctions de système d’information « SI ». ... 179
FIGURE 68 : Etapes de la conception et la réalisation d’un SI par la méthode
Liste des Tableaux
TABLEAU 1 : ANTICORPS MONOCLONAUX THERAPEUTIQUES COMMERCIALISES
PAR L’AUTORISATION DE LA FAD EN 2012 ... 35
TABLEAU 2 : CARACTERISTIQUES, DEFINITION IMMUNOHISTOCHIMIQUE DE
SUBSTITUTION ET RECOMMANDATIONS DE TRAITEMENTS POUR LES CINQ
SOUS-TYPES DES CANCERS DU SEIN ... 39
TABLEAU 3 : THERAPIES CIBLEES ANTI-EGFR UTILISEES DANS LE TRAITEMENT
DU SEIN HER2+ ... 41
TABLEAU 4 : MOLECULES INHIBITRICES DE CDK4 / 6 APPROUVEES POUR LE
CANCER DU SEIN LOCALEMENT AVANCE OU METASTATIQUE RH+ SELON LES
RESULTATS DES ESSAIS CLINIQUES DE PHASE III ... 46
TABLEAU 5 : RESUME DES ESSAIS CLINIQUES PORTANT SUR LES INHIBITEURS
DE LA PARP EN TANT QUE TRAITEMENTS DES MUTATIONS BRCA DU CANCER DU
SEIN. ... 48
TABLEAU 6 : DIFFERENTS MEDICAMENTS CIBLES LICENCIES PAR LA FDA POUR
LE TRAITEMENT DU CANCER DU POUMON NON A PETITES CELLULES « NSCLC »
... 58
TABLEAU 7 : CLASSIFICATION CMS ET CORRELATION PHENOTYPIQUE ... 65
TABLEAU 8 : TRAITEMENTS DU CANCER COLORECTAL METASTATIQUE CCR
METASTATIQUE LICENCIES ... 69
TABLEAU 9 : TYPES DE GIST, FREQUENCE ET LOCALISATION DES MUTATIONS
DES RECEPTEURS PDGFRA ET KIT ... 75
TABLEAU 11 : MEDICAMENTS APPROUVES PAR LA FDA POUR LE TRAITEMENT
DE RCC ... 85
TABLEAU 12 : LES QUATRE NIVEAUX DE CONTRAINTE DES INTERACTIONS
MEDICAMENTEUSES ... 96
TABLEAU 13 : EFFET DES ANTIACIDES SUR L'ABSORPTION DES INHIBITEURS DE
TYROSINE KINASE ... 98
TABLEAU 14 : POSOLOGIE, MODALITES D’ADMINISTRATION ET PRECAUTIONS
D’EMPLOI DES INHIBITEURS TYROSINE KINASE ... 103
TABLEAU 15 : QUELQUES PARAMETRES PHARMACOCINETIQUES DES
INHIBITEURS DE TYROSINE KINASE ... 105
TABLEAU 16 : DIFFERENTS CYTOCHROMES RESPONSABLES DE LA
METABOLISATION DES ITK ... 106
TABLEAU 17 : INTERACTIONS MEDICAMENTEUSES DES CYTOCHROMES
ENZYMATIQUES ... 108
TABLEAU 18 : EFFETS CUTANES INDUITS PAR LES THERAPIES CIBLEES ... 127
TABLEAU 19 : CONDUITE A TENIR PENDANT LE TRAITEMENT
ANTI-ANGIOGENIQUE PAR LE MEDECIN EN CAS D’ACCIDENT VEINEUX... 135
TABLEAU 20 : PRISE EN CHARGE DE DYSTHYROÏDIE ... 145
TABLEAU 21 : PRISE EN CHARGE DES TOXICITES HEMATOLOGIQUES INDUITES
PAR LES THERAPIES CIBLEES ... 147
TABLEAU 22 : RESUME DES EFFETS INDESIRABLES OCULAIRES DE DIVERS
AGENTS THERAPEUTIQUES CIBLES ET LES TRAITEMENTS ASSOCIES ... 151
TABLEAU 23 : AMENAGEMENT DES TOXICITES OCULAIRES INDUITES PAR LES
TABLEAU 24 : MEDICAMENTS HOMEOPATHIQUES POUR LE TRAITEMENT DE
CERTAINS EFFETS INDESIRABLES DES THERAPIES CIBLEES ... 158
TABLEAU 25 : EMPLOI DES HUILES ESSENTIELLES CONTRE LES TROUBLES DU
SYSTEME NERVEUX ET DU PSYCHISME ... 162
TABLEAU 26 : ETUDES INDIQUANT DIVERS PARAMETRES DE MAUVAISE
LISTE DES ANNEXES
ANNEXE 1 : FICHE «AFINITOR® PATIENTS» ELABOREE PAR L’OMIT
BRETAGNE-PAYS DE LA LOIRE ... 198
ANNEXE 2 : FICHE «AFINITOR® PROFESSIONNELS DE SANTE» ELABOREE PAR
L’OMIT BRETAGNE-PAYS DE LA LOIRE ... 200
ANNEXE 3 : FICHE «NEXAVAR® PROFESSIONNELS DE SANTE» ELABOREE PAR
L’OMIT BRETAGNE-PAYS DE LA LOIRE ... 202
ANNEXE 4 : FICHE «CABOMETYX® PROFESSIONNELS DE SANTE» ELABOREE PAR
L’OMIT BRETAGNE-PAYS DE LA LOIRE ... 204
ANNEXE 5 : EPIDEMIOLOGIE DES DIFFERENTS TYPES DE CANCER ANNEE 2018
... 206
ANNEXE 6 : SUBSTRATS, INHIBITEURS ET INDUCTEURS DE LA P-GP ... 207
Sommaire
Introduction ... 1 Chapitre I : Connaissances oncologiques primordiales destinées au pharmacien ... 6 I. HISTORIQUE DU TRAITEMENT DU CANCER ... 6 II. ONCOGENESE ... 7
Théorie De La Mutagénèse Somatique ... 7 1.1 Initiation « Phase infraclinique » ... 8 1.2 Promotion ... 9 1.3 Progression « Phase clinique » ... 9 Microenvironnement tumoral ... 12 Angiogenese ... 14 Cellule souche tumorale ... 18
III. THERAPIE CIBLEE ... 21
PRINCIPE DE THERAPIE CIBLEE ... 21 TYROSINE KINASE ... 22 2.1 Récepteurs de tyrosine kinases ... 22 2.1.1 Structure et classification des RTK ... 23 2.1.2 Mécanisme de l’activation de récepteurs de tyrosine kinases ... 24 2.1.3 Récepteur du facteur EGF ... 25 2.1.4 Récepteur du facteur VEGF ... 27 2.2 Non récepteurs tyrosine kinases « NRTK » ou tyrosine kinases cytoplasmiques . 29 SERINE/THREONINE KINASES ... 30 CLASSIFICATION DES THERAPIES CIBLEES ... 31 4.1 Nomenclature ... 31 4.2 Inhibiteurs de kinases ... 31 4.3 Anticorps monoclonaux ... 32 4.3.1 Caractéristiques structurales des anticorps monoclonaux ... 32 4.3.2 Mécanisme d’action des anticorps monoclonaux ... 33 4.3.3 Types d’anticorps monoclonaux ... 34
IV. DIFFERENTS TYPES DE CANCERS ET REVOLUTION DES THERPIES CIBLEES ... 35
CANCER DU SEIN ... 36 1.1 CARACTERISTIQUES CLINIQUES ... 36 1.2 Classifications du cancer du sein ... 38 1.2.1 Classification tissulaire ... 38 1.2.2 Classification moléculaire ... 39 1.3 Traitements cibles du cancer du sein
1.3.1 traitements des cancers du sein hormono-sensibles « RH+ » et HER2+ ... 40 1.3.1.1 Anti-HER2 ... 40 1.3.1.2 Inhibiteurs de la molécule mTOR ... 43
1.3.2 Traitement pour le cancer du sein triple négatif « TNBC » ... 46 1.3.2.1 Inhibiteurs de Poly ADP-ribose polymérase « PARP » ... 47 CANCER DE POUMON ... 49 2.1 Epidémiologie et étiologie ... 49 2.2 Symptômes cliniques ... 49 2.3 Classification ... 50 2.3.1 Histopathologie ... 50 2.3.2 Aspects moléculaires ... 51 2.4 TRAITEMENTS CIBLES DE NSCLC ... 52 2.4.1 Traitements cibles des adénocarcinomes ... 52 Inhibiteurs d’EGFR ... 52 Inhibiteurs de lymphome kinase anaplasique « ALK » ... 53 Inhibiteurs ROS1 ... 54 Inhibiteurs de BRAF ... 55 Inhibiteurs d’autres cibles génétiques ... 56 Inhibiteurs de l’angiogénèse ... 57 2.4.2 Traitement cible du cancer du poumon a cellules squameuses ... 58 CANCER COLORECTAL ... 59 3.1 Symptômes cliniques ... 59 3.2 Physiopathologie du cancer colorectal ... 59 3.2.1 Mécanisme histopathologique ... 59 3.2.2 Mécanisme moléculaire ... 61 3.3 Classification moléculaire du CCR ... 62 3.3.1 La classification moléculaire Consensus Molecular System « CMS » ... 64 3.4 Traitements du cancer colorectal ... 66 3.4.1 Inhibiteurs d’EGFR ... 66 3.4.2 Inhibiteurs de l’angiogénèse ... 68 TUMEURS STROMALES GASTRO-INTESTINALES « GIST » ... 69 4.1 Définition actuelle des GIST ... 70 4.2 Epidémiologie ... 70 4.3 Symptômes cliniques ... 70 4.4 Histologie et caractéristiques immunohistochimiques des GIST ... 71 4.5 Pathogénie des GIST ... 72 4.5.1 Mécanisme moléculaire ... 73 4.5.2 Mutations oncogéniques de KIT et PDGRA ... 73 4.6 Classification moléculaire et caractéristiques génétiques des GIST ... 75 4.7 Traitements cibles ... 76 4.7.1 GIST mutant à KIT et PDGRA positifs ... 76 4.7.1.1. Imatinib : traitement standard de 1ère ligne ... 76 4.7.1.2. Sunitinib : traitement standard de 2éme ligne ... 77 4.7.1.3. Autres thérapies ciblées ... 77
5.2 Symptômes cliniques ... 79 5.3 Histopathologie ... 80 5.4 Pathogénie du carcinome rénal à cellules claires ... 81 5.5 Traitements ciblés ... 84
V. PERSPECTIVES FUTURE ... 86
IMMUNOTHERAPIE ... 86 1.1 Inhibiteurs de points de contrôle immunitaires ... 87 1.2 Vaccins anticancéreux ... 89 1.2.1 Vaccins prophylactiques ... 89 1.2.2 Les vaccins thérapeutiques ... 89 Vaccins cellulaires ... 90 Vaccins antigéniques et anti-idiotypes ... 90 Vaccins à base de cellules dendritiques ... 91 AVANTAGES CLINIQUES DE L’IMMUNOTHERAPIE : CANCER DU SEIN METASTATIQUE ET
TNBC ... 91 Chapitre II : PHARMACOLOGIE DES THERAPIES CIBLEES ORALES ... 93 I. ONCOGERIATRIE ... 93 II. PROBLEMATIQUE DES INTERACTIONS MEDICAMENTEUSES DANS LA PRISE EN CHARGE DES PATIENTS CANCEREUX ... 94 III. INTERACTIONS MEDICAMENTEUSES ... 95
INTERACTION PHARMACOCINETIQUE ... 96 1.1 Interaction liée à l’absorption : ... 96 1.1.1 Modification de PH gastrique et de transit ... 96 1.1.2 Protéines de transport membranaires ... 99 1.1.3 Biodisponibilité ... 102 1.2 Interaction liée à la distribution ... 104 1.3 Interaction liée au métabolisme ... 105 1.4 Interaction liée à l’élimination ... 109 INTERACTIONS PHARMACODYNAMIQUES ... 109
Cardiotoxicité des anticancéreux oraux : allongement de l’intervalle QT et risque de torsade de pointe ... 109
IV. INTERACTIONS LIEE A LA PHYTOTHERAPIE ... 111
Millepertuis ... 111 Pamplemousse ... 112 Ginseng ... 113 Thé vert ... 114 Antioxydants ... 114 Plantes hépato stimulantes ... 114
Chapitre III : EFFETS INDESIRABLES DES THERAPIES CIBLEES ... 116 I. FATIGUE ... 116 II. TOXICITES CUTANEES ... 117
Physiopathologie... 117 1.1 Anti-BRAF ... 117
FOLLICULITE ... 118 AUTRES EFFETS CUTANES ... 122
III. TOXICITES DIGESTIVES ... 128 IV. TOXICITE CARDIOVASCULAIRE ... 130
Hypertension artérielle ... 130 Insuffisance cardiaque ... 131 Bradycardie ... 133 Risque thrombo-embolique ... 134 Protéinurie ... 135 V. Troubles métaboliques ... 138 Hyperglycémie ... 138 Hyperlipidémie ... 142 Dysthyroïdie ... 144
VI. EFFETS HEMATOLOGIQUES ... 146 VII. TOXICITES OPHTALMOLOGIQUES ... 148 Chapitre IV : LA MEDECINE COMPLEMENTAIRE ET ALTERNATIVE MAC ... 154 I. HOMEOPATHIE ... 155 1. Définition et avantages ... 155
Soins du support homéopathiques ... 156 2.1 Anti-EGFR ... 156 2.2 Anti-HER ... 156
II. AROMATHERAPIE ... 158
Définition ... 158 Forme d’utilisation ... 158 Bénéfice chez les patients cancéreux ... 159 Précautions d’emploi ... 159 Prise en charge de trouble de psychisme... 160
Chapitre V : SUIVI PHARMACEUTIQUE PERSONNALISE DES PATIENTS CANCEREUX ... 164 I. L’EDUCATION THERAPEUTIQUE DU PATIENT (ETP) ... 164
Selon l’OMS : ... 164
II. PRATIQUE D’UNE DEMARCHE GLOBALE ... 165
Le suivi personnalisé des patients ... 165 OBSERVANCE ... 167 2.1 Conséquences d’une mauvaise observance ... 168 2.2 Méthodes directes de mesure de l’observance ... 169 2.3 Méthodes indirectes de mesure de l’observance ... 169 DIAGNOSTIC EDUCATIF ... 171 3.1 Profil psycho-social ... 171 3.2 Représentations du patient ... 171 3.3 Connaissance du traitement ... 171 3.4 Santé subjective ou perçue ... 172
3.8 Elaboration d’un plan de prise ... 174 3.9 Communication des règles hygiéno-diététiques ... 175 Prise en charge psychologique ... 175
Chapitre VI : UN LOGICIEL DE GESTION DANS LA PRISE EN CHARGE DES PATIENTS
CANCEREUX SOUS THERAPIE CIBLEE ... 177 I. Les outils pharmaceutiques à disposition ... 177 II. Projet système d’information pour les pharmaciens d’officine ... 177
Concepts théoriques d’informatique ... 178 1.1 Système d’information « SI » ... 178 1.1.1 Définition... 178 1.1.2 Fonctions de système d’information « SI » ... 179 1.1.3 L’architecture des systèmes d’information ... 179 1.1.4 Modélisation de l’information ... 180 Méthode systématique du concept de SI « Merise » ... 180 Le niveau conceptuel ... 181 Le niveau logique ou organisationnel ... 181 Le niveau physique ... 181 1.2 Description de logiciel ... 182 1.3 Modélisation d’une base de données au niveau conceptuel « MCD » « Pharma oncother » ... 183 CONCLUSION ... 186 Recommandations et perspectives ... 188 Résumé ... 193 ANNEXES ... 197 BIBLIOGRAPHIE ... 209 Serment galien ... 219
Introduction
La thérapie ciblée est une innovation thérapeutique prometteuse, un dogme principal de la médecine personnalisée "ou médecine de précision" qui est en voie de changer les paradigmes de traitement en oncologie.
La première occurrence de la notion de médecine ciblée, du moins dans sa signification actuellement dominante de médecine génomique moléculaire personnalisée, remonte à la fin des années 1990. Son contexte d’émergence est le « Human Genome Program » le programme de séquençage intégral du génome humain. La médecine ciblée consiste à l’implication intense des connaissances moléculaires et des technologies biomédicales dans le domaine d’oncologie.[1]
La médecine ciblée est devenue le nouveau paysage des politiques de santé à l’échelle mondiale qui a suscité la mobilisation de tous les acteurs de santé : chercheurs et cliniciens.
La leucémie myéloïde chronique est l'une des hémopathies malignes à pronostic sombre qui a suscité depuis des décennies les travaux de recherche en raison de sa mortalité, l'avènement des thérapies ciblées et l'introduction de "GLIVEC" dans l'arsenal thérapeutique pour la prise en charge de la LMC a largement évolué son pronostic à cet issu la LMC est devenue un modèle typique de l'impact révolutionnaire des thérapies ciblées dans le secteur d'onco-hématologique.
Depuis novembre 2017, la firme pharmaceutique Pfizer a mis à la disposition de marché pharmaceutique marocain des médicaments ciblés dans le traitement du cancer du sein métastatique, du cancer du poumon et du cancer du rein métastatique des types de cancer solides à pronostic sombre.
Ce tournant notable dans le domaine d’oncologie nous laisse envisager quel rôle le pharmacien devrait jouer à l’heure actuelle sachant que l’officine pharmaceutique surtout marocaine connait de nombreux défis non résolus, une certaine stagnation surtout dans la mission de prise en charge des maladies chroniques.
La problématique de la prise en charge des patients atteints de maladies chroniques à plusieurs facettes : le suivi personnalisé des patients, l’éducation thérapeutique, l’observance de traitement, la communication patient pharmacien. Les enjeux de l’essor des traitements
cancéreux per os va impliquer les acteurs de santé de ville d’avantage et va mettre en évidence la problématique de prise en charge des patients atteints de maladies chroniques.
L’expertise pharmaceutique va être fortement réclamée dans le processus de prise en charge des patients cancéreux sous thérapies ciblées. Son aspect va être résumé dans deux démarches, la prise de décision en regard de l'état de patient cancéreux dans un travail en synergie avec les autres médecins oncologues et l'expertise participative entre le pharmacien et les autres médecins spécialistes pour la gérance des effets indésirables.
Ce travail de thèse a pour objectif l’élucidation de la problématique de prise en charge des patients cancéreux sous thérapies ciblées.
D’emblée, nous allons faire l’état des lieux de connaissances et théories piliers sur l’oncogenèse qui sont considérées un piédestal de l’émergence de thérapies ciblées ainsi que la physiopathologie de certains cancers solides dont la thérapie ciblée a fait un essor notable, et leurs profils cliniques en vue de développer une politique de dépistage des cancers qui s’appuie sur les pharmaciens, ainsi anticiper les nouvelles perspectives dans cette innovation oncologique.
Le risque iatrogène de médicaments ciblés avec les autres types de médicaments administrés lors de traitements est un autre volet primordial en oncogériatrie en raison de la présence des comorbidités qui est généralement associées à la polymédication. Le système de détection d’interactions médicamenteuses installées dans des logiciels dans les pharmacies d’officine présente des lacunes. Or, un prolongement de la durée du séjour à l’hôpital ou même le décès est fort probable et vraiment conséquent pour cause de l’inadéquation de l’identification des interactions médicamenteuses. Une détection pertinente des interactions médicamenteuses peut aider à prévenir de façon plus efficace la survenue des effets indésirables. Des notions de pharmacocinétique et pharmacodynamique ont été élucidées dans la partie pharmacologie.
Les traitements cancéreux ciblés sont moins nocifs que les agents de chimiothérapie cytotoxique, toutefois ils ne sont pas exempts d’effets secondaires, le profil de toxicité engendré par ces agents est différent de celui de la chimiothérapie. Ce qui nécessite une compréhension
cancéreux per os va impliquer les acteurs de santé de ville d’avantage et va mettre en évidence la problématique de prise en charge des patients atteints de maladies chroniques.
L’expertise pharmaceutique va être fortement réclamée dans le processus de prise en charge des patients cancéreux sous thérapies ciblées. Son aspect va être résumé dans deux démarches, la prise de décision en regard de l'état de patient cancéreux dans un travail en synergie avec les autres médecins oncologues et l'expertise participative entre le pharmacien et les autres médecins spécialistes pour la gérance des effets indésirables.
Ce travail de thèse a pour objectif l’élucidation de la problématique de prise en charge des patients cancéreux sous thérapies ciblées.
D’emblée, nous allons faire l’état des lieux de connaissances et théories piliers sur l’oncogenèse qui sont considérées un piédestal de l’émergence de thérapies ciblées ainsi que la physiopathologie de certains cancers solides dont la thérapie ciblée a fait un essor notable, et leurs profils cliniques en vue de développer une politique de dépistage des cancers qui s’appuie sur les pharmaciens, ainsi anticiper les nouvelles perspectives dans cette innovation oncologique.
Le risque iatrogène de médicaments ciblés avec les autres types de médicaments administrés lors de traitements est un autre volet primordial en oncogériatrie en raison de la présence des comorbidités qui est généralement associées à la polymédication. Le système de détection d’interactions médicamenteuses installées dans des logiciels dans les pharmacies d’officine présente des lacunes. Or, un prolongement de la durée du séjour à l’hôpital ou même le décès est fort probable et vraiment conséquent pour cause de l’inadéquation de l’identification des interactions médicamenteuses. Une détection pertinente des interactions médicamenteuses peut aider à prévenir de façon plus efficace la survenue des effets indésirables. Des notions de pharmacocinétique et pharmacodynamique ont été élucidées dans la partie pharmacologie.
Les traitements cancéreux ciblés sont moins nocifs que les agents de chimiothérapie cytotoxique, toutefois ils ne sont pas exempts d’effets secondaires, le profil de toxicité engendré par ces agents est différent de celui de la chimiothérapie. Ce qui nécessite une compréhension plus approfondie de tableau clinique de chaque effet ainsi que les mécanismes de sa génèse, ce qui va conditionner une prise en charge pertinente et augmenter la tolérance de « SMART
DRUG».La médecine complémentaire est l’un des thèmes controversés, à laquelle la plupart des patients cancéreux ont recours et qui nécessite un encadrement et une vigilance accrue de la part des professionnels de santé notamment les pharmaciens.
L’objectif ultime de ce travail de thèse est de motiver le pharmacien d’officine à devenir un maillon essentiel dans la chaine de cancérologie qui englobe plusieurs professionnels de santé dont les oncologues, les anatomo-pathologistes, les psychothérapeutes et les infirmiers en lui conférant les connaissances nécessaires et les outils indispensables.
Chapitre I : Connaissances
oncologiques primordiales
Chapitre I : Connaissances oncologiques primordiales
destinées au pharmacien
Le 1er chapitre de cette thèse va prodiguer des connaissances basiques et primordiales pour le pharmacien d’officine dans le domaine d’oncologie en relevant, les différents concepts et paradigmes qui ont contribué à l’émergence de la thérapie ciblée, la physiopathologie des types de cancers que la biothérapie a changé le pronostic, ainsi que la maîtrise des tableaux cliniques de types de cancers par le pharmacien va permettre d’orienter le patient et sauver sa vie surtout dans les cas de certains types de cancers qui se développent de façon discrète jusqu’à un stade tardif lorsque la maladie présente un pronostic sombre. Le rôle primordial de pharmacien est de déceler ces symptômes, d’orienter le patient vers les professionnels de santé adéquats. Le pharmacien d’officine doit être au courant des différentes limitations des thérapies ciblées et les nouvelles pistes thérapeutiques et voies de recherches à envisager dans l’avenir proche.
I. HISTORIQUE DU TRAITEMENT DU CANCER
La thérapie ciblée est le résultat d’un long parcours de travaux de recherches, visé à découvrir les mécanismes responsables de phénotype tumoral au cours de dernier siècle. Avant l’avènement des thérapies ciblées, ces travaux de recherches ont contribué à la conception de différents traitements en oncologie (figure 1). [1]
Ainsi, les traitements du cancer peuvent être subdivisés en deux catégories distinctes : [1] Les traitements classiques dits de 1ére génération : la chimiothérapie, la radiothérapie, l’hormonothérapie utilisée dans le traitement du cancer du sein et dans le traitement du cancer de la prostate.
Les traitements innovants dits de 2éme génération qui ont initié l’ère de la médecine personnalisée et qui sont subdivisés en deux catégories : les traitements ciblés (traitements par les anticorps monoclonaux et les inhibiteurs de kinases) et l’immunothérapie.
FIGURE 1 : Chronologie des traitements classiques et innovants du cancer [1]
II. ONCOGENESE
L’oncogenèse ou la cancérogenèse est un processus de multiplication anarchique de cellules normales, échappant aux mécanismes stricts de la régulation cellulaire lors de la division cellulaire, en atteignant d’autres organes cibles « processus métastatique ». [2]
Plusieurs mécanismes contribuent à l’émergence de phénotype tumoral et pour élucider ces mécanismes, plusieurs théories ont été élaborées découlant des observations cliniques in vivo et in vitro. [2]
Théorie De La Mutagénèse Somatique
Le principe de la cancérogénèse en multi-étapes intitulé le modèle du cancer à plusieurs étapes « multistage model of cancer » postule que le cancer évolue en étapes distinctes. [3] Les 1ers qui ont conceptualisé ce principe sont les deux scientifiques P. Armirage et R. Doll en 1954. Ce principe découle de la théorie de la mutagénèse somatique qui a régné durant le XXe siècle, qui définit le cancer comme une maladie cellulaire par atteinte d’ADN.[4]
Les mutations du génome confèrent au terme d’un processus multi-étapes, l’acquisition de mutations aléatoires successives, des clones cellulaires de plus en plus agressifs seraient sélectionnés, faisant émerger un phénotype tumoral (figure 2). [3 ; 4]
FIGURE 2 : Théorie des mutations somatiques [5]
1.1 Initiation « Phase infraclinique »
La première étape du processus de la cancérogénèse en multi-étapes est la phase de l’initiation. Cette phase résulte d'une altération génétique irréversible, très probablement une ou plusieurs mutations simples, transversions, transitions et / ou petites délétions dans l'ADN, provoquées par un agent génotoxique dit initiateur. Ces agents initiateurs sont soit des agents chimiques, physiques « rayons UV » ou biologiques « le cas des virus ». Des données récentes d'études moléculaires sur des tissus prénéoplasiques du poumon et du côlon humain impliquent les modifications épigénétiques comme un événement précoce de la carcinogenèse, la méthylation de l'ADN des régions promotrices des gènes peut inhiber la transcription des gènes suppresseurs de tumeurs. Pour que les mutations s’accumulent, elles doivent apparaître dans des cellules qui prolifèrent et survivent au cours de la vie de l’organisme.[6]
En dépit de la survenue des altérations génétiques et épigénétiques, les cellules résultantes ne sont pas des cellules tumorales, elles n’ont pas encore acquis une autonomie de croissance et ces cellules initiées peuvent rester quiescentes sans proliférer si elles ne subissent pas l’étape suivante, la promotion.[6]
1.2 Promotion
C’est une étape cruciale dans la formation de clones tumoraux distincts, c’est un stade réversible. Ce stade de promotion n’implique pas des changements dans la structure de l'ADN, mais plutôt dans l'expression du génome médiée par des interactions promoteur-récepteur. Le stade final irréversible de la progression est caractérisé par une instabilité caryotypique et une croissance maligne. L'apparition d'un clone cellulaire tumoral malin serait ainsi la conséquence d’une accumulation dans une seule cellule d'anomalies liées à des événements rares et non reliés entre eux. Cette nécessité d'une succession dans le temps de multiples altérations cellulaires se reflète bien dans l'augmentation de la fréquence des cancers en fonction de l'âge.[6]
1.3 Progression « Phase clinique »
C’est l’étape ultime dans le développement du cancer, la néoplasie est cliniquement détectable. La tumeur va commencer à coloniser d’autres parties du corps et va constituer des métastases grâce à des enzymes et à différents facteurs de croissances. La vitesse de croissance des cancers diffère d’un tissu à l’autre.[6]
Dans le modèle du cancer à plusieurs étapes « multistage model of cancer », la cellule maligne accumule des lésions génétiques et épigénétiques dans des cibles moléculaires clés : les oncogènes (gènes qui favorisent le cancer) et les suppresseurs de tumeurs (gènes qui empêchent la prolifération du cancer). À la fin de leur processus de transformation, les cellules cancéreuses perdent leur identité cellulaire et acquièrent l'indépendance de croissance et la résistance à l’apoptose. [7]
FIGURE 3 : Les trois phases de la cancérogenèse : initiation, promotion, progression [5]
La théorie de la mutagénèse somatique dont découle le principe de la cancérogénèse en multi-étapes a été maintes fois adoptée comme l'explication la plus probable du début de la cancérogenèse. [4] [6]
Dans les années 2000, la publication de Douglas Hanahan et Robert Weinberg a apporté une métaphore en oncologie, un pilier dans la compréhension de la génèse des cancers, en introduisant le concept «hallmarks of cancer» qui confère des caractéristiques inhérentes aux cellules malignes (figure 4), [8] ce qui marque un changement majeur dans le paradigme centro-cellulaire dont la théorie de la mutagénèse somatique a été fondée, le cancer n’est plus définit par des altérations génomiques, mais par l’acquisition des caractéristiques comportementales secondaires aux modifications génomiques. Ces caractéristiques peuvent s’exprimer indépendamment les unes des autres. Six caractéristiques clés des cellules malignes étaient proposées par ces deux auteurs : [8]
Échappement à l’apoptose, autosuffisance pour les signaux de croissance, insensibilité aux signaux antiprolifératifs, stimulation de l’angiogenèse, potentiel illimité de réplication et capacité d’évasion tissulaire et de métastases.
FIGURE 4 : Six caractéristiques clés de la cellule maligne [8]
En 2011, deux nouvelles caractéristiques s’ajoutaient aux précédentes, la reprogrammation du métabolisme énergétique (effet Warburg) et l’évasion à la surveillance immunitaire.[9]
FIGURE 5 : Poinçons et caractéristiques habilitantes émergents 2011 [9]
L’article de Hanahan et Weinberg publié en 2011 marque une rupture conceptuelle du concept centro-cellulaire de la théorie de la mutagénèse somatique et confirme largement la théorie du champ d’organisation tissulaire TOFT [7] appelée ainsi « la théorie des systèmes ». La théorie du champ d’organisation tissulaire postule que la cancérogénèse est un processus qui s’apparente avec la morphogénèse tissulaire. Au cours de développement, la prolifération et le processus de métastase sont un défaut de toutes les cellules. [10]
Le paradigme centro-cellulaire a été remplacé par une vision holistique qui contribue à l’environnement tumoral un rôle majeur dans le processus de la cancérogenèse. [11]
MICROENVIRONNEMENT TUMORAL
Le rôle majeur de la contribution du microenvironnement de la cellule maligne dans les différentes étapes de la génèse de phénotype tumoral (initiation, progression) n’est pas récent ; il remonte à 1889 au Stephan Paget par son hypothèse intitulée « des semences et du sol ». [12]
interactions entre les cellules tumorales et les autres cellules qui constituent leur microenvironnements (les cellules stromales et les cellules de la matrice extracellulaire) (Figure 6). Cette vision récemment revue fournit une explication aux différentes situations cliniques problématiques. [11 ; 13]
Le postulat de Stephen Paget a été confirmé par des études cliniques, la plus notable, c’est celle menée par Merlo et al en 2006, qui montre que la majorité des décès liés au cancer sont le résultat de la résistance des métastases aux traitements conventionnels. Les changements que subit la cellule tumorale induits par le microenvironnement pourraient expliquer le phénomène de chimiorésistances. [14]
FIGURE 6 : Schéma simplifié des différents composants du microenvironnement
tumoral et les différentes interactions entre eux [11]
L’explication de la structure et du contenu du (Tumor microenvironment) TME (figure 6) est une étape cruciale pour comprendre comment les cellules tumorales se développent et envahissent plus profondément les tissus. [11]
Outre les microorganismes et les leucocytes, les composants cellulaires du microenvironnement se constituent de fibroblastes, de vaisseaux sanguins constitués eux aussi de péricytes et de cellules endothéliales. Ces types de cellules qui vivent dans le stroma ont des caractères dynamiques, elles interagissent les uns avec les autres ainsi qu'avec les cellules tumorales via les facteurs de croissance, les cytokines et les molécules d’adhésion. Les interactions dynamiques entre les cellules épithéliales et stromales jouent un rôle essentiel dans les différents processus du développement du cancer telles que l’adhésion, la prolifération, la différentiation et la migration cellulaire. Le composant non cellulaire du stroma est la matrice extracellulaire (MEC) composée de la matrice interstitielle et de la membrane basale. La matrice interstitielle se constitue de collagène, des protéoglycanes et des glycoprotéines tandis que la membrane basale se compose de la fibronectine, des laminines, de collagène type IV et des protéines de liaison. [11 ; 15]
Le microenvironnement se définit comme un ensemble de compartiments acellulaires et cellulaires constitués de cellules cancéreuses, vasculaires, neuroendocrines, stromales, épithéliales, et immunitaires. Ces compartiments cellulaires et acellulaires forment un ensemble hétérogène, dynamique et communicant.[11]
ANGIOGENESE
L’angiogénèse ou la néoangiogénèse littéralement désigne le mécanisme de la formation d’un réseau vasculaire à partir des vaisseaux préexistants, c’est l’un des incontournables «hallmarks of cancer» décrit par Hannahan et Weinberg, elle constitue une étape cruciale de la formation des métastases. [16]
En 1971, Judah Folkman était l’un des pionniers qui ont conçu cette hypothèse en admettant que la tumeur pour accroitre au-delà de 2 mm3 nécessite de générer son propre réseau vasculaire pour assurer un apport suffisant en énergie et en oxygène, ce qui correspond au « Switch angiogénique » (figure 7). [17]
FIGURE 7 : Passage de la tumeur de la phase latente à la phase invasive « SWITCH »
angiogénique [18]
L’angiogénèse tumorale est un processus local qui correspond à la formation de néovaisseaux à partir des vaisseaux avoisinant la tumeur, les cellules endothéliales jouent un rôle essentiel, sous la dépendance de divers stimuli (facteurs de croissance, cytokines, chimiokines) générés par la tumeur (figure 8) et en suivant plusieurs étapes. [18 ; 19]
Dans le parcours de développement de la tumeur, à un stade critique l’apport vasculaire de tissu dans lequel la tumeur se développe, ne suffit pas ; une ischémie régnant dans les zones avascularisées de la tumeur, l’hypoxie résultante va stimuler massivement l’expression d’un facteur de croissance clé de l’angiogenèse le VEGF (vascular endothelium growth factor) appelé ainsi facteur pro-angiogénique qui va activer la prolifération endothéliale pour vasculariser la tumeur.[19]
Dans les conditions normales appelées « angiogénèse physiologique » qui déroule dans des situations cliniques précises, tels que la cicatrisation des plaies, les cycles de menstruation, la formation de placenta, il existe un équilibre entre les facteurs pro- angiogéniques et les facteurs anti-angiogéniques. [20]
Dans la pathologie tumorale, cet équilibre se rompt, la tumeur acquiert un pouvoir angiogénique et va exprimer massivement les facteurs pro-angiogéniques (figure 9), ce qui se traduit par une stimulation permanente de l’angiogenèse pathologique. Cette stimulation dérégulée des facteurs pro-angiogéniques donne naissance à un réseau vasculaire tumoral désorganisé, anarchique et hémorragique (figure 10). [18]
FIGURE 8 : Déséquilibre de l’expression des facteurs pro-angiogéniques et
FIGURE 9 : Différentes étapes de l’angiogénèse dans la vascularisation de la
tumeur [21]
FIGURE 10 : Réseau vasculaire tumoral sous l’effet de VEGF visionné sous
![FIGURE 6 : Schéma simplifié des différents composants du microenvironnement tumoral et les différentes interactions entre eux [11]](https://thumb-eu.123doks.com/thumbv2/123doknet/15039756.691326/57.892.127.754.450.941/figure-schéma-simplifié-composants-microenvironnement-tumoral-interactions.webp)
![FIGURE 7 : Passage de la tumeur de la phase latente à la phase invasive « SWITCH » angiogénique [18]](https://thumb-eu.123doks.com/thumbv2/123doknet/15039756.691326/59.892.114.766.103.463/figure-passage-tumeur-phase-latente-invasive-switch-angiogénique.webp)
![FIGURE 8 : Déséquilibre de l’expression des facteurs pro-angiogéniques et anti- anti-angiogéniques [18]](https://thumb-eu.123doks.com/thumbv2/123doknet/15039756.691326/60.892.157.723.293.630/figure-déséquilibre-expression-facteurs-angiogéniques-anti-anti-angiogéniques.webp)

![FIGURE 15 : Schéma représentatif de RTK et les différentes voies de signalisation cellulaires [35]](https://thumb-eu.123doks.com/thumbv2/123doknet/15039756.691326/67.892.112.786.133.548/figure-schéma-représentatif-rtk-voies-signalisation-cellulaires.webp)
![FIGURE 16 : Différentes sous-familles ou prototypes de récepteurs de tyrosine kinases [37]](https://thumb-eu.123doks.com/thumbv2/123doknet/15039756.691326/68.892.108.787.141.516/figure-familles-prototypes-récepteurs-tyrosine-kinases.webp)
![TABLEAU 1 : Anticorps monoclonaux thérapeutiques commercialisés par l’autorisation de la FAD en 2012 [44]](https://thumb-eu.123doks.com/thumbv2/123doknet/15039756.691326/79.892.108.779.238.561/tableau-anticorps-monoclonaux-thérapeutiques-commercialisés-l-autorisation-fad.webp)
