HAL Id: dumas-01676596
https://dumas.ccsd.cnrs.fr/dumas-01676596
Submitted on 5 Jan 2018
HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Le médicament : un facteur précipitant les chutes chez le
sujet âgé, revue d’ordonnances de patients admis en
service de soins de suite et de réadaptation gériatrique
pour chute
Morgane Boenisch
To cite this version:
Morgane Boenisch. Le médicament : un facteur précipitant les chutes chez le sujet âgé, revue
d’ordonnances de patients admis en service de soins de suite et de réadaptation gériatrique pour chute . Sciences pharmaceutiques. 2017. �dumas-01676596�
HAL Id: dumas-01676596
https://dumas.ccsd.cnrs.fr/dumas-01676596
Submitted on 5 Jan 2018
HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Le médicament : un facteur précipitant les chutes chez
le sujet âgé, revue d’ordonnances de patients admis en
service de soins de suite et de réadaptation gériatrique
pour chute
Morgane Boenisch
To cite this version:
Morgane Boenisch. Le médicament : un facteur précipitant les chutes chez le sujet âgé, revue
d’ordonnances de patients admis en service de soins de suite et de réadaptation gériatrique pour chute . Sciences pharmaceutiques. 2017. <dumas-01676596>
UNIVERSITE DE BORDEAUX
FACULTE DE SCIENCES PHARMACEUTIQUES
Année 2017 Thèse n°115
THESE
Présentée pour l’obtention du DIPLOME D’ETAT DE DOCTEUR EN PHARMACIE Soutenue publiquement le Mardi 19 Décembre 2017
Par
Mlle Morgane BŒNISCH
Née le 02/05/1993 à Agen
Dirigée par Mme le Docteur Stéphanie MOSNIER-‐THOUMAS
Président du jury : Mlle le Professeur Marie-‐Claude Saux (Pharmacien hospitalier)
Membres du jury : Mme le Docteur Stéphanie MOSNIER-‐THOUMAS (Pharmacien hospitalier) Mme le Docteur Joanne JENN (Médecin Gériatre)
Mr le Docteur Benoit LIGEOIX (Pharmacien officinal)
LE MEDICAMENT : UN FACTEUR PRECIPITANT
LES CHUTES CHEZ LE SUJET AGE
REVUE D’ORDONNANCES DE PATIENTS ADMIS EN SERVICE DE
SOINS DE SUITE ET DE READAPTATION GERIATRIQUE
TABLE DES MATIERES :
Liste des tableaux 5 Liste des figures 6 Liste des annexes 7 Remerciements 8 Introduction 9 PARTIE 1 : LES CHUTES CHEZ LE SUJET AGE : FACTEURS DE RISQUES ET CONSEQUENCES
I-‐ Le vieillissement 11
Définition 11
1-‐
Effets du vieillissement sur l’organisme 11
2-‐
Mécanismes moléculaires du vieillissement 11
3-‐
Démographie et aspects sociaux du vieillissement 13
4-‐
Concept de fragilité 15
5-‐
II-‐ Définition de la chute 15
III-‐ Facteurs prédisposants et facteurs précipitants la chute 16
1-‐ Facteurs prédisposants : 18
Modifications physiques et physiologiques du sujet âgé 18
a. Modifications cardiovasculaires liées à l’âge 18
b. Modifications du système nerveux liées à l’âge 21
i. Modifications fonctionnelles 21
ii. Démences vasculaires et démences de types Alzheimer 23
iii. Maladie de Parkinson 27
iv. Dépression 28
v. Troubles du sommeil 29
c. Modifications du système locomoteur : 29
Troubles ostéo-‐articulaires, musculaires, et de la marche 29
i. Affections ostéo-‐articulaires 30
ii. Affections articulaires 32
iii. Troubles musculaires 33
iv. Troubles de la marche et de l’équilibre 34
d. Atteintes visuelles 36
e. Dénutrition 37
f. Modifications pharmacocinétiques chez le sujet vieillissant 38
i. Modifications de l’absorption et de la biodisponibilité 38
Evènements précipitants la chute 41
2-‐
a. Facteurs intrinsèques 42
i. Facteurs physiques 42
ii. Facteurs médicamenteux : iatrogénie 45
b. Facteurs extrinsèques 49
LE MEDICAMENT : UN FACTEUR PRECIPITANT LES CHUTES
CHEZ LE SUJET AGE
REVUE D’ORDONNANCES DE PATIENTS ADMIS EN SERVICE DE SOINS DE SUITE ET DE
READAPTATION GERIATRIQUE POUR CHUTE
IV-‐ Conséquences de la chute : 50
Conséquences immédiates : 50
1-‐
Traumatismes, fractures, hémorragies et mortalité 50
Conséquences à moyens terme de la chute : 51
2-‐
Conséquences psychologiques et psychomotrices 51
Conséquences à long terme 52
3-‐
Facteurs de gravité 52
4-‐
V-‐ La chute : un problème de santé publique 56
PARTIE 2 : PLACE DE LA THERAPEUTIQUE DANS LE RISQUE DE CHUTE
I-‐ Evaluation du risque iatrogène et des médicaments potentiellement inappropriés (MPI) 57
2-‐ Critères de Beers 57
3-‐ Liste de LAROCHE 58
4-‐ Critères STOPP/START.v2 59
5-‐ Prescription médicamenteuse chez le sujet âgé (PMSA) 59
II-‐ Rôle de la polymédication : augmentation du risque de chute 60
III-‐ Médicaments augmentant le risque de chute 62
1-‐ Médicaments du système nerveux central 62
a. Benzodiazépines anxiolytiques 62
b. Hypnotiques 67
c. Antidépresseurs 71
d. Neuroleptiques 76
e. Autres médicaments du système nerveux central 80
f. Risque lié à la polyconsommation de psychotropes 80
2-‐ Médicaments du système cardiovasculaire 81
a. Risque d’hypotension orthostatique 81
b. Les médicaments du système cardiovasculaire et les chutes iatrogènes 83
i. Les bêta-‐bloquants 83
ii. Les diurétiques 84
iii. Inhibiteurs de l’enzyme de conversion (IEC) et Sartans 85
iv. Inhibiteurs calciques 86
v. Alpha-‐bloquants 86
vi. Antihypertenseurs centraux 87
vii. Dérivés nitrés 88
viii. Cardiotoniques : la Digoxine 89
ix. Antiarythmiques 89
c. Coprescription de médicaments du système cardiovasculaire 90
3-‐ Médicaments analgésiques opioïdes 91
4-‐ Les médicaments anticholinergiques 92
5-‐ Insuline et sulfamides hypoglycémiants 94
PARTIE 3 : REVUE D’ORDONNANCES DE PATIENTS AGES CHUTEURS EN SSR GERIATRIQUE : COMMENT DIMINUER LE RISQUE IATROGENE ?
I-‐ Contexte et objectifs : 97
1-‐ Contexte 97
2-‐ Objectifs 97
II-‐ Matériel et méthode : 98
2-‐ Critères d’inclusion et d’exclusion : 98
3-‐ Effectifs : 98
4-‐ Déroulement de l’étude : 99
5-‐ Recueil des données : 105
6-‐ Analyse statistique : 107
III-‐ Résultats : 108
1-‐ Caractéristiques de la population 108
2-‐ Analyse du Bilan Médicamenteux Optimisé 115
3-‐ Optimisation thérapeutique réalisée lors de l’hospitalisation 122
4-‐ Rappel des patients à 1 mois 125
5-‐ Rappel des patients à 6 mois 127
IV-‐ Discussion, perspectives : 130
Conclusion 139 Bibliographie 141 Annexes 147 Serment de Galien 168
-‐ TABLEAU 1 : Chiffres clés de la population française entre 1950 et 2060
-‐ TABLEAU 2 : Evolution de l’espérance de vie à 60, 75 et 85 and par sexe de 1950 à 2050 -‐ TABLEAU 3 : Score HAS-‐BLED
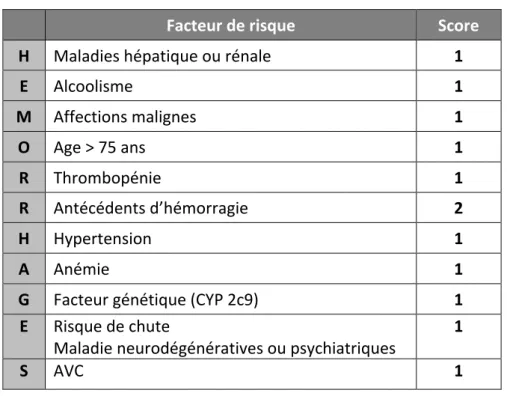
-‐ TABLEAU 4 : Score HEMORR2HAGES
-‐ TABLEAU 5 : Répartition des valeurs de vitamine D en fonction de la saison (CHU de Grenoble, 2007)
-‐ TABLEAU 6 : Familles des benzodiazépines -‐ TABLEAU 7 : Demi-‐vies des benzodiazépines -‐ TABLEAU 8 : Demi-‐vies des hypnotiques
-‐ TABLEAU 9 : Les différents bêta-‐bloquants commercialisés en France -‐ TABLEAU 10 : Médicaments augmentant le risque de chute
-‐ TABLEAU 11 : Répartition des facteurs prédisposants la chute d’origine médicamenteuse retrouvés dans la population de l’étude
-‐ TABLEAU 12 : Répartition des facteurs prédisposants la chute retrouvés dans la population de l’étude
-‐ TABLEAU 13 : Facteurs de risque iatrogéniques induits par les médicaments du système cardiovasculaire retrouvés sur le BMO des patients chuteurs inclus dans l’étude
-‐ TABLEAU 14 : Les différents médicaments du système nerveux central retrouvés sur le BMO
-‐ TABLEAU 15 : Dérivés morphiniques retrouvés sur le BMO
-‐ TABLEAU 16 : Médicaments favorisant le risque de hémorragique retrouvé sur le BMO -‐ TABLEAU 17 : Comparaison du BMO et de l’OMS
-‐ TABLEAU 18 : Blessures liées à la une chute à 1 mois à domicile
-‐ TABLEAU 19 : Etude des prescriptions des patients ayant nouvellement chuté à 1 mois -‐ TABLEAU 20 : Blessures liées à une chute à 6 mois à domicile
-‐ TABLEAU 21 : Etude des prescription des patients ayant nouvellement chuté à 6 mois
-‐ FIGURE 1 : La mutifactorialité de la chute
-‐ FIGURE 2 : Facteurs prédisposants et précipitants la chute
-‐ FIGURE 3 : Coupe de cœur colorés à hémalun-‐éosine illustrant la fibrose cardiaque de remplacement chez le rat
-‐ FIGURE 4 : Tension artérielle systolique et diastolique, selon le sexe et le grope d’âge chez une population vivant à domicile, âgée de 20 à 79 ans, Canada, de 2009 à 2011
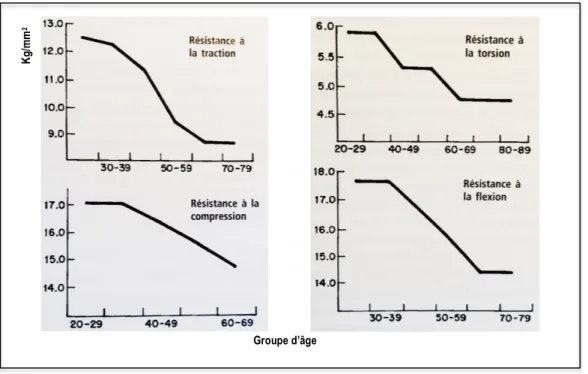
-‐ FIGURE 5 : Effets de l’âge sur le poids du cerveau de l’homme et de la femme -‐ FIGURE 6 : Changements de la résistance de l’os avec l’âge
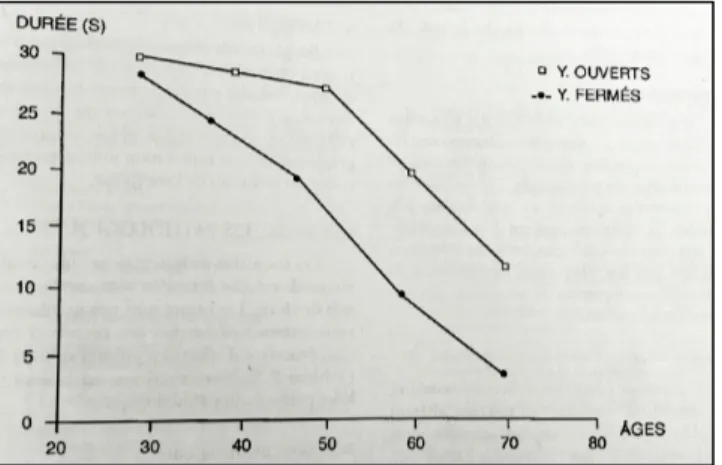
-‐ FIGURE 7 : Temps moyen d’appui sur un seul pied, les yeux ouverts et fermés en fonction de l’âge
-‐ FIGURE 8 : Conséquences psychologiques et psychomotrices
-‐ FIGURE 9 : Signalement des effets indésirables médicamenteux aux centres de pharmacovigilance français entre 1995 et 200 par rapport à l’âge avant et après ajustement à la consommation médicamenteuse
-‐ FIGURE 10 : Structure commune des benzodiazépines
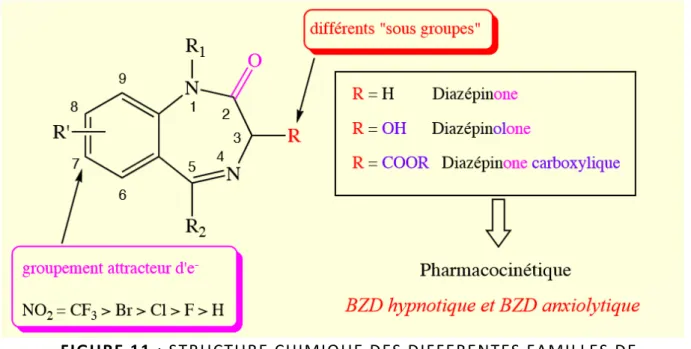
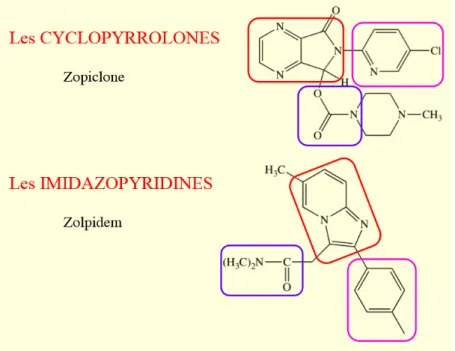
-‐ FIGURE 11 : Structure chimiques des différentes familles de benzodiazépines -‐ FIGURE 12 : Représentation chimique de l’Alprazolam
-‐ FIGURE 13 : Structure chimique du Zolpidem et du Zopiclone -‐ FIGURE 14 : Structure chimique des antidépresseurs tricycliques -‐ FIGURE 15 : Représentation chimique des composés tricycliques -‐ FIGURE 16 : Principales étiologies d’hypotension orthostatique -‐ FIGURE 17 : Répartition de la population de l’étude par classe d’âge -‐ FIGURE 18 : Répartition de la population de l’étude par sexe
-‐ FIGURE 19 : Facteurs prédisposants la chute retrouvés chez les patients inclus dans l’étude -‐ FIGURE 20 : Répartition des MMS chez les patients inclus dans l’étude
-‐ FIGURE 21 : Répartition de débits de filtration glomérulaire chez les patients inclus dans l’étude
-‐ FIGURE 22 : Facteurs iatrogènes retrouvés à l’entrée d’hospitalisation chez les patients inclus dans l’étude
-‐ FIGURE 23 : Nombre de facteurs d’origine médicamenteux prédisposant la chute -‐ FIGURE 24 : Nombre de facteurs de risque retrouvé par patient
-‐ FIGURE 25 : Prescription d’antihypertenseurs retrouvés sur le BMO -‐ FIGURE 26 : Prescription de diurétiques retrouvés sur le BMO -‐ FIGURE 27 : Prescription d’antiarythmiques retrouvés sur le BMO
-‐ FIGURE 28 : Médicaments du système cardiovasculaire inappropriés chez la personne âgée retrouvés sur le BMO
-‐ FIGURE 29 : Prescription de psychotropes retrouvés sur le BMO
-‐ ANNEXE 1 : Critères de Beers -‐ ANNEXE 2 : Liste de Laroche -‐ ANNEXE 3 : Critères STOPP/START
-‐ ANNEXE 5 : Plan de prise des médicaments remis au patient et aux aidant -‐ ANNEXE 6 : Fiche « Prévention des chutes d’origine médicamenteuse »
Aux membres du jury,
A Mademoiselle Marie-‐Claude SAUX, je vous remercie d’avoir accepté de présider ce jury. A Madame Stéphanie MOSNIER-‐THOUMAS, je te remercie sincèrement d’avoir dirigé cette thèse, de ton encadrement, ton implication et tes recommandations.
A Monsieur Benoit LIGEOIX, pour me faire l’honneur de participer à ce jury et pour m’avoir montrer le métier de pharmacien officinal pendant les trois années passées à tes côtés.
A Madame Joanne JENN, pour me faire l’honneur de participer à ce jury et pour m’avoir accueilli dans votre service.
Au service de SSR2 de l’hôpital Xavier Arnozan,
Aux docteurs JENN et FOUCAUD, aux internes en médecine et en pharmacie, et aux équipes du service de m’avoir accueilli durant mes différents stages de cinquième année, de m’avoir montré l’importance de l’optimisation thérapeutique en gériatrie, et de m’avoir permis de réaliser cette étude.
A la pharmacie Saint-‐Pierre, à Gradignan,
Pour leur formation et leur conseil tout au long des trois années passées durant mes études de pharmacie.
A mes parents,
Je tiens à vous remercier du fond du cœur, pour tout l’amour et le soutien que vous m’avez apporté depuis toujours. Merci à ma mère, qui n’a cessé de me faire réviser, de l’école primaire jusqu’à l’examen de validation de stage de sixième année de pharmacie. Papa, Maman, c’est grâce à vous qu’aujourd’hui je deviens docteur en pharmacie. Merci.
A Romain, pour ton amour, ta présence et ton soutien, pour cette thèse et au quotidien, et pour tout le bonheur que tu m’apportes chaque jour.
A ma grand-‐mère, Andrée Gabrielle BŒNISCH, qui aurait été tellement heureuse et fière d’afficher cette thèse sur le buffet, au côté de mes bulletins de note.
On estime qu’un tiers des sujets de plus de 65 ans et la moitié des plus de 80 ans font une ou plusieurs chutes par an.
L’incidence des chutes et la sévérité des complications liées aux chutes augmentent avec l’âge. Les chutes sont associées à un mauvais pronostic : elles majorent hospitalisation, dépendance, entrée en institution et entraine un taux de mortalité important.
La polypathologie du patient âgé lié conduit à un excès de prises médicamenteuses qui explique l’incidence élevée des effets indésirables, à l’origine de 5 à 10% des hospitalisations après 65 ans et 20% après 80 ans.
Le sujet âgé est plus sensible aux effets des médicaments car :
-‐ Il présente plusieurs pathologies, ce qui induit souvent une polymédication
-‐ Le métabolisme des médicaments est altéré avec le vieillissement, notamment en raison de la diminution de la fonction rénale
-‐ Les effets secondaires sont plus fréquents Ce qui entraine une augmentation du risque de chute.
Ces chutes ont une origine multifactorielle, certains facteurs sont modifiables, d’autres non.
Une intervention multifactorielle réduit de 30 à 40% le taux de rechute. Il existe plusieurs points sur lesquels on peut agir, notamment la prise de médicament.
En effet, de nombreuses ordonnances comportent des médicaments potentiellement inappropriés et des associations qui favorisent le risque de chute. En réévaluant la pertinence
de la prescription des patients âgés, on diminue le risque de iatrogénie.
I- Le vieillissement :
Définition :
1-Le vieillissement correspond à l’ensemble des processus physiologiques et psychologiques qui
modifient la structure et les fonctions de l’organisme à partir de l’âge mûr. C’est la dernière
période de la vie normale, caractérisée par un ralentissement des fonctions de l’organisme. Il est la résultante des effets intriqués de facteurs génétiques (vieillissement intrinsèque, sénescence) et de facteurs environnementaux auxquels est soumis l’organisme tout au long de sa vie.
Le vieillissement est universel et inéluctable. C’est un processus physiologique, long et progressif, à distinguer de la maladie et de ses manifestations.
L’état de santé d’une personne résulte habituellement des effets du vieillissement, associés aux effets de maladies passées, actuelles, chroniques ou aiguës. (1, 2)
Effets du vieillissement sur l’organisme :
2-Le vieillissement s’accompagne d’une diminution des capacités fonctionnelles du corps. Les principales fonctions atteintes sont les variables fonctionnelles de l’organisme, ainsi que sa
capacité à s’adapter aux situations d’agressions.
La régulation des paramètres physiologiques est moins efficace : le retour à l’homéostasie est plus lent, on observe des phénomènes d’échappement aux valeurs de base.
Les études de mesure du vieillissement sont complexes (3). En effet, le vieillissement est très variable d’un organe à l’autre ainsi que d’un individu à l’autre. On parle respectivement de
vieillissement inter-‐organe et de vieillissement interindividuel.
La population âgée se caractérise ainsi par une forte hétérogénéité.
Mécanismes moléculaires du vieillissement :
3-On ne connaît pas aujourd’hui un processus biologique unique qui expliquerait l’origine et les conséquences du vieillissement. L’avancée des connaissances actuelles montre que c’est un processus multifactoriel.
PARTIE 1 : LES CHUTES CHEZ LE SUJET AGE :
FACTEURS DE RISQUES ET CONSEQUENCES
Les différents facteurs impliqués identifiés sont :
• Les facteurs génétiques : la fréquence des altérations de l’ADN (délétions et mutations) et les anomalies de réparation augmentent de façon importante avec l’âge. Des facteurs
extérieurs, comme des agents intercalants des bases de l’ADN, l’exposition aux radiations
et aux rayons UV, et des facteurs intrinsèques, comme des troubles de la division cellulaire, interviennent. L’altération de l’ADN a de nombreuses conséquences en modifiant l’expression de certains gènes et la synthèse des protéines qu’ils commandent, en perturbant le cycle cellulaire ou l’apoptose programmée.
• Les radicaux libres ou espèces réactives de l’oxygène ROS : ce sont des espèces radicalaires formées dans la cellule lors du métabolisme de l’oxygène qui altèrent les structures cellulaires (ADN, membrane plasmique). La production de ces radicaux libres augmentent lors du vieillissement, notamment au niveau des mitochondries, et de plus les capacités de l’organisme à se protéger diminuent (baisse des systèmes enzymatiques : superoxyde dismutase, catalase ; baisse des systèmes de réparation des dommages occasionnés par les espèces réactives).
L’équilibre est rompu, ce qui conduit à un stress oxydatif qui serait impliqué dans plusieurs maladies (cancers, pathologies cardiovasculaires, sclérose latérale amyotrophique ou Maladie de Charcot, maladie d’Alzheimer, maladie de Parkinson).
• La glycation non enzymatique des protéines : c’est une réaction qui se forme entre les sucres et les protéines, notamment celles des molécules à très longue demi-‐vie comme le collagène, l’élastine, ou l’ADN. La réaction glucose + protéine va former des Bases de Schiff, qui vont s’accumuler et donner des AGE (Advanced Glycation End-‐Products). Ce sont des composés terminaux de glycation, capables d’activer des récepteurs spécifiques situés sur les macrophages, de stimuler la libération de facteurs de croissance et de cytokines pro-‐ inflammatoire. De plus, les AGE induisent la formation de pontages moléculaires, ou cross-‐
links, qui rigidifient les structures comme le collagène.
La glycation modifie les propriétés de ces protéines, les rendant plus résistantes à la protéolyse et empêchant leurs renouvellements. L’accumulation de ses macromolécules glyquées chez l’individu âgé, joue un rôle dans le vieillissement de l’organisme (appareil cardiovasculaire, peau, tendons, cristallin, glomérule rénal).
• L’altération des protéines de choc thermique ou Heat Schock Protein HSP : elles sont normalement produites en réponse aux agressions (choc thermique, traumatismes,
glucocorticoïdes). Au cours du vieillissement, la sécrétion de ces protéines est diminuée : les cellules sont moins résistantes en cas d’agression, les systèmes de réparation sont moins stimulés, le catabolisme des macromolécules endommagées est moins performant. (2,4,5,6)
Les altérations moléculaires entraînent ainsi des altérations cellulaires :
Les dommages à l’ADN et les radicaux libres étant plus nombreux avec le vieillissement, la cellule se protège en entrant en sénescence, plutôt qu’en apoptose. Ce mécanisme permet de bloquer la cellule quand son matériel est endommagé. L’accumulation de cellules sénescentes est un phénomène pouvant expliquer le vieillissement.
Les caractéristiques de la cellule sénescente sont :
-‐ Désensibilisation aux facteurs de croissance et d’apoptose
-‐ Augmentation de la taille de la cellule et de la taille des noyaux avec parfois polynucléation
-‐ Changement dans la structure de la chromatine
-‐ Augmentation de l’activité lysosomiale et de l’activité autophagique
-‐ Formation d’agrégats lipido-‐protéiques : accumulation de lipofuscine, pigment qui résulte de la dégradation des organites cellulaires et qui entrave le fonctionnement cellulaire.
-‐ Diminution de l’activité des télomérases qui se manifeste par un raccourcissement des télomères.
Démographie et aspects sociaux du vieillissement :
4-Au 1er janvier 2012, la France compte 65,35 millions d’habitants, parmi lesquels 17,1% de
personnes de plus de 65 ans, dont plus de la moitié a plus de 75 ans.
Le nombre de personnes de plus de 60 ans a crû de 22,6% en 10 ans. Comme on peut le voir dans le TABLEAU 1, entre 1950 et 2000, le nombre de personnes de plus de 60 ans a doublé (9 444 000 contre 4 727 000) et le nombre de personnes de plus de 85 a lui été multiplié par 6 entre 1950 et 2000 (1 236 000 en 2000 contre 201 000 individus âgés en 1950). D’après les prévisions démographiques de l’INSEE, en 2060 les plus de 60 ans représenteront quasiment
un tiers de la population française. Les plus de 75 ans auront doublé par rapport à 2012, et les
plus de 85 ans seront plus de 5 millions. (7,9,10)
TABLEAU 1 : CHIFFRES CLES DE LA POPULATION FRANÇAISE ENTRE 1950 ET 2060
Année Population totale Naissance Décès 60 ans ou plus 75 ans ou plus 85 ans ou plus
1950 1980 1990 2000 2012 2060 (p) 41 647 000 53 731 000 56 577 000 60 508 000 65 350 000 73 600 000 858 000 858 000 800 000 742 000 822 000 non connu 530 000 547 000 526 000 533 000 571 000 non connu 4 727 000 7 541 000 7 872 000 9 444 000 11 174 900 23 600 000 1 565 000 3 079 000 3 838 000 4 225 000 5 850 800 11 900 000 201 000 567 000 874 000 1 236 000 non connu 5 400 000 Source : INSEE
Ce vieillissement de la population résulte de l’effet conjugué de la baisse de la natalité associée à la baisse de la mortalité des plus de 60 ans.
Depuis 1900, l’espérance de vie des populations des pays industrialisés a gagné environ 30 ans.
L’espérance de vie aux âges élevés a fortement progressé. A 60 ans, elle n’était au début du
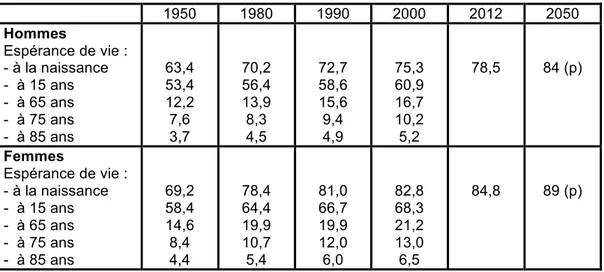
siècle que de 13 ans pour les hommes et 15 ans pour les femmes, elle est aujourd’hui respectivement de 20 ans pour les hommes et 26 ans pour les femmes. En 2020, elle devrait être de l’ordre de 23 et 28 ans. Les derniers chiffres de 2012 montrent une espérance de vie de 78,5 ans pour les hommes et 88,4 ans pour les femmes, soit une progression de 25 ans depuis 1950 comme le montre le TABLEAU 2. (7,8,10)
TABLEAU 2 : EVOLUTION DE L’ESPERANCE DE VIE A 60, 75 ET 85 ANS PAR SEXE
DE 1950 A 2050 1950 1980 1990 2000 2012 2050 Hommes Espérance de vie : - à la naissance - à 15 ans - à 65 ans - à 75 ans - à 85 ans 63,4 53,4 12,2 7,6 3,7 70,2 56,4 13,9 8,3 4,5 72,7 58,6 15,6 9,4 4,9 75,3 60,9 16,7 10,2 5,2 78,5 84 (p) Femmes Espérance de vie : - à la naissance - à 15 ans - à 65 ans - à 75 ans - à 85 ans 69,2 58,4 14,6 8,4 4,4 78,4 64,4 19,9 10,7 5,4 81,0 66,7 19,9 12,0 6,0 82,8 68,3 21,2 13,0 6,5 84,8 89 (p)
De plus, l’espérance de vie sans incapacité a également augmenté.
La pratique médicale peut non seulement allonger la durée de vie mais aussi retarder la perte d’autonomie. L’étude épidémiologique coordonnée par Alvar Svanborg à Göteborg sur 3 cohortes de septuagénaires a montré que le nombre et la gravité des maladies liées à l’âge ont reculé (11).
L’allongement de la durée de vie a ainsi entrainé un vieillissement graduel de la population, ce qui pose un problème social et médical : il nécessite une stratégie globale et une approche
pluridisciplinaire.
Concept de fragilité :
5-Il est courant en gériatrie que deux patients de même âge, ayant des comorbidités comparables évoluent très différemment lorsqu’ils sont confrontés à la même pathologie aiguë. Ce constat traduit le plus souvent un syndrome de fragilité chez l’un des deux patients. Le concept de fragilité permet de décrire un risque plus élevé d’entrée en dépendance, de morbidité et de mortalité. Il représente une probabilité élevée d’évolution péjorative face à une situation. Il n’existe pas de définition consensuelle de la fragilité, c’est un concept complexe. Une des définitions qu’on peut retrouver du concept de fragilité est l’association de maladies chroniques à une perte des réserves adaptatives, liée au vieillissement. Il se caractérise par une instabilité permanente.
La fragilité est très variable entre les individus. On peut observer un décalage entre le stimulus et la réponse, que ce soit dans le domaine moteur ou comportemental. Elle conduit à l’amplification de déficits fonctionnels et/ou un renforcement de situations pathologiques préexistantes.
La personne âgée devenue fragile est alors exposée à une morbidité accrue, avec la survenue ou l’accentuation d’une perte d’autonomie pouvant conduire à la dépendance.
Les marqueurs cliniques les plus pertinents d’un état de fragilité que l’on peut citer sont : la chute, le syndrome confusionnel et l’incontinence.
Quatre paramètres permettent de dépister l’état de fragilité : la fonction musculaire, la capacité aérobie, l’état nutritionnel et les fonctions cognitives et psychomotrices. (12, 13)
II- Définition de la chute :
De nombreuses définitions existent pour définir la chute en général et la chute de la personne âgée. Malgré le manque d’homogénéité, nous allons retenir comme définition celle de la HAS et l’OMS (14, 15), réfléchie autour de la publication de Hauer et Lamb en 2006 (16), qui recense les définitions données à la chute dans la littérature.
l’équilibre et d’être attiré au sol par son poids sous l’effet de la force pesanteur, entrainant un contact avec une surface, indépendamment de sa volonté.
Dans la majorité des définitions de la chute, on retrouve trois caractéristiques :
-‐ Premièrement le fait de se retrouver au sol dans une position de niveau inférieur par
rapport à la position de départ. La référence étant le sol, mais ce point peut différer et
se trouver à un niveau intermédiaire entre le sol et la position de départ de la personne.
-‐ Deuxièmement la notion de contact ou d’impact du corps contre une surface (sol, meuble, mur…). Elle sous-‐entend un trouble affectant l’intégrité des réflexes posturaux de protection.
-‐ Troisièmement le caractère involontaire de la chute. Il sous-‐entend l’absence d’une force extérieure exercée sur le corps et à l’origine du déséquilibre provoquant la chute.
La définition de la chute englobe ainsi le fait de tomber de sa hauteur sur le sol, mais également celui de tomber assis sur une chaise ou un lit.
A l’inverse, un déséquilibre n’entrainant pas d’impact ou de contact avec une surface ne correspond pas à une chute.
La définition de la chute à répétition chez la personne âgée retient comme critère de
répétition le fait d’avoir fait au moins deux chutes dans l’année précédent le recueil de l’information.
L’une des principales difficultés pour définir le caractère répétitif de la chute est de recueillir une information fiable sur la survenue de la chute. Le recueil de cette information peut se faire en interrogeant le patient chuteur directement, en interrogeant un proche, par l’examen clinique ou par le dossier médical en cas de complications.
III- Facteurs prédisposants et facteurs précipitants la chute :
Les chutes sont le résultat de l’interaction de facteurs complexes et interdépendants. L’interaction entre chacun n’est pas encore bien connue. Les études suggèrent toutefois que le rôle individuel de chaque facteur est faible et que la chute résulte de leur effet additif : le risque de chuter durant l’année augmente ainsi de manière linéaire avec le nombre de facteurs de risques, de 8% sans facteurs de risque à 78% pour quatre facteurs ou plus de risque (18).La littérature scientifique sur les chutes présente souvent les facteurs de risque selon trois dimensions qui interagissent entre elles. On distingue :
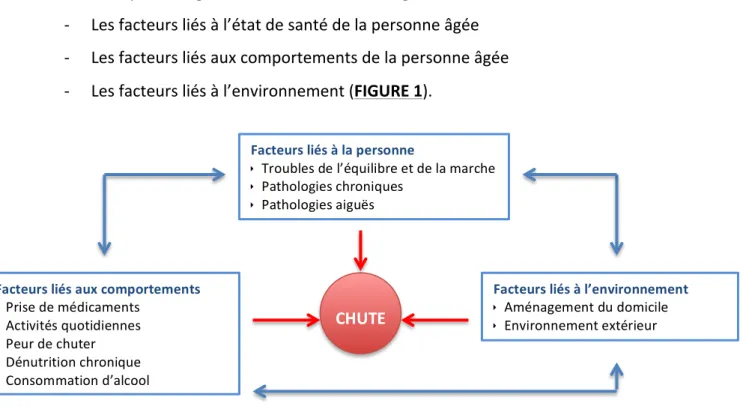
-‐ Les facteurs liés à l’état de santé de la personne âgée -‐ Les facteurs liés aux comportements de la personne âgée -‐ Les facteurs liés à l’environnement (FIGURE 1).
FIGURE 1 : LA MULTIFACTORIALITE DE LA CHUTE
Nous allons ici distinguer deux types de facteurs de risque de chute :
-‐ Les facteurs prédisposants à la chute : ils sont dus à la personne. Ce sont les conséquences de maladies chroniques et du vieillissement
-‐ Les facteurs précipitants la chute : ils sont soit intrinsèques, soit extrinsèques
FIGURE 2 : FACTEURS PREDISPOSANTS ET PRECIPITANTS LA CHUTE
Facteurs liés à la personne
ê Troubles de l’équilibre et de la marche ê Pathologies chroniques
ê Pathologies aiguës
Facteurs liés aux comportements
ê Prise de médicaments ê Activités quotidiennes ê Peur de chuter ê Dénutrition chronique ê Consommation d’alcool
Facteurs liés à l’environnement
ê Aménagement du domicile ê Environnement extérieur
CHUTE
FACTEURS PRECIPITANTS INTRINSEQUES
ê Cardiovasculaires (hypotension, troubles du rythme)
ê Neurologiques (confusion, somnolence) ê Métaboliques (hyponatrémie, hypoglycémie,
déshydratation)
ê Urinaire (incontinence, impériosités) ê Iatrogénie
FACTEURS PREDISPOSANTS
ê Cardiovasculaires ê Neurologiques
ê Ostéo-‐articulaires et musculaires ê Atteintes visuelles
ê Dénutrition
ê Modifications pharmacocinétiques FACTEURS PRECIPITANTS EXTRINSEQUES
ê Aménagement du domicile ê Environnement extérieur
1- Facteurs prédisposants :
Modifications physiques et physiologiques du sujet âgé :
a. Modifications cardiovasculaires liées à l’âge :
Les modifications cardiaques au cours du vieillissement :
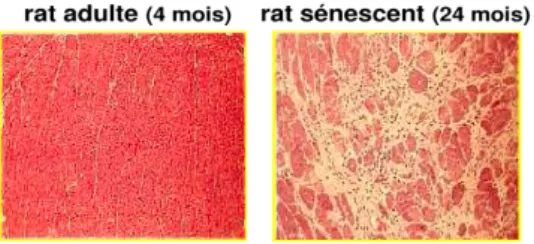
L’âge se caractérise chez le sujet âgé par une perte cellulaire au niveau cardiaque (phénomène de Hayflick) : les cardiomyocytes arrêtent de proliférer, ils se divisent moins puis meurent, et sont remplacés progressivement par des fibroblastes (FIGURE 3). La fibrose de
remplacement entraine ainsi une perte de contractilité, une augmentation progressive de la rigidité du ventricule et une diminution de la conduction électrique.
Besse et al., 1994
FIGURE 3 : COUPE DE CŒUR COLOREE A HEMALUN-‐EOSINE ILLUSTRANT LA
FIBROSE CARDIAQUE DE REMPLACEMENT CHEZ LE RAT
On observe une hypertrophie des cardiomyocytes restants qui entraine une augmentation de
l’épaisseur pariétale du ventricule gauche. La paroi est moins souple, le cœur est moins compliant. La conséquence de cette perte de compliance est une altération du remplissage diastolique. Le volume d’éjection systolique (Volume d’Ejection Systolique = Volume TéléDiastolique – Volume TéléSystolique) ainsi que la fraction d’éjection tend à diminuer. (19, 20) L’âge est caractérisé par une baisse de la fréquence cardiaque par altération des cellules du nœud sinusal et du faisceau de His. La fréquence cardiaque Fc correspond au nombre de contractions ventriculaires par seconde, exprimée en battements par minutes. La fréquence cardiaque maximum diminue progressivement avec l’âge.
Elle peut être appréciée à partir de trois formules : -‐ La formule d’Astrand : Fc max = 220 – âge -‐ La formule de Spiro : Fc max = 210 – (0,65 x âge) -‐ La formule de Sheffield : Fc max = 205 – (0,41 x âge)
Ces trois formules sont théoriques, la variation individuelle suivant l’état de santé est importante. Mais d’après ces trois formules, la fréquence maximale de contraction est donc diminuée avec l’âge. On peut estimer que la fréquence diminue d’environ une pulsation/an.
Conséquences des modifications cardiaques :
En reprenant l’équation Débit = Fréquence x VES, on en déduit que le débit cardiaque baisse avec l’âge. Cette baisse de débit est surtout visible à l’effort : le cœur ne peut plus répondre aux besoins de l’organisme de façon optimale.
Le vieillissement est ainsi caractérisé par une défaillance du cœur à fournir un débit en adéquation aux besoins de l’organisme : il y a alors risque d’insuffisance cardiaque, soit par perte de la contraction, soit par défaut de remplissage.
La perte de conduction électrique liée à la fibrose cardiaque entraine des troubles du rythme. (21)
Les modifications vasculaires liées à l’âge :
On observe une augmentation progressive, non pathologique, de la pression artérielle chez la personne âgée. Cette augmentation de pression a plusieurs causes :
-‐ Un épaississement et une modification de l’élastine de la paroi des vaisseaux liés à l’athérosclérose
-‐ Une fibrose au niveau des vaisseaux, ainsi qu’une augmentation en collagène
-‐ Une modification de la structure du collagène par glycation des fibres avec formation de ponts covalents
-‐ Un épaississement de la média par migration des cellules musculaires lisses
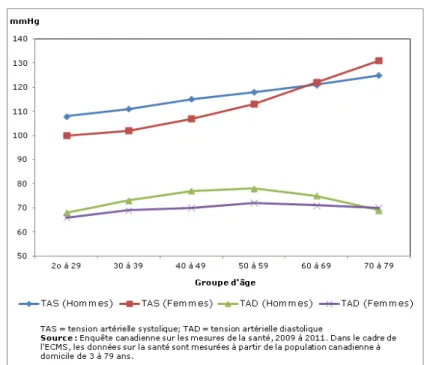
FIGURE 4 : TENSION ARTERIELLE SYSTOLIQUE ET DIASTOLIQUE, SELON LE SEXE
ET LE GROUPE D’AGE CHEZ UNE POPULATION VIVANT A DOMICILE, AGEE DE 20 A 79 ANS, CANADA, DE 2009 A 2011 (24)
Les artères deviennent plus épaisses et plus rigides avec le vieillissement : la pression artérielle augmente ainsi jusqu’à plus de 14 mmHg, comme le montre la FIGURE 4, sans être pathologique chez la personne âgée. (22).
Conséquences de l’augmentation artérielle :
Les tensions augmentant de façon physiologique avec l’âge, le diagnostic d’Hypertension Artérielle se fait en cas de tensions systoliques > 160 mmHg, et de tensions diastoliques > 90
mmHg. L’instauration d’un traitement antihypertenseur chez le sujet âgé doit se faire
progressivement et n’a qu’un objectif modeste : ramener les chiffres tensionnels sous
150/90mmHg, sans hypotension orthostatique. (23)
Modification de la réponse hémodynamique à l’orthostatisme :
Le lever entraine l’accumulation de sang dans le système veineux des membres inférieurs. La conséquence est une diminution du retour veineux et une tendance à la baisse du débit cardiaque. En réponse, le corps met en jeu plusieurs mécanismes visant à maintenir les chiffres tensionnels : des phénomènes réflexes immédiats et des modifications neuro-‐
hormonales. Les récepteurs du système baro-‐réflexe situés au niveau carotidien et sur la
crosse aortique sont activés, ils envoient un influx nerveux aux centres cardiovasculaires par deux nerfs (le nerf de Hering et le nerf vague) via le noyau NTS au niveau du centre bulbaire. Le retour se fait via les systèmes sympathique et parasympathique : par augmentation de l’activité sympathique vers le cœur et les vaisseaux, via la Noradrénaline, et par diminution de l’activité parasympathique vers le cœur. Il y a une vasoconstriction, la fréquence cardiaque et le volume d’éjection augmentent. Le débit cardiaque et les résistances périphériques augmentent. Il y a ainsi un maintien de la pression artérielle.
Plusieurs modifications de l’organisme avec le vieillissement peuvent faciliter l’apparition d’une hypotension orthostatique :
• Les récepteurs du système baro-‐réflexe sont moins sensibles
• Il y a altération du système sympathique : à la fois par modification du contrôle baroréflexe sur le système sympathique ainsi que par diminution de la sensibilité des récepteurs β-‐ adrénergiques vasculaires, de la réponse vasomotrice des vaisseaux à la Noradrénaline et d’une vasoconstriction efficace
• L’hypertrophie ventriculaire gauche et le dysfonctionnement diastolique
• La rigidification des artères altérant le fonctionnement des récepteurs liés à l’étirement des artères et la réponse vasomotrice. (25, 26, 27)
Conséquences des modifications cardiovasculaires sur le risque de chute :
Les modifications cardiovasculaires chez le sujet âgé sont des facteurs prédisposants les chutes :
â Par la défaillance du cœur à fournir un débit en adéquation aux besoins de l’organisme et avec l’âge, le risque d’insuffisance augmente (plus de 10% des plus de 75 ans).
Le malade insuffisant cardiaque est affaibli par sa pathologie (asthénie, dyspnée), son cœur a plus de risque de présenter des facteurs précipitants la chute (décompensation cardiaque, troubles du rythme).
â En favorisant plusieurs facteurs précipitants la chute, comme nous le verrons dans la partie
II-‐ b-‐ Facteurs précipitants :
-‐ Troubles du rythme
-‐ Hypotensions orthostatiques -‐ Hypotensions
-‐ Syncopes
b. Modifications du système nerveux liées à l’âge :
i. Modifications fonctionnelles
De nombreuses modifications neurobiologiques et neuropathologiques du système nerveux central ont été décrites au cours du vieillissement (2,28) :
• Au niveau structural, le vieillissement affecte le nombre et les ramifications des neurones et des cellules gliales ainsi que les synapses
Le poids du cerveau diminue d’environ 6 à 11% au cours du vieillissement, comme le montre la FIGURE 5, avec ou sans réduction du volume cérébral.
La perte neuronale diffère suivant la région du cerveau (29): la perte neuronale n’est que modérée au niveau du cervelet ou du cortex cérébral, à l’inverse au niveau du locus
cœruleus, la baisse du nombre de cellules est de 40% (d’après une étude chez des sujets de
60 ans ou plus, non atteints de maladie d’Alzheimer) (30). D’autres structures particulièrement touchées par le vieillissement sont la substance noire et le noyau basal de Meynert.
A l’inverse le nombre de cellules gliales augmente avec l’âge. Cette gliose constitue une réponse compensatrice à la fois à la réduction du nombre de neurones et à leurs modifications :
-‐ Diminution du nombre de dendrites et modifications synaptiques
-‐ Accumulation intra et intercellulaire de substances anormales telles que lipofuschine, mélanine, protéines neurofibrillaire et amyloïdes
-‐ Perturbations chimiques (perturbation de la neurotransmission) (31)
Le système vasculaire cérébral subit les mêmes changements d’athérosclérose que le reste du système vasculaire.
FIGURE 5 : EFFETS DE L’AGE SUR LE POIDS DU CERVEAU
DE L’HOMME ET DE LA FEMME (28)
• Au niveau chimique, le vieillissement influence le métabolisme, le taux de renouvellement et le nombre de récepteurs de plusieurs neurotransmetteurs, en particulier l’Acétylcholine et la Dopamine.
• Au niveau fonctionnel, le vieillissement affecte l’activité électrique cérébrale, ainsi que les processus sensoriels, moteurs, cognitifs et affectifs.
Les dysfonctionnements du système nerveux ont des conséquences sur tout l’organisme, on observe :
-‐ Des pertes sensorielle et motrice -‐ Une modification du cycle du sommeil -‐ Des troubles de la mémoire
-‐ Des désordres neurologiques et psychiatriques plus fréquents -‐ Une défaillance de l’homéostasie.
L’ensemble de ces modifications majore la vulnérabilité cérébrale des personnes âgées à l’égard des agressions, notamment le risque de syndrome confusionnel et favorise l’apparition de plusieurs pathologies, augmentant le risque de chute.
ii. Démences vasculaires et démences de types Alzheimer :
On considère une baisse des aptitudes cognitives comme un phénomène normal avec le vieillissement, qui se manifeste notamment par une perte de la mémoire.
Ce vieillissement cognitif peut devenir anormal lorsqu’il commence à avoir un retentissement dans les actes de la vie quotidienne du patient.
Le diagnostic de syndrome démentiel est clinique. Il repose sur un ensemble d’arguments apportés par l’interrogatoire du patient et des ses proches, l’évaluation des fonctions cognitives par des tests psychométriques, l’étude du comportement et le retentissement des troubles cognitifs dans les actes de la vie du patient. Le diagnostic de syndrome démentiel s’appuie sur les critères du Manuel diagnostic et statistique des troubles mentaux (DSM V) : • Apparition de troubles cognitifs multiples qui se manifestent par :
-‐ Altération progressive et acquise de la mémoire
-‐ Associée à une autre perturbation cognitive : troubles phasiques, troubles praxiques, troubles gnosiques ou troubles des fonctions cognitives
• Evolution des troubles depuis au moins 6 mois
• Retentissement sur les fonctions sociales ou professionnelles et sur les actes de la vie quotidienne
• Absence d’affection somatique ou psychiatrique pouvant expliquer ces troubles.
Il existe trois causes majeures de démence chez la personne âgée : la maladie d’Alzheimer, les démences à corps de Lewy et les démences vasculaires. Le diagnostic de démence est souvent difficile, l’étiologie entre Alzheimer, démence à corps de Lewy, fronto-‐temporale, vasculaire n’est pas toujours évidente, les causes pouvant être mixtes.
Le principal test psychométrique utilisé pour évaluer les troubles cognitifs est le Mini Mental Status Examination (MMSE) :