« L’histoire du droit et le droit comparé sont les meilleurs auxiliaires
des sciences juridiques. Les deux disciplines ont le mérite de mieux
nous faire comprendre notre droit actuel. Pour le connaître, il faut
remonter aux origines : essentiellement au droit musulman, mais aussi
aux pratiques et coutumes locales, aux apports du régime du
protectorat, sans négliger l’influence exercée par d’autres législations
étrangères.
L’histoire du droit et le droit comparé constituent par ailleurs des
instruments de réforme législative. Cela veut dire que le législateur
qui décide de modifier la législation existante ou d’introduire une
réforme nouvelle, est souvent porté à se référer :
- aux enseignements de l’histoire des institutions juridiques ;
- et aux réformes entreprises dans les autres pays »
Mohammed Jalal Essaid,
« Introduction à l’étude du droit », Collection connaissances, 2000.
Le 07 Décembre 2006 fut promulguée la loi n°17-04 portant code du médicament et de la pharmacie au Maroc, abrogeant le texte de référence, le Dahir du 19 février 1960 qui a régi la profession pharmaceutique pendant près d’un demi siècle. Ce texte était complètement dépassé en raison du développement qu’a connu cette profession sur le plan national et international.
Cette importante évolution de la réglementation pharmaceutique dans notre pays méritait qu’on s’y intéresse.
L’objectif de notre travail est d’analyser la législation pharmaceutique marocaine actuelle en étudiant son évolution historique et en la comparant aux textes français dans ce domaine.
Notre étude est divisée en six chapitres:
Chapitre 1 : histoire de l’évolution de la réglementation pharmaceutique en France et au Maroc.
Chapitre 2 : définition légale du médicament et monopole pharmaceutique.
Chapitre 3 : substances vénéneuses.
Chapitre 4 : autorisation d’exercice et autorisation de création. Chapitre 5 : déontologie des pharmaciens.
Chapitre: 1
Histoire de l’évolution de la
réglementation pharmaceutique en
France et au Maroc
I
.Institution d’une réglementation de l’exercice de la pharmacie
:Guérir est aussi vieux que l’homme et la maladie. Le métier de soulager la souffrance a évolué aux cours des siècles passant de la magie vers la science. Parallèlement est née une réglementation de plus en plus précise qui a suivi l’évolution des pratiques.
Une des plus anciennes réglementations date des arabes. En effet, des réglementations professionnelles mises en place par les Arabes ont été reprises en 1220 par Frédéric II dans le royaume de Naples et lors de la création des diverses communautés religieuses. [1]
Selon cette réglementation, les poids et les mesures étaient sévèrement contrôlés par les soins du mohtassib, le système d’Hisba a été appliqué sur la pharmacie par le calife Al-Mouktader (908-932). Ce mohtassib est l’inspecteur général des commerçants. Il avait sous ses ordres des inspecteurs secondaires ou arifs choisis dans chaque corps du métier, il fallait un homme qui soit reconnu de ses parrains pour sa rigueur, sa probité, et sa compétence pour pouvoir mener à bien sa mission. On trouve dans le livre « nihayat arretba fi talab alhisba », en 1193 de Abd Arrahmane Ibn Nasr Asserzi, les différents moyens de contrefaçon des médicaments ainsi que les méthodes de les contrôler. [1, 2]
II
.Historique de l’organisation et de la réglementation de la
pharmacie en France et au Maroc :
Le régime juridique de la profession pharmaceutique est construit autour de la notion de médicament. Il est complexe, car il ajoute au contrôle technique de ce dernier, des éléments relatifs d’une part à sa production, à sa distribution, et d’autre part à sa consommation (notamment à sa prescription par le corps
médical), enfin à son prix, à sa publicité, et à son remboursement par la sécurité sociale. Il a subi d’importantes évolutions liées au développement des connaissances scientifiques et des technologies, à celui de la thérapeutique, mais aussi à des facteurs d’ordre économique, social, voire politique, et international. Quelques retours en arrière permettent de marquer les étapes les plus importantes de cette évolution. [3,4]
II.1. Les étapes de l’organisation de la pharmacie en France :
II.1.1. Les corporations d’apothicaires et les premières réglementations :
Les speciarii, encore dénommés apothecarii ou aromatorii se regroupaient dans les premières corporations qui adoptaient des réglementations officielles ou statuts municipaux. Les premières ont été établies à Arles au XIIème siècle. A Paris, l'exercice de la pharmacie était réglementé par des édits royaux. Les apothicaires contrôlaient le recrutement de leurs confrères et leur apprenaient le métier pendant de longues années (deux à huit ans pour l'apprentissage). Le serment couronne la fin des études. C’est là l’origine du caractère de profession réglementée que la pharmacie devait conserver jusqu’à nos jours. [5, 6,7]
Pour affirmer leur monopole aussi bien dans l’intérêt de la santé publique que pour défendre leur privilège et leur indépendance, les apothicaires ont dû lutter constamment contre les concurrences illégales pratiquées par les divers corps de métiers et même par des médecins qui préparaient et vendaient eux même les remèdes, contre les charlatans et les vendeurs de potions non autorisés une guerre de préservation de ce monopole que les pharmaciens continuent à mener.
II.1.2. La déclaration royale de 1777 et la loi de Germinal de l’an XI : L’annonce du monopole des pharmaciens, s’est faite grâce à la déclaration royale du 25 Avril 1777.
Plus tard, la loi du 21 Germinal de l’an XI, première loi organique de la pharmacie, allait réglementer l’exercice de la pharmacie par des dispositions applicables en France entière (Organisation des études, exercice de la pharmacie, règles commerciales, réglementation de la publicité (article 32), prohibition de vendre les remèdes secrets (article 36). [5]
II.1.3. De la loi du 11 septembre 1941 à l’ordonnance du 04 février 1959 :
Une législation pharmaceutique a vu le jour sous le gouvernement de Vichy, par la loi du 11 septembre 1941, qui fut ensuite formellement validée par l’ordonnance du 23 Mai 1945, à l’exception des articles concernant l’organisation professionnelle.
Parmi les innovations de cette loi, celle qui reconnaissait et réglementait l’industrie pharmaceutique ainsi que la fabrication et le commerce des spécialités, qui donnait une définition des médicaments et de la spécialité pharmaceutique, et instituait un visa préalable à l’exploitation de ces spécialités pharmaceutiques, qui décidait la limitation du nombre des officines et qui réorganisait complètement l’inspection des pharmacies en créant un corps d’inspecteurs spécialisés. Elle consacrait à nouveau le monopole des pharmaciens, et elle précisait les conditions de l’exercice personnel, ainsi que les règles commerciales de la pharmacie. [3]
II.1.4. De l’ordonnance de 1959 à 1986 :
La législation de cette période s’est intéressée plus aux établissements de fabrication et de vente en gros. L’ordonnance du 23 septembre 1967 stipulait que ces établissements doivent être la propriété d’un pharmacien ou une société à la gestion ou à la direction de laquelle participe un pharmacien. La loi du 6 juillet 1978 a fait obligation aux sociétés pharmaceutiques d’assurer la direction technique de chacun de leurs sites par un pharmacien assistant.
Les critères d’octroi de l’autorisation préalable à la mise sur le marché, encore dénommée visa dans l’ordonnance de 1959 n’ont pas été fondamentalement modifiés depuis ce texte, même si certaines modifications de forme sont intervenues : les vérifications des qualités requises pour l’octroi du visa puis de l’Autorisation de Mise sur le Marché (AMM) sont depuis 1959 basées sur le principe d’expertises dans les divers domaines analytiques, pharmacologiques, toxicologiques et cliniques. Les termes "d’expertise" comme celui "d’expert" ont donné lieu à bien des discussions avant qu’ils ne soient admis à l’échelon européen par la directive 75/319/CEE du 20 mai 1975. Les essais dits « de pharmacologie humaine » fixés par le protocole clinique avaient causé un problème juridique qui reste posé dès lors que des projets de loi étudiés depuis 1984 et soumis au comité d’éthique n’avaient à cette date (1986) pas eu de suite. C’est en 1988 seulement qu’a été publiée la loi dite de Huriet-Sérusclat relative à la protection des personnes qui se prêtent à des recherches biomédicales, cette loi marque une étape décisive dans l’histoire de l’autorisation de mise sur le marché. [3, 8]
II.1.5. La réglementation pharmaceutique depuis 1986 :
La période qui va de 1986 à 1993 est profondément marquée par une accélération de l’harmonisation communautaire, stimulée par l’adoption de l’acte unique européen ratifiée par la France en décembre 1986 et fixant au 31 décembre 1992 la réalisation du grand marché.
Le champ d’application de l’autorisation de mise sur le marché a été étendu par l’adoption d’un certain nombre de directives :
- La directive 89/342/CEE du 3 mai 1989 relative aux médicaments
immunologiques.
- La directive 89/343/CEE du 3 mai 1989 relative aux médicaments radio
pharmaceutiques.
- La directive 92/73/CEE du 22 septembre 1992 relative aux médicaments
homéopathiques.
Pour les établissements pharmaceutiques, la notion de contrôle de qualité s’est développée progressivement avec les bonnes pratiques de fabrication (BPF) dont les modalités ont fait l’objet de plusieurs instructions ministérielles.
[3].
II.2. Historique de la pharmacie au Maroc :
La pharmacie au Maroc a connu une longue évolution. Plusieurs médecins et pharmaciens ont été diplômés de l’université Al-Karawiyine, mais ces études médicales ont été supprimées de cette université avant la fin du XIXème siècle.
[9]
La profession pharmaceutique moderne a évolué en trois périodes distinctes par rapport au protectorat français (1912-1956) :
II.2.1. Avant le protectorat :
Au Maroc, avant le XIX ème siècle et même au début du XX ème siècle, l’art de guérir était l’un des attributs des personnages religieux « FQIH» , la croyance populaire attribuait des pouvoirs curatifs notamment aux marabouts [9,10,11] On distingue à l’époque :
- Des Houkamas (médecins de l’époque);
- Des Tolbas ou fkih chargés surtout (du spirituel, traitant des cas résistants à la médication classique, malades du système nerveux et atteints de troubles psychiques) ;
- Des achabats ou herboristes qui exécutaient les wasfas des Houkamas, procédait aux mélanges des plantes prescrites ou qui conseillaient parfois des remèdes à leurs clients en fonction des symptômes décrits ;
- Et enfin des « attaras» qui s’occupaient surtout des drogues d’origine animale ou minérale destinées aussi bien à la médecine qu’à la cosmétologie ou à la sorcellerie. [9]
Ces attaras assimilés aux épiciers-apothicaires en Europe, étaient organisés comme les autres corps de métiers en corporations, ces dernières étaient coiffées par un chef ou «Amine» qui dépendait lui même d’un autre chef, celui des services économiques ou «Mouhtassib» qui avait pour mission la protection de la profession, le recrutement de ses membres après le constat d’une formation de base de plusieurs années, et d’une aptitude reconnue.
Ces corporations défendaient les intérêts professionnels matériels et moraux de la profession, et jouaient un rôle social en développant la solidarité mutuelle entre leurs membres et leurs familles. La profession médicale en général et «pharmaceutique» en particulier représentée par les attaras et les achabats était bien organisée et réglementée.
II.2.2. Sous le protectorat 1912-1956 :
Dés l’implantation du régime français au Maroc, un premier texte concernant le droit pharmaceutique fut instauré, non pas par l’autorité centrale, mais par l’autorité municipale relevant du Pacha de la ville (arrêté municipal du 11 septembre 1913).
Son premier article précisait que pour être autorisé à exercer au niveau de la circonscription du Pacha, le pharmacien doit posséder un diplôme confirmé par le consul du pays d’origine de l’intéressé, il présente sa demande au Pacha qui lui accorde l’autorisation. Cet arrêté fixait en outre les conditions de remplacement du pharmacien titulaire appelé à gérer son officine soit par un pharmacien assistant, soit par un étudiant en pharmacie ayant au moins effectué 5 ans de stage. Il tolérait en plus l’exercice de la profession pharmaceutique par des praticiens étrangers même non diplômés à condition que ceux-ci aient exercé leur art à la date du traité du protectorat (30 Mars 1912) depuis au moins 5 ans. [10]
Quelques mois plus tard, le 27 Avril 1914 un Dahir relevant de l’autorité centrale (Secrétariat Général du Gouvernement Chérifien) réglementait en partie l’autorisation accordée à des pharmaciens non diplômés. Il soumettait ainsi ces derniers à un examen dirigé par un pharmacien principal assisté par deux autres pharmaciens (un civil et un militaire). Ceux qui satisfaisaient à cet examen obtenaient un brevet portant la mention « Certificat de capital de pharmacien
toléré» ou pharmacien de deuxième classe. Les autres devaient cesser leurs
activités.
Ces premiers textes furent groupés le 12 Avril 1916 dans un Dahir qui était commun aux médecins, pharmaciens, dentistes et sages femmes, et qui tout en
aux fins d’enregistrement au greffe du tribunal et pour visa à l’autorité centrale, et pour la publication au niveau du bulletin officiel. Il élargissait le champs d’action de l’autorisation à l’ensemble de la zone placée sous le contrôle de la France, par contre il interdisait le cumul de l’exercice pharmaceutique et de l’exercice médical, il autorisait par dérogation, aux médecins à pratiquer la propharmacie dans les localités dépourvues de pharmacies dans un rayons de 25 Km. Il permettait au pharmacien autorisé à posséder une deuxième officine si l’intérêt public l’exige, à condition qu’elle soit installée dans la même ville et qu’elle soit gérée soit par un pharmacien assistant ou par un pharmacien toléré ou par un étudiant ayant au moins accompli 5 ans de stage dans une officine en France ou dans un pays reconnu par elle. [10]
Les pharmaciens, conformément à ce dahir, pouvaient constituer des sociétés d’importation de médicaments de France à condition que tous les actionnaires de ces sociétés soient pharmaciens.
Le Codex Medicamentarius Français ou pharmacopée française constituait l’ouvrage de référence des pharmaciens que tout pharmacien était sensé avoir dans son officine.
Il faut signaler la publication, le 25 Janvier 1916 d’un Dahir portant réglementation de l’opium, de ses alcaloïdes, de ses préparations officinales, de son importation, de son utilisation, et de sa délivrance ainsi que son stockage dans une armoire fermée à clef. En 1922 (2 décembre) la loi sur les substances vénéneuses fut promulguée par un Dahir qui réglemente leur commerce, leur étiquetage, et leur classification en tableau A, C et B et fixe les doses exonérés, ce Dahir est toujours en vigueur de nos jours! [10]
Une brève énumération des principaux Dahirs modifiants et complétant le Dahir de 12 Avril 1916 est nécessaire :
─ Le Dahir du 16 Juillet 1921 prescrivant l’affichage du diplôme ;
─ Le Dahir du 30 Juillet 1921 recommandant le dépôt du diplôme entre les
mains des autorités locales pour visa (articles 2 et 3) ;
─ Le Dahir du 19 Décembre 1922 complétant l’article 4 relatifs à l’exercice
illégal de la pharmacie ;
─ Le Dahir du 27 février 1923 sur l’exercice de la profession d’herboriste ; ─ Le Dahir de 20 Avril 1926 qui aboutit à une refonte de la quasi-totalité des
articles du Dahir du 12 Avril 1916 ( 1,2,3,4,5,6,7,7 bis,8 bis,10 et 11), et introduit en outre la notion de probité et moralité ;
─ Le Dahir de 1926 complété par le Dahir du 07 Juillet 1938 qui a fixé les
conditions de la représentation médicale. Il interdisait le colportage et la recherche de la clientèle et il définissait la dérogation accordée à l’Institut Pasteur et à ses filiales.
─ Le Dahir du 03 Mars 1928 par lequel la création d’établissement de
fabrication de produit pharmaceutique est rendue nécessaire ;
─ Le Dahir de 18 Mai 1936 instituant un service de pharmacie de nuit ;
De 1913 à 1938 tous les textes publiés réglementaient l’exercice professionnel. Et ce n’est que le 10 février 1943 qu’un Dahir fut promulgué en vue d’organiser la profession. Ainsi un conseil supérieur de la pharmacie fut constitué, aidé dans sa mission (tradition, probité, respect des lois et règlements, défense des intérêts moraux et matériels) par des chambres professionnelles et doué de prérogatives disciplinaires.
Le 14 janvier 1950 un Dahir fut promulgué, qui réglementait la fabrication, la vente, et la distribution des vaccins, des sérums thérapeutiques et des divers
produits biologiques. Pour la première fois on assimilait ces produits aux médicaments.
En conclusion, nous pouvons dire que la période coloniale de l’histoire pharmaceutique était caractérisée par deux époques distinctes :
Epoque 1913-1943 : [11]
Elle était caractérisée par la mise en place progressive des règlements et des lois régissant l’exercice professionnel. Il faut signaler toutefois leurs caractères non marocains.
Epoque 1943-1956 : [11]
Elle concerne en particulier des textes relatifs au chanvre indien, à l’inspection, et à l’organisation professionnelle par l’institution d’un conseil supérieur de la pharmacie.
Ainsi, en quelques années une profession moderne fut introduite et réglementée, en coexistence avec les Attaras et les Achabas. Elle s’est organisée progressivement en se dotant des textes réglementaires, avec un conseil des pharmaciens à l’exemple des pays développés où cette évolution a nécessité des générations.
II.2.3. Après l’indépendance:
Les textes en vigueur à la fin du protectorat français ont permis la mise sur pied d’une profession organisée, toutefois les responsables se sont trouvés confrontés aux dispositions discriminatoires des textes élaborés pour une population non marocaine. Ceci d’ailleurs, se reflétait au niveau de l’organisation professionnelle dirigée par des pharmaciens étrangers désignés par la résidence générale, alors que les marocains diplômés à cette époque étaient très peu nombreux. [11]
C’est au conseil supérieur telle qu’il a été institué en 1943, que s’est intéressé le premier Dahir d’un gouvernement marocain indépendant. Ainsi, le 15 novembre 1957 un Dahir portant loi fut promulgué pour suspendre le fonctionnement du conseil supérieur de la pharmacie et nommer un conseil provisoire de la pharmacie appelé à assumer les responsabilités du conseil supérieur.
C’est en 1960 (le 19 février) que fut promulgué le Dahir 1-59-367 réglementant toutes les professions médicales et constituant pendant près d’un demi siècle le texte de base et de référence de la pharmacie au Maroc, ce texte avait repris l’ensemble des dispositions du Dahir du 07 juillet 1938.
Enfin, depuis le 07 décembre 2006, est entrée en vigueur le Dahir
n°1-06-151 du 22 Novembre 2006, portant promulgation de la loi n°17-04 portant code
du médicament et de la pharmacie.
Chapitre : 2
Définition légale du médicament et
monopole pharmaceutique
I. Définition légale du médicament :
I.1. Introduction:
L’élément essentiel en pharmacie est la notion du médicament. Au Maroc, cette définition était le motif de promulgation du dahir du 15 février 1977 et actuellement elle est en tête du nouveau code de médicament et de la pharmacie. En France, l’importance attachée à cette définition sur le plan formel est attestée par la place qui lui est attribuée dans la législation pharmaceutique : la définition du médicament figurait au premier article de la loi organique de 1941, puis au premier article du code de santé publique. [12]
Ce chapitre comporte :
Un aperçu historique des textes relatifs à la définition du médicament. Une analyse des termes de cette définition sur laquelle se basera notre
approche critique.
I.2. Aperçu historique :
Au Maroc, la notion du médicament a été mentionnée d’une façon imprécise dans l’article 6 du Dahir de 1960. Nous retrouvons dans l’article 15 du même dahir la définition du terme « Spécialité pharmaceutique » en utilisant le terme «médicament », que le législateur a omis de définir au préalable. [15]
Il a fallu 17 ans pour que le législateur marocain la reprenne en 1977, dans la modification de l’article 15, qui faisait l’objet du Dahir de 15 février 1977.
En France, le médicament fut défini pour la première fois, lors de l’élaboration de la «loi organique» du premier septembre 1941, cette définition
était mise en harmonie avec la directive du conseil des ministres de la communauté économique européenne (C.E.E.) n°65/65 du 26 janvier 1965. Une transposition de ce texte en Droit français a été effectuée par 1'Ordonnance du 23 septembre 1967, et insérée dans l'article L.5111 du Code de la Santé Publique. [13,14]
Depuis, le droit français a connu plusieurs définitions successives, mais d’une manière générale, depuis 1941, chacune complétait et précisait la définition antérieure plus qu’elle ne la modifiait. [12]
I.3. Enoncés de la définition légale du médicament :
La nouvelle loi n° 17-04 portant code du médicament et de la pharmacie, définit dans son 1er article le médicament comme étant :
« Toute substance ou composition présentée comme possédant des propriétés curatives ou préventives à l’égard des maladies humaines ou animales, ainsi que tout produit pouvant être administré à l’homme ou à l’animal en vue d’établir un diagnostic médical ou de restaurer, corriger ou modifier leurs fonctions organiques. » [16]
La définition du législateur français est donnée par l’article L 5111-1 du code de santé publique :
« On entend par médicament toute substance ou composition présentée comme possédant des propriétés curatives ou préventives à l’égard des maladies humaines ou animales, ainsi que toute substance ou composition pouvant être utilisée chez l’homme ou chez l’animal ou pouvant leur être administrée, en vue d’établir un diagnostic médical ou de restaurer,
corriger ou modifier leurs fonctions physiologiques en exerçant une action pharmacologique immunologique ou métabolique.
Sont notamment considérés comme des médicaments les produits diététiques qui renferment dans leur composition des substances chimiques ou biologiques ne constituant pas par elles mêmes des aliments, mais dont la présence confère à ces produits, soit des propriétés spéciales recherchées en thérapeutique diététique, soit des propriétés de repas d’épreuve.
Les produits utilisés pour la désinfection des locaux et pour la prothèse dentaire ne sont pas considérés comme des médicaments.
Lorsque, eu égard à l’ensemble de ses caractéristiques, un produit est susceptible de répondre à la fois à la définition du médicament prévues au premier alinéa et à celle d’autres catégories de produits régies par le droit communautaire ou national, il est, en cas de doute, considéré comme un médicament. » [17]
D’après une simple lecture de ces définitions, nous pouvons dire que la définition légale du médicament adoptée par le législateur marocain reprend le même esprit que celui de la définition française adoptée à l’échelon européen. Toutefois, nous relevons des différences mineures. Il convient de rappeler que le respect de la précision du vocabulaire est essentiel surtout pour un juriste.
Cette définition nous permet de distinguer deux catégories de médicaments : [13]
Le médicament par présentation. Le médicament par fonction.
I.3.1. Médicament par présentation :
Pour qu’un produit soit considéré comme un médicament, trois conditions doivent être réunies. Ce produit doit être :
Une « substance » ou une « composition » ;
Présentée comme possédant des propriétés « curatives » ou « préventives » ;
« à l’égard des maladies humaines ou animales ».
Nous remarquons que la notion de médicament est ici étroitement liée d’une part à la formule du produit, d’autre part aux vertus qui lui sont attribuées et non à celles qu’il possède effectivement. [11, 18]
a- Le médicament est une « substance » ou une « composition » :
Le terme de substance peut revêtir des interprétations diverses jusqu’à un sens très large qui englobe toute sortes de produits tant simples que composés.
Mais, étant mis en opposition au terme « composition », son sens devient restreint, ce qui suggère la notion de « produit simple » pour le terme « substance » et de « pluricité » pour le mot « composition ».
La « substance » groupe à la fois :
Les drogues : produit brut naturel ou obtenu par procédés simples ne nécessitant pas de connaissances pharmaceutiques.
Et les produits élaborés par extractions ou synthèse.
Ainsi le terme de substance désigne un produit simple d’origine naturelle ou élaboré. [19]
La « composition » :
Restant non déterminée, permet des interprétations diverses, mais il faut distinguer entre les préparations et les compositions qui sont constituées d’un mélange de corps simples dont la composition avait altéré la substance, c'est-à-dire que ces corps simples ont perdu leur individualité.
La « préparation » :
Il y a cinquante ans, la préparation des médicaments était une des fonctions les plus importantes du pharmacien d’officine. Aujourd’hui, la presque totalité des médicaments est préparée dans l’industrie. [20]
Au Maroc, on faisait allusion aux préparations médicamenteuses dans l’article 6 du Dahir de 1960, mais la loi 17-04 les définit clairement dans l’article 2 sur lequel nous allons revenir dans le deuxième volet de ce chapitre « monopole pharmaceutique ».
Dans la législation française, une omission de la notion de préparation peut être relevée dans la loi de 1941 et les énoncés ultérieurs, on y attribuait le régime de composition. Mais l’article 5121-1 du code de la santé publique en vigueur, définit les différents types de préparations pharmaceutiques (magistrale, hospitalière…) [12, 21]
b- « Présentée comme possédant des propriétés curatives ou
préventives » :
Le législateur insiste sur la notion essentielle du médicament, en l’occurrence, ses propriétés thérapeutiques précisées et complétées, par son rôle prophylactique.
Il n’est pas indispensable que le produit recèle réellement les propriétés curatives ou préventives, il suffit qu’il soit présenté comme les possédant. Le législateur dit bien « possédant » et pas « ayant », ce qui impose non pas une obligation de résultat mais une obligation de moyens en terme juridique, comme cela est défini dans le contrat médical qui relit le médecin et le malade. En effet, le pharmacien ne peut en aucun cas être poursuivit pour inefficacité constatée d’un produit chez un patient donné. [12]
Cette prise en compte du critère de la présentation peut à priori heurter le bon sens, puisqu’à la limite un simple verre d’eau pourra être qualifié de médicament dès lorsqu’un charlatan quelconque le présente comme possédant une activité thérapeutique. Mais, cette définition de médicament par présentation a précisément pour objectif la lutte contre le charlatanisme. Elle permet d’exercer un contrôle sur les produits qui sont présentés comme médicaments alors qu’ils ne le sont pas. [20]
Ces termes ne précisent pas comment s’entend cette « présentation », permettant ainsi de tenir compte de la présentation implicite comme de la présentation explicite. [12]
Nous pouvons conclure que la condition de présentation est remplie lorsque le produit est décrit ou recommandé expressément comme ayant un effet curatif ou préventif. Et ceci au moyen d’autorisation de mise sur le marché, d’étiquetage, de notice…Cette condition est aussi remplie lorsqu’il apparaît, de manière implicite mais certaine, aux yeux d’un consommateur moyen, que le produit devrait avoir un tel effet eu égard à sa présentation, c’est alors un faisceau d’indices qui permet de caractériser une véritable « présentation
implicite » : forme galénique, nom de marque ou logo à connotation pharmaceutique… [20]
c- « à l’égard des maladies humaines ou animales » :
Le terme de maladies animales a été ajouté ultérieurement aux maladies humaines : les produits vétérinaires se trouvent donc désormais inclus dans la définition de médicament. Mais les pharmaciens de l’officine partagent ce monopole avec les médecins vétérinaires. [12]
Nous relevons ainsi que ces médicaments peuvent être destinés à l’homme comme à l’animal, selon les maladies, en l’occurrence celles des animaux qui sont contagieuses pour l’être humain. [22]
Les phytopathies (maladies des plantes) ne sont pas visées par cette définition. Les produits destinés aux traitements des plantes n’entrent-ils pas dans la notion du médicament ? [12]
I.3.2. Médicament par fonction :
Il s’agit de produit permettant un diagnostic médical ou employé en raison de son action sur les fonctions organiques.
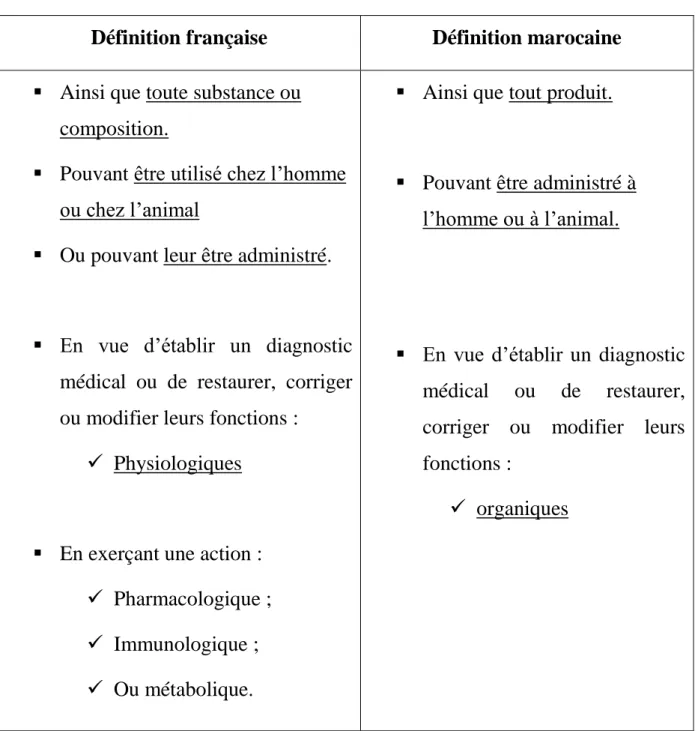
Nous suggérons le tableau suivant comme moyen de comparaison entre la définition française et celle marocaine du médicament par fonction :
Tableau I : médicament par fonction
Définition française Définition marocaine
Ainsi que toute substance ou composition.
Pouvant être utilisé chez l’homme ou chez l’animal
Ou pouvant leur être administré.
En vue d’établir un diagnostic médical ou de restaurer, corriger ou modifier leurs fonctions :
Physiologiques
En exerçant une action : Pharmacologique ; Immunologique ; Ou métabolique.
Ainsi que tout produit.
Pouvant être administré à l’homme ou à l’animal.
En vue d’établir un diagnostic médical ou de restaurer, corriger ou modifier leurs fonctions :
organiques
Nous observons que la définition marocaine utilise le terme de « produit » au lieu de terme « substance » ou « composition », déjà utilisé à la 1ère partie de la définition, contrairement à la définition française qui reprend ces termes dans
la 2ème partie de la définition. Quelle est l’utilité ou la différence envisagées par le législateur marocain, en changeant ces termes ?
- « pouvant être administré à l’homme ou à l’animal » :
Elle ne comprend pas tous les produits pouvant être utilisés pour un diagnostic mais seulement ceux qui peuvent être administré à l’homme ou à l’animal. C'est-à-dire introduits dans l’organisme ou appliqués sur lui, contrairement à la définition française. Et nous signalons que la version arabe du nouveau code, utilise le terme « wasf » qui veut dire « prescrit », ce qui ne veut pas dire forcement administré, il peut être utilisé autrement. [12,16]
- « en vue de » : Il suffit que le produit soit administré « en vue de », la
définition « fonctionnelle » du médicament se trouve donc fondée, sur une finalité ! [20]
- « restaurer, corriger ou modifier » les fonctions organiques de l’homme
ou de l’animal, cette définition avait pour but de soumettre les contraceptifs oraux au régime du médicament.
Le législateur français a changé le terme « fonctions organiques » par le terme « fonctions physiologiques » qui est un terme plus exhaustif, sachant que le terme organique concerne chaque organe individuellement, alors que le terme physiologique englobe l’ensemble du corps.
La définition française précise aussi, le mécanisme d’action du médicament : pharmacologique, immunologique, métabolique…etc.
L’article 15 du dahir de 1977, ajoutait à cette définition, des produits hygiéniques et diététiques et aussi la définition de la spécialité pharmaceutique
incluse dans le même article. Mais le législateur marocain a consacré le 1er article, uniquement pour donner une définition simple et précise du médicament. Alors que le 2éme article groupe plusieurs produits assimilés au médicament y compris les produits diététiques et hygiéniques.
Le législateur français garde les produits diététiques dans l’article L5111-1 relatif à la définition du médicament, mais l’article L5121-1, énumère presque les mêmes produits que l’article 2 de la loi marocaine n° 17-04, sauf que l’article L5121-1 donne une définition à ces produits alors que l’article 2 du code marocain les définit et ajoute qu’ils sont considérés comme des médicaments, cette assimilation aux médicaments aurait-elle une influence sur le monopole pharmaceutique ?
Le législateur français ajoute dans l’article relatif à la définition du médicament :
« Les produits utilisés pour la désinfection des locaux et pour la
prothèse dentaire ne sont pas considérés comme des médicaments ».
Nous remarquons qu’il exclut uniquement ces deux catégories de produit de la définition du médicament, nous ne pouvons deviner pourquoi le législateur les a introduit ici avec la définition de médicament.
Et il clos cette définition par :
« Lorsque, eu égard à l’ensemble de ses caractéristiques, un produit est susceptible de répondre à la fois à la définition du médicament prévue au premier alinéa et à celle d’autres catégories de produits régies par le droit
communautaire ou national, il est, en cas de doute, considéré comme un médicament ».
Nous jugeons que l’ajout de ce dernier alinéa est très important, vu le développement des recherches scientifiques et biotechnologiques dans le domaine de médicament, et les innovations thérapeutiques qui posent des questions nouvelles délicates à résoudre, ainsi le législateur français permet de qualifier un produit de médicament lorsqu’il répond aux exigences citées.
Cet alinéa n’a pas été repris par notre législateur !
II. Le monopole pharmaceutique :
II.1. Définition :
Le terme du monopole est définit comme étant un privilège exclusif de droit ou de fait que possède un individu, une entreprise ou un organisme, de fabriquer, vendre ou exploiter certains biens ou services. [23]
C’est la particularité du médicament qui constitue la justification essentielle, donc la raison d’être du monopole pharmaceutique. Ce dernier, a pour fondement la compétence du pharmacien formé pendant des années à la connaissance du médicament, sanctionné par un diplôme. Et sa justification réside dans les garanties d’ordre scientifique, technique et moral qu’offre celui-ci pour assumer la responsabilité de ses actes vis-à-vis du malade, de la vie de la personne et de l’animal au regard du danger que peut faire encourir le médicament. [24]
La définition du monopole pharmaceutique qui est restée pendant longtemps liée à celle du médicament a acquis aujourd’hui une portée beaucoup
plus large, et englobe d’autres matières dont la vente est réservée aux pharmaciens (articles 30 et 112 de la loi 17-04).
II.2. Aperçu historique :
La législation du monopole au Maroc a suivi chronologiquement une progression constante. Dans le Dahir du 12 Avril 1916, considéré comme la première charte fondamentale de la pharmacie au Maroc, elle n’a prévu que la vente du médicament. Le Dahir du 03 Mars 1928 a inclus sa fabrication et sa répartition. Le monopole a englobé, en vertu du Dahir du 17 Juillet 1938, les activités des trois secteurs de la profession à savoir la fabrication, la grossisterie et l’officine ou vente au détail du médicament. Le Dahir du 19 Février 1960 a réalisé la synthèse des textes officiels précités. Enfin le nouveau code du médicament et de la pharmacie a élargi ce monopole en tenant compte des innovations introduites dans l’exercice de la profession. [24,25]
II.3. L’étendu du monopole pharmaceutique :
L’étendu du monopole se définit à la fois par les produits et objets inclus dans ce monopole et par les opérations (fabrication, vente en gros, distribution et vente au détail, détention, dispensation..) réservées aux pharmaciens sur ces produits et objets. [12]
II.3.1. Les opérations réservées aux pharmaciens : comparaison entre le Dahir de 1960 et le nouveau code :
Nous comparons dans le tableau suivant les articles relatifs à ces opérations dans le Dahir abrogé du 19 Février 1960 et dans le Dahir du 22 Novembre 2006.
Tableau II : Opérations réservées aux pharmaciens : comparaison entre le Dahir de 1960 et le nouveau code : Le Dahir du 19 Février 1960. [26] le Dahir du 22 Novembre 2006. [16] La fabrication
10ème alinéa article 9
« la fabrication, la composition ou la préparation des produits pharmaceutiques, le conditionnement en vue de la vente au poids médicinal d’un produit quelconque dont la vente est réservée aux pharmaciens, ne peuvent
s’effectuer que sous la surveillance directe des pharmaciens » Article 117 : « le pharmacien responsable est le principal responsable des opérations suivantes constituant des actes pharmaceutiques : - l'achat et le contrôle de matières premières; - le développement galénique; - la fabrication et toute opération de conditionnement des médicaments;
- le contrôle à tous les stades de la production; - le contrôle des produits finis;
- le magasinage, la vente et la distribution;
- l'importation et le contrôle des produits pharmaceutiques importés;
- la libération des produits finis. - Tout acte
pharmaceutique doit être effectué sous la
Le contrôle de la fabrication
11ème alinéa, article 9 :
« pour assurer le contrôle direct de la fabrication, du conditionnement et de la répartition des médicaments, les établissements sont tenus de faire appel au concours d’un nombre de pharmaciens
proportionné à l’importance de l’établissement et à la nature de son activité »
La détention et la distribution des médicaments
7ème alinéa, article 6 :
« nul s’il n’est pharmacien autorisé ne pourra détenir pour la vente ou la distribution au détail, vendre ou distribuer pour l’usage de la médecine humaine ou vétérinaire aucune drogue, substance, composition ou préparation auxquelles sont attribuées des propriétés médicinales, curatives ou préventives, tout fait de cette nature étant considéré et sanctionné comme un exercice illégale de la profession pharmaceutique » surveillance effective d'un pharmacien. Article 121 : On entend
par pharmacien assistant d'un établissement pharmaceutique la
personne qui, autorisée à exercer la pharmacie, assiste le pharmacien responsable ou le pharmacien délégué dudit établissement. Cette assistance consiste en particulier dans la supervision des tâches suivantes : - achat et contrôle de matières premières ou de produits finis ; - fabrication et conditionnement de médicaments ; - contrôle de qualité ; - stockage, vente et distribution des médicaments. Vente au détail à l’officine article 10 :
« Nul ne peut offrir, mettre en vente ou vendre au public, en
dehors d’une officine,
des médicaments ou produits présentés comme jouissant des propriétés curatives ou
article 30 : voir tableau
III.
article 112 :
« Nul ne peut offrir, mettre en vente ou vendre au public, en
dehors d’une officine,
des médicaments ou
préventives et, notamment sur la voie publique, sur les marchés, à domicile ou dans les magasins , non affectés à la profession pharmaceutique »
pharmaceutiques non médicamenteux,
notamment sur la voie publique, sur les marchés, à domicile ou dans les magasins, non affectés à la profession pharmaceutique »
La nouvelle loi détermine avec plus de précision que le Dahir de 1960 les actes pharmaceutiques attribués au pharmacien responsable, délégué, ou assistant dans les établissements pharmaceutiques industriels ou grossistes répartiteurs.
La vente au public, des médicaments ou produits pharmaceutiques non
médicamenteux est un monopole du pharmacien d’officine, comme l’affirme l’article 112 du nouveau code et l’article 10 du Dahir 1960 ci-dessus. Mais le législateur ajoute à la fin de ces articles que cet opération est interdite aux magasins non affectés à la profession pharmaceutique, en fait même si un établissement est affecté à cette profession (industriel, grossiste-répartiteur….) on ne peut y vendre ces produits au public ! Malheureusement, cette pratique a toujours lieu au niveau des établissements industriels qui vendent directement au patient certains médicaments dits à usage hospitalier.
II.3.2. Les produits et objets inclus dans le monopole pharmaceutique :
Le tableau suivant résume la comparaison entre le Dahir de 1960 et le nouveau code sur les produits et objets relevant du monopole pharmaceutique :
Tableau III : Produits et objets inclus dans le monopole pharmaceutique : [27]
Le Dahir du 19 Février 1960 [26]
Le Dahir du 22 Novembre 2006 [16]
Article 13, 2ème, 3ème, 4ème alinéa :
« ils (les pharmaciens) pourront
détenir et vendre toutes drogues, tous produits chimiques ou préparations pharmaceutiques autres que ceux qui figurent au codex français à condition qu’ils soient étiquetés et vendus conformément à leur composition.
Ils ne pourront faire dans leur officine aucun autre commerce que celui des médicaments, des objets se rattachant à l’art de guérir ou à l’hygiène, des produits diététiques, des produits hygiéniques et des produits chimiques.
La vente des médicaments secrets est interdite. »
Article 30 :
« sont réservées exclusivement aux pharmaciens d’officine :
-la préparation des médicaments visés aux 1, 2, et 3 de l’article 2. -la détention des produits ci-après en vue de leur dispensation au public :
*les médicaments ainsi que les objets de pansements, produits et articles définis à l’article 4.
*les laits ainsi que les aliments lactés diététiques pour nourrissons et les aliments de régime destinés aux enfants de 1er âge.
A titre accessoire, les
pharmaciens d’officine peuvent détenir et vendre :
-toute drogue, tous produits chimiques ou préparations pharmaceutiques, autres que ceux qui figurent à la ou (les) pharmacopée en vigueur à condition qu’ils soient étiquetés et vendus conformément à leur composition.
-les produits destinés à l’entretien ou à l’application des lentilles oculaires de contact.
-les réactifs conditionnés en vue de la vente au public.
-les laits ainsi que les aliments lactés diététiques pour nourrissons
et les aliments de régime destinés aux enfants de 2ème âge.
-les huiles essentielles.
-les sucettes, les tétines et les biberons.
D’après cette comparaison nous observons que les deux textes donnent au pharmacien d’officine le droit de détenir et vendre toute drogue, tous produits chimiques ou préparations pharmaceutiques, autres que ceux qui figurent à la ou (les) pharmacopée(s) en vigueur à condition qu’ils soient étiquetés et vendus conformément à leur composition.
Le nouveau code remplace le codex français par la pharmacopée en vigueur, en attendant la publication d’une pharmacopée nationale.
Les produits relevant du monopole pharmaceutique sont mieux précisés par ce nouveau code que le Dahir de 1960.
Les préparation visés aux 1, 2, et 3 de l’article 2 sont : - La préparation magistrale.
- La préparation officinale.
- Le médicament spécialisé de l’officine.
Les produits et articles définis à l’article 4 sont les produits pharmaceutiques non médicamenteux qui sont :
- Les objets de pansements, produits et articles à usage médical figurant à la
pharmacopée.
- Les objets de pansement, produits et articles à usage médical, présentés sous
une forme stérile conformément aux conditions de stérilité décrites dans la pharmacopée.
Pourquoi cette appellation de produits pharmaceutiques non médicamenteux ?
Pourquoi le législateur n’a pas utilisé le terme de dispositif médical qui figure dans la circulaire n° 7 de 19 février 1997 ?
Ces produits, et par souci de qualité et de préservation de la santé publique, sont soumis comme les médicaments auxquels s’applique la procédure d’autorisation de mise sur le marché ; à un système d’enregistrement préalable à leur mise sur le marché (articles 52, 53, 54 de la loi 17-04).
L’article 13 du Dahir de 1960 incluait les produits hygiéniques dans le monopole pharmaceutique, cependant l’article 30 de la nouvelle loi 17-04 ne spécifie pas ces produits.
L’article 2 du code définit 19 produits et indique qu’ils sont considérés comme des médicaments. Étant considérés ainsi, ils relèvent donc du monopole pharmaceutique. Ceci représente un élargissement et une précision de ce monopole.
Si vraiment la nouvelle loi 17-04 vient pour élargir et préserver le monopole pharmaceutique ; en pratique, ce monopole n’est-il pas quotidiennement battu en brèche sous le regard des autorités comme le cas du fameux souk de médicament à Oujda : souk el fellah ?
II.3.3. Dérogations au monopole pharmaceutique :
On entend par dérogation, au sens strict du terme, dispense ou exonération.
Nous comparons dans le tableau suivant les dérogations au monopole
pharmaceutiques dans le Dahir de 1960 et le nouveau code. [29] :
Tableau IV : Dérogations au monopole pharmaceutique :
Dahir de 1960 Dahir de 2006
a. Article 5, alinéa 4 du dahir de 1960 :
Concession aux médecins établis dans des localités où il n’y a pas de pharmacies à vendre des médicaments prescrits par leurs soins à la condition spécifique de l’autorisation du secrétaire général du gouvernement et de l’absence d’une officine à moins de 25 km.
b. Article 6 du dahir de 1960 :
dérogations particulières aux établissements publics et à l’institut Pasteur.
c. Article 6 du dahir de 1960 :
dérogation aux risques endémiques (Fléaux, catastrophes naturelles…)
d. Article 16 du dahir de 1960 :
dérogation aux prisons et aux organismes privés
Article 27 :
Dérogation accordée à l’institut Pasteur pour effectuer des opérations de fabrication, d’importation et de commercialisation des médicaments d’origine biologique ainsi que les médicaments immunologiques définis au 7ème alinéa de l’article 2.
Article 28 :
Dérogation accordée au centre national de l’énergie et des techniques nucléaires, pour effectuer des opérations de fabrication, d’importation et de commercialisation des médicaments radio pharmaceutiques définis au 9ème alinéa de l’article 2.
Le nouveau code du médicament et de la pharmacie a réduit les dérogations au monopole pharmaceutique par rapport au Dahir de 1960. Il a abrogé par son dernier article, le décret royal n°074-66 du 16 septembre 1966, relatif à l’article 5, alinéa 4 du Dahir 1960, fixant les conditions de ventes des médicaments par les médecins.
Cas des produits médicamenteux à usage vétérinaire:
L’article 6 du Dahir de 1960 stipulait que tout vétérinaire diplômé pourra, sans tenir officine ouverte, délivrer des produits médicamenteux pour l’usage vétérinaire, si la localité où il opère est dépourvue de pharmacie.
La promulgation de la loi n°21-80 en 26 décembre 1980, relative à l’exercice, à titre privée, de la médecine, de la chirurgie et de la pharmacie
vétérinaires, a permis le cumul des actes pharmaceutiques et vétérinaires
(fabrication, prescription, dispensation et administration) par le vétérinaire. Cette dérogation au monopole pharmaceutique s’est transformée en un monopole partagé entre les pharmaciens et les vétérinaires. [30]
L’article 158 de la nouvelle loi n° 17-04 adopte les dispositions de la loi
21-80.
II.3.4. Le monopole pharmaceutique en France et en Europe :
L’article L4211-1 du code français de la santé publique, réserve aux pharmaciens la vente au détail et la préparation : [20,21]
- Des médicaments destinés à l’usage de la médecine humaine ;
- Des objets de pansement et de tout articles présentés comme conforme à la pharmacopée ;
- Des produits insecticides et acaricides destinés à être appliquées sur l’homme ;
- Des produits destinés à l’entretien ou à l’application des lentilles oculaires de contact ;
- La préparation des générateurs, trousses ou précurseur relatifs aux médicaments radio pharmaceutiques ;
- Des plantes médicinales inscrites à la pharmacopée sous réserve des dérogations ;
- Des huiles essentielles dont la liste est fixée par décret ainsi que de leurs dilutions et préparations ne constituant ni des produits cosmétiques, ni des produits à usage ménager, ni des denrées ou boissons alimentaires ;
- Des aliments lactés diététiques pour nourrissons et des aliments de régime destinés aux enfants du premier âge (moins de quatre mois), dont les caractéristiques sont fixés par arrêté des ministres chargés de la consommation et de la santé ;
- Des dispositifs médicaux de diagnostic in vitro destinés à être utilisés par le public.
Certains professionnels ont le droit de vendre des produits faisant partie intégrante du monopole pharmaceutique comme :
- Les médicaments vétérinaires qui peuvent être préparés, détenus et
délivrés par les vétérinaires;
- Les produits d’entretien pour lentilles de contact par les opticiens-
lunetiers ;
- Les appareils et objets susceptibles d’être utilisés à des fins abortives qui
- Les seringues et aiguilles destinées aux injections parentérales qui
peuvent être vendues par les établissements se consacrant exclusivement au commerce du matériel médico-chirurgical et dentaire, et distribuées à titre gratuit par certaines associations ou personnes menant une action de prévention du sida ou de réduction des risques chez les usagers de drogues.
Toutefois, la dérogation la plus notable concerne les médecins propharmaciens. Il s’agit de praticiens établis dans une agglomération dépourvue d’officine et qui ont pu obtenir du préfet l’autorisation de détenir à leur cabinet, un dépôt de médicaments. Ces médecins ne peuvent délivrer des médicaments qu’aux personnes auxquelles ils donnent leurs soins et dans la limite de leurs prescriptions.
En Europe, le monopole pharmaceutique n’est pas une règle. En fait, dans la communauté économique européenne, deux conceptions du monopole pharmaceutique coexistent. En Belgique, en Espagne, en Grèce, en Italie, et au Portugal, le pharmacien d’officine se voit reconnaître un monopole, en principe complet, de dispensation du médicament. En revanche, dans d’autres pays, la dispensation de certains médicaments est possible dans d’autres structures que l’officine. [31]
En Allemagne, certains médicaments (plantes médicinales, antiseptiques, laxatifs…) peuvent être vendus chez des droguistes, dans des grandes surfaces ou dans des magasins spécialisées.
Au Royaume-uni, l’officine pharmaceutique a le monopole de la vente des médicaments sur ordonnances. Mais certains médicaments spécialement
conditionnés, comme l’aspirine peuvent être vendus hors de l’officine : dans les stations services, les grandes surfaces, voire dans des distributeurs automatiques. Au Pays-Bas, également, ce monopole ne concerne que les médicaments vendus sur ordonnance. La vente des autres médicaments peut être assurée par des droguistes. Dans la liste des médicaments qui sont ainsi librement vendus on trouve, des antigrippaux, de l’aspirine ou des antiémétiques. [32, 33]
Récemment, le monopole pharmaceutique en France est attaqué par la commission européenne. En effet les autorités françaises ont reçu le 21 Mars 2007 une "lettre de mise en demeure" enjoignant à la France de revenir sur sa législation qui oblige le propriétaire d’une officine à être pharmacien et qui ne permette pas que les officines soient détenues par des groupes de grande distribution. [34,35]
La législation marocaine protège le monopole pharmaceutique plus que les législations européennes, mais la répression des atteintes à ce monopole reste défaillante.
Chapitre : 3
I. Introduction :
Est considérée comme vénéneuse, toute substance dont l’administration peut entraîner des effets nocifs et être source d’accident même à l’occasion de son utilisation thérapeutique. Il faut tenir compte aussi de la toxicité indirecte du produit, celle qui résulte d’un mauvais usage de celui-ci, mais également des éventuels abus et détournement d’usage. [20]
Ainsi le législateur a été amené à promulguer les lois régissant la fabrication, la détention, le commerce, la prescription, l’étiquetage et la dispensation de ces substances dans le but de préserver la santé publique et l’environnement.
Dans ce chapitre, après un aperçu sur l’évolution historique de la réglementation de substances vénéneuses en France et au Maroc, nous procéderons à une étude critique du Dahir de 1922 régissant ces substances au Maroc.
II. Évolution historique de la réglementation des substances
vénéneuses :
II.1. En France :
La législation française est l’aboutissement d’un long processus remontant aux temps les plus anciens, jalonné notamment par l’édit de Louis XIV en Juillet 1682 faisant suite à «l’affaire des poisons », la déclaration royale du 25 Avril 1777, les lois du 21 germinal de l’an XI, du 19 juillet 1845, du 12 juillet 1916, du 11 septembre 1941…
La loi du 12 juillet 1916 relative à l’importation, au commerce, à la détention et à l’usage des substances vénéneuses et son décret d’application du 14 septembre 1916 est l’acte de naissance des «tableaux» d’inscription des substances toxiques, stupéfiantes et dangereuses. Le tableau A réunit les «toxiques», au tableau B sont inscrits les stupéfiants, et le tableau C concerne les substances dangereuses. [1, 3,8]
L’ancienne et classique réglementation des substances vénéneuses a sensiblement évolué dans le sens des dispositions toujours plus détaillées, ceci pour assurer une meilleure protection du public à l’égard des substances toujours plus nombreuses et aux effets plus redoutables. [1,3]
II.2. Au Maroc :
Le Dahir du 02 décembre 1922 portant règlement sur l’importation, le commerce, la détention des substances vénéneuses constitue à nos jours l’unique référence, que tout professionnel dans le domaine de la pharmacie, de la médecine, du commerce et de l’agriculture est tenue de connaître et suivre rigoureusement. Ce Dahir a abrogé successivement le Dahir du 28 janvier 1916 visant l’opium et ses alcaloïdes, l’arrêté viziriel du 13 Avril 1916 complétant le précédent. Plus tard, est promulgué le Dahir du 17 Mars 1953 qui a distingué les substances vénéneuses en deux sections selon leurs destinations :
Soit à l’industrie, le commerce ou l’agriculture, soit à la médecine humaine ou vétérinaire et a constitué aussi leur mise à jour.
Ainsi, se succédèrent une série d’arrêtés : 10 Août 1953; 11 janvier 1955; 11 juillet 1960 qui furent abrogés en 1966 par l’arrêté ministériel du 11 mars
1966, qui modifiait et complétait la composition des tableaux A, C et B des substances vénéneuses exonérées des régimes des trois tableaux. [24]
30 ans plus tard, l’arrêté du ministre de la santé publique nº 1850-96 du 03 septembre 1996 est venu abroger et remplacer le tableau B de l’arrêté du 11 mars 1966.
Il faut signaler que ce Dahir du 2 décembre 1922 a connu plusieurs modifications ponctuelles de ses articles sans penser à une refonte globale.
Il comprend actuellement 45 articles, après l’abrogation des articles de 45 à 49 par le Dahir du 21 Mai 1974, relatif à la répression de la toxicomanie et la prévention des toxicomanes. Il est réparti en 4 titres dont les trois premiers classifient les substances vénéneuses en trois tableaux A, B et C, et le IVème titre relatif aux dispositions générales. [36]
III. Analyse générale du Dahir de 1922 :
Une analyse générale du Dahir de 02 décembre 1922 permet la constatation de certaines aberrations de forme et de fond :
Utilisation de termes dépassés :
Dés la première lecture du dahir, il est à remarquer l’utilisation des termes dépassés, voire aberrants :
- « préparations destinées à être absorbées par la voie stomacale » qui signifie apparemment la voie orale.
- « dose indiquée dans le codex » : remplacé depuis plusieurs décennies par la “pharmacopée”.
- dans l’article 27 alinéa 4, nous lisons «… aux producteurs indigènes ...» : après notre indépendance, ce mot n’a pas lieu de persister.
d’infraction au dahir “le procès verbal est transmis, sans délai au procureur de la république”.
- dans l’article 8 et 9 :«…arrêté du directeur général de l’agriculture, du commerce et de la colonisation » [7,36]
D’après ces deux dernières remarques, ce dahir doit même faire l’objet, dans le contexte actuel, d’une refonte formelle pour tenir compte des changements dans les autorités et organismes administratifs chargés de son application. [22]
Dans l’article 42, le législateur incite l’autorité de contrôle à effectuer des prélèvements «…dans les conditions et les formes prévues au dahir du 14 Octobre 1914 et de 19 Mars 1916 sur la répression des fraudes » : sachant que ces textes de lois sont abrogés depuis longtemps.
Remarques sur certaines dispositions du Dahir de 1922 :
Les articles 12 bis et 39 relatifs respectivement aux produits cosmétiques des tableaux A et C ont été mentionnés très brièvement. Vu l’utilisation importante de ces produits surtout en automédication, il est intéressant de consacrer un chapitre relatif aux produits cosmétiques et d’y établir ces listes.
L’article 14 se réfère uniquement à la résidence des clients pour déterminer les cas où le vétérinaire peut délivrer des médicaments contenant des substances vénéneuses, ainsi même si le vétérinaire réside dans une localité pourvue d’une officine de pharmacie, il pourra donc délivrer ces médicaments à la seule condition que la localité où résident ses clients en soit privée, et c’est souvent le cas de la plupart des clients résidant au milieu rural.
l’usage vétérinaire si la localité où il opère est dépourvue de pharmacie »
Nous concluons que ces deux articles convergent pour donner plus de prérogative aux vétérinaires, cela constitue une atteinte au monopole pharmaceutique.
Il faut noter que les listes des produits appartenant à chaque tableau ne sont pas mises à jour en pratique comme il était prévu. Les produits de la section II de chaque tableau doivent être précisés par leur dénomination scientifique et par leur nom commun ce qui facilite sa consultation.
Pour compléter cette analyse de fond en parallèle avec la législation française, nous allons passer comparativement en revue les dispositions communes et aussi les particularités de chaque tableau.
IV. Analyse des dispositions communes :
IV.1. Classification des substances vénéneuses :
IV.1.1 Au Maroc :
Le 1er article du Dahir de 1922 (modifié par le Dahir du 17 Mars 1953) précise les trois catégories de substances vénéneuses : Tableau A (produits toxiques), tableau B (produits stupéfiants) et tableau C (produits dangereux).
[36]
Cet article à apporté une précision sur la division des produits des tableaux précédemment cités en deux sections : section I pour les produits destinés au commerce à l’industrie ou l’agriculture et section II pour ceux destinés à la médecine humaine ou vétérinaire.
substance vénéneuse en général ni celle de chaque tableau. Même avec la nouvelle loi nº17-04 portant code du médicament et de la pharmacie qui réserve un chapitre pour les définitions, ces substances restent encore non définies.
IV.1.2. En France :
En se référant à l’article L 5132-1, relatif aux substances vénéneuses, du code de la santé publique français : « on entend par “substance”, les éléments chimiques et leurs composés comme ils se présentent à l’état naturels ou tels qu’ils sont produits par l’industrie, contenant éventuellement tout additif nécessaire à leur mise sur le marché ». On peut reprocher à cette définition qu’elle parait exclure les substances biologiques (plantes et drogues) pourtant, ces dernières sont bel et bien inscrites sur les listes de substances vénéneuses.
[3,37]
Après la suppression des anciennes sections I et II des “tableaux”, ces substances sont classées en deux grands groupes.
Dans le premier groupe, nous trouvons les matières premières qui sont couramment utilisées à l’officine pour préparer les médicaments, dans le second, sont placées les substances et préparations constituant des médicaments ou des produits assimilés (insecticides et acaricides destinés à être appliqués sur l’homme, produits destinés à l’entretien ou l’application des lentilles de contact).
Les matières premières sont réparties en : 1- Substances et préparations stupéfiantes ; 2- Substances et préparations psychotropes ;
3- Substances et préparations dangereuses qui sont subdivisées, selon l’article L 5132-2 du code français de la santé publique, en huit catégories :
Les médicaments et produits assimilés sont classés comme l’indique l’article L 5132-6 du code français: [20,21]
1- Soit comme stupéfiants ;
2- Soit sur la liste I, pour les substances présentant les risques les plus élevés pour la santé ;
3- Soit sur la liste II pour les autres ; 4- Et la classe des psychotropes.
Cette dernière classe n’est pas introduite dans le Dahir de 1922, même si le Maroc a signé la convention internationale contre le trafic des stupéfiants et des substances psychotropes en décembre 1988. [38]
IV.1.3. L’inflation des tableaux :
Le contenu des tableaux de substances vénéneuses n’a cessé de croître au cours du temps. Parmi les raisons de cette inflation, l’apparition de nouvelles molécules chimiques toujours plus actives, et la pharmacomanie liée à l’usage des excitants, tranquillisants et autres “médicament de confort”, dont il a fallu prévenir une utilisation abusive…
Les conséquences, cependant, ne sont pas satisfaisantes, d’une part la notion de produit “toxique” ou “dangereux” perd sa valeur symbolique devant le prescripteur, le pharmacien, et même le patient, dés lors que la plupart des médicaments entrent maintenant dans ces catégories. D’autre part, le rôle traditionnel du pharmacien se trouve entravé au profit d’une liste d’interdits, à mesure notamment que le tableau C s’étend à des produits qui ne sont pas dangereux lorsqu’ils sont destinés à leur véritable usage. [12]
Il s’avère nécessaire de tenter une redéfinition des critères de classification des substances vénéneuses, on pourrait mettre l’accent non pas sur des
![Figure 1 : Des médicaments exposés librement dans un marché [28]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037386.690626/35.892.162.699.202.791/figure-médicaments-exposés-librement-marché.webp)


![Figure 2 : Mesure de la distance entre deux officines [60]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037386.690626/98.892.162.808.411.787/figure-mesure-distance-officines.webp)
![Figure 4 : Répartition des officines dans les principales villes du Maroc[51]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037386.690626/101.892.176.765.131.913/figure-répartition-officines-principales-villes-maroc.webp)
![Figure 5 : Evolution du nombre des pharmaciens d’officine autorisés à exercer chaque année entre 1986 et 2006 au Maroc [51]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037386.690626/103.892.173.649.170.574/figure-evolution-nombre-pharmaciens-officine-autorisés-exercer-année.webp)
![Figure 6 : Evolution du nombre des pharmaciens d’officine selon l’origine des diplômes : [51]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037386.690626/106.892.163.732.103.570/figure-evolution-nombre-pharmaciens-officine-l-origine-diplômes.webp)