HAL Id: dumas-01759022
https://dumas.ccsd.cnrs.fr/dumas-01759022
Submitted on 4 Jun 2018HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
La chaîne numérique en implantologie : exemple du
système Sirona® en cabinet d’omnipratique
William Le Chaffotec, Clément Denis
To cite this version:
William Le Chaffotec, Clément Denis. La chaîne numérique en implantologie : exemple du système Sirona® en cabinet d’omnipratique. Sciences du Vivant [q-bio]. 2016. �dumas-01759022�
THÈSE D'EXERCICE / UNIVERSITÉ DE RENNES 1
UFR D'ODONTOLOGIE
Sous le sceau de l’Université Européenne de Bretagne
THÈSE EN VUE DU
DIPLÔME D'ÉTAT DE DOCTEUR EN CHIRURGIE DENTAIRE
Présentée par
William LE CHAFFOTEC
Né le 05 novembre 1988 à Vernon (27)Clément DENIS
Né le 25 décembre 1988 à Bois-Guillaume (76)La chaîne
numérique
en implantologie :
exemple du système
Sirona® en cabinet
d’omnipratique
Thèse soutenue à Rennes le 20 janvier 2016
Devant le jury composé de :
Pr. Jean-Marie VULCAIN
PU-PH à l’Université de Rennes 1 / Président
Dr. Xavier RAVALEC
MCU-PH à l’Université de Rennes 1 / Directeur de
thèse
Dr. Gérard BADER
MCU-PH à l’Université de Rennes 1 / Juge
Dr. Caroline BOLLE
AHU-PH à l’Université de Rennes 1 / Juge
Dr. Bertrand DINAHET
Praticien attaché à l’Université de Rennes 1 /
2
U.F.R. ODONTOLOGIE
UNIVERSITE DE RENNES I 1er janvier 2016
CORPS ENSEIGNANTS DE L'U.F.R. D'ODONTOLOGIE
56e SECTION : DEVELOPPEMENT, CROISSANCE ET PREVENTION
SOUS-SECTION 01 : PEDODONTIE
Professeur Emérite : M. ROBERT Jean-Claude
Professeur des Universités : M. SIXOU Jean-Louis (responsable Univ. + Hôp.) Maître de Conférences des Universités : Mme MARIE-COUSIN Alexia (plein temps) Assistant Hospitalier Universitaire : Melle LEMARÉCHAL Sabrina
SOUS-SECTION 02 : ORTHOPEDIE DENTO-FACIALE
Professeur des Universités : M. SOREL Olivier (responsable Univ. + Hôp.) Assistant Hospitalier Universitaire : M. DELVALLEZ Benjamin
Assistant Hospitalier Universitaire : M. GIVELET Morgan Assistant Hospitalier Universitaire : M. LEGRAND Nicolas Assistant Hospitalier Universitaire : Melle GUILLON Mathilde
SOUS-SECTION 03 : PREVENTION, EPIDEMIOLOGIE, ECONOMIE DE LA SANTE, ODONTOLOGIE LEGALE
Professeur des Universités : Mme BERTAUD-GOUNOT Valérie Maître de Conférences des Universités : M. PRIGENT Hervé
Assistant Hospitalier Universitaire : Mme TROHEL Gilda
Assistant Hospitalier Universitaire : Mme AMBROISE Constance
57e SECTION : SCIENCES BIOLOGIQUES, MEDECINE ET CHIRURGIE BUCCALES
SOUS-SECTION 01 : PARODONTOLOGIE
Professeur des Universités : Mme JEANNE Sylvie (responsable Univ. + Hôp.) Assistant Hospitalier Universitaire : M. GODARD Antoine
Assistant Hospitalier Universitaire : Melle BOLLE Caroline
Assistant Hospitalier Universitaire : Mr PHILIPPAKIS Alexandre SOUS-SECTION 02 : CHIRURGIE BUCCALE, PATHOLOGIE ET THERAPEUTIQUE, ANESTHESIE ET REANIMATION
Maître de Conférences des Universités : Mme LEJEUNE-CAIRON Sophie (responsable Univ.) Maître de Conférences des Universités : M. LIMBOUR Patrick (responsable Hôp.)
Maître de Conférences des Universités : M. CLIPET Fabrice Maître de Conférences des Universités : M. BADER Gérard Assistant Hospitalier Universitaire : Melle OBRY Faustine Assistant Hospitalier Universitaire : Melle MASSOT Murielle Assistant Hospitalier Universitaire : Melle THIBAUT Flora
3
SOUS-SECTION 03 : SCIENCES BIOLOGIQUES (Biochimie, Immunologie, Histologie, Embryologie, Génétique, Anatomie Pathologique, Bactériologie, Pharmacologie)
Professeur des Universités : Mme BONNAURE-MALLET Martine (responsable Univ.) Maître de Conférences des Universités : M. MEURIC Vincent
Maître de Conférences associé
des Universités : Mme MARTIN Bénédicte Assistant Associé Universitaire : Mme LECLERC Julia Assistant Associé Universitaire : Mme DAVID Sandrine
58e SECTION : SCIENCES PHYSIQUES ET PHYSIOLOGIQUES ENDODONTIQUES ET
PROTHETIQUES
SOUS-SECTION 01 : ODONTOLOGIE CONSERVATRICE, ENDODONTIQUE Professeur des Universités : M. VULCAIN Jean-Marie
Maître de Conférences des Universités : Mme DAUTEL-MORAZIN Anne (responsable Univ.) Maître de Conférences des Universités : Mme LE GOFF Anne (responsable Hôp.)
Maître de Conférences des Universités : M. TURPIN Yann-Loïg Maître de Conférences des Universités : M. PERARD Matthieu Maître de Conférences des Universités : Mme LE CLERC Justine Assistant Hospitalier Universitaire : M. GICQUEL Pierre-Etienne Assistant Hospitalier Universitaire : Melle DUMONT Laure-Anne Assistant Hospitalier Universitaire : Mr DEMOY Julien
SOUS-SECTION 02 : PROTHESES (Conjointe, Adjointe Partielle, Complète, Maxillo-Faciale) Maître de Conférences des Universités : M. RAVALEC Xavier (responsable Univ.) Maître de Conférences des Universités : M. THÉPIN Jean-Claude
Maître de Conférences des Universités : M. BEDOUIN Yvan
Assistant Hospitalier Universitaire : Mme BARRAU-VASLIN Lorianne Assistant Hospitalier Universitaire : M. CARDONA Julien
Assistant Hospitalier Universitaire : M. PLARD Hervé Assistant Hospitalier Universitaire : M. POIRIER Fabien
SOUS-SECTION 03 : SCIENCES ANATOMIQUES ET PHYSIOLOGIQUES, OCCLUSODONTIQUES BIOMATERIAUX, BIOPHYSIQUE, RADIOLOGIE
Professeur des Universités : M. CATHELINEAU Guy, Président de l'Université Maître de Conférences des Universités : Mme CHAUVEL-LEBRET Dominique (responsable Univ. +
Hôp.)
Assistant Hospitalier Universitaire : Mme MEARY Fleur
Assistant Hospitalier Universitaire : Mr LE PADELLEC Clément
ENSEIGNANTS AUTRES SECTIONS
41e section : Sciences Biologiques
Maître de Conférences : Mme TAMANAI-SHACOORI Zohreh 64e/65e section : Biochimie et Biologie Moléculaire/Biologie Cellulaire
Maître de Conférences : Mme GAUTIER-COURTEILLE Carole ******
4
Au Professeur Jean-Marie VULCAIN
Professeur des Universités
Sous-section : Odontologie conservatrice et endodontie
Vous nous avez fait l’honneur d’accepter la présidence de ce jury.
Nous tenons à vous remercier pour vos ensei-gnements, vos conseils et vos conseils tout au long de notre cursus.
Qu’il nous soit permis de vous exprimer nos remerciements les plus sincères et notre respect le plus profond.
5
Au Docteur Xavier RAVALEC
Maître de Conférence des Universités - Praticien Hospitalier
Sous-section : Prothèses (Conjointe, Adjointe Partielle, Complète, Maxillo-Faciale)
Merci de la confiance que vous nous avez accordé en acceptant la direction de cette thèse.
Nous tenons à vous remercier pour la qua-lité de votre enseignement, ainsi que pour votre simplicité et votre gentillesse durant nos années d’études.
Veuillez trouver dans ce travail l’expres-sion de notre gratitude et de nos sentiments les plus chaleureux.
6
Au Docteur Gérard BADER
Maître de Conférence des Universités - Praticien Hospitalier
Sous-section : Chirurgie buccale, Pathologie et Thérapeutique, Anesthésie et Réani-mation
Vous nous faites l’honneur de faire partie de ce jury de thèse.
Ce fût un réel plaisir d’avoir fait partie de votre équipe en Chirurgie Buccale.
Veuillez trouver ici le témoignage de notre plus grande gratitude.
7
Au Docteur Caroline BOLLE
Assistante Hospitalier Universitaire – Praticien Hospitalier Sous-section : Parodontologie
Nous vous remercions d’avoir accepté de juger notre travail en siégeant parmi ce jury.
Soyez assuré de notre respect le plus sin-cère.
8
Au Docteur Bertrand DINAHET
Praticien Attaché
Sous-section : Prothèses (Conjointe, Adjointe Partielle, Complète, Maxillo-Faciale)
Sans qui cette thèse n’aurait pu voir le jour. Vous nous avez fait le plaisir de nous appor-ter vos connaissances et votre expérience indis-pensables à la réalisation de ce travail.
Nous tenons à vous remercier pour votre in-vestissement, votre gentillesse et vos encourage-ments.
Veuillez trouver ici le témoignage de notre profonde reconnaissance et de notre amitié sin-cère.
9
Remerciements – William LE CHAFFOTEC
À mes parents. Merci pour m’avoir fait confiance dans mon parcours, d’avoir tou-jours été là quand il le fallait.
À mes grands-parents. Je vous dois beaucoup. Je garde un profond respect pour votre générosité et votre dévotion. Merci d’être là.
À ma grand-mère, Jeannette. Merci pour toutes tes petites attentions et pour ce que tu es.
À Gauthier et Clarisse. Vous m’êtes indissociables et indispensables. Je sais la chance que j’ai de vous avoir comme frère et sœur.
À Robin M. Merci pour ta franchise, tes qualités humaines, nos soirées geek et nos débriefings Mac Do du dimanche soir ! Tu as été là quand j’avais besoin de parler. Je m’estime vraiment chanceux d’avoir un ami comme toi.
À Robin S. Mon compère de baroude, depuis Madrid (c’est loin !) jusqu’à cet infâme sommet du Rinjani. On peut dire que tu m’as rendu accro, et ce n’est pas près de s’arrêter là. Oh non! « C’est non. ». Big up à cet homme exceptionnel si ce n’est son accent anglais à couper au couteau !
À mon bro, Nico. Né une journée (ou deux ? ;) ) avant moi, je mesure moi aussi le chemin parcouru depuis que j’ai aperçu ce polo Lacoste à quelques rangs devant moi dans le Marcel Simon. Merci pour le foot dans les couloirs de ton appart, pour ton lift monstrueux au tennis et pour les fous-rires. Merci d’avoir été là aux bons mo-ments depuis notre première année de médecine, épique, jusqu’à maintenant. À Wajd. Merci pour ta répartie, ton humour, nos débats-narguilé et nos parties d’échecs deux heure avant les rattrapages. Grognon et blasé, je t’aime comme tu es. Alors ne change surtout pas (sauf le LG dans COD4, ça tu peux arrêter).
À Ben, mon kiteux normand et nos parties de tennis qui ont toujours fini n’importe comment !
10 À Bertrand, mon alençonnais de cœur.
À Gab et Axelle, deux personnes qui me sont chères. Merci pour les supers moments qu’on a passés à l’appart aux Gayeulles. See you in Swiss guys.
À Juju, Max, Nico, vous formez une belle tripotée de mecs biens. Que du bon temps passé avec vous, avec un épisode caennais épique !
À Maryse, Chloé, Gaëlle, Marion, Camille, Aube, Pelag, Bébère, Caro, Rémi, Alex, et aux « D3 ». Tous autant que vous êtes : sans vous mes études n’auraient pas eu la même saveur. Merci d’être là.
À Alina, parce que tu m’as supporté et soutenu pendant la rédaction de cette thèse. À Charles, pour tout ce qu’on a partagé humainement, sportivement. Tu restes quelqu’un qui m’est cher.
À Evan et Johan, sérieusement les mecs quand j’avais besoin de décompresser vous étiez là ! Merci pour les barres et les parties jusqu’à pas d’heure.
À la team de mes vacs de prothèse : Hervé, Julien, Jerem, Matho, merci pour votre sympathie, votre pragmatisme et pour l’ambiance dans le service. J’ai passé du bon temps avec vous !
Au Dr Patrick Lesage, qui m’a énormément appris pendant mon année de stage actif. Je mesure la chance que j’ai eue, et je salue une très grande qualité de praticien, mais aussi d’homme. Salue la grande qualité du praticien, mais aussi de l’homme.
À Marco pour avoir animé mes séances de TP, mais aussi à Philouze, Cynthia, Thi-baut, Seb’ P, Julie LB, Capucine, Laure, Benouze, Damien A, Pierre LB, Laeti,, et à tous ceux qui ont ponctué mes études mais qui m’ont apporté beaucoup. Difficile de tous vous citer.
Et à Clément, évidemment. Pour m’avoir montré très tôt ce que signifie le mot « dé-termination ». Entre les barres de Snickers glacés et les barres de rires, je ne sais pas encore ce que j’ai préféré. Je suis chanceux d’avoir un ami comme toi. Allez, on a un road-trip moto post-thèse à faire d’urgence ;)
11
Remerciements – Clément DENIS
À mes parents. A ma mère pour ton aide et ton écoute, tu as toujours su me guider dans mes choix sans jamais porter de jugement. A mon père pour ces longues dis-cussions, tu m'as beaucoup appris et je sais que ce n'est pas fini!
À mon frère. Nos pintes O'kallaghan's, nos soirées mémorables, notre humour dé-bile me manquent à chaque fois que tu retournes étudier loin de nous.
À ma sœur au caractère inégalable et à son cœur en or. Ta capacité à nous suppor-ter avec Valentin m'étonnera toujours !
À mes grands-parents, depuis tout petit vous m’avez guidé sans le savoir vers ce métier passionnant.
À Marion, Julie, Louis, vous avez toujours été la pour moi! Marion, à quand notre transat à la voile?
À Olivier, le meilleur mono de planche à voile et d'aviron, merci pour ces sorties mémorables en plein hiver.
À Christophe, pour ton apprentissage et ta patience. Quatre ans après, ta manière de travailler m'influence encore.
À Laurent, le dentiste, cycliste, rameur, navigateur "jusqu'auboutiste", pour ton ac-cueil, ta gentillesse et tes cafés "broyés, pressés à 19 bar, fait maison".
À Benjamin, tu as su me faire confiance dès le début. Grâce à toi j'ai pu découvrir les différentes responsabilités qu'engage un cabinet dentaire. Heureusement il n'y a pas eu que le boulot, je garderai en mémoire nos longues discussions pendant nos pauses snickers, nos recherches de spots de grimpe entre 2 patients et tes his-toires incroyables d'alpinisme.
À Pierre et toute son équipe pour leur soutien et leur sympathie. Merci encore Pierre pour cette journée ski, sans le savoir tu m'as rendu un grand service ! À Nathalie, pour son dévouement et sa patience. Nos heures passées ensemble aussi bien à travailler qu'à se marrer m'ont formé autant que vous.
12 À William, ce fut un réel plaisir d’écrire cette thèse avec toi, ta minutie et ta quête de la perfection auront permis l'aboutissement de ce beau projet ! Le tout dans une atmosphère toujours détendue et studieuse, nos fous rires de « craquage » reste-ront ancrés dans mes souvenirs.
À Gabriel et Axelle, les personnes sur qui on peut compter sont rares et vous en faîtes partis.
À Cynthia, à son écoute, sa bienveillance. Tu as toujours su trouver les mots justes. Merci à tous ceux qui ont été à mes côtés pendant mes études : Robin, Wajd, Alex, Camille, Iaro, Ben, Bertrand, Laure.
13 « Je certifie sur l’honneur ne pas avoir repris pour mon compte des propos,
cita-tions, ou illustrations déjà publiées William LE CHAFFOTEC
« Je certifie sur l’honneur ne pas avoir repris pour mon compte des propos, cita-tions, ou illustrations déjà publiées
14
La chaîne numérique en implantologie :
exemple du système Sirona® en cabinet
15
Table des matières
1. Historique ... 20
1.1. Evolution de la planification implantaire ... 20
1.2. Le système CEREC® ... 21
1.3. Les différents systèmes de prise d’empreinte optique chez Sirona® ... 26
1.3.1. CEREC Bluecam® ... 26
1.3.2. CEREC Omnicam® ... 27
1.3.3. Comparaison des caméras Bluecam® et Omnicam® ... 28
1.3.4. L’Apollo DI® ... 31
2. La planification prothétique ... 35
2.1. Etapes générales ... 35
2.1.1. Anamnèse ... 35
2.1.2. Consentement libre et éclairé ... 38
2.1.3. Examen clinique exobuccal ... 38
2.1.4. Examen clinique exobuccal ... 41
2.1.5. Bilan radiologique initial ... 43
2.2. Le guide radiologique physique ... 46
2.2.1. Propriétés générales ... 46
2.2.2. Réalisation du guide radiologique ... 47
2.3. Le guide radiologique numérique : l’OptiGuide® ... 61
2.4. Quel guide radiologique ? Arbre décisionnel ... 64
2.5. L’étape d’acquisition radiologique tridimensionnelle en implantologie orale ... 65
2.5.1. Un bref historique ... 65
2.5.2. Scanner ou cone-beam ... 66
2.5.3. L’ORTHOPHOS® XG 3D et le GALILEOS® ... 68
2.6. Planification numérique tridimensionnelle : le système GALILEOS® ... 76
2.6.1. Historique : Simplant®, le premier logiciel de planification 3D ... 76
2.6.2. GALILEOS® Implant ... 76
3. La phase chirurgicale ... 94
3.1. Le guide chirurgical ... 94
3.1.1. Les différents guides en fonction de leur surface d’appui (Fig. 83) ... 94
3.1.2. Cahier des charges d’un guide chirurgical ... 97
3.1.3. Fabrication d’un guide chirurgical ... 97
3.2. Quelle technique chirurgicale ? ... 113
16
3.2.2. Mise en charge immédiate, précoce ou retardée ... 115
3.3. Protocole opératoire ... 116
3.3.1. La trousse chirurgicale ... 117
3.3.2. La chirurgie implantaire avec guide ... 121
4. La phase prothétique : la réalisation au cabinet dentaire ... 124
4.1. Les matériaux ... 124
4.1.1. Généralités : les céramiques ... 124
4.1.2. Les différents blocs usinables ... 125
4.2. Le matériel nécessaire ... 126
4.2.1. Le matériel permettant la prise d’empreinte optique de la position d’un implant 126 4.2.2. Les blocs utilisés en prothèse implantaire ... 129
4.3. Protocole clinique... 133
4.3.1. Utilisation du logiciel CEREC® 4.3 ... 134
4.3.2. Réalisation de l’empreinte optique ... 136
4.3.3. L’étape de modélisation ... 137
4.3.4. Partie laboratoire et pose de la couronne sur l’implant ... 139
5. Présentation de cas cliniques ... 144
5.1. Restauration d’un édentement partiel avec pose de 5 implants à l’aide du guide chirurgical Sicat ClassicGuide® ... 144
5.2. Restauration d’un édentement partiel avec pose de 4 implants à l’aide du guide chirurgical Sicat® Optiguide® ... 152
5.3. Restauration d’un édentement terminal avec pose de 2 implants à l’aide d’un guide chirurgical Cerec Guide® ... 158
6. Discussion ... 169
6.1. A propos de la chirurgie guidée ... 169
6.1.1. Avantages ... 170
6.1.2. Inconvénients ... 171
6.1.3. Précision des guides chirurgicaux et sources d’erreurs ... 171
6.2. A propos de la prothèse sur implant issue de la CAD/CAM ... 175
6.2.1. Le protocole CAD/CAM ... 175
6.2.2. A propos des matériaux utilisés... 178
Conclusion ... 180
Table des tableaux ... 184
Table des illustrations ... 186
17
Introduction
En observant l’outil numérique d’un point de vue très général, la France reste très en retard sur ce sujet dans de nombreux domaines clés (entreprises, éducation) par rapport à ses voisins européens, comme l’indique un rapport1 de 2010.
Si on s’intéresse au domaine de la CAD/CAM, de l’anglais « computer-aided design / computer-aided manufacturing » signifiant « dessin et fabrication assistés par ordi-nateur », les praticiens français équipés font encore office de pionniers. C’est notam-ment le cas de l’empreinte optique, bien que cette invention soit française (imaginée et développée par François Duret il y a 40 ans, nous y reviendrons).
La dentisterie numérique et son aboutissant, la CFAO (Conception et Fabrication As-sistée par Ordinateur) dentaire, sont pourtant des concepts plus que jamais d’actua-lité : on observe d’ailleurs une augmentation du nombre d’études publiées à ce sujet ces dix dernières années. Cette technologie touche la totalité des niveaux de produc-tion de prothèse dentaire, qu’elle soit fixée, implantaire ou orthodontique (Van Noort, 2012)2.
Dans la même idée apparaît la notion de « chaîne numérique » dans le domaine de l’implantologie orale et de la prothèse dentaire. Elle va pouvoir se définir comme un ensemble de maillons, constitué d’une série d’appareils, de machines et de logiciels corrélés entre eux. Ces différents maillons vont communiquer entre eux sous la forme d’échanges de fichiers informatiques, régis par des algorithmes informa-tiques. C’est ce que l’on appelle le « flux numérique ».
Dans cette thèse, nous avons choisi d’étudier les différentes solutions que propose l’entreprise allemande Sirona® qui représente, à l’heure actuelle, le système se rap-prochant plus d’une chaîne numérique globale dans le domaine de l’implantologie, même si d’autres sociétés comme 3M® ou Planmeca® s’en rapprochent très forte-ment.
18 Un aspect pratique de la discipline implantaire sera abordé dans ce mémoire : en effet, certaines solutions permettent de se passer des étapes de laboratoire, pour lais-ser la totalité des étapes se réalilais-ser au cabinet dentaire.
Après avoir établi un aperçu du passé en ce qui concerne la CFAO en dentisterie, puis avoir rappelé les différentes étapes nécessaires à toute planification prothétique pré-implantaire, nous nous attacherons donc dans un premier temps à étudier les différents options permettant d’aboutir à une chirurgie guidée proposées par Si-rona® ou par l’une de ses filiales spécialisée dans le domaine, Sicat®. Nous verrons ensuite l’étape correspondant à la pose chirurgicale de l’implant à l’aide du guide, puis celle permettant la réalisation de la prothèse sur l’implant. Une présentation de cas cliniques viendra illustrer les thématiques abordées et nous observerons, enfin, les différents avantages et inconvénients des techniques observées.
19
Partie I – Historique
20
1. Historique
1.1. Evolution de la planification implantaire
La voie de l’imagerie 3D a été initiée par le Dr FORTIN à partir des années 1990, qui s’est d’abord intéressé à la tomographie numérique en implantologie. Il a ainsi été co-fondateur de la société CadImplant® qui a notamment produit le premier logiciel d’aide à la planification implantaire3.
Dans les années 80, l’implantologie a d’abord permis d’apporter un confort aux pa-tients édentés totaux en permettant de stabiliser leurs prothèses. La position des implants était surtout dictée sur le volume osseux disponible lors de la réalisation du lambeau, et le prothésiste devait s’accommoder de ce positionnement implan-taire. Les moyens de connaître les volumes osseux, donc de prédéfinir la position des implants, étaient en fait peu nombreux.
Petit à petit, cette discipline s’est orientée vers le traitement des édentements par-tiels puis vers ceux mettant en jeu l’esthétique : à ce stade, connaître à l’avance la position des implants devenait alors primordial. Le projet implantaire, qui prenait auparavant la première place dans l’élaboration du plan de traitement, va donc pro-gressivement passer en second plan pour être détrôné par le projet prothétique. Ce dernier préfigure maintenant la future position des implants et non l’inverse.
Avant l’apparition du numérique, les praticiens s’aidaient à la fois de leur sens cli-nique (palpation des crêtes, date de l’édentement...) et de l’imagerie 2D (panora-mique, rétro-alvéolaire). Les praticiens se procuraient une succession de planches 2D tous les millimètres environ, panoramiques et sagittales, permettant ainsi de vi-sualiser les volumes osseux résiduels. Ceci était alors un premier pas vers l’implan-tologie guidée. Aujourd’hui, ces outils de visualisation en 2D sont toujours utilisés mais davantage comme clichés de “débrouillage”. Ils ont été remplacés par la radio-graphie dans les trois dimensions de l’espace, et l’utilisation de logiciels de planifi-cation implantaire desquels peuvent découler la production de guides chirurgicaux.
21 Aujourd’hui, pour certaines thérapeutiques implantaires, un cabinet dentaire a la possibilité de prendre en charge son patient entièrement en interne. Du projet pro-thétique à sa finalité, en passant par la pose des implants, le patient a la possibilité d’être suivi par le même praticien et dans les mêmes locaux. C’est le cas du système CEREC, de l’entreprise Sirona®.
1.2. Le système CEREC®
La CFAO (Conception et fabrication assistée par ordinateur) est apparue au cours des années 70 dans le monde de l’industrie afin de standardiser et simplifier les pro-cessus de fabrication. En dentisterie, le précurseur, François Duret, a commencé l’application de ce système à la dentisterie dans les années 704. En effet en 1973 il publie sa thèse de docteur en chirurgie dentaire sur “l’empreinte optique”, en paral-lèle d’un cursus à la faculté des sciences. Il est considéré aujourd’hui comme l’inven-teur de la CFAO dentaire.
Fig. 1. Le Pr. François Duret.
La CFAO se divise en 2 parties : la CAO, ou Conception Assistée par Ordinateur, et la
FAO, Fabrication Assistée par Ordinateur. Dans ces 2 termes nous retrouvons le mot
“assistée” :
La CAO correspond à un dialogue entre l’homme et la machine, elle est un outil pour diminuer le temps de travail.
22 La FAO, elle, correspond à l’unité d’usinage qui réalisera la pièce conçue par CAO. Les anglo-saxons parlent eux de processus CAD-CAM (Computer Aided Design - Computer Aided Manufactured).
La CFAO au cabinet dentaire se divise en 3 étapes :
1) Etape d’acquisition : c’est à l’aide d’une caméra intra-buccale qu’un
prati-cien va pouvoir transformer un élément (une dent, une prothèse...) en don-nées numériques. C’est ce qu’on appelle l’empreinte optique.
2) Etape de conception : grâce à un logiciel, les données numériques acquises précédemment vont pouvoir être modélisées. C’est à partir de ce modèle qu’une couronne sera conçue.
3) Etape d’usinage : à l’aide d’une usineuse miniaturisée, des fraises vont tailler
un bloc de matériau suivant les cotes prédéfinies lors des étapes précé-dentes5.
Entre 1975 et 1981, deux équipes ont contribué à développer la CFAO :François DURET fut le fondateur de la première équipe et créa la société Henson®. L’équipe française réalisa ainsi, en 1983, la première démonstration de CFAO dentaire et de la réalisation d’une “couronne en 20 minutes” en public lors des entretiens à Garan-cière. S’ensuivit la première couronne unitaire qu’il posa dans la bouche de sa femme lors du salon de l’Association Dentaire Française (ADF) en novembre 1985. Ce concept s’exporta aux états unis à la fin des années 80 et fut développé par une deuxième équipe, menée par le Docteur Schmidt (Université du Michigan).
23 En ce qui concerne le Cerec®, le tout premier prototype a vu le jour en 1980. Suc-cessivement, d’autres modèles plus évolués sont apparus, améliorant son efficacité, sa précision et son ergonomie. Quelques dates marquantes :
1980 : prototype du Cerec® ap-pelé “The Lemon” et inventé par le Professeur W. Mörman et le Doc-teur Brandestini (Fig. 2) ;
1988 : le Cerec Mark I® sera prin-cipalement utilisé pour la réalisa-tion d’inlays ;
1994 : le Cerec Mark II®, en plus des inlays, pourra réaliser des
on-lays et des facettes. De plus, la précision du joint dento-prothétique sera amé-liorée de 25% par rapport aux versions précédentes6, 7 ;
2000 : le Cerec Mark III® a réellement marqué le début de la “démocratisa-tion” de la CFAO prothétique. En effet, l’interface est plus simple et plus in-tuitive. L’unité d’usinage est, contrairement à ses prédécesseurs, séparée du centre d’acquisition. Nouveauté également, le logiciel est évolutif : via une connexion internet il est désormais possible de télécharger les nouvelles ver-sions ;
2009 : le Cerec AC et l’usineuse MCXL. Ajout du Cerec Connect® (envoi des données au laboratoire) et du système biogénérique.
2012 : Cerec Omnicam®, première caméra couleur chez Sirona.
24 Ces derniers temps, des évolutions majeures ont eu lieu dans le monde de la CFAO. De nombreux industriels ont compris l’avenir de cette technologie ainsi plusieurs types de caméra intra-buccales sont maintenant disponibles sur le marché.
Toutes les machines sont maintenant équipées d’une connexion internet : cela per-met d’envoyer les images intra-buccales, sous forme de fichiers, au laboratoire ha-bilité à recevoir et traiter ces demandes (pour le Cerec® on parlera de “Cerec Con-nect”® déjà énoncé plus haut).
La difficulté réside aujourd’hui dans la compatibilité de ces fichiers. En effet, en fonc-tion des marques de caméra, le type de fichier sera différent et pourra être pris en charge par le laboratoire uniquement si celui-ci possède la machine compatible. Ce-pendant on observe de plus en plus une volonté de normalisation des données de la part des constructeurs, comme l’explique par exemple Francois Duret dans une in-terview8 sur le site IDweblogs© publiée début décembre 2014, en considérant qu’il « est hors de question de développer une caméra avec un langage particulier » à l’heure actuelle, faisant de la lutte contre les systèmes fermés une priorité depuis quelques années, ces derniers « enfermant les dentistes à un seul type de langage » et obligeant les prothésistes à un seul type de matériel.
Fig. 3. De gauche à droite : Prototype, CEREC® 1, CEREC® 2, CEREC® 3.
25 D’autres évolutions majeures ont eu lieu ces dernières années : pour une empreinte optique, le poudrage a toujours été une étape obligatoire, souvent vécue comme contraignante par les praticiens. Depuis 2007, quelques sociétés ont mis au point des caméras optiques sans poudrage : l’iTero® (CaDent®) qui a été la pionnière du sans-poudrage, mais aussi la Trios® (3Shape®), et l'Omnicam® (Sirona®).
Quelle que soit la caméra optique Sirona® utilisée, le fichier enregistré par la ca-méra est au format .dxd. Si le laboratoire souhaite utiliser une autre plateforme, le prothésiste devra convertir le fichier en .stl en utilisant les logiciels fournis par Si-rona® : Open inLab® ou Open Apollo DI®.
On observe ces derniers temps l’apparition de plus en plus de systèmes concurrents dits "ouverts" : l'empreinte optique est au format .stl, le prothésiste peut ainsi tra-vailler avec plusieurs dentistes ayant des caméras optiques différentes.
Type de
système Système propriétaire fermé Fichier propriétaire à ouverture contrôlée STL ouvert
Caractéri-tiques
Ne peut être ouvert que sur le logiciel de même marque que le système d'empreinte optique.
Peut être ouvert sur un logiciel « ami » dispo-sant d'une licence parti-culière.
Peut être ouvert par n'importe quel logiciel.
Nom du système
CEREC® Sirona® Lava C.O.S®
Lava True Definition® Trios® 3Shape®
Carestream®, Planscan®, Cyrtina® Tableau 1 : Différents systèmes d’empreinte optique, différents formats de fichiers : fermé, ouvert et « à ouverture contrôlée »
Dans un futur proche, l’ensemble de ces améliorations nous laisse penser que la ca-méra numérique pourrait bientôt venir trouver sa place sur l’unit dentaire, à côté de la turbine et du contre-angle.
26
1.3. Les différents systèmes de prise d’empreinte optique
chez Sirona®
Schématiquement, on classe les caméras intra-orales de 3 manières différentes :
Enregistrement en couleur ou non Nécessité de poudrer ou non
Mode de capture d’images : statique (image par image) ou dynamique (filme en continu)
1.3.1.
CEREC Bluecam®
Cette caméra succède à la Redcam®. Dorénavant c’est la lumière bleue à courte longueur d’onde qui remplace les infrarouges classiques. Ce modèle nécessite un pou-drage pelliculaire des surfaces (environ 40-60 µm) avec de l’oxyde de titane (Optispray®, Sirona®). Ce poudrage est essentiel : en effet seules les surfaces mates sont enregistrées. Il faudra également veiller à écarter tout autre type de rayonnement lumineux : so-leil, scialytique, etc. Chaque prise de vue est déclenchée automatiquement lorsqu’une parfaite netteté de l’image est obtenue. Les différentes séquences enregis-trées permettront d’établir l’image finale.
Vient ensuite le temps de l’empreinte : la préparation et les dents adjacentes sont enregistrées. L’empreinte optique des dents antago-nistes est alors effectuée afin de générer l’occlusion à l’aide du logiciel : un mordu occlusal ou un balayage vestibulaire peuvent être enregistrés.
L’opérateur dispose ensuite de plusieurs solutions :
- envoyer l’empreinte directement au laboratoire grâce au Cerec Connect® ; - réaliser lui-même l’usinage de la pièce prothétique grâce à l’unité de FAO type MC XL.
27 Selon l’étendue de l’enregistrement, le temps nécessaire peut varier de 40 secondes à 2mn30 :
- Quadrant seul : 40 secondes ; - Arcade complète : 2 minutes ;
- Arcade comprenant les préparations + arcade antagoniste + rapport inter-ar-cade : 2 min 30.
1.3.2.
CEREC Omnicam®
Cette caméra est sortie récemment (2012) et présente un concept à l’opposé de la Bluecam® : la prise de l’empreinte se fait de manière continue, sans poudrage et en couleur.
Le poudrage étant très souvent vécu comme une étape contrai-gnante par les utilisateurs de caméra optique, sa suppression est donc une avancée majeure. Cependant une obligation per-siste : les surfaces doivent être parfaitement séchées et la vitre de la caméra ne doit pas être recouverte de buée. Sans ces 2 critères, l’empreinte sera difficile.
En outre, les mouvements de l’opérateur diffèrent de ceux de l’Omnicam® : l’enregistrement se fait en “zigzag” sur l’en-semble des surfaces à enregistrer, ou de manière linéaire face par face (palatine / linguale, vestibulaire, occlusale).
Le temps nécessaire est donc sensiblement plus long : environ 5 minutes.
28
1.3.3.
Comparaison des caméras Bluecam® et
Omni-cam®
CEREC Bluecam® Fig. 6 CEREC Omnicam® Fig. 7 Mode de prisede vue Photographie Film
Domaine d’utilisation
Restauration unitaire, quadrant (arcade
com-plète possible)
Restauration unitaire, quadrants, arcade complète (plus la zone à
saisir est importante, plus l’ab-sence de poudrage prévaut)
Longueur totale 206 mm 228 mm
Poids 270 g 313 g
Distance
/profondeur de champ
La caméra peut être po-sée directement sur les
dents
La caméra doit rester à distance des dents par un faible écart
(0-15mm)
Données ouvertes ? OUI OUI
Combinaison possible
avec une unité d’usinage OUI OUI
Mode « conseil aux
pa-tients » NON OUI
Scannage 3D en couleur NON OUI
Poudrage préalable OUI NON
29
CEREC Bluecam®
Fig. 6
CEREC Omnicam®
Fig. 7 Avantages - prise d’empreinte rapide, bien
que cet avantage tende à s’effa-cer au fil des mises à jour du lo-giciel actuel, au profit de l’Omni-cam®.
- pas de poudrage préalable - taille de l’outil de scannage plus réduite.
- cliché 3D en couleurs naturelles - simplicité d’utilisation
- possibilité d’étendre l’em-preinte à de plus grands seg-ments de maxillaire.
- possibilité de réaliser un film. Inconvénients - inconvénients liés au rajout
d’une phase : le poudrage préa-lable (temps, confort du patient). - un surpoudrage des zones proximales (poudrage trop im-portant) va entraîner une acqui-sition trop épaisse, et donc après usinage et essai en bouche, des points de contact trop faibles de la prothèse.
- impossibilité d’utilisation en cas d’extraction / implantation immédiate (poudrage décon-seillé sur l’alvéole fraîchement implantée.
- temps de prise d’empreinte plus long… mais amélioré au fil des mises-à-jour du logiciel CEREC®. - profondeur de champ inférieure à la Bluecam®
- l’absence de poudrage rend par-fois plus délicate l’empreinte des zones métalliques et de certaines céramiques.
- moins large, mais plus lourde que la Bluecam®.
30 Sirona® effectue régulièrement des mises-à-jour de son logiciel CEREC® pour l’af-finer. Lors de l’écriture de ces lignes, celui-ci en est à sa version 4.3 (remplaçant la version 4.2). Elle apporte de nombreuses améliorations et corrections de dysfonc-tions du logiciel : elle augmente notamment divers aspects de la phase d’acquisition avec l’Omnicam® : augmentation de la résolution et de la fidélité des couleurs du modèle virtuel, augmentation de la rapidité et de la fluidité du scannage.
A côté de l’Omnicam®, dernière-née chez Sirona®, d’autres marques ex-posent leurs propres arguments : la Trios® (3Shape) permet par exemple une prise de teinte simultanée à l’empreinte optique (Fig. X).
Fig. 8. Visualisation des teintes sur le logiciel Dental System® (3Shape®). D’autres se démarquent par leur précision : c’est le cas de la 3M True
Definition® (3M®) qui permet actuellement les empreintes les plus
précises du marché (étude comparant 4 caméras d’empreinte optiques (Nedelcu et al., 2014)9.
31
1.3.4.
L’Apollo DI®
L’Apollo DI® (Digital Impression) est la dernière production de la société Sirona® (2013) et la plus simple d’utilisation. Elle présente comme rôle principal la prise d’empreinte optique, en vue et de la communiquer au laboratoire partenaire via le Cerec Connect®. Cependant si le cabinet dentaire est équipé d’une unité d’usinage et de la Cerec AC® Bluecam® ou Omnicam®, les données peuvent être exploitées via une plateforme InLab®.
Comme nous l’avons dit son utilisation est simpli-fiée, son architecture aussi : une tour centrale, sur-plombée par un écran tactile vitré (absence de sou-ris et de clavier).
Le logiciel diffère de celui des autres caméras, il s’appelle l’Apollo DI connect® et son utilisation se restreint seulement à la prise d’empreinte optique. Son utilisation ne sera donc pas compatible avec une planification implantaire selon l’idée « CEREC meets GALILEOS », concept reliant l’usineuse CEREC® au logiciel de planification implantaire GALILEOS®, que nous allons décrire plus loin.
A la manière de la Cerec Omnicam®, la prise d’empreinte se fait en flux vidéo con-tinu. Cependant, un poudrage est nécessaire mais diffère de celui employé lors de l’utilisation de la Bluecam® : il s’agit de poudre d’oxyde de titane et de carbone, cette fois-ci répartie sommairement sur la surface et non totalement couvrante. Contrai-rement à la Bluecam®, le poudrage permet ici de créer des points de repères pour la reconstitution de l’image.
32 L’un des intérêts de l’Apollo DI® est son coût, inférieur à celui de la Bluecam® et de l’Omnicam®, augmentant l’accessibilité à l’empreinte optique via un investisse-ment moindre pour le cabinet (14 990€).
D’autres entreprises tentent à leur manière de démocratiser l’empreinte optique. C’est le cas notamment des caméras A-tron BlueScan3D® et
Ca-restream CS 3500® qui présentent une connectique usb, ce qui permet
de les connecter simplement à un ordinateur proche. On n’est plus dépen-dant d’une grosse unité d’empreinte comme sur le CEREC®, ni d’un sys-tème fermé puisque l’architecture des logiciels est ouverte, nous laissant le choix de travailler avec un plus grand nombre de laboratoires.
Fig. 11. Caméra optique Carestream CS 3500® reliée à un ordinateur portable.
33 La dernière avancée en la matière actuellement est la caméra Condor
Scan® (brevetée par le Pr. François Duret). De système ouvert (fichiers en
open .stl), elle se démarque par son prix abordablea, son ergonomie (lé-gère/faible encombrement : un peu plus grande qu’une turbine) et sa qua-lité d’image (plus fidèle à la réaqua-lité que l’Omnicam® par exemple) (Fig. 12).
Com
Fig. 12. Comparaison entre les images obtenues avec l’Omnicam® et la Condor Scan®.
a La Condor Scan® a été annoncée à un tarif avoisinant 15 000 euros (offre de lancement en 2014)
tout comme l’Apollo DI, contre environ 40 000 euros pour l’Omnicam® (Sirona®) et 35 000 euros pour la Trios® (3Shape®).
34
Partie II – La planification prothétique
35
2. La planification prothétique
2.1. Etapes générales
2.1.1.
Anamnèse
Motif de la consultation et profil psychologique
Cette première étape est essentielle car il faut avant tout bien comprendre et cerner les attentes du patient, pour répondre au mieux à ses besoins. Il faut d’abord évaluer le souhait : est-il purement fonctionnel (“je veux pouvoir manger”) ou présente-il une composante esthétique (“je veux pouvoir sourire”) ? A cette demande esthé-tique sera ajoutée la notion de faisabilité : est-ce une demande réalisable ou bien le parodonte réduit de mon patient me laisse-t-il à penser que sa demande est forte-ment irréalisable ?
Il est également important de juger de la capacité du patient à assurer sa venue à ses rendez-vous, sa capacité d’observance médicamenteuse, ainsi que, plus générale-ment, sa capacité à assurer une bonne hygiène bucco-dentaire.
Certains troubles psychologiques ne permettent pas de garantir les différents points cités précédemment (assiduité, observance médicamenteuse, contrôle de plaque). Ils sont alors considérés comme des contre-indications potentielles à la pose d’im-plants. Par exemple : certains troubles schizophréniques, les troubles de l’image corporelle, la dégénérescence sénile, mais aussi les troubles psychologiques engen-drés par la pharmacodépendance (alcool, drogues) (Addy et al., 2006)10.
Bilan médical général
La première rencontre avec le patient est l’occasion de remplir son questionnaire médical. Le patient va alors faire état de différents éléments, parmi lesquels : anté-cédents médico-chirurgicaux, antéanté-cédents familiaux, traitement médicamenteux en cours, allergies, hygiène bucco-dentaire et tabagisme. L’analyse de ces éléments doit nous permettre de déceler les contre-indications à l’utilisation de l’implant comme thérapeutique. Ces dernières peuvent être absolues ou relatives :
36
Contre-indications « absolues »
Les patients à haut risque d’endocardite infectieuse (EI) : o Antécédents d’EI,
o Prothèses valvulaires (mécaniques ou biologiques), o Cardiopathies congénitales cyanogènes (CCC). L’infarctus du myocarde récent (moins de 6 mois) ; L’AVC récent (moins de 6 mois) ;
La radiothérapie en phase active de traitement, ainsi que tout os fortement
irra-dié (dose supérieure à 50 Gy) lors d’une radiothérapie cervico-faciale ;
La chimiothérapie en phase active de traitement ;
Les biphosphonates par voie intraveineuse.
Contre-indications “relatives”
Dans le cas d’un patient présentant une contindication relative, la décision de re-courir à l’implant sera faite via une démarche réfléchie et documentée : estimation du rapport bénéfice/risque, discussion avec le ou les médecin(s) spécialiste(s), exa-mens complémentaires.
Générales :
Fort tabagisme ;
Grossesse ;
Diabète non équilibré ;
L’âge : l’âge minimum correspond à la fin de la croissance des maxillaires ; Certains troubles schizophréniques, certains troubles de l’image corporelle,
la dégénérescence sénile ;
Pharmacodépendance (toxicomanie, alcoolisme).
Locales :
Pathologies du sinus ou de ses structures environnantes (sinusite aigue avec geste invasif, infection osseuse) ;
37
Parodontopathie non traitée ;
Certaines affections dermatologiques de la cavité buccale.
Discussion
Ces contre-indications sont amenées à évoluer à mesure que des études sont réali-sées. Par exemple, en ce qui concerne le patient traité par biphosphonates par voie orale, l’AFSSAPS ne conclue actuellement pas que la prise de biphosphonates per os pour une ostéoporose soit une contre-indication absolue à l’implantologie.
En ce qui concerne l’âge minimum, il est admis qu’il soit prudent d’attendre la fin de la croissance de l’os implanté. Les implants, étant des éléments ankylosés, ne peu-vent pas suivre les développement des maxillaires et peupeu-vent donc interférer avec la position et l’éruption des dents (Bernard et al., 2004)11. L’exception admise
jusqu’alors était celle de la pose de deux à quatre implants dans le secteur symphy-saire mandibulaire pour stabiliser une prothèse amovible totale chez le patient at-teint d’oligodontie congénitale, à partir de l’âge de 6 ans. Dans le même sens, une étude publiée récemment sur des patients implantés avant l’âge de 16 ans et atteints d’oligodontie a conclu que “les implants dentaires sont une alternative viable” chez ces adolescents (Heuberer et al., 2014)12.
A contrario, pour ce qui est de l’âge maximum, il n’en existe théoriquement pas lors-que l’on s’attelle à la thérapeutilors-que implantaire. Cependant, l’association de cer-taines affections liées au vieillissement (forte résorption osseuse, ostéoporose, hy-posialie…) va constituer des freins à la pose d’implants.
Au final, “prudence”, “décision raisonnée” et “rapport bénéfice / risque favorable” doivent rester les maîtres-mots du praticien confronté à un patient présentant une contre-indication relative à la thérapeutique implantaire. Dans le cas d’un fort taba-gisme par exemple, il semble indispensable d’associer à un consentement éclairé une information quant aux différents moyens de sevrage tabagique possibles.
38
2.1.2.
Consentement libre et éclairé
Avant de commencer la thérapeutique implantaire, il est une obligation : celle de l’information préalable aux traitements implantaires. Cette dernière doit être ex-haustive, et contenir certains éléments parmi lesquels l’explication des différentes alternatives thérapeutiques possibles (l’information ne doit pas se limiter à l’option implantaire), les risques inhérents aux interventions chirurgicales, le suivi post-opératoire (ses conditions, les risques d’échec) ainsi que la maintenance et les vi-sites de contrôle. Cette information, délivrée de manière orale au cours d’un entre-tien, doit aboutir à un document écrit qui sera signé par le patient avant de commen-cer le traitement. Aucune règle n’est actuellement prévue quant à sa formulation, contrairement à l’information concernant le coût du traitement qui obéit, elle, à la règle du devis préalable (Code de Déontologie). Il est à noter que d’un point de vue légal, les informations aboutissant à la signature du devis et du consentement éclairé par le patient doivent être faites par le chirurgien-dentiste et non par l’assistant den-taire qui n’est pas un professionnel de santé.
Une charte13,14 a été éditée par le Conseil National de l’Ordre des Chirurgiens-Den-tistes (ONCD) sur le consentement éclairé. Ce n’est pas un document type à utiliser dans n’importe quelle situation : son objectif est de permettre aux professions mé-dicales de « connaître l’essentiel et comprendre quels sont les éléments nécessaires et suffisants à l’obtention du consentement éclairé du patient » (site internet de ONCD)15.
2.1.3.
Examen clinique exobuccal
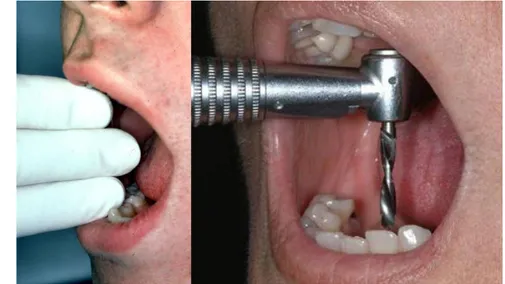
Evaluation de l’ouverture buccale
Lors de l’étape chirurgicale de pose implantaire, le praticien sera amené à travailler avec différents forets de différentes longueurs. L’évaluation de l’ouverture buccale lors de l’examen clinique (Fig. 13) va être primordiale pour vérifier qu’une bonne insertion de ces derniers soit réalisable, notamment au niveau des secteurs posté-rieurs. Cette bonne hauteur d’ouverture sera aussi déterminante pour les étapes de prise d’empreinte, d’essayage et de pose de la prothèse sur l’implant.
39 Il est communément admis qu’une ouverture buccale normale correspond à une va-leur comprise entre 40 et 60 mm. Cette fourchette doit par contre être adaptée en fonction de la marque avec laquelle le praticien travaille. Par exemple, chez Nobel® (via leur guide chirurgical NobelGuide®), l’ensemble des pièces intermédiaires (porte-implant vissé, le porte-porte-implant, tête du contre-angle) auquel on ajoute l’implant requiert une ouverture buccale d’au moins 55 mm (Fig 14) (Vaida et al., 2011)16.
Fig. 13. Contrôle de l’ouverture buccale (Photos : Vaida et al., 2011)16
Fig.14. Photographie de l’ensemble du matériel nécessaire lors d’une chirurgie implantaire guidée par le gabarit No-belGuide®. A droite, les éléments assemblés (Photos : Vaida
40 Certaines affections de l’articulation temporo-mandibulaire (ATM) peuvent contre-indiquer le traitement par l’implant. Certaines sont absolues : c’est le cas de la fa-mille des ankyloses temporo-mandibulaires (constriction permanente des mâ-choires par soudure articulaire fibreuse ou osseuse, uni ou bilatérale), avec une ou-verture buccale variant généralement entre 0 et 30 mm ; d’autres sont relatives et nécessitent d’attendre ou de traiter, c’est le cas du trismus (constriction temporaire des maxillaires lié à une contracture des muscles masticateurs).
En cas d’ouverture buccale limite, des concessions en termes de positionnement implantaire peuvent être faites en modifiant l’angulation de l’implant.
Examen de la dimension verticale (DV)
La DV correspond à la hauteur de l’étage inférieur de la face. Une diminution de cette valeur s’accompagne généralement d’une perte de l’équilibre général de la face : équilibre occlusal, articulaire, esthétique, neuromusculaire. Ne pas rétablir une bonne DV chez un patient nous expose donc à un échec thérapeutique potentiel. Pour savoir si la DV est normale ou modifiée, trois examens peuvent être réalisés : par ordre d’importance on réalisera des tests phonétiques et de déglutition, une analyse cutanée, et enfin une analyse des indices céphalométriques par une téléra-diographie de profil.
Examen du profil
La valeur de l’angle naso-labial peut nous permettre d’apprécier la résorption os-seuse chez les patients édentés. Un angle ouvert (profil concave) peut marquer une résorption du secteur antérieur maxillaire.
Examen des parties molles
Toute adénopathie ou induration des ganglions sera recherchée par un examen vi-suel et par une palpation du cou, de l’étage inférieur de la mandibule ainsi que de la région parotidienne.
41 Les muscles masticateurs, les glandes salivaires et leur ostium doivent également être appréciés à l’issue de cet examen.
2.1.4.
Examen clinique exobuccal
Examen dentaire
Un examen de l’hygiène bucco-dentaire doit être réalisé : on ne peut pas commencer une chirurgie implantaire chez un patient qui ne présente pas un contrôle de plaque rigoureux. L’anamnèse parodontale vient alors compléter l’anamnèse médicale ini-tiale. Le brossage : combien de fois par jour, avec quel type de brosse à dents ? Existe-t-il des antécédents familiaux de pathologies parodontales ?
De plus, c’est au cours de cette première approche endobuccale que l’on va s’inté-resser aux extractions à pratiquer d’emblée, c’est-à-dire aux dents non conservables quelle que soit la thérapeutique envisagée. Comme pour l’hygiène, l’idée d’un assai-nissement initial doit être privilégiée pour pouvoir envisager l’implantologie de ma-nière cohérente.
Rappelons que si le patient consulte, c’est pour remplacer une ou plusieurs dents : il peut être intéressant de classer cet édentement selon la classification de Kennedy-Applegate.
Vient enfin un examen minutieux de chacune des dents, à la recherche de lésions carieuses, fractures, restauration infiltrées, couronnes en surcontour ou inadap-tées… en fait, de manière général on recherchera tout délabrement coronaire indi-quant la réalisation d’une restauration, qu’elle soit conservatrice (composite, verre ionomère, amalgame dentaire) ou prothétique. La stabilisation de l’état endobuccal doit passer avant la thérapeutique implantaire.
Examen parodontal
Toute présence de plaque, associée ou non à du tartre et des facteurs de risque, doit appeler à une première série d’examens complémentaires. Un sondage dépistage, une radiographie panoramique, une mesure de l’indice de plaque, de l’indice gingi-val ainsi que l’indice de saignement doivent nous permettre de déceler une maladie
42 parodontale, caractérisée par la présence de poches et par une alvéolyse visible à la radiographie. Dans ce cas, d’autres examens viendront compléter l’analyse parodon-tale de notre patient : status intrabuccal, sondage des poches parodonparodon-tales, ainsi qu’un recueil des facteurs de risque locaux et généraux. La parodontopathie, classée et quantifiée, devra alors être traitée avant de commencer la thérapeutique implan-taire.
Au final, l’examen parodontal, outre son rôle dans le dépistage des maladies paro-dontales, va permettre d’évaluer l’état des tissus de soutien des dents présentes : inflammation et volume des papilles et de la gencive libre, hauteur et consistance de la gencive attachée, présence de poches et importance de l’alvéolyse près du site implantaire. En dehors des mesures de ces valeurs, différentes classifications exis-tent pour les regrouper. Par exemple, en ce qui concerne les récessions gingivales, Miller a établi une classification intéressante puisqu’il classe les récessions et donne une valeur pronostique du risque de rétraction gingivale ainsi que de la capacité de recouvrement de la récession par la chirurgie muco-gingivale. Cette dernière valeur va être capitale dans la gestion d’un cas d’implantologie intéressant le secteur anté-rieur, où l’esthétique passe notamment par la gestion des tissus mous, ces derniers étant supportés par l’os sous-jacent.
Examen occlusal
Les rapports entre les dents maxillaires et mandibulaires vont être objectivés par deux types d’examens : statique et dynamique.
L’examen statique de l’occlusion en OIM va nous informer sur la répartition des con-tacts, sur la valeur du surplomb et sur la celle du recouvrement. L’examen de rela-tion centrée (ORC) nous donnera la présence de prématurités, d’interférences tra-vaillantes et non tratra-vaillantes.
L’examen dynamique quant à lui sera réalisé par la propulsion et par les diductions à droite / gauche. Ces deux mouvements mandibulaires doivent nous donner l’as-pect du guide antérieur (compétence ? interférences ?) ainsi qu’un examen du gui-dage latéral (fonction canine, fonction groupe, partielle ou totale).
43 L’analyse de l’occlusion passe aussi par l’étude des facettes d’usure : ces dernières peuvent indiquer une parafonction (bruxisme, mauvaises habitudes). Un montage sur articulateur des modèles permettra une analyse plus précise de l’occlusion.
Examen du sourire
La ligne du sourire est dite normale, basse, ou haute (sourire “gingival”). Cet examen va être capital en cas d’édentement intéressant le secteur antérieur, et va orienter notre décision quant au choix de l’option thérapeutique, à savoir l’utilisation ou non d’artifices prothétiques (fausse gencive en résine ou en céramique). Il paraît alors intéressant de réaliser une iconographie (photographies, schémas) lors de la con-sultation.
2.1.5.
Bilan radiologique initial
La radiographie panoramique reste l’examen radiologique de choix en tant que cli-ché de débrouillage. En premier lieu, elle permet d’établir un bilan pré-implantaire primaire, en nous donnant un aperçu de la hauteur des crêtes édentées ainsi que de la proximité avec les éléments anatomiques limitants que sont les sinus maxillaires et les nerfs alvéolaires inférieurs.
En second lieu, cette radiographie va nous permettre de déceler d’éventuelles images apicales, signant des problèmes infectieux d’origine dentaire ; des traite-ments endodontiques imparfaits, analysés selon les critères de Gütman (densité, longueur, étanchéité) ; la présence de résorptions apicale, inflammatoire externe ou interne ; une augmentation de la largeur du ligament alvéolo-dentaire ; la présence de lésions carieuses. Mais cet examen panoramique reste peu précis et un bilan long-cône (ou status intrabuccal), constitué d’un ensemble de radiographies rétro-alvéo-laires, va permettre de préciser le diagnostic des lésions sus-citées.
44
2.1.6.
Définition du projet prothétique
Elle fait suite à l'analyse des données cliniques et radiographiques. L’idée, en défi-nissant le projet prothétique, est alors de déterminer le type, le nombre, le diamètre, ainsi que la position des implants.
Modèles d’étude montés sur articulateur
L’examen clinique sera complété par la prise d’empreintes d’études qui seront alors coulées. Les modèles obtenus seront ensuite montés sur articulateur pour per-mettre une analyse fine de l’occlusion (examen occlusal), une analyse des rapports inter-arcade (notamment des courbes d’occlusion), ainsi qu’une analyse précise de l’espace prothétique disponible en hauteur et dans le plan mésio-distal.
Cire ajoutée de diagnostic ou « wax-up » de diagnostic
Réalisée sur des modèles d’étude en plâtre, cette cire ajoutée va permettre de définir et de valider le projet prothétique idéal, c’est-à-dire la bonne position des dents et le respect ou la réhabilitation du schéma occlusal du patient. En secteur antérieur, la présentation de la maquette en cire va permettre au patient de valider le projet esthétique.
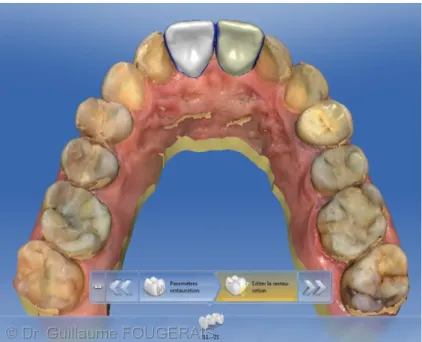
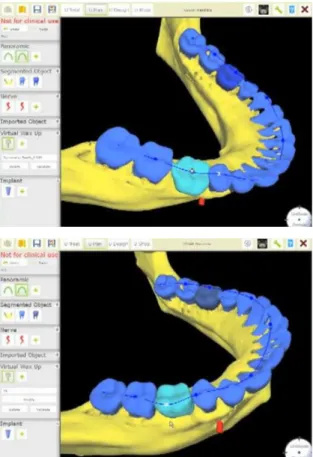
Simulation numérique (Fig. 15)
Sans passer par la cire mais à partir d’un logiciel de planification prothétique, le pra-ticien va pouvoir créer virtuellement la prothèse sur un modèle de travail numé-rique obtenu après réalisation d’une empreinte optique dans la bouche du patient.
45 Ce projet prothétique numérique créé par un premier logiciel sera ensuite intégré dans l’examen radiologique 3D, permis par un second logiciel. Cette intégration se fait par fusion de données DICOM.
Prothèse amovible provisoire de diagnostic
Dans les cas d’édentement multiples ou totaux, cette prothèse amovible va per-mettre de tester et de valider le « wax-up » imaginé par le praticien et conçu par le prothésiste. Elle nous met en condition réelle pour vérifier par exemple que la di-mension verticale d’occlusion choisie est bonne, en vérifiant la phonétique et l’es-thétique : équilibre des étages de la face, compétence labiale, support labial, sillons naso-géniens et labio-mentonnier marqués sans excès, bonne position des collets.
Fig. 15. Simulation numérique pour un cas d’édentement au niveau de 11 et 12 (cas du Dr Guillaume FOUGERAIS).
46
2.2. Le guide radiologique physique
Le guide radiologique physique s’oppose au guide radiologique numérique, créé par un logiciel (CEREC® par exemple) en fusionnant un « wax-up » virtuel à un examen radiologique 3D.
2.2.1.
Propriétés générales
Lorsqu’un « cone-beam » est réalisé pour visualiser la future position des implants, un guide chirurgical peut en découler. Ce dernier permettra la pose guidée des im-plants dont la ou les position(s) répondra(ont) au projet prothétique préalablement défini via un guide radiologique, maintenu en bouche pendant la réalisation de l'imagerie 3D. Afin de répondre aux attentes d’un tel guide, celui-ci doit présenter un cahier des charges spécifique. Un guide radiologique doit :
● être radio-opaque sans émettre d’artéfacts (bruits ou signaux parasites) : Cette radio-opacité est obtenue par incorporation de sulfate de baryum à une con-centration idéale de 20% à 30%. En effet à ce dosage il n’y a pas de signaux parasites interférant avec le guide, tous les tissus (os, gencive et dent) restent bien distinctifs (Davarpanah et al., 2011)17.
● préfigurer la future restauration prothétique :
Le praticien doit être capable de définir de manière informatique la position des im-plants en fonction du projet prothétique et des volumes osseux présents. Le guide radiologique devra donc reproduire l’enveloppe prothétique définie au préalable. L’idéal est que ce même guide coïncide avec les futurs axes implantaires, mais la réalité en est souvent différente : il faut alors savoir s’adapter avec l’os résiduel à notre disposition.
● permettre le guidage des séquences de forage implantaire :
Lors de la réalisation du guide radiologique, des puits de forages d’environ 2 mm de diamètre seront réalisés au niveau des futures couronnes qui, pour le moment, sont matérialisées par de la résine radio-opaque. Ces différents puits préfigureront l’axe
47 d’émergence des futurs implants, et apparaîtront sur le logiciel comme des cylindres dénudés de matériau radio-opaque.
● être stable :
Si on souhaite une concordance entre ce projet et la position des implants, il est pri-mordial que le guide reste stable en bouche lors de la réalisation du cone-beam (Van Assche et Al. 2007)18. Le praticien peut être amené à utiliser différents moyens pour le stabiliser : rouleaux salivaires, crochet, appui dentaire, etc.
2.2.2.
Réalisation du guide radiologique
Une fois l'indication posée d'effectuer une réhabilitation prothétique implanto-por-tée, le praticien effectue des empreintes et demande la réalisation d'un « wax-up ». Le prémontage issu des cires d’analyses validé, il en découle un guide radiologique en résine que le patient gardera en bouche pendant l'acquisition tridimensionnelle radiographique.
Les données enregistrées sont codées au format DICOM (« Digital Image for COm-munication in Medicine »), ce qui constitue le format standard pour les logiciels de radiographie numérique. Ces informations seront lues par les logiciels de planifica-tion implantaire tels que le NobelGuide®, Simplant® ou encore GALILEOS® Im-plant.
Une fois le projet informatique validé, l'ensemble pourra être envoyé au laboratoire pour l'usinage du guide chirurgical.
Un des objectifs du guide radiologique est, comme nous l'avons vu, de permettre la fabrication d'un guide chirurgical. Ce dernier est élaboré par stéréolithographie : procédé largement utilisé dans l'industrie depuis les années 80, il permet la réali-sation d'un objet aux proportions exactes définies par informatique. Or cette préci-sion peut être faussée par de nombreux facteurs :
48 Guide radiologique instable :
Deux types d'appuis peuvent être utilisés pour positionner le guide en bouche :
mu-queux ou dentaire. La dent est un tissu dur indéformable, et ses contre-dépouilles
sont exploitables pour augmenter la rétention. A l'opposé, une muqueuse est un tissu mou élastique, donc imprécis, d'autant plus s’il existe des crêtes flottantes : selon Daas et al. (2008)19 il est indispensable de réaliser une clé d'occlusion rigide pour stabiliser en bouche un guide à appui muqueux.
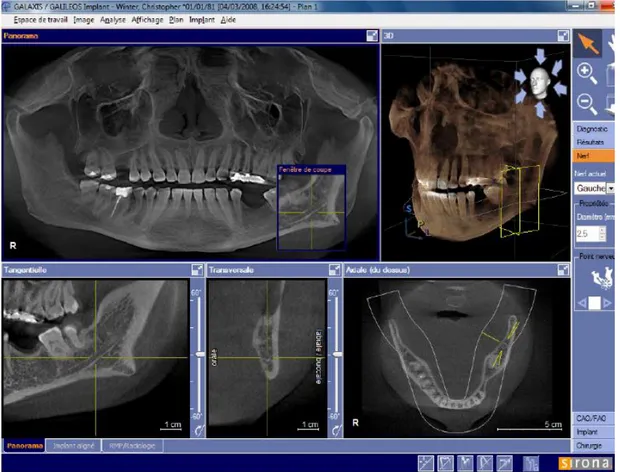
Imprécisions propres à la radiographie 3D :
Un praticien a le choix entre 2 types d'examens radiographiques : scanner ou cone-beam. Selon Loubele et al. (2005)20, le cone-beam présente une précision inférieure à 0,35mm, cela peut aller jusqu'à 0,22mm (Moore, 2005)21.
Le scanner est lui plus irradiant et onéreux. De ce fait, de moins en moins de den-tistes y ont recours alors que son niveau de précision est plus grand selon Liang et al. (2009)22 (jusqu'à 0,137mm).
Une étude analysant la précision des mesures via cone-beam dans un bilan pré-im-plantaire dans la région postérieure maxillaire n’a pas montré de différence signifi-cative avec les valeurs réelles mesurées in vivo (Veyre-Goulet et al., 2008)23.
Aujourd’hui la société Sirona® propose au chirurgien-dentiste de réaliser lui-même la prise en charge d'un patient du début à la fin, du projet prothétique à la couronne implanto-portée, entièrement au cabinet d'omnipratique. C’est la méthode dite
“chairside” : elle comprend notamment le guide radiologique, l’utilisation du
cone-beam (GALILEOS® ou ORTHOPHOS® XG 3D), le recours au guide chirurgical (usiné par le CEREC®, ou commandé à l’entreprise Sicat®), l’utilisation de l’usineuse… Ces différents points seront étudiés en détail par la suite.
2.2.2.1. Cerec Guide®
La première étape est commune à tout autre type de chirurgie implantaire : anam-nèse, diagnostic, plan de traitement, « wax-up » et discussion avec le patient. Une fois cette étape effectuée, le praticien prend une empreinte de l’arcade concernée, le
49 modèle coulé servira à la réalisation du guide chirurgical « chairside » à l’aide de l’usineuse : le Cerec guide®.
Sur ce modèle, on va d’abord veiller à ce qu’aucune contre-dépouille ne vienne per-turber la mise en place et le retrait du guide. On comble ces dernières à l’aide d’une résine photopolymérisable, par exemple le l’Opaldam® (Ultradent), le LC Block-Out Resin® (Ultradent) ou encore le Notre Dam® (Elsodent) (Fig. 16.a et b).
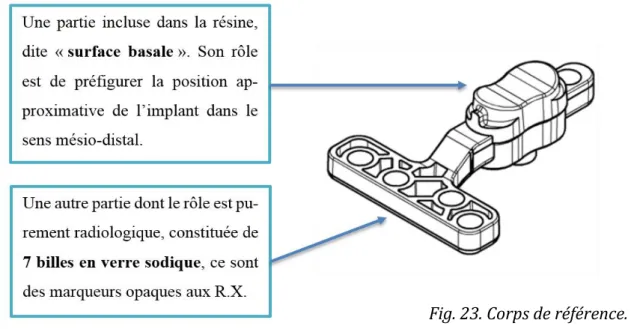
On place alors de la pâte thermoformable dans de l’eau bouillante, pour la rendre molle et pliable (Fig. 16.c). Au bout de 2 à 3 minutes, le thermoplastique est totale-ment fondu et transparent. Il peut être sorti de l’eau chaude à l’aide d’un instrutotale-ment, puis manipulé et modelé pour ensuite le déposer sur la zone édentée (Fig. 16.d). Avant sa solidification complète, un « corps de référence » (ou « reference body »), est inséré dans le matériau, approximativement à la future place des implants (Fig. 16.e et f), le plus apicalement possible.
Fig. 16.a. Comblement des contre-dépouilles à l’aide d’une résine pho-topolymérisable.
Fig. 16.b. Fin de comblement et photo-polymérisation.