La revascularisation myocardique chirurgicale
dans les sténoses du tronc commun coronaire
gauche expérience de l'hôpital militaire
d'instruction Mohammed v a propos de 80 cas /
OUZAA Mohamed Reda
TABLE DES MATIERES
DEDICACES
Pages
PLAN DE LA THESE
...1ABREVIATIONS
………..……4INTRODUCTION
...5PREMIERE PARTIE : ETUDE FONDAMENTALE
...71. RAPPEL ANATOMIQUE DE LA VASCULARISATION CORONAIRE...8
1.1. TRONC CORONAIRE GAUCHE...8
1.2. ARTERE CORONAIRE DROITE...11
2. SYSTEMATISATION DE LA VASCULARISATION ARTERIELLE DU CŒUR...12
3. VARIATIONS ANATOMIQUES DU TRONC COMMUN...15
3.1. ABSENCE DE TRONC COMMUN...15
3.2. ANOMALIES D’ORIGINE DU TRONC COMMUN...15
4. DEFINITION DE LA STENOSE DU TRONC COMMUN GAUCHE...16
5.1. L’ATHEROSCLEROSE...16
5.2. LES AUTRES CAUSES NON ATHEROSCLEREUSES...17
6. EPIDEMIOLOGIES……….21
7. DIAGNOSTIC POSITIF………24
7.1. CLINIQUE………...………24
7.2. ENREGISTREMENT ELECTROCARDIOGRAPHIE DE REPOS...26
7.3. RADIOGRAPHIE PULMONAIRE...26 7.4. ECHOCARDIOGRAPHIE...26 7.4.1. Echocardiographie transthoracique ……….………26 7.4.2. Echocardiographie transoesophagienne………27 7.4.3. Echocardiographie de stresse………..27 7.5. EPREUVE D’EFFORT……….………28 7.6. SCINTIGRAPHIE MYOCARDIQUE………28 7.7. CORONAROGRAPHIE………29 7.7.1. Techniques………29 7.7.2. Résultats………..31 7.8. AUTRES EXAMENS………..………..33 7.8.1. Tomodensitométrie multibarettes……….33 7.8.2. Ultrasons endocoronaires……….34
7.8.3. Imagerie par résonance magnétique………..35
8. TRAITEMENT DES STENOSES DU TRONC COMMUN………..…...36
8.2. METHODES DE REVASCULARISATION………..38
8.2.1. ANGIOPLASTIE TRANSLUMINALE PERCUTANEE………..38
8.2.2. LE PONTAGE AORTO-CORONAIRE………..43
8.2.2.1. Le bilan préopératoire : ………..………43
8.2.2.2. Préparation à la chirurgie………..44
8.2.2.3. Au bloc opératoire………..45
8.2.2.4. Installation en position chirurgicale du patient………46
8.2.2.5. Prélèvement et préparation des greffons………47
8.2.2.6. Technique d’économie sanguine………51
8.2.2.7. Installation et démarrage de CEC………..………52
8.2.2.8. Techniques d’anastomoses coronaires……….53
8.2.2.9. Sortie de CEC et Assistance pharmacologique………..57
8.2.2.10. Assistance circulatoire………59
8.2.2.11. Autres techniques chirurgicales………...………..61
8.2.2.12. Chirurgie coronaire mini-invasive………..62
8.2.2.13. Suites opératoires………..………65
DEUXIEME PARTIE : MATERIEL ET METHODES
………...………...71RESULTATS
………..……….92DISCUSSION
……….………101CONCLUSION
………..………125BIBLIOGRAPHIE
………..130Abréviations :
ACD : Artère coronaire droite.
ATC : Angioplastie transluminale coronaire. BCPIA : Ballon de contre pulsion intra-aortique. CASS : Coronary Artery Surgery Study.
CEC : Circulation extracorporelle. CX : Artère circonflexe.
Dg : Artère diagonale. ECG : Electrocardiogramme.
ETO : Echocardiographie Trans-oesophagienne. FEVG : Fraction d’éjection du ventricule gauche. IDM : Infarctus du myocarde.
IRM : Imagerie par résonance magnétique. IVA : Artère interventriculaire antérieure. IVP : Artère interventriculaire postérieur. MG : Artère marginale.
NFS : Numération formule sanguine. NYHA : New York Heart Association. OAD : Oblique antérieure droite. OAG : Oblique antérieure gauche. PAC : Pontage aorto-coronaire.
TABC : Tronc artériel brachio-céphalique. TCG : Tronc commun gauche.
TDM : Tomodensitométrie. VD : Ventricule droit. VG : Ventricule gauche.
Les sténoses du tronc commun gauche (TCG) sont des sténoses fixes réduisant de 50% ou plus le diamètre du vaisseau. Elles sont d’étiologie le plus souvent athéromateuse. Elles forment un sous groupe distinct des autres atteintes coronariennes par leur caractère peu fréquent, rarement isolé, leur gravité, ainsi que par leur traitement.
Aucun critère épidémiologique et/ou clinique n’est spécifiquement prédictif de l’atteinte du tronc commun gauche. De même que les explorations non invasives comportent un risque d’erreur non négligeable. L'artériographie non sélective des artères coronaires est le «gold standard» pour le diagnostic de lésions significatives du tronc commun gauche.
Le traitement chirurgical est admis depuis de nombreuses années comme le traitement de référence dans ce type de lésions, apportant une amélioration de l’espérance de vie et de la symptomatologie fonctionnelle.
Nous rapportons l’expérience du service de chirurgie cardiovasculaire de l’HMIM V de par une étude rétrospective concernant 80 patients ayant tous bénéficié d’une revascularisation myocardique chirurgicale par pontage aorto-coronaire pour sténose du TCG.
Notre travail a pour but de déterminer l’intérêt des pontages coronaires dans cette pathologie, la morbi-mortalité hospitalière de ces patients opérés et identifier les facteurs cliniques et opératoires associés à cette morbi-mortalité.
PREMIERE PARTIE :
ÉTUDE
1. RAPPEL ANATOMIQUE DE LA VASCULARISATION CORONAIRE
La vascularisation artérielle du cœur est sous la dépendance des deux artères coronaires gauche et droite, issues de l’aorte ascendante juste au-dessus des valvules semi-lunaires correspondantes.
Leurs troncs principaux cheminent dans les sillons coronaires atrioventriculaires droit et gauche et inter-ventriculaires antérieur et postérieur.
Le tronc commun de l’artère coronaire gauche est le plus important des deux artères coronaires : cette artère vascularise une partie importante du ventricule gauche (VG), son atteinte peut avoir des conséquences dramatiques sur la survie des patients, ainsi que sur la fonction systolique de leur VG.
1.1. TRONC CORONAIRE GAUCHE : 1.1.1. Origine :
Il naît du flanc antéro-gauche de l’aorte ascendante au niveau du sinus de Valsalva antéro-gauche (environ 0,5 cm au dessus des bords libres des sigmoïdes aortiques en systole).
Avec l’âge et certaines pathologies qui affectent l’aorte, il se produit une élévation et une ascension de la racine de l’aorte de telle sorte que le sinus coronaire gauche paraît plus haut que le sinus coronaire droit, il en résulte une origine et un trajet de niveau plus haut (1).
1.1.2. Trajet :
Le tronc chemine derrière l’artère pulmonaire en se moulant à son flanc postérieur.
Sa longueur plus ou moins grande détermine l’angle de division de ses deux branches terminales.
Il peut être subdivisé en trois parties : l’ostium (tronc proximal), le tronc moyen et le tronc distal.
Schéma. 1: Représentation schématique des artères coronaires.
1. Coronaire droite moyenne ; 2. marginale droite ; 3. rétroventriculaire (diaphragmatique, postérolatérale droite) ; 4. interventriculaire postérieure ; 5. tronc commun gauche; 6.
interventriculaire antérieure proximale ; 7. première marginale ; 8. interventriculaire antérieure moyenne ; 9. circonflexe distale ; 10. deuxième marginale ; 11. postérolatérale gauche.
EMC ; Traitement chirurgical de l’insuffisance coronaire, 11-030-D-60.
1.1.2.1. L’ostium du tronc commun :
Il est situé dans l’épaisseur de la paroi aortique (2 à 4 mm d’épaisseur), ce qui explique que les processus pathologiques qui affectent l’aorte peuvent
affecter l’ostium gauche (aortite syphilitique, Takayashu, pathologie rhumatoïde, aortite post radique, valvulopathies aortiques…).
Sur le plan histologique (1), l’ostium du tronc coronaire gauche est
pauvre en adventice, et riche en muscle lisse et en tissu élastique. Il est entouré perpendiculairement à son grand axe et de façon circulaire par les cellules musculaires lisses aortiques.
La quantité de tissu élastique diminue en distalité.
1.1.2.2. Le tronc proprement dit ou partie moyenne :
Il possède une longueur variable, habituellement entre 10 et 30 mm. Il existe cependant des troncs dits « courts » (<8mm), et des troncs « longs » pouvant atteindre 40 à 60 mm.
Chez l’homme, le diamètre du tronc normal est de 4,5±0,5mm, et chez la femme, à surface corporelle égale, il est légèrement plus petit à 3,9±0,4 mm.
Il est diminué chez les patients porteurs de cardiomyopathie dilatée ou d’une hypertrophie du ventricule gauche.
Son trajet se fait habituellement à gauche, en haut et un peu en avant, mais il peut être altéré par l’orientation de la rotation de l’aorte.
Sur tout son trajet, le TCG est recouvert par de la graisse et par l’épicarde excepté à son origine où il est disposé sous l’épicarde. A sa terminaison, il est en plus recouvert par l’auricule gauche (2).
1.1.2.3. La portion distale :
Elle donne par bifurcation naissance à deux branches : l’artère interventriculaire antérieur (IVA) et l’artère circonflexe (CX) ; parfois trois branches (30% des cas) ou plus (2% des cas), avec une ou plusieurs bissectrices.
1.1.3. Branches terminales:
La terminaison du tronc commun se fait par division en deux branches :
1.1.3.1. Branche interventriculaire antérieure :
Elle fournit :
• Des artères ventriculaires droites courtes et fines ; • Des artères septales antérieures ;
• Des artères diagonales.
1.1.3.2. Branche circonflexe. 1.2. ARTERE CORONAIRE DROITE :
1.2.1. Origine :
Artère coronaire droite naît du flanc antéro-droit de la portion initiale de l’aorte ascendante au niveau du sinus de Valsalva antéro-droit ou sinus coronaire droit. Depuis son origine et sur 3 à 4 mm, elle a un aspect en entonnoir par diminution de calibre jusqu’à atteindre 4 à 5 mm de diamètre.
1.2.2. Trajet :
L’artère présente trois segments :
• Le premier est court, dirigé en avant et légèrement en haut, et amène l’artère de son origine aortique au sillon coronaire droit antérieur ;
• Le deuxième segment est vertical ;
• Le troisième segment suit le sillon coronaire droit inférieur et l’amène au voisinage plus ou moins immédiat de la croix des sillons.
Ces trois segments sont séparés par deux coudes, l’un supérieur, l’autre inférieur. Ainsi, l’artère coronaire droite a un aspect coronarographique en cadre ou en C plus ou moins régulier.
1.2.3. Branches collatérales :
Elle présente deux types de branches :
• Des branches ascendantes ou atriales dont la plus importante est l’artère
atriale droite supérieure qui fournit la vascularisation du noeud sinoatrial ;
• Des branches descendantes ou ventriculaires droites que l’on distingue en : o artères ventriculaires droites antérieures,
o artère marginale ou du bord droit,
o artères ventriculaires droites inférieures.
1.2.4. Branches terminales :
Elle se termine en :
• Tronc rétroventriculaire gauche inférieur (ou branche rétroventriculaire postérieure),
• Artère interventriculaire inférieure (ou branche interventriculaire postérieure).
2. SYSTEMATISATION DE LA VASCULARISATION ARTERIELLE DU CŒUR :
Pratiquement aucun territoire cardiaque ne reçoit une vascularisation homogène de type défini ; il y a cependant des zones préférentielles pour tel ou tel système coronaire où les artères ont un aspect caractéristique.
Les branches destinées aux cavités droites sont grêles et superficielles et s’épuisent rapidement. Les branches destinées au ventricule gauche, quelle que soit leur origine, sont plus volumineuses et donnent des collatérales qui s’enfoncent dans l’épaisseur du myocarde dans lequel elles se ramifient jusqu’à l’endocarde par une arborisation très riche et fine.
Si on considère la distribution des artères à la surface du coeur, on constate qu’il y a un balancement entre le développement du système coronaire gauche et du système coronaire droit.
Schéma. 2: Dominance coronaire. A. Réseau équilibré.
B. Dominance gauche
C. Dominance droite. IVA : artère interventriculaire antérieure. CD : artère coronaire droite. Cx : artère circonflexe.
EMC, Anatomie du cœur 11-001-A-10
On peut observer trois possibilités (Schéma 2):
• Réseau coronaire équilibré : l’artère coronaire droite vascularise la face inférieure du ventricule gauche par une ou deux artères ventriculaires gauches inférieures issues du tronc rétroventriculaire postérieur gauche, tandis que la face latérale du
ventricule gauche est vascularisée par une ou deux artères latérales issues de l’artère circonflexe ;
• Réseau coronaire gauche dominant : l’artère circonflexe vascularise une partie de la face inférieure du ventricule gauche, voire la totalité ; il devient alors exclusif et peut dans ce cas fournir l’artère interventriculaire postérieure (inférieure);
• Réseau coronaire droit dominant (dans 85% des cas) : l’artère rétroventriculaire postérieure, branche de division de l’artère coronaire droite, vascularise une partie de la face latérale du coeur ou sa totalité.
En fonction du mode de distribution le plus fréquent des artères, on peut déterminer une limite moyenne entre les deux territoires (Schéma 3). La limite au niveau atrial passe à gauche du septum interatrial. L’artère coronaire droite vascularise donc non seulement l’atrium droit mais aussi le septum interatrial et une partie de l’atrium gauche.
Au niveau des ventricules, sur la face antérieure du coeur, la ligne de séparation des deux territoires part du milieu de l’infundibulum pulmonaire pour devenir parallèle au sillon interventriculaire antérieur, à 1 cm à droite de celui-ci; puis elle contourne le bord droit du coeur pour aborder la face inférieure où cette ligne va rejoindre la partie moyenne du sillon coronaire gauche inférieur.
La vascularisation du septum interventriculaire est donc double, issue du système coronaire gauche et du système coronaire droit ; le tiers apical du septum est entièrement vascularisé par la coronaire gauche. Dans les deux tiers basaux, l’artère coronaire gauche irrigue les deux tiers craniaux (artères septales antérieures) ; l’artère coronaire droite irrigue le tiers basal (artères septales inférieures).
Schéma 3: Territoires coronaires des infarctus du myocarde. A. Territoire de l’artère interventriculaire antérieure (infarctus antéro-septo-apical). B. Territoire de l’artère coronaire droite (CD) (infarctus inférieur).
C. Territoires des artères circonflexe (Cx) et droite (infarctus latéral et inférieur avec extension septale). SIV : septum interventriculaire.
EMC, Anatomie du cœur 11-001-A-10.
3. VARIATIONS ANATOMIQUES DU TRONC COMMUN :
3.1. ABSENCE DE TRONC COMMUN:
Sa fréquence est estimée à 0,4%. Il existe deux catégories d’absence du TCG : L’IVA et la circonflexe naissent séparément avec deux ostia au niveau du sinus coronaire gauche : celle-ci est la plus commune des anomalies congénitales de la circulation coronaire (3,4).
Naissance de ces deux vaisseaux ou de l’un des deux à partir d’un autre vaisseau coronaire (artère coronaire droite) ou à partir du sinus droit de Valsalva : elle représente en terme de fréquence la 2ème anomalie congénitale de la circulation coronaire (4).
3.2. ANOMALIES D’ORIGINE DU TRONC COMMUN : 3.2.1. A PARTIR DE L’AORTE :
Le tronc commun peut prendre naissance à partir du sinus coronaire droit (en cas de passage entre l’aorte et l’artère pulmonaire il existe une possibilité de cisaillement
de cette coronaire par les deux gros tronc exposant à un risque de mort subite), ou à partir du sinus postérieur de Valsalva (5, 6,7).
Le tronc commun peut également avoir une origine haute au niveau de l’aorte
ascendante « HIGH TAKE OFF » avec une fréquence de 0,013% (4).
Enfin, on peut noter la présence d’artères coronaires uniques avec un seul ostium notamment dans le cadre des cardiopathies congénitales.
3.2.2. A PARTIR DE L’ARTERE PULMONAIRE :
Cette anomalie a un retentissement dans les premiers mois de la vie. Le TCG prend naissance à partir de l’artère pulmonaire, avec développement possible d’une circulation collatérale à partir de l’artère coronaire droite (pour suppléer celle du réseau gauche qui est insuffisante).
4. DEFINITION DE LA STENOSE DU TRONC COMMUN GAUCHE :
Une sténose artérielle se définie par une réduction significative de la lumière artérielle. Le diagnostic de sténose significative du TCG est porté quand cette réduction est supérieure ou égale à 50% ; elle doit être supérieur ou égale à 70% pour les autres artères coronaires (8, 9, 10).
5. ETIOLOGIES DES STENOSES DU TRONC COMMUN GAUCHE :
Les causes d’obstruction du tronc commun sont multiples, mais l’athérosclérose est de loin la cause la plus commune, de ce fait il convient de distinguer l’étiologie athéroscléreuse d’une part, et les causes non athéroscléreuses d’autres part.
5.1. L’ATHEROSCLEROSE :
La plaque d’athérosclérose peut être le siège de calcifications témoignant de
l’ancienneté du processus athéromateux, et dont la quantification est utile pour le choix de la technique de revascularisation.
Par ailleurs, l’atteinte du tronc commun par le processus athéroscléreux est rarement isolée ou associé à une atteinte monotronculaire, dans ce cas elle touche avec prédilection l’ostium coronaire. Elle s’associe majoritairement à des atteintes pluritronculaires (bitronculaires ou tritronculaires) ; l’atteinte associée de la coronaire droite est relativement fréquente et représente un facteur de mauvais pronostic d’où la notion de tronc commun protégé qui se définit comme une sténose du tronc commun avec au moins une de ses branches distales protégée par un pontage fonctionnel ou par d’excellentes collatérales permettant d’assurer un flux coronaire satisfaisant en aval de l’obstacle (11).
5.2. LES AUTRES CAUSES NON ATHEROSCLEREUSES :
Elles donnent volontiers des lésions ostiales, et sont le plus souvent associées à des pathologies intéressant la paroi aortique.
5.2.1. LES AORTITES :
Toute pathologie systémique avec processus inflammatoire intéressant l’aorte peut être à l’origine d’une obstruction des ostia coronaires gauche ou droit ou les deux (12) :
L’aortite syphilitique est devenue de moins en moins fréquente, néanmoins 20% des aortites syphilitiques s’accompagnent d’une obstruction de l’ostium coronaire.
L’obstruction ostiale du tronc commun à été rarement rapportée chez les patients ayant une aortite en rapport avec une polyarthrite rhumatoïde (13) ou une
maladie de Takayashu (14).
L’aortite radique (15,16) est rare, puisqu’on ne l’observe que chez 0,1 à 3%
(47% ont moins de 35 ans), assez souvent chez la femme (72%), faisant suite à une irradiation médiastinale ou cervicale pour les pathologies malignes et l’indication la plus fréquente étant la maladie de Hodgkin (72%).
Les lésions sont de siége ostial et peuvent intéresser l’ostium coronaire droit ou gauche ou les deux, elles sont en général serrées et souvent isolées, le reste du vaisseau étant indemne de lésions. Sur le plan histologique, on retrouve un épaississement fibreux de la média sans lésion de l’intima.
Elle survient en moyenne dans un délai de 5 à 16 ans après la radiothérapie.
5.2.2. LES VALVULOPATHIES AORTIQUES :
Par un embole calcique à partir d’une valve aortique calcifiée ou exceptionnellement par calcification obstruant l’ostium coronaire gauche.
5.2.3. LA CHIRURGIE CARDIAQUE DE REMPLACEMENT VALVULAIRE : (17,18)
Une obstruction du tronc commun peut se voir dans les situations suivantes : Une obstruction ostiale accélérée après remplacement valvulaire aortique, se voyait particulièrement après mise en place de prothèses à bille, elle est attribuée à un effet de jet résultant de la turbulence du flux dirigé vers l’un ou les deux ostia coronaires.
Un mauvais positionnement d’une prothèse porcine ou une prothèse trop large peut obstruer l’ostium coronaire.
Un embol calcique après remplacent d’une valve aortique calcifiée, ou fragment de valve aortique ou mitrale après chirurgie de remplacement valvulaire.
5.2.4. LES ARTERITES INFLAMMATOIRES :
L’artérite intéressant les vaisseaux coronaires peut être localisée au système coronaire ou peut faire partie d’une atteinte artérielle disséminée dans le cadre d’une
panartérite noueuse (19,20) ou d’un lupus érythémateux disséminé (21).
Les lésions tendent à causer une nécrose du mur vasculaire et la thrombose, la survenue d’anévrysme est possible.
5.2.5. L’HYPERPLASIE FIBROMUSCULAIRE : (22,23)
Elle intéresse plus couramment les jeunes femmes, et est habituellement localisée aux artères rénales : les patients présentant une obstruction similaire des vaisseaux coronaires sont rares.
5.2.6. L’EMBOLIE DU TCG :
Elle peut être d’origine bactérienne ou fongique au cours des endocardites ou cruorique au cours des troubles de rythme telle la fibrillation auriculaire (24).
Certaines pathologies cardiaques sont plus fréquemment associées avec l’embolie coronaire, il s’agit de la cardiomyopathie dilatée, l’anévrysme du ventricule
gauche, les valves prothétiques, le myxome de l’oreillette gauche. L’embolie paradoxale
5.2.7. LES DISSECTIONS DU TCG : (25)
Elles peuvent être rarement secondaire à une dissection de l’aorte avec un hématome intra mural qui s’étend aux vaisseaux coronaires.
Il peut également s’agir d’une dissection primitive du tronc : dans ce cas, elle est le plus souvent iatrogène au cours d’une coronarographie sélective, d’une angioplastie ou provoquée au moment de la canulation lors d’une chirurgie cardiaque à cœur ouvert.
La dissection spontanée du tronc commun est exceptionnelle, et est le plus souvent responsable de mort subite. Elle survient chez les sujets relativement jeune avec une prédominance féminine constante, notamment dans la période du post-partum (des modifications de la paroi artérielle attribuées aux perturbations hormonales et hémodynamiques de la grossesse ont été décrites). Quand elle survient en dehors du post partum, une hypertension artérielle, un tabagisme ou un diabète sont fréquemment retrouvés.
5.2.8. LE VASOSPASME DU TCG :
Seuls quelques cas de spasme spontané au niveau du tronc commun ont été publiés (26).
Les femmes sont plus exposées ; ce phénomène vasoconstricteur survient en général sur des artères peu ou pas athéromateuses. La coronarographie avec injection de dérivés nitrés qui confirme le caractère fonctionnel de la sténose. L’évolution est généralement favorable sous traitement médical associant des inhibiteurs calciques et des antiagrégants plaquettaires
5.2.9. UNE THROMBOSE, OU UNE OBSTRUCTION TUMORALE DU TCG : (27)
Peut comprimer les vaisseaux coronaires et provoquer une ischémie myocardique.
5.2.11. LES CAUSES CONGENITALES :
L’hyperplasie, la sténose ou encore l’atrésie du tronc commun (28).
5.2.12. LES STENOSES OSTIALES IDIOPATHIQUES DU SUJET JEUNE :
0,1 à 1% des coronarographies.
5.2.13. LES CAUSES IATROGENES :
Enfin, lors d’un cathétérisme cardiaque.
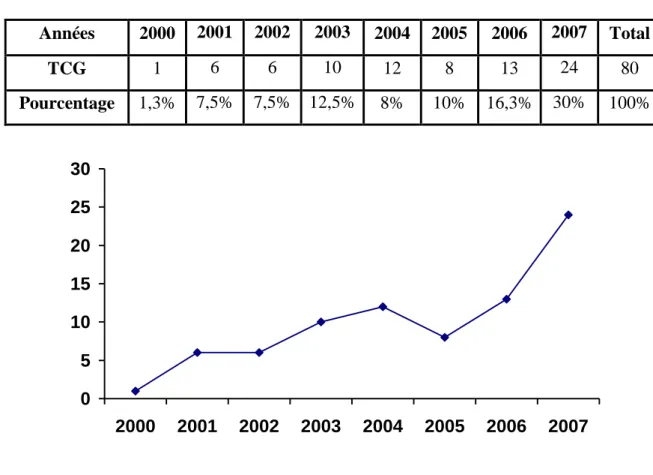
6. EPIDEMIOLOGIES :
6.1. INCIDENCE :
L’incidence de la sténose du TCG varie en fonction du nombre de coronarographies des séries étudiées, elle est en moyenne de 5% (10,29). L’incidence relativement élevée de cette pathologie s’explique par la multiplication des examens coronarographiques au sein d’une population de plus en plus âgée.
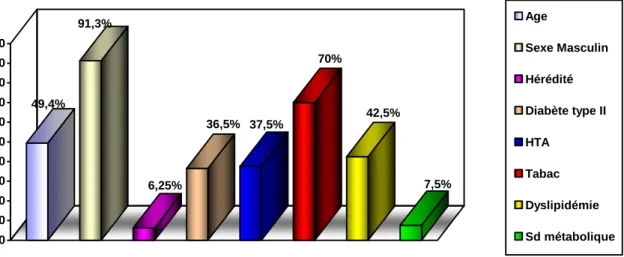
6.2. FACTEURS DE RISQUES CARDIOVASCULAIRES :
L’atteinte du tronc commun répond aux mêmes facteurs de risque que pour toute coronaropathie.
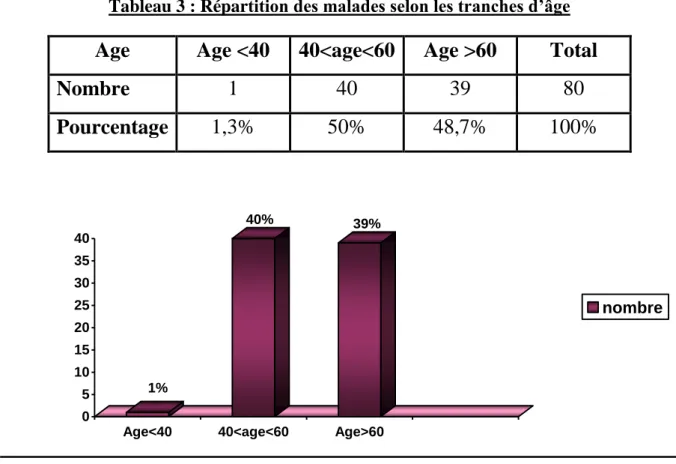
6.2.1. AGE:
L’age moyen varie autour de 58 ans (10), il semble qu’une évolution soit
commun gauche est rare chez les patients âgés de moins de 40 ans, tandis qu’elle est décelée dans 10,9% chez les patients de plus de 60 ans.
6.2.2. SEXE:
Il existe une nette prédominance masculine (3). En cas d’atteinte isolée du tronc commun, la répartition semble significativement différente, avec une atteinte préférentielle des femmes.
6.2.3. HEREDITE: (30)
L’hérédité cardiovasculaire doit être examinée avec précaution. L’observation clinique courante mentionne assez fréquemment des familles de coronariens et l’on peut considérer qu’un sujet dont l’un des parents ou des collatéraux ont présenté, avant l’âge de 50 ans, des signes d’ischémie myocardique a plus de risque qu’un autre sujet de faire un accident coronarien, cependant aucun élément génétique n’a été retrouvé.
6.2.4. DIABETE:
Facteur de risque important, le diabétique fait plus fréquemment et plus précocement l’athérosclérose coronarienne qu’un sujet non diabétique (30,32).
Les lésions coronaires du diabétique sont habituellement plus diffuses et plus longues.
6.2.5. HYPERTENSION ARTERIELLE:
Facteur de risque classique de l’athérosclérose. L’association de l’HTA avec les accidents artériels cérébraux ischémiques est plus étroite qu’avec la maladie coronaire.
Diverses études ont ressuscité récemment le rôle de l’HTA dans la genèse de l’athérosclérose coronarienne.
Pour l'athérosclérose coronarienne, le tabagisme intervient surtout en liaison avec l'hypercholestérolémie et l'HTA ; sa présence multiplie par 2 l'influence des autres facteurs de risque, dont l'association aboutit à une multiplication exponentielle des accidents (34).
6.2.7. DYSLIPIDEMIE : (31)
Toutes les études s’accordent à démontrer l’importance des perturbations lipidiques au cours de l’athérosclérose coronarienne.
6.2.8. SYNDROME METABOLIQUE: (35)
Le syndrome métabolique est caractérisé par un agrégat de désordres métaboliques dont la coexistence chez un même individu peut correspondre d’une part à un mécanisme physiopathologique commun et d’autre part expose le sujet à un risque accru de survenue ultérieure de diabète de type 2 et de maladies cardiovasculaires.
De nombreuses études (37) ont montré que les sujets atteints du syndrome métabolique présentent un risque accru de développer une maladie cardiovasculaire. Le risque accru de morbidité et de mortalité cardiovasculaire se situe dans un éventail de 1,5 à 4,6 %.
6.2.9. AUTRES:
Indépendamment de l’épidémiologie, d’autres agressions ont été mises en cause dans l’étiologie de l’athérosclérose en partant de constats expérimentaux ou anatomopathologiques.
Des désordres métaboliques tels l’élévation de l’homocysteinémie, qui est directement toxique pour l’endothélium.
Des perturbations immunitaires et certaines infections qui contribuent à l’inflammation athéroscléreuse.
Une hypo-oestrogénie d'origine hypothalamique chez les femmes pré ménopausiques est associée à un risque relatif de 7,4% de développer une maladie coronaire (38).
Le traitement substitutif de la ménopause augmente le risque de survenue d’événements cardiovasculaires et thromboemboliques chez les femmes ménopausées avec ou sans antécédent cardiovasculaire.
Certains marqueurs biologiques de l'inflammation, en particulier la CRP haute sensibilité et l'interleukine 6 ont été associés à une augmentation du risque relatif de faire un événement vasculaire d’infarctus du myocarde. Leur accessibilité (standardisation des méthodes de mesures, reproductibilité, faible coût) en rendra possible l'utilisation ultérieure en pratique courante (39).
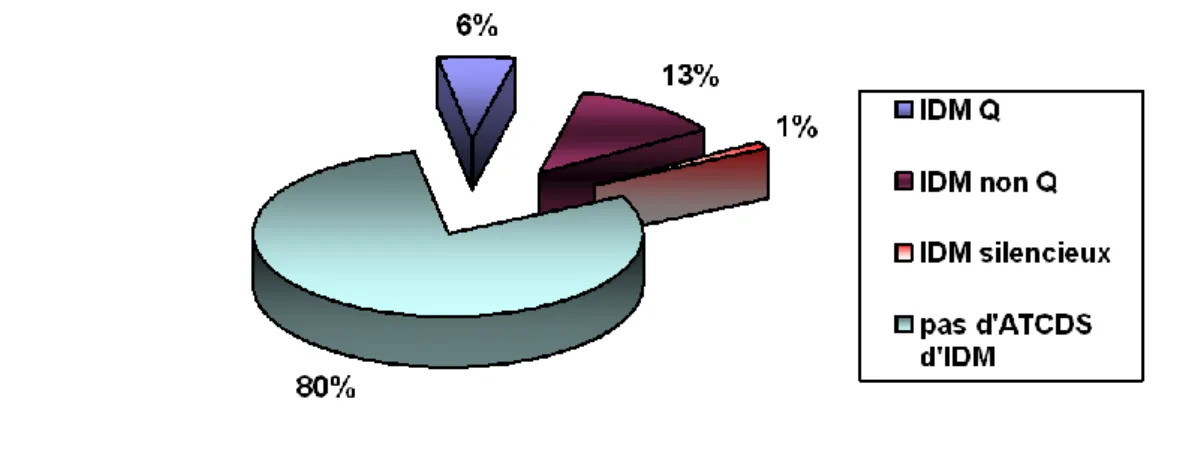
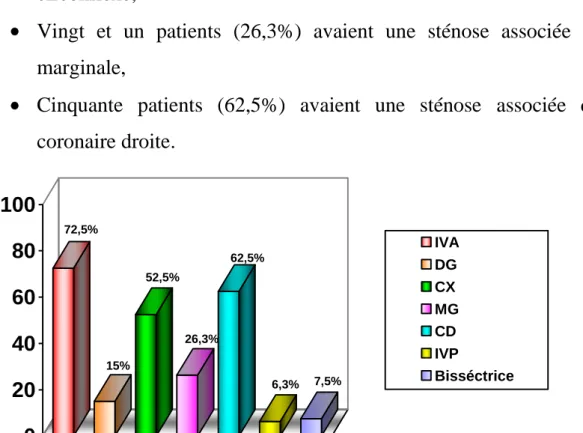
6.3. ATTEINTES CORONAIRES ASSOCIEES :
L’atteinte isolée du tronc commun gauche est rare, sa fréquence est estimée en moyenne à 3%.
Une sténose du tronc commun est en général associée à une athérosclérose coronaire diffuse et sévère, ce qui explique la grande fréquence des lésions associées, monotronculaires, bitronculaires ou tritronculaires.
L’atteinte significative de l’artère coronaire droite, définie par la présence d’une sténose d’au moins 70%, constitue un facteur pronostic important. Elle est fréquente, avec un taux variant de 56% à 79% (10,40).
L’identification de l’atteinte du TCG cliniquement et par des méthodes non invasives manque de spécificité et de sensibilité, la coronarographie reste l’examen de référence.
Aucun critère épidémiologique, ni clinique n’est prédictif d’une sténose du tronc commun gauche.
7.1. CLINIQUE :
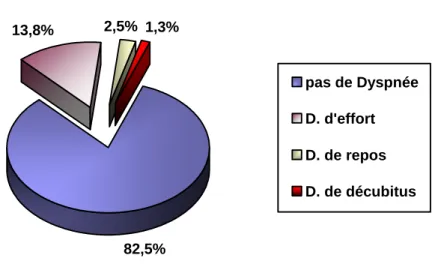
La sténose du TCG peut se manifester cliniquement par un syndrome coronarien aigu. La douleur thoracique est le point d'appel au cours des syndromes coronariens aigues. II s'agit souvent d'une douleur angineuse typique : rétrosternale, constrictive, volontier angoissante. La reconnaissance peut cependant en être plus difficile que celle de l'angor stable, car deux éléments particulièrement évocateurs peuvent manquer : la survenue à l’effort ou lors d'émotions et la cessation rapide, en quelques minutes, notamment à l'arrêt de l'effort.
Les syndromes coronariens aigus, en particulier leurs formes les plus graves, surviennent en effet la plupart du temps au repos, avec des douleurs fréquemment prolongées. Si la douleur thoracique est le signe d'appel le plus typique, il n'est pas rare que le tableau clinique soit moins évocateur, voire trompeur, en particulier chez les patients âgés et les diabétiques: douleurs limitées au niveau des sites classiques d'irradiation (bras gauche, poignets, mâchoire, creux épigastrique), parfois même simplement des troubles digestifs ou des manifestations vagales (42).
Plus rarement la sténose du TCG peut être révélée par une dyspnée qui est secondaire à une élévation de la pression télédiastolique du ventricule gauche, et traduit une ischémie extensive du VG, en accord avec le concept physiopathologique d’une sténose du tronc commun. Cependant, son appréciation peut être subjective, ce qui
explique que ce symptôme est rapporté avec des fréquences variables selon les séries (9,
43 ,44).
L’insuffisance cardiaque congestive, la mort subite et les arythmies cardiaques
sont retrouvées avec une même fréquence que dans les autres localisations de l’atteinte coronaire.
L’occlusion aiguë du TCG est responsable d’un infarctus massif avec insuffisance ventriculaire gauche (killip 3 à 4), et souvent de décès (45).
Enfin, des patients asymptomatiques peuvent avoir une sténose significative du TCG de découverte fortuite, elles sont suspectées après un test d’effort très positif pour une faible puissance (10,46).
Il n’existe pas par rapport aux patients symptomatiques, de différence, en terme de la sévérité de la sténose du tronc commun, de l’étendue des lésions coronariennes et de leur pronostic (47,48).
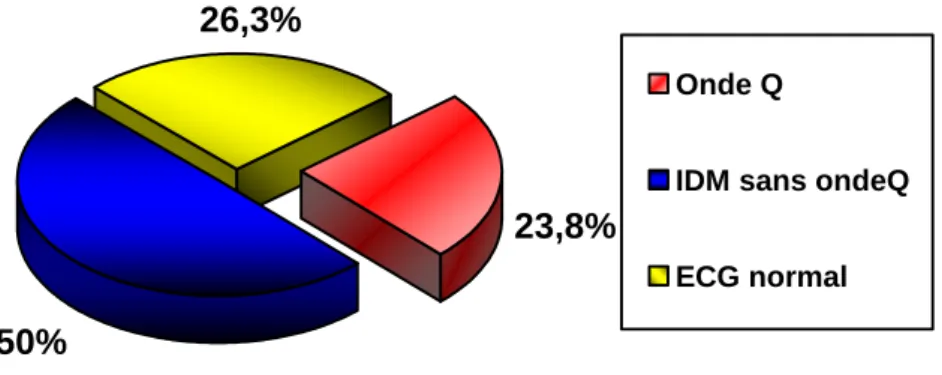
7.2. ENREGISTREMENT ELECTROCARDIOGRAPHIQUE DE REPOS:
L'électrocardiogramme est l'examen à réaliser en toute priorité, en faisant un enregistrement sur 18 dérivations. Le résultat permettra de hiérarchiser le degré de l'urgence médicale et donc le degré de gravité immédiate.
L’ECG de base n’est pas prédictif d’une sténose du TCG ; les anomalies électriques ne sont pas corrélées à la gravité de la sténose du TCG ni à la diffusion de la maladie coronarienne (49).
Un ECG de repos peut être strictement normal sans pour autant exclure une pathologie du tronc, ce qui montre le manque de spécificité de cet examen (29).
La radiographie pulmonaire a un intérêt très faible. On note parfois des images de surcharge du ventricule gauche, non spécifiques, témoins d’une cardiomyopathie ischémique évoluée, et exceptionnellement des calcifications en regard de la région du tronc, sans prédire de la sévérité de l’atteinte ni de la localisation.
7.4. ECHOCARDIOGRAPHIE :
7.4.1. ECHOCARDIOGRAPHIE TRANS-THORACIQUE :
L'échographie transthoracique apporte des renseignements sur la fonction globale du ventricule gauche, et sur la cinétique segmentaire et globale.
De plus, elle permet parfois la visualisation des vaisseaux coronaires proximaux et grâce au doppler l'étude du flux coronaire.
Cependant, cet examen est limité par une variabilité importante opérateur dépendant, et la difficulté parfois à obtenir des images adéquates selon l'échogénicité des patients (42).
7.4.2. ECHOCARGIOGRAPHIE TRANS-OESOPHAGIENNE :
Cet examen n'est pas pratiqué de routine dans le but d'explorer les vaisseaux coronaires et la recherche d'une sténose à leur niveau; lorsqu'elle est demandée elle offre des images de qualité supérieure à l’échographie, transthoracique (ceci du fait de la proximité plus importante des vaisseaux coronaires et de l'utilisation de sondes de haute fréquence) : la visualisation du tronc commun gauche et de la bifurcation est possible dans 80% des cas. Le Doppler bidimensionnel couleur permet l'analyse du flux intra coronaire (50).
7.4.3. ECHOCARDIOGRAPHIE DE STRESS :
L'échographie bidimensionnelle à l'effort et sous stimulation par différents agents pharmacologiques est devenue récemment un moyen de plus en plus courant d'évaluation de l'ischémie myocardique. Son principe repose sur la mise en évidence d'un
trouble de la contractilité segmentaire transitoire (visible à l'échographie cardiaque bidimensionnelle) qui est habituellement classé en hypokinésie, akinésie ou dyskinésie, lors d'un «stress» myocardique à l'origine des phénomènes d'ischémie.
Une épreuve d'effort graduée est le stress physiologique le plus fréquemment employé, l'évaluation de la dynamique ventriculaire étant pratiquée à l'arrêt de l'effort.
Les agents de stress pharmacologiques les plus utilisés sont le dipyridamole et la Dobutamine.
Les marqueurs d'atteinte coronaire sévère sont: des troubles étendus de la contractilité, une dilatation du ventricule gauche, une diminution de la fraction d'éjection du VG, un sous décalage marqué du segment ST, et une chute de la pression artérielle induite par le stress.
L'efficacité de l'échocardiographie de stress dans l'évaluation de l'ischémie myocardique chez les patients coronariens est bonne avec une sensibilité de 81 % et une spécificité de 89% (51).
Cependant, comme pour l'épreuve d'effort et la scintigraphie myocardique, ce test n'est pas spécifique de l'atteinte du tronc commun.
Elle est pratiquée quand l’atteinte du TCG est méconnue.
7.5. EPREUVE D’EFFORT :
Les premiers travaux concernant la pratique de l'épreuve d'effort datent d'une cinquantaine d'années (48, 52). Depuis, cet examen a pris une place essentielle parmi les explorations non invasives cardiologiques. Ses indications se sont multipliées (53).
L'épreuve d'effort est réalisée chez des patients chez qui l'atteinte du tronc commun est méconnue (avant le diagnostic angiographique), en respectant ses contre-indications
(angine de poitrine instable, infarctus du myocarde récent, Bloc auriculo-ventriculaire, HTA maligne)
Cet examen peut être prédictif d'une atteinte coronaire sévère, même s'il n'est pas spécifique de l'atteinte du tronc commun, il n'en demeure pas moins très sensible (sensibilité de 95 à 100%).
De nombreux critères ont été proposés pour identifier ces patients à haut risque, mais il est difficile de différencier l'atteinte du tronc commun des atteintes coronaires multitronculaires (54).
7.6. SCINTIGRAPHIE MYOCARDIQUE :
La scintigraphie myocardique trouve une place privilégiée dans l'arbre décisionnel diagnostique.
En effet, dans l'histoire naturelle de l'ischémie myocardique, les troubles de la perfusion précèdent les modifications électriques ou les anomalies de la cinétique segmentaire.
Elle possède une valeur additive par rapport aux données cliniques et electrocardiographiques (55).
Elle permet d’évaluer la viabilité myocardique par la présence de plage de myocarde viable au sein de segments hypoperfusés.
Elle manque de spécificité, par conséquent, il est possible de méconnaître une hypoperfusion sévère dans la région myocardique ayant la plus forte concentration de traceur (en cas de sténose serrée du tronc commun) (56).
La coronarographie est la méthode de référence dans la visualisation de l’anatomie coronaire, elle reste la clé de diagnostic en matière de sténose du tronc commun.
Sa place est primordiale dans le diagnostic de confirmation ou d’élimination de la maladie coronaire.
Elle connaît un essor spectaculaire lié au développement des techniques d’angioplastie transluminale des coronaires et aux progrès de la chirurgie.
7.7.1. Technique :
Elle est réalisée par voie artérielle (fémorale, humérale ou radiale), avec mise en place d'un introducteur et de sondes diagnostiques préformées.
Les incidences sont multiples pour l'analyse des différents segments coronariens, avec en général:
6 incidences pour le tronc commun et le réseau coronaire gauche (1 face, 2 craniale et caudale en oblique droit, et 2 en oblique gauche, 1 profil).
* L'ostium du tronc commun: OAG caudal. * La Partie moyenne: OAD caudale.
* La Portion distale : OAG caudale.
4 incidences pour la coronaire droite (1 profil, 1 face craniale ou caudale, 1 oblique droite et 1 oblique gauche).
Une ventriculographie gauche en OAG et en OAD termine l'exploration: Elle permet la mesure des volumes, le calcul de la fraction d'éjection et l'analyse de la contractilité globale et segmentaire du VG.
Le monitorage des pressions donne l'enregistrement des courbes ventriculaires, aortiques et de la courbe de retrait ventriculo-aortique à la recherche d'un gradient pathologique.
Image 1 : Sténose très serrée isolée du TCG Incidence face 0º,0º
Image prêtée par le Pr Boukili.M.A
7.7.2. Résultats :
Elle permet le dépistage dès la mise en place de la sonde dans l’ostium d’une lésion significative du TCG, ainsi que l’évaluation qualitative et quantitative.
7.5.1.1. Dépistage immédiat d'une lésion significative du tronc commun:
Il permet de diminuer les risques et peut être réalisé en effectuant la première injection de façon non sélective, à proximité de l'ostium du tronc commun dans le sinus gauche, en incidence de face, complétée si besoin par une opacification en OAD, pour dépister une lésion ostiale avant d'introduire la sonde dans l'ostium du tronc (57).
L'injection de dérivés nitrés est alors systématique devant toute suspicion d'une sténose du tronc commun.
Au moment de la canulation du réseau coronaire gauche, le cathéter doit être introduit doucement et graduellement à l'intérieur de l'ostium.
La pression au bout de cathéter doit être monitorée en permanence : Une chute de pression systolo-diastolique ou seulement diastolique témoigne d'un obstacle au bout de sonde et doit faire évoquer la possibilité d'une sténose du tronc; une première injection permet d'éliminer l'éventualité d'un cathéter placé contre la paroi de l'artère et de confirmer la sténose du tronc coronaire commun. L'injection de dérivés nitrés permet de confirmer le caractère organique de la sténose.
Une absence de reflux dans le sinus coronaire lors de l'injection sélective, même en l'absence de chute de pression, est un argument indirect de lésion significative du tronc commun.
Le diagnostic d'une sténose significative du tronc commun doit limiter le nombre d'injections.
7.5.1.2. Evaluation lésionnelle:
* L'évaluation quantitative des lésions:
La lésion est quantifiée à partir de la mesure du diamètre maximum de sténose du tronc qui est rapporté au diamètre de référence du tronc.
Le diamètre de référence est mesuré au niveau d'un segment sain proximal ou distal par rapport à la lésion lorsque la sténose est focale.
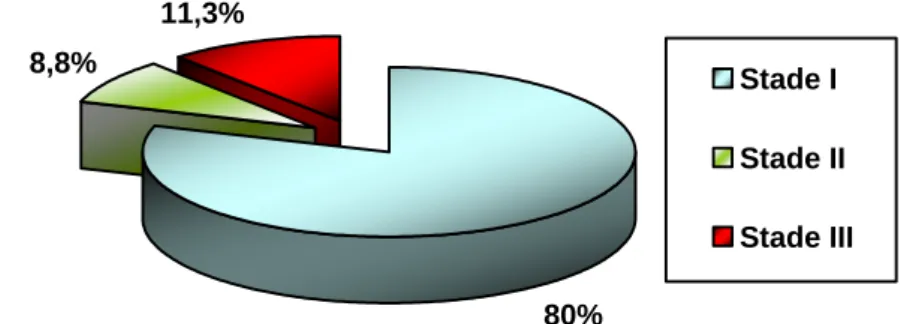
Les rétrécissements sont habituellement classés en 3 stades : Stade I : sténose serrée : 50-69%.
Stade III : sténose subocclusive : >90%.
L'évaluation quantitative angiographique des lésions du TCG est confrontée à plusieurs problèmes.
Un nombre suffisant d'incidences angiographiques dégageant le tronc commun reste le meilleur moyen de limiter ces difficultés, en rappelant que les injections doivent rester parcimonieuses.
Une autre difficulté est celle liée à l'impossibilité de mesurer un diamètre de référence quand l'atteinte est diffuse; la quantification devient très aléatoire et la mesure du diamètre maximum de sténose du tronc est rapportée soit à une mesure de référence théorique soit à une mesure de référence arbitrairement évaluée sur le diamètre cumulé des branches de division.
*L'évaluation qualitative des lésions:
Elle pose les mêmes problèmes que pour toute angiographie; l'analyse qualitative reste descriptive:
La présence de calcifications est affirmée sur la présence d'opacités dessinant plus ou moins bien le trajet artériel. L'importance du processus calcifiant peut être appréhendé sur cet aspect: calcifications importantes avec opacités fixes (présentes tout au long de la séquence cinéma), calcifications modérées avec opacités intermittentes (répétées sur quelques images de la séquence).
Une dissection donne une image de voile intraluminal.
La présence d'un thrombus est soupçonnée sur une image intra-luminale moulée par le produit de contraste.
Mais aucun de ces aspects n'est suffisamment sensible et spécifique. Seule l'angioscopie serait à même de faire le diagnostic de thrombus, mais sa réalisation est impossible au niveau du tronc coronaire commun (nécessité d'un ballon d'occlusion).
7.8. AUTRES EXAMENS :
7.8.1. Tomodensitométrie multibarettes :
La TDM multibarette 64 ou 128, constitue une des modalités d'imagerie cardiaque avancée de la nouvelle génération.
Ce scanner permet de détecter des lésions coronaires significatives lorsque l'épreuve d'effort n'est pas concluante, il pourrait donc s'intégrer comme technique complémentaire dans le dépistage de la maladie coronaire (58).
Cette nouvelle technique d'imagerie non invasive, et grâce aux développements récents concernant le nombre de détecteurs, la rapidité d'acquisition en apnée, en synchronisation rétrospective avec obtention d'images isotopiques, a permis d'affranchir les problèmes de mouvements respiratoires et cardiaques qui limitaient l'utilisation de la TDM hélicoïdale dans l'étude cardiaque.
Il peut avoir un intérêt préthérapeutique en cas de discussion d’un geste de revascularisation secondaire, en évaluant l’extension ostiale et le caractère calcifié d’une sténose du tronc commun ou de la coronaire droite, ainsi que la longueur d’une occlusion et la qualité d’un lit d’aval, et enfin en caractérisant l’implantation coronaire en cas de variantes anatomiques. Ces données peuvent en effet être mises à défaut en coronarographie.
Elle permet également une étude de l’arbre aortique, de ses principales collatérales (notamment l’artère mammaire interne), de la topographie d’un pontage aortocoronaire mis en place antérieurement et du parenchyme pulmonaire avant d’envisager une chirurgie coronaire (59).
7.8.2. Ultrasons endocoronaires :
L'échographie endovasculaire est une technique d'imagerie récente permettant l'étude de la structure de la paroi artérielle, de sa lumière et de son contenu. Réalisée au cours du cathétérisme ou d'actes de cardiologie interventionnelle, elle permet une approche échographique des lésions pariétales et/ou endoluminales. Elle est donc dotée d'une plus grande sensibilité et spécificité que la coronarographie: (60)
Elle permet une quantification plus précise de la lésion.
Elle permet une analyse qualitative plus sensible de la paroi et de la lésion (lésion homogène ou mixte, calcifiée ou non, ulcération…).
Elle a de plus montré la possibilité d'une atteinte athéromateuse significative du TCG sur des aspects angiographiques normaux ou subnormaux.
L'application la plus répandue de l'échographie endocoronaire est l'évaluation des résultats immédiats d'une procédure de revascularisation endoluminale : l'obtention d'une image échographique montrant un résultat non satisfaisant entraînera un geste complémentaire.
7.8.3. Imagerie par résonance magnétique :
L’imagerie par résonance magnétique (IRM) est devenue au cours des dernières années un examen de plus en plus utilisé dans l’exploration des patients atteints de maladie coronaire. Elle trouve sa place à plusieurs niveaux, même si elle reste encore insuffisamment demandée pour des raisons de disponibilité.
C’est aujourd’hui l’examen de référence pour l’appréciation des paramètres fonctionnels ventriculaires (volume, fraction d’éjection, masse ventriculaire) dont on connaît la valeur pronostique et l’importance dans l’adaptation thérapeutique. Dans le post infarctus, grâce aux techniques de rehaussement tardif, l’IRM permet d’analyser avec précision l’étendue de la nécrose en termes de segments et de transmuralité. Le remodelage ventriculaire et ses conséquences (altération fonctionnelle, anévrisme, thrombus pariétal) représentent une excellente indication de l’IRM, notamment en préopératoire.
L’IRM avec stress pharmacologique peut également être employée comme outil de détection de l’ischémie myocardique ; dans ce cas lesséquences utilisées sont des séquences de perfusion, ou de premier passage.
En revanche, l’angio-IRM à visée d’exploration morphologique du réseau coronaire et de mesure de sténose n’est pas encore arrivée au stade la routine (61).
8. TRAITEMENT DES STENOSES DU TRONC COMMUN
8.1. METHODES MEDICALES :
Le traitement médical est prescrit systématiquement à tous les patients chez qui une coronaropathie a été diagnostiquée.
Les patients relevant d'un traitement médical seul sont les patients symptomatiques considérés comme inopérables en raison d'un lit d'aval médiocre, non pontable, les patients dont la fraction d'éjection ventriculaire est trop altérée avec un chiffre théorique de FE inférieur à 20 %, les patients atteints d'une affection médicale à mauvais pronostic et les patients refusant l'intervention.
Il repose essentiellement sur l'administration de trinitrine, d'action rapide, par voie sublinguale ou par voie intraveineuse dans les formes sévères. La dose efficace est obtenue en augmentant par pallier la vitesse de perfusion.
La pression artérielle ne doit pas s'abaisser au dessous de 100 mmHg.
8.1.2. Traitement de fond :
Il existe 3 catégories de traitement.
8.1.2.1. Agents anti-ischémiques :
Les Bêtabloquants Les Dérivés nitrés
Les Inhibiteurs calciques
8.1.2.2. Traitements antithrombotiques :
Les Antiagréqants plaquettaires :
Acide acétyle salicylique (aspirine) Ticlopidine et clopidogrel
Inhibiteurs des récepteurs plaquettaires glycoprotéiques IIb/IIIa
L’Héparine
8.1.2.3. Traitement fibrinolytique :
Il doit être administré dans les 6 heures qui suivent la survenue de la douleur infarctoïde.
Les principales molécules utilisées sont la streptokinase, l'APSAC (anisoylated plasminogen streptokinase activator complex), et le rt-PA.
Plusieurs études ont confirmé le pouvoir des fibrinolytiques à rétablir la perméabilité vasculaire dans 60 à 80% des cas. Ce taux de perméabilité varie en fonction du produit utilisé, de sa posologie et des thérapeutiques adjuvantes (62).
La fibrinolyse, améliore la survie chez les patients présentant un syndrome coronarien aigu avec sus décalage persistant du segment ST, cependant elle peut être à l'origine de complications de gravité variable.
8.1.2.4. Mesures générales: prévention secondaire : (62)
Régime alimentaire Les statines
Contrôle de la pression artérielle Contrôle du diabète
Arrêt du tabac
8.2. METHODES DE REVASCULARISATION :
Les conditions de revascularisation myocardique sont identiques pour l'angioplastie et la chirurgie de pontage aortocoronaire, il faut en effet qu'il existe une lésion sévère, un bon lit d'aval, une fraction d'éjection supérieure à 35%.
8.2.1. ANGIOPLASTIE TRANSLUMINALE PERCUTANEE :
Les angioplasties transluminales percutanées du tronc coronaire commun ont été réalisées très tôt. En effet, l'accessibilité du tronc coronaire gauche aux techniques de revascularisation percutanée et son calibre important, ont incité les cathétériseurs à effectuer des tentatives de dilatation sur ce vaisseau dès l'avènement de ce procédé.
8.2.1.1. Angioplastie au ballon :
Les premières études utilisant les techniques d'angioplastie coronaire percutanée ont rapporté des résultats initiaux, médiocres à long terme comparés à ceux de la revascularisation chirurgicale par PAC, ainsi la revascularisation percutanée a été réservée aux patients ayant une contre indication formelle à la chirurgie ou en présence d'un TCG protégé par un ou plusieurs PAC fonctionnels et en cas d'IDM par occlusion aiguë du TCG (63).
Les mauvais résultats obtenus par dilatation standard des lésions du TCG étaient favorisés par un phénomène de retour élastique important susceptible d'initier la resténose dans les suites de l'angioplastie; ce phénomène est prédominant dans le TCG particulièrement riche en fibres élastiques (65, 66, 76).
Limites:
Les différentes techniques d'angioplastie au ballon sont exposées à de nombreuses complications:
Perprocédurales: retour élastique immédiat (constant au niveau de
l'ostium) dissection et/ ou thrombus avec risque d'occlusion aigue.
Post-procédurales : thrombose et resténose, dont la manifestation peut
être l'IDM ou la mort subite.
8.2.1.2. Stenting du TCG :
Le développement récent des endoprothèses coronaires et les progrès des techniques d'implantation associées à l'amélioration des traitements antithrombotiques péri-procéduraux (administration d'inhibiteurs des récepteurs GP IIb/IIIa) ont permis de diminuer les complications thrombotiques et hémorragiques après implantation d'une endoprothèse. En effet, l'angioplastie au ballon complétée de l'implantation systématique d'une endoprothèse du TCG a fait la preuve de son efficacité dans la réduction de
l'incidence de la resténose après dilatation (67), ceci a été attesté par d'importantes études multicentriques récentes (66, 68, 69).
Les lésions du TCG considérées favorables au Stenting sont les lésions courtes, non .calcifiées, ostiales, du tronc moyen, distales étendues à l'ostium de l'IVA ou de la Cx quand l'une de ces branches est de petit calibre ou occluse avec une bonne fonction du VG.
Un TC court < 8mm, très calcifié, une fonction VG altérée (40%), une atteinte pluri tronculaire représente des contre indications au Stenting.
Une angioplastie est considérée réussie lorsqu'il y a une diminution d'au moins 20% de la lésion initiale avec une sténose résiduelle inférieure à 30% du diamètre de la lumière du tronc commun, de plus l'absence de survenue d'une complication majeure durant la phase hospitalière (décès, infarctus du myocarde, chirurgie coronaire en urgence sont les trois critères habituellement retenus) est nécessaire pour considérer l'intervention comme un succès clinique (40,70).
Les complications immédiates du Stenting du TCG sont dominées par le risque d'occlusion aigue per ou péri procédurale entraînant un IDM, souvent mortel en
dehors d’une chirurgie urgente.Le risque de resténose représente un problème majeur dans
l'évolution à moyen terme de l'angioplastie avec Stenting du TCG,
La définition de la resténose est angiographique et correspond à la réapparition au site de la lésion initiale d'une sténose hémodynamiquement significative (réduction du diamètre de la lumière artérielle de plus de 50% par rapport au diamètre de référence).
La resténose est la conséquence d'un remodelage négatif et/ ou la constitution d'une néoprolifération intimale excessive.
Elle se manifeste au bout de 3 à 6 mois, lors de la réalisation d'un contrôle angiographique. Cliniquement la réapparition des douleurs angineuses est très
évocatrice, mais la situation est souvent plus complexe du fait de l'existence de lésions associées non traitées par angioplastie ou d'une resténose silencieuse. La réalisation d'un contrôle angiocoronarographique environ 6 mois après l'angioplastie permet un diagnostic de certitude d'une resténose. L'usage de stents actifs au niveau du tronc commun permet de réduire le taux de resténose de moitié par rapport à la dilatation aux stents nus ou à la dilatation au ballon seul (42).
Image 2 : Sténose très serrée isolée du TCG, mise en place du guide de dilatation COUGAR XT 0,014 qui franchie la lésion et se positionne en aval de celle-ci
Incidence OAD 30º Caudal
Image 3 : Mise en place directe d’un stent cypher Select plus de 3,50/18 mm
Incidence OAD 30º Caudal
Image prêtée par le Pr Boukili.M.A
Image 4 : Inflation du stent de 30 sec. à 12 atm
Incidence OAD 30º Caudal
Image 5 : Injection de contrôle après l’inflation : Le stent est bien déployé et est parfaitement perméable
Incidence OAD 30º Caudal
Image prêtée par le Pr Boukili.M.A 8.2.1.3. Autres outils :
D'autres techniques sont utilisées (telle que l'athérectomie
directionnelle, rotative, laser...), mais le nombre de cas rapportés dans les publications est limité avec un suivi inexistant.
8.2.2. LE PONTAGE AORTO-CORONAIRE : (79, 80, 81)
La chirurgie de pontage aortocoronaire est née en 1967, elle a pour principe de court-circuiter les lésions artérielles. Les pontages sont effectués avec des greffons veineux (en général veine saphène interne) avec récemment une prédilection des greffons artériels (artère mammaire interne, artère gastro-epiploique droite, artère radiale) (71), ceci a permis d'améliorer considérablement le pronostic à long terme des pontages aortocoronaires.
Les modalités chirurgicales divergent suivant les auteurs, certains recommandent de ponter en premier lieu l'artère la plus importante, d'autres la coronaire droite pour augmenter la collatéralité (72).
Le geste opératoire comporte une mortalité comprise entre 1,5 et 3% selon la sévérité des lésions coronaires et la qualité de la fonction ventriculaire gauche (73).
8.2.2.1. Le bilan préopératoire :
L’évaluation de l’atteinte coronaire étant réalisée (coronaropathie
affirmée, fonction ventriculaire appréciée), le bilan préopératoire doit comporter la recherche d’autres localisations athéromateuses, l’évaluation des fonctions respiratoires, rénales et neurologiques, le dépistage de foyers infectieux et l’appréciation du capital greffon. Ces examens ne doivent pas retarder la chirurgie.
Un athérome coronarien doit faire rechercher une autre localisation athéromateuse, le patient devant être considéré comme un patient polyvasculaire. À l’examen clinique doit s’ajouter une exploration écho doppler systématique des troncs supra-aortiques (participant au dépistage des lésions des artères à destinée céphalique et des lésions proximales des axes sous-claviers en amont de l’origine des artères mammaires) et des artères des membres inférieurs avec mesure des index de pression systolique (IPS).
Un bilan biologique pré-CEC est demandé comprenant : NFS, plaquettes,
Ionogramme avec urée et créatinine, Bilan hépatique,
Sérologies hépatites virale B et C, TPHA-VDRL, HIV1 et HIV2 Groupage ABO et RH,
Recherche d’agglutinines irrégulières, Radiographie pulmonaire (Face + Profil).
8.2.2.2. Préparation à la chirurgie :
8.2.2.2.1. Consultation chirurgicale :
Bien entendu indispensable, elle est essentielle pour instaurer la relation de confiance entre le chirurgien, le patient et sa famille. Une indication chirurgicale est confirmée ; les différents éléments de décision sont observés ; la stratégie opératoire est envisagée étant concrétisé par la signature par le patient d’un consentement éclairé (ce consentement n’est pas obligatoire actuellement au Maroc).
8.2.2.2.2. Consultation pré-anesthésique :
Une consultation d’anesthésie, devant être réalisée au minimum 2 jours avant l’intervention, en dehors des situations d’urgence ; elle est obligatoire. Elle est au mieux et généralement réalisée le jour même de la consultation chirurgicale. Elle permet d’apprécier l’état général du patient, de rechercher d’éventuels facteurs de risque anesthésique, d’apprécier le risque opératoire à l’aide de différents scores préopératoires. Elle peut de ce fait remettre en cause la légitimité d’une indication opératoire.
8.2.2.2.3. Prescriptions préopératoires :
Elles concernent notamment les précautions à prendre vis-à-vis des traitements prescrits : arrêt de l’aspirine 8 jours avant l’intervention (plusieurs équipes ne l’arrêtent plus), de la ticlopidine et du clopidogrel 10 jours avant, arrêt des inhibiteurs de l’enzyme de conversion 2 jours avant et arrêt des digitaliques 3 jours avant l’intervention. Une prémédication est prescrite au malade.
Une kinésithérapie préopératoire est fortement conseillée chez les patients présentant des broncho-pneumopathies chroniques. La prescription d’une
contention thoracique pour la phase postopératoire immédiate (corset souple) peut être un adjuvant utile, notamment en cas d’utilisation des deux artères mammaires.
L’instauration d’une autotransfusion n’est possible en chirurgie coronaire que chez un patient parfaitement stable.
8.2.2.3. Au bloc opératoire :
8.2.2.3.1. Accueil du malade et anesthésie :
Installation en décubitus dorsal, scope, dynamap, 2 voies veineuses périphériques de gros calibre, branchement de perfusion, solutés de remplissage.
La mise en condition dépend des équipes, Pression artérielle sanglante,
Induction anesthésique, Intubation + ventilation, Mise en place de :
Voie veineuse centrale ou cathéter de Swan Ganz Thermomètre rectal et oesophagien,
Sonde naso-gastrique, Sonde urinaire,
Autres : en fonction des protocoles de chaque équipe. 8.2.2.3.2. Mise en place du ballon de contre pulsion intra-aortique :
La mise en place du BCPIA avant l’induction est systématique pour certaine équipe chez les patients porteurs de sténoses du TCG.
Subocclusion du TCG TCG non protégé, TCG avec IDM récent,
TCG avec dysfonctionnement du VG, TCG symptomatique.
8.2.2.4. Installation en position chirurgicale du patient :
Le patient est installé en décubitus dorsal, sur un matelas chauffant, les
bras le long du corps dans des manchons pour éviter les compressions. Un billot est placé sous les épaules pour obtenir une légère extension du cou. Le badigeonnage consiste en l’application de solution antiseptique (type Bétadinet) sur le thorax, le cou, l’abdomen et les membres inférieurs (photo 1).
Photo 1 : Installation du malade en position chirurgicale
Plusieurs protocoles existent, mais la technique est sensiblement identique suivant les centres. Elle consiste en plusieurs lavages, en commençant par les zones d’incision et en finissant par les zones septiques, en attendant entre chaque
application que cela sèche, sans essuyer. En ce qui concerne les membres inférieurs, deux installations sont possibles : soit seule la zone de prélèvement de la veine saphène interne est incluse dans le champ, soit la totalité du membreinférieur est dans le champ. Quelle que soit l’installation, la totalité du membre inférieur est badigeonnée et le pied est placé dans un jersey stérile .La disposition des champs se fait selon la technique de recouvrement progressif.
8.2.2.5. Prélèvement et préparation des greffons :
Le matériel de pontage est dans la majorité des cas des autogreffes veineuses ou artérielles. Les autres conduits, homogreffes, hétérogreffes ou synthétiques, sont d’utilisation exceptionnelle. Le greffon mammaire, supérieur au greffon saphène, s’est imposé.
La discussion actuellement est à l’utilisation des deux artères mammaires, voire à l’utilisation exclusive de greffons artériels. Un greffon pédiculé (ou in situ) est laissé avec son pédicule, son origine vasculaire. Cela peut être le cas avec les artères mammaires ou l’artère gastroépiploïque.
Un greffon libre n’est pas laissé sur son pédicule et nécessite donc une réimplantation proximale généralement réalisée sur l’aorte ascendante. C’est le cas des greffons saphènes, radiaux, épigastriques, voire mammaires ou gastroépiploïques lorsque leur longueur est trop courte.
8.2.2.5.1. Greffon saphène : (photo 2)
La veine saphène interne a été et reste encore le greffon le plus utilisé en chirurgie coronaire. La veine saphène externe est très peu utilisée. Les autres greffons veineux sont anecdotiques. A la jambe, la veine saphène interne a un calibre plus adapté qu’à la cuisse.
Photo 2 : Prélèvement du greffon saphène
– Avantages : la facilité et la rapidité du prélèvement, la longueur disponible, la facilité d’utilisation, un flux maximal d’emblée.
– Inconvénients : la discordance des diamètres avec la coronaire, la nécessité d’une réimplantation proximale, son prélèvement délabrant et un faible taux de perméabilité à moyen et long termes.
– Résultats : l’hyperplasie fibromusculaire intimale de la première
année suivie par l’athérosclérose des greffons saphènes est à l’origine des résultats décevants de ces greffons. Le taux annuel d’occlusion est de 2 % entre la première et la cinquième année postopératoire, de 5 % ultérieurement de telle sorte que, à 12 ans, 50 % des greffons sont occlus et 50 % des greffons perméables sont pathologiques.
8.2.2.5.2. Greffon mammaire : (photo3)
Le pontage de l’IVA par l’artère mammaire interne gauche (AMIG) in situ s’est imposé comme le gold standard de la chirurgie coronaire.
Photo 3 : Prélèvement du greffon mammaire
– Avantages : greffon artériel pédiculé dont les taux de perméabilité à
court et long terme sont excellents.
– Inconvénients : les difficultés de prélèvement et d’utilisation, une longueur limitée, la possibilité de spasmes, la dévascularisation sternale, la fréquence des épanchements pleuraux en cas d’ouverture pleurale, le risque de lésion phrénique.
– Résultats : l’AMIG a les meilleurs taux de perméabilité (96 % à 1 an,
90 % à 10 ans). Néanmoins, les taux de perméabilité varient en fonction de l’artère mammaire (gauche ou droite), utilisée en greffon in situ ou en greffon libre.
8.2.2.5.3. Autres types de greffons artériels : Artère radiale :
Utilisée dès 1970 par Carpentier, l’artère radiale connaît un regain d’intérêt en chirurgie coronaire. Le mode de prélèvement (dissection avec pédicule en prenant les deux veines satellites), de préparation (artère rincée et légèrement dilatée plutôt que forcée avec une solution sanguine contenant de la papavérine) et l’utilisation en continu, dès la période péri-opératoire, d’inhibiteurs calciques expliquent ce regain d’intérêt.