Qualité du traitement pharmacologique de
l’insuffisance cardiaque chez les ainés du Québec et
impact sur les résultats de santé
Thèse
Catherine Girouard
Doctorat en sciences pharmaceutiques (pharmaco-épidémiologie)
Philosophiae doctor (Ph.D.)
Québec, Canada
© Catherine Girouard, 2016
Résumé
L’insuffisance cardiaque est un problème de santé important chez les ainés. Selon les lignes directrices, un traitement de qualité doit comporter les médicaments diminuant la mortalité et les hospitalisations (le traitement standard), mais ne doit pas comporter de médicaments potentiellement inappropriés en insuffisance cardiaque. On ne connait ni l’effet du vieillissement sur l’exposition au traitement standard chez les ainés ni l’effet d’un traitement de qualité sur les résultats de santé. Cette thèse a pour objectif d’estimer l’effet de l’usage d’un traitement de qualité sur les résultats de santé chez les ainés suite à un premier diagnostic d’insuffisance cardiaque.
À l’aide des bases de données administratives gérées par la Régie de l’assurance maladie du Québec, nous avons réalisé deux études de cohorte pour déterminer l’effet du vieillissement sur l’exposition au traitement standard chez les ainés et les facteurs associés à l’exposition aux β-bloqueurs, qui sont nécessaires au traitement standard. Pour déterminer l’effet de l’exposition aux β-bloqueurs et aux médicaments potentiellement inappropriés (anti-inflammatoires non-stéroidiens, thiazolidinediones, nifédipine et bloqueurs des canaux calciques non-dihydropyridines) sur le risque d’hospitalisation, nous avons effectué une étude cas-témoins imbriquée dans une cohorte.
Chez les ainés ayant eu un premier diagnostic d’insuffisance cardiaque, la probabilité d’être exposé au traitement standard diminue avec l’augmentation en âge. Les patients pour lesquels un β-bloqueur est moins susceptible d’être initier sont ceux âgés de 90 ans et plus et ceux souffrant de maladie pulmonaire obstructive chronique. L’exposition à un β-bloqueur est associée à une diminution du risque de décès et d’hospitalisation. Par contre, l’exposition aux médicaments potentiellement inappropriés est associée à une augmentation du risque d’hospitalisation.
Bien que les ainés soient sous-exposés au traitement standard de l’insuffisance cardiaque, ils bénéficient de l’exposition à un β-bloqueur pour diminuer la mortalité et les hospitalisations tout comme les adultes plus jeunes. Il est donc important de traiter les ainés selon les lignes directrices et, afin d’aider les cliniciens, les recommandations de celles-ci devraient être généralisées aux ainés.
Abstract
Heart failure (HF) patients should be exposed to drugs reducing mortality and hospitalization (standard treatment), but should not be exposed to drugs potentially inappropriate in HF. This thesis presents population-based studies performed with the Quebec public health administrative databases. Among seniors newly diagnosed with HF, the probability of exposure to standard treatment decreases with increasing age. Patients aged 90+ and those with chronic obstructive pulmonary disease are less likely to initiate a β-blocker. Exposure to a β-blocker is associated with a decreased risk of death and hospitalization. Exposure to potentially inappropriate drugs (nonsteroidal anti-inflammatory drugs, thiazolidinediones, nifedipine and non-dihydropyridine calcium channel blockers) is associated with an increased risk of hospitalization. Since HF quality treatment improves health outcomes in HF seniors, treatment guidelines should be extended to seniors.
Table des matières
Résumé ... iii
Abstract ... v
Table des matières ... vii
Liste des tableaux ... xi
Liste des figures ... xiii
Liste des abréviations ... xv
Remerciements ... xix
Avant-propos ... xxi
INTRODUCTION DE LA THÈSE: CHAPITRE 1 ... 1
1.1 Problématique ... 2
1.2 Objectif général de la thèse et aperçu de sa présentation ... 4
CHAPITRE 2 ... 7
2.1 L’insuffisance cardiaque ... 8
2.1.1 Définition et manifestations ... 8
2.1.2 Facteurs de risque et prévention ... 9
2.1.3 L’insuffisance cardiaque en chiffres : incidence et prévalence ... 10
2.1.4 Le fardeau de l’insuffisance cardiaque ... 10
2.1.4.1 Impact de l’insuffisance cardiaque sur la qualité de vie ... 11
2.1.4.2 Impact de l’insuffisance cardiaque sur les hospitalisations ... 11
2.1.4.3 Impact de l’insuffisance cardiaque sur la mortalité ... 11
2.1.4.4 Impact de l’insuffisance cardiaque sur les fonctions cognitives ... 12
2.1.4.5 Impact de l’insuffisance cardiaque sur les coûts pour la société ... 13
2.2 Les traitements de l’insuffisance cardiaque recommandés par les lignes directrices . 14 2.2.1 Les β-bloqueurs ... 15
2.2.2 Les inhibiteurs de l’enzyme de conversion de l’angiotensine (IECA) ... 15
2.2.3 Les antagonistes des récepteurs de l’angiotensine ... 16
2.2.4 L’association d’hydralazine et d’isosorbide dinitrate ... 16
2.2.5 Les médicaments potentiellement inappropriés chez les personnes souffrant d’insuffisance cardiaque ... 17
2.2.5.1 Les anti-inflammatoires non-stéroïdiens ... 17
2.2.5.2 Les thiazolidinediones ... 18
2.2.5.3 La nifédipine ... 20
2.2.5.4 Les bloqueurs de canaux calciques non-dihydropyridines ... 21
2.3 Conclusion de l’état des connaissances sur l’insuffisance cardiaque et ses traitements ... 22
CHAPITRE 3 ... 25
3.1 Les modifications du système cardiovasculaire associées au vieillissement ... 26
3.1.3 Changements de la structure cardiaque ... 27
3.1.4 Changements de la fonction cardiaque ... 28
3.2 Les modifications de la pharmacocinétique et de la pharmacodynamique associées avec le vieillissement ... 28
3.2.1 Les changements de la pharmacocinétique ... 28
3.2.2 Les changements de la pharmacodynamie ... 30
3.3 La fragilité ... 31
3.3.1 Qu’est-ce que la fragilité? ... 32
3.3.2 Les modèles conceptuels de la fragilité ... 33
3.3.3 La prévalence de la fragilité ... 34
3.3.4 Le lien entre la fragilité et les maladies cardiovasculaires ... 36
3.3.4.1 La fragilité et l’insuffisance cardiaque : l’œuf ou la poule ? ... 36
3.3.4.2 Impact de la fragilité chez les individus souffrant de maladies cardiovasculaires ... 37
3.5 L’effet des médicaments recommandés par les lignes directrices sur la mortalité et les hospitalisations ... 38
3.5.1 L’effet des traitements cardiovasculaires sur la mortalité des ainés souffrant d’insuffisance cardiaque ... 40
3.5.1.1 L’effet des β-bloqueurs sur la mortalité chez les ainés ... 40
3.5.1.2 L’effet des IECA sur la mortalité chez les ainés ... 42
3.5.1.3 L’effet des ARA sur la mortalité chez les ainés ... 43
3.5.1.4 L’effet de la digoxine sur la mortalité chez les ainés ... 45
3.5.1.5 L’effet des antagonistes de l’aldostérone sur la mortalité chez les ainés ... 45
3.5.1.6 L’effet de l’hydralazine en association avec l’isosorbide dinitrate sur la mortalité chez les ainés ... 46
3.5.1.7 L’effet des traitements cardiovasculaires utilisés en combinaison sur la mortalité chez les ainés ... 47
3.5.1.8 Conclusion de l’effet des médicaments cardiovasculaires sur la mortalité chez les ainés ... 47
3.5.2 L’effet des médicaments cardiovasculaires sur les hospitalisations chez les ainés ... 48
3.5.2.1 L’effet des β-bloqueurs sur les hospitalisations chez les ainés ... 48
3.5.2.2 L’effet des IECA sur les hospitalisations chez les ainés ... 51
3.5.2.3 L’effet des ARA sur les hospitalisations chez les ainés ... 52
3.5.2.5 L’effet de la digoxine sur les hospitalisations chez les ainés ... 53
3.5.2.6 L’effet des antagonistes de l’aldostérone sur les hospitalisations chez les ainés ... 53
3.5.2.7 L’effet de l’hydralazine en association avec l’isosorbide dinitrate sur les hospitalisations chez les ainés ... 54
3.5.2.8 Conclusion de l’effet des médicaments cardiovasculaires sur les hospitalisation chez les ainés ... 54
3.6 Conclusion menant aux objectifs de la thèse ... 54
CHAPITRE 4 ... 57
4.1 Les objectifs spécifiques de la thèse ... 58
CHAPITRE 5 ... 59
5.1 Les bases de données administratives de la Régie de l’assurance maladie du Québec (RAMQ) ... 60
5.2 Les données provenant de l’Institut de la statistique du Québec ... 61
5.3 Validité des diagnostics médicaux et de l’information sur les médicaments provenant des bases de données administratives ... 61
CHAPITRE 6 ... 65
6.1 Résumé de l’étude ... 66
6.2 Underexposure of seniors to heart failure drug therapy ... 67
6.2.1 Abstract ... 67 6.2.2 Introduction ... 68 6.2.3 Methods ... 69 6.2.4 Results ... 72 6.2.5 Discussion ... 73 6.2.6 Supplemental material ... 83 CHAPITRE 7 ... 85 7.1 Résumé de l’étude ... 86
7.2 Determinants of β-blocker initiation and discontinuation in a population-based cohort of seniors newly diagnosed with heart failure ... 87
7.2.1 Abstract ... 87 7.2.2 Introduction ... 88 7.2.3 Methods ... 90 7.2.4 Results ... 93 7.2.5 Discussion ... 95 7.2.6 Supplemental material ... 109 CHAPITRE 8 ... 115 8.1 Résumé de l’étude ... 116
8.2 Effect of β-blocker exposure on all-cause mortality and hospitalization among seniors newly diagnosed with heart failure ... 117
8.2.1 Abstract ... 117 8.2.2 Introduction ... 118 8.2.3 Methods ... 119 8.2.4 Results ... 123 8.2.5 Discussion ... 124 8.2.6 Conclusion ... 126 8.2.7 Supplemental Material ... 132 CHAPITRE 9 ... 137 9.1 Résumé de l’étude ... 138
9.2 Effect of contraindicated drugs for heart failure on mortality and hospitalization
among seniors with heart failure ... 139
9.2.1 Abstract ... 139 9.2.2 Introduction ... 140 9.2.3 Methods ... 141 9.2.4 Results ... 145 9.2.5 Discussion ... 145 9.2.7 Supplemental material ... 154 CHAPITRE 10 ... 157 10.1 Discussion de la thèse ... 158
10.1.1Synthèse des résultats ... 158
10.1.2 Forces et limites des études ... 160
10.1.2.1 Forces ... 160
10.1.2.2 Limites ... 161
10.2 Implications et perspectives futures ... 164
Liste des tableaux
Tableau 3.1 Liste des déficits inclus dans l’indice des déficits cumulés de Mitniski et
Rockwood ... 56 Table 6.1 Daily minimum target doses for drugs included in the heart failure drug therapy
... 77 Table 6.2 Baseline characteristics of the 86,428 patients aged 65+ years newly diagnosed
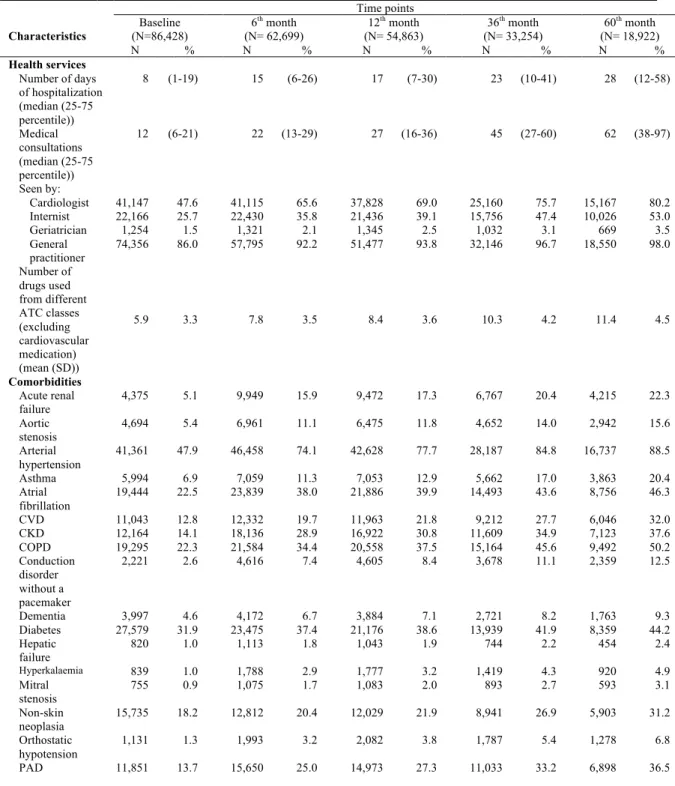
for heart failure ... 78 Table 6.3 Use of health services and observed comorbidities during the 365-day period
before the initial heart failure diagnosis (baseline) plus the interval up to each of the particular time points (at 6, 12, 36, and 60 months post-HF diagnosis) ... 79 Table 6.4 Influence of the passage of time (by 6-month intervals after heart failure
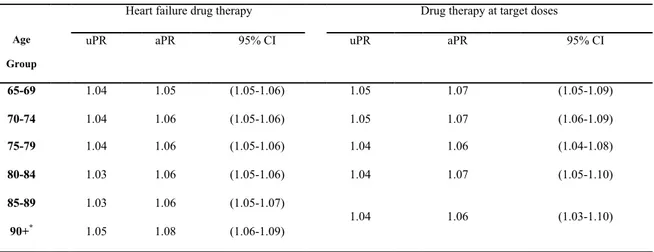
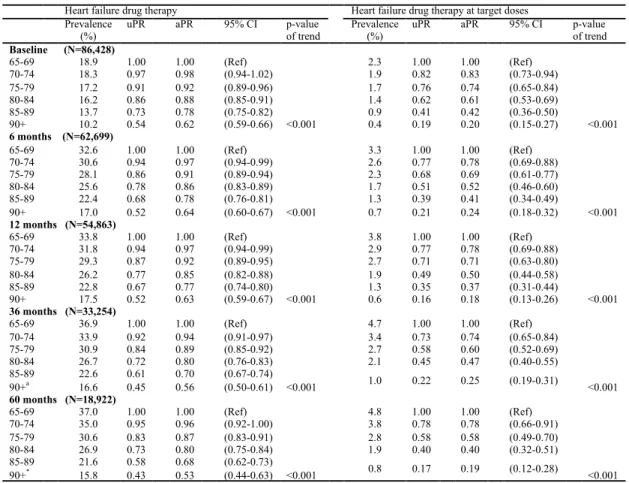
diagnosis) on prevalence ratios of exposure to heart failure drug therapy and drug therapy at target doses over the 60 month-period following heart failure diagnosis, according to age ... 83 Table 6.5 Prevalence ratios of exposure to heart failure drug therapy and to drug therapy at
target doses, according to age ... 84 Table 7.1 Characteristics of the study population according to the use of a β-blocker at time
of heart failure diagnosis (N = 119,184) ... 100 Table 7.2 Determinants of β-blocker initiation after heart failure diagnosis among those
who did not use a β-blocker before (N =91,131) ... 102 Table 7.3 Determinants of β-blockera discontinuation among those who initiated a
β-blocker after heart failure diagnosis (N=32,989) ... 104 Table 7.4 Univariate analysis of determinants of β-blocker initiation after heart failure
diagnosis among those who had not used a β-blocker before (N =91,131) ... 109 Table 7.5 Univariate analysis of determinants of β-blocker discontinuation among those
who initiated a β-blocker after heart failure diagnosis (N=32,989) ... 112 Table 8.1 Characteristics of the seniors newly diagnosed with heart failure (HF) ... 127 Table 8.2 List of the 42 health deficits included in the frailty index ... 132 Table 8.3 Unadjusted effect of β-blocker exposure after HF diagnosis on mortality
according to age group ... 133 Table 8.4 Unadjusted effect of β-blocker exposure after HF diagnosis on mortality
according to age group and to exposure to an ACEi/ARB at time of HF diagnosis ... 134 Table 8.5 Unadjusted effect of β-blocker exposure after HF diagnosis on hospitalization
according to age group ... 135 Table 8.6 Unadjusted effect of β-blocker exposure after HF diagnosis on hospitalization
according to age group and to exposure to an ACEi/ARB at time of HF diagnosis ... 136 Table 9.1 Characteristics of the study population ... 149 Table 9.2 List of the 47 health deficits included in the frailty index ... 154
Table 9.3 Effect of exposure to nonsteroidal anti-inflammatory drugs (NSAIDs),
thiazolidinediones, nifedipine and non-dihydropyridines calcium channels blockers (CCB) on all-cause hospitalization ... 155
Liste des figures
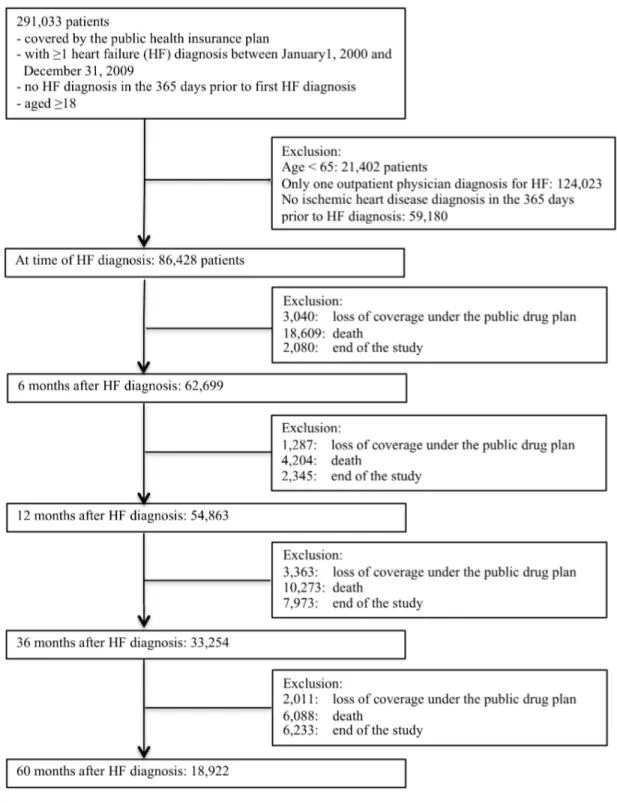
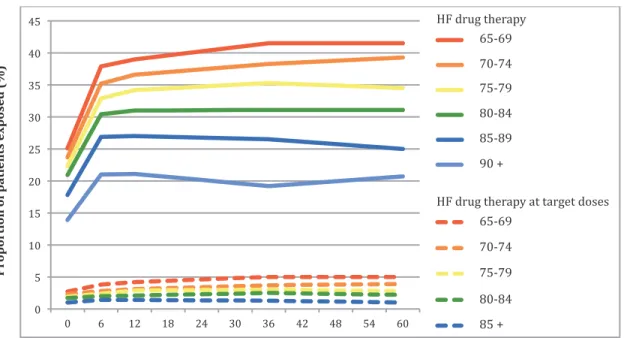
Figure 6.1 Flow chart ... 80 Figure 6.2 Proportion of seniors exposed to heart failure (HF) drug therapy and to drug
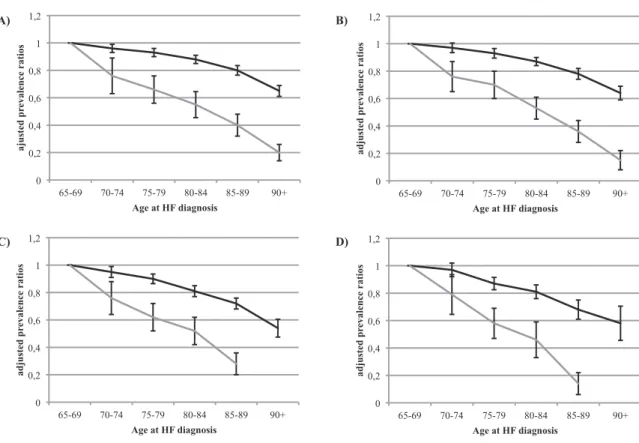
therapy at target doses at HF diagnosis and 6, 12, 36 and 60 months after HF diagnosis according to age. ... 81 Figure 6.3 Prevalence ratios of exposure to heart failure (HF) drug therapy and to drug
therapy at target doses, according to age ... 82 Figure 7.1: Selection of the study population ... 106 Figure 7.2 Probability of β-blocker initiation after heart failure diagnosis among those not
exposed to a β-blocker at time of HF diagnosis. ... 107 Figure 7.3 Probability of β-blocker discontinuation among patients who initiated a
β-blocker after heart failure diagnosis. ... 108 Figure 8.1 Selection of the study population ... 129 Figure 8.2 Effect of β-blocker exposure after HF diagnosis on mortality according to a) age
groups and b) exposure to an ACEI/ARB at time of HF diagnosis. ... 130 Figure 8.3 Effect of β-blocker exposure after HF diagnosis on hospitalization according to
a) age groups and b) exposure to an ACEI/ARB at time of HF diagnosis. ... 131 Figure 9.1 Selection of the study population ... 152 Figure 9.2 Effect of current exposure to nonsteroidal anti-inflammatory drugs (NSAIDs),
thiazolidinediones, nifedipine and non-dihydropyridines calcium channels blockers (CCB) on all-cause hospitalizations. ... 153
Liste des abréviations
95% CI 95% confidence interval
ACC-AHA American College of Cardiology- American Heart Association
ACEI Angiotensin converting enzyme inhibitor
AINS Anti-inflammatoire non-stéroïdien
AOR Adjusted odd ratio
aPR Adjusted prevalence ratio
ARA Antagoniste des récepteurs de l’angiotensine II
ARB Angiotensin II receptor blocker
ASA Aspirine
ATC Anatomical Therapeutic Chemical classification system
ATLAS Assessment of Treatment with Lisinopril and Survival
BCC Bloqueurs des canaux calciques
BEST Beta-blocker Evaluation of Survival Trial
CCB Calcium channel blocker
CHARM Candersartan in Heart Failure Assessment of Reduction in Mortality and
morbidity
CIM Classification Internationale des Maladies
CKD Chronic kidney disease
COPD Chronic obstructive pulmonary disease
CVD Cerebrovascular disease
ELITE Evaluation of Losartan in the elderly
GIS Guaranteed income supplement
GP General practitioner
HF Heart failure
HFpEF Heart failure with preserved left ventricular ejection fraction
HR Hazard ratio
IC 95% Intervalle de confiance à 95%
ICD Implantable cardioverter-defibrillator
ICD-9 International Classification of Diseases, 9th revision ICD-10 International Classification of Diseases, 10th revision
IECA Inhibiteur de l’enzyme de conversion de l’angiotensine
IHD Ischaemic heart disease
IQR Interquartile range
Med-Écho Système de maintenance et exploitation pour l’étude des données de la clientèle hospitalière
mg Milligramme
mm de Hg Millimètre de mercure
NYHA New York Heart Association
OR Odds ratio
PAD Peripheric atherosclerotic disease
RAMQ Régie de l’assurance maladie du Québec
RC Rapport de cotes
RCT Randomized controlled trials
RPa Rapport de prévalences ajusté
RPAM Régime public d’assurance médicaments
RR Risque relatif
RTi Rapport de taux d’incidence
SD Standard deviation
SENIORS Study of the Effects of Nebivolol Intervention on Outcomes and Rehospitalisation in Seniors with Heart Failure
TZD Thiazolidinediones
uPR Unadjusted prevalences ratio
Remerciements
Tout au long de mes études au doctorat, j’ai rencontré des personnes merveilleuses qui m’ont permis d’atteindre mes objectifs et qui ont rendu cette épreuve (oui, cela a été une épreuve à certains moments!…) mémorable et que je tiens à remercier.
Tout d’abord, je souhaite remercier mes parents, Yves et Michèle, qui m’ont toujours encouragée et supportée. Je vous remercie du fond du cœur et je vous aime.
Ensuite, je souhaite remercier ma directrice, Docteure Jocelyne Moisan. Merci Docteure Moisan de m’avoir accueillie à la Chaire, de m’avoir fait confiance avec mes mille et une questions de recherche et de m’avoir permis d’y répondre. Mais, surtout, merci pour le soutien bienveillant.
Aussi, merci à mon co-directeur, Docteur Paul Poirier, pour votre énergie incroyable, vos nombreux conseils et commentaires et pour le modèle de clinicien-chercheur que vous êtes. Merci au Docteur Jean-Pierre Grégoire pour votre œil de lynx, votre rigueur et vos commentaires toujours pertinents.
Merci aux professeures de la Chaire sur l’adhésion aux traitements, les docteures Line Guénette et Sophie Lauzier, pour votre disponibilité et vos encouragements.
Merci à Éric Demers pour ta rapidité et ton efficacité, mais surtout pour ta patience devant mes nombreuses demandes et mes ajouts de dernière minute.
Merci à tous ceux que j’ai côtoyés à l’Unité de recherche pour votre bonne humeur et votre disponibilité. Merci particulièrement à Gabriel, Amine, Hichem, Mariam, Carlotta, Richi et Arsène d’avoir rendu cette aventure des plus agréable.
Merci à Guillaume pour ta patience, ta confiance, tes encouragements, ton sourire et ta présence rassurante.
Merci à mes très chères amies, Anik, Émilie, Sandrine et Sophie, pour votre écoute lors de mes questionnements existentiels, pour nos virées un peu partout, mais surtout pour votre amitié incroyable.
Je souhaite aussi remercier les organismes qui m’ont offert des bourses de formation et qui m’ont ainsi permis de me consacrer à ma formation. Merci à l’Université de Sherbrooke (2010-2011), au Réseau québécois de recherche sur le vieillissement (2012-2013), à la Chaire de gériatrie de l’Université Laval (2013-2014) et au Fonds de recherche du Québec-Santé (bourse de formation au doctorat pour professionnel de la santé, 2014). Je souhaite aussi remercier les partenaires qui ont financé ce projet, soit la Chaire sur l’adhésion aux traitements de l’Université Laval et Servier Canada.
Finalement, merci aussi aux évaluateurs de cette thèse, les Docteurs Marie-Jeanne Kergoat, Pierre J. Durand, Line Guénette, Jocelyne Moisan et Paul Poirier, pour vos précieux commentaires.
Avant-propos
Cette thèse comporte quatre articles dont je suis l’auteur principal qui ont été soumis pour publication dans des revues avec comité de lecture. J’ai été responsable de la rédaction du protocole de recherche, de l’élaboration du plan des analyses statistiques, de l’interprétation des résultats et de la rédaction des trois articles suivants :
1. Catherine Girouard, Jean-Pierre Grégoire, Jeanne-Françoise Kayibanda, Paul Poirier, Éric Demers et Jocelyne Moisan. Underexposure of seniors to heart
failure drug therapy (article accepté le 20 octobre 2015 pour publication dans Journal of Population Therapeutics and Clinical Pharmacology).
2. Catherine Girouard, Jean-Pierre Grégoire, Paul Poirier, et Jocelyne Moisan.
Determinants of β-blocker initiation and discontinuation in a population-based cohort of seniors newly diagnosed with heart failure (article soumis à
International Journal of Cardiology).
3. Catherine Girouard, Jean-Pierre Grégoire, Paul Poirier, et Jocelyne Moisan. Effect
of contraindicated drugs for heart failure on mortality and hospitalization among seniors with heart failure (article soumis à Journal of the American Geriatrics Society).
Pour le dernier article, j’ai effectué les mêmes tâches que précédemment mentionnées, mais j’ai aussi réalisé les analyses statistiques.
4. Catherine Girouard, Émilie-Prudence Belley-Côté, Jean-Pierre Grégoire, Paul
Poirier et Jocelyne Moisan. Effect of β-blocker exposure on all-cause mortality
and hospitalization among seniors newly diagnosed with heart failure (article
INTRODUCTION DE LA THÈSE
CHAPITRE 1
PROBLÉMATIQUE
1.1 Problématique
L’insuffisance cardiaque est un problème de santé courant. Au Canada, on estime que 500 000 personnes en souffrent 1. Selon les prédictions démographiques, en 2036, le
nombre de personnes âgées de 65 ans et plus au Canada devrait osciller entre 9,9 millions et 10,9 millions, soit plus du double de la population observée en 2009 (4,7 millions) 2.
Puisque la prévalence de l’insuffisance cardiaque augmente avec l’âge, celle-ci est appelée à devenir plus élevée.
L’insuffisance cardiaque a un impact significatif sur la santé des individus qui en souffrent. La qualité de vie des patients diminue dans toutes les sphères étudiées 3. De plus, ils voient
leur espérance de vie diminuer considérablement. Cette condition est associée à une mortalité toutes causes confondues à un an de 12,6 %, ce qui est 3,6 fois plus élevé que dans la population générale. La mortalité atteint 28 % chez les individus aux stades les plus avancés 4.
Aux États-Unis, les coûts de santé attribuables à l’insuffisance cardiaque totalisaient un montant de 23 milliards de dollars américains en 2000 (soit 1,5 % du budget total de la santé). D’ailleurs, pour la majorité des pays industrialisés, 1,1 à 1,9 % des dépenses en santé sont attribuées à l’insuffisance cardiaque 5,6. Les hospitalisations sont responsables de la majorité des dépenses dues à l’insuffisance cardiaque puisqu’elles sont responsables de 65 % de celles-ci 7.
Plusieurs traitements pharmacologiques et non pharmacologiques peuvent diminuer la morbidité et la mortalité chez les patients souffrant d’insuffisance cardiaque. La plupart des patients nécessiteront un traitement à vie. Afin que les effets observés dans les essais cliniques soient reproduits dans la pratique, il est logique de penser que les patients doivent recevoir les traitements recommandés (médicaments et doses) par les lignes directrices de traitement. De telles lignes directrices ont été émises par la Société Canadienne de Cardiologie 8 et l’American College of Cardiology en association avec l’American Heart
Association (l’ACC-AHA) 9. Ces lignes directrices recommandent l’utilisation de
médicaments pour traiter les symptômes de la maladie, comme les diurétiques, et une combinaison de médicaments pour ralentir la progression de la maladie. Cette combinaison
doit être prescrite à tous les patients souffrant d’insuffisance cardiaque avec diminution de la fraction d’éjection du ventricule gauche. Elle comprend un β-bloqueur et un inhibiteur de l’enzyme de conversion de l’angiotensine (IECA). Les antagonistes des récepteurs de l’angiotensine II (ARA) et l’hydralazine accompagnée d’un dérivé nitré sont des options de traitement suggérées pour les patients ne pouvant tolérer les IECA. La combinaison de ces médicaments (un β-bloqueur en combinaison avec un IECA ou un ARA ou l’hydralazine en association avec un dérivé nitré) constitue le traitement standard de l’insuffisance cardiaque. Par ailleurs, les lignes directrices spécifient que certains médicaments ne devraient pas être pris par les patients souffrant d’insuffisance cardiaque puisqu’ils ont un impact négatif sur la fonction cardiaque. Ces médicaments sont les anti-inflammatoires non-stéroidiens (AINS), les thiazolidinediones, la nifédipine et les bloqueurs de canaux calciques non-dihydropyridines. Leur usage est qualifié de potentiellement inapproprié. Donc, pour qu’un patient soit considéré comme étant exposé à un traitement de qualité de l’insuffisance cardiaque, il doit être exposé au traitement standard en l’absence de médicaments potentiellement inappropriés.
Toutefois, il y a un manque de preuve au niveau des données probantes concernant le traitement de l’insuffisance cardiaque à prodiguer aux ainés. En effet, peu d’ainés sont inclus dans les essais cliniques 10 malgré le fait que la prévalence de la maladie soit très
élevée dans ce groupe et qu’ils contribuent de façon importante aux hospitalisations pour insuffisance cardiaque 11. Lorsque des résultats sont rapportés chez les ainés, ils
proviennent souvent d’analyses n’ayant pas la puissance statistique nécessaire afin de bien documenter l’effet des médicaments. Ainsi, soit elles sont effectuées sur un petit groupe de sujets, soit elles résultent d’analyses secondaires.
Donc, bien que les lignes directrices 8,9 recommandent que les ainés souffrant
d’insuffisance cardiaque soient exposés au traitement standard de l’insuffisance cardiaque, l’application de cette recommandation dans la pratique n’est pas connue. On ignore aussi l’effet de l’augmentation en âge chez les ainés sur l’application de cette recommandation et sur les facteurs associés à l’exposition au traitement standard chez les ainés. De plus, les ainés souffrant d’insuffisance cardiaque présentent de multiples comorbidités 12,13 pour
des options thérapeutiques 14. Ils sont donc à risque d’être exposés à des médicaments
potentiellement inappropriés en cas d’insuffisance cardiaque. Cependant, l’influence de l’exposition à ces médicaments sur les hospitalisations est insuffisamment documentée chez les ainés. Ces informations sont nécessaires afin de permettre aux cliniciens de juger des risques et des bénéfices d’exposer les ainés atteints d’insuffisance cardiaque à un traitement de qualité, c’est-à-dire tant au traitement recommandé par les lignes directrices, soit le traitement standard de l’insuffisance cardiaque, qu’aux médicaments potentiellement inappropriés.
1.2 Objectif général de la thèse et aperçu de sa présentation
L’objectif principal de cette thèse est d’estimer l’effet de l’usage d’un traitement de qualité sur les résultats de santé chez les patients âgés de 65 ans ou plus ayant eu un premier diagnostic d’insuffisance cardiaque entre le 1er janvier 2000 et le 31 décembre 2009 au
Québec.
Dans cette thèse, nous présentons tout d’abord, au chapitre 2, l’état des connaissances sur l’insuffisance cardiaque. Par la suite, nous abordons les particularités de l’état de santé des ainés au chapitre 3. Nous présentons les objectifs spécifiques de la thèse au chapitre 4. Afin de répondre à ces objectifs, nous avons effectué quatre études. Puisque nous utilisons les bases de données administratives de la Régie de l’assurance maladie du Québec (RAMQ) comme source de données pour chacune de ces études, nous présentons d’abord le contenu de ces banques au chapitre 5. Ensuite, nous répondons à l’objectif de la thèse en deux parties. La première partie est consacrée au traitement standard de l’insuffisance cardiaque chez les ainés. Cette partie, présentée aux chapitres 6 à 8, inclus trois études qui touchent la description de l’exposition au traitement standard, les facteurs associés à l’exposition aux β-bloqueurs et l’effet de l’exposition aux β-bloqueurs sur la mortalité et les hospitalisations chez les ainés souffrant d’insuffisance cardiaque. La deuxième partie touche l’effet de l’exposition aux médicaments potentiellement inappropriés en insuffisance cardiaque sur la les hospitalisations. L’étude pour cette partie est présentée au chapitre 9. Finalement, en conclusion de la thèse, nous présentons la synthèse des résultats, les forces et les faiblesses des études réalisées, une réflexion sur l’implication de nos résultats et les perspectives futures.
Puisque ce document porte sur la qualité du traitement de l’insuffisance cardiaque et son effet sur les patients âgés de 65 ans et plus, nous souhaitons clarifier certains termes qui sont utilisés tout au long de cette thèse. Tout d’abord, nous utilisons le terme «ainé» afin de référer aux personnes âgées de 65 ans et plus. Lorsque nous souhaitons référer à des patients d’un groupe d’âge spécifique, nous précisons les intervalles de ce groupe d’âge sauf pour les patients âgés de 85 ans et plus auxquels nous référons en utilisant le terme «les plus âgés parmi les ainés» (traduction libre pour le terme oldest old communément utilisé dans la littérature anglosaxone).
CHAPITRE 2
2.1 L’insuffisance cardiaque
2.1.1 Définition et manifestations
L’insuffisance cardiaque est une maladie chronique définie comme étant «un état pathophysiologique dans lequel une anomalie de la fonction cardiaque est responsable de l’incapacité du cœur à pomper le sang à un taux correspondant aux besoins métaboliques des tissus» 15. L’insuffisance cardiaque peut se présenter avec une fraction d’éjection du
ventricule gauche diminuée ou préservée 9. Lorsque la fraction d’éjection est préservée, il
peut y avoir ou non une dysfonction diastolique. La fonction diastolique peut être quant à elle préservée, comme dans les cas dus aux maladies du péricarde, aux conditions à haut débit cardiaque (anémie, thyrotoxicose et grossesse) et aux maladies valvulaires (régurgitation mitrale, sténose mitrale et régurgitation aortique) 16. Par contre, la fonction
diastolique est fréquemment altérée.
Les symptômes de l’insuffisance cardiaque peuvent découler de la congestion des lits vasculaires pulmonaires (dyspnée et orthopnée) ou systémiques (œdème périphérique et congestion hépatique, entre autres) ou du faible débit cardiaque (fatigue, faible tolérance à l’effort) 9. Le degré de limitation fonctionnelle causé par les symptômes d’insuffisance
cardiaque est souvent rapporté selon l’échelle de la New York Heart Association (NYHA) 9.
Cette classification comporte quatre classes et les patients sont classifiés dans l’une de celles-ci selon le niveau d’activité auquel les symptômes surviennent. Ainsi, les symptômes peuvent survenir à un niveau d’effort qui limiterait aussi un individu ne souffrant pas d’insuffisance cardiaque (classe I), durant des activités d’intensité modérée (classe II), durant des activités d’intensité légère (classe III) ou au repos (classe IV) 9.
Afin de mettre en évidence le caractère évolutif de l’insuffisance cardiaque, l’ACC-AHA a développé un système en stades 9. Il est composé de quatre stades (de A à D) représentant deux étapes où les buts du traitement sont différents : les patients aux stades A et B ont un risque élevé de développer de l’insuffisance cardiaque alors que ceux qui sont aux stades C et D souffrent d’insuffisance cardiaque qui doit être traitée. Les patients du stade A ont des facteurs de risque d’insuffisance cardiaque mais n’ont pas d’anomalie structurelle cardiaque ou de symptômes d’insuffisance cardiaque. Ceux au stade B ont développé une anomalie structurelle cardiaque mais ne présentent aucun symptôme d’insuffisance cardiaque.
L’apparition de symptômes d’insuffisance cardiaque correspond au stade C, le troisième stade. Lorsque l’insuffisance cardiaque devient réfractaire et que le patient nécessite des traitements spécialisés (par exemple une transplantation cardiaque ou la nécessité d’agents inotropes en continu) ou des soins de fin de vie, le patient est alors considéré comme étant au dernier stade, le stade D.
2.1.2 Facteurs de risque et prévention
Les principaux facteurs de risque de l’insuffisance cardiaque sont la maladie cardiaque athérosclérotique (ou maladie cardiaque ischémique) 17,18, le tabagisme 17, l’hypertension
artérielle 17,18, l’obésité 17, le diabète de type 2 17,18 et les valvulopathies 17. La maladie
cardiaque athérosclérotique et l’hypertension artérielle sont les facteurs de risque majeurs dans les pays occidentaux. D’ailleurs, la maladie cardiaque athérosclérotique est responsable des deux tiers des cas d’insuffisance cardiaque 18. Aussi, une tension artérielle
supérieure à 160/100 mm de Hg double le risque de développer de l’insuffisance cardiaque par rapport à une tension artérielle dite normale (140/90 mm de Hg) 19. De plus,
l’hypertension artérielle agit en synergie avec d’autres facteurs de risque. En effet, suite à un infarctus du myocarde, la présence d’hypertension artérielle augmente de façon
significative le risque d’insuffisance cardiaque 20. Par contre, le traitement de
l’hypertension artérielle diminue les risques d’insuffisance cardiaque. En effet, selon les résultats d’une méta-analyse 21, le traitement de l’hypertension artérielle diminue de 39 %
le risque de développer de l’insuffisance cardiaque chez des sujets âgés de 80 ans et plus. Djousse et coll. ont suivi pendant une période moyenne de 22,4 ans une cohorte composée de 20 900 hommes pour évaluer l’impact des habitudes de vie sur la survenue de l’insuffisance cardiaque 22. Les six habitudes de vie évaluées par les chercheurs étaient le
maintien d’un poids sain, de l’exercice régulier, une prise d’alcool modérée, l’absence de tabagisme, une consommation quotidienne de fruits et de légumes et une consommation de céréales au déjeuner. Ceux mettant en pratique au moins quatre de ces six mesures avaient un risque plus faible (risque à vie de 10 %) de développer de l’insuffisance cardiaque que ceux qui n’appliquaient aucune de ces six habitudes de vie (risque à vie de 21 %).
2.1.3 L’insuffisance cardiaque en chiffres : incidence et prévalence
Le pourcentage d’individus souffrant de plusieurs maladies chroniques augmente avec l’âge et l’insuffisance cardiaque n’est pas une exception. Dans la cohorte de Framingham, la prévalence d’insuffisance cardiaque chez les individus âgés entre 50 et 59 ans était de 8/1000 tandis qu’elle était de 66/1000 dans le groupe âgé entre 80 et 89 ans 23. Puisque,
selon les projections de l’Institut de la Statistique du Québec, la population du Québec devrait atteindre 9,2 millions d’individus en 2056 et que le poids démographique des ainés passera de 14 % en 2006 à 28 % en 2056 2, la prévalence de l’insuffisance cardiaque est
aussi appelée à augmenter. Alors que la prévalence est la proportion d’individus ayant la maladie à un moment précis, l’incidence est le nombre de nouveaux cas d’une maladie (l’insuffisance cardiaque dans ce cas-ci) dans une période de temps spécifique. Tout comme la prévalence, l’incidence de l’insuffisance cardiaque augmente avec l’âge. D’ailleurs, 85 % des nouveaux diagnostics d’insuffisance cardiaque sont posés chez les ainés 24. Aussi, une analyse de la cohorte de Framingham 19, rapporte une incidence de
l’insuffisance cardiaque augmentant avec l’âge. En fait, dans cette cohorte, l’incidence annuelle chez les hommes était de 2/1000 à 35 ans et de 12/1000 chez les individus âgés entre 65 et 94 ans 19. Ces données sont pour le syndrome de l’insuffisance cardiaque en général. Or, les symptômes d’insuffisance cardiaque peuvent se présenter avec une diminution de la fraction d’éjection du ventricule gauche mais aussi en présence d’une fraction d’éjection du ventricule gauche préservée. La prévalence de cette deuxième forme varie entre 34 % 25 et 55 % 26 chez les ainés souffrant d’insuffisance cardiaque. Ces deux
conditions sont distinctes et ne correspondent pas à un continuum 27,28. En effet, il a été
estimé qu’entre 7 % 28 et 18 % 27 des patients présentant initialement de l’insuffisance
cardiaque avec fraction d’éjection préservée développaient une diminution de la fraction d’éjection durant une période variant entre quatre et sept ans 27,28. La survenue d’une
atteinte cardiaque tel un infarctus aigu du myocarde durant la période entre la mesure de base et la découverte de la diminution de la fraction d’éjection du ventricule gauche était un prédicteur de la diminution de la fonction du ventricule gauche 27,28.
2.1.4 Le fardeau de l’insuffisance cardiaque
Suite au diagnostic d’insuffisance cardiaque, il y a très souvent une détérioration de la capacité fonctionnelle avec le temps 9. Il est fréquent que la sévérité des symptômes fluctue
et ce, même en l’absence de changement de médication. L’insuffisance cardiaque a un effet important sur la qualité de vie, son parcours est parsemé d’hospitalisations et elle mène, ultimement, à une diminution de la survie. Aussi, elle a un impact sur les fonctions cognitives. Finalement, l’insuffisance cardiaque est aussi associée à des coûts importants pour la société.
2.1.4.1 Impact de l’insuffisance cardiaque sur la qualité de vie
La qualité de vie des patients souffrant d’insuffisance cardiaque est diminuée dès les premiers stades de la maladie comparativement à celle d’une population ne souffrant pas d’insuffisance cardiaque. Holzapfel et coll. ont observé une détérioration dans sept dimensions de la qualité de vie (la perception de santé, la fonction physique, la fonction sociale, la santé mentale, la douleur, la vitalité et les rôles physique et émotionnel) avec la progression de la maladie 29.Cette diminution de la qualité de vie est telle que, lorsque des
chercheurs soumettent des patients à des situations hypothétiques, certains se disent prêts à risquer un décès induit par un effet indésirable des médicaments afin de ressentir une amélioration de leur condition 30. De plus, une diminution de la qualité de vie chez les
patients souffrant d’insuffisance cardiaque est aussi un prédicteur de mortalité et d’hospitalisation 31.
2.1.4.2 Impact de l’insuffisance cardiaque sur les hospitalisations
L’insuffisance cardiaque est responsable de la majorité des hospitalisations chez les ainés 11. Chez les ainés souffrant d’insuffisance cardiaque aux États-Unis, le taux
d’hospitalisation en 2006 était de 22,9/1000 chez les hommes et de 19,6/1000 chez les femmes 32. De plus, 8 % des patients de ce groupe d’âge nécessitent une réadmission dans les six mois suivant l’hospitalisation initiale 33. Aussi, l’insuffisance cardiaque est une
cause fréquente de consultation à l’urgence pour les patients demeurant dans un centre hospitalier de soins de longue durée (elle est la raison de 16% des consultations à la salle d’urgence) 34. Les hospitalisations sont des marqueurs de mauvais pronostic. En effet, la
mortalité augmente suite à des hospitalisations fréquentes ou prolongées 35-38.
2.1.4.3 Impact de l’insuffisance cardiaque sur la mortalité
La mortalité est considérable chez les sujets souffrant d’insuffisance cardiaque. Dans la cohorte de Framingham, la survie médiane suite à un diagnostic d’insuffisance cardiaque
était de 1,7 an chez les hommes et 3,2 ans chez les femmes 23. Seulement 25 % des hommes
et 38 % des femmes étaient vivants 5 ans après le diagnostic 23. La différence de survie
entre les sexes était significative malgré l’ajustement pour l’âge 39. Dans une étude
effectuée en Ontario, parmi 9 000 patients hospitalisés pour un nouveau diagnostic d’insuffisance cardiaque, la période de temps médiane entre ce diagnostic et le décès était de 2,4 ans 5. Les pourcentages de patients décédés un an et cinq ans suite au diagnostic étaient de 33 % et 68 %, respectivement 5. D’ailleurs, les taux de mortalité dus à
l’insuffisance cardiaque sont plus élevés que ceux de la plupart des cancers 40. Des résultats
similaires ont été rapportés aux États-Unis 41. Il est estimé que la mortalité chez les patients
souffrant d’insuffisance cardiaque est causée à part égale par une mort subite et par l’aggravation de l’insuffisance cardiaque 42. Parmi les facteurs associés à une augmentation
du risque de mortalité chez les ainés, il y a l’âge élevé (plus marqué chez les 75 ans et plus), être de sexe masculin, souffrir de diabète et avoir une diminution de la fraction d’éjection du ventricule gauche (surtout si elle est inférieure à 30 %) 43. Aussi, parmi les
facteurs de risque de mortalité chez les patients souffrant d’insuffisance cardiaque, notons que la fragilité est un facteur indépendant de prédiction de la mortalité 44,45 et que les
modèles de prédiction du risque de mortalité l’incorporant prédisent avec davantage de précision le risque de mortalité que la classe fonctionnelle selon le NYHA 46.
2.1.4.4 Impact de l’insuffisance cardiaque sur les fonctions cognitives
L’insuffisance cardiaque est associée à une détérioration des fonctions cognitives. Zuccala et coll. rapportent que la prévalence de troubles cognitifs légers se situe entre 53 et 58 % chez les patients souffrant d’insuffisance cardiaque légère à modérée 47. Dans une revue
systématique de la littérature incluant 22 études, Vogels et coll. 48 ont estimé que le risque
de présenter des troubles cognitifs est augmenté de 62 % chez les patients souffrant d’insuffisance cardiaque comparativement aux contrôles normaux. Les fonctions cognitives atteintes sont, en ordre de fréquences décroissantes, la mémoire, l’attention, la capacité à résoudre des problèmes, la capacité d’apprentissage et le temps de réaction 49. Parmi les
facteurs prédictifs de troubles cognitifs chez les patients souffrant d’insuffisance cardiaque, Vogels et coll. 48 ont identifié le niveau d’intelligence, le stade de l’insuffisance cardiaque
2.1.4.5 Impact de l’insuffisance cardiaque sur les coûts pour la société
L’insuffisance cardiaque est associée à des coûts importants. En effet, dans les pays développés, l’insuffisance cardiaque est responsable de 1,1 à 1,9 % des dépenses en santé 6.
Parmi ces dépenses, 50 % à 74 % sont dues aux hospitalisations ou à des soins dans des centres hospitaliers de soins de longue durée 6. En 2006, aux États-Unis, les coûts totaux
associés à la prise en charge d’un patient souffrant d’insuffisance cardiaque pour une année étaient estimés à près de 11 000 $ US 6. Ces coûts incluent les soins ambulatoires, les
hospitalisations et les coûts des médicaments. Toujours aux États-Unis, les coûts des traitements médicamenteux des ainés souffrant d’insuffisance cardiaque sont estimés à 3 823 $ US annuellement. D’ailleurs, Chen et coll. 50 ont identifié que l’âge plus élevé
(50-64 ans et 65 ans et plus comparativement à moins de 50 ans), la prise d’un plus grand nombre de médicaments (dix et plus) et un nombre élevé de comorbidités étaient tous des facteurs associés à des coûts plus importants du traitement de l’insuffisance cardiaque. Lors d’une hospitalisation pour insuffisance cardiaque au Canada, le coût moyen par patient pour chaque jour d’hospitalisation est de 911 $ CAN 24. Ce coût varie entre 779 $ CAN
pour les patients âgés de 85 ans et plus et 1 339 $ CAN pour les patients âgés entre 20 et 49 ans 24. En effet, alors que les durées de séjour sont plus longues chez les patients très âgés (12 jours comparativement à 8 pour les patients âgés entre 20 et 49 ans), les patients âgés sont moins susceptibles d’être admis dans des unités spécialisées, de subir des procédures ou des chirurgies cardiovasculaires, d’être transférés dans un autre hôpital de soins aigus et de recevoir des soins par un interniste ou un cardiologue, qui sont toutes des interventions associées à des coûts plus élevés 24.
L’insuffisance cardiaque a donc des répercussions importantes tant pour l’individu qui en est atteint (diminution de la qualité de vie, augmentation des hospitalisations et du risque de décès) que pour la société (coûts importants associés au traitement de l’insuffisance cardiaque). Heureusement, des traitements pharmacologiques dont l’efficacité a été démontrée existent afin de diminuer le fardeau de l’insuffisance cardiaque.
2.2 Les traitements de l’insuffisance cardiaque recommandés par les
lignes directrices
Selon les lignes directrices du traitement de l’insuffisance cardiaque 8,9,51, un traitement de
qualité est constitué des médicaments diminuant les risques de mortalité et d’hospitalisation et ne comprend pas de médicaments pouvant aggraver l’insuffisance cardiaque (les médicaments potentiellement inappropriés en insuffisance cardiaque). Ces lignes directrices sont régulièrement mises à jour. Les traitements médicamenteux présentés dans cette section ont été recommandés par l’ACC-AHA en 2009 9 et 2013 51 (dernières lignes
directrices parues) pour le traitement des patients souffrant d’insuffisance cardiaque avec une diminution de la fraction d’éjection du ventricule gauche. En effet, il n’y a pas, à ce jour, de traitement dont l’efficacité a été démontrée pour le traitement des patients souffrant d’insuffisance cardiaque avec fonction du ventricule gauche préservée 52. Pour ces derniers,
les lignes directrices ne recommandent pas de traitement spécifique, mais recommandent plutôt le traitement des comorbidités sous-jacentes, soit le contrôle de la fréquence ventriculaire en présence d’arrythmie auriculaire, le traitement de l’hypertension artérielle, la revascularisation s’il y a présence d’ischémie et le soulagement de la congestion pulmonaire et des oedèmes périphériques 9.
Les recommandations présentées dans cette section sont divisées en trois classes 9. La
classe I inclut les traitements dont les bénéfices surpassent nettement les risques associés à l’exposition. La classe II inclut les traitements dont les bénéfices dépassent les risques, mais pour lesquels davantage de données seraient nécessaires. Finalement, la classe III inclut les traitements dont les risques dépassent les bénéfices. Les recommandations présentent aussi le niveau de preuves sur lequel elles sont basées (niveau de preuve A : les données proviennent de méta-analyses ou de multiples études cliniques à répartition aléatoire; niveau de preuve B : les données proviennent d’une seule étude clinique à répartition aléatoire ou d’études cliniques à répartition non aléatoire; niveau de preuve C : les données proviennent de consensus d’experts, d’études de cas ou de normes de traitement) 9.
2.2.1 Les β-bloqueurs
Tout d’abord, les β-bloqueurs sont recommandés dès le stade B de l’insuffisance cardiaque (stade dans lequel les patients présentent du remodelage ou des anomalies de la structure du ventricule gauche en l’absence de symptômes d’insuffisance cardiaque) suite à un infarctus aigu du myocarde (classe I, niveau de preuve A) ou, en l’absence d’un antécédent d’infarctus du myocarde, si la fraction d’éjection du ventricule gauche est diminuée (classe I, niveau de preuve C) 9. Ils sont aussi recommandés dans le traitement de routine de
l’insuffisance cardiaque chez tous les patients ayant des symptômes d’insuffisance cardiaque (stades C et D) et une diminution de la fraction d’éjection du ventricule gauche (classe I, niveau de preuve A) 9. Cette recommandation est présente dans les lignes
directrices depuis 2001 53. Elle s’appuie sur les résultats d’études cliniques à répartition
aléatoire dans lesquelles il a été observé que l’exposition au bisoprolol, au carvedilol ou au métoprolol diminuait le risque de mortalité. La recommandation ne peut être étendue à l’ensemble des β-bloqueurs puisqu’une augmentation du risque de décès a été rapportée chez les patients souffrant d’insuffisance cardiaque exposés au bucindolol 54. Les effets
indésirables les plus fréquents des β-bloqueurs sont l’hypotension (présente chez un maximum de 27 % des patients exposés), les bradycardies (10 % des patients exposés), la fatigue (10 % des patients exposés), les cauchemars (10 % des patients exposés), les étourdissements (10 % des patients exposés) et les bronchospasme (1% des patients exposés) 55.
2.2.2 Les inhibiteurs de l’enzyme de conversion de l’angiotensine (IECA)
Les β-bloqueurs réduisent davantage la mortalité et la morbidité lorsqu’ils sont pris avec un IECA 9. C’est pourquoi il est important de combiner précocement les deux classes de
médicaments. Les IECA sont recommandés dès le stade B de l’insuffisance cardiaque (stade dans lequel les patients présentent du remodelage ou des anomalies de la structure du ventricule gauche en l’absence de symptômes d’insuffisance cardiaque) suite à un infarctus aigu du myocarde (classe I, niveau de preuve A) ou, en l’absence d’un antécédent d’infarctus du myocarde si la fraction d’éjection du ventricule gauche est diminuée (classe I, niveau de preuve A) 9. Ils sont aussi recommandés dans le traitement de routine de
l’insuffisance cardiaque chez tous les patients ayant des symptômes d’insuffisance cardiaque (stades C et D) et une diminution de la fraction d’éjection du ventricule gauche
(classe I, niveau de preuve A) 9. Les IECA font partie du traitement de routine de
l’insuffisance cardiaque et sont recommandés depuis 1995 dans les lignes directrices de traitement 56. Ils ont un effet favorable sur la survie et leur usage diminue la fréquence des
hospitalisations. Les effets indésirables fréquents des IECA sont la toux (6 % des patients exposés), l’hypotension artérielle (5 % des patients exposés), l’hyperkaliémie (4 % des patients exposés) et une augmentation de la créatinine sérique (10 % des patients exposés) 55. Étant donné ce profil d’effets favorables, le traitement avec un IECA devrait
être débuté précocement à moins de contre-indications (angioedème, choc cardiogénique et insuffisance rénale anurique provoquée par l’IECA). En présence de telles contre-indications, un traitement alternatif doit être envisagé 9.
2.2.3 Les antagonistes des récepteurs de l’angiotensine
Malgré que les IECA demeurent le traitement de choix des patients souffrant d’insuffisance cardiaque au stade C, les ARA peuvent être utilisés par les patients ne pouvant tolérer les IECA à cause d’effets indésirables (classe I, niveau de preuve A) ou, en première intention de traitement, lorsqu’ils sont déjà utilisés par les patients pour une autre indication que l’insuffisance cardiaque (classe II, niveau de preuve A) 9. En effet, les ARA diminuent les
hospitalisations et la mortalité chez leurs utilisateurs 9. Les effets indésirables des ARA sont l’angioedème et l’hypotension artérielle 55. Les ARA sont recommandés depuis 2001 dans les lignes directrices 53.
2.2.4 L’association d’hydralazine et d’isosorbide dinitrate
L’hydralazine est un vasodilatateur artériel ayant peu d’effet sur le tonus veineux et sur les pressions de remplissage cardiaque. L’association avec l’isosorbide dinitrate permet une vasodilatation à la fois artérielle et veineuse. Ce traitement en association a un effet moindre que les IECA sur l’amélioration de la survie, sauf chez les patients de race afro-américaine. L’association d’hydralazine et d’isosorbide dinitrate ne doit donc pas être la première option à considérer pour le traitement de l’insuffisance cardiaque. Malgré que l’efficacité de cette combinaison ait été peu étudiée, elle peut être considérée chez les patients ne pouvant tolérer les IECA et les ARA (classe II, niveau de preuve C) 9.
L’association d’hydralazine et d’isosorbide dinitrate est recommandée dans les lignes directrices comme alternative aux IECA et aux ARA depuis 1995 56. Les effets indésirables
fréquents avec l’hydralazine sont les céphalées, les étourdissements, les palpitations, la tachycardie et l’hypertension artérielle paradoxale 55. Les effets indésirables fréquents avec
les nitrates sont les céphalées, l’hypotension artérielle et la tachycardie réflexe 55.
2.2.5 Les médicaments potentiellement inappropriés chez les personnes souffrant d’insuffisance cardiaque
Certains médicaments devraient être évités chez un patient souffrant d’insuffisance cardiaque 57. Ces médicaments sont les AINS, les thiazolidinediones, la nifédipine et les
bloqueurs des canaux calciques non-dihydropyridines.
2.2.5.1 Les anti-inflammatoires non-stéroïdiens
Les médicaments de la classe des AINS inhibent la cyclooxygénase, une enzyme nécessaire à la transformation de l’acide arachidonique en prostaglandine et en thromboxane 58. Elle
prend deux formes : 1) la cyclooxygénase-1, qui est présente dans plusieurs cellules dont les plaquettes, et 2) la cyclooxygénase-2, qui est induite par les cytokines inflammatoires de plusieurs types de cellules 58. En inhibant les cyclooxygénases, les AINS exercent un effet
anti-inflammatoire mais risquent de déclencher plusieurs effets indésirables : 1) une diminution de la filtration glomérulaire, 2) une augmentation de la tension artérielle systémique, 3) des saignements (particulièrement des saignements gastro-intestinaux) et, 4) de l’oedème 58. Malgré ces effets indésirables, les AINS sont fréquemment utilisés par les
ainés. En effet, 26,7 % des ainés en Alberta ont utilisé au moins un anti-inflammatoire durant une période de six mois 59. Cette utilisation n’est pas banale parce qu’il existe
actuellement des preuves que l’exposition aux AINS augmente le risque de développer de l’insuffisance cardiaque 60 et qu’elle augmente le risque d’évènements de santé indésirables
pour ceux souffrant d’insuffisance cardiaque. D’ailleurs, Van den Hondel et coll. 61 ont
estimé l’effet de l’exposition aux AINS sur les paramètres échographiques chez des individus demeurant dans la communauté et n’ayant pas d’insuffisance cardiaque. Ils ont observé que l’utilisation d’AINS était associée à une rétention liquidienne et à une augmentation des dimensions systoliques et diastoliques du ventricule gauche.
Gislason et coll. 62 ont étudié le risque de décès et d’hospitalisation pour infarctus du
myocarde ou pour insuffisance cardiaque associés à la prise d’AINS suite à une première hospitalisation pour insuffisance cardiaque. Parmi les 107 092 patients inclus dans leur
étude (âge moyen de 78 ans), 36 354 (33,9 %) ont reçu au moins une prescription pour un AINS suite à l’hospitalisation. Comparativement aux patients non exposés aux AINS, les patients y étant exposés avaient un risque de décès (RR variant entre 1,22 et 2,08, selon l’AINS utilisé) et d’hospitalisation (RR variant entre 1,16 et 1,40, selon l’AINS utilisé) plus élevé. Feenstra et coll. 63 ont aussi remarqué que lorsque les patients sont exposés à un
AINS suite au diagnostic d’insuffisance cardiaque, leur risque d’hospitalisation est augmenté.
Trois études ont été menée afin de déterminer si certains AINS étaient plus sécuritaires que d’autres 62,64,65. Gislason et coll. 62 ont évalué le risque de décès et d’hospitalisation selon le
type d’AINS utilisé. Pour ce faire ils ont comparé le risque de décéder ou d’être hospitalisé parmi les exposés à chacun des AINS comparativement à l’absence d’exposition. Peu importe l’AINS utilisé, les risques de décéder ou d’être hospitalisé étaient augmentés. De plus, le risque augmentait avec l’augmentation des doses 62. Hudson et coll. 64,65 ont quant à eux comparé les différents AINS non sélectifs avec le célécoxib (un AINS inhibant seulement la COX-2). Ils ont démontré que le célécoxib est associé à un risque plus faible de décès 64 et de réadmission pour de l’insuffisance cardiaque que les autres AINS 64,65.
Donc, bien que les AINS soient utilisés de façon fréquente, ils sont associés à un risque augmenté de décès et d’hospitalisation chez les patients souffrant d’insuffisance cardiaque et doivent donc être évités par ces patients.
2.2.5.2 Les thiazolidinediones
Les médicaments de la classe des thiazolidinediones, la pioglitazone et la rosiglitazone, sont des agonistes du récepteur activé par les proliférateurs de peroxysomes ϒ. Ces médicaments augmentent la sensibilité des cellules à l’insuline et permettent ainsi de contrôler la glycémie tout en étant associés à un faible risque d’hypoglycémie. De 2,5 à 10,7 % des patients exposés à une thiazolidinedione développent des oedèmes périphériques 66-69. Aussi, l’utilisation de thiazolidinedione est associée à une augmentation
du volume intravasculaire 55 pouvant causer des signes et des symptômes d’insuffisance
cardiaque chez les patients diabétiques avec une diminution de la réserve cardiaque. D’ailleurs, les auteurs de deux méta-analyses ont démontré une augmentation du risque de développer de l’insuffisance cardiaque lorsque exposé à la pioglitazone 70,71 ou à la
rosiglitazone 72. Malgré ce risque augmenté, l’exposition des patients diabétiques souffrant
d’insuffisance cardiaque aux thiazolidinediones est fréquente. Seong et coll. 73 ont calculé
que 10,4 % des patients diabétiques âgés entre 65 et 99 ans souffrant d’insuffisance cardiaque en Corée étaient exposés à une thiazolidinedione alors que cette proportion était plus faible pour les patients ne souffrant pas d’insuffisance cardiaque (8,8 %). Ils ont mis en évidence que le risque de prescription d’une thiazolidinedione était 9 % plus élevé pour les patients diabétiques souffrant d’insuffisance cardiaque que chez ceux n’en souffrant pas (rapport de cotes [RC] 1,09, intervalle de confiance à 95 % [IC 95 %] : 1,05-1,14). Aussi, Masoudi et coll. 74 ont remarqué une augmentation de l’exposition aux thiazolidinediones
chez les patients diabétiques souffrant d’insuffisance cardiaque entre 1998-1999 (7,2 %) et 2000-2001 (16,1 %).
Peu de données sont disponibles quant au risque d’exposition aux thiazolidinediones chez les patients souffrant d’insuffisance cardiaque. Ce peu de preuve rend difficile l’estimation du risque réel associé à l’exposition aux thiazolidinediones chez les patients souffrant d’insuffisance cardiaque. Ainsi, Masoudi et coll. 75 ont évalué les risques de l’exposition
aux thiazolidinediones sur la mortalité et les hospitalisations chez les patients suite à une hospitalisation pour de l’insuffisance cardiaque. Ils ont observé que le risque de mortalité toutes causes à un an était plus faible chez les utilisateurs de thiazolidinediones (ou de metformine) que chez les non-utilisateurs (rapport de taux d’incidence [RTi] 0,87, IC 95 % : 0,80-0,94). Ce risque n’était pas modifié par la valeur de la fraction d’éjection du ventricule gauche. Par contre, le risque de réhospitalisation pour de l’insuffisance cardiaque était plus élevé, mais de façon non statistiquement significative (RTi 1,06, IC 95 % : 1,00-1,09), alors que le risque d’hospitalisation toutes causes n’était pas augmenté chez les utilisateurs de thiazolidinediones. De leur côté, Tang et coll. 76 ont étudié l’effet de
l’exposition à une thiazolidinedione chez des patients diabétiques souffrant d’insuffisance cardiaque avec fraction d’éjection abaissée (c’est-à-dire ≤ 45%) durant une période de 12 mois. Parmi 111 patients exposés à une thiazolidinedione, 19 (17,1 %) ont présenté de la rétention liquidienne. Parmi ces 19 patients, 2 ont présenté de l’œdème pulmonaire et 5 ont dû être hospitalisés pour le traitement de leur rétention liquidienne 76.
2.2.5.3 La nifédipine
La nifédipine fait partie de la classe des bloqueurs de canaux calciques dihydropyridines. Les médicaments de cette classe ont un effet neurohumoral qui s’exerce surtout sur les muscles lisses vasculaires. Ils diminuent les résistances vasculaires systémiques tout en ayant peu d’effet inotrope et chronotrope 77. Par contre, la nifédipine a un effet inotrope
négatif 57 alors que les bloqueurs des canaux calciques de deuxième génération (amlodipine
et félodipine) sont davantage vasosélectifs et moins cardiodépresseurs 78. Les effets
hémodynamiques de la nifédipine ont été comparés à ceux du captopril 79 chez 18 patients
souffrant d’insuffisance cardiaque. Les améliorations de la tolérance à l’effort et de la classe fonctionnelle lors de l’exposition au captopril n’ont pas été retrouvées lors de l’exposition au nifédipine 79. D’ailleurs, Elkayam et coll. 80 ont démontré, suite à une étude
sur 51 patients souffrant d’insuffisance cardiaque, que l’exposition à la nifédipine, comparativement à l’exposition à l’isosorbide dinitrate, était associée à une détérioration clinique et à une augmentation des épisodes d’hospitalisation. Par contre, ces effets négatifs ne sont pas présents chez les patients utilisant des bloqueurs de canaux calciques dihydropiridines de la deuxième génération. Un étude clinique à répartition aléatoire a étudié l’effet de la félodipidine sur la tolérance à l’exercice, la fonction du ventricule gauche et la qualité de vie en plus d’évaluer la sécurité associée à son utilisation chez des patients souffrant d’insuffisance cardiaque 81. Dans cette étude effectuée entre 1991 et
1994, 450 patients ont été inclus. Les résultats ont démontré que la félodipine n’avait pas d’effet sur la tolérance à l’exercice ou sur la qualité de vie. Une légère amélioration de la fonction du ventricule gauche (2,1 ± 7,0 %) était retrouvée trois mois après le début du traitement mais ne persistait pas 12 mois plus tard. Par contre, la survenue d’hospitalisation et la mortalité n’étaient pas plus fréquentes dans le groupe de patients exposés à la félodipine. Aussi, l’effet de l’exposition à l’amlodipine chez les patients souffrant d’insuffisance cardiaque sévère (NYHA III-IV) avec une fraction d’éjection du ventricule gauche abaissée (< 30 %) a été évaluée dans une étude clinique à répartition aléatoire 82.
Dans cette étude de 1 153 patients, l’utilisation d’amlodipine avait un effet neutre sur la morbidité cardiovasculaire et sur la mortalité. Un avantage sur la mortalité a été retrouvé dans un sous-groupe de personnes exposées à l’amlodipine n’ayant pas d’antécédent d’angine (RTi 0,59, IC 95 % : 0,44-0,81). Une deuxième étude a démontré qu’il n’y avait
pas de différence entre la cause de décès entre les individus exposés au placebo et ceux exposés à l’amlodipine et que les individus exposés à l’amlodipine dont la cause de l’insuffisance cardiaque n’était pas ischémique avaient un risque diminué de mortalité toutes causes (RTi 0,54, IC 95 % : 0,37-0,79) et de mortalité de cause cardiovasculaire (RTi 0,52, IC 95% : 0,35-0,77) 83.
Donc, alors que l’utilisation des bloqueurs de canaux calciques dihydropyridines de deuxième génération semble être sécuritaire chez les patients souffrant d’insuffisance cardiaque, l’utilisation de la nifédipine semble être associée à un risque augmenté de subir un évènement de santé indésirable. Par contre, l’augmentation de ce risque a été observé non pas dans des études ayant comparé l’effet de la nifédipine à l’effet d’un placebo mais proviennent plutôt d’études ayant comparé la nifédipine à des traitements ayant démontré des bénéfices pour diminuer la mortalité et les hospitalisations chez les patients souffrant d’insuffisance cardiaque 9. Le risque associé à l’exposition à la nifédipine chez les patients souffrant d’insuffisance cardiaque demeure donc incertain.
2.2.5.4 Les bloqueurs de canaux calciques non-dihydropyridines
Les bloqueurs des canaux calciques non-dihydropyridines sont le diltiazem et le vérapamil. Ces deux médicaments ont un effet chronotropique négatif 57 qui peut être néfaste chez les patients souffrant d’insuffisance cardiaque. Par contre, il existe peu de données sur le risque associé à l’exposition à un bloqueur des canaux calciques non-dihydropyridines chez les patients souffrant d’insuffisance cardiaque. Une des raisons est que la compagnie faisant la mise en marché du vérapamil a émis une mise en garde pour les patients souffrant d’insuffisance cardiaque lors de la commercialisation du médicament 57. Les données sur
les effets néfastes de l’exposition aux bloqueurs des canaux calciques non-dihydropyridines proviennent donc majoritairement de l’effet du diltiazem et du vérapamil suite à un infarctus aigu du myocarde. L’effet du diltiazem sur les événements cardiovasculaires a effectivement été observé dans une étude évaluant l’effet du diltiazem (comparativement au placebo) sur la mortalité et la survenue d’un infarctus du myocarde chez des patients en ayant déjà eu un 84. Alors que l’utilisation du diltiazem avait un effet neutre sur les résultats
de santé, il y avait une modification des résultats selon la présence ou non de congestion pulmonaire (et donc d’insuffisance cardiaque). Les individus exposés au diltiazem et ayant
une évidence d’insuffisance cardiaque soit observée cliniquement (surcharge pulmonaire) ou à l’échographie cardiaque (fraction d’éjection du ventricule gauche inférieure à 0,40) avaient un risque augmenté de faire un nouvel évènement cardiaque (RTi 1,41 ; IC 95 % : 1,01-1,96). Goldstein et coll. 85 ont par la suite aussi démontré que, suite à un infarctus aigu
du myocarde, les patients ayant des signes ou des symptômes d’insuffisance cardiaque étaient plus à risque de développer de l’insuffisance cardiaque s’ils étaient exposés au diltiazem plutôt qu’au placebo.
Le risque cardiovasculaire associé à l’exposition au vérapamil a été évalué dans deux études 86,87. Ont été inclus dans la première, des patients âgés de 75 ans et moins ayant subit
un infarctus du myocarde (les patients souffrant d’insuffisance cardiaque étaient exclus) 86.
Les auteurs ont observé que l’exposition au vérapamil comparée à l’exposition à un placebo ne diminuait pas le risque de mortalité (à 6 et à 12 mois) ou d’infarctus du myocarde (à 6 mois), mais augmentait le risque de développer de l’insuffisance cardiaque durant le suivi. La deuxième étude a été menée chez les patients souffrant de maladie cardiovasculaire. Les risques de décès pour toutes causes confondues, de survenu d’un infarctus du myocarde ou d’un accident vasculaire cérébral chez des personnes traitées contre l’hypertension avec du vérapamil SR ont été comparés aux mêmes risques chez les personnes traitées avec de l’aténolol 87. Les résultats ont été stratifiés selon la présence d’un antécédent d’insuffisance
cardiaque. Il n’y avait pas de différence sur les résultats de santé pour les deux groupes (patients avec et sans antécédent d’insuffisance cardiaque).
2.3 Conclusion de l’état des connaissances sur l’insuffisance cardiaque et
ses traitements
En conclusion, l’insuffisance cardiaque est un problème de santé majeur étant donné ses répercussions tant sur la qualité de vie, les hospitalisations, la mortalité, l’impact sur les fonctions cognitives et les coûts qui lui sont associés. Heureusement, il existe des traitements pharmacologiques dont l’efficacité a été démontrée dans les études cliniques à répartition aléatoire afin de diminuer les effets néfastes de l’insuffisance cardiaque. Ces traitements sont la combinaison d’un β-bloqueur avec un IECA. Lorsque l’IECA n’est pas toléré, il peut être remplacé par un ARA 8,9. L’association d’hydralazine et d’isosorbide