Prophylaxie pré-exposition (PrEP) pour la prévention du
VIH chez les travailleuses du sexe au Bénin
Thèse
Aminata Mboup
Doctorat en épidémiologie
Philosophiæ doctor (Ph. D.)
Prophylaxie pré-exposition (PrEP) pour la prévention du
VIH chez les travailleuses du sexe au Bénin
Thèse
AMINATA MBOUP
Sous la direction de :
Dr Michel Alary, directeur de recherche
Dr Souleymane Diabaté, codirecteur de recherche
Résumé
Malgré tous les efforts de prévention et de traitement réalisés à ce jour, l’infection au virus de l’immunodéficience humaine (VIH) continue d’être un problème de santé publique. Proposer de nouvelles méthodes de prévention pour réduire la transmission du VIH est donc essentiel. L’utilisation des antirétroviraux (ARV) pour prévenir la transmission et l’acquisition de l’infection à VIH semble prometteuse à cette fin. Deux méthodes de prévention, le traitement précoce (early antiretroviral therapy: E-ART) pour les personnes séropositives et la prophylaxie pré-exposition (PrEP) pour les personnes séronégatives ont prouvé leur efficacité dans les essais cliniques mais devraient être évaluées dans les conditions réelles de vie hors du cadre des essais cliniques. Ainsi, l’objectif de cette thèse était d’évaluer la pertinence et la faisabilité d’ajouter ces deux nouvelles méthodes de prévention au paquet de prévention et traitement actuellement offert aux travailleuses du sexe (TS) au Bénin.
Dans le projet de démonstration présenté, 361 TS ont été recrutées et suivies pendant 12 à 24 mois dont 105 TS sous E-ART et 256 TS sous PrEP. Dans un premier temps, des indicateurs clés ont été mesurés. L’acceptabilité était de 95,5% pour l’E-ART et 88,3% pour la PrEP. La rétention à la fin de l’étude était de 59,0% pour l’E-ART et 47,3% pour la PrEP. L’observance auto-rapportée à l’E-ART était plus élevée que l’observance auto-rapportée à la PrEP qui a significativement diminué au cours du suivi. Nos résultats ne suggèrent pas de compensation de risque avec la PrEP. Par la suite, nous avons comparé les tendances de trois mesures d’observance à la PrEP avec des équations d’estimation généralisées (GEE). Le dosage du tenofovir (TFV), considéré comme mesure de référence a été comparé aux mesures auto-rapportées et au décompte des pilules. Le dosage du TFV a indiqué que l’observance à la PrEP a significativement diminué durant l’étude. Le décompte des pilules et les mesures auto-rapportées ont surestimé l’observance. Le dosage du TFV est la mesure la plus appropriée pour mesurer l’observance dans cette population à haut-risque mais son coût empêche son utilisation systématique.
Finalement, nous avons identifié les prédicteurs de l’observance à la PrEP. Un âge plus avancé, une durée plus courte dans l’étude et une intention élevée de prendre la PrEP au début de l’étude étaient les seuls facteurs associés à l’observance.
En conclusion, la PrEP pourrait être intégrée comme choix au paquet de prévention combinée du VIH offert aux TS au Bénin. Toutefois, la PrEP ne protège pas contre les autres infections sexuellement transmissibles. Elle est une méthode de prévention individuelle pour les personnes à haut-risque d’infection au VIH pour qui les moyens de prévention traditionnels n’ont pas fonctionné ou ne sont pas adaptés. L’E-ART par contre pourrait avoir un grand impact pour une meilleure prise en charge clinique du VIH chez les TS et pour la prévention de sa transmission au niveau populationnel. Toutefois, pour la mise en œuvre de la PrEP et de l’E-ART, les interventions doivent tenir compte de la réalité des TS, et en particulier leur mobilité pour assurer une bonne observance et une bonne rétention.
Abstract
HIV infection continues to be a public health burden despite all the prevention and treatment efforts accomplished to date. It is therefore essential to propose new prevention methods to reduce the transmission of HIV. The use of antiretrovirals (ARVs) to prevent the transmission and acquisition of HIV infection seems promising for this purpose. Two prevention methods, early antiretroviral (E-ART) and pre-exposure prophylaxis (PrEP) have proven their efficacy in clinical trials but should be evaluated in "real life" outside the framework of clinical trials. The objective of this thesis was therefore to assess the relevance and feasibility of adding these two new prevention methods to the prevention and treatment package currently offered to female sex workers (FSWs) in Benin.
In this demonstration project, 361 FSWs were recruited and followed for 12 to 24 months, 105 FSWs for E-ART and 256 FSWs for PrEP. First, key indicators were measured. Uptake was 95.5% for E-ART and 88.3% for PrEP. Retention at the end of the study was 59.0% for E-ART and 47.3% for PrEP. Self-reported adherence to E-ART was higher than self-reported adherence to PrEP, which decreased significantly during follow-up. Additionally, our results do not suggest any risk compensation with PrEP. We then measured PrEP adherence using 3 different measures and compared the trends using generalized estimating equations (GEE). Tenofovir (TFV) concentration in plasma, considered as the gold standard, was compared to self-reports and pill counts. Adherence to PrEP measured by TFV concentration decreased significantly over the course of the study. The pill counts and self-reported measures overestimated adherence. The TFV concentration in plasma appears to be the most appropriate measure for adherence in this high-risk population. However, its high cost limits its systematic use. Finally, we identified the predictors of adherence to PrEP. Older age, shorter duration in the study, and high intention to take PrEP at the start of the study were the only factors associated with adherence.
In conclusion, PrEP could be included as a choice in the combined HIV prevention package offered to FSWs in Benin. However, PrEP does not protect against other sexually transmitted infections. It is an individual prevention method for people at high risk of HIV infection for whom traditional means of prevention have not worked or are not adapted. E-ART, on the other hand, could have a great impact for the prevention of HIV at the population level, while significantly improving clinical care for HIV-infected FSWs. However, for the implementation of PrEP and E-ART, the interventions must take into account the reality of FSWs, particularly their mobility to ensure good adherence and retention.
Table des matières
Résumé ...ii
Abstract ...iv
Table des matières ...vi
Liste des tableaux ...ix
Liste des figures ...xi
Liste des abréviations, sigles, acronymes ... xii
Remerciements ... xvi
Avant-propos ... xviii
Introduction ... 1
Chapitre 1 Mise en contexte et état des connaissances ... 4
1.1 Aperçu de l’épidémie mondiale du VIH/SIDA ... 4
1.2 Aperçu de l’épidémie du VIH/SIDA en Afrique subsaharienne ... 4
1.3 Situation épidémiologique du VIH au Bénin... 5
1.4 Facteurs influençant la transmission par voie sexuelle du VIH ... 6
1.5 Méthodes de prévention de la transmission du VIH ... 9
1.5.1 Les méthodes de prévention traditionnelles du VIH ... 9
1.5.1.1 L’utilisation du préservatif ... 9
1.5.1.2 La circoncision masculine ... 11
1.5.2 Les méthodes de prévention biomédicales du VIH ... 12
1.5.2.1 Le traitement des IST ... 12
1.5.2.2 Le traitement précoce (E-ART) ... 13
1.5.2.3 La prophylaxie pré-exposition (PrEP) ... 16
1.6 PrEP : Une innovation dans les stratégies de prévention du VIH ... 19
1.6.1 Les modalités de prise de la PrEP ... 19
1.6.2 Les projets de démonstration sur la PrEP orale ... 20
1.6.3 L’importance de l’observance thérapeutique au traitement pour une PrEP efficace ... 21
1.6.4 Les méthodes de mesure de l’observance à la PrEP ... 22
1.6.4.1 Les méthodes subjectives... 22
1.6.4.2 Les méthodes objectives ... 24
1.6.5 Les facteurs associés à l’observance à la PrEP ... 26
1.6.6 La compensation des risques sous PrEP... 27
1.6.7.1 Les effets secondaires de la PrEP ... 28
1.6.7.2 Le développement de résistance aux ARV avec la PrEP ... 29
1.6.8 D’autres formes de PrEP ... 29
Chapitre 2 Objectifs ... 32
Chapitre 3 Méthodologie ... 33
3.1 Données manquantes ... 33
Chapitre 4 Early antiretroviral therapy and daily pre-exposure prophylaxis for HIV prevention among female sex workers in Cotonou, Benin: a prospective observational demonstration study ... 36
4.1 Résumé ... 37 4.2 Abstract ... 38 4.3 Introduction ... 40 4.4 Methods ... 41 4.5 Results ... 45 4.6 Discussion ... 48 4.7 Conclusions ... 51 4.8 Competing interests ... 53 4.9 Author contributions ... 53 4.10 Acknowledgments ... 53 4.11 Supplementary information ... 63
Chapitre 5 Comparison of adherence measurement tools used in a pre-exposure prophylaxis demonstration study among female sex workers in Benin ... 84
5.1 Résumé ... 85 5.2 Abstract ... 86 5.3 Introduction ... 88 5.4 Methods ... 89 5.5 Results ... 93 5.6 Discussion ... 96 5.7 Authors’ contributions ... 100 5.8 Acknowledgements ... 101 5.9 Supplementary information ... 108
Chapitre 6 Determinants of HIV pre-exposure prophylaxis (PrEP) adherence among female sex workers in a demonstration study in Cotonou, Benin: a study of behavioral and demographic factors ... 111
6.1 Résumé ... 112
6.3 Introduction ... 114
6.4 Materials and methods ... 115
6.5 Results ... 118 6.6 Discussion ... 120 6.7 Acknowledgements ... 124 6.8 Authors’ contributions ... 124 Chapitre 7 Discussion ... 133 Conclusion ... 145 Bibliographie ... 147
Liste des tableaux
Tableaux principaux
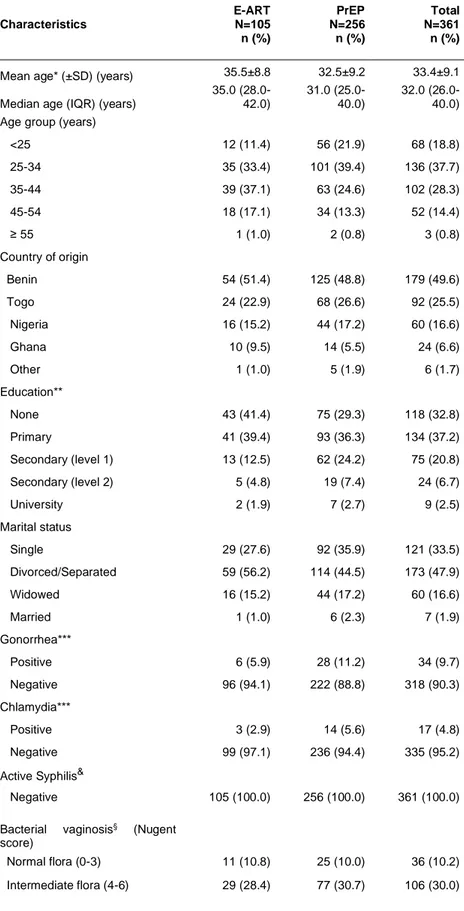
Table 1-1 Résultats des principaux essais cliniques sur la prophylaxie pré-exposition au VIH orale quotidienne (PrEP) ... 18 Table 4-1 Baseline characteristics of female sex workers recruited in an E-ART-PrEP demonstration project in Cotonou. Benin (2014-2016) ... 55 Table 5-1 Comparison of weighted proportions of optimal* daily adherence to PrEP at baseline (day 14) and at all final visits measured by 3 different methods in the E-ART-PrEP demonstration project in Cotonou, Benin106 Table 5-2 Comparison of weighted proportions of detectable* adherence to PrEP at baseline (day 14) and at all final visits measured by 3 different methods in the E-ART-PrEP demonstration project in Cotonou, Benin107 Table 6-1 Factors associated with optimal daily adherence measured by Tenofovir plasma concentration ... 126 Table 6-2 Descriptive statistics of the constructs used to evaluate optimal daily adherence to PrEP in a demonstration project conducted among female sex workers in Benin (2014-2016) ... 128 Table 6-3 Constructs from the Theory of Planned Behavior (TPB) associated with optimal adherence intention at the beginning of the study ... 129 Table 6-4 Factors associated with optimal daily adherence measured by blood drug concentration using the Planned Behavior Theory ... 131
Tableaux supplémentaires
Supplementary Table 4-1 Reasons for declining E-ART and PrEP among eligible female sex workers
participating in the E-ART/PrEP demonstration project in Cotonou, Benin (2014-2016) ... 65 Supplementary Table 4-2 Comparison of baseline characteristics between female sex workers recruited for E-ART and FSWs eligible for E-E-ART but not recruited in the E-E-ART-PrEP demonstration project in
Cotonou,Benin (2014-2016) ... 66 Supplementary Table 4-3 Comparison of baseline characteristics between female sex workers recruited for PrEP and FSWs eligible for PrEP but not recruited in the E-ART-PrEP demonstration project in Cotonou. Benin (2014-2016) ... 67 Supplementary Table 4-4 Retention among female sex workers recruited in the E-ART/PrEP demonstration project in Cotonou, Benin (2014-2016) ... 68 Supplementary Table 4-5 Reasons for not completing follow-up till the end of the study among female sex workers participating in the E-ART/PrEP demonstration project in Cotonou, Benin (2014-2016) ... 69 Supplementary Table 4-6 Self-reported adherence to E-ART in the last month at each scheduled follow-up visit in E-ART-PrEP demonstration project Cotonou, Benin (2014-2016) ... 70 Supplementary Table 4-7 Comparison of adherence (≥90% vs <90%) to E-ART at baseline and at final visit in the E-ART-PrEP demonstration project Cotonou, Benin (2014-2016) ... 71 Supplementary Table 4-8 Comparison of adherence (<50% vs >50%) to E-ART at baseline and at final visit in the E-ART-PrEP demonstration project Cotonou, Benin (2014-2016) ... 71 Supplementary Table 4-9 Viral load by scheduled visit among female sex workers participating in the E-ART-PrEP demonstration project in Cotonou, Benin (2014-2016) ... 71
Supplementary Table 4-10 Self-reported adherence to PrEP in the last 7 days at each scheduled study visit in E-ART-PrEP demonstration project, Cotonou, Benin (2014-2016) ... 72 Supplementary Table 4-11 Association between age and perfect adherence (did not miss any pill in the last week) measured by self-reports among female sex workers participating in the E-ART-PrEP demonstration project in Cotonou, Benin (2014-2016) ... 73 Supplementary Table 4-12 Comparison of adherence to PrEP in the last 7 days at baseline (day 14) and at final visits in the E-ART-PrEP demonstration project Cotonou, Benin (2014-2016) ... 74 Supplementary Table 4-13 Comparison of adherence to PrEP (≥4 pills vs all other levels) in the last 7 days at baseline (day 14) and at final visits in the E-ART-PrEP demonstration project Cotonou, Benin (2014-2016) ... 74 Supplementary Table 4-14 Trends in the mean number of clients in the previous 2 and 14 days as reported by female sex workers; E-ART-PrEP demonstration project, Cotonou, Benin (2014-2016) ... 75 Supplementary Table 4-15 Trends in the proportions of female sex workers who reported less than 5 clients in the last 2 days and less than 20 clients in the last 14 days; E-ART-PrEP demonstration project, Cotonou, Benin (2014-2016) ... 76 Supplementary Table 4-16 Trends in the proportions of female sex workers who reported having had sex with a regular partner in the previous 2 and 14 days; E-ART-PrEP demonstration project, Cotonou, Benin (2014-2016) ... 77 Supplementary Table 4-17 Trends in the proportions of E-ART and PrEP women who reported consistent condom use (100%) with their clients during the previous 2 days and 14 days; E-ART-PrEP demonstration project Cotonou, Benin (2014-2016) ... 82 Supplementary Table 4-18 Trends in the proportions of E-ART and PrEP women who reported consistent condom use (100%) with their regular sexual partners during the previous 2 and 14 days; E-ART-PrEP demonstration project, Cotonou, Benin (2014-2016) ... 83 Supplementary Table 5-1 Relationship between the number of pills taken in the last week and the tenofovir (TFV) and emtricitabine (FTC) plasma concentrations ... 108 Supplementary Table 5-2 Unweighted adherence based on tenofovir (TFV) or emtricitabine (FTC) plasma concentrations at the different study visits ... 109
Liste des figures
Figures principales
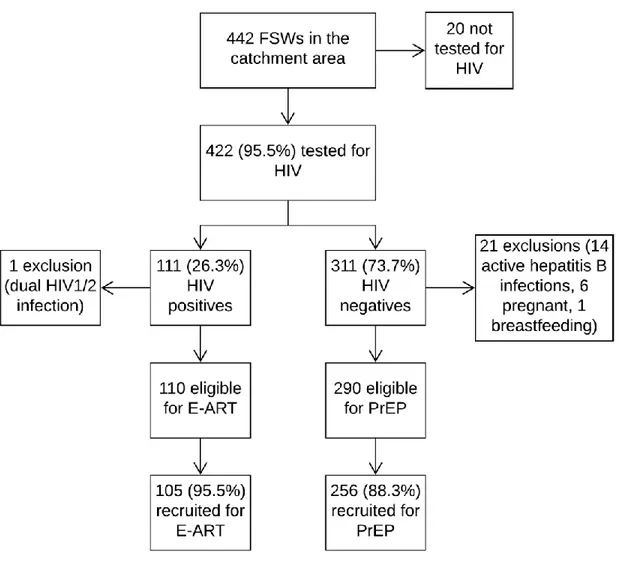
Figure 4.1 Flowchart of screening coverage, HIV prevalence and E-ART/PrEP uptake among FSWs in
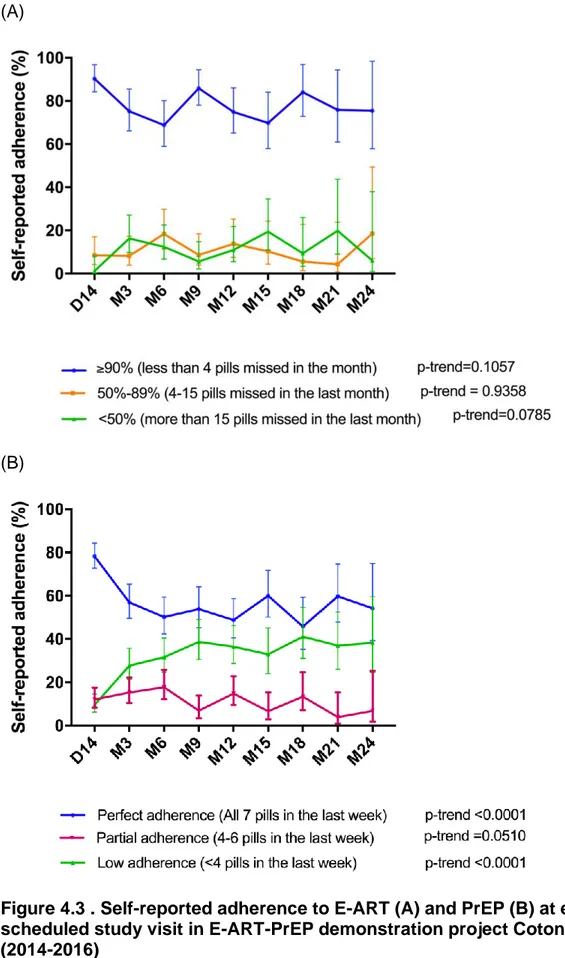
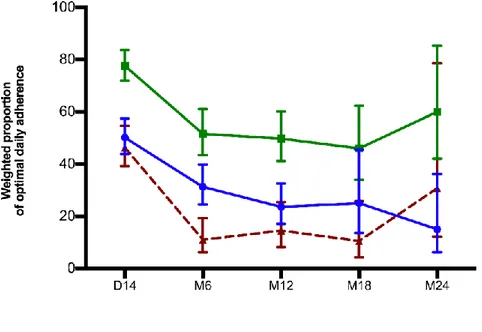
Cotonou, Benin, 2014-2016 ... 54 Figure 4.2 HIV E-ART and PrEP cascades among FSWs in the demonstration study in Cotonou, Benin, 2014-2016. (A) E-ART cohort (B) PrEP cohort... 57 Figure 4.3 . Self-reported adherence to E-ART (A) and PrEP (B) at each scheduled study visit in E-ART-PrEP demonstration project Cotonou Benin (2014-2016) ... 59 Figure 4.4 Trends of sexual behavior among E-ART and PrEP participants in the last 2 or last 14 days;E-ART-PrEP demonstration project, Cotonou, Benin (2014-2016) ... 62 Figure 5.1 Weighted proportion of optimal* daily adherence (100%) to PrEP measured by TFV blood
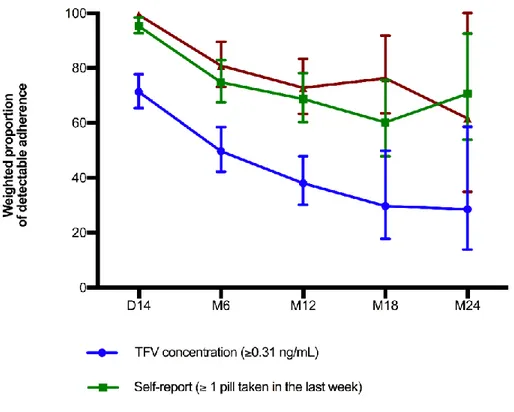
concentration, self-report and pill count in the PrEP demonstration study conducted among female sex workers in Cotonou, Benin ... 102 Figure 5.2 Weighted proportion of detectable* adherence to PrEP measured by Tenofovir (TFV) blood
concentration, self-report and pill count in the PrEP demonstration study conducted among female sex workers in Cotonou, Benin ... 104 Figure 6.1 Theoretical framework used to explain adherence to PrEP among female sex workers in the E-ART/PrEP demonstration project conducted in Benin 2014-2016 ... 125
Figure supplémentaire
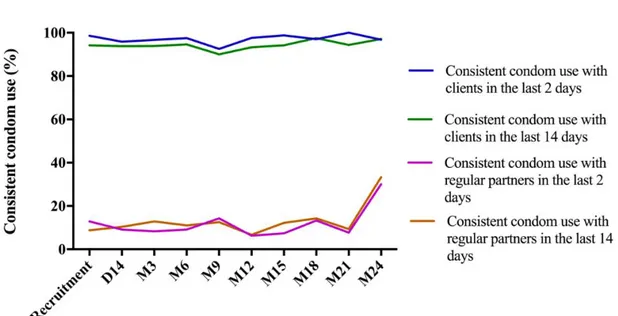
Supplementary Figure 4-1 Trends in sexual behaviors in the last 2 and 14 days among female sex workers (FSWs) in Benin demonstration E-ART-PrEP project. (A) Mean number of clients among FSWs under early antiretroviral therapy (E-ART). (B) Mean number of clients among FSWs under HIV pre-exposure prophylaxis (PrEP). (C) Proportion of FSWs under E-ART reporting having sex with a regular partner. (D) Proportion of FSWs under PrEP reporting having had sex with a regular partner. (E) Self-reported consistent condom use (100%) among FSWs under E-ART. (F) Self-reported consistent condom use (100%) among FSWs under PrEP ... 80
Liste des abréviations, sigles, acronymes
ACASI Audio computer-assisted self-interview AIDS Acquired Immune Deficiency Syndrome anti-HBc Hepatitis B core antibody
anti-HBs Hepatitis B surface antibody ART Antiretroviral therapy ARV Antirétroviraux
BTS Bangkok Tenofovir Study CASI Computer-assisted self-interview CD4 Cellules lymphocytaires T CD4 CDC Centers for Disease Control D-14 Day 14 follow-up visit DBS Dried-blood spot
DIST Dispensaire des IST (clinique à Cotonou, Benin) E-ART Early antiretroviral therapy
FDA Food and Drug Administration FSWs Female sex workers
FTC Emtricitabine
FTFI Face to face interview
GEE Generalized estimating equations
HARSAH Hommes ayant des relations sexuelles avec d’autres hommes HBsAg Hepatitis B surface antigen
HIV Human Immunodeficiency Virus IC Intervalle de confiance
IPCW Inverse probability of censoring weighting LLOQ Lower limit of quantification
M6 Month 6 follow-up visit M12 Month 12 follow-up visit M18 Month 18 follow-up visit M24 Month 24 follow-up visit
MEMS Medication Event Monitoring System MSM Men who have sex with men OMS Organisation Mondiale de la Santé
ONUSIDA Programme commun des Nations Unies sur le VIH/SIDA
POC Point-of-care
PR Prevalence ratio
PrEP Pre-exposure prophylaxis SMS Short message system STIs Sexually transmitted infections
TDF/FTC Tenofovir disoproxil fumarate/emtricitabine (Truvada®)
TIB Theory of interpersonal behavior TPB Theory of planned behavior TS Travailleuse du sexe
TFV Tenofovir
UDI Utilisateurs de drogue injectable VIH Virus de l’immunodéficience humaine
À mes parents, mes idoles, sans qui rien de tout cela n’aurait été possible À mon mari, Lamine, qui m’a soutenu et encouragé tout au long de ce parcours
« Tout vient à point à qui sait attendre » Clément Marot
Remerciements
Un adage sénégalais dit bien: « celui qui prend l’initiative de citer, prend également
le risque d’oublier ou de se tromper ». Bien qu’étant un projet individuel, cette thèse
est le résultat de plusieurs rencontres et contributions incommensurables. Au cours des prochains paragraphes, mon objectif sera donc de ‘braver’ cet adage.
Je ne saurais commencer sans remercier Allah par qui tout arrive. Gloire Lui soit rendue.
Je voudrais exprimer ma profonde gratitude à mon directeur de recherche, Dr. Michel Alary. Merci d’avoir suivi ce travail de sa conception à son achèvement. Vos conseils, votre flexibilité, votre support autant moral que financier et votre disponibilité ont été des catalyseurs durant ce parcours.
Je ne saurais omettre l’apport de mon co-directeur de recherche, Dr. Souleymane Diabaté. Merci pour vos conseils et suivis.
A mes parents, Pr. Souleymane Mboup et Marie Louise Lopez. Merci de m’avoir inculqué cette passion pour la recherche scientifique et d’avoir frayé la voie pour moi. Je vous serai toujours reconnaissante pour vos sacrifices, votre soutien et les valeurs inculquées. Papa, je souhaite vivement que tu sois fier à la lecture de cette thèse et que tu la considères comme un pas vers l'excellence et le professionnalisme que tu incarnes si bien.
A mon mari, Lamine Seye, merci d’être un si grand exemple de patience. Mes mots ne sauraient exprimer ma reconnaissance pour tes encouragements, ton support et tous tes sacrifices. Toute cette aventure a débuté par tes incitations. Je ne peux que prier pour toi. Cette thèse est aussi la tienne. Ensemble, nous l'avons visualisée, rêvée et conçue telle une équipe soudée quels que soient les obstacles.
A mes deux perles, Aminata Imane et Marième Louise, la fierté dans vos yeux compense pour toutes mes absences. J’espère que mon sens du sacrifice et ma
Je ne saurais passer sous silence l’immense apport des équipes du projet PrEP au Bénin et au CHU de Québec – Université Laval pour leur énergie et leur dévouement inlassables. Des remerciements chaleureux à l’endroit du Dr Luc Béhanzin, Dr Fernand Guédou, Myrto Mondor, Johanne Leroux et particulièrement Dr Mélanie Drolet pour son initiative de me mettre en contact avec le Dr Michel Alary. Je voudrais aussi remercier Dr Badara Cissé et Dr Moussa Sarr pour leurs conseils et support dans ce long parcours.
Merci à mes condisciples et amis du programme de doctorat en épidémiologie de l’Université Laval pour les moments enrichissants partagés qui ont contribué à alléger les difficultés de ce parcours.
Enfin, merci à ma grande sœur adorée Marème et son mari El-Hadj Ndaw, à mes frères, Libasse et Jean-Papys, ma cousine Ndeye Arame Seck, mes neveux et nièces, mes amis Ndoumbe Fall, Ibou Fall, Aminata Diallo, Alioune Diouf, Mireille Kalou et à ma belle-famille Aminata Mbow, Pape Ousmane Seye, Sophie, Babacar et mon anti-stress Khady. Votre appui, votre compréhension et votre amitié ont été des plus remarquables.
Pour tous ceux dont le nom n’a pas été cité mais qui de près ou de loin m’ont apporté un quelconque soutien, sachez que je vous en suis grandement reconnaissante.
Avant-propos
Cette thèse de doctorat en épidémiologie a été réalisée sous la direction du Dr. Michel Alary, professeur titulaire au département de médecine sociale et préventive de l'Université Laval et sous la codirection de Dr. Souleymane Diabaté, professeur adjoint au département de médecine sociale et préventive de l'Université Laval. L’objectif général de la thèse est d’évaluer la pertinence et la faisabilité de la Prophylaxie pré-exposition (PrEP) pour la prévention du virus de l’immunodéficience humaine (VIH) chez les travailleuses du sexe (TS) dans un pays d’Afrique subsaharienne caractérisé par une épidémie de type concentré. Cet objectif général a été évalué considérant trois objectifs spécifiques qui ont chacun abouti à une publication scientifique. Ces objectifs ont déjà été présentés lors de mon examen de projet de recherche durant l’automne 2014.
Les données utilisées proviennent d’une étude de démonstration visant à étudier la faisabilité de la mise en œuvre d’un traitement précoce des personnes infectées par le VIH (early antiretroviral therapy : E-ART) et la prophylaxie pré-exposition (pre-exposure prophylaxis : PrEP) chez les TS professionnelles de Cotonou, Bénin. Trois articles sont présentés dans cette thèse pour évaluation et pour chacune de ces publications je suis la première auteure. Dr. Michel Alary, chercheur principal de l’étude de démonstration E-ART/PrEP, est le dernier auteur (auteur senior) de tous les trois articles. Le premier article intitulé « Early antiretroviral therapy and daily pre‐ exposure prophylaxis for HIV prevention among female sex workers in Cotonou, Benin : a prospective observational demonstration study » a été accepté pour publication dans la revue Journal of the International AIDS Society le 19 Octobre 2018 et a été publié le 22 Novembre 2018. Pour cet article, j’ai participé à la gestion des données, aux analyses statistiques et leurs interprétations et j’ai aussi rédigé la première version du manuscrit et je l’ai révisé en fonction des commentaires reçus. Il y a 21 co-auteurs outre Dr Alary et moi-même. Tous les co-auteurs sont impliqués dans le projet de démonstration E-ART/PrEP dont ce premier objectif de ma thèse est une composante. Il s’agit de Dr Luc Béhanzin, Dr Fernand Guédou, Dr Nassirou
Kessou, Dr Mamadou Diallo, Dr René Kêkê, Dr Moussa Bachabi, Dr Kania Dramane, Lily Geidelberg, Dr Fiona Cianci, Dr Christian Lafrance, Dr Dissou Affolabi, Dr Souleymane Diabaté, Dr Marie-Pierre Gagnon, Dr Djimon Marcel Zannou, Dr Flore Gangbo, Dr Marie-Claude Boily et Dr Peter Vickerman. Dans le projet de démonstration E-ART/PrEP, les deux méthodes de prévention E-ART et PrEP ont été combinées pour des raisons d’efficacité et surtout des raisons éthiques. En effet, la combinaison des deux interventions implique que toutes les TS fréquentant la clinique où l’étude a été menée ont eu l’opportunité de recevoir une certaine forme de médicaments antirétroviraux en plus des conseils sur l’observance thérapeutique. De plus, d'un point de vue éthique, il aurait été difficile de justifier une approche dans laquelle des médicaments antirétroviraux seraient administrés aux femmes séronégatives tandis qu’on offrirait pas de manière active et systématique de traiter les TS asymptomatiques séropositives. De ce fait, ce premier article proposé est basé sur les deux interventions (E-ART et PrEP). Cependant, les deux articles suivants proposés dans la thèse utilisent juste les données du volet PrEP de l’étude de démonstration.
Le deuxième article intitulé « Comparison of adherence measurement tools used in a pre-exposure prophylaxis demonstration study among female sex workers in Benin » a été soumis le 12 Novembre 2019 à la revue Medicine : HIV/AIDS, a été accepté le 31 Mars 2020 et publié le 21 Mai 2020. Pour cet objectif, j’ai élaboré le plan d’analyse. J’ai opéré et interprété toutes les analyses statistiques sous la supervision de mon directeur de thèse. J’ai rédigé le premier draft de l’article. J’ai fait la synthèse de tous les commentaires des co-auteurs et j’ai révisé conséquemment la version finale de l’article. Les co-auteurs sont Dr Luc Béhanzin, Dr Fernand Guédou, Dr Katia Giguère, Dr Nassirou Geraldo, Dr Djimon Marcel Zannou, Dr René K. Kêkê, Dr Moussa Bachabi, Dr Flore Gangbo, Dr Dissou Affolabi, Dr Mark A. Marzinke, Dr Craig Hendrix et Dr Souleymane Diabaté.
Le troisième et dernier article intitulé « Factors associated with adherence in a demonstration study on HIV pre-exposure prophylaxis (PrEP) among female sex workers (FSWs) in Cotonou, Benin » a été soumis le 14 Avril 2020 à la revue
Sexually Transmitted Diseases et accepté le 5 Janvier 2021. Les co-auteurs sont les mêmes que celui du deuxième article sauf Dr Katia Giguère, Dr Dissou Affolabi et Dr Nassirou Geraldo. Pour cet article, j’ai aussi élaboré le plan d’analyse. J’ai fait et interprété toutes les analyses statistiques sous la supervision de mon directeur de thèse. J’ai rédigé la première version de l’article et j’ai révisé la version soumise à la suite des commentaires des co-auteurs.
Introduction
Malgré tous les efforts de traitement et de prévention réalisés à ce jour, l'épidémie du virus de l’immunodéficience humaine (VIH) persiste. En 2016, le nombre de nouvelles infections s'élevait à 1,8 millions, ce qui correspond à environ 5 000 infections par jour [1]. Le plus lourd fardeau est observé en Afrique subsaharienne, où la transmission est majoritairement hétérosexuelle [2], avec 61% de ces nouveaux cas d’infection [3]. En Afrique de l'Ouest, l'épidémie est de type concentrée1 chez les femmes travailleuses du sexe (TS) qui sont impliquées directement ou indirectement dans 75‐90% des cas de transmission du VIH vers la population générale, essentiellement par le biais de leurs clients et autres partenaires sexuels masculins [4-6]. La prévalence du VIH chez les TS dans cette région est 12 fois plus élevée que celle chez les autres femmes en âge de procréer [7]. Dans de telles situations, il est important de poursuivre voire intensifier les efforts de prévention et de traitement à l'égard des TS afin de mieux contrôler l'épidémie du VIH. Une amélioration de l’approche de prévention combinée incluant déjà des composantes comportementales, biomédicales et structurelles est donc nécessaire pour le milieu prostitutionnel en général et plus particulièrement pour les TS, en plus d’assurer le traitement adéquat de celles qui sont déjà infectées.
L’utilisation récente des antirétroviraux (ARV) pour prévenir la transmission du VIH pourrait avoir un impact considérable sur les populations et accélérer le contrôle de l’épidémie. Des essais randomisés complétés sur l’utilisation des ARV avant exposition au VIH (prophylaxie pré-exposition ou PrEP) ont montré leur efficacité à réduire l’infection au VIH chez des hétérosexuels au Botswana, Kenya et Ouganda [8, 9], des hommes ayant des relations sexuelles avec d’autres hommes (HARSAH) aux USA [10], et des utilisateurs de drogue injectable (UDI) en Thaïlande [11].
1 Une épidémie concentrée est une épidémie où certains groupes de la population ont une prévalence
beaucoup plus élevée que la population générale. La présence de ces groupes favorise le maintien de l’épidémie. Une épidémie généralisée par contre est une épidémie qui perdure dans la population générale même sans l’existence de groupes à haut risque.
Toutefois, deux essais cliniques menés chez des femmes à haut risque en Afrique de l’est et du sud (essais VOICE et FEM-PrEP) [12, 13] n’ont pas montré un bénéfice de la PrEP orale. Il a été démontré que les échecs de ces deux essais sont principalement liés aux problèmes de faible observance aux ARV plutôt qu’à une faible efficacité biologique [12-17]. Bien que l’efficacité de la PrEP orale continue comme stratégie de prévention contre le VIH ait été prouvée dans la plupart des essais randomisés complétés à ce jour [8-11], elle reste à évaluer dans les conditions réelles de vie. En effet, elle dépend de plusieurs facteurs comme la fréquence de dépistage, l’acceptabilité et l’observance au traitement qui pourraient varier dans différents contextes culturels, sociaux et personnels. Il serait donc important d’étudier ces observations en situation réelle et en dehors du contexte des essais cliniques afin de savoir si les stratégies de prévention axées sur la PrEP seraient acceptées et apporteraient une contribution significative à la prévention du VIH surtout chez les populations à haut risque. En raison de l'information limitée sur la mise en œuvre de la PrEP en Afrique de l’Ouest, en particulier chez les TS, l’objectif de cette thèse est d’étudier la faisabilité et la pertinence d’inclure la PrEP dans l’offre de prévention combinée existante chez les TS du Bénin. Au Bénin, en 2015, la prévalence du VIH était d’environ 1% dans la population générale alors qu’elle s’élevait à 15,7% chez les TS [18].
Les données utilisées dans cette thèse proviennent d’une étude prospective observationnelle menée de septembre 2014 à décembre 2016 chez les TS au Bénin dont l’objectif était d’évaluer la faisabilité et la pertinence d’ajouter deux nouvelles méthodes de prévention du VIH : le traitement précoce comme prévention (E-ART : early antiretroviral therapy) et la PrEP au paquet de prévention combinée qui comprend toute une gamme d’approches biomédicales, structurelles et comportementales déjà offerte aux TS au Bénin. L’E-ART consiste en l’utilisation précoce des ARV indépendamment du statut clinique par les personnes séropositives afin d’empêcher la transmission du VIH à autrui. Dans cette thèse, je présente trois articles. Le premier article présente les résultats principaux des deux méthodes de prévention (E-ART et PrEP) évaluées dans l’étude de démonstration.
Le deuxième et le troisième article se limitent aux données de la PrEP. Considérant l’importance de l’observance pour l’efficacité de la PrEP, les objectifs de ces deux articles étaient donc : 1) de comparer trois méthodes de mesure de l’observance utilisées dans l’étude de démonstration et 2) d’identifier les facteurs associés à l’observance à la PrEP.
Chapitre 1 Mise en contexte et état des
connaissances
1.1 Aperçu de l’épidémie mondiale du VIH/SIDA
Presque 40 ans après son émergence, le VIH continue d’être un véritable problème de santé publique. Depuis le début de l’épidémie, 75,7 millions (IC à 95%: 55,9-100 millions) de personnes ont été infectées par le VIH et 32,7 millions (IC à 95%: 24,8-42,2 millions) sont décédées de suite de maladies liées au sida. En 2019, le nombre de personnes séropositives était estimé à 38,0 millions (IC à 95%: 31,6-44,5 millions) et 1,7 millions (IC à 95%: 1,2-2,2 millions) de personnes étaient nouvellement infectées. Au cours de cette même année, on estime que 690 000 (IC à 95%: 500 000-970 000) personnes sont mortes à cause du VIH [3]. S’il est vrai que depuis 2010 les nouvelles infections ont été réduites de 16% et que les décès liés au sida ont aussi été réduits de 33%, l’épidémie est loin d’être contrôlée [19]. Il existe une grande hétérogénéité de l’épidémie du VIH non seulement entre les continents mais aussi entre les régions en termes de prévalence, d’incidence, de décès et de couverture du traitement. Certains pays sont plus touchés que d’autres et dans un même pays, il y a souvent d’importants écarts du niveau d’infection entre états, provinces ou régions, zones rurales et urbaines ou districts [3, 20-24].
1.2 Aperçu de l’épidémie du VIH/SIDA en Afrique subsaharienne
L’Afrique subsaharienne est la région la plus sévèrement touchée par l’épidémie du VIH [24, 25]. La transmission du VIH dans cette région est majoritairement hétérosexuelle [25]. En 2017, 71% des personnes vivant avec le VIH dans le monde résidaient en Afrique subsaharienne. Cette région abrite 65% des nouvelles infections au VIH et 75% des décès liés au Sida dans le monde alors qu’elle ne représente que 13% de la population mondiale [26, 27]. L’Afrique subsaharienne est également caractérisée par une hétérogénéité géographique de l’épidémie. Les pays du sud et de l’est sont les plus touchés avec une épidémie de type généralisée [20, 27]. Dans les pays de l’ouest, par contre, l’épidémie est de type concentré avec
des prévalences plus élevées dans les groupes dits à haut risque [2, 28, 29]. Les groupes à haut risque les plus reconnus sont les TS et les HARSAH. Des études ont estimé que 75% à 90% des cas de transmission du VIH vers la population générale étaient liés au travail du sexe par le biais des clients et autres partenaires sexuels des TS [4-6]. Ces données montrent la nécessité pour les programmes de traitement et prévention du VIH de cibler le milieu du travail du sexe afin de limiter la propagation de l’épidémie.
1.3 Situation épidémiologique du VIH au Bénin
La république du Bénin est située en Afrique occidentale. Le Bénin est limité au Nord par le Niger, au Sud par l’Océan Atlantique, à l’Ouest par le Togo et à l’Est par le Nigeria. Le nombre d’habitants était évalué à 11,4 millions en 2018 [26]. Cotonou, la plus grande ville du pays, est la capitale économique. Le Bénin est confronté à une épidémie du VIH de type concentré. Depuis 2002, la prévalence du VIH s’est stabilisée à environ 1,2% dans la population générale. Par contre, de fortes prévalences sont rapportées au sein de certaines populations clés plus exposées aux risques d’infection, notamment les TS, leurs partenaires, les HARSAH et les UDI [30]. En 2017, la prévalence du VIH était estimée à 7,0% chez les HARSAH et 2,2% chez les UDI [31]. Chez les TS, la prévalence du VIH était estimée à 15,5% en 2015 et à 8,5% en 2017. Chez les clients des TS, la prévalence était estimée à 1,3% en 2015 [30, 31]. Malgré la diminution de la prévalence chez les TS, elle reste toujours élevée et cela pourrait compromettre le contrôle de l’épidémie au Bénin. À Cotonou, il a été estimé que presque toutes les infections chez les femmes et 76% chez les hommes étaient dues directement ou indirectement aux contacts sexuels avec les TS [4, 6, 32]. Il serait donc pertinent d’identifier et de tenter les nouvelles méthodes préventives du VIH chez les TS afin de renforcer les programmes de prévention et de prise en charge. De plus, les conclusions tirées de ce travail pourraient être utiles pour d'autres juridictions où les TS sont une population prioritaire pour le contrôle de l'épidémie du VIH.
1.4 Facteurs influençant la transmission par voie sexuelle du VIH
Le VIH peut être transmis par le sang, les produits sanguins contaminés, d'une mère à sa progéniture pendant la grossesse, l'accouchement ou l'allaitement ou par contact sexuel non-protégé. La transmission par voie sexuelle reste de loin le mode de transmission prédominant. En effet, elle est à l’origine de plus de 90% des nouvelles infections par le VIH dans le monde [33]. Au sein d’une population, le risque pour un individu d’être infecté par le VIH dépend de la probabilité de rentrer en contact avec une personne infectée et de la probabilité de transmission du virus lors de ce contact. La probabilité d’entrer en contact avec une personne infectée par le VIH dépend elle-même de la prévalence du VIH dans la population donnée et du nombre de contacts réalisés. Cependant, la probabilité de transmission du virus dépend entre autres de la susceptibilité à l’infection de l’individu sain, du type de contact, et de l’infectiosité de la personne infectée [34]. Le risque de transmission du VIH lors d’un seul rapport sexuel est faible, mais peut être considérablement augmenté par la présence de co-facteurs [35]. Ces co-facteurs incluent la pénétration anale ou vaginale non protégée, la présence d’une autre infection sexuellement transmissible (IST), la charge virale et le stade de l’infection par le VIH, les rapports sexuels pendant les règles, et les saignements coïtaux.
En l’absence de préservatif, les pénétrations anales sont les pratiques les plus à risque de transmission du VIH comparativement aux relations sexuelles vaginales lesquelles sont associées à un risque plus élevé que les relations sexuelles orales. En effet, la muqueuse rectale est différente de la muqueuse vaginale et a une plus forte densité de cellules cibles du VIH (nodules lymphoïdes) faisant en sorte qu’elle est plus sensible aux abrasions que la muqueuse vaginale [36]. Les données sur la prévalence des rapports sexuels anaux sont limitées et incertaines à cause du biais de désirabilité sociale associé à la mesure de cette pratique sexuelle. Une étude menée chez 466 TS d’Abidjan en Côte d’Ivoire a rapporté que les rapports sexuels anaux sont couramment pratiqués par les TS et leurs partenaires. En effet, 20% (IC à 95% : 15-26%) des TS avaient rapporté avoir des rapports sexuels anaux dans
une semaine de travail normale. Cependant, les rapports sexuels anaux sont souvent sous-estimés et sont un important facteur pour l'acquisition et la transmission du VIH dans ce groupe [37]. Dans une autre étude menée en Eswatini chez 325 TS, la prévalence des rapports sexuels anaux avec tout type de partenaires dans le dernier mois était estimée à 44% (IC à 95%: 34-54%) [38]. Au Bénin, dans une enquête menée chez des hommes mariés hétérosexuels de Cotonou, 17,5% (IC à 95%: 13,2-22,6%) avaient rapporté avoir des relations sexuelles anales avec une femme [39]. Les résultats d’une méta-analyse ont montré que le risque de transmission hétérosexuelle du VIH par acte sexuel dépend du type d’activité sexuelle. En effet, dans cette méta-analyse, le risque de la transmission anale homme-femme a été estimée à 1.69% (IC à 95%:0,32-8,91%) alors que le risque de la transmission vaginale homme-femme était juste de 0,08% (IC à 95%: 0,05-0,11% ) [40]. Ces données suggèrent que la prévalence des rapports sexuels anaux pourrait être sous-estimée dans les populations à haut-risque telles que les TS du Bénin. Étant donné la haute prévalence des rapports sexuels anaux et le risque élevé d’infection avec cette pratique sexuelle, les TS sont très vulnérables à l’infection du VIH. Ce risque est accentué par le nombre important de partenaires sexuels et la haute prévalence du VIH dans le milieu du travail du sexe. Toujours au Bénin, une autre étude a rapporté que la prévalence du VIH chez les TS qui avaient plus de 10 clients lors de la semaine précédente était 1,4 fois plus élevée que la prévalence du VIH chez les TS qui avaient moins de 10 clients [41].
Les IST joueraient un rôle prépondérant dans la propagation de l’épidémie du VIH en Afrique du fait de leur forte prévalence en augmentant de façon significative le risque de transmission [42]. En effet, les IST facilitent la transmission sexuelle du VIH en augmentant l’infectiosité des personnes séropositives et aussi en augmentant la susceptibilité des personnes séronégatives. La présence d’une IST chez le partenaire non-infecté peut accroître sa susceptibilité au VIH en créant une effraction de la barrière muqueuse génitale facilitant l’entrée du virus dans l’organisme et une inflammation locale, à l’origine d’un afflux de cellules et notamment de cellules cibles du VIH. De même, la présence d’une IST chez les
individus contaminés par le VIH peut accroitre leur infectiosité en augmentant l’excrétion virale au niveau génital et, indirectement, la virémie [36]. Au Bénin, une étude a rapporté que l’infection à VIH était seulement associée aux infections à chlamydia et à gonocoque symptomatiques avec au moins une lésion cervicale et non aux infections asymptomatiques [43]. Une autre étude sur l’incidence de la gonorrhée et du chlamydia chez les TS a rapporté que même si la prévalence de ces deux IST a diminué régulièrement au cours des deux dernières décennies grâce aux interventions structurelles, cliniques et au changement de comportement, les TS continuent de subir des réinfections [44]. De ce fait, les stratégies de prévention du VIH devraient être renforcées dans cette population vulnérable.
Parmi les facteurs influençant la transmission du VIH, on peut noter la charge virale qui dépend du stade d’infection par le VIH [45, 46]. Les stades précoces et tardifs de l’infection par le VIH sont des périodes de haute infectivité du fait de la réplication virale élevée. Le risque d’infection et de transmission du VIH est donc plus élevé durant ces deux stades [36]. Une méta-analyse des cofacteurs de transmission hétérosexuelle a rapporté que les probabilités de transmission par relation sexuelle étaient de 2,5/1000 au stade précoce de l’infection, 1,9/1000 au stade tardif comparativement à 1/1000 pour les partenaires de référence dont l’infection était entre ces deux stades [47]. Dans une autre méta-analyse, le risque de transmission hétérosexuelle était respectivement multiplié par 9,2 et par 7,3 lors des stades précoces et tardifs de l’infection comparativement à la phase chronique de l’infection où la charge virale est réduite [40].
D’autres facteurs tels que les rapports sexuels pendant les règles et les saignements coïtaux peuvent aussi influencer la transmission du VIH. En effet, les rapports sexuels pendant les règles augmentent à la fois la susceptibilité des femmes exposées et l’infectiosité des femmes séropositives. Les saignements coïtaux sont aussi associés à un risque accru de transmission sexuelle de l’homme vers la femme [36].
Les efforts déployés depuis plusieurs décennies pour prévenir la transmission du VIH n’ont pas permis de limiter son expansion. Une nouvelle approche paradigmatique, la prévention combinée, apporte désormais un changement de stratégie dans la lutte contre le VIH/SIDA. L’objectif de cette approche est de construire les synergies essentielles entre les stratégies de prévention dites comportementales, structurelles et biomédicales. Les stratégies de prévention comportementales ont pour objectif de changer les comportements individuels et collectifs favorisant la transmission du VIH pour des comportements moins risqués (i.e : la promotion et l’encouragement de l’utilisation constante du préservatif et la réduction du nombre de partenaires sexuels). Les stratégies de prévention structurelles quant à elles agissent plus sur les facteurs sociaux, culturels, économiques, juridiques, et éducatifs susceptibles de fragiliser les personnes les plus exposées à l’épidémie et de faire face aux changements de comportement. En effet, les facteurs de risque structurels augmentent indirectement le risque d'infection au VIH en limitant l'accès aux services de traitement et prévention contre le VIH et les IST. Les facteurs structurels visent à limiter les influences de la pauvreté, la discrimination, la violence physique et sexuelle, la stigmatisation et l’exclusion sociale [7]. Les interventions biomédicales incluent le traitement des IST et la prise de médicaments antirétroviraux par les personnes séropositives et aussi les personnes séronégatives pour la prévention. Les interventions qui visent donc à réduire l’infectiosité d’un individu séropositif auront pour la plupart du temps un effet synergique avec les interventions qui visent à réduire la susceptibilité d’un individu séronégatif. Dans le projet de démonstration E-ART/PrEP, l’approche de la prévention combinée a été privilégiée. Les méthodes de prévention utilisées sont détaillées dans la section suivante [48].
1.5 Méthodes de prévention de la transmission du VIH
1.5.1 Les méthodes de prévention traditionnelles du VIH
Selon la culture et le contexte, les moyens de prévention contre la transmission sexuelle du VIH préconisés incluent l’abstinence, la fidélité mutuelle entre partenaires séronégatifs, l’utilisation correcte et systématique du préservatif et la modification des comportements à risque [49]. L’utilisation correcte et systématique du préservatif durant les rapports sexuels est reconnue comme une mesure de prévention très efficace contre la transmission du VIH et d’autres IST [34, 50-54]. Le préservatif est largement accessible et est le moyen le plus répandu et le plus utilisé pour se protéger et protéger les autres du VIH et autres IST et des grossesses non désirées [55]. Les préservatifs en latex créent une barrière physique imperméable aux agents infectieux des liquides génitaux. De ce fait, l’utilisation du préservatif durant les rapports sexuels demeure la méthode de base pour la prévention de la transmission sexuelle du VIH chez les TS qui, à cause de leur profession, ne sont pas abstinentes et ont plusieurs partenaires sexuels au cours de leur vie.
L’utilisation systématique du préservatif, selon une méta-analyse, conférerait une protection contre l’infection au VIH de 80% avec une variation de 35% à 94% comparativement à sa non utilisation [54]. En Afrique Sub-Saharienne, la prévalence du VIH est plus faible chez les TS utilisant de façon constante le préservatif [56-59]. Au Bénin, à Cotonou plus précisément, la proportion de TS ayant rapporté une utilisation systématique du préservatif avec leurs clients dans les 30 jours précédents a largement augmenté dans les dernières années. En effet, la proportion était de 29,7% en 1993 et a augmenté à 87,7% en 2008 [59]. Simultanément, avec l’augmentation de l’utilisation du préservatif durant la période de 1993 à 2008, les prévalences du VIH et de certaines IST ont diminué. La prévalence du VIH a baissé de 53,3% à 30,4%, celle de la chlamydia de 9,4% à 2,8% et celle de la gonorrhée de 43,2% à 6,4%. L’augmentation de l’utilisation du préservatif chez les TS de Cotonou aurait significativement réduit la prévalence et l’incidence du VIH aussi bien chez les TS que dans la population générale [60].
L’utilisation du préservatif demeure cependant problématique pour certaines TS. Les TS sont souvent peu éduquées, stigmatisées, marginalisées et confrontées à des
violences physiques, sexuelles et psychologiques. Ces facteurs font qu’elles ont moins de capacité à imposer ou négocier l’utilisation systématique du préservatif [61-64]. L’utilisation du préservatif par les TS avec certains de leurs partenaires est souvent sous-optimale, en particulier avec les partenaires réguliers non-payants. En effet, il est rapporté que l’utilisation du préservatif s’avère être faible avec des partenaires/clients réguliers et/ou avec des petits amis [65-67]. Au Bénin, dans une étude de Alary et al., les TS ont rapporté une utilisation moyenne du préservatif de 80% avec les clients dans la dernière semaine précédant l’entretien comparativement à seulement 20% avec leur partenaire régulier [68]. Les partenaires/clients réguliers et/ou petits amis des TS ont souvent d’autres partenaires sexuelles qui ne sont pas des TS [66, 69]. Ces comportements à risque ajoutés à l’utilisation inconsistante du préservatif favorisent la transmission de l’infection au VIH. Il est important de souligner que les informations sur l’utilisation du préservatif sont souvent auto-rapportées et sujettes au biais de désirabilité sociale [70-72]. Ainsi, on s’attend à ce que plusieurs TS surestiment leur utilisation du préservatif. De plus, la prévention du VIH en utilisant le préservatif est confrontée à des limites telles l’utilisation non-systématique, une pose et un usage incorrects et parfois des glissements et des ruptures [63, 73].
1.5.1.2 La circoncision masculine
Plusieurs études ont souligné l’effet protecteur de la circoncision masculine. Cette pratique qui consiste en l’ablation de la majeure partie du prépuce réduirait de 50 à 60 % le risque d’acquisition du VIH chez l’homme [74-76]. Plusieurs arguments sur le plan biologique existent pour expliquer la susceptibilité des hommes non circoncis à l’infection par le VIH. Durant les rapports sexuels, le prépuce est rétracté exposant ainsi le prépuce interne qui abrite un plus grand nombre de cellules cibles du VIH [77, 78]. De plus, le prépuce est sensible aux abrasions et aux déchirements. Aussi, la circoncision peut avoir un effet protecteur en diminuant le risque d’ulcérations génitales associées à un risque élevé d’acquisition du VIH [78]. Un effet protecteur direct de la circoncision masculine n’a pas été clairement observé sur l’infection par le VIH chez les femmes. Cependant, même si la circoncision masculine ne protège
pas directement les femmes, elle aura un effet indirect chez les femmes car avec l’augmentation de cette pratique, l’incidence du VIH chez les partenaires sexuels potentiels diminuera [79, 80]. Depuis 2007, l’Organisation Mondiale de la Santé (OMS) a reconnu les avantages de la circoncision et a recommandé l’intégration de cette pratique comme une stratégie importante de prévention de la transmission hétérosexuelle du VIH de la femme à l’homme [81]. Au Bénin, la circoncision est très courante et la plupart des hommes la font pour des raisons religieuses ou culturelles [4, 82].
Les méthodes de prévention traditionnelles citées n’ont pas permis d’endiguer l’infection à VIH chez les TS au Bénin et la prévalence reste toujours élevée. De nouveaux moyens de prévention complémentaires sont donc nécessaires. La section qui suit détaille les méthodes de prévention biomédicales utilisées dans le projet de démonstration E-ART/PrEP.
1.5.2 Les méthodes de prévention biomédicales du VIH
1.5.2.1 Le traitement des IST
Comme mentionné plus haut, les IST sont des facteurs de risque importants pour l’acquisition et la transmission sexuelle du VIH [42]. Le dépistage et le traitement des IST ont été mis en œuvre depuis les années 1990 pour diminuer la prévalence de ces infections et notamment du VIH par le biais d’organigrammes de prise en charge syndromiques peu coûteux et ne nécessitant pas forcément des tests de laboratoires [83, 84]. Cependant, ce n’est qu’en 1995 que le premier essai clinique a été mené afin d’évaluer l’effet de l’augmentation du dépistage et du traitement des IST sur l’incidence du VIH dans la population générale. Cet essai clinique mené à Mwanza en Tanzanie sur une durée d’environ deux ans auprès de 12,537 hommes et femmes a montré que l’augmentation du traitement des IST avait diminué de 42% l’incidence du VIH dans cette population (rapport d’incidence 0,58 ; IC à 95% : 0,42-0,79) [85]. Par la suite, un autre essai clinique a été conduit à Rakai en Ouganda auprès de 12,726 participants pour évaluer si plusieurs traitements de masse des
IST à 10 mois d’intervalles aurait un effet sur l’incidence du VIH. Les résultats de cet essai Ougandais n’ont montré aucun effet du traitement des IST sur l’incidence du VIH malgré une baisse des IST [86, 87]. Les divergences des résultats de ces deux essais cliniques ne sont nécessairement pas contradictoires mais plutôt complémentaires. Ces divergences peuvent s’expliquer par le fait que les deux essais ont testé différentes interventions dans différents contextes épidémiologiques et avec des méthodes d’évaluation différentes. L’épidémie en Ouganda était beaucoup plus mature avec une incidence et une prévalence élevées et stables dans la population générale alors que celle de la Tanzanie était en progression avec une incidence faible et une prévalence croissante mais faible au moment de l’étude. De plus, la plupart de la transmission se faisait hors des groupes à haut risque d’IST ce qui serait une explication du faible impact de l’intervention [88]. Bien qu’il ressorte de la comparaison de ces deux études que l’impact du traitement des IST sur l’incidence du VIH dépend du stade de l’épidémie, le traitement des IST demeure pertinent pour tout type d’épidémie du VIH. En traitant une personne atteinte d’IST, la durée de susceptibilité accrue au VIH de cette personne est réduite et donc le traitement est pertinent comme une méthode de prévention individuelle. Au Bénin, les premières interventions ciblant les TS ont débuté en 1988 dans un centre de santé communal à Cotonou et consistaient en des soins pour les IST et la promotion du préservatif. Cette clinique ne recevait qu’un nombre limité de TS. Ce n’est qu’en 1992 que le projet Canadien d’appui à la lutte contre le Sida en Afrique de l’Ouest a permis un renforcement et une extension des interventions auprès des TS. Grâce à ce projet, en 1993, le dispensaire de soins IST (DIST) adapté à la prise en charge des TS a été créé et intégré au centre de santé communal [32]. Depuis lors, le DIST offre gratuitement le dépistage et traitement des IST et du VIH ainsi que des préservatifs aux TS de Cotonou. L’étude présentée dans cette thèse a été conduite au DIST et plus de détails seront mentionnés dans le premier article de la thèse.
Ces dernières années ont connu une innovation dans les stratégies de prévention du VIH avec deux méthodes de prévention biomédicales basées sur les ARV: le traitement précoce comme prévention (E-ART) et la PrEP. Ces deux méthodes de prévention biomédicales se sont montrées encourageantes dans la lutte contre l’épidémie du VIH et s’ajoutent aux autres méthodes de prévention telles que la circoncision masculine et l’utilisation du préservatif. L’E-ART consiste au traitement précoce des individus séropositifs indépendamment du statut clinique pour les soigner et diminuer le risque de transmission du VIH aux partenaires non-infectés. En effet, cette stratégie vise à réduire la charge virale des personnes séropositives et donc la probabilité de transmission du virus [45, 89]. Le traitement préventif du VIH est utilisé depuis le milieu des années 1990 pour la prévention de la transmission mère-enfant. En effet, un essai clinique randomisé mené en 1994 a rapporté une réduction de la transmission verticale du VIH de 25% à 8% chez les mères séropositives prenant de la zidovudine avant et pendant l’accouchement [90]. Depuis lors, le dépistage des femmes enceintes et le traitement des mères séropositives avec des ARV pendant la grossesse, l’accouchement et l’allaitement a montré une réduction du risque de transmission aux enfants de plus de 90% [91].
L’administration des ARV aux personnes séropositives était basée sur un décompte de cellules lymphocytaires T CD4 (CD4) servant de proxy pour le statut immunitaire. En 2006, l’OMS recommandait que toutes les personnes séropositives au VIH avec un taux de CD4 inférieur à 200 cellules/mm3 soient éligibles pour un traitement ARV [92]. En 2013, ce seuil est passé à 500 cellules/mm3. Cependant, depuis 2015, l’OMS recommande l’initiation du traitement aux ARV chez toute personne infectée par le VIH, indépendamment de son taux de CD4 ou de son statut clinique [93]. Un essai clinique nommé HPTN 052 est l’étude phare qui a permis de valider la stratégie E-ART. Cet essai clinique multicentrique a été conduit auprès de 1763 couples hétérosexuels sérodiscordants. Les résultats ont montré que le traitement antirétroviral précoce a permis de réduire jusqu’à 96% le risque de transmission sexuelle du VIH au partenaire séronégatif comparativement au traitement à partir d’un seuil de 250 CD4/mm3. Les résultats intermédiaires de cette étude étaient
publiés depuis 2011 [94] et les données définitives ont été publiées en 2016 après 10 années de suivi sur l’ensemble de la cohorte [95]. Par ailleurs, les résultats de HPTN 052 ont également montré un impact positif du E-ART en réduisant l’incidence de la morbidité et de la mortalité de 41% chez les participants séropositifs recevant le traitement précoce comparativement aux participants séropositifs dans le bras du traitement retardé [94]. Dernièrement, l’étude PARTNER, une étude observationnelle prospective de Rodger et al. conduite dans 75 sites de 14 pays européens a aussi confirmé l’efficacité du E-ART pour prévenir la transmission du VIH. L’étude a été menée en deux phases (PARTNER1 et PARTNER2). La première étape conduite de septembre 2010 à mai 2014 a inclus des couples hétérosexuels et homosexuels sérodiscordants tandis que la deuxième phase, une extension jusqu’en avril 2018, a uniquement concerné des couples homosexuels. Dans la première phase, les données de 588 couples hétérosexuels et 340 couples homosexuels ont été analysées. Durant une période médiane de suivi de 1,3 ans par couple, aucune transmission de l’infection à VIH ne s’est produite. Ces couples n’utilisaient aucun moyen de protection à part le fait que le partenaire séropositif était sous traitement ARV et avait une charge virale indétectable. Dans la deuxième phase, sur 76 088 rapports sexuels non-protégés, aucune transmission de l’infection du VIH n’a été observée [96, 97]. Ces résultats fournissent des évidences complémentaires sur l’efficacité du E-ART dans la prévention de la transmission du VIH aussi bien pour les couples homosexuels que les couples hétérosexuels. D’autres études ont aussi rapporté un risque de transmission du VIH moins élevé chez les couples sérodiscordants où le partenaire positif avait une charge virale plasmatique indétectable [98]. L’E-ART peut donc être bénéfique au niveau individuel par la suppression de la charge virale mais aussi au niveau populationnel étant donné une augmentation du dépistage du VIH et la mise sous ARV des séropositifs [98-100]. Depuis 2016, l’organisation américaine « Prevention Access Campaign », une coalition internationale de défenseurs des droits des militants et des chercheurs, fait répandre les données scientifiques en un message simple : « Indétectable= Intransmissible (I=I) ». Ceci a pour but de sensibiliser les personnes
sur le fait qu’une personne sous ARV avec un taux d’observance élevé et une charge virale indétectable maintenue pendant 6 mois ne peut pas transmettre le VIH [101].
1.5.2.3 La prophylaxie pré-exposition (PrEP)
La PrEP consiste à la prise d’un ARV dénommé Truvada (TDF/FTC) avant exposition au VIH par des personnes non-infectées mais à haut risque d’infection afin de réduire le risque d’acquisition du virus. Le Truvada® (TDF/FTC) est une co-formulation de deux ARV à dose fixe c’est-à-dire, chaque comprimé de Truvada® est composé de 200mg d’emtricitabine (FTC) et de 300 mg de tenofovir disoproxil fumarate (TDF) [102]. La réflexion sur l’utilisation de PrEP comme outil de prévention de la transmission sexuelle du VIH est aussi née après la démonstration de l’efficacité d’une prophylaxie antirétrovirale pour la prévention de la transmission mère-enfant du VIH [90, 103-105] et dans des études de primates non-humains où une protection partielle ou totale à l’infection a été observée [106-108]. Au moment de l’étude E-ART/PrEP présentée dans cette thèse, six essais cliniques randomisés (ECR) en double aveugle avaient été complétés dont quatre ont montré l’efficacité de la PrEP orale quotidienne pour la prévention de l’acquisition du VIH [8-13]. Dans ces essais cliniques, les participants recevaient un traitement préventif contre le VIH complémentaire aux méthodes de prévention traditionnelles du VIH (counseling, préservatif, dépistage et traitement des infections sexuellement transmissibles, etc.). Les résultats de quatre essais cliniques « iPrEx [10], Partners PrEP [8], TDF2 Study [9], Bangkok Tenofovir Study (BTS) [11]» ont montré que la prise quotidienne des ARV tenofovir ou tenofovir et emtricitabine (Truvada) avait réduit la transmission du VIH de 44% chez les HARSAH [10], de plus de 70% chez les hétérosexuels [8, 9] et de 49% chez les injecteurs de drogue [11] avec une forte observance aux médicaments. Cependant, deux essais cliniques conduits chez des femmes à haut risque en Afrique, FEM-PrEP[12] et VOICE [13] n’ont pu démontrer l’efficacité de la PrEP quotidienne contre l’acquisition du VIH principalement à cause d’une faible observance au Truvada [12, 13, 109]. Plus de détails sur ces six études citées sont présentés dans le Tableau 1.1.
Sur la base de ces observations, en juillet 2012, le FDA (Food and Drug Administration) a approuvé le traitement quotidien avec Truvada pour la prévention de l’infection au VIH-1 chez les individus non-infectés et ayant un risque élevé d’infection. Le CDC (Centers for Disease Control) a, par la suite, publié des recommandations pour son utilisation par les couples sérodiscordants, les HARSAH et les transgenres [110-114]. En 2015, les recommandations ont été élargies par l’OMS pour que la PrEP soit un choix de prévention supplémentaire pour toute personne s’exposant de façon accrue aux risques d’infection par le VIH. Ces recommandations font suite aux résultats de la revue systématique avec méta-analyse de Fonner et al. qui a rapporté que lorsque l’observance à la PrEP était supérieure à 70%, le risque d’acquisition du VIH était diminué de 70% (risque relatif de 0,30 avec un IC à 95% de 0,21-0,45) [115].
Comme mentionné plus haut, cette thèse se focalise principalement sur la PrEP. De ce fait, les prochaines sections de notre travail seront consacrées aux différents aspects de la PrEP notamment les projets de démonstration, l’importance de l’observance, les différentes mesures d’observance, les facteurs associés à l’observance, la compensation des risques, l’innocuité de cet outil préventif, les modalités de prise de la PrEP et les différentes formes de PrEP.
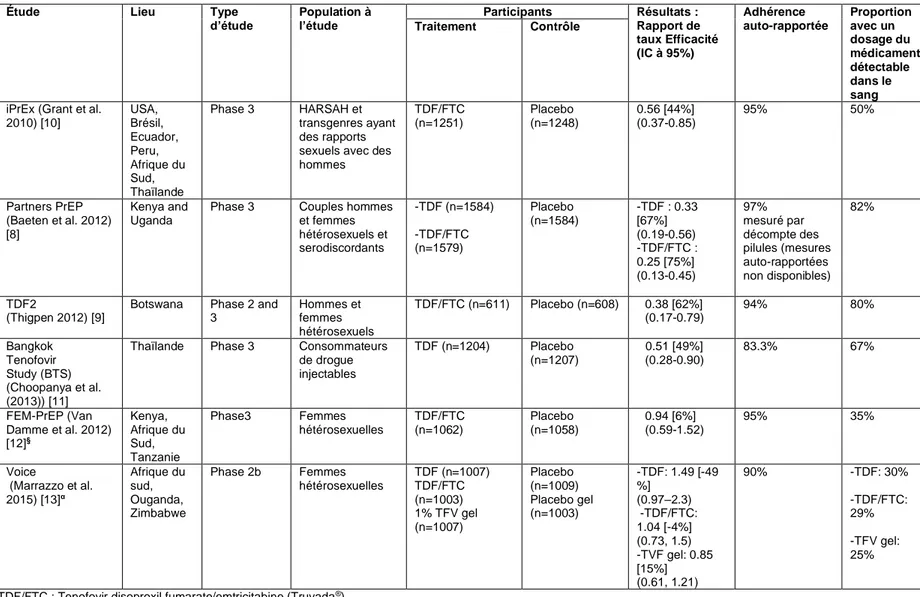
Table 1-1 Résultats des principaux essais cliniques sur la prophylaxie pré-exposition au VIH orale quotidienne (PrEP)
Étude Lieu Type
d’étude Population à l’étude Participants Résultats : Rapport de taux Efficacité (IC à 95%) Adhérence auto-rapportée Proportion avec un dosage du médicament détectable dans le sang Traitement Contrôle
iPrEx (Grant et al. 2010) [10] USA, Brésil, Ecuador, Peru, Afrique du Sud, Thaïlande Phase 3 HARSAH et transgenres ayant des rapports sexuels avec des hommes TDF/FTC (n=1251) Placebo (n=1248) 0.56 [44%] (0.37-0.85) 95% 50% Partners PrEP (Baeten et al. 2012) [8] Kenya and Uganda
Phase 3 Couples hommes et femmes hétérosexuels et serodiscordants -TDF (n=1584) -TDF/FTC (n=1579) Placebo (n=1584) -TDF : 0.33 [67%] (0.19-0.56) -TDF/FTC : 0.25 [75%] (0.13-0.45) 97% mesuré par décompte des pilules (mesures auto-rapportées non disponibles) 82% TDF2 (Thigpen 2012) [9]
Botswana Phase 2 and 3 Hommes et femmes hétérosexuels TDF/FTC (n=611) Placebo (n=608) 0.38 [62%] (0.17-0.79) 94% 80% Bangkok Tenofovir Study (BTS) (Choopanya et al. (2013)) [11]
Thaïlande Phase 3 Consommateurs de drogue injectables TDF (n=1204) Placebo (n=1207) 0.51 [49%] (0.28-0.90) 83.3% 67% FEM-PrEP (Van Damme et al. 2012) [12]§ Kenya, Afrique du Sud, Tanzanie Phase3 Femmes hétérosexuelles TDF/FTC (n=1062) Placebo (n=1058) 0.94 [6%] (0.59-1.52) 95% 35% Voice (Marrazzo et al. 2015) [13]α Afrique du sud, Ouganda, Zimbabwe Phase 2b Femmes hétérosexuelles TDF (n=1007) TDF/FTC (n=1003) 1% TFV gel (n=1007) Placebo (n=1009) Placebo gel (n=1003) -TDF: 1.49 [-49 %] (0.97–2.3) -TDF/FTC: 1.04 [-4%] (0.73, 1.5) -TVF gel: 0.85 [15%] (0.61, 1.21) 90% -TDF: 30% -TDF/FTC: 29% -TFV gel: 25%
TDF/FTC : Tenofovir disoproxil fumarate/emtricitabine (Truvada®)
TFV : Tenofovir
1.6 PrEP : Une innovation dans les stratégies de prévention du
VIH
1.6.1 Les modalités de prise de la PrEP
La PrEP peut être prise selon deux modes d’emploi, une prise quotidienne ou de façon intermittente (ou PrEP à la demande). La prise quotidienne consiste à prendre un comprimé de Truvada tous les jours. À ce jour, c’est la modalité recommandée pour toutes les personnes à haut-risque d’infection au VIH [116]. Les données pharmacologiques suggèrent que les concentrations de Truvada pouvant conférer une protection sont atteintes entre 4 à 7 jours après le début de la prise chez les HARSAH et après 7 jours chez les femmes [117].
La PrEP intermittente consiste à prendre deux comprimés de Truvada entre 2 heures et 24 heures avant le rapport sexuel puis un comprimé 24 heures après la première prise et un autre comprimé 24 heures après la seconde prise. Pour la PrEP intermittente, les comprimés sont donc utilisés que lorsque la personne prévoit des rapports sexuels dans les prochaines heures. L’efficacité de ce mode d’emploi n’a été démontré que chez les HARSAH à haut risque de contracter le VIH [116]. L’étude IPERGAY est le premier essai clinique de la PrEP intermittente chez les HARSAH. L’étude a été conduite au Canada et en France et a montré une efficacité de 86% (IC à 95% :40-98%) de la PrEP intermittente. Dans cette étude, le groupe contrôle a même été interrompu à cause de l’efficacité de la PrEP et tous les participants ont reçu la PrEP [118]. En 2017, une étude de démonstration ouverte avec les participants de IPERGAY (ANRS-IPERGAY) a aussi confirmé l’efficacité de la PrEP intermittente chez les HARSAH avec une réduction de l’incidence du VIH de 97% comparativement au groupe contrôle [119]. En 2018, suite à une analyse intérimaire d’une étude de démonstration en cours sur la PrEP continue et la PrEP intermittente dans différentes populations, l’OMS a recommandé la PrEP intermittente pour les HARSAH comme autre possibilité de prévention [116].