Impact d’un programme modifiant les habitudes de vie
sur la fonction diastolique ventriculaire gauche dans le
syndrome métabolique
Mémoire
Jacinthe Leclerc
Maîtrise en sciences pharmaceutiques
Maître ès sciences (M.Sc.)
Québec, Canada
© Jacinthe Leclerc, 2014
Résumé
Il est reconnu que les changements au niveau des habitudes de vie ont des impacts favorables sur la santé cardiovasculaire. La dysfonction diastolique ventriculaire gauche est d’ailleurs un problème cardiaque très répandu. La réversibilité de ce trouble cardiaque suite à une intervention non-pharmacologique a peu été étudiée. Dans le cadre de cette maîtrise, il a été observé que la dysfonction diastolique est réversible suite à un programme de modification des habitudes de vie d’une durée d’un an. Les déterminants, en début d’étude, qui caractérisaient les participants ayant amélioré leur fonction diastolique en cours d’intervention étaient une tolérance au glucose détériorée, une tension artérielle systolique à l’effort plus élevée ainsi qu’une meilleure performance lors de l’épreuve maximale d’effort. Les bénéfices significatifs gagnés en cours de programme au niveau des différents indices d’adiposité, de la résistance à l’insuline ainsi que de la tolérance à l’effort n’étaient pas reliés à l’amélioration de la dysfonction diastolique.
Abstract
It is known that lifestyle changes have positive impact on cardiovascular risk factors. Left ventricular diastolic dysfunction is certainly the most prevalent cardiovascular disease. Not a lot is found in the literature regarding the reversibility of this dysfunction. During this project, it was observed that diastolic dysfunction is reversible following a 1-year lifestyle modification program. Baseline characteristics of participants who improved their diastolic function were an impaired glucose tolerance, a higher systolic blood pressure at maximal effort as well as a better performance at maximal effort test. Changes in adiposity measures, insulin resistance and exercise tolerance induced by this program did not correlate with improvements in diastolic function.
Table des matières
Résumé...I Abstract ... V Table des matières ... VII Liste des tableaux... X Liste des figures ... XI Liste des abréviations et des sigles ... XIII Avant-propos ... XIV
Chapitre 1 : Introduction ... 1
Chapitre 2.1 : Prévention et facteurs de risque cardiovasculaires ... 3
Prévention ... 4
Les facteurs de risque des maladies cardiovasculaires ... 4
Âge, sexe et ethnicité ... 4
Histoire familiale et environnement ... 6
Facteurs de risque comportementaux ... 8
Tabagisme... 8
Obésité ... 9
Sédentarité ... 10
Qualité nutritionnelle ... 11
Facteurs de risque biologiques ... 13
Hypertension artérielle ... 13
Hypercholestérolémie ... 14
Hyperglycémie ... 15
Chapitre 2.2 : Le syndrome métabolique ... 17
L’hyperglycémie ... 17
L’hypertension artérielle ... 19
La dyslipidémie ... 20
L’obésité abdominale ... 21
Chapitre 2.3 : Obésité viscérale et syndrome métabolique en cardiologie ... 24
Les effets métaboliques de l’obésité ... 26
Glande endocrine ... 27
Augmentation de la demande métabolique ... 27
Impact de l’obésité en cardiologie ... 27
Impact fonctionnel ... 28
Impact électrophysiologique ... 28
Impact circulatoire ... 28
Impact d’une perte de poids ... 29
1. Impact fonctionnel ... 29
2. Impact électrophysiologique ... 29
3. Impact circulatoire ... 29
Chapitre 2.4 : Dysfonction diastolique ventriculaire gauche ... 31
Anatomie et physiologie du cœur ... 31
La diastole et ses déterminants ... 34
La relaxation isovolumétrique ... 35
Le remplissage rapide du ventricule ... 36
Diastase ... 36
La systole auriculaire ... 37
Les déterminants de la fonction diastolique ... 37
Dysfonction diastolique et insuffisance cardiaque ... 38
Les grades de dysfonction diastolique ... 46
Traitements de la dysfonction diastolique ... 47
Chapitre 2.5 : Évaluation de la tolérance à l’effort ... 49
Indications ... 49
Modalités ... 50
Protocole ... 51
Test d’effort sous-maximal vs. maximal ... 53
Variables (valeurs normales) et interprétation ... 54
Chapitre 2.6 : Interventions préventives et curatives de l’obésité et du syndrome métabolique ... 58
Activité physique ... 60 Chapitre 3.1 : La recherche ... 63 Problématique ... 63 Chapitre 3.2 : Méthodologie ... 65 Schéma de l’étude ... 65 Interventions ... 65 Chapitre 3.3 : Résultats ... 69
Caractéristiques de la réversibilité de la dysfonction diastolique ventriculaire gauche ... 69
Réduction de l’adiposité ... 70
Amélioration de la tolérance à l’effort ... 70
Amélioration de l’intolérance au glucose ... 72
Chapitre 3.4 : Discussion ... 76
Aucune corrélation entre la réversibilité de la DDVG et les mesures d’adiposité... 77
Tension artérielle systolique maximale supérieure pour le groupe ayant amélioré leur DDVG ... 78
Limitations ... 79
Liste des tableaux
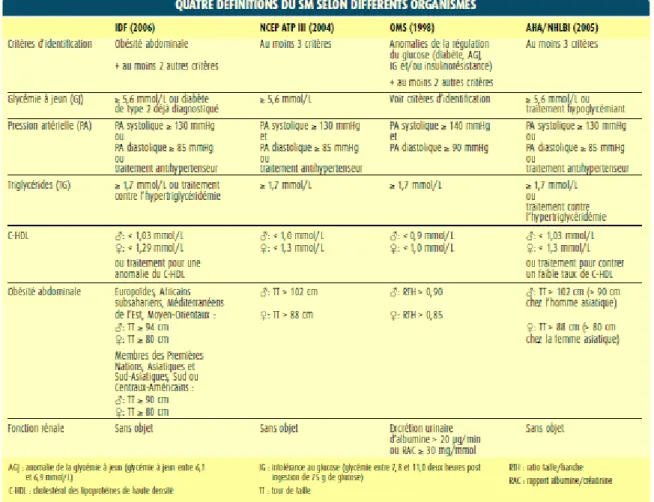
Tableau 1 : Quatre définitions du SMet selon différents organismes ... 18
Tableau 2 : Critères de Framingham pour l’insuffisance cardiaque ... 39
Tableau 3 : Grades de dysfonction diastolique ... 47
Tableau 4 : Protocole de Bruce ... 52
Tableau 5 : Caractéristiques au départ et 1 an post-intervention selon l’amélioration de la DDVG ... 74
Tableau 6 : Caractéristiques de la fonction diastolique ventriculaire gauche pré et post intervention d’un an ... 75
Liste des figures
Figure 1 : Facteurs de risque cardiovasculaire... 5
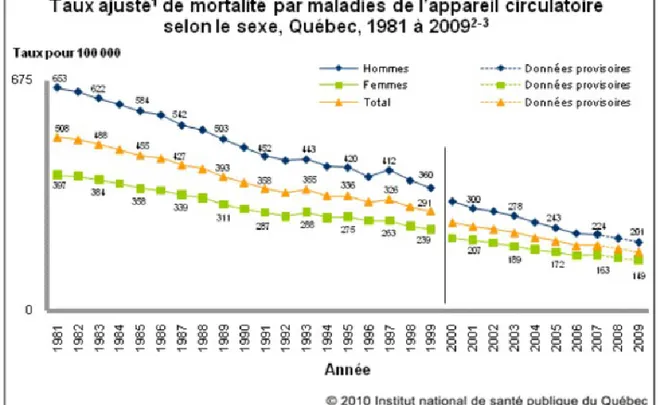
Figure 2 : Taux ajusté de mortalité par maladies de l'appareil circulatoire selon le sexe, Québec, 1981 à 2009 ... 6
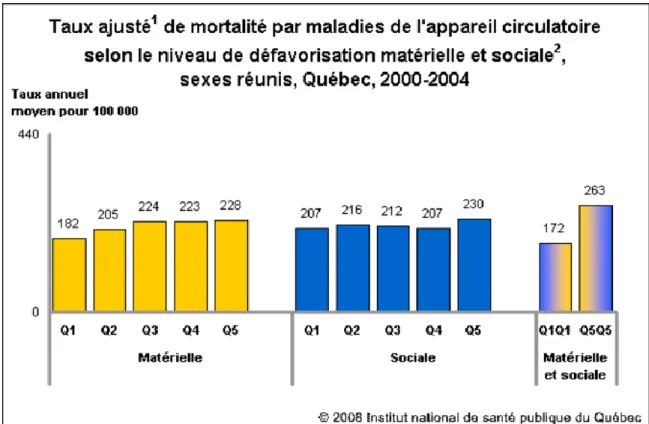
Figure 3 : Taux ajusté de mortalité par maladies de l’appareil circulatoire selon le niveau de défavorisation matérielle et sociale, sexes réunis, Québec, 2000-2004... 7
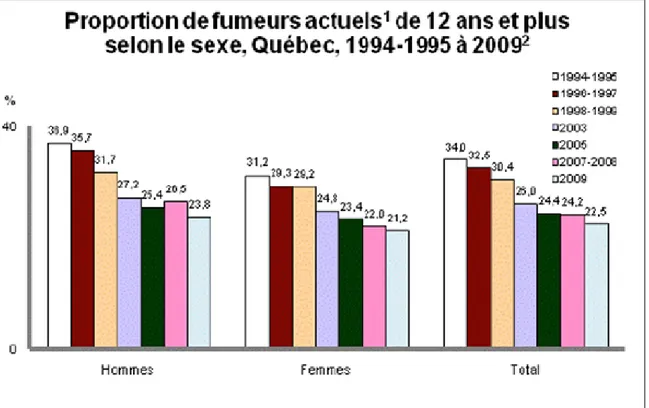
Figure 4 : Proportion de fumeurs actuels de 12 ans et plus selon le sexe, Québec, 1994-1995 à 2009 ... 8
Figure 5 : Proportion de la population de 18 ans et plus souffrant d'obésité selon le sexe, Québec, 1987 à 2009 ... 9
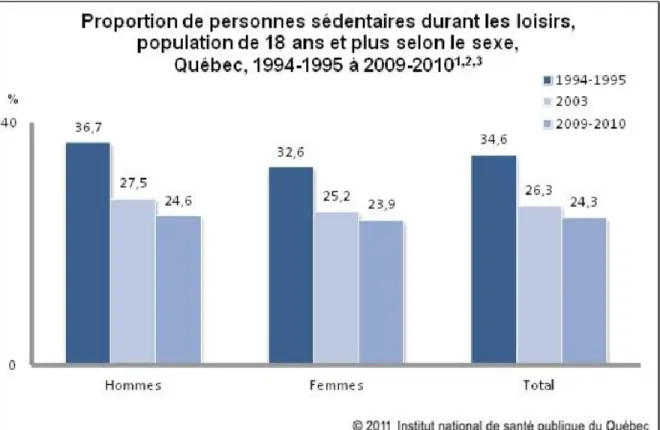
Figure 6 : Proportion de personnes sédentaires durant les loisirs, population de 18 ans et plus selon le sexe, Québec, 1994-1995 à 2009-2010 ... 11
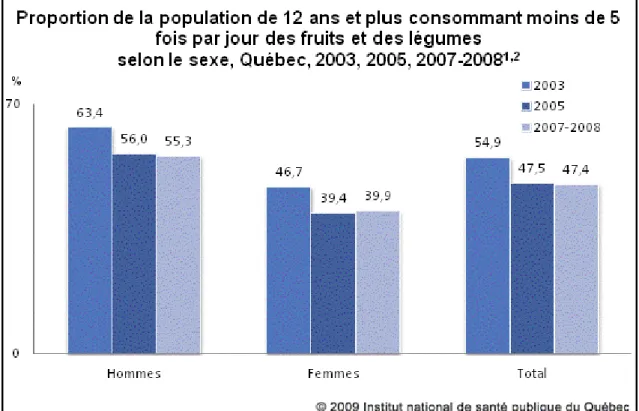
Figure 7 : Proportion de la population de 12 ans et plus consommant moins de 5 fois par jour des fruits et des légumes selon le sexe, Québec, 2003, 2005, 2007-2008 ... 13
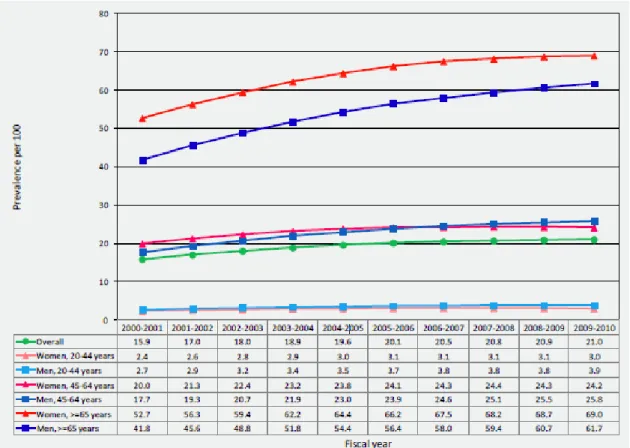
Figure 8 : Prévalence relative brute d’hypertension artérielle au Québec en 2009-2010 ... 14
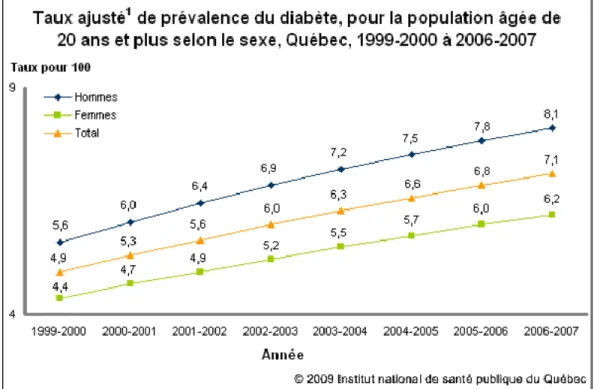
Figure 9 : Taux ajusté de prévalence du diabète, pour la population âgée de 20 ans et plus selon le sexe, Québec, 1999-2000 à 2006-2007 ... 15
Figure 10 : Forme androïde (obésité viscérale) vs. gynoïde (obésité sous-cutané) ... 25
Figure 11 : Image issue de la tomodensitométrie pour la quantification du tissu adipeux viscéral ... 26
Figure 12 : Cavités et parois du coeur ... 31
Figure 13 : Anatomie du coeur ... 32
Figure 14 : Circulation cardiovasculaire ... 33
Figure 15 : Phases du cycle cardiaque ... 35
Figure 16 : Exemple d’image obtenue à l’échocardiographie, au Doppler pulsé, au niveau mitral. ... 41
Figure 17 : Exemple d’image obtenue à l’échocardiographie, au Doppler pulsé, au niveau des veines pulmonaires. ... 43
Figure 18 : Exemple d’image obtenue à l’échocardiographie, au Doppler tissulaire, au niveau du septum. ... 44
Figure 19 : Exemple d’image obtenue à l’échocardiographie, au Doppler couleur M-Mode, au niveau de l’apex. ... 45
Figure 20 : Échelle d’effort perçu de Borg ... 51
Figure 21 : Nomogramme de Duke ... 57
Figure 22 : Réversibilité de la dysfonction diastolique suite à l’intervention d’un an ... 69
Figure 24 : Diminution du tissu adipeux viscéral (cm3) suite à l’intervention d’un an ... 71
Figure 25 : Amélioration de la tolérance à l’effort suite à l’intervention d’un an ... 72 Figure 26 : Glycémie à jeun et post-OGTT suite à l’intervention d’un an ... 73
Liste des abréviations et des sigles
ACSM : American College of Sports Medecine AHA : American Heart Association
ATP : Adénosine triphosphate
AUC : Aire sous la courbe (area under the curve) CT : Circonférence de taille
C-HDL : Lipoprotéines de haute densité C-LDL : Lipoprotéines de faible densité C-VLDL : Lipoprotéines de très faible densité DASH : Dietary Approaches to Stop Hypertension DDVG : Dysfonction diastolique ventriculaire gauche DT : Temps de décélération
HOMA-IR : Homeostasis model assessment of insulin resistance IC : Intervalle de confiance
IDF : International Diabetes Federation IMC : Indice de masse corporelle
IUCPQ : Institut universitaire de cardiologie et de pneumologie de Québec IVRT : Temps de relaxation isovolumétrique (isovolumetric relaxation time) MAPA : Mesure ambulatoire de la pression artérielle
MCV : Maladies cardiovasculaires METs : Équivalents métaboliques
NCEP ATP III : National Cholesterol Education Program Adult Treatment Panel III NHLBI : National Heart, Lung and Blood Institute
OGTT : Oral glucose tolerance test OMS : Organisation mondiale de la santé
RPP MAX : Double-produit à l’effort maximal (rate-pressure product) SMet : Syndrome métabolique
TAS MAX : Tension artérielle systolique maximale à l’effort TG : Triglycérides
VAT : Tissu adipeux viscéral (visceral adipose tissue) VO2max : Consommation d’oxygène par les tissus Vp : Vélocité de propagation
Avant-propos
Au moment où j’écris ces lignes, je m’apprête à entamer ma 23e rentrée scolaire. Toute jeune, je trouvais le jour de la rentrée scolaire aussi excitant que la journée de Noël. Croyez-le ou non, c’est toujours le cas aujourd’hui. Bien que ma motivation vis-à-vis à l’école soit toujours restée aussi importante dans ma vie, mon ambition face à ma carrière a quant à elle, évolué. Enfant, je me voyais devenir astronaute. Adolescente, je visais plutôt le domaine de la santé. Jeune adulte, j’ai connu les forces armées canadiennes et débuté mes études en soins infirmiers. Plus de 10 ans plus tard, je suis maintenant femme, mère de famille, carriériste sur le marché du travail, et fière d’avoir complété une maîtrise qui m’a énormément appris, tant au niveau personnel que professionnel.
Je dois l’admettre, j’ai jusqu’à maintenant eu la chance de rencontrer les bonnes personnes aux bons moments. Chronologiquement, ma carrière dans les forces canadiennes, mon baccalauréat et mon travail comme nouvelle infirmière à l’urgence d’un hôpital spécialisé en traumatologie, mon entrée dans l’industrie pharmaceutique, mon retour à ma région natale puis la réalisation de cette maîtrise sont toutes des étapes marquantes de ma courte carrière que je dois, en partie, à la rencontre de gens extraordinaires m’ayant encouragée et supportée. J’en suis très reconnaissante. Tout particulièrement, je dois souligner le support et les encouragements de mon conjoint, Guillaume, ainsi que de mes parents, André et Danielle, qui comprennent mon besoin d’accomplissement et de perfectionnement. Également, mon directeur de maîtrise, Dr Paul Poirier, qui comprend la réalité de plusieurs occupations à temps complet : le travail, le rôle de parent et le désir d’avancer ainsi que la nécessité de se perfectionner. Enfin, je suis reconnaissante d’avoir un petit garçon de trois ans tout aussi débordant d’énergie que curieux : « Maman, il est où ton cœur? Je veux l’écouter avec ton stéthoscope. » J’espère pouvoir lui transmettre ma passion et mon enthousiasme pour l’école, car toutes ces années qu’il passera à étudier seront tellement plus intéressantes avec la flamme ardente d’en apprendre toujours davantage.
Chapitre 1 : Introduction
Au Canada, la prévalence du syndrome métabolique (SMet) est de 19,1% [1]. Cette condition implique incontestablement un risque accru de diabète et de maladies cardiovasculaires. Le lien entre le SMet et la résistance à l’insuline est déjà établi, une glycémie élevée étant d’ailleurs l’une des caractéristiques du SMet. S’additionnent à cela l’obésité abdominale, l’hypertension artérielle et la dyslipidémie qui sont les autres critères du SMet [2-4]. Ces critères sont également des facteurs de risque cardiovasculaires [5].
Quant à elle, la dysfonction diastolique est l’anomalie cardiaque la plus fréquente. Présente chez plus de 25% des adultes de plus de 40 ans, elle est indépendamment reliée à l’âge et à l’obésité [6]. Ce problème se manifeste tout particulièrement lorsque le tissu adipeux s’est accumulé au niveau abdominal [7]. Ce tissu graisseux trop abondant entraîne, d’une part, une demande métabolique accrue, un surcroît de volume liquidien pour subvenir aux besoins et une surcharge de travail au cœur [8]. D’autre part, des altérations mécaniques du myocarde (lipotoxicité) et de la fonction endothéliale par la sécrétion d’adipokines pourraient contribuer à la détérioration de la fonction cardiaque [8]. Des études ont évalué la relation transversale entre la présence de dysfonction diastolique, le tissu adipeux viscéral, la résistance à l’insuline et l’intolérance à l’effort [9, 10]. Par contre, les études actuellement disponibles ont étudié la réversibilité de seulement certaines caractéristiques de la dysfonction diastolique et l’association avec seulement l’une ou l’autre des deux variables précédemment citées [11-19].
Sur une période de trois ans, le laboratoire du Dr Després et du Dr Poirier a suivi une centaine d’hommes âgés de 30 à 65 ans souffrant d’obésité viscérale dans le cadre du programme de recherche « Synergie ». Ce programme proposait une modification des habitudes de vie par l’alimentation saine et la pratique d’activité physique, le tout encadré par des professionnels de la santé. Les résultats obtenus à la visite d’un an ont été évalués afin de connaître les déterminants de l’amélioration de la fonction diastolique ventriculaire
gauche par rapport à la variation de la composition corporelle en termes de distribution de la graisse, la variation de la résistance à l’insuline ainsi que l’amélioration de la capacité à l’effort. Les travaux ont été conduits dans le but de tester trois hypothèses :
1- Une diminution de l’adiposité viscérale par la modification des habitudes de vie dans le cadre d’un programme tel que « Synergie » entraînera une amélioration de la fonction diastolique du ventricule gauche;
2- Il y aura une association entre l’amélioration de la dysfonction diastolique du ventricule gauche et l’amélioration de la résistance à l’insuline;
3- L’amélioration de la capacité à l’effort sera associée à l’amélioration de la dysfonction diastolique ventriculaire gauche.
Ainsi, le présent travail a impliqué l’analyse des données d’échocardiographie et de tomodensitométrie, puis l’analyse des résultats du test oral de tolérance glucose et du test de tolérance à l’effort obtenus avant et après l’intervention d’un an. Les méthodes d’analyses sont détaillées au chapitre 3.
Dans la première section de ce mémoire, la plus récente littérature y sera résumée concernant les facteurs de risque cardiovasculaires, le SMet, l’obésité viscérale et la cardiologie, la dysfonction diastolique, l’évaluation de la tolérance à l’effort et finalement, les interventions préventives et curatives de l’obésité viscérale. La deuxième et dernière section de ce mémoire présentera la problématique de recherche, la méthodologie, les résultats et la discussion de ces derniers.
Chapitre 2.1 : Prévention et facteurs de risque cardiovasculaires
La moitié des décès dans le monde est attribuable aux maladies cardiovasculaires (MCV) [20]. La prévention des facteurs de risque est donc primordiale pour diminuer le fardeau sociétal, familial et individuel relié à ces problèmes chroniques de santé. Cette section discutera de l’épidémiologie des MCV, des facteurs de risque cardiovasculaires ainsi que de la prévention qui y est reliée.
Du point de vue de l’épidémiologie, les MCV incluent les maladies du cœur proprement dites, les maladies vasculaires cérébrales ainsi que les maladies des vaisseaux périphériques [5]. Bien qu’elles ne comptaient que pour 31% de toutes les maladies existantes au monde en 2008, près de la moitié de la mortalité globale était reliée aux MCV [20]. L’infarctus du myocarde domine les causes de mortalité cardiovasculaire chez l’homme (46%) alors que chez la femme, les maladies vasculaires cérébrales et les infarctus sont presque à parité, soit à 37 et 38% respectivement [20]. Plus près de chez nous, le taux de mortalité canadien standardisé pour l’âge, pour les MCV, était de 151,9 pour 100 000 habitants en 2007 [21]. Aux États-Unis, les MCV sont aussi la cause principale de morbidité et de mortalité. D’ailleurs, un groupe d’experts travaille activement sur les objectifs américains de santé cardiovasculaire [5]. Ce comité, créé en 2008, a émis des recommandations de santé publique qui ont été approuvées par l’American Heart Association (AHA) [5]. Leur objectif était le suivant : « D’ici 2020, améliorer la santé cardiovasculaire de tous les américains de 20% et réduire la mortalité causée par les MCV de 20% » (traduction libre, [5]). Ainsi, il a été noté que la diminution spécifique du taux de décès suite aux maladies coronariennes entre 1980 et 2000 était en partie due (50%) à la diminution des facteurs de risque tels que l’hypercholestérolémie, l’hypertension artérielle et le tabagisme. L’utilisation étendue des traitements efficaces contre les MCV expliquent l’autre moitié de la diminution des décès de cause coronarienne [5]. Le fardeau global des MCV n’a cependant pas diminué depuis 1980 étant donné que la prévalence du diabète et de l’obésité sont en constante croissance; ils sont eux-mêmes des facteurs de risque de MCV [5].
Prévention
En cardiologie, les concepts de prévention primaire et secondaire sont bien connus par la plupart des cliniciens [5]. Dans la littérature, la prévention primaire réfère aux efforts voués à prévenir le premier évènement cardiovasculaire chez des individus à risque [5]. Par exemple, un individu souffrant d’hypertension artérielle peut modifier ses habitudes de vie et se faire prescrire un médicament antihypertenseur dans le but de prévenir un accident vasculaire cérébral [5]. Une équipe américaine pousse le concept de prévention primaire à un second niveau; selon eux, il devrait être appliqué à tous, peu importe le niveau de risque de chacun [5]. Le groupe explique son idée par des revues de littérature prouvant que même chez les individus jeunes et en santé, certains facteurs de risque des MCV s’accumulent inévitablement au fil du temps. Des stratégies préventives au niveau populationnel sont donc favorables à l’amélioration de la santé de la population [5].
Les facteurs de risque des maladies cardiovasculaires
Les facteurs de risque des MCV se classent en deux catégories (Figure 1) : 1) non-modifiables et 2) non-modifiables. Les facteurs de risque non-non-modifiables sont bien connus : l’âge, le sexe, l’ethnicité, l’histoire familiale et l’environnement [22, 23].
Âge, sexe et ethnicité
Le vieillissement, le sexe masculin (Figure 2) et les individus de race noire sont des facteurs reliés à une morbidité cardiovasculaire accrue [22, 23]. En effet, l’Organisation mondiale de la santé a subdivisé la population mondiale en 14 régions pour ensuite évaluer les proportions du risque cardiovasculaire sur 10 ans. Le risque d’évènement cardiovasculaire augmente progressivement avec l’âge, et il est particulièrement marqué chez les hommes et dans certaines régions américaines, où la proportion peut s’élever jusqu’à 54,2% [23]. Étant donné que les facteurs de risque sont cumulatifs et que leurs effets perdurent dans le temps, il est pertinent d’adopter des comportements visant à réduire les facteurs de risque modifiables pour vivre le plus longtemps possible sans maladie [24].
Figure 1 : Facteurs de risque cardiovasculaire
Histoire familiale et environnement
Les facteurs familiaux susceptibles d’influencer la santé cardiovasculaire sont transmis des parents aux enfants dans les familles à risque. Ces facteurs ne concernent pas seulement les gènes, mais aussi l’environnement culturel, les habitudes de vie familiales, la pauvreté et l’interaction entre tous ces facteurs [22]. Un individu avec une histoire paternelle d’accident vasculaire cérébral aura un risque relatif de développer le même problème de santé de 2,4 (IC 95%, 0,96-6,03). Lorsque l’histoire provient du côté maternel, le risque relatif se situe à 1,4 (IC 95%, 0,6 Ŕ 3,25) [22]. Un faible niveau socio-économique est relié à une mortalité cardiovasculaire accrue [25]. Au Québec, les individus se situant dans le cinquième quintile du niveau socio-économique avaient un taux annuel moyen de décès de 263 par 100 000 habitants en 2000-2004 (Figure 3). En guise de comparaison, ce taux ne
Figure 2 : Taux ajusté de mortalité par maladies de l'appareil circulatoire selon le
s’élevait qu’à 172 décès par 100 000 habitants pour la même période, pour les gens se situant dans le premier quintile, soit les plus fortunés [25].
Les facteurs de risque modifiables, quant à eux, sont également bien documentés. Ils sont d’ailleurs les bases du « 2020 Impact Goal » pour l’amélioration de la santé cardiovasculaire aux États-Unis [5]. Le groupe de travail les divise en deux sous-groupes, soit; 1) les comportements de santé et, 2) les facteurs de santé biologiques. Ces facteurs de risque comportementaux sont le tabagisme, l’obésité, la sédentarité et la malnutrition. Les facteurs de risques de santé biologiques sont l’hypercholestérolémie, l’hypertension artérielle et l’hyperglycémie [5, 22].
Figure 3 : Taux ajusté de mortalité par maladies de l’appareil circulatoire selon le
Facteurs de risque comportementaux Tabagisme
En 2009, la proportion de fumeurs s’élevait à 22,5% au Québec (Figure 4) [26]. Les conséquences néfastes de la cigarette sur la santé cardiovasculaire ont été abondamment décrites dans les dernières années [27]. D’ailleurs, une baisse de la proportion de fumeurs de l’ordre d’environ 12% a été notée depuis 1994 [26]. La baisse la plus importante a été observée chez les hommes (13,1%), bien qu’ils soient toujours plus « fumeurs » que les femmes (23,8 vs. 21,2%) [26]. Il faut se rappeler que le sexe masculin est aussi plus sujet aux MCV. Pour rencontrer le critère idéal de santé cardiovasculaire, l’adulte âgé de plus de 20 ans ne devrait jamais avoir fumé ou avoir cessé il y a plus d’un an [5]. Les jeunes de 12 à 19 ans ne devraient jamais avoir essayé de fumer ou ne pas avoir fumé une cigarette entière [5].
Figure 4 : Proportion de fumeurs actuels de 12 ans et plus selon le sexe, Québec,
Obésité
L’obésité se définit par un indice de masse corporelle (IMC) équivalent ou supérieur à 30 kg/m2 [20]. En 2009, au Québec, 17% des adultes souffraient d’obésité (Figure 5). La tendance est à la hausse depuis la fin des années 1980, où l’on n’observait que 8% de québécois obèses [28]. Ici encore, les hommes se démarquent avec une augmentation plus importante (plus de 2,5 fois) de la proportion d’obèses par rapport à 1987. Lloyd-Jones et al ont utilisé la valeur d’IMC de 25 kg/m2et moins pour le critère de santé cardiovasculaire optimale [5]. Pour les enfants et les jeunes adultes (2 à 19 ans), il devrait se situer sous le 95e percentile d’IMC [5]. Une étude a d’ailleurs associé le surplus de poids (IMC entre 25,0 et 29,9 kg/m2) chez les enfants avec la fréquence des annonces publicitaires de malbouffe à la télévision [20]. La prévalence de surpoids dans la population était directement reliée à la fréquence des publicités, les États-Unis remportant la première position avec une fréquence de 200 publicités de malbouffe par 20 heures de télévision. Ceci était associé à une prévalence de surpoids de 26% [20].
Figure 5 : Proportion de la population de 18 ans et plus souffrant d'obésité selon le sexe,
Sédentarité
Depuis les années 1990, le taux de sédentarité pendant les périodes de loisirs a diminué de 30,0% au Québec (Figure 6). En effet, se situant aux alentours de 34,6% au milieu des années 1990, la proportion d’adultes sédentaires en dehors des heures de travail se retrouvait à 24% en 2009-2010 [29]. Les hommes sont 33% moins sédentaires depuis 1995 alors que cette amélioration se situe à 27% pour les femmes. Les bénéfices sur la santé cardiovasculaire se manifestent à partir de 150 minutes d’activité physique d’intensité modérée par semaine [5]. La quantité de bénéfices gagnés est même dépendante de la « dose » d’activité physique. Les recommandations de pratique d’activité physique pour une santé cardiovasculaire optimale vont donc en ce sens : 150 minutes/semaine et plus, d’intensité modérée comme la marche, ou 75 minutes et plus d’intensité élevée [5]. Pour les jeunes de 12 à 19 ans, il est recommandé de pratiquer 60 minutes et plus d’activité physique d’intensité modérée à élevée chaque jour, ce qui équivaut à 420 minutes et plus par semaine [5]. Le terme « sédentarité » a récemment été différencié du terme « comportement sédentaire » dans la littérature [30, 31]. Ainsi, il a été suggéré d’utiliser l’adjectif « inactif » pour décrire les individus ne faisant pas suffisamment d’activité d’intensité modérée à vigoureuse. En contrepartie, un comportement sédentaire serait plutôt toutes activités à basse dépense énergétique (≤ 1,5 METs) pendant de la période d’éveil, en position assise par exemple [30, 31].
Qualité nutritionnelle
L’alimentation est un sujet très médiatisé depuis quelques années. Tout particulièrement, l’alimentation saine, les chroniques d’experts, les livres visant la prévention des maladies par les aliments et l’exercice sont populaires auprès du public québécois. Cependant, 47% des québécois de 12 ans et plus ne consommaient pas les portions recommandées de fruits et de légumes, en 2007-2008 (Figure 7). Heureusement, la tendance est à la hausse depuis 2003 : les québécois mangent 14% plus de fruits et de légumes en 2008 vs. 2003 [32]. Le groupe de travail de l’AHA [5] a créé un score d’alimentation-santé (Healthy-diet score) dans le but de standardiser l’évaluation du facteur de risque cardiovasculaire qu’est la qualité nutritionnelle. D’après eux, les bases de l’alimentation devraient se construire selon un plan alimentaire reconnu comme la diète DASH (Dietary Approaches to Stop
Hypertension, [33]). Ainsi, le score d’alimentation-santé se calcule en fonction de cinq
critères précis, fondés sur une diète d’environ 2000 kcal par jour :
Figure 6 : Proportion de personnes sédentaires durant les loisirs, population de 18 ans
1. Fruits et légumes : ≥ 1,1 l (4,5 tasses) par jour;
2. Poisson : ≥ 2 portions de 105 ml (3,5 oz) par semaine (préférablement des poissons gras);
3. Grains entiers riches en fibres ( ≥ 1,1 g de fibres par 10 g de glucides) : ≥ trois portions de 30 ml (1 oz) par jour;
4. Sodium : ˂ 1500 mg par jour;
5. Breuvages sucrés : ≤ 450 kcal (1,1 l ou 36 oz) par semaine.
Un adulte âgé de 20 ans et plus étant en mesure d’additionner quatre à cinq de ces critères présente un niveau de qualité nutritionnelle optimale. Un individu n’ayant que deux ou trois de ces critères aura un niveau intermédiaire de santé cardiovasculaire tandis que l’obtention de 0 à 1 critère équivaut au niveau le plus bas de santé cardiovasculaire [5]. Les niveaux se classent de la même façon pour les enfants et les jeunes de 5 à 19 ans. Aux États-Unis, la base de données issue des Centers for Disease Control and Prevention via le sondage d’évaluation nationale sur la santé et la nutrition (NHANES 2005-2006, [34]) a permis d’estimer la prévalence de chacun des niveaux de risque relié aux critères de qualité nutritionnelle. Ainsi, la majorité des adultes et des jeunes se trouvaient au niveau le plus bas en 2005-2006, avec des proportions de 76% et 91% respectivement.
Facteurs de risque biologiques Hypertension artérielle
L’hypertension artérielle touchait 24% de la population québécoise en 2009-2010 [35]. Les hommes et les femmes âgés de plus de 65 ans sont les plus affectées par cette maladie (Figure 8). L’hypertension artérielle est en tête des facteurs de risque quant aux nombre de décès cardiovasculaires (13%), suivi par le tabagisme (9%), la sédentarité (6%) et l’obésité (5%) [20]. Pour une santé cardiovasculaire optimale, la tension artérielle chez les adultes de plus de 20 ans ne devrait pas dépasser 120/80 mmHg [5, 36]. Chez les jeunes de 12 à 19 ans, la tension artérielle devrait se situer en-dessous du 90e percentile [5].
Figure 7 : Proportion de la population de 12 ans et plus consommant moins de 5 fois
Hypercholestérolémie
L’hypercholestérolémie se caractérise par un taux élevé de cholestérol dans le sang. De 2009 à 2011, 39% des canadiens avaient une cholestérolémie supérieure à 6,2 mmol/L (240 mg/dl) [37], considérée comme élevée et risquée [38]. Le niveau de risque relié au cholestérol total se définit par un taux équivalent ou supérieur à 5,2 mmol/L (200 mg/dl) [5, 38]. Concernant le cholestérol-LDL, le seuil optimal devrait être inférieur à 2,6 mmol/L (100 mg/dl) [38], des lignes directrices récentes suggèrent même 2,3 mmol/L (90 mg/dl) [39]. L’Europe est la région où la prévalence de l’hypercholestérolémie est la plus élevée (56 à 73%), alors que les pays asiatiques et sud-africains sont les moins touchés par cette maladie (14 à 32%) [37]. Le groupe de travail du « 2020 Impact Goal » spécifie donc que les individus ayant un taux de cholestérol total équivalent ou supérieur à 6,2 mmol/L se situent au niveau de santé cardiovasculaire le moins favorable [5]. Le niveau intermédiaire
Figure 8 : Prévalence relative brute d’hypertension artérielle au Québec en
Figure 9 : Taux ajusté de prévalence du diabète, pour la population âgée de 20 ans et
plus selon le sexe, Québec, 1999-2000 à 2006-2007
comprend les adultes se situant entre 5,2 et 6,1 mmol/L ou qui sont traités avec un hypocholestérolémiant pour atteindre la cible de 5,2 mmol/L. Le niveau optimal de santé cardiovasculaire est obtenu lorsqu’un adulte présente une cholestérolémie inférieure à 5,2 mmol/L [5]. En ce qui concerne les jeunes de 6 à 19 ans, le niveau de santé cardiovasculaire optimal requiert un niveau de cholestérol inférieur à 4,4 mmol/L (172 mg/dl) [5].
Hyperglycémie
La prévalence du diabète chez les québécois de 20 ans et plus était de 8% en 2008-2009. Les hommes sont 1,3 fois plus affectés que les femmes, avec des prévalences de 9 et 7% respectivement [40]. La tendance est à la hausse depuis la fin des années 1990 (Figure 9). L’American Diabetes Association définit le niveau optimal de sucre dans le sang à ˂ 5,6 mmol/L (100 mg/dl) [41]. Ainsi, un adulte ayant ce niveau de glycémie remplit le critère de santé cardiovasculaire optimale selon les objectifs de l’AHA [5]. À l’opposé, une glycémie
équivalente ou supérieure à 7 mmol/L (126 mg/dl) situerait un individu dans le niveau de santé cardiovasculaire le moins favorable. Les valeurs pour les jeunes de 12 à 19 ans sont exactement les mêmes que celles des adultes [5].
Ces sept facteurs de risque forment l’Ideal 7, le regroupement des facteurs de risque mesurables qui permettront d’apprécier l’évolution de la santé cardiovasculaire aux États-Unis dans les prochaines années [5]. D’une façon plus large, cette présentation est utile pour fournir des objectifs de santé clairs ainsi que des recommandations d’habitudes de vie saines pour guider tous les cliniciens dans le traitement de leurs patients [5].
Tel que discuté, le tabagisme est en réduction au Québec. Les messages de santé publique des dernières années ont certainement contribué à cette prise de conscience sociale. La sédentarité et la malnutrition, telles que présentées dans le présent chapitre, sont également en diminution chez les québécois. Ceci est en soit une bonne nouvelle, car le risque de MCV devrait conséquemment diminuer. Effectivement, les gens décèdent actuellement moins de MCV par rapport aux années 1980 [25]. Toutefois, ils ne se perçoivent pas nécessairement en meilleure santé [42]. Il faut se rappeler que l’obésité et le diabète sont malheureusement en constante progression chez les québécois.
Bien qu’ils soient connus et largement étudiés, les facteurs de risque et les facteurs protecteurs des MCV sont encore à l’étude. Une étude a même récemment démontré la corrélation entre la possession d’un animal de compagnie et la réduction du risque de MCV [43]. De toutes évidences, les facteurs protecteurs pour la santé cardiovasculaire sont toujours un sujet chaud dans la littérature.
Chapitre 2.2 : Le syndrome métabolique
Le SMet n’est pas une pathologie proprement dite. En fait, il est plutôt un regroupement de plusieurs anomalies du métabolisme prédisposant au développement de MCV et de diabète de type 2. Bien qu’il n’y ait pas encore de consensus dans la littérature concernant les critères diagnostiques, il importe d’en discuter les principaux points. Quatre sociétés importantes se sont avancées quant à l’identification de critères permettant le diagnostic du SMet en clinique: l’International Diabetes Federation (IDF) [2], le National Cholesterol
Education Program Adult Treatment Panel III (NCEP ATP III) [3], l’American Heart Association/National Heart, Lung and Blood Institute (AHA/NHLBI) [4] et, l’Organisation
mondiale de la santé (OMS) [44]. Essentiellement, le SMet se caractérise par l’hyperglycémie, l’augmentation de la tension artérielle, la dyslipidémie, tout particulièrement une hypertriglycéridémie et un faible taux de lipoprotéines de haute densité (C-HDL), ainsi que l’obésité abdominale (Tableau 1). Ces critères sont des facteurs de risque de MCV [45, 46]. Chacun de ces critères seront définit plus en profondeur ci-dessous.
L’hyperglycémie
Mesurée à jeun à l’aide d’une prise de sang, la glycémie normale devrait être inférieure à 6,1 mmol/L selon l’Association Canadienne du Diabète [47]. Cependant, les critères définissant le SMet proposent une glycémie à jeun égale ou supérieure à 5,6 mmol/L [3, 4, 44]. L’IDF inclut aussi le critère d’un diabète de type 2 déjà diagnostiqué alors que l’AHA considère un traitement hypoglycémiant déjà débuté [4].
Les variations du taux de sucre sanguin sont normalement régulées par la sécrétion d’insuline [48]. Suite à un repas, par exemple, les sucres ingérés sont absorbés par la muqueuse du système digestif puis diffusés dans le sang. L’augmentation de la glycémie qui s’ensuit stimulera le pancréas, plus précisément les cellules pancréatiques bêta (β)
Tableau 1 : Quatre définitions du SMet selon différents organismes
situées au sein des îlots de Langerhans [48]. Ces cellules hormonopoïétiques ainsi stimulées produiront de l’insuline.
En se liant à son récepteur membranaire spécifique, cette hormone favorise, entre autres, le transport du glucose à l’intérieur des cellules cibles de l’organisme. Normalement, les cellules musculaires et adipeuses sont les premières servies, énergétiquement parlant. Lorsque les besoins immédiats de l’organisme sont comblés, le glucose disponible est stocké sous forme de glycogène en vue d’éventuels besoin. Enfin, le glucose n’ayant pas été utilisé ou stocké en glycogène sera emmagasiné sous forme de triglycérides dans les cellules adipeuses ainsi qu’au niveau du foie [48].
Dans l’éventualité où la membrane des cellules musculaires et adipeuses résiste au transport du glucose à l’intérieur de celles-ci, d’avantage d’insuline sera sécrétée par le pancréas comme moyen de compensation. Au bout d’un certain temps, même ce surplus d’insuline ne suffira plus et le glucose ne pourra plus pénétrer les cellules. L’insulinorésistance fera donc son apparition. Généralement lié à un excès de tissu adipeux au niveau musculaire et viscéral, ceci entraînera inévitablement l’hyperglycémie [49].
Les tests utilisés en clinique pour diagnostiquer une hyperglycémie sont généralement réalisés à jeun. La prise de sang mesurant le taux de glucose est le premier indicateur de l’état glycémique et est le test de choix pour l’établissement du critère de SMet. L’étape suivante vise généralement à évaluer la tolérance au glucose ainsi que la résistance à l’insuline par un test oral de tolérance au glucose (Oral Glucose Tolerance Test, OGTT) [41]. Ces tests seront expliqués davantage au chapitre 3, dans la section méthodologie de l’étude.
L’hypertension artérielle
Pour la population en général, une tension artérielle inférieure à 140/90 mmHg est recommandée selon le Programme d’éducation canadien sur l’hypertension, tant pour les individus souffrant de diabète que ceux n’en souffrant pas [50]. Les critères des différentes définitions du SMet proposent une limite inférieure ou égale à 130/85 mmHg [2-4], à l’exception de l’OMS qui s’en tient au 140/90 mmHg [44]. Ces trois premières sociétés y ajoutent aussi l’option d’un traitement antihypertenseur à considérer comme critère du SMet [2-4]. Ces critères diffèrent aussi de la norme de santé cardiovasculaire idéale de l’AHA, qui est de 120/80 [5].
Pression ou tension artérielle sont synonymes et réfèrent aux pressions maximales (systoliques) et minimales (diastoliques) exercées sur les parois des artères pendant le cycle
cardiaque [48]. Mesurée par un tensiomètre, la pression artérielle nous renseigne sur l’état d’élasticité des artères ainsi que sur le volume de sang propulsé à chaque contraction cardiaque. L’un des facteurs modulant à la hausse la pression artérielle est donc l’augmentation du volume sanguin, lui-même résultant de l’augmentation de la demande métabolique reliée à un surplus de poids [45, 51].
Les mesures de tension artérielle doivent être réalisées selon les normes reconnues, tel qu’expliqué par le Programme éducatif canadien sur l’hypertension artérielle [52]. Généralement, le tensiomètre du clinicien sert d’outil préliminaire au diagnostic. Il faut par contre demeurer prudent car les résultats de certains patients peuvent être faussés à la hausse par le stress que représente l’évaluation elle-même (communément appelée hypertension de la blouse blanche, généralement surévaluée) ou encore à la baisse (hypertension masquée). Des mesures alternatives telles que la Mesure Ambulatoire de la Pression Artérielle (MAPA) ou tout simplement des mesures fréquentes à domicile seraient donc favorisées [52].
La dyslipidémie
Les valeurs normales des triglycérides doivent être inférieures ou égales à 1,7 mmol/L. Ce critère diagnostic du SMet est le seul pour lequel les quatre sociétés s’entendent [2-4, 44]. De plus, l’IDF et l’AHA/NHLBI ajoutent à cela, comme dans le cas de la tension artérielle, un traitement contre l’hypertriglycéridémie. Le C-HDL, quant à lui, peut caractériser le SMet lorsque ses valeurs sont inférieures à 1,03 mmol/L pour les hommes [2, 4] et entre 1,29 et 1,30 mmol/L pour les femmes [2-4]. L’OMS et le NCEP suggèrent des valeurs moins élevées pour les hommes (0,90 à 1,00 mmol/L). L’OMS est le seul à avoir la valeur de 1,00 mmol/L pour les femmes, ce qui est la plus basse de tous les critères proposés [44]. Les lipides sont une famille de molécules insolubles dans l’eau. Ces molécules doivent inévitablement se lier à des complexes de protéines dans le but d’acquérir la capacité de traverser les membranes cellulaires [48]. Nous distinguons les lipoprotéines par leur densité, définie en pourcentage de lipides qu’elles contiennent. Ainsi, plus la proportion de
lipides est élevée, plus la densité de la molécule est faible. Les lipoprotéines à plus haute densité sont les plus favorables pour la santé étant donné que leur travail consiste à capter le surplus de cholestérol en périphérie et de le transporter vers le foie où le cholestérol sera dégradé et éliminé. Bien que leur travail ne s’y limite pas, les C-HDL font en quelque sorte « le ménage » [48]. Les lipoprotéines à faible densité (C-LDL), quant à eux, proviennent de la formation des résidus de cholestérol à très faible densité (C-VLDL) qui n’ont pas servi au transport des triglycérides du foie vers les tissus périphériques. Ils sont utiles pour constituer les membranes cellulaires, régler la synthèse du cholestérol et fabriquer des hormones. En cas de surplus, ils sont mis en réserve. Les triglycérides sont une composante de chacune des lipoprotéines, en proportion plus importante dans les chylomicrons en provenance de l’intestin [48]. Ces dernières ont la densité moléculaire la plus faible de toutes les lipoprotéines.
Les lipides se mesurent de la même façon que la glycémie, soit par une prise de sang réalisée chez l’individu à jeun. Les plus récentes lignes directrices pour le diagnostic et le traitement de la dyslipidémie ont établit les valeurs cibles de démarrage d’une thérapie hypolipémiante à des niveaux de C-LDL ≥ 3,5 à 5,0 mmol/L, entre autre, tout dépendant du niveau de risque de l’individu [39]. Lorsqu’un traitement est initié, les C-LDL devraient atteindre ≤ 2 mmol/L ou une diminution de 50% de leur valeur initiale. En résumé, les critères diagnostiques du SMet se basent à partir de valeurs de C-HDL et de TG mais, à ce jour, les options de traitements demeurent ciblées selon les valeurs des C-LDL.
L’obésité abdominale
Une accumulation de tissu adipeux au niveau de la taille devient critique lorsque le tour de taille devient égal ou supérieur à 94 cm pour les hommes et 80 cm pour les femmes, selon l’IDF (IDF 2006). Le NCEP ATP III et l’AHA/NHLBI s’entendent, quant à eux, pour un seuil ≥ 102 cm et ≥88 cm pour les hommes et les femmes, respectivement [3, 4]. Enfin, l’OMS, utilise un indice d’adiposité différent des autres sociétés, soit le ratio taille/hanche, où l’on divise la circonférence de taille par la circonférence au niveau des hanches. Si
celui-ci se situe > 0,90 pour les hommes et > 0,85 pour les femmes, cela devient un critère d’obésité abdominal et de SMet.
L’obésité abdominale est reconnue pour exposer les patients qui en souffrent à un plus haut risque de MCV [7, 53]. En effet, un surplus de tissus adipeux à l’abdomen n’est pas seulement associé à des dépôts graisseux entourant les organes tels le foie, le pancréas, le cœur et les muscles squelettiques, mais aussi à l’intérieur de ceux-ci [54]. L’invasion des tissus fonctionnels par les lipides se nomme lipotoxicité [45]. Cela mène éventuellement au dysfonctionnement des organes atteints. Ce sujet sera abordé plus en détails dans la section suivante.
Pour établir un diagnostic de SMet, un certain nombre de critères doivent être rassemblés chez un même individu. De fait, le NCEP ATP III et l’AHA/NHLBI s’entendent à l’effet que trois critères sont suffisants pour déterminer le SMet [3, 4]. L’OMS, quant à lui, mentionne en priorité un trouble de la régulation du glucose (quel qu’il soit) additionné de deux autres critères. D’ailleurs, cet organisme prend aussi en considération la qualité de la fonction rénale parmi ses caractéristiques du SMet [44]. Enfin, seule l’IDF priorise l’obésité abdominale avec l’ajout de deux critères pour diagnostiquer le SMet [2].
Le SMet se traite tout d’abord par la modification des habitudes de vie. Un rythme de vie sédentaire et une mauvaise alimentation en sont souvent la principale cause, bien que certains facteurs génétiques puissent jouer en défaveur de l’individu qui en est atteint [55]. Le chapitre 2.6 sera consacré aux interventions non-pharmacologiques visant l’amélioration des habitudes de vie pour mener à une perte de poids. L’étape suivante de traitement est bien entendu la médication, qu’elle soit hypotensive, hypolipémiante ou hypoglycémiante, selon la condition de santé de l’individu.
Le SMet peut facilement passer inaperçu. En effet, outre l’obésité abdominale qui peut gêner certains mouvements, les individus qui en souffrent ne se sentiront pas plus malades pour autant. Ils pourraient croire, à tort, qu’ils sont en parfaite santé, malgré leur surplus de poids. Le dépistage précoce du SMet par les professionnels de la santé peut être un outil important pour détecter les anomalies qui pourraient nuire à la qualité de vie à moyen ou long terme.
Chapitre 2.3 : Obésité viscérale et syndrome métabolique en cardiologie
Tel que vu précédemment, l’obésité est en constante augmentation au Québec. En effet, en 1987, 8% des québécois souffraient d’obésité alors que cette proportion est grimpée à 17% en 2009 [28]. Dans les prochaines pages, l’obésité viscérale, ses effets métaboliques ainsi que son impact en cardiologie seront discutés.
L’obésité viscérale
Plusieurs mesures d’adiposité sont utilisées en clinique et dans la littérature. L’une des plus reconnues est le calcul de l’IMC [7, 46, 56]. Cette mesure représente la masse en kilogramme divisé par la taille au carré. Bien que cette mesure ne permette pas de faire la distinction entre la masse grasse et la masse maigre ou la distribution du tissu adipeux, elle est certainement la plus utilisée [46]. Selon la classification de l’IMC, un surplus de poids se définit par une valeur entre 25 et 29,9 kg/m2, alors que l’obésité débute lorsque cet indice surpasse les 30 kg/m2. Cette dernière catégorie se divise ensuite en quatre classes, soit l’obésité de grade 1, 2, 3 et l’obésité extrême (IMC ≥ 50 kg/m2) [7, 57]. L’obésité est généralement associée au SMet. Tel que vu dans la section précédente, les critères du SMet considèrent la mesure du tour de taille plutôt que l’IMC pour mieux caractériser la localisation du tissu adipeux [7, 56]. Mesuré au niveau de la crête iliaque, cet indicateur permet une détection des individus dont l’IMC est adéquat mais qui présentent une obésité dite viscérale, ou androïde (Figure 10) [46].
Figure 10 : Forme androïde (obésité viscérale) vs. gynoïde (obésité sous-cutané)
Les études ont montré que l’obésité viscérale était un meilleur déterminant du risque cardiovasculaire que la mesure de l’IMC [7]. Il n’y a toujours pas de consensus quant aux limites supérieures « à risque » du tour de taille, du point de vue de la cardiologie. Elles varient de 80 à 88 cm pour les caucasiennes et de 94 à 102 cm pour les caucasiens [2, 58]. En recherche, l’examen à l’aide de la tomodensitométrie peut être utilisé pour quantifier le tissu adipeux viscéral (Figure 11). Le ratio taille-hanche, soit la mesure du tour de taille divisé par la mesure du tour de hanches [46], est aussi une méthode reconnue afin d’estimer la proportion de graisse abdominale [56]. Une relation linéaire a été démontrée entre l’augmentation des indices d’adiposité et la morbidité cardiovasculaire [59]. Plus précisément, des études ont rapportés qu’un ratio taille-hanche élevé ainsi qu’une circonférence de taille élevée étaient de meilleurs prédicteurs de MCV éventuelles, pour un IMC donné [59]. Pour les caucasiens, le ratio taille-hanche ne devrait pas excéder 0,85 chez les femmes et 0,9 chez les hommes [58].
Figure 11 : Image issue de la tomodensitométrie pour la quantification du tissu adipeux
viscéral
Les effets métaboliques de l’obésité
Le surplus de tissu adipeux dans l’organisme agit littéralement sur tout le métabolisme. Voici un résumé de ses effets [45, 51, 53]:
1. Agit comme une glande endocrine;
2. Favorise le développement de certains cancers;
3. Cause une obstruction mécanique pour le fonctionnement de certains organes; 4. Augmente le taux d’acides gras libres dans le sang;
5. Augmente la demande métabolique; 6. Cause une lipotoxicité;
7. Comble les espaces de réserve sous-cutanés;
8. Provoque une réponse immunitaire inadéquate / est infiltré de macrophages. Les effets endocriniens et métaboliques sont approfondis ci-dessous.
Glande endocrine
Le surplus de tissus adipeux entraîne la sécrétion de plusieurs adipokines. Parmi celles-ci se trouvent l’interleukine-6, le facteur nécrosant tumoral alpha et la protéine C-Réactive, tous responsables de l’état d’inflammation chronique présent en situation d’obésité [45, 53]. Des molécules similaires à l’insuline sont également sécrétées, l’insulin-like growth factor-1 et l’insulin-binding protein 3. Ceci contribue à la résistance à l’insuline si communément observée dans le SMet [45, 53]. D’autres adipokines sont aussi libérées et causent des modifications métaboliques telles qu’un état prothrombotique et une vasoconstriction périphérique [45, 53].
Augmentation de la demande métabolique
Tel qu’il sera vu en détail dans la prochaine section (chapitre 2.3), l’augmentation de la demande métabolique causée par le surplus de tissu adipeux entraîne l’augmentation du volume sanguin [51], une précharge augmentée, un surcroît de travail ventriculaire gauche, et éventuellement, une dysfonction diastolique [45, 51]. Si elle n’est pas traitée ou prise en charge à temps, cette dysfonction diastolique risque d’évoluer jusqu’à l’insuffisance cardiaque [51]. Les conséquences de l’obésité sur le coeur sont détaillées ci-dessous.
Impact de l’obésité en cardiologie
La présence du SMet (obésité viscérale et autres critères métaboliques) double le risque relatif de MCV [59, 60]. Les conséquences d’un surplus de tissu adipeux sur le cœur sont de nature fonctionnelle, électrophysiologique et circulatoire.
Impact fonctionnel
Tel que mentionné ci-dessus, la demande énergétique augmente pour subvenir aux besoins métaboliques du surplus de tissu adipeux. Ceci implique une augmentation du volume sanguin. Le surcroît de travail ainsi engendré entraîne, à moyen terme, une altération de la fonction et de la structure du muscle cardiaque [7, 51]. Éventuellement, ces altérations peuvent se détériorer jusqu’à l’insuffisance cardiaque et une piètre qualité de vie [7].
Impact électrophysiologique
Plusieurs facteurs reliés à la présence d’obésité abdominale peuvent influencer la lecture d’un électrocardiogramme [7]:
Le déplacement du cœur à cause de l’élévation du diaphragme en position couchée; L’hypertrophie du ventricule gauche causée par son surcroît de travail au niveau du
muscle cardiaque;
La distance séparant le cœur des électrodes qui est augmentée à cause de l’accumulation de tissus adipeux sous-cutané;
Les problèmes pulmonaires causés par l’apnée du sommeil.
Les variables habituellement analysées à l’électrocardiogramme s’en trouveront majoritairement augmentées : le rythme cardiaque, l’intervalle PR et QRS, le voltage du segment QRS ainsi que l’intervalle QT [7]. Enfin, l’obésité augmente de 50% le risque de souffrir de fibrillation auriculaire [7].
Impact circulatoire
L’obésité viscérale est associée à la présence de plaques athérosclérotiques dans les artères coronaires [7]. Non seulement l’athérosclérose nuit-elle à l’approvisionnement sanguin du muscle cardiaque par l’obstruction partielle à complète des vaisseaux, mais elle augmente aussi le risque d’accidents vasculaires cérébraux [22]. Les individus souffrant du SMet ont d’ailleurs plus de risque de souffrir d’évènements cardiovasculaires et d’en mourir, le
risque relatif étant de 1,78 à 2,40 [7, 60]. Une fois de plus, les indices d’adiposité viscérale tels que le tour de taille ou le ratio taille-hanche seraient de meilleurs prédicteurs de MCV éventuelles comparativement à l’IMC seul [7]. Dans les cas de pontage aorto-coronariens, il a été rapporté que les patients avec SMet risquaient d’avantage de complications post-opératoires telles que la fibrillation auriculaire. Le SMet est aussi un facteur de risque accru de mortalité suite à l’intervention [7]. Le SMet a finalement été associé au développement de la sténose aortique et à une progression plus rapide de la dégénérescence d’une valve qui a été remplacée [7].
Impact d’une perte de poids
Plusieurs effets positifs sont reliés à la perte de poids intentionnelle chez les individus initialement obèses [39]. Comme les impacts de l’obésité et du SMet en cardiologie, les bénéfices d’une perte de poids sur le système cardiovasculaire sont de nature fonctionnelle, électrophysiologique et circulatoire [7].
1. Impact fonctionnel :
a. Amélioration de la fonction diastolique et systolique ventriculaire gauche;
b. Diminution de la masse du ventricule gauche; 2. Impact électrophysiologique:
a. Ralentissement du rythme cardiaque au repos; b. Normalisation de la variabilité cardiaque; 3. Impact circulatoire :
a. Diminution du volume sanguin circulant;
b. Diminution du volume d’éjection systolique et du débit cardiaque; c. Diminution des pressions veineuses au niveau pulmonaire;
d. Diminution de l’œdème périphérique; e. Diminution de la tension artérielle.
Somme toute, le poids n’est certainement pas le seul le critère pour mesurer le risque cardiovasculaire d’un patient donné. Les mesures d’adiposité centrale, ou viscérale, sont
des indicateurs plus fiables des impacts délétères de l’obésité et du SMet sur le système cardiovasculaire.
Figure 12 : Cavités et parois du coeur
Tiré de Marieb et al, 2010
Chapitre 2.4 : Dysfonction diastolique ventriculaire gauche
L’anomalie cardiaque la plus fréquemment rencontrée est la dysfonction diastolique ventriculaire gauche (DDVG). En effet, elle est présente chez au moins 25% des adultes âgés de plus de 40 ans [6]. Reliée à l’obésité, elle est de mieux en mieux définie dans la littérature. Il est connu que cette anomalie est associée à différents troubles métaboliques et à l’obésité [45, 61] tout en étant un fort prédicteur d’évènements cardiovasculaires [6]. D’ailleurs, la présence de DDVG est la cause d’approximativement la moitié des cas d’insuffisance cardiaque [6]. Les prochaines sections discuteront l’anatomie et la physiologie cardiaque normales, les principes de base de la diastologie, ses déterminants, la DDVG ainsi que les moyens diagnostiques et les traitements possibles.
Anatomie et physiologie du cœur
La cavité centrale du thorax, le médiastin, héberge le cœur. Enveloppé dans le péricarde, il repose obliquement sur la face supérieure du diaphragme. Le muscle cardiaque, aussi nommé myocarde, est entouré d’une couche extérieure et intérieure, l’épicarde et l’endocarde respectivement (Figure 12). C’est le myocarde qui effectue la contraction et la relaxation cardiaque [48].
Figure 13 : Anatomie du coeur
Tiré de Marieb et al, 2010
Le cœur contient quatre cavités (Figure 13). Dans la partie supérieure du cœur se trouvent deux oreillettes, séparées par le septum interauriculaire. Dans la partie inférieure du cœur se trouvent deux ventricules, séparés par le septum interventriculaire. Des valves sont situées entre chacune des chambres supérieures et inférieures. Le ventricule gauche a une paroi plus épaisse que le ventricule droit et il forme l’apex du cœur. Les oreillettes sont toutefois de la même taille [48].
Figure 14 : Circulation cardiovasculaire
Les chambres supérieures du cœur reçoivent le sang en provenance de la périphérie, par des veines, alors que les chambres inférieures l’expulsent vers les organes, par des artères (Figure 14). Plus précisément, les veines caves supérieures et inférieures arrivent à l’oreillette droite avec du sang chargé en dioxyde de carbone (CO2) en provenance des organes du corps. Le sang passera à travers la valve tricuspide pour s’accumuler dans le ventricule droit jusqu’à la prochaine contraction, la systole. Le ventricule droit, qui se contractera, propulsera le sang aux poumons via les artères pulmonaires. Le sang sera alors oxygéné pour ensuite revenir au cœur par les quatre veines pulmonaires qui déverseront leur contenu dans l’oreillette gauche. Le sang passera par une autre valve, la valve mitrale, pour s’accumuler dans le ventricule gauche en attendant la prochaine systole ventriculaire. Le sang sera conséquemment propulsé dans l’aorte puis ira oxygéner les organes du corps [48].
Au niveau microscopique, les fibres d’actine et de myosine se contractent et se détendent de façon cyclique et synergique dans le but de produire des contractions efficaces [48]. Bien que les cellules cardiaques soient autoexcitables, le muscle qu’elles constituent est relié au système nerveux autonome et c’est ce dernier qui gère le rythme des contractions. Le cœur contient aussi des cellules non contractiles servant à produire et propager l’influx électrique en vue de provoquer une contraction bien organisée [48]. Le facteur déterminant la quantité de sang qui remplira le ventricule avant chaque contraction est la précharge. Par exemple, un volume sanguin plus important augmentera la précharge. La postcharge, quant à elle, est définie comme la pression s’opposant à la force ventriculaire lors de la contraction. Cette pression est exercée par les valves de l’aorte et le tronc pulmonaire, pour les ventricules gauche et droit respectivement [48].
La diastole et ses déterminants
Le cycle cardiaque est divisé en deux phases, soit la systole et la diastole (Figure 15). Cette première est caractérisée par la contraction du muscle ventriculaire suite à la fermeture des
Figure 15 : Phases du cycle cardiaque
Tiré de Marieb et al, 2010
valves auriculo-ventriculaires. Son but premier est de propulser le sang du cœur gauche aux organes du corps et celui du cœur droit, aux poumons [8, 48]. Cette phase se nomme aussi « éjection systolique ». La diastole, quant à elle, est la phase de relaxation. Elle débute au moment où la valve aortique et pulmonaire se ferment jusqu’à la fin du remplissage en provenance de l’oreillette (et fermeture de la valve auriculo-ventriculaire). Quatre stades caractérisent la diastole, soit :
1. La relaxation isovolumétrique; 2. Le remplissage rapide du ventricule; 3. La diastase;
4. La systole auriculaire.
Ces stades seront décrits brièvement ci-dessous. Pour les biens du présent texte, nous nous concentrerons sur la diastole ventriculaire gauche.
La relaxation isovolumétrique
La relaxation isovolumétrique est la première phase de la diastole. Elle débute lorsque la valve aortique se ferme et se poursuit jusqu’à l’ouverture de la valve mitrale [8]. Tel que son nom l’indique, il n’y a pas de changement de volume pendant cette phase. Cependant, la pression ventriculaire chute drastiquement pendant la relaxation isovolumétrique. La vitesse du déclin de la pression dans la cavité est mesurée par une formule mathématique tenant compte de quatre variables : (1) la pression dans le ventricule au moment où la valve aortique se ferme, (2) la pression à la fin de la relaxation isovolumétrique, soit lorsque la valve mitrale s’ouvre, (3) le temps entre ces deux étapes, ainsi (4) qu’une constante nommée valeur de T (T value) [8]. Une valeur de T élevée signifie une relaxation lente
alors qu’une valeur T basse signifie une relaxation rapide. Cette dernière est souhaitable pour une meilleure santé cardiaque. Avant que la valve mitrale ne s’ouvre, la pression à l’intérieur du ventricule gauche diminue jusqu’à être inférieure à la pression de l’oreillette gauche. Cette différence de pression entraîne inévitablement l’ouverture de la valve mitrale et le début de la phase 2 de la diastole [8], le remplissage rapide.
Le remplissage rapide du ventricule
La deuxième phase de la diastole est le remplissage rapide du ventricule gauche. Logiquement, comme la première phase se termine avec l’ouverture de la valve mitrale, cette phase caractérise le début du remplissage [8]. L’abaissement progressive de la pression qui s’observe dans le ventricule, potentialisé par le recul élastique du muscle ventriculaire, produit un effet de succion qui attire rapidement le volume sanguin se situant dans l’oreillette gauche. Plus le ventricule gauche relaxera rapidement, plus grand sera le gradient de pression entre les deux chambres et plus vite entrera le sang en provenance de l’oreillette [8]. Les deux tiers du volume sanguin entrent dans le ventricule pendant cette phase de remplissage rapide. Lorsque les pressions s’équilibrent entre la chambre supérieure et la chambre inférieure, le remplissage rapide est terminé [8]. L’étape suivante est la diastase.
Diastase
La diastase survient immédiatement avant la contraction auriculaire; c’est le moment pendant lequel les pressions entre l’oreillette gauche et le ventricule gauche sont égales. Bien qu’il reste du sang dans l’oreillette, ce dernier ne s’écoule pas, ou peu, comme le gradient de pression est nul [8]. Il faudra une contraction auriculaire pour terminer le remplissage ventriculaire.
La systole auriculaire
La dernière phase de la diastole est caractérisée par la contraction auriculaire, qui augmente la pression dans l’oreillette et permet l’écoulement du sang restant vers le ventricule déjà rempli aux deux tiers. Ainsi, le ventricule se remplira à pleine capacité et sera prêt pour l’éjection systolique [8].
Les déterminants de la fonction diastolique
Respectant les phases de la diastole, les déterminants de cette dernière sont :
1. La relaxation active du myocarde : s’étendant de la première à la deuxième phase de la diastole, la relaxation du myocarde implique l’utilisation d’énergie, l’adénosine triphosphate (ATP), ainsi que le transfert de calcium hors des myocytes [8, 48]. Une altération au niveau de l’un ou l’autre de ces mécanismes, comme en cas d’hypercalcémie pourrait ralentir la vitesse de relaxation du myocarde et ainsi retarder le remplissage [8].
2. La compliance ventriculaire gauche : le ratio de différence de volume sur la différence de pression du ventricule (dV/dP) caractérise la compliance du ventricule gauche. L’inverse de la compliance se nomme « rigidité » ventriculaire et est représentée par la formule inverse, soit dP/dV. La compliance ventriculaire gauche est dépendante de plusieurs facteurs : l’élasticité du myocarde, la taille et la forme de la chambre ventriculaire ainsi que l’épaisseur de ses parois, les gradients de pressions auriculo-ventriculaires, la pression pleurale, pour n’en nommer que quelques-uns [8]. La compliance ventriculaire est entre autres définie par la compliance intrinsèque du myocarde. La rigidité intrinsèque du myocarde survient secondairement à une suraccumulation de collagène dans le myocarde, suite à une hypertrophie résultant d’un surcroît de pression à long terme, par exemple. Normalement, le collagène présent dans le muscle cardiaque joue un rôle de conversion des forces contractiles des myocytes en pression intraventriculaire. La
quantité de collagène est aussi déterminante de la forme et de la taille du ventricule [8].
3. La fonction auriculaire : l’oreillette gauche joue principalement deux rôles dans la diastole. Tout d’abord, le remplissage rapide du ventricule gauche fait d’elle un réservoir, le sang passant passivement de la chambre auriculaire à la chambre ventriculaire. Deuxièmement, son rôle devient actif lors de la contraction auriculaire et permet ainsi le remplissage des derniers 20 à 30% de volume ventriculaire manquant pour une diastole complète. Avec la vieillesse ou en cas de troubles cardiaques, la proportion de sang éjecté de l’oreillette tendera à augmenter pour compenser une diastole « passive » déficiente et maintenir un débit cardiaque adéquat [8].
S’additionnent à ces trois déterminants la fréquence cardiaque, ayant un impact sur le débit cardiaque, ainsi que le péricarde, qui peut faire un effet d’étau empêchant une dilatation optimale du ventricule lors du remplissage, comme en cas de péricardite constrictive [8].
Dysfonction diastolique et insuffisance cardiaque
L’insuffisance cardiaque est divisée en deux grands groupes, soit l’insuffisance cardiaque avec fraction d’éjection réduite (HFrEF) et l’insuffisance cardiaque avec fraction d’éjection préservée (HFpEF). Cette dernière est aussi nommée « insuffisance cardiaque diastolique ». Les études démontrent que la forme d’insuffisance cardiaque avec fonction d’éjection maintenue aurait une prévalence de près de 50% [8]. Les critères diagnostiques d’une dysfonction cardiaque sont nombreux et controversés. Si les critères cités dans les lignes directrices sont rencontrés et qu’en plus, un patient présente des signes et symptômes d’insuffisance cardiaque accompagnés d’une fraction d’éjection supérieure à 50% (préservée), un diagnostic de HFpEF pourrait alors être posé selon le Working group for the
European Society of Cardiology [8]. Cependant, il est possible qu’un individu souffre de
DDVG sans se rendre compte que son problème de santé soit de nature cardiaque. En effet, les symptômes reliés à la DDVG sont non-spécifiques : par exemple, la fatigue et l’essoufflement pourraient être attribuables à une foule d’autres conditions. Les critères de