THÈSE
Pour l'obtention du grade de
DOCTEUR DE L'UNIVERSITÉ DE POITIERS UFR des sciences fondamentales et appliquées
Institut de chimie des milieux et matériaux de Poitiers - IC2MP (Diplôme National - Arrêté du 7 août 2006)
École doctorale : Sciences pour l'environnement - Gay Lussac (La Rochelle) Secteur de recherche : Chimie organique, minérale, industrielle
Cotutelle : Université Technique Gh Asachi IASI
Présentée par : Carmen Ciotonea
Synthèse et caractérisation de catalyseurs monométalliques et bimétalliques à base de métaux de transition pour les
réactions d'hydrogénation chimiosélective Directeur(s) de Thèse :
Sébastien Royer, Emil Dumitriu
Soutenue le 01 juillet 2015 devant le jury
Jury :
Président Dan Cascaval Profesor, Universitatea tehnică Gheorghe Asachi, Iaşi, România Rapporteur Alexandra Raluca Iordan Profesor, Universitatea Alexandru Ioan Cuza, Iaşi, România Rapporteur Vasile Hulea Professeur, École nationale supérieure de Chimie, Montpellier Membre Sébastien Royer Maître de conférences, Université de Poitiers
Membre Emil Dumitriu Profesor, Universitatea tehnică Gheorghe Asachi, Iaşi, România
Membre Sabine Petit Directeur de recherche, IC2MP, CNRS, Poitiers
Membre Frédéric Richard Maître de conférences, Université de Poitiers
Membre Marcel Ionel Popa Profesor, Universitatea tehnică Gheorghe Asachi, Iaşi, România
Pour citer cette thèse :
Carmen Ciotonea. Synthèse et caractérisation de catalyseurs monométalliques et bimétalliques à base de métaux
THÈSE
Pour l'obtention du grade de
DOCTEUR DE L'UNIVERSITÉ DE POITIERS UFR des Sciences Fondamentales et Appliquées
Institut de Chimie des Milieux et Matériaux de Poitiers - IC2MP (Diplôme National - Arrêté du 7 août 2006)
École doctorale : Sciences pour l'environnement - Gay Lussac Secteur de recherche : Chimie organique, minérale et industrielle Cotutelle : Université Technique « Gheorghe Asachi » de Iasi (Roumanie)
Présentée par : Carmen CIOTONEA
SYNTHESE ET CARACTERISATION DE CATALYSEURS
MONOMETALLIQUES ET BIMETALLIQUES A BASE DE METAUX
DE TRANSITION POUR LES REACTIONS D’HYDROGENATIONS
CHIMIOSELECTIVES
Directeur(s) de Thèse : Sébastien Royer, Sabine Petit et Emil Dumitriu
JURY
Rapporteurs: Hulea Vasile, Professeur – Institut Charles Gerhardt de Montpellier
Iordan Alexandra Raluca, Professeur – Université Alexandru Ioan Cuza de Iasi Membres: Sébastien Royer, Maître de Conférences – HDR, Université de Poitiers
Sabine Petit, Directrice de Recherche, Université de Poitiers
Emil Dumitriu, Professeur émérite, Université Technique "Gheorghe Asachi" de Iasi Frédéric Richard, Maître de Conférences – HDR, Université de Poitiers
Dan Cascaval, Professeur, Université Technique "Gheorghe Asachi" de Iasi Marcel Ionel Popa, Professeur, Université "Technique Gheorghe" Asachi de Iasi
THÈSE
Pour l'obtention du grade de
DOCTEUR DE L'UNIVERSITÉ DE POITIERS UFR des Sciences Fondamentales et Appliquées
Institut de Chimie des Milieux et Matériaux de Poitiers - IC2MP (Diplôme National - Arrêté du 7 août 2006)
École doctorale : Sciences pour l'environnement - Gay Lussac Secteur de recherche : Chimie organique, minérale et industrielle Cotutelle : Université Technique « Gheorghe Asachi » de Iasi (Roumanie)
Présentée par : Carmen CIOTONEA
SYNTHESE ET CARACTERISATION DE CATALYSEURS
MONOMETALLIQUES ET BIMETALLIQUES A BASE DE METAUX
DE TRANSITION POUR LES REACTIONS D’HYDROGENATIONS
CHIMIOSELECTIVES
Directeur(s) de Thèse : Sébastien Royer, Sabine Petit et Emil Dumitriu
JURY
Rapporteurs: Hulea Vasile, Professeur – Institut Charles Gerhardt de Montpellier
Iordan Alexandra Raluca, Professeur – Université Alexandru Ioan Cuza de Iasi Membres: Sébastien Royer, Maître de Conférences – HDR, Université de Poitiers
Sabine Petit, Directrice de Recherche, Université de Poitiers
Emil Dumitriu, Professeur émérite, Université Technique "Gheorghe Asachi" de Iasi Frédéric Richard, Maître de Conférences – HDR, Université de Poitiers
Dan Cascaval, Professeur, Université Technique "Gheorghe Asachi" de Iasi Marcel Ionel Popa, Professeur, Université "Technique Gheorghe" Asachi de Iasi
5 Mulțumiri
Țin să mulțumesc conducătorilor mei de doctorat, Dl. Prof. emerit Dr. Ing. Emil DUMITRIU (Universitatea Technică „Gheorghe Asachi” din Iaşi), Dl MCF-HDR Dr. Sebastien ROYER și Dnei DR-HDR Dr. Sabine PETIT (Universtitatea din Poitiers, Franţa) care au acceptat sa fie coordonatorii mei de doctorat și să îndrume activitatea mea știintifică. Le mulțumesc pentru sprijinul acordat pe perioada acestor patru ani de doctorat.
Mulţumesc în special domnișoarei Dr. Biochim. Brînduşa DRĂGOI şi domnului S.l. Dr. Ing. Adrian UNGUREANU care cu multă răbdare și profesionalism m-au încurajat permanent pe toată durata doctoratului, iar prin sprijinul oferit mi-au permis să duc la bun sfârșit această lucrare.
Mulțumesc membrilor comisiei care au acceptat să analizeze teza mea de doctorat : Dl Prof. Dr. Ing. Hulea Vasile (Ecole Nationale Supérieure de Chimie, Montpellier, Franța), Dra Prof. Dr. Chim. Alexandra Iordan (Universitatea Al. I. Cuza, Iași), Dl Prof. Dr. Ing. Popa Ionel Marcel (Universitatea Technică „Gheorghe Asachi”), Dl MCF-HDR Dr. Frederic Richard (Universtitatea din Poitiers).
Le mulţumesc colegilor din Laboratorul de Cataliza, Universitatea Technică „Gheorghe Asachi” din Iaşi în special lui Dr. Ing. Alexandru Chirieac pentru inițierea mea practică în metodele de sinteză și caracterizare a catalizatorilor.
Doresc să mulțumesc personalului de la Pole Mesure Physique din cadrul IC2MP, Universtitatea din Poitiers, Franţa, în special Dnei Sandrine Arrii-Clacens și Dlui Stephane Pronier. De asemenea, le mulţumesc colegilor de la Universitatea din Poitiers, din cele două echipe SamCat și HydrASA, personal didactic și de cercetare, precum și foştilor și actualilor doctoranzi, care prin sfaturile și ajutorul oferit au fost alături de mine în cei trei ani de teză.
6 CUPRINS
Mulțumiri 8
Introducere 9
CAPITOLUL I. STUDIU DE LITERATURA 69 I.1. PREPARAREA CATALIZATORILOR ÎNALT DISPERSAŢI PE SUPORTURI MEZOPOROASE 70
I.1.1. Aspecte generale 70
I.1.2. Prepararea catalizatorilor prin impregnare 73
I.1.2.1. Apecte generale privind metodele de preparare ale catalizatorilor depuşi pe suport 73
I.1.2.2. Apecte generale privind impregnarea 74
I.1.2.3. Impregnarea umedă incipientă urmată de uscare blândă 81
I.1.2.4. Prepararea catalizatorilor prin metoda impregnării cu doi solvenți 82
I.1.3. Prepararea catalizatorilor prin metoda infiltrării topiturii 84
I.1.4. Prepararea catalizatorilor prin metoda depunerii prin precipitare 86
I.2.SUPORTURI POROASE FOLOSITE ÎN PREPARAREA CATALIZATORILOR METALICI ÎNALT
DISPERSAŢI 89
I.2.1. Clasificarea materialelor poroase 89
I.2.2. Sinteza materialelor mezoporoase ordonate 90
I.2.2.1. Apecte generale 90
I.2.2.2. Materiale mezoporoase de tip SBA-15 93
I.2.2.2.1. Mecanismul de formare al SBA-15 94
I.2.2.2.2. Modificarea diametrului porilor 96
I.2.2.2.3. Eliminarea agentului de structurare 101
I.2.2.3. Alumina mezoporoasă ordonată (AMO) 103
I.2.2.3.1. Sinteza aluminei mezoporoase ordonată 104
I.2.2.3.2. Factori care infuențează proprietățile texturale ale AMO 105
I.2.2.3.3. Prepararea aluminei mezoporoase ordonate prin metoda AAIE 108
I.3. REACŢIIDEHIDROGENARECHEMOSELECTIVĂ 110
I.3.1. Aspecte generale 110
I.3.2. Mecanismul reacției de hidrogenare a aldehidelor α,β- nesaturate 115
I.3.3. Factorii care influențează selectivitatea catalizatorilor 118
I.3.4. Catalizatori pentru reacția de hidrogenare a cinamaldehidei 121
I.3.4.1. Catalizatori monometalici 121
I.3.4.2. Catalizatori bimetalici 125
CAPITOLUL II. PARTEA EXPERIMENTALA 127
II.1. PREPARARE A SUPORTURILOR ŞI CATALIZATORILOR 128
II.1.1. Prepararea suporturilor mezoporoase 128
II.1.1.1. Prepararea silicei mezoporoase de tip SBA-15 128
II.1.1.2. Prepararea silicei mezoporoase de tip SBA-15 cu texturi diferite 128
II.1.1.3. Prepararea suporturilor de tip AMO 129
II.1.1.4. Prepararea suporturilor AMO cu mărimi diferite ale porilor 129
II.1.2. Prepararea catalizatorilor metalici prin metoda IWI-MD 129
II.1.3. Prepararea catalizatorilor metalici prin metodele WI şi IWI 130
7
II.1.5. Prepararea catalizatorilor metalici metoda MI 131
II.1.6. Prepararea catalizatorilor metalici prin metoda DP 133
II.2. CARACTERIZAREA SUPORTURILOR ŞI CATALIZATORILOR 134
II.2.1. Analiza elementală 134
II.2.2. Difracţia de raze X 135
II.2.3. Fizisorbţia azotului 137
II.2.4. Reducerea termoprogramată 139
II.2.5. Chemosorbţia disociativă a N2O 140
II.2.6. Microscopia electronică de transmisie 141
II.3. EXPERIMENTE CATALITICE: reacţia de hidrogenare a trans-cinamaldehidei 142
II.3.1. Experimente catalitice realizate la presiune atmosferică 142
II.3.2. Experimente catalitice realizate la presiune de 10 bari 143
II.3.3. Analiza calitativă şi cantitativă a amestecului de reacţie 143
CAPITOLUL III. REZULTATE ORIGINALE 147 III.1.PREPARAREAŞICARACTERIZAREACATALIZATORILORMONOMETALICIDEPUŞIPE
SILICEMEZOPOROASĂSBA-15 148
III.1.1. Catalizatori preparaţi prin metoda IWI-MD 148
III.1.1.1.Influența texturii suportului 148
III.1.1.1.1. Prepararea suportului de SBA-15 cu texturi diferite. 148
A. Difracția de raze X la unghiuri mici 149
B. Fizisorbția azotului 150
III.1.1.1.2Prepararea catalizatorilor pe suporturi de SBA-15 cu texturi diferite 151
A. Difracția de raze X 152
B. Fizisorbția azotului 154
C. Hidrogenarea cinamaldehidei 158
Concluzii 160
III.1.1.2.Influența timpului de uscare 161
A. Difracția de raze X 161
B. Reducerea termoprogramată 164
C. Difracția de raze X in-situ în atmosferă de aer și în atmosferă de hidrogen 165
D. Microscopia electronică de transmisie 168
E. Hidrogenarea cinamaldehidei 169
Concluzii 171
III.1.1.3. Influența temperaturii de uscare 172
A. Difracția de raze X 172
B. Fizisorbția azotului 174
C. Hidrogenarea cinamaldehidei 178
Concluzii 181
III.1.1.4. Influența încărcării cu metal 181
A. Caracterizarea fizico-chimică a materialelor 181
A. Hidrogenarea cinamaldehidei 184
Concluzii 185
III.1.2. Catalizatori preparaţi prin metodele DP, IWI şi WI 186
III.1.2.1. Prepararea catalizatorilor prin metoda DP 186
8
B. Fizisorbția azotului 189
C. Microscopia electronică de transmisie 191
D. Difracția de raze X in-situ în atmosferă de hidrogen 191
E. Reducerea termoprogramată 193
III.1.2.2. Comparație între catalizatorii preparaţi prin metodele DP, IWI și WI 195
A. Difracția de raze X 195
B. Fizisorbția azotului 196
C. Microscopia electronică de transmisie 197
D. Difracția de raze X in situ în atmosferă de hidrogen 199
E. Reducerea termoprogramată 200
F. Hidrogenarea cinamaldehidei 203
Concluzii 206
III.1.3. Catalizatori preparaţi prin metoda MI 206
A. Difracția de raze X 207
B. Fizisorbția azotului 211
C. Microscopia electronică de transmisie 217
D. Reducerea termoprogramată 221
E. Hidrogenarea cinamaldehidei 224
Concluzii 227
III.2.PREPARAREAŞICARACTERIZAREACATALIZATORILORMONOMETALICIDEPUŞIPE
ALUMINĂMEZOPOROASĂ 229
III.2.1. Prepararea aluminei mezoporoase ordonate cu diferite texturi 229
A. Microscopia electronică de transmisie 230
B. Fizisorbția azotului 231
III.2.2. Prepararea catalizatorilor prin metodele TS și MI 233
A. Caracterizarea fizico-chimică a materialelor 234
B. Hidrogenarea cinamaldehidei 237
III.2.3. Prepararea catalizatorilor cu diferite grade de încărcare în metal prin metoda MI 239
A. Caracterizarea fizico-chimică a materialelor 239
B. Hidrogenarea cinamaldehidei 245
Concluzii 246
III.3.PREPARAREAŞICARACTERIZAREACATALIZATORILORBIMETALICIDEPUŞIPESILICE
MEZOPOROASĂSBA-15 247
A. Caracterizarea fizico-chimică a materialelor 247
B. Hidrogenarea cinamaldehidei 253
Concluzii 256
Concluzii generale 257
9 Lista cu figuri
Figura I.1. Parametrii care pot influența dimensiunea nanoparticulelor și încărcarea cu metal în timpul
preparării unui material catalitic [Maki arvela si al.201] 11
Figura I.2. Caracteristici ale metodelor de preparare a materialelor catalitice prin impregnare [Zhong et
al.,2013] 14
Figura I.3. Deplasarea soluției de precursor metalic spre suprafața externă în timpul etapei de uscare. Reprezentare schematică a aranjării/deplasării lichidului în timpul uscării în corpul suportului umplut cu apă. Se observă formarea bulelor de gaz datorată sucției porilor [Zhong et al.,2013] 14 Figura I.4 Fenomene de transport pentru: 1) Wet Impregnation-WI și 2) Incipient Wetness
Impregnation-IWI. Imagini reproduse după [de Jong et al., 2009] 15
Figura I.5. Reprezentare schematică a distribuției precursorilor în porii suportului anorganic 16 Figura. I.6. Fenoemene de transfer implicate în etapa de platou la temperatura de uscare (A) şi în perioada
de răcire (B) 18
Figura I.7. exemple de efecte ale condiţiilor de uscare asupra distribuţiei fazei active a unui catalizator de Pt/alumina: (a) după impregnare, (b) după uscare la 20 °şi (c) duă uscare la 100 °C [Azzeddine et al. 2007] 18 Figura I.8. Mecanismul de formare al filosilicaților de nichel prin metoda DP. Imagine MET a suportului de SBA-15(stânga), Imagine MET al materialului Ni/SBA-15 după preparare prin metoda DP 26 Figura. I.9. Structura unui filosilicat de tip 1:1 (straturi TO), și filosilicat de tip 2:1 (straturi TOT) 26
Figura I.10. Clasificarea materialelor poroase conform IUPAC 27
Figura I.11. Materiale mezoporoase din clasa M41S: (MCM-41, MCM-48 și MCM-5) 27 Figura. I.12. Mecanism propus pentru formarea materialelor MCM-41 [Kresge, et al., 1992] 28 Figura I.13. Principalele strategii de sinteză a materiale mezoporoase [Galo et al., 2002] 29 Figura I.14. Interacții între specii anorganice și capul hidrofil al agentului de structurare [Huo et al., 1994] 30 Figura.I.15. Formula chimică generală a unui copolimer tribloc. 31 Figura I.16. Schema ce ilustrează modelul propus de Rushtein și colab. pentru primele stadii de sinteză al
materialelor de tip SBA-15 [Ruthstein et al., 2004] 33
Figura I.17. Fazele ce pot fi întâlnite în sistemul binar apă-surfactant 34 Figura. I.18. Diagrama de fază pentru Pluronic P123 în apă [Wanka et al., 1994] 34
Figura.I.19. Structura moleculei de tetraetilortosilicat 35
10
Figura I.21. Efectul temperaturii de tratament hidrotermal asupra porozității materialului de tip SBA-15 pentru A) 35 °C<T<60 °C, B) T ~100 °C, C) T>130 °C [Galarneau et al., 2002] 37 Figura.I.22. Tipuri de micropori si mezopori în materialul de tip SBA-15 [Bérubé et al., 2005] 38 Figura. I.23. Etapele din timpul calcinarii unui material de tipul SBA-15 în atmosferă de aer [Bérubé et al.,
2008] 40
Figura I.24. Formarea de AMO pe template-uri dure (metoda de nanoreplicare) [Liu et al., 2007] 42
Figura.I.25. Mezostructurarea materialelor prin evaporare (Metoda AAIE) 45
Figura I.26. Schema de preparare a AMO prin metoda AAIE [Hartmann et al., 2012] 45
Figura I.27. Energia de activare pentru : A) reacție necatalizată și B) reacție catalizată 46 Figura. I.28. Stereoizomeri formaţi prin adiţia la legătua olfinică a ciclohexenei 48 Figura. I.29. Reacția generală de hidrogenare a aldehidelor α,β-nesaturate 48 Figura. I.30. Cinamaldehida (denumirea IUPAC (2E)-3-fenilpropil-2-enal) 49
Figura. I.31. Efectul mesomeric în aldehidele α,β-nesaturate 50
Figura. I.32. Reacția de hidrogenare la legătura dublă C=C 51
Figura. I.33. Adsorbția preferețială la aldehidele α,β- nesaturate [Claus et al., 1998] 52 Figura. I.34. Mecanismul de adsorbție și adiție de hidrogen la aldehidele α,β- nesaturate propus de către
Horiuti-Polanyi [Claus et al., 1998] 53
Figura II. 1. Difractie de raze X. Principiul Legii lui Bragg 69
Figura II. 2. Aranjamentul porilor în silicea mezoporoasă ordonată de tip SBA-15 [Szczodrowski et al.,
2008] 69
Figura II.3. Difracția la unghiuri mici pentru silicea mesoporoasă de tip SBA-15 70 Figura II.4. Clasificarea IUPAC a izotermelor de adsorbtie/desorbtie 72 Figura II. 5 Imagine MET reprezentativă pentru SBA-15 [Zhao et al., 1998b] 74 Figura II.6. Montajul reacției de hidrogenare a t-cinamaldehidei. Intrare H2; 2 – Barbotor; 3 - Plită prevazută cu agitare magnetică; 4 – Magnet; 5 - Amestec de reacție; 6 - Refrigerent ascedent 76 Figura I.1. Efectul temperaturii de tratament hidrotermal asupra porozității materialelor de tip SBA-15: A) 35⁰C<T<60⁰C, B) T ~100⁰C, C) T>130⁰C [Galarneau et al., 2002] 78 Figura III.2. Difractogramele de raze X la unghiuri mici pentru suporturile preparate la diferite temperaturi
ale tratamentului hidrotermal 79
Figura III.3. Izotermele de adsorbție/desorbție (stânga) şi distribuția mărimii porilor (dreapta) pentru suporturile preparate la diferite temperaturi ale tratamentului hidrotermal 80
11
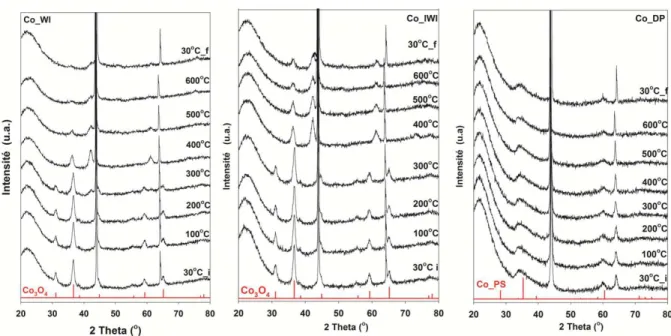
Figura III.4. Difractogramele de raze X la unghiuri mari pentru materialele care conțin formele oxidice de nichel (stânga), cobalt(mijloc) și cupru (dreapta) preparate pe suporturi de SBA-15[x] prin metoda IWI-MD
83
Figura III.5. Izotermele de adsorbție/desorbție (stânga) şi distribuția mărimii porilor (dreapta) pentru materiale care conțin formele oxidice de nichel, cobalt și cupru depuse pe suportul SBA-15[60] preparate
prin metoda IWI-MD 84
Figura III.6. Izotermele de adsorbție/desorbție (stânga) şi curbele de distribuţie ale mărimii porilor (dreapta) pentru materiale care conțin nichel, cobalt și cupru depuse pe suportul SBA-15[100] preparate prin metoda
IWI-MD 85
Figura III 7. Izotermele de adsorbție/desorbție (stânga) şi curbele de distribuţie ale mărimii porilor (dreapta) pentru materiale care conțin nichel, cobalt și cupru depuse pe suportul SBA-15[140] prin metoda IWI-MD
87 Figura III.8. Conversia cinamaldehidei în funcție de timpul de reacție pentru catalizatorii M[x] după reducere sub flux de H2 la 350 °C (probele de Ni[x] si Cu[x]) şi 500 °C (probele de Co[x]).(Condiţii de reacţie: Treacţie = 150 C, 0,265 g catalizator, 1 mL CNA, 25 mL carbonat de propilen ca solvent, flux de H2 =
1 L/h, viteza de agitare = 900 rpm) 88
Figura III.9. Difractogramele de raze X la unghiuri mari pentru materialele care conțin formele oxidice de nichel 5% (stânga), nichel 10% (mijloc) și cupru 10% (dreapta) preparate prin metoda IWI-MD şi uscate la
diferite intervale de timp 10
Figura III.10. Evoluţia mărimii cristalitelor oxizilor de cupru şi nichel cu timpul de uscare 92 Figura III.11. Curbele RTP (stânga) difractogramele de raze X corespunzătoare acestora (dreapta) pentru materialele care conțin formele oxidice de nichel 5% preparate prin metoda IWI-MD 94 Figura III.12. Difractogramele de raze X in-situ după uscare timp de 150 de zile şi calcinare în aer la 500 °C, înregistrate pentru Ni 5% (stânga), Ni 10 % (mijloc) şi Cu 10 % (dreapta).preparate prin metoda
IWI-MD 95
Figura III.13. Difractogramele de raze X in-situ după reducere în atmosferă de hidrogen înregistrate pentru Ni 5% calcinat (stânga), Ni 5% uscat 2 zile (mijloc) şi Cu 10 % uscat 2 zile (dreapta) preparate prin metoda
IWI-MD 97
Figura III.14. Imagini MET pentru probele Ni 5% (A) şi Ni 10 % (B) uscate timp de 60 de zile şi respectiv, 150 de zile, apoi calcinate la 500 °C. Comparativ, imagini MET pentru probele uscate 60 de zile şi reduse
direct în flux de H2la 600 °C 98
Figura III.15. Conversia cinamaldehidei în funcție de timpul de reacție pentru catalizatorii de tip Ni 5%, preparaţi prin metoda IWI-MD şi a căror precursori au fost supuşi la diferiţi timpi de uscare. 100(Condiţii de reacţie: Treacţie= 150 °C, 0,265 g catalizator, 1 mL CNA, 25 mL carbonat de propilen ca solvent, flux de H2
= 1 L/h, viteza de agitare = 900 rpm) 100
Figura III.16. Difractogramele de raze X la unghiuri mari pentru materialele care conțin formele oxidice de nichel (stânga), cobalt (mijloc) și cupru (dreapta) preparate prin IWI-MD şi uscate la diferite temperaturi 103
12
Figura III.17. Izotermele de adsorbție/desorbție (stânga) şi distribuţia mărimii porilor (dreapta) pentru materialele care conțin formele oxidice de nichel depus pe suport de SBA-15 prin metoda IWI-MD şi uscate
la diferite temperaturi 104
Figura III.19. Izotermele de adsorbție/desorbție (stânga) şi distribuţia mărimii porilor (dreapta) pentru materialele care conțin cobalt depus pe suport de SBA-15 prin metoda IWI-MD şi uscate preparate la diferite
temperaturi 106
Figura III.20. Tipuri de pori existente în materialele de tip oxid metalic depus pe suportul mezoporos
SBA-15 106
Figura III.21. Conversia cinamaldehidei în funcție de timpul de reacție pentru catalizatorii de nichel (stânga), cobalt (mijloc) și cupru (dreapta) preparate preparaţi prin IWI-MD şi uscaţi la diferite temperaturi. (Condiţii de reacţie: Treacţie = 150 C, 0,265 g catalizator, 1 mL CNA, 25 mL carbonat de propilen ca
solvent, flux de H2 = 1 L/h, viteza de agitare = 900 rpm) 108
Figura III.22. Difractogramele de raze X la unghiuri mari pentru materialele care conțin formele oxidice de nichel (stânga), cobalt (mijloc) și cupru (dreapta) cu diferite grade de încărcare în metal preparate prin
IWI-MD 111
Figura III.23. Izotermele de adsorbție/desorbție (stânga) şi distribuţia mărimii porilor (dreapta) pentru materialele care conțin formele oxidice de nichel, cobalt și cupru cu grade de încărcare în metal de 10 % şi
preparate prin metoda IWI-MD 111
Figura III.24. Imagini MET pentru materialele care conțin fromele oxidice de nichel, cobalt și cupru cu grade de încărcare în metal de 10 % şi preparate prin metoda IWI-MD 112 Figura III.25. Conversia cinamaldehidei în funcție de timpul de reacție pentru cataliozatorii de nichel, cobalt și cupru cu grade de încărcare în metal de 10 % şi preparate prin metoda IWI-MD.(Condiţii de reacţie: Treacţie = 150 C, 0,265 g catalizator, 1 mL CNA, 25 mL carbonat de propilen ca solvent, flux de H2 = 1 L/h, viteza
de agitare = 900 rpm) 113
Figura III.26. Difractogramele de raze X la unghiuri mari pentru materialele care conțin Ni, Cu și Co
preparate prin metoda DP 116
Figura III.27. Principalele procese care au loc în DP 117
Figura.III.28. Izotermele de adsorbție/desorbție (stânga) şi distribuţia mărimii porlior (dreapta) pentru
materialele care conțin Ni, Cu și Co preparate prin metoda DP 118
Figura III.29. Imagini MET pentru materialele care conțin Ni, Cu și Co preparate prin metoda DP, după
calcinare la 500 ºC 120
Figura III.30. Difractogramele de raze X in-situ după reducere termoprogramată la diferite temperaturi realizate pentru nichel (stânga), cobalt (mijloc) și cupru (dreapta) preparate prin metoda DP 121 Figura III.31. Imagini MET pentru materialele care conțin Ni, Cu și Co preparate prin metoda DP
dupăreducere în atmosferă de H2, la 600°C 122
13
Figura.III.33. Difractogramele de raze X la unghiuri mari pentru materialele ce conțin Ni, Cu și Co preparate prin metodele IWI, WI și DP. (*) reprezentand filosilicatului de cobalt (Co3(Si2O5)2(OH)2) 124
Figura III.34. Izotermele de adsorbție/desorbție ale materialelor care conțin cobalt pe suport de SBA-15 preparate prin metodele IWI, WI și DP.
125 Figura III.35. Imagini MET pentru materiale be bază de nichel, cobalt şi cupru preparate prin metodele IWI, WI și DP, după calcinare la 500 ºC
127 Figura.III.36. Difractogramele de raze X in-situ înregistrate după reducerea termoprogramată la diferite temperaturi pentru materialele care conțin cobalt, preparate prin metodele IWI, WI și DP
128 Figura III.37. Profilele RTP ale materialelor ce conțin Co (A), Ni și Cu (B) preparate prin metodele IWI și DP
129 Figura.III.38. Conversia cinamaldehidei în funcție de timpul de reacție pentru materialele care conțin cobalt (stânga) nichel și cupru (dreapta) preparate prin metodele IWI, WI și DP
132 Figura III.39. Difractogramele de raze X la unghiuri mari pentru materialele care conțin formele oxidice de nichel depus pe suport calcinat (stânga) și pe suport necalcinat (dreapta) preparate prin MI 137 Figura III.40. Difractogramele de raze X la unghiuri mari pentru materialele care conțin formele oxidice de cobalt depus pe suport calcinat (stânga) și pe suport necalcinat (dreapta) prin MI 138 Figura III.41. Difractogramele de raze X la unghiuri mari pentru materialele care conțin formele oxidice de cupru depus pe suport calcinat (stânga) și pe suport necalcinat (dreapta) prin MI 139 Figura III.42. Izotermele de adsorbție/desorbție a azotului (stânga) şi distribuția mărimii porilor (dreapta) pentru materialele care conțin formele oxidice de nichel depus pe suport calcinat prin metoda M 141 Figura III.43. Izotermele de adsorbție/desorbție a azotului (stânga) şi distribuția mărimii porilor (dreapta) pentru materialele care conţin formele oxidice de nichel depus pe suport necalcinat prin metoda MI 142 Figura III.44. Izotermele de adsorbție/desorbție a azotului (stânga) şi distribuţia mărimii porilor (dreapta) pentru materialele care conțin formele oxidice de cobalt depus pe suport calcinat şi necalcinat prin metoda
MI 143
Figura III.45. Izotermele de adsorbție/desorbție a azotului (stânga) şi distribuţia mărimii porilor (dreapta) pentru materialele care conțin formele oxidice de cupru depus pe suport calcinat şi necalcinat prin metoda MI
145 Figura III.46. Microscopia electronică de transmisie pentru materialele care conțin nichel preparate pe
suport calcinat prin metoda MI si impregnare 146
Figura III.47. Microscopia electronică de transmisie pentru ce conțin pentru nichel prepate pe suport
14
Figura III.48. Histrogramele probelor ce conțin Nichel preparate prin MI pe suport necalcinat: Ni_a1-
(stânga), Ni_a2-(mijloc) Ni_a4-(dreapta) 147
Figura III.49. Microscopia electronică de transmisie pentru ce conțin pentru cobalt preparate prin metoda
MI 148
FiguraIII.50. Microscopia electronică de transmisie pentru Cu_a2 preparată prin MI 149 Figura III.51. Profilele RPT pentru materialele ce conțin pentru nichel preparate pe suport calcinat(stânga)
și suport necalcinat(dreapta) 151
Figura III.52. Profilele RTP pentru materialele care conțin cobalt (pe suport calcinat-stânga), pe suport necalcinat- mijloc) și cupru pe suport calcinat şi necalcinat (dreapta) preparate prin metoda MI 152 Figura III.53. Conversia cinamaldehidei în funcţie de timpul de reacţie pentru materialele care conțin nichel (stânga), cobalt (mijloc) și cupru (dreapta) preparate prin metoda MI. (Condiţii de reacţie: Treacţie= 150 °C, 0,265 g catalizator, 1 mL CNA, 25 mL carbonat de propilen ca solvent, flux de H2 = 1 L/h, viteza de agitare
= 900 rpm) 54
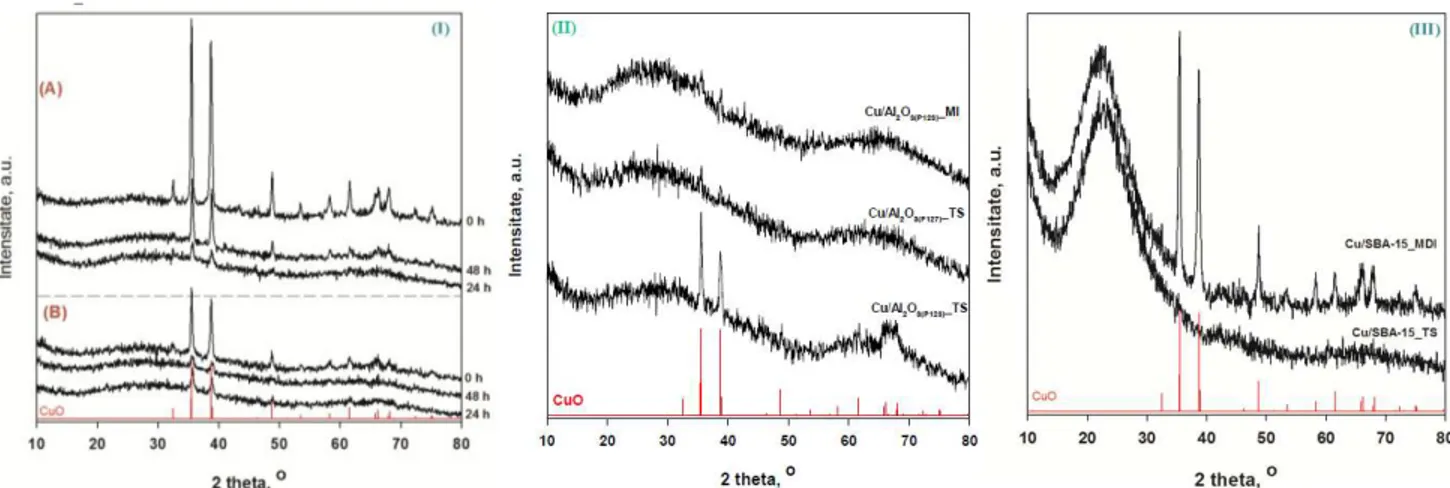
Figura III.54. Reprezentarea schematică a localizării şi dispersiei nanoparticulelor oxizilor metalici preparaţi prin metoda MI optimizată în funcţie de natura suportului SBA-15 157 Figura III.55. Microscopia electronică de transmisie pentru suporturile de AMO cu diferite texturi. 160 Figura III.56. Izotermele de adsorbție/desorbție a azotului pentru suporturile AMO cu diferite texturi. 160 Figura III.57. Izotermele de adsorbtie/desorbşie a azotului (stânga) și curbele de distributie a mărimii porilor (dreapta) pentru AMO preparate cu P123 prin același protocol de sinteză 161 Figura III.58 Difractograme de raze X pentru (I) Cu/Al2O3(P123)(10 wt. % Cu) preparat prin MI (influenţa timpului tratamentului termic și a modului de pregătire a suportului – [(A) calcinat si (B) necalcinat]; (II) Cu/Al2O3 (5 wt. % Cu) preparat prin mai multe metode (influența metodei de preparare și a copolimerului) și
(III) Cu/SBA-15 (5 wt. % Cu) preparat prin MDI și TS 163
Figura III.59. CurbeRTP reprezentative pentru probele de cupru preparate pe SBA-15 şi AMO prin metode
diferite 165
Figura III.60. Conversia CNA vs timpul de reacție (A) și selectivitatea la CNOL (B) pentru catalizatori de cupru/alumina preparați prin MI și TS; conversia CNA și distribuția tipică a produselor de reacție pentru un catalizator de cupru depus pe alumină mezoporoasă – Cu/Al2O3(P123)__MI (C) și selectivitățile la produsele de reacție pentru acelați catalizator (D).(Condiții de reacție: 1 mL CNA, 250 mg catalizator, 40 mL
izo-propanol, Treactie = 130 °C, 10 bar H2) 167
Figura III.61. Difratogramele de raze X pentru probele CuO/Al2O3 cu diferite grade de încărcare 169
Figura III.62. Izotermele de adsorbție (stânga) și curbele de distribuție ale mărimii porilor (dreapta) pentru
probele CuO/Al2O3 169
Figura III.63. Imagini MET pentru proba Cu/Al2O3_5% (stanga); Spectru EDX reprezentativ (dreapta) 171
15
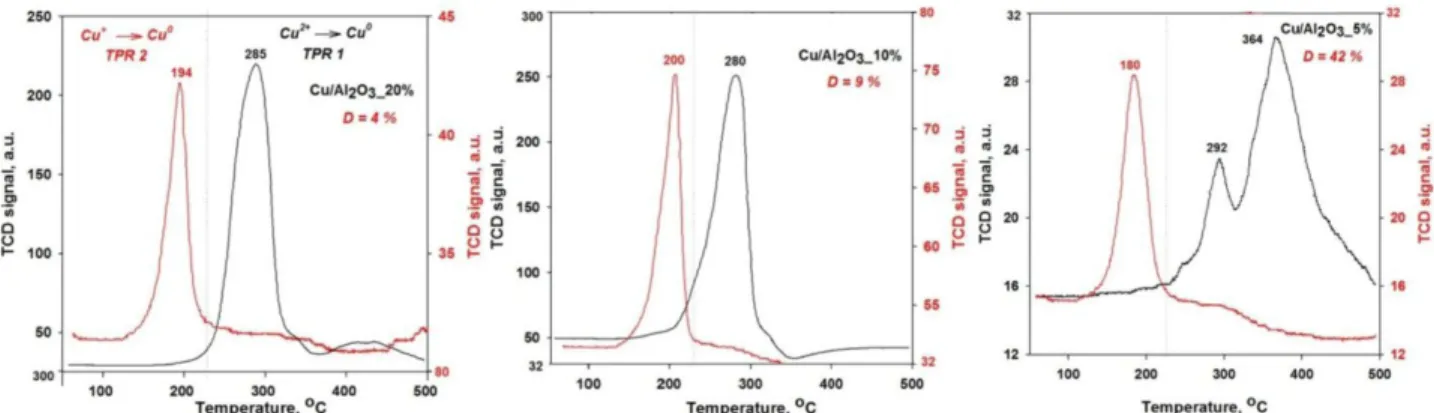
Figura III.65. Curbele RTP pentru probele CuO/Al2O3: negru – TPR 1 – înregistrat inainte de titrarea cu N2O; roşu – TPR 2 – TPR înregistrat după titrarea cu N2O 173
Figura III.66. Conversia CNA vs timpul de reacție (A) și selectivitatea la CNOL (B), HCNOL (B) și HCNA (C) pentru cei trei catalizatori de Cu/Al2O3. (Condiții de reacție: 1 mL CNA, 250 mg catalizator, 40 mL
izo-propanol, Treactie = 130 °C, 10 bar H2) 175
Figura III.67. Difractogramele de raze X la unghiuri mici (A) si unghiuri mari (B) pentru probele calcinate de tip CuCo/SBA-15. Izotermele de adsorbție-desorbție a azotului (C) si distribuția mărimii porilor calculata
prin NL-DFT (E) pentru probele calcinate de tip CuCo/SBA-15 177
Figura III.68. Imagini MET reprezentative pentru probele calcinate de tip CuCo/SBA-15:A – CuCo01, B –
CuCo28, C – CuCo11 178
Figura III.69. Curbele TPR pentru probele de tip CuCo/SBA-15 179
Figura III.70. Difractogramele de raze X inregistrate in-situ pentru probele de tip CuCo/SBA-15 dupa reducere termoprogramata la diferite temperaturi (A) – CuCo01; (B) – CuCo28; (C) – CuCo11 şi (D) –
CuCo82 180
Figura III.71. Imagini MET reprezentative pentru catalizatorii de tip CuCo/SBA-15: A – CuCo01, B –
CuCo28, C – CuCo11 181
Figura III.72. Conversia CNA in funcție de timpul de reacție (A), selectivitatea la CNOL (B), HCNA (C) si HCNOL (D) pentru catalizatorii de tip CuCo/SBA-15. (Condiții de reacție : Treducere = 500 °C pentru proba CuCo01 si 350 °C pentru celelalte probe; Treactie = 150 °C, 0.265 g catalizator; 1 mL CNA, 25 mL carbonat de propilen in calitate de solvent, flux de H2 = 1 L h-1 , viteza de agitare = 900 rpm) 182 Figura III.73. Conversia CNA in functie de timpul de reacție (A), selectivitatea la CNOL (B), HCNA (C) si HCNOL (D) pentru catalizatorii de tip CuCo/SBA-15. (Condiții de reacție : Treducere = 500 °C pentru proba CuCo01 si 350 °C pentru celelalte probe; Treactie = 130 °C, 0.256 g catalizator; 1 mL CNA,40 mL
16 Lista cu tabele
Tabel I.1. Metode uzuale pentru obținerea catalizatorilor suportați [Zhong et al.,2013] 13 Tabel I.2. Exemple de materiale anorganice care prezintă diferite interacții între surfactant și rețeaua
anorganică 30
Tabel III.1. Proprietățile texturale ale suporturilor de SBA-15 preparate la diferite temperaturi ale
tratamentului hidrotermal 81
Tabel III.2. Dimensiunea cristalitelor calculată cu ecuația Scherrer pentru materialele care conțin formele oxidice de nichel, cobalt și cupru preparate pe SB-15 cu diferite texturi 82 Tabel III.3. Proprietățile texturale ale materialelor care conțin nichel, cobalt și cupru depuse pe suportul
SBA-15[60] preparate prin metoda IWI-MD 85
Tabel III.4. Proprietățile texturale ale materialelor care conțin nichel, cobalt și cupru depuse pe suport de
SBA-15[100] prin metoda IWI-MD 86
Tabel III. 5. Proprietățile texturale ale materialelor ce conțin Nichel, Cobalt și Cupru pe suport de
SBA-15[140] preparate prin metoda IWI-MD 87
Tabel III.6. Conversia CNA şi selectivităţile la produsele de reacţie pentru catalizatorii pe bază de nichel,
preparaţi pe suporturi de SBA-15 cu texturi diferite 90
Tabel III.7. Conversia CNA şi selectivităţile la produsele de reacţie pentru catalizatorii de tip Ni 5%, preparaţi prin metoda IWI-MD şi a căror precursori au fost supuşi unor perioade de uscare diferite 100 Tabel III.8. Proprietățile texturale ale materialelor care conțin nichel depus pe suport de SBA-15 preparate
prin IWI-MD şi uscate la diferite temperaturi 104
Tabel III.9.Proprietățile texturale ale materialelor care conțin cupru depus pe suport de SBA-15 preparate
prin IWI-MD şi uscate la diferite temperaturi 105
Tabel III.10. Proprietățile texturale ale materialelor care conțin cobalt pe suport de SBA-15 preparate prin
IWI-MD şi uscate la diferite temperaturi 107
Tabel III.11. Conversia CNA şi selectivităţile la produsele de reacţie pentru catalizatorii pe bază de nichel şi cobalt preparaţi prin metoda IWI-MD şi uscaţi la diferite temperaturi 108 Tabel III.12. Proprietățile texturale ale materialelor care conţin formele oxidice de nichel, cobalt și cupru cu grade de încărcare în metal de 10 % şi preparate prin metoda IWI-MD 111 Tabel.III.13. Activitățile si selectivitătile ale materialelor preparate prin metoda IWI-MD, studiul încărcării
cu metal 114
Tabel III.14. Proprietățile texturale ale materialelor ce conțin nichel, cobalt și cupru preparate prin metoda
DP 119
Tabel.III.15. Proprietățile texturale ale materialelor care conțin Cobalt preparate prin metodele IWI, WI și
6
Tabel III.16. Conversia CNA şi selectivităţile la produsele de reacţie pentru catalizatorii pe bază de Cu, Ni
şi Co preparaţi prin IWI, WI şi DP 133
Tabel III.17. Proprietățile texturale ale suportului de SBA-15 și ale materialelor care conțin Ni preparate
prin metoda MI pe suport calcinat 141
Tabel III.18. Proprietățile texturale ale suportului de SBA-15 și materialelor care conțin Ni preparate pe
suport necalcinat prin metoda MI 143
Tabel III.19. Proprietățile texturale ale suportului de SBA-15 și ale materialelor care conțin Co preparate
prin metoda MI 144
Tabel III.20. Proprietățile texturale ale suportului de SBA-15 și materialelor ce conțin cupru preparate prin
metoda MI 145
Tabel.III.21. Conversia CNA şi selectivităţile la produsele de reacţie pentru catalizatorii pe bază de nichel,
cobalt şi cupru preparaţi prin MI 156
Tabel III.22. Reţete optimizate pentru suporturile de alumină mezoporoasă ordonată (AMO) 158 Tabel.III.23. Proprietățile texturale ale suporturilor AMO cu diferite texturi 161 Tabel III.24. Proprietățile texturale ale AMO preparate cu P123 prin același protocol de sinteză 162 Tabel III.25. Proprietățile texturale ale probelor de cupru preparate pe AMO cu texturi diferite 164 Tabel III.26. Proprietatile fizico-chimice ale probelor CuO/Al2O3 170
Tabel III.27. Proprietățile catalizatorilor Cu/Al2O3 determinate din titrarea cu N2O 174
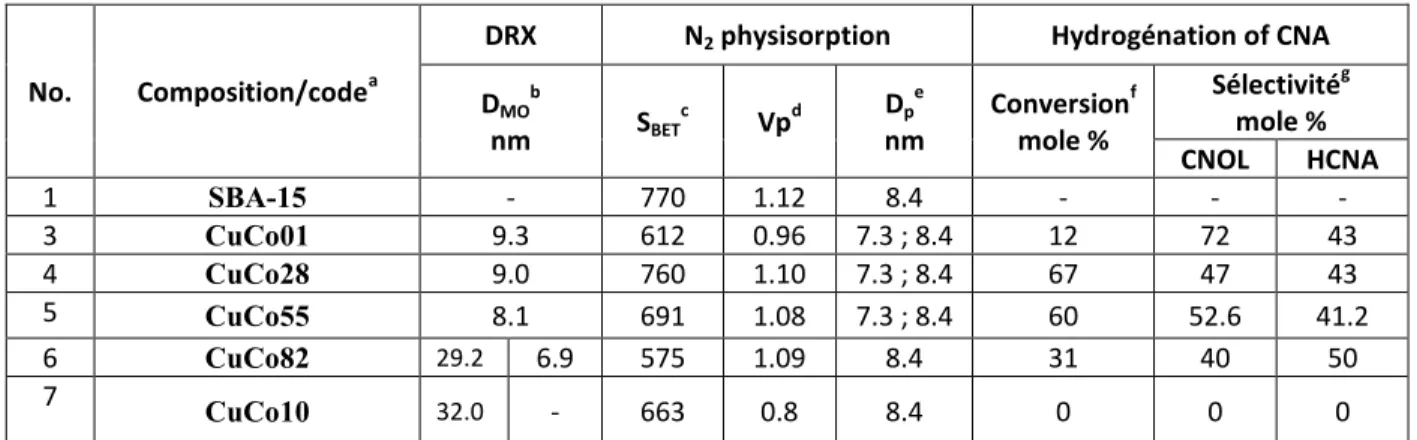
Tabel III.28. Proprietățile structurale si texturale ale suportului SBA-15 si ale materialelor CuCo/SBA-15
8 Introducere
Datorită importanței proceselor catalitice din industria chimică și a necesității continue ca acestea să fie îmbunătățite, în scopul de a reduce poluarea de mediu, dar și de a reduce costurile, se fac multe eforturi pentru a dezvolta noi căi de sinteză care să permită îmbunătățirea proprietăților fizico-chimice ale catalizatorilor și care să maximizeze activitățile lor. Una din preocupările actuale din domeniul catalizei și al nanotehnologiei este acela de a dezvolta catalizatori care să poată fi modelați uşor în funcție de aplicația industrială în care sunt folosiți.
Parametrii de sinteză care pot fi ajustați pentru a obține mărimea particulelor dorită și o interacțiune particulă/suport adecvată sunt: natura precursorului metalic, concentrația precursor, timpul de contact dintre soluție și solid, temperatura, pH-ul din timpul sintezei sau tratamentele post-sinteză care pot determina forma finală obținută pentru faza activă: spălarea, uscarea și calcinarea.
Una dintre cele mai simple și ieftine metode de prepare a materialelor care conțin metale depuse pe un suport este impregnarea, sub cele mai uzuale variante: impregnarea umedă și impregnarea umedă incipientă. Aceste metode au ca dezavantaj dispersii scăzute ale particulelor de dimensiuni mari sau în cazul metodei de impregnare umedă, localizarea metalului în special la exteriorul suportului. Aceste probleme apar în timpul uscării din cauza folosirii prin unei cantități mari de solvent și a unor viteze rapide de evaporare.
O metodă eficientă de dispersare a metalului pe suporturi oxidice este metoda infiltrării topiturii. Această metodă implică mojararea precursorului metalic și suportului, ambele în fază solidă, fără utilizarea unui solvent. Astfel sunt eliminate dezavantajele create de prezenţa solventului.
O tehnică utilizată pentru prepararea unor catalizatori cu faze metalice bine dispersate pe suport şi care permite grade de încărcare cu fază activă mai mari decât la celelalte metode este depunerea prin precipitare. Folosirea silicei, de exemplu, ca suport, implică dizolvarea parțială a acesteia, condiție necesară pentru precipitarea precursorului metalic sub formă de filosilicați, aceaștia fiind utilizați ca precursori pentru obținerea fazelor active foarte bine dispersate pe suprafața suportului.Toate aceste eforturi sunt depuse pentru a obține catalizatori eficienţi pentru
9
reacţiile de hidrogenare, ca de exemplu, hidrogenarea cinamaldehidei, care aparţine familiei de aldehide -nesaturate. Acestă reacţie a fost selectată datorită importanţei industriale, toate produsele de hidrogenare sunt folosite fie ca atare, fie ca intermediari pentru produse utile în industria farmaceutică, parfumerie, industria alimentară etc.
Prin urmare, obiectivul principal al tezei mele este acela de a prepara catalizatori pe bază de metale tranzitionale: Ni, Cu și Co, pe suporturi de silice mezoporoasă ordonată și alumină mezoporoasă ordonată, folosind metode simple de prparare optimizate - impregnare umedă incipientă urmată de uscare în condiții blânde, impregnarea cu doi seolvenţi, depunerea prin precipitare, infiltrarea topiturii și depunere prin precipitare.
Capitolul I conține un studiu bibliografic axat pe informatiile de literatură referitoare la catalizatorii eterogeni pe bază de metale nobile și ne-nobile și a factorilor care influenţează performanțele catalitice ale acestora. De asemenea, se face o trecere în revistă a principalelor metode de preparare a catalizatorilor depuşi pe suport cu centralizare, în mod particular, asupra problematicilor acestor metode.
Capitolul II este dedicat părții experimentale în care sunt descrise metodele de sinteză ale suportului SBA-15 și ale materialelor catalitice și tehnicile de caracterizare folosite în vederea determinării proprietăților fizico-chimice ale acestor materiale.
Capitolul III este cea mai amplă parte a tezei şi include rezultatele originale asupra materialelor catalitice obţinute prin metode de preparare optimizate. Capitolul este divizat în două părţi principale: prima parte este axată pe proprietăţile fizico-chimice şi catalitice ale materialelor pe bază de metale tranziţionale monocomponte preparate pe suportul de silice mezoporoase SBA-15 în timp ce partea a doua este centrată pe proprietăţile fizico-chimice şi catalitice ale materialelor pe bază de metale tranziţionale monocomponte preparate pe suportul de alumină mezoporoasă. De asemenea, s-a realizat şi un studiu asupra materialelor pe bază de metale tranziţionale bicomponte preparate pe suportul de silice mezoporoasă SBA-15.
În finalul tezei sunt prezentate concluziile generale, referinţele bibliografice şi publicaţiile aferente tezei.
10
11
RESUME DU DOCUMENT
-VERSION FRANCAISE-
12
Chapitre I.
Résumé étendu du contenu du manuscrit de Doctorat
Objectif du Doctorat et contenu du document
L’objectif proposé pour mon Doctorat était la préparation de matériaux catalytiques à base de métaux de transition performants pour la réaction d’hydrogénation chimiosélective du cinnamaldéhyde. Les phases actives étudiées étaient à base de métal de transition (Ni, Co, Cu), supportés sur des matériaux à porosité organisée. L’étude peut être divisée en trois parties distinctes, selon la nature du support utilisé et les phases supportées. La première partie, la plus conséquente, traite de la dispersion de métaux de transition sur des supports siliciques, dans le cas de la préparation de catalyseurs monométalliques. La seconde partie, de taille plus restreinte, traite de la dispersion de métaux de transition sur des supports aluminiques. La troisième partie porte sur la préparation de catalyseurs bimétalliques (sur des supports siliciques). Les chapitres suivants décrivent l’ensemble des études expérimentales menées au cours du Doctorat.
Chapitre I.2. Matériaux préparés par la voie IWI-MD
Dans ce chapitre est présentée la préparation des catalyseurs à base de Ni, Co et Cu par la méthode IWI-MD (Incipient Wetness Impregnation –Mild Drying). Nous avons effectué plusieurs études afin de valider l’efficacité de cette méthode de préparation pour la dispersion de métaux de transition sur les supports mésoporeux. Les études successives sont: (i) influence de la texture du support, (ii) influence de la température de séchage, (iii) influence du temps de séchage; (iv) influence de la teneur en métal.
L’objectif a été de démontrer la faisabilité de produire des particules supportées de faibles tailles (de l’ordre du nanomètre) en utilisant une technique aussi simple que l’imprégnation dans l’eau. A ces tailles de particules, des activités significativement améliorées, par rapport aux matériaux classiquement préparés, sont alors obtenues.
Chapitre I.3. Matériaux préparés par la voie DP
Des matériaux catalytiques à base de Ni, Co et Cu ont été préparés en utilisant la méthode de déposition par précipitation, effectuée par décomposition thermique de l’urée. L’objectif de l’utilisation de cette méthode était de disperser des phases métalliques à un degré élevé, mais
13
également d’améliorer significativement la résistance au vieillissement thermique et au frittage des particules métalliques produites.
Chapitre I.4. Imprégnation par la méthode MI
Dans ce troisième chapitre, nous avons étudié la méthode d’infiltration des sels fondus, dite de Melt Infiltration (MI). Par rapport à la méthode présentée dans la littérature, l’étude du processus de diffusion dans les pores du précurseur démontre de la nécessité d’une étape intermédiaire de vieillissement afin d’assurer une infiltration complète du précurseur dans la porosité du support. D’autre part, nous avons également montré qu’il était possible de faire croitre les particules métalliques sélectivement dans la porosité secondaire de faible taille, présente dans les murs de la silice SBA-15 utilisée comme support hôte.
Ces trois premiers chapitres ont été effectués en utilisant la silice de type SBA-15 comme support. Le dernier chapitre de ce doctorat présente des premiers résultats obtenus pour la préparation de catalyseurs d’hydrogénation supportés sur Alumine Mésoporeuse Ordonnée (AMO).
Chapitre I.5. Catalyseurs supportés sur AMO
Dans ce chapitre, nous avons donc préparés des matériaux catalytiques à base de Ni et de Cu sur des supports AMO obtenus par la voie d’auto-assemblage induit par évaporation (AAIE, ou encore EISA pour evaporation induced self-assembly). Les paramètres étudiés sont :
Effet de la texture du support, à partir d’alumines présentant des tailles de pores différentes;
Effet du mode de déposition des métaux (IWI-MD, MI et TS). Chapitre I.6. Catalyseurs bimétalliques
Cette étude a été réalisée dans le but d’éprouver la méthode de préparation IWI-MD pour la préparation de catalyseurs bimétalliques. Des systèmes bimétalliques, contenant du cobalt et du cuivre (Cu-Co), ont ainsi été préparés et caractérisés. Leurs propriétés catalytiques ont été ensuite évaluées.
14
I.1. Les catalyseurs métalliques dispersés, généralités
L’étude de la synthèse et de la caractérisation de nanoparticules métalliques est au cœur de la recherche actuelle dans le domaine de la catalyse hétérogène. Ces nanoparticules, généralement supportées dans le cas de la préparation de catalyseurs hétérogènes, peuvent être obtenues par deux voies principales: (i) en solution - les particules (métalliques, oxydes) vont croître en trois dimensions et seront ensuite déposées / immobilisées sur un support adéquat; (ii) un précurseur métallique sera déposé à l’interface solution-support, ce dernier sera ensuite décomposé et activé par une succession de traitements thermiques.1,2Une préoccupation actuelle, dans le domaine de la catalyse hétérogène, est de déterminer des paramètres de synthèse permettant d’orienter la croissance des phases actives, et générer des matériaux présentant des propriétés physiques et chimiques améliorées. La dimension de la particule métallique peut ainsi être ajustée en modifiant les paramètres de synthèse, par conséquent, les dimensions de ces particules peuvent varier entre la taille d’un cluster (uniquement quelques atomes), jusqu’à des dimensions macroscopiques de particules de métaux ou d’oxydes métalliques. Pour une application en catalyse hétérogène, ces nanoparticules, généralement de faibles tailles (de l’ordre de quelques nanomètres à quelques dizaines de nanomètres), vont être immobilisées sur un support poreux présentant des propriétés texturales, chimiques et mécaniques compatibles avec l’application visée. Ces supports vont généralement être de type carbone, silice, alumine, titane, cerine-zircone, etc. Le support est en général stable thermiquement, et ce, même à des températures élevées (> 500°C). Il confère également, au catalyseur, des propriétés permettant son utilisation dans des procédés industriels. Ces propriétés sont, par exemple, une mise en forme macroscopique (sphères, extrudés, trilobs…), des tenues mécaniques élevées, un réseau poreux large afin de faciliter la diffusion de molécules, des propriétés de surface conditionnant la stabilité sur le long terme des phases actives divisées.1
Les caractéristiques uniques des nanoparticules, déposées sur un support, sont mises en évidence par leurs propriétés spécifiques, issues de leur morphologie (forme et taille), de leur dispersion, et des propriétés électroniques pouvant être modifiées par l’interaction avec le support. En comparaison avec les catalyseurs massiques, les catalyseurs supportés présentent des activités améliorées, mais également des sélectivités en réaction pouvant être modifiées. En effet, la réduction de la taille des particules entraîne une augmentation de la densité des sites exposés, mais également induit une augmentation significative des défauts de surface localisés sur les arêtes, les coins et les bords des particules.3,4,5 Ainsi, alors que certains métaux sont pratiquement inactifs
15
lorsque sous la forme de particules massiques, ces éléments deviennent actifs lorsque dispersé à la surface d’un support. L’activité des catalyseurs solides est en effet généralement proportionnelle avec la surface active exposée rapportée à l’unité du volume du catalyseur. Pour cette raison, un nombre élevé des particules de faible dimension par unité de volume permettra d’obtenir des activités catalytiques élevées. Malheureusement, un problème récurrent à l’utilisation des nanoparticules est leur forte propension à croître en taille dès des températures de traitement et d’activation intermédiaires (> 300°C). Ainsi, leur stabilisation à la surface d’un support devient une nécessité afin d’élargir leur champs d’application.61
En raison de l’importance croissante des procédés catalytiques dans l’industrie chimique, ainsi que la nécessité de l’amélioration continue de leurs performances afin de diminuer leur empreinte environnementale, de nombreux efforts sont effectués afin de développer de nouvelles voies de synthèse permettant d’orienter les propriétés des matériaux finaux, et maximiser leurs activités. De ce fait, de nombreux paramètres de synthèse peuvent être étudiés et ajustés afin d’obtenir une taille de particule et une interaction particule / support adéquates : les propriétés de surface du support, la nature du précurseur métallique, la concentration du précurseur, le temps de contact solution / solide, la température d’imprégnation, le pH d’imprégnation... Les traitements post-synthèse sont également importants et conditionnent la forme finale obtenue pour la phase active: étapes de lavage, températures de séchage et de calcination, mode de réduction (gaz, solution), rampe de température et atmosphère utilisée pour la réduction. Tous ces facteurs ayant chacun un effet marqué sur les propriétés du matériau catalytique final.1,2
Ci-dessous sont résumés certaines approches proposées dans la littérature, et étudiées dans le cadre de ce travail de Doctorat.
I.1.1. Méthode de préparation des matériaux divisés par imprégnation
Les matériaux catalytiques supportés peuvent être préparés à partir d’une multitude de protocoles expérimentaux différents. Les méthodes de synthèse les plus communes pour stabiliser des nanoparticules métalliques sur un support présentant une surface spécifique élevée sont succinctement décrites dans le Tableau 1, puis détaillés dans les paragraphes suivants.
Tableau 1. Voies d’imprégnation classiquement utilisées afin de préparer des catalyseurs supportés (Vs-volume de solution, Vp-volume poreux du support).1
Type d’Imprégnation Caractéristiques Avantage/Désavantage
Incipient Wetness Impregnation (IWI), également appelée Capillary
Vs≤ Vp ; la quantité de précurseur
16
Impregnation or Dry Impregnation
Traduction : imprégnation à
humidité naissante, imprégnation à sec
la teneur désirée en métal; le
précurseur métallique est
généralement fortement
concentré dans la solution d’imprégnation (dans certains cas, à des concentrations proches de la limite de solubilité du précurseur)
permet également de contrôler la teneur en métal aisément.
D: interaction entre l’espèce en
solution du métal et le support faible.
Wet Impregnation (WI)
Traduction : imprégnation humide, imprégnation en excès de solvant
Vs > Vp ; le précurseur métallique
est en solution à des
concentrations inférieures au cas IWI. Le solide est immergé intégralement dans la solution, et il est récupéré ensuite par filtration ou bien par évaporation de l’excès de solvant.
A: cette voie de préparation
permet d’obtenir une
homogénéité du mélange support / précurseur améliorée.
D: la filtration est généralement
nécessaire, ce qui peut induire un dépôt incomplet du précurseur sur le support (soit des teneurs métalliques inférieures à la teneur théorique calculée).
Grafting
Traduction : greffage
Vs > Vp ; la méthode implique une
interaction forte entre le
précurseur métallique en solution et les sites de surface du support.
A: interaction forte précurseur
métallique / support. Le
précurseur est ainsi stabilisé à la surface du support (formation d’une liaison chimique).
D: l’applicabilité de cette méthode
est limitée à certains systèmes. Il
est généralement nécessaire
d’utiliser des solvants et des
précurseurs métalliques
organiques. Strong electrostatic adsorption
(SEA)
Traduction : imprégnation par adsorption électrostatique forte
Vs > Vp ; La solution contenant le précurseur est en large excès par rapport au volume poreux du support. Le pH de la solution doit avoir une valeur optimale pour assurer une interaction forte avec les sites de surface du support.
A: adsorption forte du précurseur
par interaction électrostatique à la surface du support. Ainsi, une seule couche du précurseur métallique peut être formée.
D: le pH optimal doit être
déterminé et doit être maintenu constant tout au long de l’étape d’imprégnation.
Deposition-Precipitation (DP)
Traduction : déposition par
précipitation
Vs > Vp ; La solution contenant le précurseur métallique est en excès par rapport au volume poreux. Le pH de cette solution doit être augmenté progressivement, puis stabilisé à une valeur permettant la
précipitation des hydroxydes
métalliques à la surface du support. Cette étape peut être effectuée par décomposition en température d’une solution d’urée.
A: permet d’obtenir des teneurs en
métaux élevées. L’espèce
métallique précipitée peut se trouver en forte interaction avec la surface du support
D: le pH doit être ajusté tout au
17
Une méthode simple est donc la préparation de l’espèce active divisée par imprégnation sur un support poreux. Les supports usuels présentent des volumes poreux de l’ordre du cm3
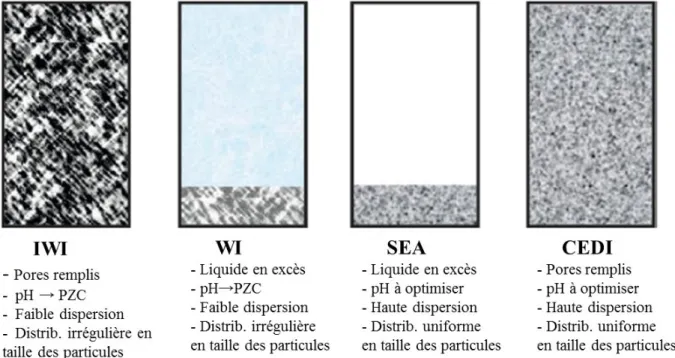
/g-1. La quantitéde sites anioniques et/ou cationiques de surface du support est influencée par la nature de la surface, ainsi que par les propriétés morphostructurales du solide (structure cristallographiques, dimension des pores, traitement thermique d’activation préalable). Dans le cas de la présence de groupement hydroxydes de surface, la réactivité de ces sites de surface ne permet pas la stabilisation d’un précurseur par des liaisons électrostatiques fortes. Ainsi, une interaction forte ne peut être générée que par greffage chimique (comme par exemple lors de l’adsorption d’un précurseur acétylacétonate de métal, suivie de sa décomposition partielle par réaction avec le groupement –OH de surface). Néanmoins, la génération d’une interaction forte entre le précurseur métallique et les sites de surface n’est pas une nécessité, et les imprégnations en milieu aqueux sont généralement préférées. De fait, les voies d’imprégnation de type IWI ou bien WI sont largement plus utilisées que les voies de type greffage ou bien SEA. Cependant, les voies de préparation IWI et WI peuvent présenter d’importants inconvénients. Ainsi, dans le cas de l’utilisation de la voie IWI, la migration d’une fraction importante du précurseur métallique vers la surface externe du support lors de l’étape de séchage peut être observée. D’autre part, un autre désavantage à l’utilisation de ces méthodes est la répartition en taille irrégulière des particules générées, et les faibles dispersions obtenues. Ces
Figure 1. Caractéristiques des méthodes de préparation des matériaux catalytiques par imprégnation.
18
deux dernières caractéristiques proviennent notamment de la très faible interaction, ou de l’absence d’interaction, entre les précurseurs en solution et les sites de surface du support. Il est néanmoins possible, avec un ajustement des paramètres thermiques de la préparation, de minimiser ces effets, et d’obtenir des matériaux présentant des homogénéités améliorées.
Un moyen simple est, par exemple, l’utilisation d’une rampe de séchage lente, afin de diminuer le phénomène de migration du précurseur vers l’extérieur du support.Lors de la préparation des phases actives supportées par la voie WI, l’utilisation d’un volume de solvant en large excès par rapport au volume poreux du support permet d’obtenir une répartition significativement améliorée du précurseur dans l’ensemble de la porosité du support. Le principal désavantage de cette méthode est que l’étape de filtration, appliquée afin d’éliminer l’excès de solvant, peut entraîner une perte de précurseur métallique dans les solutions de lavage du fait des faibles interactions entre la surface du support et l’espèce métallique stabilisée à sa surface.7 Ce type d’inconvénient n’est, par exemple,
pas observé dans le cas de l’utilisation de la voie IWI malgré l’absence d’interaction espèce métallique / support. Ci-dessous sont présentées plus en détail les méthodes utilisées dans le cadre de ce Doctorat.
I.1.1.1. Imprégnation à sec et séchage dans des conditions douces (Incipient Wetness Impregnation - Mild Drying - IWI-MD)
La préparation des phases supportées par cette méthode est similaire à une préparation classique IWI. La quantité de solution de précurseur est égale au volume poreux du support, et la concentration de la solution est dépendante de la quantité de précurseur à déposer sur le support. La différence avec la voie IWI classique vient du processus de séchage appliqué suite à l’étape d’imprégnation. Le séchage est, dans ce cas, effectué à une température basse, et pendant une durée longue. Cette étape de séchage à basse température permet d’améliorer la dispersion du précurseur à la surface du support et permet également un contrôle de la migration du précurseur vers l’extérieur de la porosité du support préalablement à sa décomposition thermique. En effet, l’augmentation de la viscosité de la solution contenant le précurseur, lors de l’étape lente d’évaporation, entraîne une diminution de la mobilité des espèces à la surface du support, ce qui, in fine, induit la formation de particules de plus faibles tailles et plus homogènement dispersées au sein de la porosité. Un phénomène de redispersion du précurseur peut même être observé sous certaines conditions, lors de l’utilisation de solutions visqueuses de précurseurs métalliques.8 L’utilisation d’une étape
19
plus forte précurseur métallique – site de surface du support. La génération de telles interactions est à l’origine d’un frittage limité des particules lors des traitements thermiques.9
En outre, lors de l’utilisation de supports présentant des porosités ordonnées (silices ou alumines mésoporeuses), la préparation des métaux supportés par cette approche permet la formation de particules confinées dans la porosité. Cet effet de confinement est bénéfique à la stabilité thermique des particules, qui présenteront des propriétés améliorées à haute température.9
I.1.1.2. Imprégnation par la voie deux solvants (Two Solvent - TS)
La méthode de préparation par la voie deux solvants est une variante de la voie d’imprégnation WI, et implique l’utilisation de deux solvants (l’eau et un solvant organique). Cette voie a été rapportée pour la première fois pour la préparation de MnO2 sur des supports de type SBA-15.10ref.
La voie TS a également été appliquée avec succès à la préparation de Co3O4 sur des matériaux de
type SBA-15 11,12,13,14, ainsi que pour l’imprégnation de AgO15 et de systèmes bimétalliques Cr-Co.16
La préparation par la voie TS comporte trois étapes distinctes : (i) la quantité nécessaire du précurseur métallique est initialement mise en solution dans une quantité d’eau égale au volume poreux du support; (ii) la silice (mésoporeuse dans les études préalablement citées) est dispersée dans le n-hexane pour former une suspension hydrophobe; (iii) la solution contenant le précurseur métallique est ajouté goute à goute au mélange n-hexane/support, sous agitation forte. Le mélange est ensuite maintenu à la température ambiante afin de permettre à la solution aqueuse de diffuser dans les pores de la silice et de remplacer le n-hexane. Après filtration et séchage, le solide récupéré va subir des traitements d’activation classiques (calcination, réduction).
I.1.1.3. Imprégnation par infiltration des précurseurs à l’état fondu (Melt Infiltration - MI)
Une voie de synthèse récente, développée pour la préparation de matériaux supportées, est la voie dite de Melt Infiltration ou encore imprégnation par les sels fondus. Dans cette voie de synthèse, l’imprégnation du précurseur à l’état liquide permet d’éviter l’utilisation d’un solvant. Cette voie de synthèse est rapportée pour la première fois en 2004 par Wang et coll. pour la préparation de cuivre divisé à la surface de la silice.17 Cette méthode peut être nommée de
différentes manières dans la littérature : solvent free impregnation (imprégnation sans solvant,)18,19
solid-state grinding (broyage solide),20 ou capillary infiltration (infiltration capillaire).21 La préparation des matériaux par MI est effectuée en deux étapes: i) le mélange physique par broyage
20
des deux composants (précurseur + support); ii) les traitements post-synthèse : diffusion, calcination, et possiblement réduction.
Comparée aux imprégnations de type WI ou IWI,22,23 cette méthode présente plusieurs
avantages. Ainsi, il est possible par la voie MI de préparer des matériaux présentant des teneurs en métal élevées. Dans le cas de l’imprégnation IWI, la teneur maximale est tributaire de la solubilité du précurseur métallique dans l’eau et du volume poreux du support. De plus, dans le cas de la préparation par MI, l’absence de solvant permet également d’éviter les phénomènes de migration du précurseur vers la surface externe du support lors de l’étape de séchage.
I.1.1.4. Déposition par précipitation (DP)
La méthode de déposition par précipitation est généralement utilisée afin de déposer des hydroxydes et/ou oxydes métalliques sous la forme de particules de faibles tailles sur un support préalablement activé. La précipitation est induite, soit par l’ajout d’un agent de précipitation, soit par ajustement du pH. Le précurseur métallique, initialement en solution, est ainsi précipité à la surface d’un support, et forme, avec les sites de surface du support, des interactions fortes. Cette méthode a été rapportée pour la première fois par Stöwenert en 1943.24 Plus récemment, Geus et
coll., en 1992, ont rapporté la synthèse de CuO dispersée sur la surface de SiO2.25 Louis et coll. ont
également étudié en détail la méthode DP. Ces auteurs utilisèrent l’urée décomposée thermiquement comme base afin d’ajuster le pH à une valeur permettant la précipitation des hydroxydes de métaux de transition sur la silice.26 Le mécanisme de déposition-précipitation du nickel sur la surface de la silice, et la formation de phyllosilicate, a également été élucidé par Burratin et coll.27
Ces auteurs ont ainsi démontré l’importance de certains facteurs influençant l’efficacité du dépôt, la dimension des particules générées, ainsi que l’environnement du métal de transition. Il s’agit notamment du temps de précipitation, de la nature de la surface du support, et de l’agent choisi pour la précipitation. Parmi les principaux avantages liés à l’utilisation de cette méthode, il est possible de citer : (i) la production de matériaux actifs présentant des surfaces actives élevées (et donc des dispersions élevées), (ii) une distribution uniforme en taille des particules sur la surface du support, (iii) la stabilisation des métaux dans un environnement chimique stable, permettant de produire des matériaux résistants au frittage.28
21 I.1.2. Propriétés des supports
Une étape clé dans la préparation d’un matériau supporté efficace est le choix du support. En effet, l’activité du matériau catalytique est liée à la morphologie et aux propriétés de surface du support sélectionné. En effet, alors que certains supports sont inertes pour de nombreuses réactions (comme SiO2), d’autres supports présentent des sites acides de surface (Brönsted et/ou Lewis), des
sites basiques, ou bien des sites redox, qui peuvent avoir une influence sur la réaction catalytique. Lorsque le support est mis en contact avec le précurseur métallique en solution, différents phénomènes ont lieu: interactions électrostatiques, formation de liaisons chimiques, dissolution / reprécipitation du support. La nature des interactions se formant entre le support et le précurseur métallique dépendent bien évidemment des propriétés de surface du support, et vont influencer la dispersion et la stabilité de la phase active. Nous allons revenir ci-après sur la classification des matériaux, ainsi que les propriétés spécifiques des matériaux utilisés dans le cadre de cette étude de Doctorat.
I.1.2.1.Classification des matériaux poreux
Les matériaux poreux ont été classifiés par l’IUPAC en fonction de la taille de leurs pores en 3 classes: matériaux microporeux (taille de pore < 2 nm), matériaux mésoporeux (dont la taille de pore est comprise entre 2 et 50 nm), et matériaux macroporeuses (taille de pore > 50 nm) (Figure 2). Dans le cadre de ce travail, nous avons utilisé exclusivement des supports mésoporeux ordonnés, c’est-à-dire présentant des pores réguliers et ordonnés à grande échelle. La synthèse de ces matériaux mésostructurés est basée sur la combinaison des deux domaines importants, que sont la science des matériaux et les procédés sol-gel, et la chimie des tensio-actifs. Ces matériaux mésoporeux ordonnés, initialement obtenus avec la silice, présentent des surfaces spécifiques et des volumes poreux élevés. Les modes de synthèse développés permettent également de moduler la taille des pores, ainsi que la composition chimique de la surface et des parois.