CODEX
DES MEDICAMENTS
VETERINAIRES
DE TUNISIE
2016
Professeur Agrégé Samir BEN YOUSSEF Docteur Mariem HAJJI
CODEX
DES MEDICAMENTS
VETERINAIRES
DE TUNISIE
AVERTISSEMENT
Le présent Codex est purement informatif, sous toutes réserves de droit et sans aucune reconnaissance préjudiciable et sans que celui-ci n’octroie de droits à des tiers ou ne les exonère de leurs obligations. Concernant les informations sur les spécialités
autorisées, seules les monographies des médicaments
valent comme texte officiel. En matière de législation, seuls les textes publiés dans le Journal Officiel de la République Tunisienne [29] constituent la source officielle.
Les prix des médicaments dans le présent travail sont mentionnés à titre indicatif et valables pour l’année 2015, les prix officiels sont de la compétence du ministère du commerce en Tunisie.
Les auteurs remercient particulièrement Dr Dalel KAMOUN et Dr Mondher DHOUIB pour leur contribution à la réalisation de cet ouvrage.
i
DES MEDICAMENTS VETERINAIRES
DE TUNISIE
® INTRODUCTION I. MEDICAMENTS ANTI-INFECTIEUX 7 1. Antibiotiques 11 1.1. β lactamines 11 1.1.1. Pénicillines 11 1.1.2. Céphalosporines 171.1.3. Les inhibiteurs des β lactamases 20
1.2. Aminosides 21 1.3. Tétracyclines 26 1.4. Macrolides et apparentés 30 1.4.1 Macrolides 31 1.4.2. Lincosamides 35 1.4.3. Synergistines 37 1.5. Antibiotiques polypeptidiques 38 1.5.1. Polymexines 38 1.5.2. Bacitracine et thiostrepton 41 1.6. Antibiotiques divers 42 1.6.1. Acide fusidique 42 1.6.2. Rifamycines 43 1.6.3. Pleuromutilines 43 1.6.4. Antibiotiques ionophores 45 1.7. Phénicols 46 2. Antibactériens artificiels 49 2.1. Sulfamides 49 2.2. Diaminopyrimidines 52 2.3. Quinolones et fluoroquinolones 54
II. MEDICAMENTS ANTIPARASITAIRES 59 1. Endo-ectoparasiticides (Lactones macrocycliques) 59
1.1. Avermectines 59
2. Antiparasitaires externes 64 2.1. Antiparasitaires externes curatifs 64
2.1.1. Pyréthrinoïdes 64
2.1.2. Formamidines 68
2.1.3. Phénylpyrazoles 70
2.2. Antiparasitaires externes préventifs 73
2.2.1. Analogues de l’hormone juvénile 73
3. Anthelminthiques 74 3.1. Nématodicides 75 3.1.1. Macrolides antiparasitaires 75 3.1.2. Benzimidazoles 75 3.1.3. Imidazothiazoles 80 3.1.4. Tétrahydropyrimidines 82 3.1.5. Salicylanilides 84 3.1.6. Mélarsomine 86 3.1.7. Praziquantel 87 3.1.8. Nitroxinil 89 4. Anticoccidiens 90 4.1. Sulfonamides 91
ii 4.4. Polyéthers ionophores 93 5. Piroplasmicides 94 5.1. Imidocarbe 94 6. Autres antiparasitaires 96 6.1. Antimoniate 96 6.2 Buparvaquone 97 6.3. Thymol 97 6.4. Fluvalinate 98
III. MEDICAMENTS ANTIFONGIQUES 99
1. Griséofulvine 100
2. Azoles antifongiques 101
3. Antibiotiques polyéniques 104
IV. MEDICAMENTS ANTI-INFLAMMATOIRES 105
1. Anti-inflammatoires non stéroïdiens 105
1.1. Salicylés 108
1.2. Dérivés de la pyrazolone ou pyrazoles 109
1.3. Fénamates 111
1.4. Dérivés des acides aryl- alcanoïques 113
1.5. Paracétamol 115
2. Anti-inflammatoires stéroïdiens 117
V. MEDICAMENTS DE LA REPODUCTION 121
1. Progestagènes 122
2. Hormones gonadotropes et facteurs de contrôle 124
3. Prostaglandines et analogues 128
4. Utérotoniques 130
4.1. Ocytocine 130
4.2. Ergométrine et sérotonine 132
5. Mélatonine 133
VI. MEDICAMENTS DES FONCTIONS DIGESTIVES 135
1. Antispasmodiques 135
1.1 Métamizole 135
1.2 Prifinium 136
2. Excitants de la motricité des réservoirs gastriques 137
2.1 Strychnine 137
VII. MEDICAMENTS AGISSANT SUR LE METABOLISME 139
1. Vitamines 139 1.1. Vitamine A 139 1.2. Vitamine B 139 1.3. Vitamine C 140 1.4. Vitamine E 140 1.5. Vitamine K 140
1.6. Association vitamine A + vitamine D3 + vitamine E 141
2. Minéraux et acides aminés 144
3. Produits de diététique et additifs alimentaires 146
VIII. MEDICAMENTS DU SYSTEME NERVEUX CENTRAL 149
ET PERIPHERIQUE
1. Phénothiazines 151
1.1. Acépromazine 151
2. Anesthésiques dissociatifs 152
2.1. Kétamine 152
3. Les agonistes alpha-2-adrénergiques 155
3.1. Détomidine et médétomidine 155
4. Agents utilisés pour l’euthanasie 157
iii
X. MEDICAMENTS DIURETIQUES 161
XI. MEDICAMENTS TOPIQUES 165
1. Médicaments de la mamelle 165
1.1. Antibiotiques à usage intra-mammaire 165
1.2. Crèmes mammaires 170
2. Médicaments à usage gynécologique 171
3. Antiseptiques 172
4. Cicatrisants 174
XII. MEDICAMENTS AGISSANT SUR L’IMMUNITE 175
A. VACCIN ANTI-RABIQUE 175
B. VACCINS POUR ANIMAUX DE LOISIR ET DE RENTE 176
1. Vaccins du cheval 176
1.1. Vaccin de la rhinopneumonie équine 176
1.2. Vaccin de la grippe équine 177
2. Vaccins des ruminants 179
2.1. Vaccination des bovins 179
2.1.1. Vaccin contre les mammites 179
2.1.2. Vaccin de la diarrhée néo-natale 180
2.1.3. Vaccin contre les maladies respiratoires IBR, PI3, BVD
et les virus BRS 181
2.1.4. Vaccin contre la brucellose 182
2.2. Vaccination des ovins 183 2.2.1. Vaccin contre la fièvre catarrhale ovine ou Bluetongue 183
2.2.2. Vaccin contre la clavelée 183
2.2.3. Vaccin contre l’entérotoxémie 184
2.3. Vaccination des ovins et caprins 185
2.3.1. Vaccin contre la brucellose 185
2.3.2. Vaccin contre les avortements 185
2.4. Vaccination des bovins, ovins et caprins 186
1.4.1. Vaccin de la fièvre aphteuse 186
1.4.2. Vaccin contre l’entérotoxémie 187
1.4.3. Vaccin contre les maladies respiratoires 187
3. Vaccins des lapins 188
3.1. Vaccin de la maladie hémorragique du lapin 188
3.2. Vaccin des toxi-infections à clostridies 189
4. Vaccins volaille 189
4.1. Maladie de Marek 189
4.2. Maladie de Newcastle 191
4.3. La bronchite infectieuse 193
4.4. La maladie de Gumboro 194
4.5. Le syndrome de chute de ponte 196
4.6. La rhinotrachéite 197
4.7. L’encéphalomyélite 198
4.8. La coccidiose 199
4.9. L’entérite hémorragique de la dinde 200
4.10. La variole 201 4.11. L’influenza aviaire 202 4.12. Infection à Reovirus 203 4.13. Infections à Coronavirus 203 4.14. Vaccins en association 204 5. Vaccins du dromadaire 205 5.1. Variole 205
C. VACCINS POUR ANIMAUX DOMESTIQUES 206
1. Vaccins du chien 206
1.1. Vaccin vivant de la parvovirose 206
iv
2.1. Vaccin polyvalent RCP FeLV 209
XIII. PRODUITS DE DIAGNOSTIC 210
1. Tuberculines 210
2. Produits de diagnostic des mammites 210
3. Recherche d’anti-infectieux dans les DAOA 211
ANNEXE I 213
ANNEXE II 217
ANNEXE III 223
3
Introduction
L’objectif du Codex des Médicaments Vétérinaires de Tunisie est d’inventorier l’arsenal thérapeutique actuellement à la disposition des médecins vétérinaires afin de fournir un outil comparatif entre les spécialités et promouvoir l’usage rationnel des médicaments, en procurant aux praticiens vétérinaires des informations complétant les monographies des médicaments disposant d’une autorisation de mise sur le marché (AMM) en Tunisie. Le Codex des Médicaments Vétérinaires de Tunisie comporte également des produits de diététique et d’hygiène et de diagnostic.
Les informations fournies sont basées sur les preuves scientifiques justifiant la qualité, l’efficacité et l’innocuité des médicaments pour les animaux, le consommateur de produits alimentaires d’origine animale et l’environnement. Les données présentées dans le Codex des médicaments vétérinaires de Tunisie concernent non seulement les propriétés pharmacologiques et thérapeutiques mais également l’aspect économique. Les prix publics en Dinar Tunisien toutes taxes comprises (DT TTC) de chaque spécialité pharmaceutique sont indiqués (donnée essentielle pour le vétérinaire et pour l’éleveur).
Pour faciliter l’accès à des informations complètes et promouvoir une approche comparative, les spécialités pharmaceutiques sont regroupées en différents chapitres sur la base de leurs classes thérapeutiques, pharmacologiques, anatomiques et chimiques. Un commentaire précède chaque chapitre afin de donner aux vétérinaires un aperçu des avantages et des inconvénients de chacun des groupes. Une attention toute particulière sera prêtée aux classes pharmacologiques dominantes, à savoir aux médicaments anti-infectieux, antiparasitaires, anti-inflammatoires et vaccins.
Dans certains cas particuliers et uniquement pour les animaux de compagnie, des médicaments à usage humain sont présentés à titre indicatif, lorsque le principe actif en question ne dispose pas d’une AMM vétérinaire en Tunisie, en attendant l’évolution de la législation Tunisienne et la promulgation de l’équivalent de la loi de la « Cascade » en vigueur en Europe.
Le Codex des Médicaments Vétérinaires de Tunisie comprend à l’heure actuelle environ 500 « produits vétérinaires », dont 370 médicaments chimiques (159 antibiotiques et 86 antiparasitaires), 37 additifs alimentaires ainsi que 93 médicaments immunologiques (vaccins…etc.) dont 62 destinés à la volaille, 21 destinés aux ruminants et le reste répartis sur différentes espèces.
Les antibiotiques et les antiparasitaires occupent la majeure partie de l’arsenal thérapeutique vétérinaire tunisien (respectivement 32% et 17%) suivis des additifs alimentaires (7.5%). Les médicaments immunologiques (vaccins…etc.) représentent (18.5%).
Les autres classes thérapeutiques (anti-inflammatoires, diurétiques, anesthésique…etc.) sont peu représentés.
Ce qui peut parfois obliger le praticien vétérinaire au recours à des médicaments humains (hors AMM), particulièrement en ce qui concerne la thérapeutique de
4
l’appareil respiratoire, appareil uro-génital, la gestion de la douleur animale et l’ophtalmologie.
Les spécialités disposant d'une AMM pour les carnivores domestiques sont peu nombreuses en Tunisie. Vu leur indisponibilité, les médecins vétérinaires ont recours à l’utilisation des médicaments humains.
Certaines spécialités disposant d’une AMM ne sont hélas pas disponibles sur le marché pour différentes raisons. Le marché des médicaments vétérinaires pour les carnivores domestiques étant exigu, beaucoup de laboratoires ne se lancent pas dans des demandes d'AMM pour des spécialités pourtant commercialisées en Europe. A ce titre, aucune spécialité à base d'antibiotiques destinée aux traitements des infections en ophtalmologie n'est disponible en Tunisie, le vétérinaire n'a alors d'autre choix que de prescrire des médicaments humains ! Il est important de rappeler que pour la prescription d’un médicament, le vétérinaire est amené à rédiger une ordonnance. La prescription de l’ordonnance est un acte à ne pas négliger et qui revêt une importance particulière dans la mesure où le vétérinaire prescripteur est le seul responsable de son contenu. L’ordonnance doit donc obéir à certaines normes essentielles :
L’ordonnance doit porter de façon évidente l’identité du prescripteur (Dr.vétérinaire) et les mentions suffisantes pour pouvoir le joindre (Adresse et numéro de téléphone). La mention de son numéro d’inscription au conseil national de l’ordre des Médecins Vétérinaires est facultative.
L’ordonnance doit impérativement être datée.
L’espèce et l’animal bénéficiaires du traitement doivent figurer, et cela, si c’est possible, par les moyens d’identification (tatouage dermique ou puce électronique). Les mentions de la race, de l’âge et du poids peuvent se révéler nécessaires à l’exécutant de la prescription s’il est différent du prescripteur pour lui permettre de délivrer les médicaments en toute responsabilité.
Chaque prescription de l’ordonnance doit clairement laisser apparaître dans sa présentation l’inscription d’une part (qui désigne le ou les médicaments à mettre à la disposition de la personne chargée d’appliquer le traitement), et l’instruction d’autre part (mode d’utilisation des médicaments).
L’ordonnance manuscrite doit être écrite avec un procédé d’écriture indélébile etinfalsifiable, rédigée de façon concise et simple, et bien entendu, lisible. Elle
doit être authentifiable par la signature de son rédacteur. Elle doit constituer pour l’exécutant (pharmacien ou vétérinaire) et le propriétaire un message qui doit être
parfaitement compris.
La rédaction d’une ordonnance comporte 3 parties :
- L’inscription : dans cette partie, le prescripteur doit décrire avec précision le ou les médicaments prescris nécessaires au traitement. Doivent être indiquées leurs
dénominations, la forme pharmaceutique et éventuellement la concentration
retenue si plusieurs possibilités sont offertes, ainsi que la quantité (nombre
d’unités) à délivrer. Cependant, les modalités d’inscription ne sont pas les mêmes
selon que le vétérinaire prescrit une spécialité pharmaceutique, une préparation officinale ou une préparation magistrale.
- La souscription : il s’agit d’indications particulières du prescripteur destinées au préparateur (en général le pharmacien) concernant la réalisation d’un médicament extemporané. Cependant, tant l’intervention d’un pharmacien que la préparation
5
magistrale de médicaments étant peu courantes, cette partie est souvent absente des prescriptions.
- L’instruction : il s’agit du mode d’emploi du ou des médicaments prescrits, destiné au propriétaire de l’animal. Doivent figurer toutes les recommandations concernant l’administration du médicament : la dose prescrite en volume ou en unité et par kg
de poids vif de l’animal, modalités et la fréquence d’administration, la durée du
traitement et l’éventuel temps d’attente* pour les animaux producteurs de denrées alimentaires destinés à la consommation humaine.
*NB : Le temps d’attente est le temps à respecter entre la dernière administration du médicament à usage vétérinaire et la collecte des denrées alimentaires (abattage, traite...). Ce temps précise la durée
pendant laquelle les denrées alimentaires issues d’un animal traité ne peuvent être commercialisées en vue de la consommation humaine. Ainsi un temps d’attente égale à 0, veut dire que la denrée alimentaire d’origine animale peut être mise à la consommation humaine 0 jours après la fin du traitement et non pas pendant le traitement.
Pour chaque médicament destiné aux animaux producteurs de denrées alimentaires, un temps d’attente, pour la viande, le lait, les œufs et le miel, est inscrit dans sa monographie. Le respect de ce temps d’attente est d’une importance majeure, étant donnée le risque lié à la présence de résidus de médicaments sur la santé de l’homme.
Le devoir du vétérinaire est aussi de protéger la santé humaine ! Ceci passe avant tout par le respect des bonnes pratiques vétérinaires, le respect des temps d’attentes et la valorisation de l’importance de la communication entre vétérinaire et propriétaires des animaux producteurs de denrées alimentaires.
COMMENTAIRE PHARMACO-THERAPEUTIQUE
Les données pharmaco-thérapeutiques présentées dans ce Codex le sont de manière standardisée. Les rubriques prennent en compte, autant que possible, les « Résumés des Caractéristiques des Produits » ou RCP des médicaments vétérinaires actuellement commercialisés en Tunisie. Seules les données essentielles sont présentées, il est en effet impossible d’intégrer toutes les données sur chaque médicament.
Deux médicaments appartenant à un même groupe pharmaco-thérapeutique peuvent avoir des indications différentes selon le positionnement sur le marché choisi par le laboratoire producteur. La consultation de la monographie reste donc essentielle. Il se peut aussi que des données de la littérature, non mentionnées dans les monographies, soient intégrées dans les commentaires. L’usager du Codex tiendra compte aussi du fait que l’information de certaines rubriques ne peut pas être exhaustive. Seules les données essentielles sont ainsi reprises dans les rubriques Interactions et Effets indésirables.
Les rubriques traitées pour chaque classe thérapeutique sont les suivantes :
- Indications : Il s’agit des indications thérapeutiques de chaque principe actif. - Pharmacodynamie: description de l’action et des effets de la substance active. - Pharmacocinétique : résumé du devenir d’un principe actif et de ses
métabolites le cas échéant, dans l’organisme de l’animal cible.
- Contre-indications :cellesgénéralement énumérées dans les monographies. - Effets indésirables :principaux effets indésirables.
6
- Interactions :principales interactions entre les médicaments, ou entre ceux-ci et d’autres substances d’origine alimentaire par exemple, et parfois les influences de la substance active sur les résultats des tests de biologie et de biochimie clinique.
- Précautions particulières/Risques pour l’homme :mesures particulières à prendre en compte ou remarques utiles. Dans certains cas, les risques pour l’homme liés à la manipulation, à l’ingestion accidentelle ou à l’injection du médicament ou au contact avec l’animal traité sont signalés.
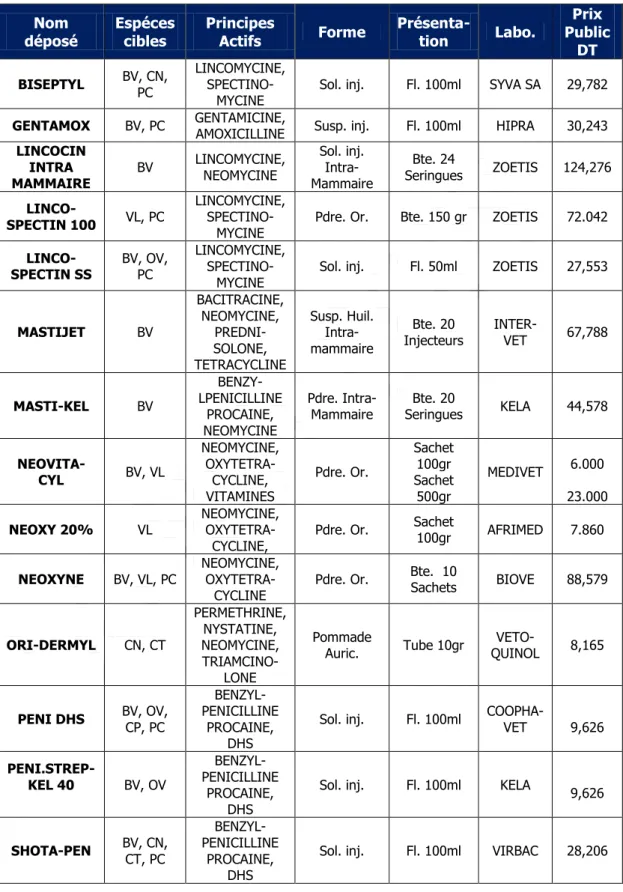
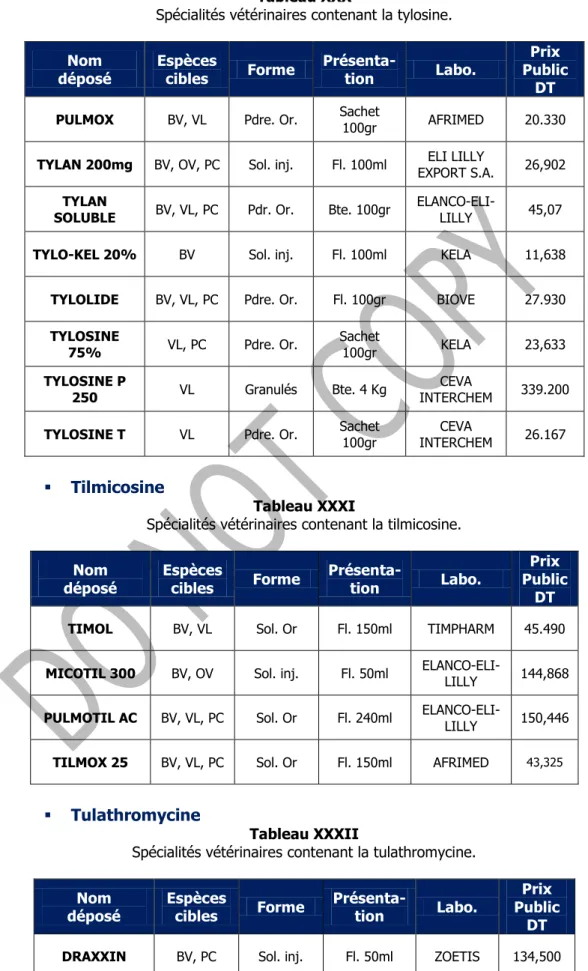
Après chaque commentaire pharmaco-thérapeutique, les spécialités disponibles sur le marché tunisien sont indiquées par classe pharmaco-thérapeutique et par principe actif dans des tableaux présentés selon ce qui suit :
Spécialités vétérinaires contenant 1 seul principe actif.
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public
DT xxxx xxxx xxxx xxxx xxxx xxxx
Spécialités contenant des principes actifs en association.
Nom
déposé Espèces cibles Principe Actif Forme Présenta-tion Labo.
Prix Public
DT xxxx xxxx xxxx xxxx xxxx xxxx xxxx
Spécialités contenant des vaccins.
Nom déposé Forme Présenta- tion Labo. Public Prix
DT
xxxx xxxx xxxx xxxx xxxx
Les espèces cibles sont désignées par des abréviations comme suit :
BV : Bovins - OV : Ovins - CP : Caprins - CV : Cheval - DR : Dromadaire - VL : Volaille - CT : Chat - CN : Chien - FU : Furet - PS : Poisson - ABL : Abeille - PC : Porc - CB : Cobaye - AS : Animaux Sauvages.
Afin de faciliter les différentes recherches dans le Codex des Médicaments Vétérinaires de Tunisie celui-ci comporte en annexes : un index des principes actifs majeurs, un index des médicaments par classe thérapeutique et un index des médicaments par nom de spécialité.
7
I. MEDICAMENTS ANTI-INFECTIEUX
Généralités
Le traitement des infections bactériennes fait appel à une grande diversité de médicaments très actifs qui constituent la chimiothérapie anti-infectieuse. Les anti-infectieux sont classiquement regroupés en fonction de leur origine en deux catégories : des composés d'origine naturelle, produits par des microorganismes, les antibiotiques, et des composés artificiels, les antibactériens artificiels, encore appelés antibiomimétiques. Ils occupent une place importante dans l’arsenal thérapeutique aussi bien en Tunisie qu’à l’échelle mondiale. À cause de leur large disponibilité, leur coût généralement faible et de leur relative innocuité, les anti-infectieux sont parmi les médicaments les plus mal utilisés [41].
Ces médicaments ont révolutionné le pronostic d'un certain nombre de maladies autrefois incurables (tuberculose, brucellose…etc.) et ont largement contribué à l'essor de l'élevage. Ils constituent la première classe de médicaments utilisés en médecine vétérinaire avec une part de marché mondial de 30 % environ. L’analyse des données sur les classes thérapeutiques utilisées, permet de constater que le marché tunisien est dominé par les anti-infectieux qui représentent en chiffre d’affaires 35 % des ventes. Leur importance tient également au risque présenté par les antibiorésistances bactériennes suite à leur large utilisation. Les bactéries d'une manière générale, après un contact prolongé avec la plupart des antibiotiques, deviennent en effet moins sensibles, voire résistantes à ces antibiotiques. Ce problème devient très préoccupant car tous les antibiotiques, quels qu'ils soient, ont tendance, au fil des années, à perdre une partie, voire la totalité de leur efficacité vis-à-vis de certaines bactéries, ils subissent ainsi à la suite de leur usage massif, une véritable "usure" avec le temps [265].
Les vétérinaires et les médecins partagent un arsenal thérapeutique anti-infectieux limité à une dizaine de familles d’antibiotiques, dont l’extension vers de nouvelles familles sera vraisemblablement limitée dans les prochaines années. Chaque utilisation d’antibiotique contribue en effet à réduire la susceptibilité des bactéries pathogènes et commensales [282].
Plusieurs instances au niveau international (Organisation mondiale de la santé OMS, organisation mondiale de la santé animale OIE...) ont engagé des réflexions sur la détermination d’antibiotiques dits "critiques", prenant en compte des considérations épidémiologiques spécifiques et la perception de l’importance du renforcement d’un encadrement au regard de l’usage. Ces antibiotiques "critiques" sont considérés revêtant une importance particulière à la fois pour la
« Les antibiotiques sont en fait le seul groupe de médicaments qui lorsqu’administrés
à quelques individus, peuvent avoir un impact sur des populations entières »
Karl Weiss 2011 Microbiologiste et infectiologue
8
santé humaine et la santé animale. À cet effet, un groupe d’experts scientifiques de l’OIE a élaboré des listes dans lesquelles des critères ont été sélectionnés pour déterminer le degré d’importance des classes d’agents antimicrobiens en médecine vétérinaire. Selon ces critères, les fluoroquinolones et les céphalosporines doivent être considérés comme des antibiotiques de deuxième intention, jamais de première intention, à utiliser dans un but thérapeutique, jamais prophylactique. C’est en fonction de l’attitude responsable des praticiens que l’usage des ces composés continuera à être autorisé à la profession vétérinaire [242].
A l’heure actuelle, sur le plan mondial, les craintes proviennent surtout de germes multi-résistants comme les Staphylococcus Aureus Résistant à la Méthicilline ou SARM chez les poulets à l’engrais, les porcs et les bovins, et les entérobactéries productrices de β lactamase à spectre étendu (ci-après : BLSE ou ESBL en anglais), dont la présence s’accroît également chez l’homme, et qui ne peuvent être combattus que par de rares antibiotiques de réserve.
L’antibiorésistance constitue alors un des défis médicaux majeurs du XXIème
siècle. Il existe en effet des bactéries naturellement résistantes aux antibiotiques aux doses thérapeutiques administrées. En revanche, la résistance peut être acquise par des bactéries préalablement sensibles. Ce phénomène de résistance acquise repose sur divers mécanismes de sélection de souches de bactéries résistantes, capables d'être transmise à l'homme.
L’association amoxicilline-acide clavulanique, les céphalosporines (en particulier : les spécialités administrées par voie orale) et les fluoroquinolones sont particulièrement générateurs de résistances bactériennes.
L’utilisation raisonnée des antibiotiques est un objectif essentiel en termes de santé humaine et de santé animale et ce afin de lutter contre le développement de résistances bactériennes et éviter ainsi « l’usure prématurée » des antibiotiques. Elle repose sur un ensemble de recommandations et de mesures pratiques (diagnostic bactériologique, antibiogramme) destinées à choisir le médicament antibiotique le plus adapté et à empêcher et/ou à réduire la sélection de micro-organismes résistants aux antimicrobiens chez les animaux. L’antibiothérapie raisonnée permet de réserver l’efficacité des médicaments antibiotiques et garantir leur utilisation rationnelle chez les animaux afin de renforcer leur efficacité et leur innocuité, respecter l’obligation éthique et la nécessité économique de maintenir les animaux en bonne santé, prévenir ou limiter, dans la mesure du possible, le transfert des micro-organismes (ainsi que leurs déterminants de résistance) au sein des populations animales, empêcher ou restreindre le transfert des micro-organismes résistants ou des déterminants de résistance des animaux vers l’homme, préserver l’efficacité des médicaments antibiotiques employés en médecine humaine et prolonger dans le temps l’efficacité de chaque substance antimicrobienne.
9
Principes de l’approche globale de l’utilisation raisonnée des
antibiotiques
L’approche globale de l’utilisation raisonnée des antibiotiques repose sur cinq éléments :
i. La prévention des maladies infectieuses, ii. Le diagnostic précis et l’antibiogramme, iii. La justification de l’antibiothérapie, iv. Le choix correct de l’antibiotique,
v. L’utilisation appropriée.
La prévention des maladies infectieuses reste le moyen le plus efficace tant pour la réduction de l’utilisation des antibiotiques que pour le bien être animal. Une prophylaxie hygiénique et médicale est la clé de cette approche via le respect des règles d’hygiène dans tous ses aspects et l’implantation d’un programme complet de vaccination en fonction des circonstances épidémiologiques. Le respect des techniques de l’asepsie et le respect des règles d’hygiène permet de réduire l’utilisation des antibiotiques.
Pour établir son diagnostic, le vétérinaire s’appuie sur les signes cliniques ou nécropsiques, les résultats des examens complémentaires mis en œuvre, complétés nécessairement par les données épidémiologiques qu’il détient du fait de sa connaissance approfondie de l’animal et de son environnement. L’utilisation empirique des antibiotiques peut être remplacée par le recours au diagnostic bactériologique (identification du pathogène) et par la réalisation de test de sensibilité de ce dernier aux divers antibiotiques, ceci permettra d’optimiser l’antibiothérapie et de diminuer son utilisation dans les cas de pathologies virales. L’antibiogramme permet de mettre en évidence d’éventuels phénomènes de résistance acquise. Il apporte de précieuses informations aux réseaux d’épidémiosurveillance de la résistance. Il aide le prescripteur dans ses choix, mais ne détermine pas seul le choix de l’antibiotique à utiliser. La réalisation de l’antibiogramme permet de réduire les problèmes liés à l’antibiothérapie probabiliste.
La collection sur l’échelle nationale de données actualisées sur les différentes résistances bactériennes apparues, réalisées dans des laboratoires d’analyses accrédités reste le meilleur moyen pour guider les professionnels de santé dans leurs choix.
Avant d’entamer une antibiothérapie et même dans le cas où le diagnostic est correct, le praticien se doit de justifier cette utilisation en s’assurant qu’il n’ya pas d’autres alternatives, par exemple dans le cas où l’animal présente une infection grave et que l’abattage est la meilleure solution. Ceci dans le secteur aviaire et aquacole est impraticable, l’antibiothérapie doit être alors basée sur des résultats d’analyse de laboratoire.
D’un point de vue clinique, le choix du principe actif repose sur 4 éléments : l’efficacité clinique, les effets secondaires, le risque sur le développement des résistances bactériennes et les effets indésirables sur la flore commensale de l’animal.
Une attention particulière doit être attribuée au statut immunitaire de l’animal et du type d’antibiotique utilisé, en effet, un antibiotique bactériostatique dépend de l’immunité active de l’animal. Il est donc inutile de les utiliser sur dans animaux immunodéprimés, âgés ou en période de gestation. Le spectre d’activité de
10
l’antibiotique est une importante composante à maitriser. Le respect de la posologie du médicament permet de diminuer le développement de résistances. Le respect de la posologie, l’intervalle entre deux administrations et la durée du traitement sont essentiels pour assurer l’usage rationnel de l’antibiotique et ainsi minimiser les échecs thérapeutiques, exploiter le potentiel maximal du médicament et respecter les temps d’attente. Une dose inférieure à celle recommandée, augmente l’intervalle entre deux doses, réduit la durée du traitement, peut conduire à une recrudescence de l’infection et ainsi augmenter le risque de sélections de germes résistants [151].
Les règles de l’utilisation raisonnée pour le vétérinaire sont :
Frapper vite : car plus la taille du foyer infectieux est faible, plus
l'antibiotique pourra les détruire rapidement et facilement et plus le risque d'apparition d'antibiorésistances est réduit,
Frapper fort : pour réduire les risques de sélection des germes les
moins sensibles et donc de développement d'antibiorésistances. On administre parfois pour cette raison en début de traitement, pendant les 12 ou 24 premières heures, une "dose d'attaque", c'est-à-dire une dose double de la dose fixée ultérieurement, la "dose d'entretien". Attention aux doses insuffisantes. Les valeurs données par les laboratoires pharmaceutiques ne sont que des doses indicatrices. Elles doivent être adaptées selon la sensibilité présumée du germe, selon la localisation de l'infection, selon l'état des défenses immunitaires des animaux, enfin selon la toxicité éventuelle de l'antibiotique. Il sera ainsi parfois
nécessaire de doubler ou tripler les doses habituelles pour le traitement de certaines infections. On recommande traditionnellement d'administrer des doses et d'appliquer un rythme d'administration qui assurent en permanence des concentrations sériques au minimum égales aux concentrations minimales inhibitrices CMI (du moins pour les
antibiotiques bactériostatiques) et si possible 4 fois supérieures pendant la plus grande partie du traitement.
Frapper assez longtemps : pour empêcher le réveil d'une infection
incomplètement éliminée. Bien que cette notion doive être revue en fonction des propriétés pharmacodynamiques concentration-dépendantes ou non de l’antibiotique, il convient de respecter les posologies
recommandées par les laboratoires pharmaceutiques.Le traitement d'une infection générale facilement accessible par l'antibiotique sera d'une durée minimale comprise entre 3 à 7 jours. Un traitement avec un antibiotique bactériostatique (5 à 7 jours) doit être en principe plus long qu'avec un antibiotique bactéricide (3 à 5 jours). Dans le cas d'infections localisées difficiles à atteindre (infection cutanée ou osseuse), les
traitements sont beaucoup plus longs encore, de 15 jours à 1 mois, voire davantage.
Frapper juste : car l’utilisation des antibiotiques critiques doit reposer
sur des résultats de laboratoire démontrant non seulement leur efficacité sur le pathogène isolé responsable des problèmes cliniques, mais aussi les résistances de ce pathogène aux autres antibiotiques utilisables.
11
1. ANTIBIOTIQUES
1.1. β lactamines
Les β lactamines sont des antibiotiques antibactériens, qui possèdent un mode d'action commun (action bactéricide sur les bactéries en phase de multiplication), mais qui se distinguent par leur pharmacocinétique, leur spectre d’activité et la sensibilité aux mécanismes de résistance.
Ils sont composés d’un noyau β lactame, ont un caractère nettement acide (pKa
≈ 3 - 5) et leur toxicité est très faible.
Au fur et à mesure que la résistance s’est étendue, de nouveaux composés ont apparus avec une stabilité accrue aux β lactamases, et des agents protecteurs pour inhiber ces β lactamases [102] [275]. Ce sont les inhibiteurs des β lactamases.
En médecine vétérinaire, des représentants de trois groupes sont utilisés : pénicillines, céphalosporines, et inhibiteurs des β lactamases.
1.1.1. Pénicillines
Les pénicillines sont des β lactamines à noyau péname, de caractère liposoluble. Ce sont des acides faibles, ce qui permet la préparation de sels alcalins (sodique) et organiques (sel de procaïne…), mais aussi d’esters (pénéthamate) utilisés en thérapeutique.
Indications - spectre d’activité - résistances
Les indications des pénicillines sont nombreuses dans le cadre du traitement des infections bactériennes à germes sensibles :
La pénicilline G est utilisée pour le traitement de certaines maladies spécifiques telles que la leptospirose (dues à des spirochètes) et le rouget du porc [286].
Les pénicillines M sont indiquées pour le traitement des infections
staphylococciques sécrétrices ou non de βlactamases, le traitement local des mammites streptococciques et staphylococciques des vaches laitières et le traitement général par voie orale des staphylococcies cutanées chez le chien.
Les pénicillines A sont indiquées pour le traitement des infections provoquées par des bactéries à Gram + ou Gram -, le traitement général des septicémies, des infections digestives (colibacillose, salmonellose), respiratoires et urinaires, le traitement local des mammites à Gram + et Gram - et le traitement général des staphylococcies cutanées (mais seulement en association avec l’acide
clavulanique).
La dose normale d'utilisation de la pénicilline G est de 15 000 à 50 000 UI.kg-1.
La dose habituelle d'utilisation des autres pénicillines est de 10 à 20 mg.kg-1.
Les pénicillines se caractérisent en général par un spectre d’activité (tableau V) étroit sauf pour les aminopénicillines qui possèdent un spectre élargi. Les benzylpénicillines sont, actives contre beaucoup de bactéries à Gram + aérobies et anaérobies, y compris tous les streptocoques β hémolytiques et le genre
Clostridium, ainsi que contre certaines bactéries à Gram - (Haemophilus, Pasteurella, Actinobacillus, Mannheimia, Fusobacterium…etc.). Elles sont cependant sensibles aux β lactamases produites par certains staphylocoques.
12
Tableau V
Spectre d’activité des principaux groupes de pénicillines en médecine vétérinaire
Pénicillines
du groupe G Aminopénicillines Pénicillines M
Bacilles et coques à Gram +
Bactéries à Gram + : aérobies et anaérobies sauf staphylocoques producteur de pénicillinases Bactéries à Gram - : Pasteurella Bactéries anaérobies strictes : Clostridium, Fusobacterium Spirochètes : Leptospira
Spectre est élargi :
Bactéries à Gram + : aérobie et anaérobie (sauf staphylocoques producteurs de β- lactamases) : Staphylococcus, Streptococcus, Corynebacterium, Listeria. Bactérie à Gram - : E. coli, Pasteurella, Salmonella, Proteus.
Cette classe est active sur les germes couverts par les pénicillines naturelles et les bactéries sécrétrices de β-lactamases comme Staphylococcus aureus.
Les résistances bactériennes aux pénicillines sont essentiellement causées par la production de β-lactamases de bactéries à Gram + ou à Gram - .
Les pénicillines G sont détruites par ces enzymes alors que les pénicillines de semi-synthèse comme les pénicillines M sont résistantes aux β lactamases des germes à Gram + et celles du groupe A sont résistantes aux β lactamases des germes à Gram - .
Afin de potentialiser l'action des pénicillines en bloquant l'action de ces enzymes de résistance, l’acide clavulanique, produit naturellement par Streptomyces clavuligerus (inhibiteur « suicide » d'un certain nombre de β lactamases) est parfois administré en association avec notamment l’amoxicilline.
Pharmacocinétique
La pharmacocinétique est très spécifique à chacune de ces substances. Elle varie d’une espèce à l’autre et est fortement influencée par l’habillage chimique du composé et la forme galénique des médicaments. En intramusculaire, les sels de sodium en solution aqueuse sont très rapidement résorbés et éliminés, ce qui oblige à des ré-administrations toutes les 4 heures pour maintenir des taux thérapeutiques efficaces. En revanche, les sels organiques confèrent des taux plasmatiques plus faibles mais prolongés, le sel de procaïne en suspension aqueuse permet ainsi d’espacer les administrations toutes les 8 ou 12 heures [262].Le taux de liaison aux protéines plasmatiques est de 52% pour la benzylpénicilline [21].
La résorption digestive est nulle pour la pénicilline G, détruite par l’acidité gastrique mais elle est variable pour les autres pénicillines. Elle est médiocre et varie de 20 à 50% pour l’ampicilline et excellente pour l’amoxicilline (supérieure à 90%). La distribution des β lactamines est essentiellement extracellulaire et étendue à l’ensemble des tissus. Les pénicillines subissent peu de biotransformations et ne passent dans le liquide céphalorachidien que lors de méningites (excepté pour l’ampicilline).
13
L’élimination est surtout rénale, avec une sécrétion tubulaire active expliquant les concentrations élevées observées dans l’urine, d’où l’intérêt des pénicillines pour le traitement des infections urinaires à germes sensibles. Pour l’ampicilline, l’élimination est biliaire avec un cycle entéro-hépatique de nature à augmenter la toxicité digestive chez certaines espèces (lagomorphes, rongeurs et cheval) [111].
Pharmacodynamie
Les pénicillines sont des antibiotiques bactéricides, temps dépendants. Leur mécanisme d’action repose sur une analogie structurale avec la D-alanine-D-alanine (D-Ala-D-Ala) et la fixation sur le site actif à activité transpeptidasique, d’où inhibition de la synthèse du peptidoglycane et arrêt de la croissance bactérienne. Cette action s’exerce uniquement sur les bactéries en phase de multiplication, chez lesquelles la synthèse du peptidoglycane est la plus intense, ceci oppose les pénicillines à la plupart des autres antibiotiques bactéricides.
Effets indésirables et toxiques
Les effets indésirables sur l’animal traité sont limités à une hypersensibilité, en relation avec la formation de protéines pénicilloylées responsables d’accidents allergiques chez des sujets déjà sensibilisés. Ces accidents se limitent en général à des troubles bénins chez l’animal se traduisant par de l’urticaire et du prurit. La procaïne, rentrant dans la composition de certains esters lors de la préparation de la pénicilline G (pénicilline-procaïne), peut induire des symptômes nerveux centraux chez le cheval, qui est particulièrement sensible à cette substance [155]. Les pénicillines sont faiblement éliminées par le lait, ce qui peut engendrer de la diarrhée, de la candidose ou des réactions allergiques chez les jeunes animaux allaités.
Les résidus de pénicillines dans les denrées alimentaires jouent un rôle déclenchant d’accidents allergiques chez le consommateur. La dose qui déclenche cette toxicité est de 15 UI de pénicilline G.
Afin de protéger la santé du consommateur, des limites maximales de résidus (LMRs en ppb ou μg/Kg ont été fixées dans les diverses denrées alimentaires d’origine animale sauf pour les œufs). Elles figurent dans la note de service 742/200 du 28 mars 2006 de la DGSV et avenant du 9 mars 2010.
Les résidus de pénicillines sont également redoutés dans l’industrie laitière de transformation (yaourt et fromages) en raison de leur effet inhibiteur des lactobacilles et des pertes économiques considérables engendrées.
Contre-indications
L’hypersensibilité aux pénicillines est une contre-indication majeure.
Les pénicillines sont à proscrire chez le lapin, le chinchilla, le cobaye et le hamster, car elles peuvent provoquer une dérive de la flore caecale voir des entérocolites dysentériformes mortelles.
Chez les équidés, des précautions d’emploi doivent être mises en place lors de l’emploi de l’ampicilline à cause des risques de désordres digestifs assez graves qui peuvent survenir chez cette espèce.
14
Interactions
L’association pénicillines-acide clavulanique permet de combattre les résistances bactériennes. L’association avec d’autres antibiotiques bactéricides, comme les aminoglycosides, est possible et permet une action synergique.
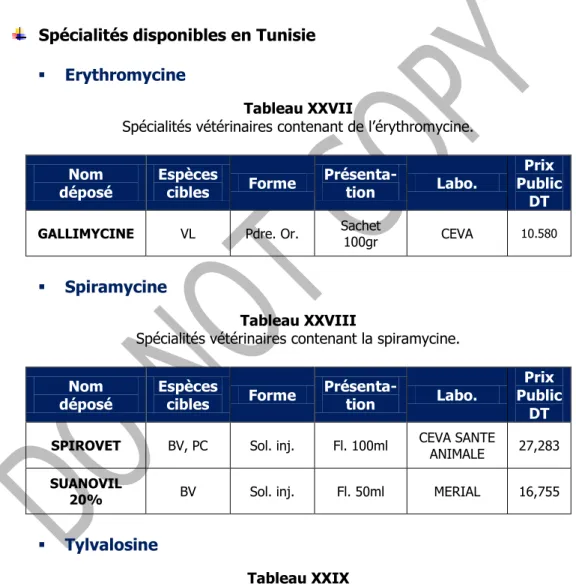
Spécialités disponibles en Tunisie
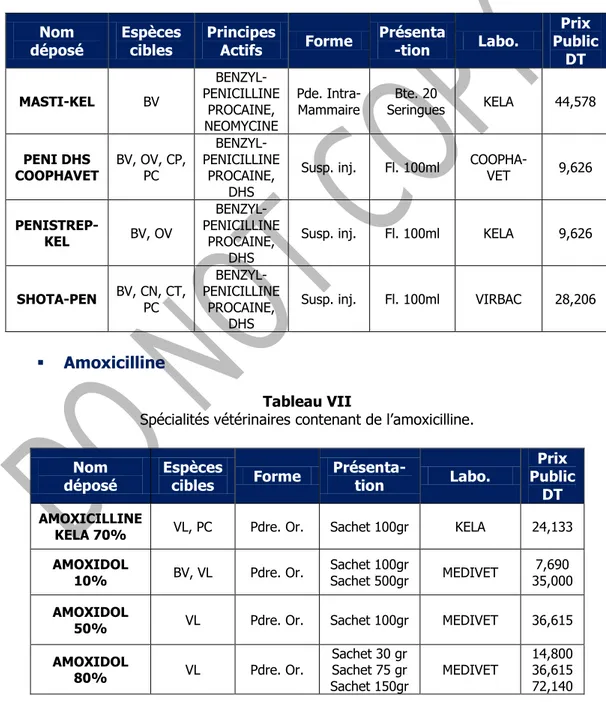
Pénicilline G en association Tableau VI
Spécialités vétérinaires contenant de la pénicilline G en association.
Nom déposé Espèces cibles Principes Actifs Forme Présenta -tion Labo. Prix Public DT MASTI-KEL BV BENZYL-PENICILLINE PROCAINE, NEOMYCINE Pde.
Intra-Mammaire Seringues Bte. 20 KELA 44,578
PENI DHS COOPHAVET BV, OV, CP, PC BENZYL-PENICILLINE PROCAINE, DHS
Susp. inj. Fl. 100ml COOPHA-VET 9,626
PENISTREP-KEL BV, OV BENZYL-PENICILLINE PROCAINE, DHS
Susp. inj. Fl. 100ml KELA 9,626
SHOTA-PEN BV, CN, CT, PC
BENZYL-PENICILLINE
PROCAINE, DHS
Susp. inj. Fl. 100ml VIRBAC 28,206
Amoxicilline
Tableau VII
Spécialités vétérinaires contenant de l’amoxicilline.
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public
DT AMOXICILLINE
KELA 70% VL, PC Pdre. Or. Sachet 100gr KELA 24,133 AMOXIDOL
10% BV, VL Pdre. Or. Sachet 100gr Sachet 500gr MEDIVET 35,0007,690
AMOXIDOL
50% VL Pdre. Or. Sachet 100gr MEDIVET 36,615 AMOXIDOL 80% VL Pdre. Or. Sachet 30 gr Sachet 75 gr Sachet 150gr MEDIVET 14,800 36,615 72,140
15
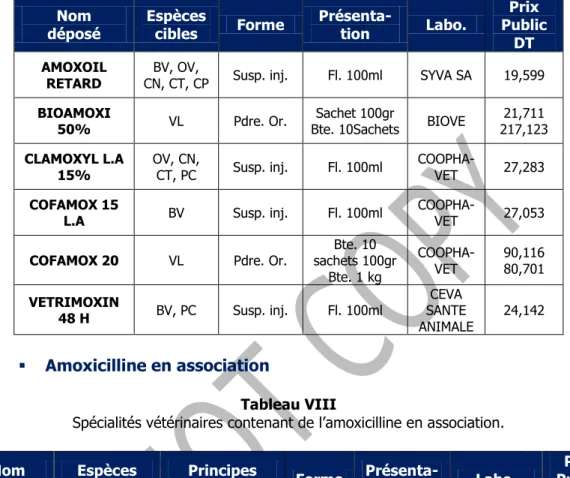
Tableau VII (suite)
Spécialités vétérinaires contenant de l’amoxicilline.
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public
DT AMOXOIL
RETARD CN, CT, CP BV, OV, Susp. inj. Fl. 100ml SYVA SA 19,599
BIOAMOXI
50% VL Pdre. Or. Bte. 10Sachets Sachet 100gr BIOVE 217,123 21,711
CLAMOXYL L.A
15% OV, CN, CT, PC Susp. inj. Fl. 100ml COOPHA-VET 27,283
COFAMOX 15
L.A BV Susp. inj. Fl. 100ml
COOPHA-VET 27,053
COFAMOX 20 VL Pdre. Or. sachets 100gr Bte. 10 Bte. 1 kg COOPHA-VET 90,116 80,701 VETRIMOXIN 48 H BV, PC Susp. inj. Fl. 100ml CEVA SANTE ANIMALE 24,142 Amoxicilline en association Tableau VIII
Spécialités vétérinaires contenant de l’amoxicilline en association.
Nom
déposé Espèces cibles Principes Actifs Forme Présenta-tion Labo.
Prix Public
DT
GENTA-MOX BV, PC AMOXICILLINE, GENTAMICINE Susp. inj. Fl. 100 ml HIPRA S.A 27.589
SYNULOX INTRAMA-MMAIRE BV AMOXICILLINE, ACIDE CLAVULANIQUE, PREDNISOLONE Susp.
Huil. Applicateurs Bte. 12 ZOETIS 55,722
SYNULOX
RTU BV, OV, PC
AMOXICILLINE, ACIDE
CLAVULANIQUE Susp. inj Fl. 100ml ZOETIS 39,083
Ampicilline
Tableau IX
Spécialités vétérinaires contenant de l’ampicilline.
Nom déposé Espèces cibles Forme Présenta-tion Laborato. Public Prix DT AMPISOL BV, OV, CP,
VL, PC Pdre. Or.
Sachet 100 gr
Bte. 10 Sachets COOPHAVET
7,181 69,94
16
Ampicilline en association
Tableau X
Spécialités vétérinaires contenant de l'ampicilline en association.
Nom
déposé Espèces cibles Principes Actifs Forme Présenta-tion Labo.
Prix Public DT AMPIDEXA-LONE BV, CV, PC AMPICILLINE, COLISTINE, DEXAMETHA-SONE
Sol. inj. Fl. 100ml
COOPHA-VET 15,564
COLAMPI I BV, OV, CP, PC AMPICILLINE, COLISTINE Sol. inj. Fl. 100ml BIOVE 17,563
DIAVET BV AMPICILLINE, COLISTINE Pdre. Or. Bte. 10 Sachet
70gr MEDIVET 19.600
MAMIFORT BV, OV, CP AMPICILLINE, CLOXACILLINE Susp. Intra-Mamm. Bte. 4 Seringues SYVA SA 8,719 MAMIFORT
SECADO BV CLOXACILLINE AMPICILLINE,
Susp. Intra-Mamm. Bte. 4 Seringues SYVA SA 11,401 Cloxacilline Tableau XI
Spécialités vétérinaires contenant de la cloxacilline.
Nom
déposé Espèces cibles Forme Présentation Labo.
Prix Public
DT DRYCLOXA
-KEL BV Mammaire Pde.Intra- Seringues Bte. 20 KELA 2.096
Cloxacilline en association
Tableau XII
Spécialités vétérinaires contenant de la cloxacilline en association.
Nom
déposé Espèces cibles Principes Actifs Forme Présenta-tion Labo. Public Prix MAMIFORT BV, OV, CP AMPICILLINE,
CLOXACILLINE Susp. Intra-Mamm. Bte. 4 Seringues SYVA SA 8,719 MAMIFORT
SECADO BV CLOXACILLINE AMPICILLINE, Susp. Intra-Mamm. Seringues Bte. 4 SYVA SA 11,401
MAMMI-TEL BV CLOXACILLINE, COLISTINE
Susp. Hui.Intra-Mammaire
Bte. 4
17
1.1.2. Céphalosporines
Les céphalosporines sont des β lactamines élaborées totalement ou partiellement par des micro-organismes du genre Cephalosporium [286].
Elles sont caractérisées sur le plan chimique par la présence d'un noyau β lactame condensé avec un cycle dihydrothiazine (noyau "céphème"). Ce sont des composés liposolubles qui présentent comme toutes les β lactamines un caractère nettement acide. Leur noyau est beaucoup plus stable que le noyau "péname" des pénicillines, ce qui leur permet de mieux résister globalement à l'action des diverses β lactamases bactériennes.
On distingue quatre générations de céphalosporines en fonction de leur chronologie d'apparition sur le marché à laquelle correspond une activité antibactérienne particulière [49].
Indications - spectre d’activité - résistances
Toutes les céphalosporines doivent désormais être considérées comme des antibiotiques de deuxième intention et ne doivent pas être habituellement employées. Elles devraient être réservées dans des cas particuliers, après échec d’antibiothérapie plus classique.
Les céphalosporines de 3ème et 4ème génération sont à réserver autant que
possible à la médecine humaine pour éviter le développement des résistances. Tableau XIII [216]
Principales céphalosporines utilisées en médecine humaine et vétérinaire*
Première
génération génération Deuxième génération Troisième génération Quatrième Céfalotine Céfaloridine Céfazoline Céfalexine Céfapirine Céfradine Céfadroxil Céfamandole Céfoxitine Céfuroxime Céfalonium Céfotaxime Céfopérazone Ceftiofur Aftriaxone Céftazidime Céfovécine Cefquinome
*Céphalosporines utilisées en médecine vétérinaire indiquées en caractères gras.
Les céphalosporines sont indiquées pour le traitement général des septicémies, infections respiratoires, urinaires, osseuses et cutanées. Elles sont aussi indiquées lors d’entérites bactériennes à germes sensibles aux céphalosporines ainsi que le traitement local des mammites à germes sensibles [78].
La céfalexine, le ceftiofur et la cefquinome sont indiqués pour le traitement d’infections générales, respiratoires, urinaires, osseuses et cutanées (staphylococcies cutanées). La molécule la plus employée en médecine canine est la céfalexine. Cette molécule avec la céfazoline, la céfopérazone, le céfalonium et le cefquinone sont aussi indiquées pour le traitement local des mammites à germes sensibles.
Les céphalosporines possèdent a priori un spectre large, mais qui varie selon la génération. En effet l’activité antibactérienne s’accroit de la 1ère à la 3ème
génération sur les bactéries à Gram - au détriment de l’activité sur les bactéries à Gram +. Ainsi la première génération possède un spectre proche de celui de la
18
benzylpénicilline. Elle est active sur les Staphylocoques, y compris ceux producteurs de β-lactamases, Streptocoques, Entérobactéries (colibacilles, salmonelles, klebsielles), Pasteurelles (Pasteurella multocida), Mannhemia haemolytica, Actinobacillus pleuropneumoniae et inactive sur Pseudomonas aeruginosa.
La deuxième génération, possède un spectre d’activité proche de celui des Aminopénicillines. Il est élargi à de nombreuses bactéries à Gram - (entérobactéries) y compris les souches sécrétrices de β-lactamases et elles sont aussi inactives sur Pseudomonas aeruginosa.
La troisième génération a une activité intrinsèque vis-à-vis des bacilles à Gram - considérablement accrue et une grande stabilité aux β-lactamases. L’activité sur
Pseudomonas aeruginosa est variable : la céfopérazone a une bonne activité sur cette bactérie. Elles sont inactives sur les Listeria et les entérocoques.
Les dérivés de quatrième génération possèdent une meilleure activité sur les bactéries à Gram + que celles de la troisième génération, notamment sur les staphylocoques et les streptocoques [31].
L’aquisition de la résistance aux céphalosporines est due à trois mécanismes ; la modification des PBP (penicillin binding proteins) ce qui diminue leurs affinité aux céphalosporines, l’augmentation de l’efflux et l’inactivation enzymatique par les β-lactamases [139].
Les BLSE (Bêta-lactamase à Spectre Elargi) sont des enzymes sont capables d’hydrolyser les céphalosporines de troisième génération [58].
Les entérocoques et Listeria monocytogenes sont naturellement résistants aux céphalosporines. Les cas de résistance aux céphalosporines de 3ème et 4ème
génération sont de plus en plus fréquents en médecine vétérinaire. Bien que l’usage systémique des céphalosporines ne donne que de faibles concentrations dans le système gastro-intestinal, il ressort de certaines études que ces concentrations sont suffisamment élevées pour la sélection d’E. Coli résistants.
Pharmacocinétique
La médiocre résorption digestive pour la plupart des céphalosporines, fait que leur emploi se fait presqu’exclusivement par la voie parentérale quand on recherche un effet général [31].
La distribution des céphalosporines dans l’organisme est très large (poumons, os, liquides…), elles peuvent par conséquent être utilisées dans de nombreuses affections. Cependant, elles ne passent pas la barrière méningée. Les céphalosporines ont une action majoritairement extracellulaire du fait des propriétés chimiques. Elles subissent peu de biotransformations. Leur élimination se fait majoritairement par les urines, elle est rapide [248]. Le temps de demi-vie des céphalosporines est en général 1 à 2 heures [139]. La céfovécine se différencie des autres céphalosporines par sa forte liaison aux protéines et sa longue demi-vie d’élimination rénale avec une longue durée d’action chez le chien et le chat. Elle atteint des concentrations actives pendant 14 jours après une seule injection d’une solution aqueuse de sel de sodium. Elle est principalement excrétée sous sa forme active inchangée dans les urines.
Pharmacodynamie
Tout comme les pénicillines, les céphalosporines inhibent la biosynthèse de la paroi sur les bactéries en croissance, leur noyau de base céphème est plus stable
19
que le noyau péname des pénicillines, il augmente leur résistance aux β lactamases.
Effets indésirables et toxiques
Les céphalosporines sont considérées comme des médicaments sûrs d’emploi, avec peu d’effets indésirables en relation avec la spécificité d’action de ces antibiotiques sur la paroi bactérienne. Certains effets secondaires peuvent être observés avec les nouvelles générations de céphalosporines telles que des troubles hémorragiques associés à une hypoprothrombinémie et des déformations plaquettaires.
Afin de protéger la santé du consommateur, des limites maximales de résidus (LMRs en ppb ou μg/Kg ont été fixées dans les diverses denrées alimentaires d’origine animale). Elles figurent dans la note de service 742/200 du 28 mars 2006 de la DGSV et avenant du 9 mars 2010.
Ainsi des LMRs définitives ont été fixées pour le cefquinome et le ceftiofur chez les bovins et pour la céfazoline chez les bovins, ovins et caprins. Seul le cefquinome a fait l’objet de fixation de LMR chez les équidés.
Contre-indications
Chez les carnivores, l'administration orale peut parfois provoquer des vomissements et de la diarrhée. La toxicité de la céfalexine est très faible, mais des réactions allergiques, parfois croisées avec les pénicillines, sont rarement observées.
Précautions particulières
Afin de favoriser l’usage rationnel des céphalosporines, quelques restrictions et mises en garde majeures ont été imposées au niveau mondial. Le recours à l’antibiogramme devrait être systématiquement appliqué avant la mise en place de ces traitements.
Spécialités disponibles en Tunisie
Céfalexine
Tableau XIV
Spécialités vétérinaires contenant de la céphalosporine de première génération. Nom
déposé Espèces cibles Principes Actifs Forme Présenta-tion Labo.
Prix Public DT RILEXINE TRAITEMENT 200mg BV CEFA-LEXINE Pde. Intra-Mammaire Bte. 4 Seringues VIRBAC 15,756
20
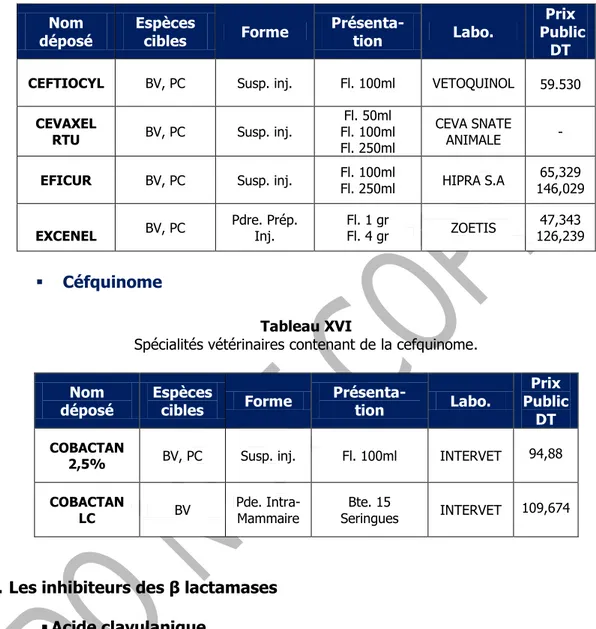
Ceftiofur
Tableau XV
Spécialités vétérinaires contenant du ceftiofur
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public
DT CEFTIOCYL BV, PC Susp. inj. Fl. 100ml VETOQUINOL 59.530
CEVAXEL
RTU BV, PC Susp. inj.
Fl. 50ml Fl. 100ml Fl. 250ml
CEVA SNATE
ANIMALE -
EFICUR BV, PC Susp. inj. Fl. 100ml Fl. 250ml HIPRA S.A 146,029 65,329
EXCENEL BV, PC Pdre. Prép. Inj. Fl. 1 gr Fl. 4 gr ZOETIS 126,239 47,343
Céfquinome
Tableau XVI
Spécialités vétérinaires contenant de la cefquinome.
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public
DT COBACTAN
2,5% BV, PC Susp. inj. Fl. 100ml INTERVET 94,88
COBACTAN LC BV Pde. Intra-Mammaire Bte. 15 Seringues INTERVET 109,674
1.1.3. Les inhibiteurs des β lactamases
Acide clavulanique
L'acide clavulanique est un inhibiteur de la majorité des β lactamases, élaboré par Streptomyces clavuligerus. Il dérive du noyau oxapéname et possède une activité antibactérienne intrinsèque faible mais protège l'activité de la β lactamine qui lui est associée [139].
Indications - spectre d’activité - résistances
L’indication de l’acide clavulanique (associé à un antibiotique, généralement l’amoxicilline) se justifie par l’extension du spectre d’activité de l’antibiotique à des pathogènes importants comme les staphylocoques et certains germes à Gram - producteurs de β lactamases.
L’acide clavulanique inhibe les β lactamases des staphylocoques et des Klebsiella. Il est sans effet sur les céphalosporinases des entérobactéries (résistance naturelle d’Enterobacter cloacae, Serratia marcescens…etc.). L’association
21
amoxicilline-acide clavulanique, qui est largement utilisée en thérapeutique, possède un spectre d’activité proche de celui des céphalosporines de première et de deuxième génération.
Pharmacocinétique
L’association d’un inhibiteur avec un antibiotique ne modifie pas la pharmacocinétique de l’antibiotique associé.
Pharmacodynamie
L’acide clavulanique forme un substrat suicide et se lie de manière irréversible à la βlactamase, empêchant ainsi son action ultérieure sur les β lactamines. Il s’agit d’une inhibition compétitive irréversible.
Spécialités disponibles en Tunisie
Acide clavulanique
Tableau XVII
Spécialités vétérinaires contenant de l'acide clavulanique en association.
Nom
déposé Espèces cibles Principes Actifs Forme Présenta-tion Labo. Public Prix SYNULOX INTRA-MAMMAIRE BV AMOXICILLINE, ACIDE CLAVULANIQUE, PREDNISOLONE Susp. Huil. Intra-mammaire Bte. 12 Applicateurs ZOETIS 55,722 SYNULOX RTU BV, OV, PC AMOXICILLINE, ACIDE
CLAVULANIQUE Susp. inj. Fl. 100ml ZOETIS 39,083
SYNULOX COMPRIME
250 MG CN
AMOXICILLINE, ACIDE
CLAVULANIQUE Comp. Bte. 100 ZOETIS 39.959
SYNULOX COMPRIME
500 MG
CN AMOXICILLINE, ACIDE CLAVULANIQUE
Comp. Bte. 10 ZOETIS 10.275
1.2. Aminosides
Les aminosides ou aminocyclitols ou encore aminoglycosides sont des hétérosides aminés, bactéricides à spectre variable possédant un noyau central aminocyclitol.
Ils sont hydrophiles à caractère basique, ce qui permet la préparation de sels d’acides. Ils peuvent être soit d’origine naturelle, élaborés par des souches de
Streptomyces (streptomycine, néomycine, kanamycine) ou d'Actinomyces
(gentamicine), soit obtenus par semi-synthèse.
On classe les aminosides en fonction de leur origine, de la nature et des oses qui s'y rattachent.
22
Parmi les composés naturels, on distingue : - Dérivés de la streptidine : streptomycine,
- Dérivés de la désoxy-2-streptamine : néomycine, framycétine, paromomycine, kanamycine et dérivés, apramycine, gentamicine, sisomicine, tobramycine,
Les composés de semi-synthèse dérivent principalement de [321] : - Streptomycine : dihydrostreptomycine (DHS),
- Kanamycine : amikacine, dibékacine, - Sisomicine : nétilmicine.
Indications - spectre d’activité - résistances
Les aminosides sont employés en thérapeutique pour le traitement curatif des maladies infectieuses bactériennes provoquées par des germes sensibles. Ils sont indiqués par voie parentérale principalement dans des usages généraux : septicémies, infections pulmonaires (pasteurelloses) et urinaires (cystites uniquement). Ils sont également employés par des voies locales appropriées pour le traitement d'infections localisées:
- Entérites (la néomycine en particulier),
- Mammites (voie intra-mammaire avec la néomycine), - Cystites colibacillaires,
- Infections cutanées superficielles et des otites (néomycine), - Infections oculaires (néomycine, gentamicine),
- Otites à Pseudomonas aeruginosa (gentamicine).
La paromomycine est préconisée dans le traitement ou la prévention de la cryptosporidiose du veau et du chevreau.
La dose habituelle d'utilisation des aminosides est de 10 à 20 mg.kg-1 P.V., celle
de la gentamicine est de 3 à 6 mg. kg-1 P.V. [155].
Le spectre d’activité des aminosides est large couvrant les bactéries à Gram - et les staphylocoques, surtout les streptocoques mais inactif sur les germes anaérobies stricts. La streptomycine est active contre le Bacille tuberculeux. Le spectre d’activité de la spectinomycine se rapproche de celui de la streptomycine. La Gentamycine possède un spectre élargi à Pseudomonas aeruginosa et mycoplasma synoviae. La paromomycine agit sur les protozoaires tels que cryptosporidium parvum, agent de la cryptosporidiose du veau et du chevreau.
Les aminosides sont l'un des groupes d'antibiotiques chez lesquels les antibiorésistances se développent le plus rapidement. Ces résistances sont en effet actuellement très importantes, atteignant de 50% à 90 % pour certaines souches bactériennes [139].
Les aminosides de semi-synthèse ont un nombre réduit d’hydroxyles par rapport aux composés parentaux naturels d’où une meilleure résistance.
23
Pharmacodynamie
Les aminosides sont des antibiotiques bactéricides concentration-dépendant, qui après pénétration à travers la paroi bactérienne, interfèrent avec la sous-unité 30 S des ribosomes pour inhiber la synthèse protéique [165].
Leur action est doubles, ils inhibent la biosynthèse des protéines bactériennes et perturbent la perméabilité de la membrane bactérienne. La spectinomycine se distingue des autres aminosides par un pouvoir bactériostatique empêchant uniquement la phase d’initiation de la synthèse des protéines.
Pharmacocinétique
La pharmacocinétique est conditionnée par le caractère hydrosoluble, basique et l’excellente stabilité de ces composés (notamment la DHS). Leur absorption est très faible par voie orale, mais ils peuvent être indiqués en cas d’infection localisée du tube digestif par des bactéries à Gram - .
Après une administration parentérale, la distribution des aminosides se limite aux fluides extracellulaires donc essentiellement plasmatiques et interstitiels. Ils franchissent difficilement les barrières biologiques et n’atteignent que de faibles concentrations dans le lait, les sécrétions bronchiques ou le liquide cérébrospinal. Les biotransformations sont pratiquement nulles. Ils sont éliminés rapidement et en nature par filtration glomérulaire et se concentrent dans le cortex rénal.
Contre-indications
Lors d’insuffisance rénale sévère, les aminosides sont contre-indiqués en raison de leur tropisme pour le cortex rénal.
Il ne faut pas les utiliser en même temps que d’autres antibiotiques potentiellement néphrotoxiques comme les sulfamides et les antibiotiques polypeptidiques. La combinaison avec les diurétiques (furosémide, mannitol) accroît leurs effets indésirables. La toxicité générale de la néomycine interdit son emploi par voie générale.
Effets indésirables
Les aminosides sont parmi les antibiotiques dont la toxicité est relativement élevée [320]. Selon la molécule, la toxicité est variable.
Des accidents de toxicité aiguë avec des troubles essentiellement fonctionnels sont observés soit lors de surdosages thérapeutiques, soit surtout en cours d’anesthésie. Ce ci est lié à leurs propriétés curarisantes en bloquant la libération pré-synaptique de l’acétylcholine. Le chat est le plus sensible à ce type d’accident (ne jamais dépasser 250 mg de DHS chez cette espèce).
Des accidents de toxicité chronique avec des troubles lésionnels sont observés lors d’emploi prolongé (10 à 15 jours) par voie générale à des doses thérapeutiques et surtout à des doses élevées tels que des accidents d’ototoxicité et de néphrotoxicité.
La néomycine et la framycétine sont les plus néphrotoxiques parmi les aminosides
24
Interactions
La néphrotoxicité est potentialisée par l’emploi de furosémide et d’antibiotiques polypeptidiques. L’association aux antibiotiques bactéricides agissant sur les germes en phase de multiplication est synergique, notamment aux β lactamines (pénicilline-streptomycine), mais aussi aux lincosamides (spectinomycine-lincomycine) pour le traitement d’infections bactériennes gastro-intestinales.
Spécialités disponibles en Tunisie
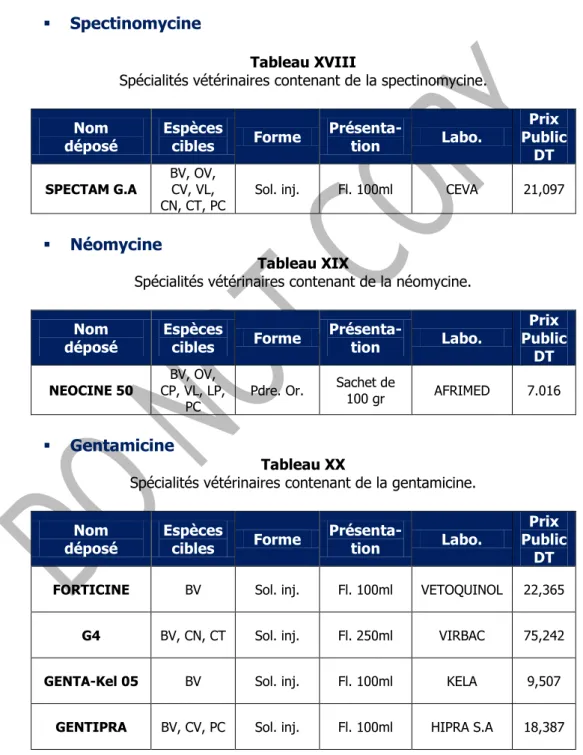
Spectinomycine
Tableau XVIII
Spécialités vétérinaires contenant de la spectinomycine.
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public DT SPECTAM G.A BV, OV, CV, VL,
CN, CT, PC Sol. inj. Fl. 100ml CEVA 21,097
Néomycine
Tableau XIX
Spécialités vétérinaires contenant de la néomycine.
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public DT NEOCINE 50 CP, VL, LP, BV, OV, PC Pdre. Or. Sachet de 100 gr AFRIMED 7.016 Gentamicine Tableau XX
Spécialités vétérinaires contenant de la gentamicine.
Nom
déposé Espèces cibles Forme Présenta-tion Labo.
Prix Public
DT FORTICINE BV Sol. inj. Fl. 100ml VETOQUINOL 22,365
G4 BV, CN, CT Sol. inj. Fl. 250ml VIRBAC 75,242
GENTA-Kel 05 BV Sol. inj. Fl. 100ml KELA 9,507