HAL Id: tel-01715011
https://tel.archives-ouvertes.fr/tel-01715011
Submitted on 22 Feb 2018HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Kaixian Zhu
To cite this version:
Kaixian Zhu. Évaluation sur banc d’essai des algorithmes des machines ventilatoires. Pneumologie et système respiratoire. Université Paris-Saclay, 2016. Français. �NNT : 2016SACLS021�. �tel-01715011�
NNT : 2016SACLS021
THESE DE DOCTORAT
DE L’UNIVERSITE PARIS-SACLAY,
préparée à l’Université Paris-Sud
ÉCOLE DOCTORALE N°569
Innovation Thérapeutique : du Fondamental à l’Appliqué
Spécialité de Doctorat : Physiologie, Physiopathologie
Par
M. Kaixian Zhu
Evaluation sur Banc d’Essai des Algorithmes des
Machines Ventilatoires
Thèse présentée et soutenue à Clamart, le 11 janvier 2016:
Composition du Jury :
M. F. Lofaso Professeur, Université Versailles Saint-Quentin en Yvelines
Président M. R. Farré Professeur, Universitat de Barcelona Rapporteur M. J-C. Meurice Professeur, Université de Poitiers Rapporteur M. G. Roisman Praticien hospitalier, Hôpital
Antoine-Béclère, Hôpital Universitaire Paris-Sud
Examinateur M. P. Escourrou Professeur, Université Paris-Sud Directeur de thèse M. S. Aouf Ancien Directeur du Département
Medico-Technique, Air Liquide Healthcare
THESE DE DOCTORAT
De l’Université Paris-Saclay,
Préparée à l’Université Paris-Sud
Ecole Doctorale N°569
Innovation Thérapeutique : Du Fondamental à l’Appliqué
Evaluation sur Banc d’Essai des Algorithmes des
Machines Ventilatoires
Présentée par
Kaixian ZHU
à Clamart, le 11 janvier 2016
Soutenue devant le jury composé de :
Pr. Frédéric LOFASO
Université Versailles Saint-Quentin en
Yvelines
Président
Pr. Ramón FARRÉ
Universitat de Barcelona
Rapporteur
Pr. Jean-Claude MEURICE
Université de Poitiers
Rapporteur
Dr. Gabriel ROISMAN
AP-HP Hôpital Antoine-Béclère
Examinateur
Pr. Pierre ESCOURROU
Université Paris-Sud
Directeur de thèse
Résumé
Les troubles respiratoires du sommeil, notamment le syndrome d’apnée du sommeil, représentent un problème de santé publique. Ils contribuent aux symptômes diurnes comme la somnolence sévère et sont associés à des maladies chroniques.
Depuis quelques années, une variété d’appareils de traitement ventilatoire a été développée pour traiter les troubles respiratoires du sommeil, principalement les maladies liées à l’obstruction de la voie aérienne supérieure (apnée obstructive) ou à la commande centrale (apnée centrale). Ces appareils fonctionnent suivant des principes différents, en raison de leurs propres algorithmes, qui sont souvent mal connus et protégés par les fabricants. Les évaluations des appareils de ventilation sont effectuées pendant les traitements cliniques chez des patients. Il est donc difficile de comparer ces différents appareils dans les mêmes conditions à cause des variabilités inter- et intra-patient. Un banc d’essai pourrait permettre de tester les réponses des appareils dans les conditions standardisées et reproductibles.
Cette thèse a consisté à construire un banc d’essai qui permet de reproduire les signaux de patients et de respecter de la physiologie humaine. La réaction du banc d’essai prend aussi en compte la réaction de l’appareil à tester sur le système, i.e., ce modèle fonctionne en « boucle fermée ».
Avec le banc d’essai construit, les différentes machines de pression positive continue (PPC) autopilotée disponibles sur le marché ont été évaluées pour leurs algorithmes ainsi pour leurs modes confort. De plus, trois machines de ventilation auto-asservie (ASV) ont été soumises aux différents événements respiratoires du sommeil créés par un autre modèle d’un principe similaire. Nous avons montré que les machines de PPC autopilotée ne sont pas équivalentes pour l’efficacité du traitement et la précision des données du rapport. Les modes confort pourraient éventuellement dégrader l’efficacité du traitement de PPC si la pression thérapeutique n’est pas ajustée lors de leur introduction au traitement. Pour les machines ASV, leurs réponses ne sont pas suffisantes pour normaliser la respiration et les réglages des machines peuvent influencer l’efficacité du traitement.
Les résultats pourraient compléter les données cliniques et fournir une option complémentaire pour le processus futur de certification de ces dispositifs médicaux.
Summary
Sleep disordered breathing including sleep apnea is a major public health problem. It contributes to daytime sleepiness and is associated with chronic diseases.
In recent years, a variety of ventilation devices have been developed with the objective of treating sleep disorders related to the upper airway obstruction (obstructive apnea) or the central command (central apnea). These devices operate with different algorithms, which are little known and protected by the device manufacturers. Since most devices are evaluated during patient treatment, it is difficult to compare them in the same conditions due to inter- and intra-patient variability. Bench test has been proposed to evaluate the device responses in standardized and reproducible conditions.
This thesis was aimed to develop a respiratory bench model able to reproduce patients’ signals and also in concordance with human physiology. The bench model can take into account the pressure responses of tested devices and works in a “closed loop” setting.
With this bench model, several commercially available auto-titrating continuous positive airway pressure devices were evaluated for their auto-titration algorithms as well as their pressure-relief modes. Also, three adaptive servo-ventilation devices were evaluated by subjecting various sleep disordered breathing events that were generated by another bench model of a similar principle. We demonstrated that eleven auto-titrating continuous positive airway pressure devices were not equivalent in terms of their treatment efficacy and the data accuracy in the device report. The pressure-relief modes may attenuate the efficacy if not adjusted at the time of their introduction. The responses of adaptive servo-ventilation devices were not sufficient to normalize the breathing flow and their efficacy depended on the initial settings.
The current certification process of these ventilatory devices, which focus mainly on clinical aspects, may be completed by the results of our bench.
Remerciements
Cette thèse CIFRE est le fruit d’une collaboration entre l’Université Paris-Sud et Air Liquide Healthcare, elle s’est déroulée au sein de l’entreprise ALEHOS à Gentilly et du laboratoire du sommeil au CHU Antoine-Béclère à Clamart.
Ma plus grande gratitude va au professeur Pierre Escourrou, mon directeur de thèse, et docteur Sami Aouf, mon co-directeur de thèse chez Air Liquide, qui m’ont permis de me lancer dans l’aventure de cette thèse et m’ont accordé leur confiance et leur soutien. Sans eux ce travail n’aurait jamais vu le jour.
Je tiens à remercier les membres du jury pour l’intérêt qu’ils ont porté à ce travail : professeurs Ramón Farré et Jean-Claude Meurice pour avoir accepté de rapporter ma thèse, professeur Frédéric Lofaso, pour les conseils scientifiques qu’il m’a donnés lors de ma soutenance de mi-thèse, docteur Gabriel Roisman pour nos échanges fructueux tout au long de ce travail.
Ces trois dernières années ont filé à une vitesse folle : de Clamart à Gentilly, du poumon Michigan au poumon Ingmar... Mes remerciements s’adressent à toute l’équipe PMT avec qui j’ai eu la chance de travailler au quotidien. Je pense notamment à Sébastien Hardy pour ses corrections pertinentes apportées à ce mémoire, à Charles-Philippe Thévenin pour sa disponibilité à répondre à mes questions et à transmettre ses connaissances et sa vision de la technologie médicale, et à Amélie Sagniez pour nos échanges autant professionnels que personnels (tes blagues « Carambar » par exemple)… Enfin merci à tous ceux, au sein d’ALEHOS, qui ont contribué d’une manière ou d’une autre, à la réussite de ce projet.
Ma gratitude s’adresse également aux différents partenaires de cette thèse : Docteurs Claudio Rabec et Jésus Gonzalez, pour leur soutien au projet (malgré le fait que notre travail n’ait pas été inclus dans ce manuscrit, un joli papier est en cours !) ; Jacques Mulon du CRCD pour son aide efficace apportée au super plan de la boîte de Starling et surtout sa gentillesse ; toute l’équipe du service EFM de l’Hôpital Béclère, pour leur accueil chaleureux lors de mes passages toutes les semaines.
Je pense aussi au Professeur Denis Chemla, pour nos échanges scientifiques passionnants et surtout pour ses petits mots d’encouragement de temps en temps qui ont réchauffé mon cœur.
Cette thèse m’a permis de faire la connaissance de Luc, Kelly, Clémentine, Kahina, Ravina, Céline, Marion, avec qui j’ai passé des moments très agréables, surtout nos sorties entre amis.
Je n’oublie pas l’ANRT, qui a financé ce travail. Je me rappelle combien j’ai été impatient d’attendre leur décision d’octroi de cette CIFRE…
Publications associées à ce travail :
Zhu K, Kharboutly H, Ma J, Bouzit M, Escourrou P. Bench Test Evaluation of Adaptive
Servoventilation Devices for Sleep Apnea Treatment. J Clin Sleep Med 2013, 9 (9): 861–71.
Zhu K, Roisman G, Aouf S, Escourrou P. All APAPs Are Not Equivalent for the Treatment of
Sleep Disordered Breathing: A Bench Evaluation of Eleven Commercially Available Devices.
J Clin Sleep Med 2015, 11 (7): 725-34.
Article accepté pour publication :
Zhu K, Aouf S, Roisman G, Escourrou P. Pressure-relief features of fixed- and auto-titrating
CPAP may impair their efficacy: Evaluation with a respiratory bench model. Accepted for
publication in Journal of Clinical Sleep Medicine, October 6
th, 2015.
Sommaire
Résumé ... 1
Summary ... 3
Remerciements ... 5
Index des illustrations ... 11
Index des tables ... 12
Liste des abréviations ... 13
Objectifs ... 15
Chapitre 1 Les pathologies respiratoires du sommeil ... 17
1.1 Syndrome d’apnées-hypopnées obstructives du sommeil ... 18
1.1.1 Physiopathologie ... 18
1.1.2 Traitement ... 19
1.2 Syndrome d’apnées-hypopnées centrales du sommeil ... 22
1.2.1 Physiopathologie ... 22
1.2.2 Traitement du SAHCS hypercapnique par assistance ventilatoire ... 24
1.2.3 Traitement du SAHCS non-hypercapnique par assistance ventilatoire ... 24
Chapitre 2 Les bancs d’essai ... 27
2.1 Les bancs d’essai dans la littérature ... 28
2.2 Banc d’essai associé à cette thèse ... 31
2.2.1 Poumon actif ASL5000 ... 31
2.2.2 Résistance de Starling... 33
2.2.3 Simulation du ronflement ... 34
Chapitre 3 Résultats ... 37
3.1 Evaluation des onze machines de ventilation en PPC autopilotée sur un banc d’essai ... 38
3.1.1 Introduction ... 38
3.1.2 Article 1 ... 39
3.1.3 Résumé de l’article 1 ... 51
3.2 Evaluation des modes de confort aux appareils PPC sur un banc d’essai ... 52
3.2.1 Introduction ... 52
3.2.2 Article 2 ... 53
3.3 Evaluation des appareils de ventilation auto-asservie sur un banc d’essai ... 74
3.3.1 Introduction ... 74
3.3.2 Article 3 ... 75
3.3.3 Résumé de l’article 3 ... 89
Chapitre 4 Discussion générale ... 91
4.1 Validité du banc d’essai : Les voies aériennes supérieures et la résistance de Starling ... 92
4.1.1 Modèle de la « balance des forces » ... 92
4.1.2 Modèle de la « résistance de Starling » ... 93
4.2 Banc d’essai vs. Essais cliniques ... 107
4.3 A qui incombe en Europe et sur le marché Nord-Américain la responsabilité d’évaluation d’un DM ? ... 108
Chapitre 5 Conclusion ... 111
Références bibliographiques ... 113
Annexes ... 121
A.1 Etude de la variabilité de la fréquence cardiaque nocturne et syndrome d’apnées du sommeil123 A.1.1 Résumé ... 123
A.1.2 Article 4 ... 125
Index des illustrations
Figure 1-1 Les facteurs qui participent au déclenchement de l'obstruction des VAS 19
Figure 1-2 Le traitement du SAHOS par PPC 20
Figure 1-3 Physiologie de la ventilation au cours du sommeil 23
Figure 2-1 Exemple du banc d'essai avec poumon de test Michigan pour l'évaluation des ventilateurs
30
Figure 2-2 Photo du banc d'essai 31
Figure 2-3 Principe du fonctionnement du poumon actif ASL5000 33
Figure 2-4 Coupe transversale de la résistance de Starling 34
Figure 2-5 Le signal du ronflement avec le spectre de fréquence 35
Figure 4-1 Modèle de la "balance des forces" 92
Figure 4-2 Modèle de la "résistance de Starling" 94
Figure 4-3 Le débit maximal vs. la pression nasale: mesure sur banc d'essai vs. Courbe théorique
95 Figure 4-4 Caractéristiques débit-pression aval du tube collabable 96 Figure 4-5 Exemple de formes de débit constatées chez les patients et comparaison
des formes de débit entre les cas de la résistance de Starling et de la DEN
97 Figure 4-6 Débit pression et la morphologie du modèle Starling pendant une
limitation de débit avec DEN
99 Figure 4-7 Evolution des formes de débit et de Pds avec l'effort inspiratoire de 1 à 20
cmH2O
100 Figure 4-8 Relation entre V'max intra, Pus et la baisse de Pds (ΔPds) de la résistance de
Starling du banc d’essai 101
Figure 4-9 Plan V’max intra-Pus-Pds 102
Figure 4-10 Plans débit-ΔPds pendant un cycle de respiration avec différentes Pus
(=mask pressure)
103 Figure 4-11 Plan DEN- Pds et la baisse de Pds (ΔPds) avec différentes Pus 104
Index des tables
Table 2-1 Les bancs d'essai pour l'évaluation d'appareils PPC autopilotées dans la littérature
28 Table 4-1 Comparaison Banc d’essai vs. Essais cliniques : les avantages et les
inconvénients
Liste des abréviations
510(K) FDA 510(k) premarket notification
AI Aide inspiratoire
ASV Ventilation auto-asservie
Bilevel PAP PPC à double niveau de pression
C Compliance
CDRH Center for devices and radiological health
CE Conformité européenne
CompSA Apnée du sommeil complexe
CSR Respiration Cheyne-Stokes
DEN/NED Dépendance d'effort négatif
DM Dispositif médical
EMG Electromyographie
EPAP Pression expiratoire
FDA US Food and Drug Administration FEVG Fraction d'éjection ventriculaire gauche
IAH Index d'apnée-hypopnée
JCSM Journal of Clinical Sleep Medicine
ON Organisme Notifié
Paw Pression à la voie aérienne
Pcrit Pression critique de fermeture/d'occlusion
Pds Pression en aval des VAS
Peff ds Pression effective en aval des VAS
Peff us Pression effective en amont des VAS
PIL Pression intraluminale
PMA Premarket Approval
Pmus Pression des muscles respiratoires
Pmus_dila Pression de la contraction des muscles dilatateurs oropharyngés
Pout Pression autour des VAS (pression à l'intérieur de la résistance de Starling)
PPC Pression positive continue
PSG Polysomnographie
Ptiss Pression tissulaire
Pus Pression en amont des VAS
Pus collap Pression en amont du segment collabé des VAS
Rus Résistance en amont des VAS
SAHCS Syndrome d'apnée-hypopnées centrales du sommeil SAHOS Syndrome d'apnée-hypopnées obstructives du sommeil
V Volume
VAS Voies aériennes supérieures
V'max Débit maximal
V'max inter Débit maximal inter-cycles
V'max intra Débit maximal intra-cycle
VNDP Ventilation à Deux Niveaux de Pression ΔPds Baisse de pression en aval des VAS
Objectifs
L’objectif de cette thèse est de réaliser un banc d’essais fiable pour évaluer la performance des machines de pression positive continue (CPAP) auto-pilotée, de ventilation auto-asservie (ASV) ainsi que des autres machines de ventilation non invasive pour le domicile présentes et à venir sur le marché.
Le banc d’essai doit permettre de tester les appareils pendant une longue durée, de reproduire les signaux de patients. Aussi, il doit respecter la physiologie humaine et prend en compte l’action de l’appareil à tester.
Les résultats obtenus sur ce banc d’essai pourraient être comparés avec les résultats des tests cliniques pour déterminer les complémentarités des deux approches. Ainsi, l’évaluation sur banc pourrait servir à améliorer les méthodologies actuelles de la certification des appareils de ventilation avant leur arrivée sur le marché.
Chapitre 1 Les pathologies respiratoires du
sommeil
Les troubles respiratoires du sommeil font partie des problèmes de santé publique majeurs, dont le syndrome d’apnées-hypopnées obstructives du sommeil (SAHOS) touche de 5% à 7% de la population adulte. Le SAHOS est une pathologie qui peut entrainer des conséquences sévères sur la somnolence et les complications cardiovasculaires, ainsi être associée aux autres troubles respiratoires chroniques.
Le syndrome d’apnées-hypopnées centrales du sommeil (SAHCS) est un arrêt transitoire de la commande des muscles respiratoires. Les apnées centrales peuvent être associées à des respirations périodiques de type Cheyne-Stokes et trouvées chez des patients atteints d’insuffisance cardiaque.
Comme ces maladies sont liées à différents mécanismes, une variété des appareils de traitement ventilatoire a été développée.
Ce chapitre présente les troubles respiratoires du sommeil, leur mécanisme et les appareils pour leurs traitements.
1.1 Syndrome d’apnées-hypopnées obstructives du sommeil
1.1.1 Physiopathologie
Une apnée ou hypopnée obstructive est un arrêt complet ou une diminution du flux aérien lors de la respiration par obstruction du niveau du pharynx avec la persistance des efforts respiratoires. Le pharynx est la portion la plus compliante et collabable des voies aériennes supérieures (VAS), situé entre les structures rigides du nez et du larynx. Le pharynx est soumis à un gradient de pression transmurale déterminé par la pression intraluminale (PIL) et la pression péritissulaire. Cette
dernière dépend de la contraction des muscles dilatateurs oropharyngés (Pmus_dila) (action dilatatrice), et
du poids des tissus mous (pression tissulaire : Ptiss) (action occlusive). La pression critique de
fermeture (Pcrit) correspond à la pression transmurale en dessous laquelle les VAS sont entièrement
fermées.
Le calibre des VAS dépend du gradient de pression transmural et de la compliance de ses parois. Pour un gradient transmural donné : plus la compliance des parois est importante, plus le calibre des VAS est réduit (Sériès 2004; J. L. Pépin, Tamisier, and Levy 2011). En pratique, la compliance est impossible à mesurer isolement, et elle dépend notamment des forces tissulaires dans les VAS, i.e., la Ptiss.
A chaque inspiration, la PIL s’abaisse au dessous de la pression atmosphérique et provoque la
fermeture de la VAS. Cette pression représente la principale force de collapsus des VAS. En revanche, la Pmus_dila représente la force dilatatrice. Afin de maintenir les VAS ouvertes, il faut que les muscles
dilatateurs soient suffisamment activés. Néanmoins, cette activité musculaire est inhibée par le sommeil. Des tissus trop mous (Ptiss) ou l’obésité peuvent entrainer le rétrécissement des VAS et
l’augmentation de la pression critique (Pcrit), qui correspond à la pression transmurale en dessous
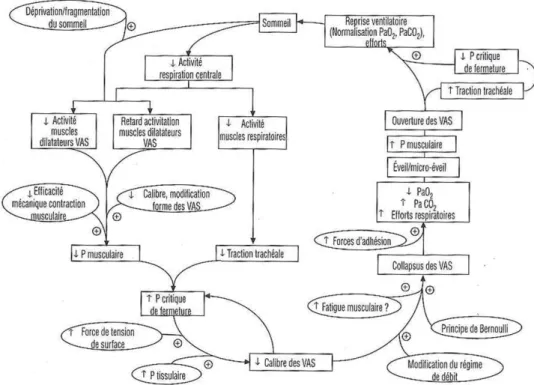
laquelle la VAS est entièrement fermée (Sériès 2004; J. L. Pépin, Tamisier, and Levy 2011). Figure 1-1 montre l’ensemble des facteurs qui participent à l’obstruction des VAS.
Figure 1-1 Les facteurs qui participent au déclenchement de l’obstruction des VAS (Sériès 2004)
1.1.2 Traitement
i. Ventilation en pression positive continue (PPC) à pression fixe
La ventilation en pression positive continue (PPC) est le traitement de référence pour les patients atteints du SAHOS (Malhotra and White 2002). Ce traitement a été proposé et décrit pour la première fois en 1981 par Sullivan et al. (Sullivan et al. 1981). Il consiste à insuffler de l’air au patient via un masque nasal ou facial afin de maintenir l’ouverture des VAS au cours du sommeil (Figure 1-2).
Les études cliniques montrent que l’effet mécanique direct de la PPC sur la VAS peut supprimer les événements respiratoires obstructifs et traiter la somnolence. A long terme, les effets bénéfiques du traitement de la PPC sur les performances cognitives et la qualité de vie ont été confirmés de même par la réduction de la mortalité cardiovasculaire (Meurice and Philip-Joet 2004; J. L. Pépin, Tamisier, and Levy 2011).
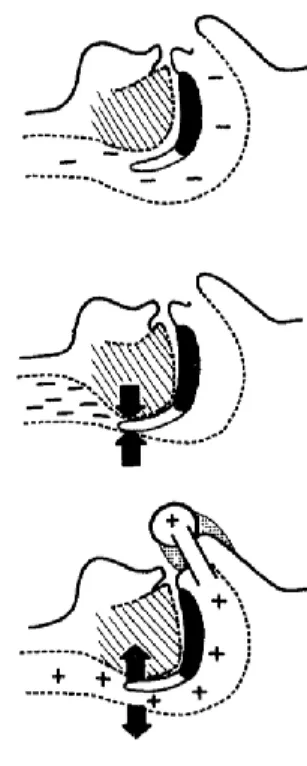
Figure 1-2 Le traitement du SAHOS par PPC (Sullivan et al. 1981). Panel du haut : les voies
aériennes supérieures sont maintenues ouvertes par le tonus musculaire pendant l’éveil du patient. Panel du milieu : lors d’une apnée obstructive, la pression en aval du pharynx devient négative avec les efforts respiratoires. Panel du bas : grâce à la PPC délivrée à l’aide d’un masque, le pharynx est maintenu ouvert et le débit respiratoire est assuré.
L’efficacité du traitement de la PPC est limité par l’adhésion du patient (Weaver and Grunstein 2008; Weaver and Sawyer 2010). Dans la littérature, le pourcentage des patients non-compliants au traitement de la PPC (temps d’utilisation < 4 heures/nuit) varie de 29% à 83% (Weaver and Grunstein 2008). Cette mauvaise compliance peut être due à plusieurs facteurs : caractéristiques du patient, sévérité de la maladie, effets secondaires liés au masque, difficulté d’adaptation à la pression, l’environnement dans lequel le patient vit et aussi de l’efficacité de la PPC (Weaver and Grunstein 2008; Weaver and Sawyer 2010).
ii. Ventilation en PPC autopilotée
Depuis quelques années, une nouvelle génération d’appareils de PPC autopilotée a été développée. Ces machines intelligentes permettent d’adapter la pression selon la détection des événements respiratoires et d’obtenir un niveau optimal de pression efficace qui varie en fonction de la position du patient, des stades du sommeil, de la prise médicamenteuse ou d’alcool. Le confort du patient est donc pris en compte dans le but d'améliorer la compliance au traitement de longue durée (Berthon-Jones et al. 1996; Teschler et al. 1996).
Ces appareils autopilotés peuvent aussi être utilisés pour la détermination de la pression efficace qui corrige tous les événements respiratoires. La titration constitue la première étape de la prise en charge du patient. En fait, la titration conventionnelle sous surveillance d’un technicien dans un laboratoire du sommeil coûte cher, et la titration avec la PPC autopilotée peut être réalisée sans surveillance ou associée à une polysomnographie (PSG) de contrôle. Plusieurs études ont montré que la titration automatique par PPC autopilotée, que ce soit en laboratoire ou à domicile, donne des bons résultats comparé à la titration conventionnelle (Philip-Joët 2006, -).
Dans la littérature, quelques études ont montré l’efficacité du traitement par PPC autopilotée à long terme sur les apnées et la somnolence associée (Meurice, Marc, and Sériès 1996; d’Ortho et al. 2000; Meurice et al. 2007). Par contre, le gain en compliance au traitement comparé à la PPC fixe est limité (I. Smith and Lasserson 2009).
Patruno et al. ont montré que le traitement par la PPC autopilotée est associé à une activité sympathique du patient plus importante par rapport au traitement par la PPC fixe (Patruno et al. 2014). De même, ses effets sur les risques cardiovasculaires ne sont pas aussi bénéfiques que ceux de la PPC fixe (Patruno et al. 2007). Ce traitement ne doit pas être utilisé chez les patients atteints d’insuffisance cardiaque, à cause des conséquences hémodynamiques défavorables liées aux grandes variations de pression au cours du traitement.
iii. Autres variétés du traitement en PPC pour le SAHOS
Sanders et al. (Sanders and Kern 1990) ont proposé de traiter le SAHOS avec un niveau de pression différente entre l’inspiration et l’expiration : on parle de PPC à double niveau de pression (Bilevel PAP), dont la pression délivrée est plus faible à l’expiration afin de faciliter l’expiration spontanée du patient en maintenant l’ouverture de la VAS avec un niveau de pression expiratoire faible mais suffisant. L’objectif de ce type de ventilation est de baisser la pression thérapeutique et d’obtenir une meilleure observance du traitement. Néanmoins, dans la méta-analyse de Cochrane, il n’y a pas de différence significative de l’adhésion au traitement entre la Bilevel PAP et la PPC fixe (I. Smith and Lasserson 2009).
Afin de résoudre les effets secondaires d’inconfort respiratoire et d’intolérance à la pression, des modes de confort qui accompagnent le traitement de la PPC ont été proposés par la plupart des fabricants des appareils. Souvent, les cliniciens rajoutent le mode de confort lorsque le patient se plaint de la pression excessive à l’expiration au cours du traitement.
C-Flex », qui applique une réduction de pression au début de l’expiration. Néanmoins, il n’y a pas accord dans la littérature sur son effet bénéfique sur l’observance thérapeutique et les autres modes de confort ne sont pas bien connus (I. Smith and Lasserson 2009; Brown 2011; J. P. Bakker and Marshall 2011).
iv. Autres alternatives aux traitements de ventilation
Il existe des orthèses d’avancée mandibulaire. Leur but est d’ouvrir l’espace derrière la langue en avançant la mâchoire inférieure afin de permettre à l’air de passer correctement. La possibilité d’obstruction est ainsi réduite. Ce traitement est néanmoins moins efficace que la PPC, et réservée aux patients qui n’acceptent pas le traitement de la PPC ou qui ont un SAHOS modéré ou un ronflement simple.
Outre ces traitements mentionnés plus haut, il existe d’autres alternatives plus rares, comme la chirurgie.
1.2 Syndrome d’apnées-hypopnées centrales du sommeil
1.2.1 Physiopathologie
Au contraire d’un événement respiratoire obstructif, une apnée ou hypopnée centrale correspond à un arrêt ou une diminution du débit aérien lié à une absence ou une réduction transitoire de la commande des muscles respiratoires. Une apnée centrale se distingue par l’absence d’efforts respiratoires. Chez un même patient, les troubles respiratoires obstructifs ou centraux peuvent être présents. Le type de trouble respiratoire est déterminé par le mécanisme prédominant. Une apnée centrale peut aussi faire partie composante d’une apnée mixte qui débute par un mécanisme central auquel succède un mécanisme obstructif.
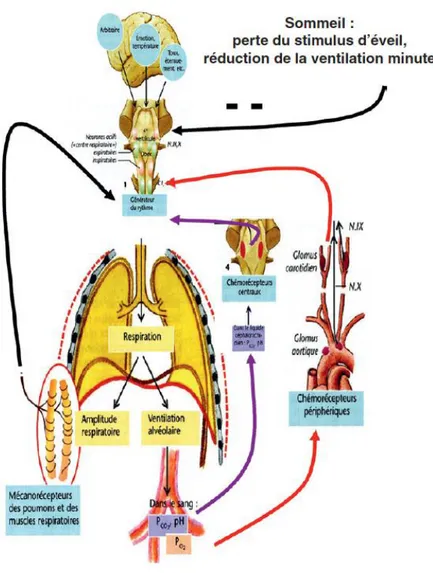
A l’éveil, la respiration est assurée par le contrôle cortical (stimulus d’éveil) et comportemental qui empêche les pauses respiratoires. Mais ce contrôle n’est pas ou peu fonctionnel pendant le sommeil. En sommeil, la ventilation est presque exclusivement sous le contrôle métabolique assuré par les centres respiratoires qui reçoivent les informations sur la pression partielle artérielle en CO2 (PaCO2) provenant des chémorécepteurs centraux et périphériques (Figure 1-3). Une baisse de la PaCO2 au seuil apnéique peut entrainer baisse de la commande ventilatoire ainsi une apnée ou hypopnée centrale.
Figure 1-3 Physiologie de la ventilation au cours du sommeil (Levy, Tamisier, and Pépin 2011).
On distingue deux mécanismes d’apnées centrales. Le premier est un dysfonctionnement de la commande respiratoire (centres respiratoires ou chémorécepteurs) ou de l’effecteur respiratoire (muscles respiratoires) avec pour conséquence une hypoventilation alvéolaire. Le patient de ce premier mécanisme souvent présente une hypercapnie diurne (Chaouat 2003; Oltean and Escourrou 2004; Berry 2012).
Le deuxième mécanisme est l’instabilité de la commande respiratoire dans les conditions normales, i.e., apnée centrale idiopathique, ou sous traitement ventilatoire, i.e., apnée du sommeil complexe (CompSA), qui est une apparition d’apnées centrales au cours du traitement des apnées obstructive par PPC. Cette instabilité est dû à la petite différence entre la PaCO2 et le seuil apnéique du patient, et peut s’associer au changement du stade du sommeil ou au micro-éveil (Berry 2012). De plus, chez les patients en insuffisance cardiaque, il existe une réponse ventilatoire exagérée au CO2 avec induction
d’une hyperpnée secondaire générant une apnée centrale (Levy, Tamisier, and Pépin 2011). Ici on parle de la respiration périodique ou respiration Cheyne-Stokes (Cheyne-Stokes Respiration, CSR) caractérisée par un crescendo-decrescendo de ventilation. Les patients avec ce mécanisme d’apnée centrale ne sont pas hypercapniques le jour mais la tendance à être hypocapniques.
1.2.2 Traitement du SAHCS hypercapnique par assistance ventilatoire
Le traitement de référence pour le SAHCS hypercapnique et l’hypoventilation alvéolaire centrale est la ventilation à deux niveaux de pression (VNDP) (Levy, Tamisier, and Pépin 2011). La VNDP est plus utilisée en mode « spontaneous timed (ST) », avec une aide inspiratoire (AI) et une fréquence de sécurité afin de prévenir la survenue d’apnées centrales. Une pression expiratoire (EPAP) est proposée pour stabiliser la VAS et éliminer les événements obstructifs associés. Dans le cas idéal, une titration sous PSG doit être effectuée au départ du traitement afin de déterminer les pressions adéquates (Berry 2012).
1.2.3 Traitement du SAHCS non-hypercapnique par assistance ventilatoire
i. En absence d’insuffisance cardiaque
Du fait que l’apnée centrale idiopathique est rare, il n’y pas de données sur l’efficacité du traitement ou d’étude en long-terme dans la littérature sur son traitement (Levy, Tamisier, and Pépin 2011; Berry 2012).
En ce qui concerne l’apnée complexe, le meilleur traitement reste discutable. En absence de la respiration Cheyne-Stokes, le traitement de la PPC fixe en long terme a été montré efficace bien que le patient présente souvent des événements respiratoires résiduels au début du traitement.
Une alternative au traitement de la PPC est la ventilation auto-asservie (ASV) ou la VNDP. Les objectifs de la machine ASV sont d’envoyer une aide inspiratoire variable en fonction de la référence du débit respiratoire ou du volume du patient, afin de corriger les événements respiratoires et de stabiliser la respiration. Une pression expiratoire fixe ou autopilotée est proposée afin de traiter les événements obstructifs et de stabiliser les VAS. Souvent, l’EPAP est proche de la valeur de la PPC fixe pour les apnées obstructives. Le traitement de l’ASV a montré une efficacité pour la majorité de
patients qui souffraient d’apnée complexe (Berry 2012).
ii. En présence d’insuffisance cardiaque
Le traitement ventilatoire pour l’apnée centrale avec l’insuffisance cardiaque reste discuté (Berry 2012). L’ASV est proposé aux patients porteurs CSR avec l’insuffisance cardiaque afin de stabiliser leur respiration. La machine corrige les événements respiratoires en ajustant son aide ventilatoire en fonction de la ventilation du patient mesurée. De ce fait, la qualité du sommeil du patient peut être améliorée (Berry 2012). A propos de son effet bénéfique à long terme et la morbi-mortalité, plusieurs études sont en cours (Haute Autorité de Santé 2015), dont l’étude SERVE-HF a pour l’objectif d’évaluer chez les patients d’insuffisance cardiaque sévère avec une fraction d’éjection ventriculaire gauche (FEVG) inférieure ou égale à 45% (Cowie et al. 2013). L’analyse préliminaire de cette étude montre une augmentation de mortalité chez le groupe en insuffisance cardiaque sévère traité par l’ASV par rapport au groupe contrôle.
La PPC fixe est aussi proposée aux patients atteints d’insuffisance cardiaque avec un SAHCS. Plusieurs études de durée de 1 à 3 mois ont montré que ce traitement peut apporter une amélioration aux patients en termes de la qualité du sommeil et de la fraction d’éjection (Berry 2012). Pour l’effet sur la mortalité à long terme, l’étude CANPAP a inclus 130 patients dans le bras contrôle et 128 patients dans le bras PPC (Arzt et al. 2007). Cette étude n’a pas montré un bénéfice de survie avec la PPC fixe, et la courbe de survie était en faveur du bras contrôle au détriment du bras PPC. Néanmoins, plus de 50% patients n’ont pas répondu au traitement et ont eu un IAH non corrigé (>15 événements/h) (Berry 2012; Haute Autorité de Santé 2015).
Chapitre 2 Les bancs d’essai
Dans la continuité des évaluations cliniques, les tests sur les bancs d’essai pourraient permettre de tester les réponses des appareils dans les conditions standardisées et reproductibles.
Dans ce chapitre, d’abord nous présentons les bancs d’essai qui ont été déjà décrits dans la littérature et leurs principes de fonctionnement.
En suite, nous expliquons notre banc d’essai, présentons en particulier ses composants principaux comme le poumon actif ASL 5000 et la résistance de Starling.
2.1 Les bancs d’essai dans la littérature
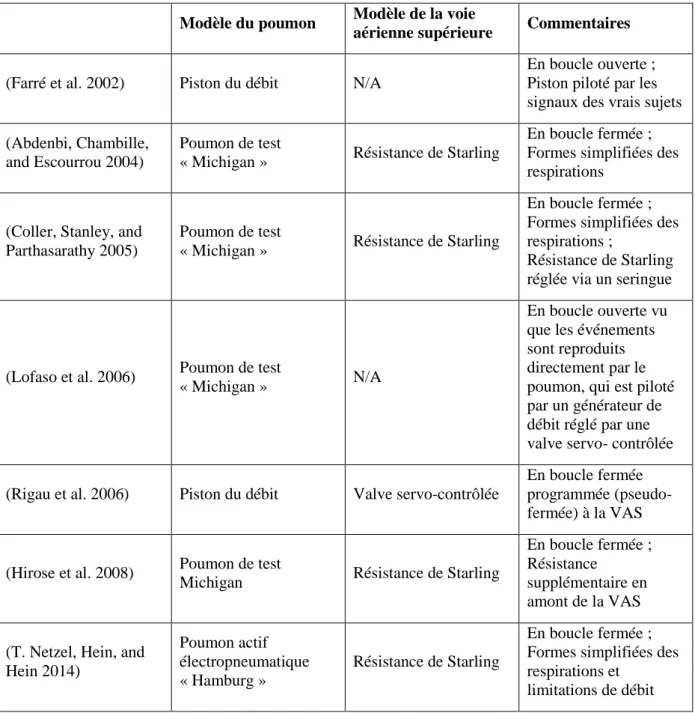
Dans la littérature, quelques études portant sur l’évaluation d’appareils PPC autopilotées sur des bancs d’essai ont été proposées (Farré et al. 2002; Abdenbi, Chambille, and Escourrou 2004; Coller, Stanley, and Parthasarathy 2005; Lofaso et al. 2006; Rigau et al. 2006; Hirose et al. 2008; T. Netzel, Hein, and Hein 2014). Tableau 2-1 montre les principes de ces bancs d’essai.
Table 2-1 Les bancs d’essai pour l’évaluation d’appareils PPC autopilotées dans la littérature
Modèle du poumon Modèle de la voie
aérienne supérieure Commentaires
(Farré et al. 2002) Piston du débit N/A
En boucle ouverte ; Piston piloté par les signaux des vrais sujets (Abdenbi, Chambille,
and Escourrou 2004)
Poumon de test
« Michigan » Résistance de Starling
En boucle fermée ; Formes simplifiées des respirations
(Coller, Stanley, and Parthasarathy 2005)
Poumon de test
« Michigan » Résistance de Starling
En boucle fermée ; Formes simplifiées des respirations ;
Résistance de Starling réglée via un seringue
(Lofaso et al. 2006) Poumon de test
« Michigan » N/A
En boucle ouverte vu que les événements sont reproduits directement par le poumon, qui est piloté par un générateur de débit réglé par une valve servo- contrôlée
(Rigau et al. 2006) Piston du débit Valve servo-contrôlée
En boucle fermée programmée (pseudo-fermée) à la VAS
(Hirose et al. 2008) Poumon de test
Michigan Résistance de Starling
En boucle fermée ; Résistance
supplémentaire en amont de la VAS
(T. Netzel, Hein, and Hein 2014) Poumon actif électropneumatique « Hamburg » Résistance de Starling En boucle fermée ; Formes simplifiées des respirations et
Ces bancs d’essai peuvent être classés en deux catégories suivant le mode de réaction de l’obstruction simulée au fonctionnement de la machine testée: système qui ne réagit pas à la réponse de la machine (boucle ouverte) et système qui prend en compte la réaction du banc d’essai à l’action de la machine à tester (boucle fermée). Ce dernier est plus physiologique.
Un premier modèle en boucle ouverte a été proposé par Farré et al. (Farré et al. 2002). Ce modèle est principalement constitué d’un simulateur de patient, qui est capable de reproduire les débits composés des événements respiratoires enregistrés d’un vrai sujet. De plus, il permet aussi de simuler les ronflements et les fuites. Au cours du test, la pression du masque et le débit sont enregistrés afin d’évaluer la réponse de l’appareil soumis aux événements créés. Un modèle similaire a été réalisé par Lofaso et al. (Lofaso et al. 2006) dans le but d’évaluer la détection des événements de limitation de débit respiratoire. Notons que ces deux modèles ne présentent pas d’obstruction mécanique dans les circuits, ainsi tous les événements respiratoires anormaux, y compris les événements obstructifs, sont reproduits artificiellement en contrôlant le débit.
Au vu de cet inconvénient, Rigau et al. (Rigau et al. 2006) ont amélioré le modèle de Farré et al. en ajoutant une valve obstructive servo-contrôlée dans le circuit. Ainsi la résistance de la voie aérienne peut être simulée. D’après l’auteur, cette valve obstructive peut être contrôlée en boucle fermée, et la résistance simulée est dépendante de la pression appliquée par la PPC autopilotée. Mais la loi de contrôle de cette valve n’est pas précisée. Comme leur ancien modèle, le simulateur peut reproduire la forme du débit enregistrée d’un vrai sujet. Cependant, ce débit est déjà la conséquence de la combinaison de l’effort respiratoire et de l’obstruction de la voie aérienne du patient. De ce fait, la pression la PPC autopilotée ne modifie le débit et le niveau d’ouverture de la valve que dans des limites étroites préprogrammées. Ce modèle ne peut donc être considéré comme une vraie boucle fermée.
Au lieu de contrôler une valve obstructive, Abdenbi et al. (Abdenbi, Chambille, and Escourrou 2004) ont implanté une « résistance de Starling » composée d’un tube compliant afin de simuler la résistance des voies aériennes supérieures. Le niveau d’ouverture du tube est réglable en fonction de la pression transmurale qui lui est appliquée. Cet élément permet au banc d’essai de fonctionner en boucle fermée en adaptant précisément le degré de l’obstruction à la réponse en pression positive de l’appareil. Les autres modèles similaires ont été réalisés par les groupes de Coller, de Hirose et de Netzel (Coller, Stanley, and Parthasarathy 2005; Hirose et al. 2008; T. Netzel, Hein, and Hein 2014). En particulière, Hirose et al. (Hirose et al. 2008) ont complété ce modèle en ajoutant une résistance supplémentaire en amont de la voie aérienne, qui pourrait influencer l’ouverture du tube, selon leur hypothèse. Néanmoins, cette résistance supplémentaire ne correspond pas à la physiologie humaine. De plus, nous pouvons aussi remarquer que les deux modèles sont incapables de reproduire les formes caractéristiques de débit respiratoires qui pourraient éventuellement influencer le fonctionnement des
appareils.
Outre la voie aérienne supérieure, le modèle du poumon également prend son importance en particulier pour les évaluations des ventilateurs. Parmi les publications mentionnées plus haut, trois types des modèles du poumon ont été appliqués : poumon de test Michigan (Training and Test Lung, Michigan Instrument, Grand Rapids, Michigan) (Abdenbi, Chambille, and Escourrou 2004; Coller, Stanley, and Parthasarathy 2005; Lofaso et al. 2006; Hirose et al. 2008), piston piloté par l’ordinateur qui simplement reproduit le débit du patient (Farré et al. 2002; Rigau et al. 2006), et poumon actif plus sophistiqué qui prend en compte de la résistance et la compliance (T. Netzel, Hein, and Hein 2014).
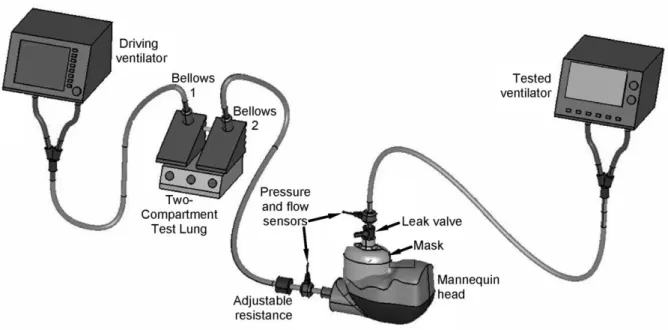
Le poumon Michigan est un modèle mécanique qui contient deux soufflets. L’un des soufflets (maître) est connecté à un ventilateur pilote et simule les activités du muscle respiratoire du patient. L’autre (esclave) est connecté à la machine de ventilation à évaluer (Figure 2-1). Les propriétés du poumon sont réglées de manière mécanique, par exemple la compliance du système est réglée par la position d’un ressort sur le soufflet. Cela pourrait entrainer la variabilité dans les résultats du test. De plus, ce système n’est pas conçu pour simuler des respirations complexes et caractériser l’effort respiratoire du patient.
Figure 2-1 Exemple du banc d’essai avec poumon de test Michigan pour l’évaluation des ventilateurs (Chatburn 2009)
Le piston du débit piloté par l’ordinateur peut reproduire la forme de débit du patient de façon précise, et nous permet d’étudier la réaction de machine de ventilation en réponse à des patterns respiratoires spécifiques. Cependant le système est en boucle ouverte et ne répond pas aux ventilateurs
testées. Le modèle que Netzel et al. ont développé et utilisé dans leur étude correspond à un poumon actif qui permet d’ajuster les propriétés mécaniques et de paramétrer les cycles de respiration. D’après la description, leur système fonctionne en boucle fermée. Cependant, les détails sur les principes de fonctionnement ne sont pas clairs (D.-I. T. Netzel et al. 2009).
2.2 Banc d’essai associé à cette thèse
Le banc d’essai (Figure 2-2) est capable de produire la respiration normale ou des séquences de respiration pathologique, en tenant en compte à la fois de l’état des VAS, la commande centrale, et des propriétés du système thoraco-pulmonaire. Ce modèle fonctionne en boucle fermée de la réponse à l’appareil ventilatoire à tester.
Notre banc d’essai est principalement composé d’un poumon actif ASL5000 (Ingmar Medical, Pittsburgh, USA) et d’une résistance de Starling (Figure 2-2).
Figure 2-2 Photo du banc d’essai
2.2.1 Poumon actif ASL5000
Le poumon actif ASL 5000 correspond à un piston piloté par un ordinateur (Figure 2-3). Le volume est mesuré directement en temps réel par la position du piston. Le débit est calculé comme la dérivée du volume par rapport au temps. Dans ce modèle, le piston se déplace via une boucle fermée de la
pression dont la loi de contrôle est basée sur l’équation différentielle suivante (Chatburn 2009; IngMar Medical, Ltd. 2013):
Paw(t)+ΔPmus(t)=V(t)/C+R(dV(t)/dt) Equation 2-1
Où
Paw : la pression à la voie aérienne (la sortie du poumon actif);
Pmus : la pression des muscles respiratoires qui correspond à l’effort de malade ;
V : le volume ; C : la compliance ; R : la résistance.
Les valeurs de la R et C sont définies par l’utilisateur, et R peut en plus être définie indépendamment pour l’inspiration et l’expiration. Dans ce modèle, la compliance et la résistance sont simulées par la position et la vitesse du piston d’après les équations suivantes (Chatburn 2009; IngMar Medical, Ltd. 2013):
dV=C·dPaw Equation 2-2
dV/dt=dPaw/R Equation 2-3
Le modèle d’effort respiratoire du patient est caractérisé par le profil de la Pmus qui est une fonction
du temps. Ce modèle permet à l’utilisateur de personnaliser l’effort respiratoire de chaque cycle d’une séquence de respiration active. Si la Pmus est réglée à 0, le poumon est en mode passif. Il faut noter que
lorsque la sortie est obstruée, la Paw générée sera identique à la Pmus.
Le système peut fonctionner aussi en mode Flow Pump qui reproduit un débit demandé (SmartPumpTM mode). Avec ce mode, le système fonctionne en boucle ouverte et le feedback de pression est ignoré, i.e., le modèle perd alors les réglages des propriétés comme la résistance et la compliance.
Figure 2-3 Principe du fonctionnement du poumon actif ASL 5000 (IngMar Medical, Ltd. 2013)
En clinique, lors d’une apnée obstructive, l’effort inspiratoire contre une VAS fermée peut entrainer une pression intrathoracique très négative qui peut atteindre -80 cmH2O (Shamsuzzaman
AM, Gersh BJ, and Somers VK 2003). Vu que le poumon actif génère une pression qui égale la Pmus
lorsque les VAS sont fermées, et que cette pression n’est pas suffisante pour générer une dépression intrathoracique importante, dans nos essais l’ASL 5000 est donc configuré en Flow Pump pendant les événements obstructifs. Dans ce cas là, le piston de l’ASL 5000 est piloté en débit d’une respiration normale en boucle ouverte, et donc capable de générer une pression négative très importante (<-70 cmH2O) à chaque inspiration en aval de la VAS fermée.
2.2.2 Résistance de Starling
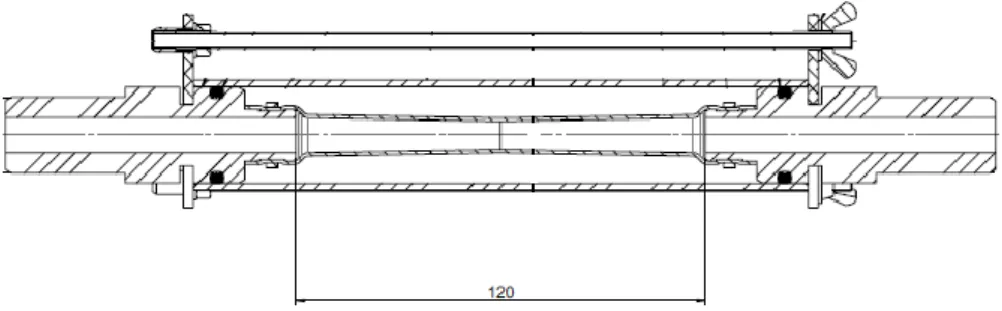
Les VAS peuvent être simulées par une résistance de Starling (A. R. Schwartz et al. 1988; P. L. Smith et al. 1988; Gleadhill et al. 1991; Gold and Schwartz 1996). La résistance de Starling est composée d’un tube souple monté dans une chambre hermétique remplie d’air, et ce tube possède une coupe transversale plate (Figure 2-2). Ce tube collabable de 120 mm de long est interposé entre les
deux embouts de Φ15 mm. Les caractéristiques de la résistance de Starling sont présentées dans la partie discussion (Figure 2-4).
Figure 2-4- Coupe transversale de la résistance de Starling.
A l’intérieur de l’enceinte de la résistance de Starling, un tube caoutchouc de 120 mm de long est interposé entre les deux embouts faisant 15 mm de diamètre.
2.2.3 Simulation du ronflement
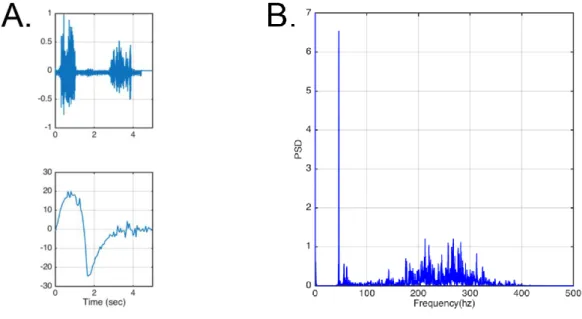
Le ronflement est un son généré par la vibration du voile du palais et des parois pharyngées. Il est un signe important du SAHOS. Le son du ronflement a été caractérisé par des fréquences acoustiques spécifiques de 5 à 136 Hz (Ayappa and Rapoport 2003).
Sur le banc d’essai, le ronflement est produit par une enceinte Bluetooth (UE984-000298, Logitech) qui se situe dans une chambre hermétique connectée au masque (Figure 2-2). Le son du ronflement est extrait d’un enregistrement de patient et correspond à un cycle de respiration. Ce son est déclenché à l’inspiration et persiste pendant l’inspiration ainsi qu’expiration (Figure 2-5-A). De plus, le son est filtré par un filtre passe-bas (Fréquence de coupure = 100 Hz) afin d’enlever les hautes fréquences du spectre. Figure 2-5-B représente la densité spectrale de puissance (DSP) finale. Le pic du spectre est à 46 Hz.
Figure 2-5 Le signal du ronflement avec le spectre de fréquence.
A. En haut : le signal du ronflement ; En bas : le débit résultant. B. La DSP du signal du ronflement après
Chapitre 3 Résultats
Ce chapitre est réparti en quatre volets, correspondant aux quatre travaux principaux réalisés au cours de ma thèse.
Le premier travail avait comme objectif d’évaluer et de comparer onze machines PPC auto-pilotée disponibles sur le marché. Les résultats obtenus nous ont montré que ces machines ne sont pas équivalentes pour le traitement des troubles respiratoires du sommeil (Article 1 JCSM 2015). Dans la continuité de ce premier projet, le second travail a consisté à comprendre les principes des modes confort patient implantés dans les machines PPC, et connaître leur impact sur le traitement des apnées obstructives (Article 2 accepté dans JCSM 2015). Le troisième consistait à évaluer trois machines de ventilation auto-asservie, et à comprendre leurs différentes caractéristiques en réponse à des anomalies respiratoires (Article 3 JCSM 2013).
3.1 Evaluation des onze machines de ventilation en PPC autopilotée sur un
banc d’essai
3.1.1 Introduction
Une méta-analyse récente montre un gain limité sur le temps d’utilisation de 0,2h/nuit pour la PPC autopilotée par rapport à la PPC fixe (I. Smith and Lasserson 2009). Plusieurs études cliniques montrent que cette limite peut être liée à un fonctionnement inadéquat de certaines PPC autopilotée et leurs efficacité thérapeutique a été questionnée par certaines études (Rodenstein 2008; Alan T. Mulgrew et al. 2010; Ueno et al. 2010; Denotti et al. 2012). Ces appareils fonctionnent suivant des principes différents, en raison de leurs algorithmes qui sont souvent inaccessibles et protégés par les fabricants.
Les appareils fournissent un rapport dans lequel figurent le temps d’utilisation et les détails du traitement comme la pression thérapeutique et l’IAH résiduel. Ce rapport est souvent utilisé par les cliniciens pour évaluer l’efficacité du traitement. Cependant la précision et la fiabilité de ces données ne sont pas connues et ont été évaluées par plusieurs études cliniques (Desai et al. 2009; Ueno et al. 2010; Denotti et al. 2012; Ikeda et al. 2012; Berry et al. 2012; Cilli, Uzun, and Bilge 2013; Nigro et al. 2014; Li et al. 2015).
L’objectif est de déterminer si les appareils PPC autopilotée sont efficaces pour éliminer les événements respiratoires du sommeil simulés sur notre banc d’essai, et si les performances thérapeutiques de ces appareils sont similaires ? Dans la continuité des évaluations cliniques, nous voudrions savoir si les données enregistrées des appareils surtout l’IAH sont concordantes avec les données estimées à partir des mesures du banc d’essai.
3.1.2 Article 1
All APAPs Are Not Equivalent for the Treatment of Sleep Disordered Breathing : A Bench Evaluation of Eleven Commercially Available Devices
Kaixian Zhu, Gabriel Roisman, Sami Aouf et Pierre Escourrou
3.1.3 Résumé de l’article 1
Dans cette étude, nous avons évalué onze PPC autopilotée avec un nouveau banc d’essai, qui est principalement composé d’un poumon actif et d’une résistance Starling. Ce banc permet de tester les appareils de traitement ventilatoire en boucle fermée au niveau non seulement de la voie aérienne supérieure, mais aussi du poumon.
Les appareils ont été testés sur deux protocoles différents : i) séquences courtes d’événements respiratoires spécifiques, i.e., apnées obstructives et centrales, hypopnées et ronflements; ii) deux scénarios généraux qui se rapprochent plus des conditions cliniques : l’un dure 95 minutes qui correspond à un cycle du sommeil, et l’autre dure 6 heures qui correspond à une nuit complète du sommeil. Dans ces deux scénarios, tous les types d’événement respiratoire ont été intégrés. L’évaluation a porté sur la performance thérapeutique et la précision des données fournies dans le rapport de l’appareil.
Les principaux résultats sont les suivants : i) la majorité des appareils testés a répondu aux apnées et hypopnées obstructives. Cependant, le temps de réaction et le débit résultant étaient différents. Certains appareils n’ont pas répondu qu’avec l’ajout des signaux spécifiques ; ii) Cinq appareils ont répondu aux ronflements ; iii) Quatre appareils n’ont pas monté en pression sur les apnées centrales ; iv) pour le scénario de 6 heures, l’efficacité du traitement était très différente d’un appareil à un autre. Cinq appareils ont réussi à diminuer IAH résiduel à un niveau inférieur à 5/h. v) pour le scénario de 95 minutes, seulement deux appareils ont réussi à réduire l’IAH à un niveau inférieur à 5/h, et les IAH fournis dans les rapports des appareils étaient différents de ceux estimés du banc d’essai : trois appareils ont sous-estimé cet index de >10%.
A partir de ces résultats, nous avons montré que les appareils PPC autopilotées ne sont pas équivalents pour l’efficacité du traitement et la précision des données du rapport. Chaque appareil répond à un profil patient particulier selon les types d’événements qu’il présente.
3.2 Evaluation des modes de confort aux appareils PPC sur un banc d’essai
3.2.1 Introduction
La PPC est le traitement de référence pour le SAHOS, cependant l’efficacité de ce traitement dépend d’utilisation régulière des machines par le patient. La difficulté à tolérer la pression délivrée par l’appareil PPC est l’un des facteurs les plus importants qui puissent affecter la compliance au traitement du patient (Weaver and Grunstein 2008; G. K. Shapiro and Shapiro 2010; Wickwire et al. 2013).
De ce fait, différentes modalités pour délivrer la pression ont été développées, dont l’une consiste à diminuer la pression pendant l’expiration afin de faciliter l’expiration du patient et d’améliorer la compliance. A partir de ce principe, les fabricants d’appareil de PPC ont développé des variantes de cette fonction et ont implanté leurs propres versions dans leurs appareils. En pratique, ce mode de confort est souvent rajouté pendant le traitement lorsque le patient se plaint de la pression excessive après la titration manuelle ou automatique.
Néanmoins, le bénéfice de cette modalité sur la compliance au traitement n’est pas concordant dans la littérature (Aloia et al. 2005; Nilius et al. 2006; A. T. Mulgrew et al. 2006; Kakkar and Berry 2007; Marshall, Neill, and Campbell 2008; J.-L. Pépin et al. 2009; J. Bakker, Campbell, and Neill 2010; Chihara et al. 2013; Brown 2011). De plus, l’impact de ces fonctions de confort sur l’efficacité de traitement n’est pas clair (Wickwire et al. 2013; J. P. Bakker and Marshall 2011).
Dans ce travail, nous nous posons la question de savoir si les modes confort patient pourraient changer l’efficacité du traitement du SAHOS par PPC fixe et autopilotée.
3.2.2 Article 2
Pressure-Relief Features of Fixed- and Auto-Titrating CPAP may Impair Their Efficacy : Evaluation with a Respiratory Bench Model
Kaixian Zhu, Sami Aouf, Gabriel Roisman et Pierre Escourrou
Manuscrit accepté pour publication dans la revue Journal of Clinical Sleep Medicine le 6 Octobre 2015
Title: Pressure-relief features of fixed- and auto-titrating CPAP may impair their efficacy: Evaluation 1
with a respiratory bench model 2
3
Authors: Kaixian Zhu, M.S.1,2,3; Sami Aouf, M.D.1; Gabriel Roisman, M.D., Ph.D.2; Pierre Escourrou, 4
M.D., Ph.D.2,3 5
6
1. Air Liquide Healthcare, Gentilly, France; 7
2. Sleep Disorders Center, AP-HP Antoine-Béclère Hospital, Clamart, France; 8
3. EA3544, Faculty of Pharmacy, Paris-Sud University, Châtenay-Malabry, France. 9
10
Subtitle: CPAP treatment efficacy with pressure-relief features 11
12
Correspondence to: Kaixian Zhu, Air Liquide Healthcare, 28 Rue d’Arcueil, 94250 Gentilly, France. 13
Tel : +33 1 49 69 45 67 ; Email: kaixian.zhu@airliquide.com 14
15
Disclosure statement: 16
This was not an industry supported study. This research was supported by a CIFRE grant to K.Zhu, 17
from the French Ministry of Higher Education and Research. The authors have indicated no financial 18
conflicts of interest. 19
20 21
Abstract
1Study objectives: Pressure-relief features are aimed at improving the patient’s comfort during CPAP 2
treatment for obstructive sleep apnea. The objective of this study was to determine the impact of these 3
therapy features on fixed-CPAP and auto-titrating CPAP (APAP) treatment efficacy. 4
Methods: Seven pressure-relief features applied by three CPAP devices were included in our study 5
(Remstar Auto: C-Flex 3, C-Flex+ 3, A-Flex 3, P-Flex; AirSense 10: EPR 3; Prisma 20A: SoftPAP 2 6
and 3). In fixed-CPAP, the devices were subjected to a 10-minute bench-simulated obstructive apnea 7
sequence (initial apnea-hypopnea index, AHI=60/h) with and without pressure-relief features. In 8
APAP, the sequence was lengthened to 4.2 hours (initial AHI=58.6/h). The residual AHI and 9
mean/median pressure were compared with and without pressure-relief features. 10
Results: Compared to conventional CPAP, where pressure was adjusted to be just sufficient to control 11
the simulated obstructive events, C-Flex+ 3, P-Flex and EPR 3 failed normalize the breathing flow and 12
did not reduce the AHI. The mean pressures with the three features were 1.8, 2.6 and 2.6 cmH2O
13
respectively lower than the conventional CPAP. Compared to conventional APAP, similar levels of 14
control were observed with pressure-relief features, apart from P-Flex where the delivered mean 15
pressure was lower and residual AHI greater. The device-reported mean/median pressures in APAP 16
with A-Flex 3, P-Flex, EPR 3 and SoftPAP 3 were higher than that measured on the bench. 17
Conclusions: Pressure-relief features may attenuate CPAP efficacy if not adjusted for at the time of 18
their introduction. In clinical practice, efficacy can be ensured by increasing the therapeutic pressure 19
delivered by fixed-CPAP or by enabling the pressure-relief features prior to initial pressure titration. 20
Device-reported pressures in APAP devices with pressure relief activated may overstate delivered 21
pressures. 22
23
Key words:
CPAP, Pressure-relief features, Bench test. 2425
Brief Summary
26Current knowledge/Study rationale: Pressure-relief features are aimed at improving the patient’s 27
comfort during CPAP treatment for OSA. However, the effect of these therapy features on CPAP 28
treatment efficacy is not well determined. 29
Study impact: Pressure-relief features may impair the efficacy of CPAP treatment. The treatment 30
efficacy can be ensured by increasing the therapeutic pressure or by enabling the pressure-relief 31
features prior to initial pressure titration. 32
Introduction
1Continuous positive airway pressure (CPAP) is an effective treatment for obstructive sleep apnea 2
(OSA). However, the effectiveness of treatment mainly depends on regular use of CPAP device and 3
patient’s tolerance to the treatment. Many factors are involved in CPAP adherence: side effects related 4
to the equipment such as nasal discomfort and difficulty adapting to the pressure, disease severity, 5
patient characteristics and motivation, and other surrounding factors, such as family, physician, 6
healthcare professionals and their interventions. 1–3 7
One side effect of CPAP treatment is the difficulty of exhaling against a positive pressure which is 8
considered as a cause of reduced adherence to CPAP. As a solution, various CPAP delivery modalities 9
have been developed on the basis that a lower expiratory pressure would be better tolerated. Auto-10
titrating CPAP (APAP) adjusts the pressure and maintains the airway patency in real time during the 11
therapy, and the adherence of APAP has been reported as same as that of conventional CPAP. 4 12
Bilevel PAP is designed to provide a lower expiratory pressure to reduce the average pressure level, 13
while no improvement in adherence has been reported. 4–7 Pressure-relief CPAP is another modality of 14
pressure delivery, which is proposed as an optional therapy feature for patient’s comfort during the 15
treatment and has been implemented in most fixed-CPAP or APAP devices. This CPAP modality is 16
aimed at reducing pressure during expiration to facilitate patient exhalation. 17
Currently, almost all CPAP manufacturers provide their own proprietary versions of pressure-relief 18
CPAP. However, there is no instruction or caution from the manufacturers regarding the use of these 19
features, which are often added after the initial titration when the patient complains of excessive 20
pressure. Besides, the majority of studies on such therapy feature are restricted to C-Flex (Philips 21
Respironics,
Murrysville, USA
), and the literature does not consistently support its usefulness. 8–16 22For other pressure-relief features available on the market, the additional benefits still remain unclear. 23
3,17
24
Bench studies have been proposed to evaluate the responses of APAP devices in different conditions, 25
such as the presence of predefined sleep-disordered breathing (SDB) patterns and air leak, 18–25 while 26
no such study to date has focused on pressure-relief CPAPs and APAPs. We investigated seven 27
pressure-relief features developed by three CPAP device manufacturers with a previously reported 28
bench model. 25 29
Methods
1- Bench model and simulation of obstructive apneas 2
Evaluations were carried out on a previously described bench model. 25 Consisting of an active lung 3
model and a Starling resistor, the bench model is able to simulate different SDB patterns such as 4
obstructive apneas, hypopneas and flow limitations. The human upper airway is mimicked by the 5
Starling resistor, and the control of airway patency can be achieved by adjusting the pressure inside 6
the resistor. The CPAP device and the bench are connected by a standard tubing (1.8 meter long and 7
22 mm diameter), and a calibrated leak port (24 L/min at 10 cmH2O) is presented in order to mimic
8
the intentional leak in nasal masks. Mask pressure (Pm) and airflow (V’) are recorded for further
9
analyses. 10
During obstructive apnea simulation, the breathing effort is generated by the piston movement. The 11
pressure inside the Starling resistor is set at 9 cmH2O, and the critical closing and full opening
12
pressures were measured at around 6 and 11 cmH2O, respectively.
13
- Studied pressure-relief features 14
Three CPAP devices were included in the current study: Remstar Auto P-Flex (Philips Respironics), 15
AirSense 10 AutoSet (Resmed, Sydney, Australia) and Prisma 20A (Weinmann, Hamburg, Germany). 16
Studied pressure-relief features and their principles are shown in Table 1. During the test, each feature 17
was set at the maximum level if adjustable, i.e., achieving the maximally reduced pressure during 18
expiration. 19
- Pressure-relief CPAP/APAP efficacy 20
i. Protocol 21
Fixed-CPAP: With simulated apneas, a manual titration of pressure was firstly conducted to obtain 22
the therapeutic pressure for each CPAP device with pressure-relief features disabled (conventional 23
CPAP): the pressure was increased from 4 cmH2O in a stepwise manner with a minimum increment
24
(0.5 cmH2O for Remstar Auto and Prisma 20A, 0.2 cmH2O for AirSense 10 AutoSet) until the
25
breathing flow was fully normalized. Afterwards, the devices were set at obtained titration pressure, 26
and subjected to a predefined short obstructive apnea sequence with pressure-relief features enabled. 27
The short breathing sequence lasted 10 minutes, which was considered sufficient since fixed-CPAP 28
efficacy is time-independent. A 30-second obstructive apnea occurred every minute, i.e., total Apnea-29
Hypopnea Index (AHI) =60/h. A similar reference test was carried out without pressure-relief feature 30
(conventional CPAP) for each device. Tests were repeated twice for reproducibility. A third test was 31
executed if the coefficient of variance of the first two tests was higher than 10%. 32
APAP: The devices were set to APAP mode with open pressure range (4-20 cmH2O), and subjected to
33
a long obstructive apneas sequence with pressure-relief features enabled. The long breathing sequence 34