HAL Id: dumas-02014486
https://dumas.ccsd.cnrs.fr/dumas-02014486
Submitted on 11 Feb 2019HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Les médecins généralistes haut-normands proposent-ils
le dispositif intra-utérin à leurs patientes nullipares ?
Soline Manzo
To cite this version:
Soline Manzo. Les médecins généralistes haut-normands proposent-ils le dispositif intra-utérin à leurs patientes nullipares ?. Médecine humaine et pathologie. 2018. �dumas-02014486�
FACULTE MIXTE DE MEDECINE ET DE PHARMACIE DE ROUEN
Année 2018
N°
THESE
pour le DOCTORAT EN MEDECINE
(Diplôme d’Etat)
Par
Soline MANZO
Né(e) le 09/04/1986 à Clermont-Ferrand
Présentée et soutenue publiquement le 06 Décembre 2018
Les médecins généralistes haut-normands
proposent-ils le dispositif intra-utérin à leurs patientes
nullipares ?
Président du jury : Madame le Professeur Véronique MERLE
Membres du jury : Madame le Professeur Elisabeth MAUVIARD
Monsieur le Docteur Emmanuel HAZARD
Directeur de thèse : Madame le Docteur Janick LEFEBVRE
2
Par délibération en date du 3 Mars 1967, la faculté a arrêté que les
opinions émises dans les dissertations qui lui seront présentées
doivent être considérées comme propres à leurs auteurs et qu’elle
n’entend leur donner aucune approbation ni improbation.
3
ANNEE UNIVERSITAIRE 2017 - 2018 U.F.R. SANTÉ DE ROUEN
--- DOYEN :
Professeur Pierre FREGER
ASSESSEURS : Professeur Michel GUERBET
Professeur Benoit VEBER
Professeur Pascal JOLY
Professeur Stéphane MARRET
I - MEDECINE
PROFESSEURS DES UNIVERSITES – PRATICIENS HOSPITALIERS
Mr Frédéric ANSELME HCN Cardiologie
Mme Gisèle APTER Havre Pédopsychiatrie
Mme Isabelle AUQUIT AUCKBUR HCN Chirurgie plastique
Mr Fabrice BAUER HCN Cardiologie
Mme Soumeya BEKRI HCN Biochimie et biologie moléculaire
Mr Ygal BENHAMOU HCN Médecine interne
Mr Jacques BENICHOU HCN Bio statistiques et informatique médicale
Mr Olivier BOYER UFR Immunologie
Mme Sophie CANDON HCN Immunologie
Mr François CARON HCN Maladies infectieuses et tropicales
Mr Philippe CHASSAGNE (détachement) HCN Médecine interne (gériatrie) – Détachement
Mr Vincent COMPERE HCN Anesthésiologie et réanimation chirurgicale
Mr Jean-Nicolas CORNU HCN Urologie
Mr Antoine CUVELIER HB Pneumologie
Mr Pierre CZERNICHOW (surnombre) HCH Epidémiologie, économie de la santé
Mr Jean-Nicolas DACHER HCN Radiologie et imagerie médicale
Mr Stéfan DARMONI HCN Informatique médicale et techniques de
4
Mr Pierre DECHELOTTE HCN Nutrition
Mr Stéphane DERREY HCN Neurochirurgie
Mr Frédéric DI FIORE CB Cancérologie
Mr Fabien DOGUET HCN Chirurgie Cardio Vasculaire
Mr Jean DOUCET SJ Thérapeutique - Médecine interne et gériatrie
Mr Bernard DUBRAY CB Radiothérapie
Mr Philippe DUCROTTE HCN Hépato-gastro-entérologie
Mr Frank DUJARDIN HCN Chirurgie orthopédique - Traumatologique
Mr Fabrice DUPARC HCN Anatomie - Chirurgie orthopédique et
traumatologique
Mr Eric DURAND HCN Cardiologie
Mr Bertrand DUREUIL HCN Anesthésiologie et réanimation chirurgicale
Mme Hélène ELTCHANINOFF HCN Cardiologie
Mr Manuel ETIENNE HCN Maladies infectieuses et tropicales
Mr Thierry FREBOURG UFR Génétique
Mr Pierre FREGER HCN Anatomie - Neurochirurgie
Mr Jean François GEHANNO HCN Médecine et santé au travail
Mr Emmanuel GERARDIN HCN Imagerie médicale
Mme Priscille GERARDIN HCN Pédopsychiatrie
M. Guillaume GOURCEROL HCN Physiologie
Mr Dominique GUERROT HCN Néphrologie
Mr Olivier GUILLIN HCN Psychiatrie Adultes
Mr Didier HANNEQUIN HCN Neurologie
Mr Fabrice JARDIN CB Hématologie
Mr Luc-Marie JOLY HCN Médecine d’urgence
Mr Pascal JOLY HCN Dermato – Vénéréologie
Mme Bouchra LAMIA Havre Pneumologie
Mme Annie LAQUERRIERE HCN Anatomie et cytologie pathologiques
Mr Vincent LAUDENBACH HCN Anesthésie et réanimation chirurgicale
Mr Joël LECHEVALLIER HCN Chirurgie infantile
Mr Hervé LEFEBVRE HB Endocrinologie et maladies métaboliques
Mr Thierry LEQUERRE HB Rhumatologie
Mme Anne-Marie LEROI HCN Physiologie
Mr Hervé LEVESQUE HB Médecine interne
Mme Agnès LIARD-ZMUDA HCN Chirurgie Infantile
5
Mr Bertrand MACE HCN Histologie, embryologie, cytogénétique
M. David MALTETE HCN Neurologie
Mr Christophe MARGUET HCN Pédiatrie
Mme Isabelle MARIE HB Médecine interne
Mr Jean-Paul MARIE HCN Oto-rhino-laryngologie
Mr Loïc MARPEAU HCN Gynécologie - Obstétrique
Mr Stéphane MARRET HCN Pédiatrie
Mme Véronique MERLE HCN Epidémiologie
Mr Pierre MICHEL HCN Hépato-gastro-entérologie
M. Benoit MISSET HCN Réanimation Médicale
Mr Jean-François MUIR (surnombre) HB Pneumologie
Mr Marc MURAINE HCN Ophtalmologie
Mr Philippe MUSETTE HCN Dermatologie - Vénéréologie
Mr Christophe PEILLON HCN Chirurgie générale
Mr Christian PFISTER HCN Urologie
Mr Jean-Christophe PLANTIER HCN Bactériologie - Virologie
Mr Didier PLISSONNIER HCN Chirurgie vasculaire
Mr Gaëtan PREVOST HCN Endocrinologie
Mr Jean-Christophe RICHARD
(détachement) HCN Réanimation médicale - Médecine d’urgence
Mr Vincent RICHARD UFR Pharmacologie
Mme Nathalie RIVES HCN Biologie du développement et de la
reproduction
Mr Horace ROMAN HCN Gynécologie - Obstétrique
Mr Jean-Christophe SABOURIN HCN Anatomie - Pathologie
Mr Guillaume SAVOYE HCN Hépato-gastrologie
Mme Céline SAVOYE–COLLET HCN Imagerie médicale
Mme Pascale SCHNEIDER HCN Pédiatrie
Mr Michel SCOTTE HCN Chirurgie digestive
Mme Fabienne TAMION HCN Thérapeutique
Mr Luc THIBERVILLE HCN Pneumologie
Mr Christian THUILLEZ (surnombre) HB Pharmacologie
Mr Hervé TILLY CB Hématologie et transfusion
M. Gilles TOURNEL HCN Médecine Légale
Mr Olivier TROST HCN Chirurgie Maxillo-Faciale
Mr Jean-Jacques TUECH HCN Chirurgie digestive
6
Mr Benoît VEBER HCN Anesthésiologie - Réanimation
chirurgicale
Mr Pierre VERA CB Biophysique et traitement de l’image
Mr Eric VERIN HB Service Santé Réadaptation
Mr Eric VERSPYCK HCN Gynécologie obstétrique
Mr Olivier VITTECOQ HB Rhumatologie
Mme Marie-Laure WELTER HCN Physiologie
MAITRES DE CONFERENCES DES UNIVERSITES – PRATICIENS HOSPITALIERS
Mme Noëlle BARBIER-FREBOURG HCN Bactériologie – Virologie
Mme Carole BRASSE LAGNEL HCN Biochimie
Mme Valérie BRIDOUX HUYBRECHTS HCN Chirurgie Vasculaire
Mr Gérard BUCHONNET HCN Hématologie
Mme Mireille CASTANET HCN Pédiatrie
Mme Nathalie CHASTAN HCN Neurophysiologie
Mme Sophie CLAEYSSENS HCN Biochimie et biologie
moléculaire
Mr Moïse COEFFIER HCN Nutrition
Mr Serge JACQUOT UFR Immunologie
Mr Joël LADNER HCN Epidémiologie, économie de la
santé
Mr Jean-Baptiste LATOUCHE UFR Biologie cellulaire
Mr Thomas MOUREZ HCN Virologie
Mr Gaël NICOLAS HCN Génétique
Mme Muriel QUILLARD HCN Biochimie et biologie
moléculaire
Mme Laëtitia ROLLIN HCN Médecine du Travail
Mr Mathieu SALAUN HCN Pneumologie
Mme Pascale SAUGIER-VEBER HCN Génétique
Mme Anne-Claire TOBENAS-DUJARDIN HCN Anatomie
Mr David WALLON
PROFESSEUR AGREGE OU CERTIFIE
HCN Neurologie
Mr Thierry WABLE UFR Communication
7
II - PHARMACIE
PROFESSEURS
Mr Thierry BESSON Chimie Thérapeutique
Mr Roland CAPRON (PU-PH) Biophysique
Mr Jean COSTENTIN (Professeur émérite) Pharmacologie
Mme Isabelle DUBUS Biochimie
Mr Loïc FAVENNEC (PU-PH) Parasitologie
Mr Jean Pierre GOULLE (Professeur
émérite) Toxicologie
Mr Michel GUERBET Toxicologie
Mme Isabelle LEROUX - NICOLLET Physiologie
Mme Christelle MONTEIL Toxicologie
Mme Martine PESTEL-CARON (PU-PH) Microbiologie
Mr Rémi VARIN (PU-PH) Pharmacie clinique
Mr Jean-Marie VAUGEOIS Pharmacologie
Mr Philippe VERITE
MAITRES DE CONFERENCES
Chimie analytique
Mme Cécile BARBOT Chimie Générale et Minérale
Mr Jérémy BELLIEN (MCU-PH) Pharmacologie
Mr Frédéric BOUNOURE Pharmacie Galénique
Mr Abdeslam CHAGRAOUI Physiologie
Mme Camille CHARBONNIER (LE CLEZIO) Statistiques
Mme Elizabeth CHOSSON Botanique
Mme Marie Catherine CONCE-CHEMTOB Législation pharmaceutique et économie de la santé
Mme Cécile CORBIERE Biochimie
Mr Eric DITTMAR Biophysique
Mme Nathalie DOURMAP Pharmacologie
Mme Isabelle DUBUC Pharmacologie
8
Mr Abdelhakim ELOMRI Pharmacognosie
Mr François ESTOUR Chimie Organique
Mr Gilles GARGALA (MCU-PH) Parasitologie
Mme Nejla EL GHARBI-HAMZA Chimie analytique Mme Marie-Laure GROULT Botanique
Mr Hervé HUE Biophysique et mathématiques Mme Laetitia LE GOFF Parasitologie – Immunologie
Mme Hong LU Biologie
M. Jérémie MARTINET (MCU-PH) Immunologie Mme Marine MALLETER Toxicologie Mme Sabine MENAGER Chimie organique Mme Tiphaine ROGEZ-FLORENT Chimie analytique Mr Mohamed SKIBA Pharmacie galénique Mme Malika SKIBA Pharmacie galénique Mme Christine THARASSE Chimie thérapeutique Mr Frédéric ZIEGLER Biochimie
PROFESSEURS ASSOCIES
Mme Cécile GUERARD-DETUNCQ Pharmacie officinale
Mr Jean-François HOUIVET Pharmacie officinale
PROFESSEUR CERTIFIE
Mme Mathilde GUERIN Anglais
ASSISTANT HOSPITALO-UNIVERSITAIRE
Mme Anaïs SOARES Bactériologie
ATTACHES TEMPORAIRES D’ENSEIGNEMENT ET DE RECHERCHE
Mme Anne-Sophie CHAMPY Pharmacognosie
M. Jonathan HEDOUIN Chimie Organique
Mme Barbara LAMY-PELLETER Pharmacie Galénique
9
LISTE DES RESPONSABLES DES DISCIPLINES
PHARMACEUTIQUES
Mme Cécile BARBOT Chimie Générale et minérale
Mr Thierry BESSON Chimie thérapeutique
Mr Roland CAPRON Biophysique
Mme Marie-Catherine CONCE-CHEMTOB Législation et économie de la santé
Mme Elisabeth CHOSSON Botanique
Mme Isabelle DUBUS Biochimie
Mr Abdelhakim ELOMRI Pharmacognosie
Mr Loïc FAVENNEC Parasitologie
Mr Michel GUERBET Toxicologie
Mr François ESTOUR Chimie organique
Mme Isabelle LEROUX-NICOLLET Physiologie
Mme Martine PESTEL-CARON Microbiologie
Mr Mohamed SKIBA Pharmacie galénique
Mr Rémi VARIN Pharmacie clinique
Mr Philippe VERITE Chimie analytique
10
III – MEDECINE GENERALE
PROFESSEUR Mr Jean-Loup HERMIL (PH-PH) MAITRE DE CONFERENCE
UFR Médecine générale
Mr Matthieu SCHUERS (MCU-PH) UFR Médecine générale
PROFESSEURS ASSOCIES A MI-TEMPS – MEDECINS GENERALISTE
Mr Emmanuel LEFEBVRE UFR Médecine Générale
Mme Elisabeth MAUVIARD UFR Médecine générale
Mr Philippe NGUYEN THANH UFR Médecine générale Mme Marie Thérèse THUEUX UFR Médecine générale
MAITRE DE CONFERENCES ASSOCIE A MI-TEMPS – MEDECINS GENERALISTES
Mr Pascal BOULET UFR Médecine générale
Mr Emmanuel HAZARD UFR Médecine Générale
Mme Marianne LAINE UFR Médecine Générale
Mme Lucile PELLERIN UFR Médecine générale
Mme Yveline SEVRIN UFR Médecine générale
11
ENSEIGNANTS MONO-APPARTENANTS
PROFESSEURS
Mr Serguei FETISSOV (med) Physiologie (ADEN)
Mr Paul MULDER (phar) Sciences du Médicament
Mme Su RUAN (med) Génie Informatique
MAITRES DE CONFERENCES
Mr Sahil ADRIOUCH (med) Biochimie et biologie moléculaire (Unité Inserm 905) Mme Gaëlle BOUGEARD-DENOYELLE (med) Biochimie et biologie moléculaire (UMR 1079) Mme Carine CLEREN (med) Neurosciences (Néovasc)
M. Sylvain FRAINEAU (med) Physiologie (Inserm U 1096)
Mme Pascaline GAILDRAT (med) Génétique moléculaire humaine (UMR 1079)
Mr Nicolas GUEROUT (med) Chirurgie Expérimentale Mme Rachel LETELLIER (med) Physiologie
Mme Christine RONDANINO (med) Physiologie de la reproduction
Mr Antoine OUVRARD-PASCAUD (med) Physiologie (Unité Inserm 1076)
Mr Frédéric PASQUET Sciences du langage, orthophonie
Mme Isabelle TOURNIER (med) Biochimie (UMR 1079)
CHEF DES SERVICES ADMINISTRATIFS : Mme Véronique DELAFONTAINE
HCN - Hôpital Charles Nicolle HB - Hôpital de BOIS GUILLAUME
CB - Centre Henri Becquerel CHS - Centre Hospitalier Spécialisé du Rouvray CRMPR - Centre Régional de Médecine Physique et de Réadaptation SJ – Saint Julien Rouen
12
REMERCIEMENTS
A Madame le Professeur Véronique MERLE, Professeur d’Epidémiologie et de Santé Publique
Nous sommes très sensibles à l’honneur que vous nous faites en acceptant de présider ce jury de thèse,
C’est avec un profond respect que nous vous exprimons nos remerciements.
A Madame le Professeur Elisabeth MAUVIARD, Professeur Associé de Médecine Générale
Vous me faites l’honneur de juger ce travail, veuillez trouver ici l’expression de mes sincères remerciements et de mon profond respect.
A Monsieur le Docteur Emmanuel HAZARD,
Maître de Conférences Associé de Médecin Générale
Vous me faites l’honneur de juger ce travail, veuillez trouver ici l’expression de mes sincères remerciements et de mon profond respect.
A Madame le Docteur Janick LEFEBVRE, Docteur en Médecine Générale
13
Pour m’avoir accueillie, soutenue et encouragée durant mon SASPAS, avec votre mari le Docteur Emmanuel LEFEBVRE, me permettant de m’affirmer et de trouver enfin un mode d’exercice de la médecine générale qui me correspond,
Pour m’avoir montré le chemin de ma future pratique avec bienveillance, gentillesse et disponibilité,
Merci sincèrement.
A mes différents Maîtres de Stage et les services qu’ils représentent,
Du service de Médecine Polyvalente du CHI de Louviers (Docteur Yann POULINGUE) au Service de Gynécologie-Obstétrique d’Evreux (Docteur Elise MACHEVIN)
J’ai acquis grâce à vous un savoir médical polyvalent, une méthodologie rigoureuse, appris la prise en charge globale des patients et découvert mon intérêt pour la gynécologie.
Merci pour votre précieuse formation, pour vos conseils avisés et votre bienveillance.
Aux médecins du cabinet Paul Hélot, les Docteurs BOISDIN, LOUIS-CLEMENT, MARETTE-STEPOWSKI, GERMAIN, GONDRY et MARTINEZ (qui prend maintenant un repos bien mérité) ainsi qu’à leurs formidables secrétaires Frédérique et Sandrine,
Merci de m’avoir si bien accueillie au sein de votre cabinet, de m’avoir fait confiance et confié vos patients sans hésitation,
Merci de votre bonne humeur communicative,
14 A mes parents,
Je ne sais par où commencer…
Merci pour les sacrifices, l’investissement personnel et le soutien moral et matériel que vous nous avez porté tout au long de notre jeunesse (et tout au long de mes interminables études) dans l’unique intérêt de notre réussite,
Merci de m’avoir inculqué les valeurs fondamentales, l’altruisme et l’empathie, la persévérance et la combativité, me permettant d’affronter la vie d’adulte, d’être le médecin et la personne que suis aujourd’hui,
Merci pour votre présence indéfectible, Merci pour votre amour.
A mon frère,
Merci pour les fous rires, les souvenirs tout au long de notre enfance,
Merci de ta présence rassurante aujourd’hui, par ton calme et ton pragmatisme sans failles, ton écoute et ta bienveillance, tu sais m’apaiser et me tranquilliser.
Je vous aime.
A mes amies de toujours, Manelle et Sophie,
Même si la distance nous sépare, rien n’altérera l’importance que vous avez à mes yeux. Merci pour tous les fous rires, les moments partagés, votre oreille attentive à chaque instant. Merci d’avoir toujours été là, dans les bons comme dans les mauvais moments.
A mes amies « plus récentes »,
Olivia et Joanne, je suis heureuse d’avoir partagé toutes ces « galères médicales » avec vous. Elles m’ont permis de vous rencontrer et de vous compter aujourd’hui parmi mes amies précieuses. Merci pour tout le soutien apporté. (Merci à Jason pour son rire et sa « réassurance statistique »). Lucille, ma Lulu, ma confidente, ma statisticienne, une de mes plus belles rencontres rouennaises. Merci pour ces soirées entre filles. Merci d’être là chaque moment.
15
A tous mes coexternes et cointernes qui ont rendu les stages plus agréables tout au long de mon cursus médical, et qui sont devenus plus que de simples collègues de travail (Pierre, Marie L, Marie-Ca, Popo, Juliette, Camille, et j’en oublie…).
A mon Ange, mon Paul,
Merci de ton soutien, de ton aide quotidienne, de tes mots réconfortants, Merci de ton amour,
16
SOMMAIRE
GLOSSAIRE ... 20
INTRODUCTION ... 21
1. Description des populations étudiées ... 23
1.1. Les nullipares ... 23
1.1.1. Définition ... 23
1.1.2. Caractéristiques générales... 23
1.1.3. La couverture contraceptive des nullipares ... 24
1.2. La démographie médicale actuelle ... 25
1.2.1. La démographie médicale globale ... 25
1.2.2. La démographie des médecins généralistes ... 26
1.2.3. La démographie médicale des gynécologues ... 26
2. Les dispositifs intra-utérins ... 28
2.1. L’histoire du DIU ... 28
2.1.1. Les prémices de la contraception intra-utérine ... 28
2.1.2. Les DIU de première génération : les dispositifs en plastique ... 28
2.1.3. Les DIU de deuxième génération : les dispositifs au cuivre ... 29
2.1.4. Les DIU de troisième génération : les dispositifs hormonaux ... 29
2.2. Les caractéristiques communes aux DIU ... 30
2.2.1. Les indications communes ... 30
2.2.2. Les contre-indications communes ... 30
2.2.3. Les conditions d’insertion ... 31
2.2.4. Les prescriptions préalables ... 32
2.2.5. Les techniques de pose ... 33
2.2.6. Le suivi post-insertion ... 37
2.3. Les différents modèles de DIU ... 37
2.3.1. Les DIU au cuivre ... 37
2.3.1.1. Généralités ... 37
2.3.1.2. Mode d’action ... 38
2.3.1.3. Indications spécifiques ... 38
17
2.3.2. Les DIU au Lévonorgestrel ... 39
2.3.2.1. Généralités ... 39
2.3.2.2. Mode d’action ... 40
2.3.2.3. Indications spécifiques ... 41
2.3.2.4. Contre-indications et effets indésirables ... 41
2.4. Les complications des DIU ... 42
2.4.1. Grossesses extra et intra-utérines ... 42
2.4.2. Les maladies inflammatoires pelviennes ... 42
2.4.3. La difficulté d’insertion ... 44
2.4.4. L’expulsion du DIU ... 44
2.4.5. La perforation utérine... 44
2.5. Réglementation et incidence médico-légale ... 45
3. Particularités du DIU chez la nullipare ... 47
3.1. Recommandations officielles du DIU chez la nullipare ... 47
3.2. Le cadre légal du DIU chez la nullipare, en particulier mineure ... 48
3.3. Les DIU chez la nullipare : ce que dit la littérature ... 48
3.3.1. Taux d’utilisation, efficacité et acceptabilité du DIU chez la nullipare ... 48
3.3.2. Les complications et effets indésirables chez la nullipare sous DIU ... 50
3.3.2.1. Les grossesses extra-utérines chez la nullipare sous DIU ... 50
3.3.2.2. Les maladies inflammatoires pelviennes chez la nullipare sous DIU ... 50
3.3.2.3. La difficulté d’insertion des DIU chez la nullipare ... 51
3.3.2.4. Les expulsions de DIU chez la nullipare ... 51
3.3.2.5. La perforation utérine chez les nullipares sous DIU ... 52
3.3.3. Les DIU chez la nullipare en médecine générale ... 52
3.3.3.1. De façon générale ... 52
3.3.3.2. Données préalablement obtenues en Haute-Normandie ... 53
3.4. Taux d’IVG en France ... 56
3.5. La polémique des pilules de 3e et 4e génération ... 57
ETUDE ... 59 1. Objectifs de l’étude ... 59 2. Matériel et méthode ... 60 2.1. Questionnaire quantitatif ... 60 2.2. Diffusion du questionnaire ... 61 2.3. Analyse statistique ... 61 3. Résultats ... 62
3.1. Profil des médecins généralistes de l’effectif ... 62
3.1.1. Répartition en fonction du sexe ... 62
3.1.2. Répartition en fonction de l’âge ... 63
3.1.3. Répartition en fonction du nombre d’années d’exercice ... 64
18
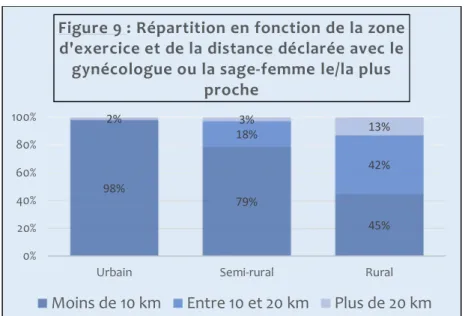
3.1.5. Répartition en fonction de la distance déclarée avec le/la gynécologue ou sage-femme le/la plus proche 67
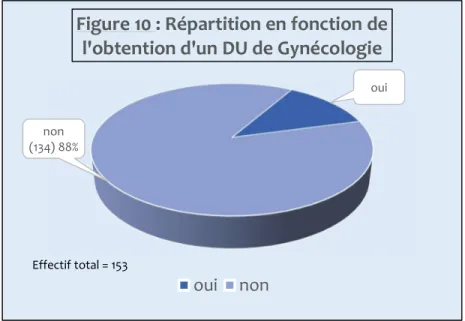
3.1.6. Répartition en fonction de l’obtention d’un DU de gynécologie ... 69
3.2. La connaissance des médecins généralistes des indications du DIU chez la nullipare ... 71
3.2.1. La connaissance de l’indication de l’utilisation possible d’un DIU chez la nullipare ... 71
3.2.2. La connaissance des types de DIU indiqués chez la nullipare ... 71
3.3. Evaluation des pratiques des médecins généralistes concernant l’information contraceptive sur les DIU auprès de leurs patientes nullipares ... 73
3.3.1. L’information contraceptive sur les DIU délivrée par les médecins généralistes auprès de leurs patientes nullipares ... 73
3.3.2. Les critères d’éligibilité de délivrance de l’information ou de la prescription éventuelle d’un DIU chez une femme nullipare ... 74
3.4. Les freins et les déterminants à l’utilisation du DIU par les patientes nullipares rapportés par les médecins généralistes ... 77
3.4.1. Les freins au choix du DIU des patientes nullipares rapportés par les médecins généralistes ... 77
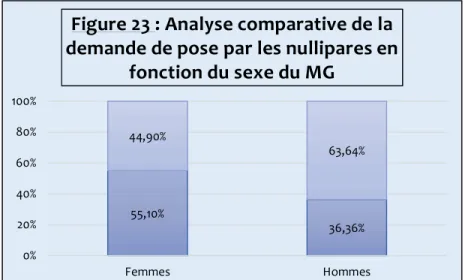
3.4.2. La demande de pose de DIU par les femmes nullipares vue par les médecins généralistes ... 81
3.5. Les pratiques et méthodes de pose des DIU par les médecins généralistes ... 85
3.5.1. La pratique de pose de DIU par les médecins généralistes de façon générale ... 85
3.5.2. La pratique de la pose de DIU par les médecins généralistes chez les femmes nullipares ... 87
3.5.3. Les méthodes de pose des DIU chez les femmes nullipares ... 89
3.5.3.1. Les types de DIU préférentiellement utilisés par les médecins généralistes chez les femmes nullipares ... 89
3.5.3.2. La réalisation d’un prélèvement vaginal avant la pose d’un DIU chez la femme nullipare ... 93
3.5.3.3. La prescription d’antalgiques avant la pose d’un DIU chez la femme nullipare ... 94
3.5.3.4. La prescription d’anxiolytiques avant la pose d’un DIU chez la femme nullipare ... 96
3.5.3.5. La prescription d’analogues de la prostaglandine (Misoprostol®) avant la pose de DIU chez la femme nullipare ... 97
3.5.3.6. L’utilisation d’une pince de Pozzi pendant la pose d’un DIU chez la femme nullipare ... 98
3.5.3.7. La prescription d’une échographie de contrôle après la pose d’un DIU chez une femme nullipare 100 3.6. Les freins et les pratiques des médecins généralistes face à la demande de pose de DIU par les patientes nullipares ... 102
3.6.1. Les freins à la pose d’un DIU ressentis par les médecins généralistes chez une patiente nullipare ... 102
3.6.2. La conduite tenue face à un refus de la part des médecins généralistes de pose de DIU chez une femme nullipare ... 104
3.6.3. Les risques perçus par les médecins généralistes à la pose d’un DIU chez une femme nullipare ... 105
3.7. La demande de formation des médecins généraliste de pose de DIU chez la femme nullipare 107 4. Discussion ... 109
4.1. Limites et forces de l’étude ... 109
4.1.1. Des biais de sélection ... 109
19
4.1.3. La représentativité de l’échantillon ... 110
4.2. Discussion des résultats de l’étude ... 111
4.2.1. Le profil des médecins généralistes répondants... 111
4.2.2. Les médecins généralistes haut-normands proposent le DIU à leurs patientes nullipares ... 111
4.2.3. Les pratiques et méthodes de pose des DIU par les médecins généralistes haut-normands ... 113
4.2.3.1. La pose de DIU par les médecins généralistes haut-normands ... 113
4.2.3.2. Les méthodes de pose des DIU par les médecins généralistes haut-normands chez les femmes nullipares ... 114
4.2.4. Les freins ressentis par les médecins généralistes haut-normands vis-à-vis de la pose de DIU chez leurs patientes nullipares ... 116
4.2.4.1. Les freins au choix du DIU des patientes nullipares rapportés par les médecins généralistes haut-normands ... 116
4.2.4.2. Les freins des médecins généralistes haut-normands vis-à-vis de la pose de DIU chez les femmes nullipares ... 117
4.3. Les perspectives et enjeux soulevés par cette thèse ... 118
CONCLUSION ... 121
BIBLIOGRAPHIE ... 123
20
GLOSSAIRE
ACOG : American College of Obstetricians and Gynecologists AINS : Anti Inflammatoires Non Stéroïdiens
AMM : Autorisation de Mise sur le Marché
ANAES : Agence Nationale d’Accréditation et d’Evaluation en Santé DIU : Dispositif Intra-Utérin
DU : Diplôme Universitaire
DRESS : Direction de la Recherche, des Etudes, de l’Evaluation et des Statistiques EVA : Echelle Visuelle Analogique
GEU : Grossesse Extra-Utérine GIU : Grossesse Intra-Utérine HAS : Haute Autorité de Santé
IST : Infection sexuellement transmissible IVG : Interruption Volontaire de Grossesse LNG : Lévonorgestrel
MG : Médecin Généraliste
MIP : Maladie Inflammatoire Pelvienne OMS : Organisation Mondiale de la Santé
21
INTRODUCTION
Depuis la législation de la contraception par la loi Neuwirth en 1967, le paysage contraceptif n’a cessé d’être en constante évolution, l’offre s’étant étoffée au fur et à mesure des années, atteignant un large éventail de méthodes contraceptives actuellement disponibles [1].
Les habitudes de prescription se sont construites au fil des évolutions sociétales et médicales, avec de nouvelles recommandations et législations, ainsi qu’avec l’apparition de nouvelles méthodes de contraception (implant, anneau vaginal, patch), permettant de proposer un arsenal thérapeutique varié, venant compléter une offre déjà existante (pilule, dispositif intra-utérin et préservatif) [1]. Aujourd’hui en France, 7 femmes sur 10 recourent à une méthode contraceptive médicalisée [1], et chacune d’entre elle peut trouver une contraception adaptée à son mode de vie et à ses attentes. Or, ces dernières ne sont pas les mêmes qu’hier, n’ont pas le même parcours de vie et le même rapport à la sexualité que les générations précédentes, le choix de la contraception devant alors être le plus personnalisé possible.
Cependant, malgré cette offre de plus en plus diversifiée, de nombreuses études en Santé Publique ont permis de mettre en évidence un schéma contraceptif resté longtemps figé : l’utilisation du préservatif au début de l’activité sexuelle, l’adoption de la pilule lors de l’installation en couple, et le DIU une fois que le couple a obtenu les enfants désirés [2].
Pourtant, l’étude des indices de Pearl1 de ces différents contraceptifs montre que ce schéma peut
apparaître comme inadapté à ces différents stades de la vie sexuelle, l’efficacité théorique des contraceptifs utilisés préférentiellement au début de la vie sexuelle n’étant pas très élevée, alors que le désir de grossesse est souvent le plus bas [2].
1Nombre de grossesses observées pour 100 femmes utilisant une contraception donnée durant
22
Malgré l’autorisation du DIU (ou « stérilet ») chez les femmes nullipares par de nombreuses grandes instances médicales à partir de 2004 (ANAES [3], HAS [4], OMS [5]), l’évolution des mentalités et des pratiques semble prendre du temps.
Parallèlement, 211 900 IVG ont été réalisées en France en 2016, soit 14,4 IVG pour 1000 femmes âgées de 15 à 49 ans, les femmes de 20 à 24 ans étant les plus concernées (26,7 femmes pour 1000) [6]. Ce chiffre est resté globalement stable depuis 1975, année de la promulgation de la loi Weil, autorisant l’IVG [7]. Lors de mon passage en gynécologie-obstétrique, j’ai d’ailleurs été frappée par ce constat, face au nombre important de jeunes filles venues en consultation pour une demande d’IVG ; dans la grande majorité des cas, il m’a semblé que ces jeunes patientes considéraient que leur contraception n’était pas adaptée à leur mode de vie. Leur discours semblait régulièrement être le reflet d’une méconnaissance des alternatives contraceptives, sous-entendant bien souvent que leur médecin prescripteur ne leur avait pas proposé d’alternative de contraception.
Toutes ces constatations sont sans compter sur la polémique récente fin 2012 sur les pilules de 3e
et 4e générations, qui selon les premières études, a permis d’enclencher un début de changement
dans les habitudes et volontés contraceptives des patientes, obligeant à une adaptation des médecins [1].
23
1. Description des populations étudiées
1.1.
Les nullipares
1.1.1. DéfinitionLe suffixe « -pare », provenant étymologiquement du latin « parere », est utilisé pour former des noms correspondant à une notion de naissance, d’engendrement, d’accouchement. En gynécologie-obstétrique, la parité désigne donc le nombre d’accouchements d’une femme, et plus précisément le nombre d’enfants mis au monde vivants, les morts fœtales et les mortinaissances étant exclues.
Par extension, une femme nullipare est une femme dont la parité est nulle, qui n’a donc jamais accouché d’un enfant vivant. Dès qu’une femme a accouché au moins une fois d’un enfant vivant, il est alors possible d’utiliser le terme « multipare ».
1.1.2. Caractéristiques générales
Selon l’INSEE, en 2015, en France, les femmes donnent naissance à leur premier enfant à 28,5 ans en moyenne, soit quatre ans et demi plus tard qu'en 1974. L’âge de la première maternité ne cesse d’augmenter depuis cette date. La proportion des femmes nullipares est donc en constante augmentation (Annexe 1).
Ce recul de l’âge de la première maternité est à mettre en relation avec un changement dans les mœurs et les mentalités depuis 1975, notamment concernant le comportement sexuel. En effet, le contexte de sexualité en France s’est modifié avec l’amélioration du statut social des femmes. L’augmentation de la scolarisation de celles-ci, la prolongation de la durée de leurs études et leur entrée massive sur le marché du travail, ont contribué à retarder la première grossesse dans la vie des femmes, tout en accentuant leur autonomie vis-à-vis des hommes [8].
Au recul de l’âge de la première maternité, il faut ajouter un âge au premier rapport sexuel diminuant progressivement depuis 1975 (17,6 ans pour les femmes en 2009), avec une première maternité survenant en moyenne 9,5 ans après les premiers rapports sexuels (contre 5,5 ans il y a 25 ans) [7].
24
Les femmes restent donc exposées à un risque de grossesse non désirée plus longtemps qu’auparavant. Cette période de « jeunesse sexuelle », entre les premiers rapports et la première mise en couple stable, n’a cessé de s’allonger, d’où la nécessité d’une contraception la plus adaptée possible aux désirs et au mode de vie des femmes [9]. Cette notion est d’autant plus importante à prendre en compte que le nombre de partenaires sexuels augmente pour les femmes des générations récentes par rapport à leurs aînées (1,8 partenaires sexuels différents en 1970, 3,3 en 1992, 4,4 en 2006) [8], les relations sexuelles hors contexte de conjugalité étant plus fréquentes. Ces constatations sont la conséquence d’un changement des habitudes en matière de sexualité qui se trouvent de plus en plus déconnectées de ses enjeux strictement reproductifs. La décision d’une première grossesse est aujourd’hui bien souvent « programmée » dans un contexte affectif stable et « au bon moment » de la trajectoire professionnelle des parents, afin de rentrer dans le cadre d’une certaine « norme procréative » [9].
Les enjeux en matière de contraception sont donc majeurs afin de limiter les risques de grossesses non désirées ; la diversité des parcours conjugaux est à prendre en compte en adaptant les méthodes de contraception aux conditions de vie sociale, professionnelle, affective et sexuelle des femmes.
1.1.3. La couverture contraceptive des nullipares (Annexe 2) [2]
Depuis de nombreuses années, le modèle contraceptif français semble figé et peu flexible. Le début de la vie sexuelle voit une utilisation majoritaire du préservatif, la pilule apparaissant dans la vie de la jeune femme dès que sa vie sexuelle se régularise [1]. Le DIU ne semble utilisé que lorsque les couples ont eu les enfants qu’ils désiraient.
Selon INPES en 2010, 91,2% des femmes âgées de 15 à 29 ans en couple ou ayant une relation amoureuse stable et soucieuse d’un risque de grossesse non prévue déclarent utiliser un moyen de contraception pour éviter une grossesse.
La pilule demeure la méthode de contraception la plus utilisée : 60,4% des femmes de 15 à 19 ans et 59,5% des femmes de 20 à 24 ans en couple ou déclarant une relation amoureuse stable, concernées par un risque de grossesse non prévue et utilisant un moyen contraceptif y ont eu recours en 2016 [1].
25
L’utilisation du DIU chez les femmes nullipares, même si elle reste anecdotique, semble augmenter depuis quelques années, en particulier chez les plus de 20 ans (sur l’ensemble des jeunes filles de 15 à 29 ans, l’augmentation observée entre 2005 (4,5 %) et 2010 (5,9 %) est très proche de la significativité (p=0,06)). Elle semble cependant majoritairement limitée aux femmes ayant déjà eu au moins un enfant (parmi les 25-29 ans, 7,6% des femmes nullipares ont recours à un DIU, contre 31,8% chez les femmes qui ont des enfants [1]).
Cette couverture contraceptive semble être conditionnée par divers facteurs socio-économiques et territoriaux. Ainsi, une situation financière difficile, une zone de résidence rurale avec difficultés de suivi par un spécialiste semblent constituer des facteurs discriminants dans l’accès aux nouvelles méthodes de contraception et dans la recherche d’un contraceptif régulier le plus adapté à la situation de la patiente [2]. La démographie médicale semble donc un élément essentiel dans l’utilisation d’une contraception adaptée et la prévention de grossesses non prévues.
1.2.
La démographie médicale actuelle
1.2.1. La démographie médicale globale
D’après l’Atlas de la Démographie Médicale en France de 2017 [10], il existe un vieillissement préoccupant des médecins inscrits au tableau de l’Ordre des Médecins. Les médecins âgés de 60 ans et plus représentaient 47% de l’ensemble des médecins inscrits au tableau contre 27% en 2007, alors que ceux âgés de moins de 40 ans représentent 15% de l’ensemble de la profession.
De plus, la proportion de médecins retraités augmente. Depuis 2007, les médecins retraités enregistrent un accroissement de 93,6% de leurs effectifs tandis que le nombre d’actifs n’a augmenté, sur la même période, que de 0,9%.
Par ailleurs, la profession se féminise avec 42% de femmes inscrites au tableau de l’Ordre en 2017, contre 37% en 2007. Parmi les médecins âgés de moins de 40 ans, les femmes représentent 62% de l’ensemble des inscrits au tableau de l’Ordre.
La région Haute-Normandie fait partie des régions où la densité médicale est faible ; en 2015, on comptait 245,5 médecins en activité régulière pour 100 000 habitants, pour une moyenne nationale à 281,4 médecins pour 100 000 habitants [11].
26
1.2.2. La démographie des médecins généralistes
Le nombre de médecins généralistes diminue en France. En 2017, le tableau de l’Ordre recensait 88 137 médecins généralistes en activité régulière, soit une diminution de 9,1% des effectifs depuis 2007 [10]. D’après les analyses de l’Ordre des Médecins, cette tendance à la baisse des effectifs va se confirmer au moins jusqu’en 2025 pour atteindre 79 262 médecins généralistes en France. En 2018, dans les 70 bassins de vie de la région Haute-Normandie, il a été recensé 1422 médecins généralistes libéraux et mixtes, ce qui représente une baisse des effectifs de 12% depuis 2010 [12] En 2015, la densité des médecins généralistes en activité régulière dans l’Eure était de 101,5 pour 100 000 habitants, dans la Seine-Maritime de 131 pour 100 000 habitants.
Ces médecins généralistes vieillissent ; âgés en moyenne de 53 ans en 2015 en Haute-Normandie, 32% des médecins généralistes sont âgés de 60 ans et plus et 13% sont âgés de moins de 40 ans dans la région.
Enfin sur le plan national, le secteur libéral se désertifie chez les médecins généralistes parmi lesquels on observe une diminution de l’effectif global libéral (64 778 en 2007 contre 48 872 en 2018). En Haute-Normandie, l’effectif total des médecins généralistes exerçant exclusivement en secteur libéral a diminué d’environ 10% depuis 2010 [10].
1.2.3. La démographie médicale des gynécologues
La discipline « gynécologie » est divisée en 3 spécialités : deux d’entre elles sont des disciplines médicales (la gynécologie médicale et obstétrique et la gynécologie médicale), la 3e est une
discipline chirurgicale (la gynécologie-obstétrique). Ces spécialités connaissent également une diminution importante de ses effectifs.
On recense en France en 2018, 4549 gynécologues-obstétriciens (versus 3 532 en 2010), 1048 gynécologues médicaux (versus 1 645 en 2010) et 1016 gynécologues médicaux et obstétricaux (versus 1 944 en 2010) [12].
En 2017, l’âge moyen des gynécologues médicaux hommes est de 59 ans, 57 ans pour les femmes, avec plus de 62% de l’effectif total ayant plus de 60 ans [10]. Les départs à la retraite à venir vont
27
sans doute accentuer les pénuries de gynécologues médicaux, la faible augmentation du numerus clausus pour cette spécialité ne permettront pas de compenser ces départs à la retraite.
28
2. Les dispositifs intra-utérins
2.1.
L’histoire du DIU [13]
2.1.1. Les prémices de la contraception intra-utérine
La première utilisation de dispositifs intra-utérins à visée contraceptive semble dater de l’Antiquité, les Bédouins insérant dans la cavité utérine de leurs chamelles de petits cailloux ronds afin d’éviter une grossesse au cours de leurs voyages dans le désert.
La première utilisation d’un DIU à visée contraceptive humaine a été décrite par Richard Richter en 1909 à Waldenburg. Il était constitué d’un anneau fait de fils tirés de vers à soie (ou crins de Florence).
En 1928, le docteur allemand Ernst Gräfenberg publia les résultats cliniques de son anneau de fil d’argent spiralé, permettant à son dispositif d’être connu dans le monde entier.
En 1933, au Japon, le Dr Tenrei Ota a développé un DIU en argent ou en or, en ajoutant une structure centrale à l’anneau de Gräfenberg, permettant de diminuer les taux d’expulsion. Il fût également le premier à tenter d’utiliser du plastique dans ses dispositifs, mais la faible qualité du plastique a été responsable d’échecs.
2.1.2. Les DIU de première génération : les dispositifs en plastique
Deux docteurs, qui ont travaillé de façon contemporaine, ont marqué l’histoire des DIU en orientant leurs recherches vers les dispositifs en matière thermoplastique, qui a pour propriété d’être « à mémoire de forme », permettant donc aux dispositifs d’être déformés pour s’introduire plus facilement dans la cavité utérine.
- Le Dr Lazar C. Margulies, en 1960, travaille autour de cette matière thermoplastique et invente son DIU en forme de spirale, initialement positionné dans un tube inserteur permettant, grâce à un poussoir, d’introduire le DIU dans la cavité utérine sans avoir à dilater le col préalablement. Il fut également le premier à introduire du sulfate de baryum dans le dispositif afin de le rendre radio-opaque.
- Le Dr Jack Lippes, en 1961, a inventé le Lippes Loop, de forme trapézoïde, s’adaptant parfaitement à la forme de la cavité utérine. Il a également ajouté à son DIU un
29
monofilament de nylon facilitant le retrait du dispositif, et permettant à la patiente de vérifier sa présence. Suite à la découverte de son confrère, le Dr Margulies, il installe également son DIU dans un tube inserteur. Le Lippes Loop a connu un succès mondial. S’en suivirent l’apparition de DIU de diverses formes variées et parfois originales (Annexe 3). A l’image du DIU Dalkon Shield, qui du fait de la composition de son fil de retrait constitué par des centaines de microfilaments de nylon, favorisait l’ascension de micro-organismes vaginaux dans l’utérus, et qui a été à l’origine d’un scandale sanitaire dans les années 1970 aux Etats-Unis. Il a été rendu responsable de plusieurs décès par septicémie et d’avortements septiques, entrainant environ 300.000 ports de plaintes contre le laboratoire ayant commercialisé le DIU. En outre, ce scandale a entaché l’image des DIU en général aux Etats-Unis mais aussi dans le monde entier, image négative qui persiste encore actuellement.
2.1.3. Les DIU de deuxième génération : les dispositifs au cuivre
Deux scientifiques ont permis l’apparition du DIU au cuivre :
- Le Dr Jaime Zipper Abragan, qui, en 1968, a mis en évidence l’effet anti-nidation des ions métalliques, dont le cuivre, sur la cavité utérine sur les lapins femelles.
- Le Dr Howard J. Tatum, qui, supposa qu’une forme « en T » du DIU, permettrait de diminuer les risques d’expulsion, car correspondant plus à la forme de la cavité utérine lorsqu’elle se contracte.
Leur travail de concert a permis d’inventer l’actuel TCu380A qui représente encore aujourd’hui le Gold Standard des DIU au cuivre.
2.1.4. Les DIU de troisième génération : les dispositifs hormonaux
Dès la fin des années 1960, le Dr Antonio Scommegna a démontré les effets de la progestérone sur l’utérus, postulant que cette hormone naturellement présente dans le corps humain entraînant une atrophie de la muqueuse utérine, pourrait être utile dans la prévention de l’implantation et la réduction des saignements, les ménorragies étant les principales causes de retrait des DIU au cuivre.
30
En 1976, il conçoit un DIU « en forme de T », à base plastique, mais remplaçant le bras vertical par un réservoir de progestérone cristallisé. Malheureusement, ce DIU n’a pas connu une grande popularité devant la durée de vie trop courte du dispositif (1 an).
A la même période, le Dr Jouni Valter Tapani Luukkainen conçoit en 1976 un DIU « en forme de T » dont le bras vertical a été remplacé par un réservoir relarguant une dose constante quotidienne de 20 µg de lévonorgestrel sur une période de 5 ans. Il s’agit du Mirena®, premier DIU hormonal à être
commercialisé et encore d’actualité aujourd’hui.
Depuis, sont sortis la version « mini » du Mirena® en 2014, le Jaydess®, puis tout récemment en 2018
une version « intermédiaire », le Kyleena®.
2.2.
Les caractéristiques communes aux DIU [Vidal, 4,5]
2.2.1. Les indications communes
La principale indication commune des DIU est la contraception intra-utérine pour toute femme en âge de procréer, et pas uniquement destinée à la multipare, afin d’éviter une grossesse non désirée. Considéré comme très efficace, le DIU affranchit les utilisatrices d’une observance quotidienne parfois contraignante.
2.2.2. Les contre-indications communes
Les contre-indications communes sont : - Toute grossesse suspectée ou avérée
- Le post-partum au-delà de 48h et jusqu’à 4 semaines - Une infection puerpérale en post-partum
- Le post-abortum septique (immédiatement pour les DIU au cuivre, inférieur à 3 mois pour les DIU au LNG)
- Une maladie inflammatoire pelvienne en cours, récente ou récidivante ou des affections associées à risque accru d’infection pelvienne (tuberculose génito-urinaire avérée par exemple)
31
- Une infection génitale basse, une cervicite purulente en cours ou une infection à Chlamydiae trachomatis ou gonococcie en cours
- Des saignements vaginaux anormaux d’étiologie inconnue (suspicion de pathologie grave) - Des anomalies congénitales ou acquises de l’utérus entrainant une déformation de la cavité
utérine de telle sorte qu’il est impossible d’y insérer un DIU (fibromyomes par exemple) - Une affection maligne du col/corps utérin (cancer)
- Une maladie trophoblastique gestationnelle maligne
2.2.3. Les conditions d’insertion
La décision d’insertion d’un DIU demande des précautions particulières préalables afin d’éliminer une contre-indication à l’utilisation et à la pose d’un DIU.
Elle passe avant tout par un interrogatoire précis visant à déterminer les antécédents médicaux (infectieux, oncologiques) et chirurgicaux gynéco-obstétricaux connus de la patiente, les contraceptions déjà utilisées et leur tolérance. Il permet d’évaluer les projets de grossesse de la patiente, ses habitudes sexuelles (évaluation du risque d’IST et du risque de grossesse actuelle) ainsi que des plaintes fonctionnelles éventuelles (ménorragie, dysménorrhée, dyspareunie, métrorragies inexpliquées).
Il doit également y avoir un examen gynécologique minutieux. Ce dernier doit être complet avec un examen bimanuel soigneux permettant de mettre en évidence la version, la flexion et l’axe de l’utérus, ainsi qu’une éventuelle anomalie anatomique ou pathologique.
Il est établi que la période de pose idéale se situe plutôt en début de cycle menstruel (première partie du cycle), l’orifice cervical étant alors plus dilaté, facilitant l’insertion et le risque de grossesse étant moins probable (accord professionnel).
Une information claire, loyale et objective sur les risques de complications doit être systématiquement délivrée. Elle doit porter notamment sur les risques de maladie inflammatoire pelvienne, de grossesse (intra ou extra utérine), et sur les risques potentiels mais non démontrés de stérilité tubaire [5].
32 2.2.4. Les prescriptions préalables
Tout médecin ou sage-femme prescrivant un DIU doit préalablement s’assurer de l’absence d’infection cervicale ou génitale haute (endométrite, salpingite). Ceci passe par un interrogatoire et un examen gynécologique permettant d’évaluer le risque d’IST de la patiente en demande de contraception intra-utérine. La réalisation d’un prélèvement vaginal systématique à l’ensemble des patientes ne semble pas établie. En revanche, d’après l’HAS [4] et le CNGOF [14] ainsi que de nombreuses études et autres revues de la littérature [15, 16], il semble nécessaire de le proposer à celles qui sont à risque d’IST.
Selon l’ANAES [3], les facteurs de risque d’IST sont : - Un antécédent personnel d’IST
- Une infection génitale en cours ou récente - Un âge inférieur à 25 ans
- Des partenaires sexuels multiples - Des rapports sexuels non protégés
Ce prélèvement vaginal est à effectuer avant la pose du DIU, si possible lors d’une consultation préalable à la consultation d’insertion, sauf dans le cas où le risque de perdue de vue est important. Il est alors préconisé de réaliser le prélèvement dans le même temps que l’insertion du DIU ; il n’est alors pas nécessaire d’en attendre les résultats [16, 17].
L’antibioprophylaxie systématique ne semble en aucun cas indiquée [4, 16, 18, 19]. Le RCOG émet cependant une réserve en ce qui concerne les patientes à haut risque d’IST dont la compliance pourrait rendre difficile un traitement avant l’insertion et dont les résultats du prélèvement vaginal ne sont pas disponibles au moment de la pose. Il préconise alors de proposer une antibioprophylaxie couvrant Chlamydiae Trachomatis.
L’administration d’antalgiques de palier 1 ou 2 avant l’insertion semble être d’usage afin d’en diminuer la douleur [3,4], surtout chez la patiente nullipare. Cependant, de nombreuses études tendent à prouver l’inefficacité de ces traitements. En effet, Hubacher D. et al. en 2006 [20] puis Ngo LL. et al. en 2016 [21], ont respectivement testé l’administration d’Ibuprofène 400mg et de Naproxène 550 mg en prophylaxie anti-douleur. Ces études ont été réalisées de façon randomisée, en double-aveugle, versus placebo sur une cohorte de respectivement 2019 et 188 femmes. Les résultats sont identiques pour les deux études : il n’a pas été retrouvé d’efficacité des AINS en
33
prémédication au moment de la pose. En revanche, il semble exister une efficacité du Naproxène 550 mg sur les douleurs à distance de la pose (15 minutes).
Le Misoprostol® 200 à 400 µg, analogue de la prostaglandine E1 utilisé habituellement au cours des IVG médicamenteuses pour ses propriétés contractiles du corps utérin et de dilatation cervicale utérine, semble être utilisé par certains pour faciliter l’insertion du DIU (hors AMM). Cependant, les multiples études réalisées sur ce sujet, dont une méta-analyse d’essais contrôlés randomisés datant de 2014, n’ont pas démontré d’efficacité de la molécule sur la facilité d’insertion ou sur la douleur ressentie par la patiente [22, 23].
Le CNGOF évoque la possibilité d’une prémédication par anxiolyse chez les patientes anxieuses [14]. Plusieurs thèses qualitatives ont évoqué une prémédication par anxiolyse par certains médecins avant l’insertion d’un DIU [24, 25] ; une étude préconise l’utilisation d’un anxiolytique de demi-vie courte dans le but de limiter l’inconfort lié à la pose, réduire l’anxiété anticipatoire et faciliter le geste technique [26]. Cependant, aucune étude randomisée, contrôlée versus placebo en double aveugle n’a été retrouvée dans la littérature concernant l’innocuité de l’anxiolyse en prémédication.
Enfin, une récente méta-analyse de Juin 2018 a démontré l’efficacité du bloc para-cervical2 à la
Lidocaïne®, qui malgré une douleur liée au bloc en lui-même, aurait permis aux patientes qui ont eu l’anesthésie, d’avoir des scores EVA inférieurs aux scores des patientes n’en ayant pas eu, que ce soit pour la pose de la pince de Pozzi, pour l’insertion du DIU mais également dans les suites immédiates de la pose [27].
2.2.5. Les techniques de pose
Trois types du DIU différents existent (Annexe 4) :
- Les DIU en « Y » ont les « bras » repliés vers le haut dans le tube inserteur ; - Les DIU en « T » ont les « bras » repliés vers le bas dans le tube inserteur
- Les DIU en « Ω », de par leur forme, n’entrent jamais complètement dans le tube inserteur (seule la tige y est incluse, les « bras » restant à l’extérieur à tout moment).
2 Un bloc paracervical implique l'injection d'un anesthésique local autour du col de l'utérus pour
34
Il convient avant tout geste de se référer à la notice propre à chaque type de DIU, les positionnements des bagues ou les tubes inserteurs différant d’un DIU à l’autre.
La patiente est installée sur une table idéalement de gynécologie, allongée sur le dos en position « gynécologique », ou en décubitus latéral ou position « à l’anglaise ».
Le port de gants non stériles est suffisant, mais l’insertion doit se faire dans des conditions d’asepsie strictes.
Après la pose d’un spéculum de taille adaptée afin de visualiser correctement le col utérin, il est conseillé de le désinfecter à l’aide de Bétadine® gynécologique.
La technique dite « classique » utilise une pince de Pozzi à placer au niveau de la lèvre antérieure du col utérin en cas d’utérus antéversé, sur la lèvre postérieure en cas d’utérus rétroversé. Il convient de prévenir la patiente de l’éventualité d’une douleur. La pince va permettre de stabiliser le col utérin au moment de l’insertion du tube inserteur et de faciliter la pose en alignant le canal cervical avec le reste du corps utérin en exerçant une légère traction qui doit être maintenue tout au long de la pose.
Une hystérométrie est alors réalisée afin d’évaluer la profondeur utérine ainsi que la direction de la cavité utérine. Elle est réalisée à l’aide d’un hystéromètre stérile souple, parfois fourni sous forme de « kit de pose » avec le DIU (par exemple les sets de pose avec DIU type SETHYGYN).
Pour les DIU en « T » et en « Y » :
- Préparer le DIU : s’assurer que l’emballage du DIU n’ait pas été ouvert ni endommagé. Après ouverture de l'emballage de moitié, manipuler le dispositif à plat ou dirigé vers le haut pour éviter les risques de chute sur le sol.
o Régler la bague mobile du tube inserteur à travers le plastique de l’emballage en fonction des indications de la notice propre au DIU utilisé (extrémité supérieure ou inférieure à placer au niveau de la valeur correspondant en centimètres à la profondeur utérine de la patiente).
o Faire glisser le poussoir dans le tube inserteur le long des fils de nylon.
o Faire entrer le DIU dans le tube inserteur (en tirant simultanément sur les deux fils de nylon afin de faire rentrer le corps et les bras du DIU dans le tube inserteur pour les DIU en forme de « Y », en poussant le poussoir pour les DIU en « T »). Laisser affleurer l'extrémité des bras juste au-dessus de l'extrémité du tube inserteur pour faciliter le passage atraumatique du col. Il est recommandé de ne pas laisser le DIU plus de 5 minutes dans le tube inserteur.
35 o Le dispositif est alors prêt à être installé. - Introduction du dispositif d’insertion :
o Exercer une traction sur le col avec la main gauche (si opérateur droitier) grâce à la pince de Pozzi.
o Introduire l’extrémité distale du tube inserteur dans le canal cervical et le pousser jusqu'à ce que la bague soit au contact du col. Dans ces conditions, le DIU ne touche pas le fond utérin.
o Maintenir fixe le poussoir et tirer vers soi le tube inserteur jusqu’au témoin du poussoir (là encore, représenté de façon différente selon les DIU). Les bras du DIU sont alors libérés dans la cavité utérine.
o Pour les DIU en « Y » uniquement : repousser l'ensemble inserteur et poussoir jusqu'à ce que la bague vienne de nouveau au contact du col. A ce moment-là, les branches du DIU sont plaquées sur le fond utérin. Maintenir fixe le poussoir et faire glisser de nouveau le tube inserteur vers soi jusqu'au bout.
o Le DIU est alors en place hors du tube. - Retrait du dispositif d’insertion :
o Retirer le poussoir puis le tube inserteur.
o Couper les fils, après vérification de la bonne position du DIU, à 2 ou 3 cm de l'orifice externe du col.
o Retirer la pince et le spéculum.
o Maintenir la patiente allongée quelques minutes afin de prévenir la survenue d’un malaise vagal.
Pour les DIU en « Ω », il n’y a pas de poussoir :
- Régler la bague mobile sur le tube inserteur au niveau de la mesure retrouvée à l’hystéromètre.
- Introduire le tube inserteur jusqu’à la bague. - Retirer le tube, le DIU restant en place. - Couper les fils.
Pour les DIU hormonaux, un nouveau système de pose a été commercialisé en 2014. L’insertion se fait désormais à une seule main à l’aide d’un curseur serti au tube inserteur et coulissant sur une poignée attachée au poussoir :
- Pousser le curseur vers l’avant avec le pouce afin de faire entrer le DIU dans le tube inserteur.
36
- Introduire le dispositif de pose jusqu’à ce que la bague soit à 2 cm environ du col utérin, faire coulisser le curseur d’un cran vers l’arrière.
- Repousser le tube vers l’avant jusqu’à la butée de la bague contre le col et reculer le curseur avec le pouce d’un deuxième cran pour libérer entièrement le DIU.
Il existe une technique alternative d’insertion de DIU, dite technique « directe », ou « de la torpille », également appelée méthode de Cristalli-Bonneau, ou « pose en floraison ». Cette dernière reste assez méconnue, une seule et unique étude ayant été retrouvée sur le moteur de recherche PubMed [28], uniquement descriptive, ne portant que sur une petite cohorte de 50 patientes. Cette méthode a également été défendue par des médecins comme le Dr Martin Winckler ou dans certains blogs médicaux, décrivant la technique comme moins douloureuse pour la patiente et réduisant le risque de spasme utérin. Elle semble également plus simple, plus rapide, et nécessite moins d’instruments, puisque la pince de Pozzi n’est plus obligatoire, et l’hystérométrie inutile. Un article publié en 2015 dans la revue Exercer décrit cette technique en se basant sur deux mémoires réalisés à l’aide d’entretiens semi-dirigés auprès de professionnels de santé utilisant cette méthode [29], principalement pour les DIU en « Y ».
Le principe de base est que seul le DIU pénètre dans la cavité utérine : - Introduire le spéculum.
- Réaliser une désinfection.
- Placer éventuellement la bague entre 3 et 4 cm sur le tube inserteur en tant que point de repère.
- Introduire le tube inserteur jusqu’à sentir une légère résistance ou jusqu’à ce que la bague touche le col, c’est-à-dire jusqu’à l’arrivée à l’orifice interne du col.
- Pousser doucement le DIU à l’aide du poussoir, sans bouger le tube inserteur. Le DIU se déplie dans la cavité utérine.
- Retirer d’abord le poussoir, puis le tube inserteur.
- Couper les fils assez longs (2-4 cm), pour éviter leur disparition lors de la possible ascension du DIU.
37 2.2.6. Le suivi post-insertion
L’HAS préconise une consultation de contrôle 1 à 3 mois après la pose du DIU [4] afin de s’assurer que celui-ci est bien toléré, qu’il n’a pas été expulsé (visualisation des fils) et qu’il n’y pas de symptômes pouvant faire évoquer une maladie inflammatoire pelvienne.
Les contrôles seront ensuite annuels ou plus rapprochés s’il existe des signes d’appel cliniques. Certains médecins déclarent prescrire une échographie pelvienne de contrôle en cas d’ascension des fils, par réassurance de la patiente ou parfois de lui-même [25]. Une étude a pourtant prouvé qu’une échographie systématique n’est pas indiquée [30].
Le CNGOF se positionne en indiquant que « la pratique d’une échographie en routine immédiatement après la pose d’un DIU pour contrôler sa position est un acte rassurant qui n’est cependant pas recommandé systématiquement quand l’insertion s’est déroulée sans difficulté » [31].
2.3.
Les différents modèles de DIU (Annexe 4)
2.3.1. Les DIU au cuivre 2.3.1.1. Généralités
Le DIU au cuivre est composé d’un support en plastique radio opaque, à bras latéraux flexibles, autour duquel s’enroule un fil de cuivre.
La surface de cuivre est de 375 ou 380 mm2 en fonction des dispositifs. Un fil de nylon attaché au
support permet le contrôle de la présence du dispositif et le retrait.
Le taux de grossesse non intentionnelle au cours de la première année d’utilisation pour une utilisation « correcte et régulière », donc considérée comme parfaite, du DIU au cuivre est de 0,6%. En France, le taux de grossesse en utilisation « courante » est de 1,1% contre 0,8% aux Etats-Unis (Annexe 5).
On peut donc remarquer que l’efficacité théorique du DIU au cuivre est proche de l’efficacité courante (à titre de comparaison, le taux de grossesse au cours de la première année d’utilisation parfaite pour les pilules contraceptives orales est de 0,3% contre 9% en utilisation courante)
38
Le taux d’abandon de la méthode après un an d’utilisation en France est de 15%, contre 22% aux Etats-Unis.
Les différents laboratoires ont développé des modèles dits « shorts » dont la taille est adaptée aux utérus plus petits des nullipares.
Les DIU au cuivre coûtent en moyenne 29,28€ en France [Vidal], et sont remboursables à 65% par l’Assurance maladie. Ils sont commercialisés sous le statut de dispositif médical.
2.3.1.2. Mode d’action [4, 32]
Le mode d’action principal qui résulte d’un effet cytotoxique du cuivre sur les gamètes, est à l’origine d’une altération des spermatozoïdes ainsi que des ovules, entraînant ainsi une inhibition de la fécondation, constituant donc une réelle contraception, et non pas une méthode abortive. Le cuivre est également responsable d’un afflux local de leucocytes au niveau de l’endomètre, accentuant la dégradation des spermatozoïdes, occasionnant une inflammation locale altérant l’implantation embryonnaire.
2.3.1.3. Indications spécifiques [3, 4, 5]
L’indication spécifique du DIU au cuivre, en plus de son activité contraceptive efficace, est la contraception d’urgence en tant que rattrapage après un rapport sexuel non protégé. Les résultats obtenus avec les DIU au cuivre dans le cadre d’une utilisation post-coïtale sont bien meilleurs que la contraception d’urgence hormonale et avec un délai de pose possible jusqu’à 5 jours après la date estimée de l’ovulation. Le DIU au cuivre est à considérer comme la méthode la plus efficace en cas de rapport non protégé (taux d’échec de 0,1 à 0,2%, quel que soit le moment du cycle). De plus, du fait de l’absence d’activité hormonale, il reste indiqué dans les maladies cardiovasculaires et thromboemboliques ainsi que dans les cancers hormonodépendants (cancer du sein notamment). Il est également indiqué en cas de diabète, d’infection à VIH (stade de l’OMS 1 ou 2), d’épilepsie, et ne semble interagir avec aucun traitement médicamenteux. En particulier, en ce qui concerne l’idée fausse que les AINS diminueraient l’efficacité des DIU, une étude cas-témoin de 2006 a clairement mis en évidence que la prise d’AINS ne constitue pas un facteur de risque
39
d’échec de la contraception par DIU au cuivre [33] ; une méta-analyse de la Cochrane Database a même démontré que les AINS peuvent constituer une aide médicamenteuse intéressante dans la gestion des dysménorrhées et/ou des hyperménorrhées liées au DIU au cuivre [34].
2.3.1.4. Contre-indications et effets indésirables
Les contre-indications propres aux DIU au cuivre sont : - Les dysménorrhées sévères
- La maladie de Wilson
- Dans le lupus, une thrombopénie grave - L’hypersensibilité au cuivre
Les effets indésirables propres aux DIU au cuivre sont principalement liés aux changements du profil de saignement des patientes, avec la possibilité d’une augmentation de la durée et du volume de saignement au moment des règles. Il est possible de soulager ces ménorragies grâce à l’aide d’acide tranexamique (Exacyl®) qui a prouvé son efficacité contre placebo [35]. Des dysménorrhées sont également susceptibles de survenir suite à la pose d’un DIU au cuivre, qui peuvent être soulagées, comme nous l’avons vu précédemment, par des AINS.
2.3.2. Les DIU au Lévonorgestrel 2.3.2.1. Généralités
Le DIU au LNG est composé d’un support en plastique en forme de « T », muni d’un anneau d’argent pour certains, visible en échographie. Il contient un réservoir de LNG, qui est un progestatif, dans sa branche verticale à des dosages différents selon le type de DIU. Un fil de nylon attaché au support permet le contrôle de la présence du dispositif et le retrait.
Le taux de grossesse non intentionnelle au cours de la première année d’utilisation pour une utilisation « correcte et régulière », donc considérée comme parfaite, du DIU au LNG est de 0,2%. En France, le taux de grossesse en utilisation « courante » est de 1,1% contre 0,2% aux Etats-Unis (Annexe 5).
40
Tout comme le DIU au cuivre, les DIU au LNG ont une efficacité théorique proche de l’efficacité courante.
Le taux d’abandon du DIU au LNG après un an d’utilisation en France est de 15% contre 20% aux Etats-Unis.
Trois DIU au LNG sont commercialisés en France :
- Le Mirena®, qui possède une réserve de 52mg de LNG, diffuse une quantité de 20µg/24h de LNG sur une durée de 5 ans.
- Le Jaydess®, qui possède une réserve de 13,5mg de LNG, diffuse une quantité de 12µg/24h de LNG sur une durée de 3 ans.
- Le Kyleena®, le dernier arrivé récemment sur le marché en Juillet 2017, qui possède une réserve de 19,5mg de LNG, diffuse une quantité de 9µg/24h de LNG sur une durée de 5 ans [36].
Les DIU Jaydess® et Kyleena® sont plus courts (28mm) et moins chers (99,42€) que le Mirena® (32mm et 110,16€). Ils sont tous remboursés à 65% par l’Assurance Maladie, et contrairement aux DIU au cuivre, sont commercialisés sous le statut de médicament.
Il n’est cependant indiqué dans la contraception qu’en seconde intention, après le DIU au cuivre.
2.3.2.2. Mode d’action [32]
Les DIU au LNG agissent au niveau endométrial et cervical :
- Au niveau endométrial, l’imprégnation par le LNG va entraîner, sur le plan histologique, une atrophie glandulaire avec décidualisation et infiltration granulocyto-macrophagique du tissu conjonctif sous-jacent, responsable d’une atrophie endométriale et donc d’une altération de l’implantation. Il induirait de plus l’expression d’un inhibiteur physiologique de la fécondation, bloquant l’interaction spermatozoïde-ovocyte. Il est également responsable d’une augmentation de l’indice de pulsatilité des artères utérines en phase lutéale, recréant des conditions semblables à un début de cycle.
- Au niveau cervical, la progestérone modifie la synthèse et la sécrétion du mucus cervical ; la glaire cervicale devient alors épaisse, impropre à la migration et à la capacitation des spermatozoïdes.