HAL Id: dumas-01214025
https://dumas.ccsd.cnrs.fr/dumas-01214025
Submitted on 9 Oct 2015HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Déterminants cliniques de la prescription antibiotique
dans l’otite moyenne aiguë de l’enfant et de l’adulte en
médecine générale
Étienne Soubran
To cite this version:
Étienne Soubran. Déterminants cliniques de la prescription antibiotique dans l’otite moyenne aiguë de l’enfant et de l’adulte en médecine générale. Médecine humaine et pathologie. 2015. �dumas-01214025�
UNIVERSITE DE BORDEAUX
U.F.R. DES SCIENCES MEDICALES
Année 2015 N°91
THESE
POUR LE DIPLOME D’ETAT DE DOCTEUR EN MEDECINE
Présentée et soutenue publiquement
Le 8 juillet 2015
Par Etienne SOUBRAN
Né le 08 février 1984 à Bayonne
DETERMINANTS CLINIQUES DE LA PRESCRIPTION
ANTIBIOTIQUE DANS L’OTITE MOYENNE AIGUE DE
L’ENFANT ET DE L’ADULTE EN MEDECINE GENERALE
Membres du Jury
JL. DEMEAUX Professeur, Université de Bordeaux Président
D. NEAU Professeur, Université de Bordeaux Rapporteur
V. FRANCO-‐VIDAL Professeur, Université de Bordeaux Juge
X. LEDUC Docteur, Bordeaux Juge
JP. JOSEPH Professeur, Université de Bordeaux Directeur
Remerciements :
A Monsieur le Professeur Jean Louis DEMEAUX
Professeur des Universités, Université de Bordeaux,
Directeur adjoint du Département de Médecine Générale,
Médecin généraliste,
Pour m’avoir fait l’honneur de présider mon jury de thèse.
Merci pour votre aide précieuse au sein du département de médecine générale.
Recevez ici toute ma reconnaissance et mon profond respect.
A Monsieur le Professeur Didier NEAU
Professeur des Universités, Université de Bordeaux,
Praticien Hospitalier,
Pour avoir accepté d’être le rapporteur de ce travail.
Veuillez croire en mes sentiments les plus respectueux.
A Madame le Professeur Valérie FRANCO-‐VIDAL
Professeur des Universités, Université de Bordeaux,
Praticien Hospitalier,
Vous m’avez fait l’honneur, sans hésitation, de faire partie de mon jury de thèse.
Je vous en remercie chaleureusement et vous prie de trouver ici le témoignage de
ma gratitude et de mon profond respect.
A Monsieur le Docteur Xavier LEDUC
Docteur en médecine générale,
Merci de m’avoir fait l’honneur d’accepter de juger ce travail. Merci surtout d’avoir
guider mes premiers pas en médecine générale.
Trouve ici le témoignage de ma reconnaissance, de mon profond respect et de ma sincère amitié.
A Monsieur le Professeur Jean Philippe JOSEPH
Professeur associé de Médecine générale, Université de Bordeaux,
Coordonnateur du DES de Médecine Générale,
Médecin généraliste,
Pour avoir mené la direction de ce travail.
Merci pour votre disponibilité, votre écoute, et vos conseils.
Merci pour tout ce que vous faites pour la médecine générale à Bordeaux.
Recevez ici toute ma gratitude et mon profond respect.
A ma femme, Marie. Tu as été et tu demeures toujours d’un soutien sans faille. Tu as suivi et partagé toutes les difficultés, mais aussi tous les moments de bonheur qui m’ont conduit jusqu’à ce jour. Que nos vœux les plus chers se réalisent. Je t’aime très fort.
A mes parents qui m’ont tout donné pour réussir. A toi Papa qui a fait naître en moi l’envie de faire ce beau métier. Un simple merci ne suffira pas pour être à la hauteur de tout ce que vous m’avez apporté. Vous êtes des exemples pour moi et je vous en suis reconnaissant pour l’éternité. Je vous aime.
A ma sœur, Charlotte, qui a accompagné mes débuts, à mes belles petites nièces Jeanne et Manon et à leur papa Hervé.
A mon frère, Antoine, pour ses visites bordelaises et son soutien, mes adorables neveux Inès et Hugo, et à leur maman Gaëlle.
Je vous souhaite à tous tout le bonheur que vous méritez et suis fier de vous compter parmi les miens.
A ma tante, Marraine, pour tout l’amour que tu nous témoignes.
A ma « vraie » marraine et mon parrain, pour votre présence à mes cotés lors des évènements importants de la vie dont fait parti celui-‐ci.
A mes beaux parents, Françoise et Patrick. A Pauline, Mathieu et Camille ; Virginie, Olivier, Pierre et Antoine. Merci de m’avoir accueilli dans cette « belle » famille qui porte si bien son nom.
A mes collocs et témoins, Rémi et Fab pour tous ces moments passés ensemble et tous ces souvenirs. Votre amitié est précieuse.
A Duf, pour toutes ces années fac et cette amitié forte restée intacte.
A mon presque colloc Mamad pour toutes ces heures de BM passées à travailler, … et à rigoler quand même (JM4à4,…).
Au Dr Larrègle pour ses talents vraiment cachés de Valérie Damidot et son indication restrictive du MODOPAR®.
A mes copains, ou plutôt copines de fac, Alice, Lulu (d’avant fac même), Axelle, Virg, Julie D.
Aux bordelais, Bény & Nada, Julien & Marie, Thibault & Pauline, Jérôme & Julie, Marylis & Gautier.
A tous mes copains landais non sus cités et qui m’apportent tant. Pilou, Berti, Coluche, Croust, Adri, Brayou & Mat. Que le plaisir de se retrouver reste toujours aussi fort.
Aux footeux seignossais pour tous ces moments forts.
Tous les cointernes rencontrés et dont la vie fait qu’on se voit moins.
Au groupe Médical Thiers : Paul Henry, Xavier, François, Hermann, Mélanie, Christine et Nadéra pour tout ce que vous m’avez appris et apporté. Je vous suis infiniment reconnaissant.
Au Dr Cathy pour ton aide précieuse dans ce travail.
A ma grand mère « Mamie », mon grand père « Tachi » et tío Miguel dont les souvenirs sont constants.
Table des matières
I-‐ Introduction ... 8
II-‐ Généralités ... 9
1-‐ Historique ... 9
2-‐ Rappels anatomiques et physiologiques de l’appareil auditif (5) ... 9
2-‐1-‐ Anatomie ... 9
2-‐2-‐ Physiologie de l’audition ... 11
3-‐ Epidémiologie ... 12
4-‐ Physiopathologie (11) ... 12
5-‐ Bactériologie des OMA ... 13
6-‐ Signes cliniques ... 13
7-‐ Diagnostic différentiel ... 15
8-‐ Prise en charge et recommandations ... 15
8-‐1-‐ Stade congestif ... 15 8-‐2-‐ Stade purulent ... 16 8-‐2-‐1-‐ L’antibiothérapie ... 16 8-‐2-‐2-‐ Traitement symptomatique ... 17 8-‐2-‐3-‐ Paracentèse ... 17 9-‐ Complications (13) ... 18 9-‐1-‐ Otite séromuqueuse ... 18 9-‐2-‐ Mastoïdite aigüe ... 18
9-‐3-‐ Evolution prolongée et échec de l’antibiothérapie ... 18
9-‐4-‐ Labyrinthite ... 19
9-‐5-‐ Paralysie faciale périphérique ... 19
9-‐6-‐ Complications endocrâniennes (6) ... 19
III-‐ Antibiotiques et otite moyenne aiguë ... 21
1-‐ Historique des antibiotiques ... 21
2-‐ Résistance aux antibiotiques des germes impliqués dans l’otite moyenne aiguë (8) ... 22
2-‐1-‐ Streptococcus pneumoniae ... 22
2-‐1-‐1-‐ Mécanisme de résistance ... 22
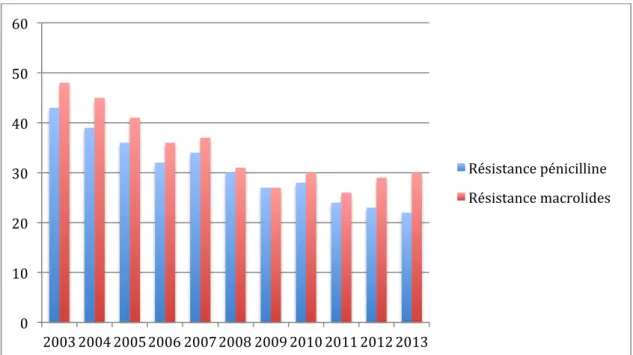
2-‐1-‐2-‐ Evolution des résistances ... 23
2-‐2-‐ Haemophilus influenzae ... 24
2-‐3-‐ Moraxella catarrhalis ... 24
3-‐ Evolution de la consommation antibiotique ... 25
3-‐1-‐ Unité de mesure et de comparaison ... 25
3-‐2-‐ Evolution de la consommation en France ... 25
4-‐ Alternative au tout antibiotique : mise en place des plans antibiotiques ... 26
4-‐1-‐ Le premier plan antibiotique 2001-‐2005 : 20 novembre 2001 (19) ... 26
4-‐2-‐ Deuxième phase du plan antibiotique 2007-‐2010 (27 novembre 2007) ... 27
4-‐3-‐ Le plan d’alerte sur les antibiotiques 2011-‐2016 ... 28
IV-‐ Etude clinique ... 30
1-‐ Objectifs principal et secondaire ... 30
2-‐ Matériels et méthodes ... 30
2-‐1-‐ Présentation de l’étude ... 30
2-‐2-‐ Elaboration du questionnaire ... 30
2-‐3-‐ Mode d’administration ... 31
2-‐4-‐ Rappels de participation à l’étude ... 31
2-‐5-‐ Recueil de données ... 32
3-‐ Résultats ... 33
3-‐1-‐2-‐ Caractéristiques des médecins ... 33
3-‐1-‐3-‐ Caractéristiques des patients ... 33
3-‐1-‐4-‐ Caractéristiques quantitatives de la prescription antibiotique ... 34
3-‐1-‐5-‐ Lien entre les caractéristiques du médecin et la prescription antibiotique ... 34
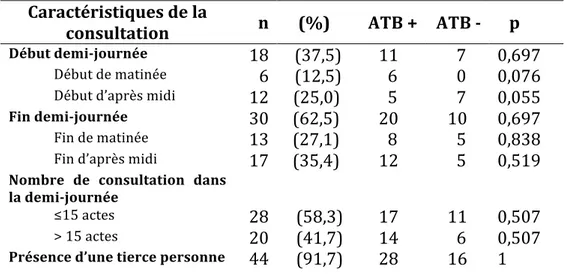
3-‐1-‐6-‐ Lien entre les caractéristiques de la consultation et la prescription antibiotique ... 36
3-‐1-‐7-‐ Lien entre les signes cliniques et la prescription antibiotique ... 37
3-‐1-‐8-‐ Caractéristiques qualitatives de la prescription antibiotique ... 42
3-‐2-‐ Résultats du groupe MR ... 46
3-‐2-‐1-‐ Nombre de réponses ... 46
3-‐2-‐2-‐ Caractéristiques des médecins ... 46
3-‐2-‐3-‐ Caractéristiques des patients ... 46
3-‐2-‐4-‐ Caractéristiques quantitatives de la prescription antibiotique ... 46
3-‐2-‐5-‐ Lien entre les caractéristiques du médecin et la prescription antibiotique ... 47
3-‐2-‐6-‐ Lien entre les caractéristiques de la consultation et la prescription antibiotique ... 48
3-‐2-‐7-‐ Liens entre les signes cliniques et la prescription antibiotique ... 49
3-‐2-‐8-‐ Caractéristiques qualitatives de la prescription antibiotique ... 54
3-‐3-‐ Comparaison des 2 groupes étudiés ... 58
3-‐3-‐1-‐ Comparaison des déterminants de prescription dans les groupes MDS et MR ... 58
3-‐3-‐2-‐ Comparaison des prescriptions antibiotiques dans les groupes MDS et MR ... 60
V-‐ Discussion ... 63
1-‐ Forces et faiblesses ... 63
1-‐1-‐ Forces de cette étude ... 63
1-‐2-‐ Les biais de l’étude ... 63
1-‐2-‐1-‐ Biais de sélection ... 63
1-‐2-‐2-‐ Biais d’observation ... 63
1-‐2-‐3-‐ Biais de mesure ... 64
1-‐3-‐ Faiblesse de l’effectif ... 64
2-‐ Résultats observés ... 65
2-‐1-‐ Les déterminants cliniques de la prescription antibiotique dans l’OMA ... 65
2-‐1-‐1-‐ Facteurs déterminants mis en évidence et significatifs ... 65
2-‐1-‐2-‐ Facteurs de prescription antibiotique systématique ... 66
2-‐1-‐3-‐ Facteurs non significatifs ... 67
2-‐2-‐ Analyse de la prescription antibiotique dans l’OMA ... 69
2-‐2-‐1-‐ Une forte prescription antibiotique ... 69
2-‐2-‐2-‐ Explications de cette forte prescription ... 70
2-‐2-‐3-‐ Solutions pour diminuer la prescription antibiotique dans l’OMA ... 71
2-‐2-‐4-‐ L’amoxicilline apparaît comme l’antibiotique de choix ... 72
2-‐2-‐5-‐ Beaucoup de prescriptions à doses infra posologiques ... 73
2-‐2-‐6-‐ Beaucoup de durées de prescription non respectées ... 74
VI-‐ Conclusion ... 75
VII-‐ Bibliographie ... 76
I-‐ Introduction
L’otite moyenne aigue (OMA) est une pathologie courante en médecine générale, principalement chez l’enfant. Plus de la moitié des enfants en auront une avant l’âge de 7 ans. L’otite de l’enfant constitue la principale pathologie pédiatrique identifiée dans la prescription antibiotique et représente 8,1 % des motifs totaux de prescription en 2013 en France (1).
Les dernières recommandations (2) sur la prise en charge de l’otite moyenne aigüe limitent la place de l’indication des antibiotiques dans cette pathologie. En effet, l’indication d’une antibiothérapie, dans un cas d’OMA, est privilégiée d’emblée chez les enfants en dessous de 2 ans. Au delà de cet âge, l’abstention de toute prescription antibiotique, en dehors de signes cliniques de mauvaise tolérance, est recommandée.
La France, malgré la diminution de ses prescriptions antibiotiques, reste un gros prescripteur, le quatrième au niveau européen (1). Les résistances des agents bactériens aux antibiotiques, et en particulier les résistances du pneumocoque à la pénicilline, sont directement corrélées au niveau de consommation antibiotique. Différents plans antibiotiques se sont succédés ces dernières années afin de lutter contre l’augmentation croissante des prescriptions antibiotiques et des résistances bactériennes (3).
Dans ce contexte de forte prescription antibiotique, et à l’heure où les politiques de santé publique tentent de changer les mentalités du « tout
antibiotique », nous nous sommes interrogés sur l’influence du tableau clinique quant à la prescription d’un antibiotique dans l’OMA de l’enfant et de l’adulte en médecine générale.
Pour conduire ce travail, nous avons choisi de mener une étude de pratique des médecins généralistes installés en Aquitaine et recevant un interne en stage praticien. Ces pratiques des médecins maîtres de stages étaient évaluées sous la forme d’un audit de la part de leurs internes. Nous avons également étudié un groupe de médecins non installés : celui des médecins remplaçants du sud ouest, sous la forme d’un questionnaire rempli sur le prochain cas d’OMA vu en consultation par le médecin remplaçant lui-‐même.
L’objectif principal de notre étude était d’évaluer les déterminants cliniques qui influencent la prescription antibiotique dans l’OMA de l’enfant et de l’adulte en médecine générale. L’objectif secondaire de cette étude consistait à analyser le respect des recommandations de la prescription antibiotique dans la prise en charge de cette pathologie par les médecins généralistes.
Nous effectuerons dans une première partie un rappel sur l’OMA et sa prise en charge, puis dans une seconde partie, nous nous intéresserons à l’évolution de la consommation antibiotique ainsi qu’aux résistances antibiotiques des germes impliqués dans l’OMA. Enfin après une présentation de la méthodologie, nous présenterons les résultats obtenus au cours de notre étude, puis nous les
II-‐ Généralités
L’otite moyenne aigue est une pathologie infectieuse de la partie moyenne de l’oreille.
1-‐ Historique
Les premiers écrits, et les premiers traitements de l’otite aigue, datent de la Grèce antique et ramène à Hippocrate (4).
L’otite était décrite comme une douleur intense, initialement au niveau de la tête, accompagnée de dysurie et de délire. Au septième jour, le patient succombait souvent, à moins qu’une éruption par les narines ou les oreilles lui permette d’en réchapper.
Avant l’éruption, le traitement préconisé reposait sur une application d’eau chaude sur la tête, à l’aide d’éponges, ainsi que la boisson d’un mélicrat étendu d’eau ou de farine d’orge. Un peu de vin blanc aqueux pouvait être utilisé. Après la phase d’éruption par le nez et les oreilles, la disparition de la fièvre et la douleur, on s’injectait de l’eau pure dans les oreilles et on appliquait une éponge de miel. Si l’écoulement persistait, on introduisait de la fleur d’argent, de la sandaraque1, de la
céruse2. Les vaporisations permettaient à l’oreille séchée de se débarrasser des
débris accumulés.
A l’époque de la médecine empirique, bien avant la découverte des antibiotiques, l’otite était considérée comme une maladie grave, potentiellement mortelle.
2-‐ Rappels anatomiques et physiologiques de l’appareil auditif (5)
2-‐1-‐ Anatomie
L’oreille se divise classiquement en 3 parties : l’oreille externe, l’oreille moyenne, et l’oreille interne.
Figure 1 : schéma général de l'oreille (6)
1 Du grec ancien -‐ résine végétale extraite du cyprès de l’Atlas, originaire d’Afrique du Nord. 2 Son aspect blanc immaculé lui louait toutes les vertus divines.
L’oreille externe :
Elle comprend 2 parties :
-‐ le pavillon, lame fibro-‐cartilagineuse, qui permet de diriger les ondes vers le conduit auditif externe (CAE).
-‐ Le CAE, formé d’une portion externe cartilagineuse, et d’une portion interne, osseuse. Le CAE est fermé par le tympan.
L’oreille moyenne :
L’oreille moyenne est formée de cavités comprenant la caisse du tympan et les cellules mastoïdiennes, aérées par la trompe d’Eustache qui débouche dans le rhino-‐pharynx.
Le tympan est composé de la pars flaccida, située au-‐dessus des ligaments tympano-‐maléaires, et de la pars tensa, partie tendue et vibrante de la membrane.
Figure 2 : schéma de l'oreille moyenne (7)
Le marteau, dont le manche est enchâssé dans le tympan, s’articule avec l’enclume, elle-‐même articulée avec l’étrier. Le tout constitue le système tympano-‐ ossiculaire qui va transmettre les vibrations sonores à l’oreille interne, par l’intermédiaire de la platine de l’étrier qui obture la fenêtre ovale.
Le muscle stapédien, innervé par le nerf facial (VII), s’insère sur l’étrier. Ce muscle est à l’origine d’un réflexe de protection acoustique aux stimuli d’intensité sonore trop importants : c’est le réflexe stapédien.
L’oreille interne :
L’oreille interne ou labyrinthe comprend 2 organes sensoriels :
-‐ la cochlée : labyrinthe antérieur
Il s’agit d’un organe spiralé, siège de l’organe acoustique récepteur : organe de Corti. Il contient 2 types de cellules ciliées : les cellules ciliées internes (CCI) et les cellules ciliées externes (CCE). Les CCI font synapse avec la plupart des fibres du nerf cochléaire, et sont considérées comme les véritables cellules transductrices de la cochlée. Les CCE sont munies de propriétés contractiles et ont pour rôle de moduler l’information mécanique arrivant aux CCI.
-‐ le vestibule : labyrinthe postérieur
Voies nerveuses et centres nerveux auditifs :
Le nerf auditif chemine dans le conduit auditif interne et pénètre dans le tronc cérébral au niveau de la protubérance.
Les différents relais (noyaux cochléaires et complexe olivaire supérieur au niveau du tronc cérébral ; le colliculus inférieur au niveau du mésencéphale ; les corps genouillés médians au niveau du thalamus) conduisent l’information au thalamus puis au cortex auditif situé dans le lobe temporal.
2-‐2-‐ Physiologie de l’audition
La gamme de fréquences des sons audibles se situe entre 20 et 20000 Hertz chez l’homme normal.
On distingue un appareil de transmission assuré par l’oreille externe et l’oreille moyenne. Une atteinte de ces structures est responsable de surdité dite de transmission.
L’oreille externe localise les sons et les amplifie.
L’oreille moyenne transmet les sons à l’oreille interne et protège cette dernière contre les éventuelles agressions sonores.
Transmission des sons à l’oreille interne :
Les vibrations sonores sont transmises jusqu’à la fenêtre ovale grâce au système tympano-‐ossiculaire vers l’oreille interne. L’oreille moyenne a également un rôle d’amplificateur. Cette amplification est due au levier que constituent les osselets et surtout à la grande différence de surface tympan/fenêtre ovale. Une fréquence de 1000 Hz sera amplifiée par l’oreille moyenne de 30-‐35 dB.
Protection cochléaire :
Une stimulation sonore trop importante neutralise le système amplificateur, grâce à la mise en jeu du réflexe stapédien.
Il provoque la contraction du muscle de l’étrier. Il s’agit d’un réflexe poly-‐ synaptique, dont la voie afférente est assurée par la VIIIème paire crânienne, et la voie efférente par la VIIème paire. Ce réflexe est bilatéral. Une stimulation acoustique trop importante d’un côté déclenchera automatiquement le réflexe des 2 cotés.
Le temps de latence est d’environ 20 à 40 ms. Un son ayant une attaque rapide peut provoquer un traumatisme sonore.
L’appareil de perception est composé du nerf auditif (VIII), et des voies auditives centrales. L’atteinte de ces éléments provoque une surdité dite de perception.
3-‐ Epidémiologie
L'otite moyenne aiguë (OMA) représente la première infection bactérienne de l'enfant de moins de 5 ans. En effet, près d’un tiers des motifs de consultations pédiatriques sont liés aux OMA et à leurs séquelles (8).
Le pic de fréquence se situe entre 6 et 18-‐24 mois, selon les études. Avant
l’âge de 3 ans, 80 % des enfants auront eu un épisode d’OMA.
Certains facteurs favorisent la survenue des OMA :
-‐ la crèche et toute vie précoce en collectivité dans un habitat urbain (9) -‐ le tabagisme passif
-‐ les antécédents familiaux d’otites récidivantes -‐ l’absence d’allaitement maternel
-‐ la précarité des conditions de vie et d’hygiène -‐ les saisons automne-‐hiver
-‐ la récurrence des OMA est associée à la précocité de survenue du 1er épisode
-‐ l’utilisation d’une tétine de succion (par modification de l’équilibre de pression entre le nasopharynx et l’oreille moyenne).
Les enfants de sexe masculin seraient plus à risque selon une étude américaine réalisée à Boston (10).
Certaines études révèlent que la prévalence de cette pathologie est plus élevée chez certaines ethnies comme les Esquimaux, les Aborigènes australiens et les Indiens américains (8).
4-‐ Physiopathologie (11)
Toute OMA provient d’une affection rhinopharyngée par l’intermédiaire de la trompe d’Eustache.
Chez l’enfant, le rhinopharynx présente une charge infectieuse importante. L’enfance correspond à la période où l’individu n’est plus couvert par les anticorps maternels, et va devoir s’immuniser contre les divers agents pathogènes : c’est la
phase d’apprentissage immunitaire.
Ainsi les infections rhinopharyngées sont très fréquentes durant cette période, et vont être responsables d’une hypertrophie des végétations adénoïdes,
qui vont jouer le rôle de réservoir microbien. Cette hypertrophie va favoriser la stase des sécrétions nasales, provoquant la pullulation microbienne ainsi que des troubles de ventilation du cavum.
La fréquence importante des OMA s’explique par la coexistence de rhinopharyngites à répétition, et par le fait que la trompe d’Eustache est plus ou moins perméable, mais surtout plus courte et plus horizontale, favorisant ainsi la migration des germes (ces particularités anatomiques sont expliquées par la croissance crânio-‐faciale ; la morphologie adulte étant obtenu vers 6-‐7 ans).
5-‐ Bactériologie des OMA
Les micro-‐organismes en cause sont issus de la flore commensale du nasopharynx. L’oreille moyenne, physiologiquement stérile, est colonisée par ces agents pathogènes, le plus souvent dans les suites d’une infection virale.
Avant l’ère des antibiotiques, les trois germes les plus souvent rencontrés étaient Streptococcus pyogenes, Streptococcus pneumoniae et Staphylococcus aureus (8).
L’écologie s’est par la suite modifiée, sous l’influence probable de l’avènement des antibiotiques. Depuis les dernières décennies, les pathogènes les plus fréquemment trouvés sont Streptococcus pneumoniae, Haemophilus influenzae (20-‐50 %, selon les pays) et, dans une moindre mesure Moraxella catarrhalis. Cependant, plusieurs études montrent une augmentation du nombre des otites à M.
catarrhalis jusqu’à des taux de 20 % environ (8).
En France, H. influenzae (40 %) prédomine, devant S. pneumoniae (31 %) et M.
catarrhalis (8 %) (12).
Avant l’âge de 6 mois, l’épidémiologie bactérienne est un peu différente. Entérobactéries et Streptocoques bêta hémolytique du groupe A sont trouvés plus fréquemment.
Les autres espèces Streptococcus pyogenes, Staphylococcus aureus,
Alloiococcus otitidis et Turicella otitidis sont beaucoup plus rarement trouvées.
L’impact des bactéries à croissance difficile telle Chlamydiae et Mycoplasma
pneumoniae, est mal connu. A noter tout de même que les infections à plusieurs
germes représentent environ 10 % des OMA.
6-‐ Signes cliniques
L’otite moyenne aiguë correspond à une inflammation aiguë d’origine infectieuse des cavités de l’oreille moyenne (caisse du tympan et cavités mastoïdiennes).
Les signes fonctionnels sont l’otalgie et ses équivalents (enfant grognon se touchant l’oreille, pleurs, insomnie, irritabilité).
Les signes généraux sont dominés par la fièvre, ou l’hypothermie chez le nourrisson, les frissons, les céphalées. Parfois des symptômes digestifs (vomissements, diarrhées) peuvent être présents.
Le diagnostic est rarement fait à l’occasion d’une complication : convulsion hyperthermique, paralysie faciale, vertige, méningite.
L’otoscopie est caractérisée par l’inflammation de la membrane tympanique
associée à un épanchement rétro tympanique, extériorisé (otorrhée), ou non
extériorisé (opacité, effacement des reliefs normaux ou bombement).
On différencie plusieurs stades dans l’OMA :
-‐ stade congestif : le tympan est rosé ou rouge vif non bombant, avec disparition du triangle lumineux, mais les reliefs ossiculaires restent visibles, et il n’y a pas d’épanchement rétro tympanique.
-‐ Stade purulent ou suppuré ou collecté : le tympan est rouge vif (ou blanc laiteux), bombant, avec disparition du triangle lumineux et effacement des reliefs ossiculaires.
-‐ Stade purulent spontanément perforé : le tympan est rouge, bombé, avec une perforation punctiforme laissant soudre des gouttelettes de pus.
Figure 3 : otite moyenne aigüe droite collectée (11)
1) Tympan bombant, épaissi, érythémateux
2) Manche du marteau mal visible en raison du bombement de la membrane tympanique
Certaines particularités cliniques peuvent orienter vers l’agent causal :
-‐ Haemophilus influenzae : l’inflammation tympanique s’associe à une conjonctivite purulente, ce qui définit le syndrome otite-‐conjonctivite. Ces otites sont souvent peu fébriles et peu douloureuses.
-‐ Pneumocoque : la fièvre est souvent supérieure à 38.5 °C et les otalgies sont intenses.
-‐ Virus grippal : l’otite est en général bénigne mais très douloureuse. Le syndrome grippal oriente vers le diagnostic, et l’otoscopie le confirme : présence de phlyctènes hémorragiques au niveau du tympan, et/ou du conduit adjacent.
7-‐ Diagnostic différentiel
-‐ L’otite externe ou le furoncle du conduit : les douleurs sont exacerbées par la mastication, la pression du tragus ou la mobilisation du pavillon de l’oreille.
-‐ Le zona auriculaire : au stade initial, le diagnostic peut être difficile à faire, mais l’éruption dans la conque (zone de Ramsay-‐Hunt) signe le diagnostic. Une paralysie faciale peut être associée.
-‐ L’otalgie réflexe : surtout chez l’adulte, à rattacher à un problème pharyngé, dentaire ou articulaire (articulation temporo-‐mandibulaire). L’otoscopie est alors normale.
8-‐ Prise en charge et recommandations
Les dernières recommandations de l’AFSSAPS de novembre 2011 précisent clairement les indications de l’antibiothérapie dans la prise en charge de l’otite moyenne aigue (2).
8-‐1-‐ Stade congestif
Le traitement n’est que symptomatique :
-‐ Désobstruction rhinopharyngée : préférer le sérum physiologique aux vasoconstricteurs.
-‐ Instillations auriculaires, surtout à visée antalgique et décongestionnante.
-‐ Antalgiques, AINS et antipyrétiques par voie générale.
-‐ Les antibiotiques ne sont pas indiqués à ce stade.
-‐ La surveillance clinique et otoscopique associée au traitement symptomatique est souvent suffisante.
8-‐2-‐ Stade purulent 8-‐2-‐1-‐ L’antibiothérapie
a) Indications :
Chez l’enfant de moins de 2 ans, l’antibiothérapie d’emblée est recommandée (grade A).
Chez l’enfant de plus de 2 ans :
-‐ Si la symptomatologie est peu bruyante, l’abstention de toute antibiothérapie est recommandée en première intention. Il est également conseillé d’effectuer une réévaluation de l’enfant à 48/72 heures sous traitement symptomatique. L’antibiothérapie est alors conseillée en l’absence d’amélioration ou en cas d’aggravation.
-‐ Si la symptomatologie est bruyante (fièvre élevée, otalgie intense) ou s’il existe des difficultés de compréhension des consignes, une antibiothérapie peut-‐être prescrite d’emblée (grade B).
En cas de tympans mal ou non vus, l’antibiothérapie ne doit pas être prescrite à l’aveugle.
En cas de difficultés pour nettoyer les conduits auditifs externes :
-‐ après l’âge de 2 ans, en l’absence d’otalgie, le diagnostic d’OMA purulente est très peu probable
-‐ avant l’âge de 2 ans, si le diagnostic est évoqué, la visualisation des tympans est nécessaire et on doit avoir recours à un ORL
b) Choix de la molécule et posologie :
L’amoxicilline à la dose de 80-‐90 mg/kg/j en 2 ou 3 prises quotidiennes,
est à privilégier en première intention. Il s’agit de la molécule orale la plus efficace sur les pneumocoques de sensibilité diminuée à la pénicilline, et elle est active sur plus de 80 % des H. influenzae.
Si le temps entre les 3 prises ne peut être équidistant (toutes les 8 heures), il est préférable d’administrer le produit en 2 prises.
La durée du traitement varie selon les cas :
-‐ de 8 à 10 jours chez l’enfant de moins de 2 ans (grade A)
-‐ de 5 jours chez l’enfant de plus de 2 ans (accord professionnel)
Les autres antibiotiques ont un rapport bénéfice-‐risque défavorable (efficacité moindre : cefpodoxime, érythromycine-‐sulfafurazole, cotrimoxazole ; effets indésirables plus fréquents : amoxicilline-‐acide clavulanique, cefpodoxime, érythromycine-‐sulfafurazole, cotrimoxazole).
c) Cas particuliers :
On note néanmoins quelques cas particuliers où l’on préfèrera instaurer :
-‐ amoxicilline-‐acide clavulanique : syndrome otite-‐conjonctivite (forte probabilité d’Haemophilus influenzae),
-‐ cefpodoxime : allergie vraie aux pénicillines sans allergie aux céphalosporines,
-‐ érythromycine-‐sulfafurazole ou cotrimoxazole, en cas de contre-‐indication aux bêta-‐lactamines (pénicillines et céphalosporines),
-‐ l’utilisation de ceftriaxone en une seule injection IM doit rester exceptionnelle et se conformer à l’AMM uniquement (impossibilité à administrer un traitement par voie orale).
En cas d’évolution clinique favorable, le contrôle systématique des tympans en fin de traitement n’est pas nécessaire (2).
8-‐2-‐2-‐ Traitement symptomatique
La prise en charge médicamenteuse de la douleur chez l’enfant repose en première intention sur le paracétamol et sur l’ibuprofène en seconde intention.
En cas de douleur importante et persistante malgré les molécules de première ligne, on peut avoir recours à la codéine orale associée au paracétamol si l’enfant a plus d’un an.
8-‐2-‐3-‐ Paracentèse
Elle consiste en une incision dans le quadrant postéro-‐inférieur du tympan. Elle assure le drainage de l’abcèdation. Réalisée sous anesthésie dans la plupart des cas, ses indications sont limitées aux situations suivantes :
-‐ OMA collectée hyperalgique,
-‐ OMA collectée très fébrile résistante aux antipyrétiques,
-‐ toute situation nécessitant une bactériologie (complication, otites trainantes ou récidivantes, nourrisson de moins de 3 mois, déficit immunitaire, altération de l’état général).
9-‐ Complications (13)
9-‐1-‐ Otite séromuqueuse
Elle vient compliquer 10 à 20 % des OMA. Elle est à différencier de l’épanchement post-‐otitique. Cette complication très fréquente oblige tout patient ayant eu une OMA et dont l’évolution est suspecte d’évoquer le diagnostic d’otite séromuqueuse (évolution prolongée associée à une hypoacousie) à effectuer un contrôle otoscopique dans les 4 à 6 semaines suivant son épisode.
Le contrôle systématique des tympans après une OMA est discuté. Comme il a été noté ci-‐dessus, le collège français des enseignants ORL recommande un contrôle des tympans après une OMA dans les 4 à 6 semaines (11), alors que les dernières recommandations de la Fédération Française d’Infectiologie (2) préconisent, en cas d’évolution clinique favorable, de ne pas réexaminer les tympans après un épisode d’OMA.
9-‐2-‐ Mastoïdite aigüe
Cette complication est devenue rare (environ 2 cas pour 1000 otites) (14). Le diagnostic doit être suspecté devant une douleur spontanée ou à la palpation de la mastoïde, une voussure rétro-‐auriculaire refoulant le pavillon vers l’avant et le bas (signe de Jacques) et comblant le sillon auriculaire, ou en cas d’abaissement de la paroi postéro-‐supérieure du conduit auditif avec effacement de l’angle de raccordement du tympan au conduit auditif externe. Les signes d’accompagnement à type de fièvre et de signes généraux peuvent être plus ou moins marqués.
Un prélèvement anatomopathologique, obtenu par aspiration d’otorrhée, paracentèse ou ponction d’abcès sous-‐périosté rétro-‐auriculaire, est indispensable. Les germes les plus courants sont le Pneumocoque, l’Haemophilus ou le
Staphylocoque.
L’examen tomodensitométrique recherche des complications méningo-‐ encéphaliques.
En l’absence d’amélioration sous traitement antibiotique bien conduit, le traitement devient chirurgical, et repose sur une mastoïdectomie, sous couverture antibiotique large (6).
9-‐3-‐ Evolution prolongée et échec de l’antibiothérapie
Elle se manifeste par une persistance des signes généraux ou fonctionnels et/ou devant l’absence d’amélioration des signes otoscopiques.
Il est alors recommandé d’effectuer un prélèvement bactériologique (prélèvement d’otorrhée spontanée ou paracentèse), afin de mettre en place une antibiothérapie adaptée.
On parle d’évolution prolongée au-‐delà de 3 semaines malgré un ou plusieurs traitements antibiotiques.
L’hospitalisation est parfois nécessaire devant l’importance des signes généraux.
L’évolution sous antibiothérapie permet de distinguer 2 types de tableaux :
-‐ l’otite trainante : amélioration franche des signes généraux et de l’aspect tympanique sous antibiothérapie adaptée
-‐ la mastoïdite sub-‐aiguë : peu ou pas d’amélioration sous antibiotiques adaptés. Le traitement chirurgical par mastoïdectomie s’impose alors (rare de nos jours).
9-‐4-‐ Labyrinthite
Elle se manifeste par une impression d’instabilité ou des vertiges, des nausées et/ou vomissements. Il convient de rechercher un nystagmus, qui peut être homolatéral à la lésion (nystagmus d’irritation), ou controlatéral (nystagmus de destruction, plus péjoratif).
Le traitement est symptomatique : anti-‐émétiques et anti-‐vertigineux ; ainsi que curatif par antibiothérapie parentérale à fortes doses, nécessaire afin d’éviter l’extension méningée. Dans certains cas, on peut avoir recours à la chirurgie.
9-‐5-‐ Paralysie faciale périphérique
L’installation est brutale et précoce, le pronostic favorable, avec régression des symptômes sous traitement antibiotique adapté. Un traitement par corticoïde peut être ajouté, une fois le germe identifié et contrôlé par les antibiotiques.
9-‐6-‐ Complications endocrâniennes (6)
Les complications endocrâniennes sont devenues très rares.
Méningite :
Elle survient par extension de l’infection au travers du labyrinthe, du sinus latéral, ou par passage direct depuis l’oreille moyenne.
Abcès cérébraux du lobe temporal :
La fièvre est élevée et on retrouve des signes neurologiques (céphalées et vomissements) avec possibilité de complications : hypertension intracrânienne,
déficits neurologiques sensitifs, moteurs ou visuels. Le traitement repose sur une antibiothérapie parentérale à fortes doses et sur un drainage neurochirurgical par ponction.
Abcès cérébelleux :
Bien que rare, la persistance de céphalée et la présence d’un syndrome cérébelleux doivent faire évoquer le diagnostic. L’imagerie en urgence s’impose, ainsi que le drainage chirurgical.
Thrombophlébite du sinus latéral :
Elle est en règle générale la conséquence d’une extension postérieure de mastoïdite. La fièvre est élevée, et il existe un syndrome méningé, qui n’est pas souvent franc, et ce d’autant moins qu’une antibiothérapie a été administrée préalablement. L’imagerie cérébrale s’impose et le traitement chirurgical consiste en une mastoïdectomie.
III-‐ Antibiotiques et otite moyenne aiguë
Les antibiotiques ont été la plus grosse avancée thérapeutique de la médecine dans la seconde moitié du XXème siècle. En revanche, le début du troisième millénaire s’ouvre sur une crainte majeure : la résistance croissante des bactéries aux antibiotiques, qui pose un sérieux problème de santé publique.
Face à ce problème, divers plans antibiotiques se sont succédés afin de maîtriser et rationnaliser la prescription.
1-‐ Historique des antibiotiques
Les propriétés antiseptiques des plantes étaient utilisées de façon empirique : les Egyptiens distribuaient de l’ail aux ouvriers des pyramides afin de les protéger.
Ce n’est par contre que vers la fin du XIXème siècle qu’on fit le lien entre maladies et microbes, et que la théorie des germes commença à voir le jour (15).
En 1879, Neisser attribua la blennorragie à un microbe, et en 1880, Pasteur atténua la virulence de certains agents pathogènes afin qu’ils servent à immuniser contre les maladies, plutôt qu’à les provoquer (les prémices de la vaccination).
En 1889, l’Allemand Rudolf Emmerich fut le premier à découvrir une substance antibiotique : la pyocyanase, qui avait comme propriétés celle de détruire certains agents pathogènes de la typhoïde, du charbon, de la peste, la diphtérie ou certains abcès cutanés. Mais devant le caractère instable et toxique de cette substance, cette découverte fut nuancée.
En 1890, Von Behring et Kitasato mirent en évidence que des antitoxines étaient présentes dans le sang d’individus qui se rétablissaient d’un épisode de diphtérie.
Le 3 septembre 1928, à l’hôpital Sainte Marie de Londres, le docteur Alexander Fleming, de retour de vacances fit une découverte inattendue. Il s’aperçut que ses cultures de Staphylocoque avaient été contaminées par des colonies de moisissures issues de souches d’un champignon qu’utilisait son voisin de paillasse. Il remarqua que le Staphylocoque ne s’était pas développé autour de ses moisissures et émit l’hypothèse qu’une substance sécrétée par le champignon empêchait le développement du Staphylocoque.
Fleming venait de découvrir la pénicilline, dont les implications médicales ne furent réelles que quelques années plus tard, grâce aux travaux de 2 autres chercheurs : Howard Florey et Ernst Chain. Tous trois furent récompensés en 1945 du prix Nobel de médecine.
La découverte des antibiotiques a changé le monde plus qu’aucune autre classe de médicaments et a réduit de 90 % la mortalité due aux maladies infectieuses dans les pays développés.
Grâce à eux, des grands fléaux comme la tuberculose (responsable de 50 000 morts en France en 1940), la typhoïde, le choléra, la lèpre, la syphilis ont en partie disparu, … du moins dans les pays riches.
2-‐ Résistance aux antibiotiques des germes impliqués dans l’otite
moyenne aiguë (8)
La découverte des antibiotiques fut une avancée thérapeutique majeure. Néanmoins, leur utilisation, souvent par excès, a eu pour conséquence de faire accroître considérablement les niveaux de résistance des bactéries aux antibiotiques. Ces résistances n’épargnent pas les germes en cause dans l’otite moyenne aiguë.
2-‐1-‐ Streptococcus pneumoniae 2-‐1-‐1-‐ Mécanisme de résistance
2-‐1-‐1-‐1-‐ Résistance à la pénicilline
La résistance des pneumocoques à la pénicilline G est liée à une diminution d’affinité des protéines liant les pénicillines (PLP). Ces PLP sont des enzymes qui permettent la synthèse du peptidoglycane, principal élément de la paroi bactérienne. Cette résistance est chromosomique, et provient d’événements de transformation et de recombinaison intra-‐ ou inter-‐espèces avec des streptocoques de la flore oropharyngée.
Sensibilité, résistance de bas niveau (ou de niveau intermédiaire), résistance de haut niveau à la pénicilline :
Une souche est considérée comme sensible à la pénicilline lorsque la concentration minimale inhibitrice (CMI) est strictement inférieure à 0,125 mg/L. Les pneumocoques de sensibilité diminuée à la pénicilline (PSDP) sont répartis en 2 sous classes :
-‐ résistance de bas niveau si la CMI est comprise entre 0,125 et 1 mg/L,
-‐ résistance de haut niveau si la CMI est strictement supérieure à 1 mg/L.
Certains arguments cliniques doivent faire suspecter un risque de PSDP :
-‐ Age < 18 mois,
-‐ prise récente d’une amino-‐pénicilline dans les 3 mois, -‐ vie en collectivité (crèche).
2-‐1-‐1-‐2-‐ Résistance aux macrolides
Les macrolides luttent contre la prolifération bactérienne par inhibition de la synthèse protéique au niveau de l’ARN des micro-‐organismes.
La résistance des pneumocoques aux macrolides résulte d’une levée de l’inhibition de cette synthèse protéique bactérienne.