On note sur le tableau 1 que :
Tanins catéchiques
Ils sont présents dans toutes les plantes : les feuilles d’Urtica dioica et de Pétroselinum sativum ainsi que les graines de l’Hordeum vulgare et de Nigella sativa
. Tanins galliques
Les tanins galliques ont été détectés seulement dans les feuilles du Thymus vulgaris.
Alcaloïdes
Ils sont présents dans les organes testés de chaque plante avec des teneurs allant de 0,1 à 1 %, la plus importante a été enregistrée chez les graines de l’ Hordeum vulgare.
Saponosides
Ils ont été détectés seulement chez les graines de Nigella Sativa et les feuilles du Pétroselim Sativum. L’indice de mousse dans ce dernier est très important, de l’ordre de 2000.
Anthraquinones
Elles sont présentes avec un taux important dans les feuilles du Thymus vulgaris et Urtica dioica. Les autres parties des plantes y sont dépourvues.
Flavonoides
La phytochimie a révélé leurs présences dans toutes les plantes à l’exception des graines de Nigella Sativa.
Coumarines
Elles sont surtout présentes dans les feuilles d’Urtica dioica, Matricaria cammomilla et Thymus vulgaris
.Maintenant que nous avons déterminé les familles actives dans les plantes étudiées, nous essayons de tester leur effet antibactérien sur Escherichia Coli, Staphylococcus aureus, Klebsiella Pneumoniae et Pseudomonas Aeuriginosa, en se mettant dans les conditions d’utilisations des plantes par les malades.
Les mêmes plantes ont été soumises par la suite à une extraction par solvants organiques de polarité croissante afin de localiser le ou les principes actifs responsables de l’activité antibactérienne [80] et d’extraire le plus de principes actifs.
II-7 Préparation des solutions des substances naturelles
Pour notre étude, nous avons choisi les méthodes de préparation utilisées en Algérie, la décoction et la macération.
54
Nous avons varié les temps de préparation pour chaque tisane :
La décoction a été prévue à 15 minutes et à 1 heure.
La digestion à 3 heures et à 45 minutes.
Enfin la macération à 24 heures et à 72 heures.
Différents types d'extraits ont été préparées à partir de la poudre des organes des plantes utilisées [89].
II-7-1 Décoction
Nous avons effectué une décoction à 10%. 250 g de poudre ont été mis dans 2500 ml d'eau distillée et porté à ébullition pendant le temps voulu. Le mélange refroidi a été filtré. Le filtrat récupéré est appelé décocté. Ce dernier est concentré au rotavapor (buchi switzerland) à 40 ° C et conservés dans des bocaux stériles à - 20° C.
II-7-2 Macération
Une macération aqueuse a également été effectuée sur 50 g de poudre avec 500ml d'eau pendant le temps déterminé. L’extrait récupéré après filtration est appel é marc. Ce dernier a été concentré au rotavapor à 40 ° C et conservé à - 20° C.
II-7-3 Digestion à 50 ° C
250 g de poudre ont été mis dans 2500 ml d'eau distillée et porté à 50 ° C pendant 3 heures ou 45 minutes.
Après filtration, le digeste a également été concentré par rotavapor à 40 ° C et conservé à - 20° C.
II-7-4 Extraction par des solvants à polarité croissante
L’extraction par solvant consiste à séparer les constituants d’un mélange à l’aide d’un solvant volatil qui ne se mélange pas avec l’eau. Le solvant se charge des molécules à extraire grâce à sa forte affinité avec elles. Pour récupérer les principes actifs, on élimine ensuite le solvant par distillation.
L'extraction par solvant sert à extraire les huiles essentielles des écorces et des racines des plantes aromatiques, qui supportent mal la chaleur de la distillation [78].
Mode opératoire
Les plantes sont soumises à l’extraction par solvant organique de polarité croissante afin de localiser le ou les principes actifs responsables de cette activité inhibitrice. Chaque solvant permettant d’extraire un ensemble de composés secondaires (tableau 16).
II-7-4-1 Extraction par l’éther de pétrole
250 g de poudre de chaque plante ont été mélangés avec 1500 ml d'éther de pétrole et placés sous agitation.
55
Chaque 24 heures, on rajoute 500ml de ce solvant pendant trois jours.
II-7-4-2 Extraction par le dichlorométhane
Après filtration sur papier Whatmann, le résidu de l'extraction précédente est mis en agitation avec 1500 ml de dichlorométhane. Le mélange est ensuite filtré.
II-7-4-3 Extraction par le méthanol
Le troisième solvant utilisé est le méthanol ; 1500 ml de ce dernier est mélangé avec le résidu précédant et mis en agitation pendant 3 jours.
II-7-4-4 Extraction par l’éthanol
Le résidu de l'extraction par le méthanol a été repris avec 1500ml d'éthanol à 80 % en moyenne de 500 ml par jour et laissé sous agitation pendant trois jours.
II-7-4-5 Préparation de la solution aqueuse
A la fin de l'extraction avec les solvants organiques et après filtration, la poudre épuisée a été séchée pendant 24 h, puis porté à 50 ° C puis à 100 ° C avec 1,5 litre d'eau distillée, à chaque fois pendant 3 heures. Les extraits sont ensuite concentré sous vide à 40 ° C à l’aide d’un rotavapor et conservés à - 20 ° C.
La figure 9 résume les étapes du mode opératoire.
56
57
Extrait éthéré Concentré sous vide à 40 0C
et conservé à -20 ° C
Résidu de poudre Poudre de plante 250g
Éther de pétrole 1500ml Agitation+filtration
Résidu de poudre Dichlorométhane 1500ml
Agitation+filtration
Résidu de poudre Méthanol 1500ml
Agitation+filtration
Éthanol 1500ml Agitation+filtration
Résidu de poudre Digestion 50 0C
Décoction
Figure 9 : Extraction par solvants à polarité croissante de la poudre des plantes
Extrait dichlorométhané Concentré sous vide à 40 0C
et conservé à -20 ° C
Extrait méthanolé Concentré sous vide à 40 0C
et conservé à -20 ° C
Extrait éthanolé Concentré sous vide à 40 0C
et conservé à -20 ° C
Agitation+filtration
Solution aqueuse Concentré sous vide à 40 0C
et conservé à -20 ° C poudre épuisée
Tableau 16 : les composés libérés par des solvants organiques lors d’une extraction [70,78].
Solvants utilisés Composés libérés
Ether de pétrole Alcaloïdes, terpènes, coumarines, acides gras
dichlorométhane Les terpènes
Méthanol Anthocyanine, tanins, saponines, flavones, phénones, polyphénol Ethanol Tanins, polyphénoles, flavonol, terpènes, stéroles, alcaloïdes.
Eau froide Protéines, acides aminés, gommes, mucilages, sels minéraux
Eau bouillante Amidon, pectines
II-8 Etude de l'effet des extraits des plantes sur les bactéries II-8-1 Microgrammes
Les germes utilisés dans la détermination de l’activité antibactérienne des différents extraits des plantes sont les suivants : Gram (+) : Staphylococcus aureus (ATCC 25923) ; Gram (-) négative : Klebsiella
Pneumoniae (ATCC 35657), Pseudomonas Aeuriginosa (ATCC 10145), E.Coli (ATCC 11775).
Rappelons que ces bactéries sont responsables de la lithiase d’infection.
II-8-2 Etude de l'activité antibactérienne
Les extraits obtenus des différentes plantes ont été pesés et dissous dans le diméthyle sulfoxide (DMSO) de façon à obtenir une concentration finale de 100 mg/ml. Ces derniers ont été filtrés à travers des filtres de 0,45 µm de diamètre et conservés à 4 ° C.
Nous avons adopté pour l'étude de l'activité antibactérienne, la méthode de diffusion du disque [90]. Des disques de papier buvard vierges de 6 mm de diamètre numérotés de 1 à 12 ont été imprégnés avec 10 µl d’extrait préparé (100 mg/ml). Ces derniers sont mis en contacte avec les milieux de culture Muller Hinton, préalablement ensemencé avec un inoculum de 10
6UFC /ml
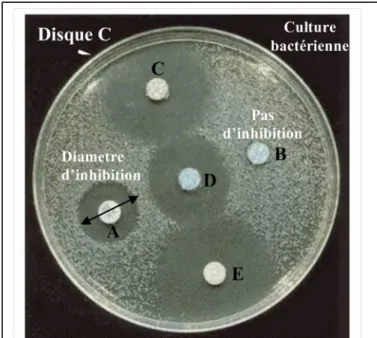
-1des souches bactériennes dans des boites de pétri [91]. Un disque imprégné par 10 µl de DMSO est considéré comme témoin. Les boites sont incubées à 37° C. Après 24 H d'incubation, l'activité antibactérienne est évaluée en mesurant le diamètre des zones d’inhibition de chaque souche bactérienne en millimètre. L’absence de la zone d’inhibition est traduite par l’absence de l’activité antibactérienne (figure 10).
58
II-8
-2-1 Etude de l’effet des extraits de Matricaria chamomilla a) Escerichia coli
Les photographies 1, 2 et 3 montrent l’effet des extraits de Matricaria chamomilla sur Escherichia coli, Staphylococcus aureus et Klebseilla pneumoniae avec leurs diamètres des zones d’inhibition (d).
59
Figure 10 : antibiogramme par la méthode de diffusion en milieu gélose (A, B, C, D, E : disques imprégnés des extraits différents.
Photo 1 : (1) : l’effet des plus importants extraits de Matricaria chamomilla sur Escherichia coli.
L’extrait d’éther de pétrole (1) (d=28mm). (2) : dichlorométhane (d=10mm). (3) :l’extrait du méthanol (d= 6 mm). (4) : l’extrait d’éthanol (d= 6 mm). (5) : témoin (d= 6 mm). (10) : marc 24h (d= 6 mm).
(11) : digeste 45 min (d= 6 mm). (12) : décocté de 15 min (d=40 mm).
2 1
3
4
5
1 0
1 1 1
2
D’après cette figure, le décocté de 15 min de cette plante exerce un effet inhibiteur remarquable sur la souche Esckerichia Coli avec un diamètre de la zone d'inhibition de 40mm, suivi par l’extrait d'éther de pétrole qui a pour diamètre 28mm.
Pour les plantes, l’activité antibactérienne est considérée importante pour les extraits dont le diamètre des zones d’inhibition est supérieur ou égale à 15 mm [92].
b) Staphylococcus aureus
D’après cette photographie, on remarque que pour Staphylococcus aureus c’est le marc de 24 heures qui a inhibé le plus ce germe avec une zone d’inhibition de 30mm diamètre. Les autres extraits étaient sans effets
c) pseudomonas aeruginosa
Pour cette souche, on a enregistré un effet antibactérien moyen des extraits de Matricaria chamomilla vis-à-vis de cette bactérie. Les plus actifs sont le marc de 72heures, digeste de 3 heures et le décocté d’une heure avec des zones d’inhibition de 16 mm et 18mm respectivement.
60
Photo 2 : L’effet des plus importants extraits de Matricaria chamomilla sur Staphylococcus aureus.
(10) : marc de 24h (d=30 mm). (11) : digeste 45 min (d= 6mm). (12) décocté 15 min (d= 6mm).
1 0
1 1 1
2
Cette figure nous montre l’importance de l’effet antibactérien de quelques extraits de cette plante vis-à-vis de Klebsiella pneumoniae. Tels que les extraits, 2, 3, 6 et 10 qui correspondent respectivement aux dichlorométhane, méthanol, marc de 72h et celui de 24 h avec des zones d’inhibition de 26 mm, 38 mm, 35 mm et 40 mm.
Les résultats des études expérimentales de l’effet des extraits de Matricaria chamomilla sur
ueNuméro du disq 1 2 3 4 5 6 7 8 9 10 11
Solvants Ether
de pétrole
Dichloro-
méthane Méthanol Ethanol Témoin DMSO
Marc 72h
Digeste 3h
Décocté 1h
Solution aqueuse Marc
24h
Digeste 45min
Diamètre des zones d’inhibition pour chaque bactérie en (mm)
Escherichia coli
28 8 6 6 6 6 6 6 11 6 6
Staphylococcus aureus
28 16 18 16 6 25 6 18
6 30 6
Pseudomonasaeruginosa
7 7 6 6 6 16 16 18 6 6 6
Klebsiella
pneumoniae
6 26 38 6 8 35 8 6 6 40 6
les bactéries pathogènes sont représentés dans tableau 17.
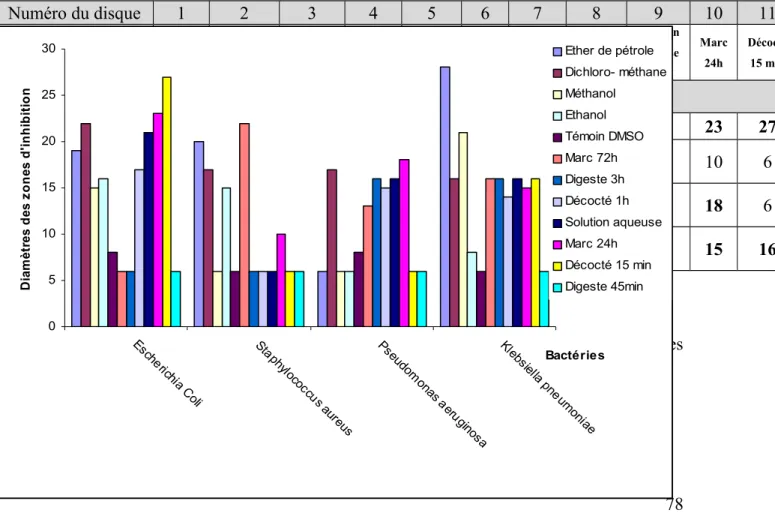
Sur l’histogramme 1, nous avons reporté les diamètres des zones d’inhibition en mm pour chaque bactérie.
Tableau 17: l’effet des extraits de Matricaria chamomilla sur les bactéries exprimé en diamètre des zones d’inhibition en mm.
61
0 5 10 15 20 25 30 35 40 45
Bactéries
Diamètres des zones d'inhibition
Ether de pétrole Dichloro- méthane Méthanol
Ethanol Témoin DMSO Marc 72h Digeste 3h Décocté 1h Solution aqueuse Marc 24h Décocté 15 min Digeste 45min
Histogramme 1: L’effet de Matricaria chamomilla sous différents modes de préparations sur les souches bactériennes représenté par le diamètre des zones d’inhibition
Photo 3 : (1) : L’effet des plus importants extraits de Matricaria chamomilla sur Klebsiella pneumoniae L’extrait d’éther de pétrole (d=6mm). (2) : l’extrait du dichlorométhane (d= 26mm). (3) l’extrait du méthanol (d= 38mm). (6) : marc de 72 h (d=35 mm). (10) : marc de 24 h (d= 40 mm). (4) : l’extrait d’éthanol (d=6mm). (5) : témoin (d=8mm). (7) : digeste 3h (d=6mm). (8) : décocté 1h (d=6mm). (9) : solution aqueuse (d=6mm). (11) : digeste 45min (d=6mm). (12) : décoction 15 min (d=6mm).
1
5 4
3 2
8 4 7
9
6
1
2 1
1
1
0
A partir de ces résultats, nous constatons que toutes les bactéries sont sensibles au moins à deux extraits de Matricaria chamomilla. Les bactéries les plus sensibles à cette plante sont Klebsiella pneumoniae et E.coli. La sensibilité de Pseudomonas aerugenosa, aux extrais de cette plante était moins importante. Le seul pouvoir antibactérien enregistré est celui du décocté de 1h avec une zone d’inhibition de 18 mm.
II-8
-2-2 Etude de l’effet des extraits d’Urtica dioica
Sur les photographies 4,5 et 6 sont représentés les effets des extraits d’Urtica doica sur E.coli, Staphylococcus aureus et Pseudomonas aeruginosa respectivement avec leurs diamètres des zones d’inhibition (d)
a) Escherichia coli
62
La photographie 4 montre la sensibilité de cette souche aux extraits 1,2 et 4 qui correspondent respectivement aux extraits d’éther de pétrole, de dichlorométhane et d’éthanol. Ce dernier a provoqué la plus importante zone d’inhibition (d = 32 mm). Les extraits 1 et 2 semblent avoir un effet en synergie.
b) Staphylococcus aureus
L’extrait du méthanol a marqué un diamètre de 32 mm. Rappelons que le témoin (DMSO)
63
Photo 4 : l’effet des plus importants extraits d’Urtica doica sur E. coli. (1) : de l’extrait d’éther de pétrole (d=
27mm). (2) : l’extrait de dichlorométhane (d=11mm). (3) : l’extrait du méthanol (d= 6 mm). (5) : témoin (d= 6 mm). (4) : l’extrait d’éthanol (d=32mm).
1
2
3
4 5
Photo 5: (1) : l’effet des plus importants extraits d’Urtica doica sur Staphylococcus aureus. (1) éther de pétrole (d= 6 mm). (2) dichlorométhane(d= 6 mm). (4) : éthanol (d= 6 mm). (5) : témoin (d= 6 mm). (3) : l’extrait du méthanol (d=32mm).
1
2
3
4 5
n’exerce aucun effet sur cette bactérie.
c) Pseudomons aeruginosa
Cette souche est sensible à l’extrait de l’éther de pétrole et celui de dichlorométhane avec des zones d’inhibition de 20mm et 16 mm respectivement.
d) Klebsiella pneumoniae
Le marc de 24 heures et le décocté de 15 minutes de cette plante ont donné l’activité antibactérienne la plus importante avec cette bactérie. Les zones d’inhibitions enregistrées sont 27mm et 25 mm respectivement.
Le tableau 18, regroupe les diamètres des zones d’inhibition pour chaque plante et chaque bactérie.
Tableau 18: l’effet des extraits d’Urtica doica sur les bactéries exprimé en diamètre
64
64
Photo 6 : l’effet des plus importants extraits d’Urtica doica sur pseudomonas aeruginosa.
(1) : l’extrait d’éther de pétrole (d= 16mm). (2) : l’extrait dichlorométhane (d= 20mm). (3):
l’extrait de méthanol (d= 6 mm). (4) : l’éthanol (d= 6 mm). (5) : témoin (d= 6 mm). (6) : marc 72h (d= 6 mm). (7) : digeste 3h (d= 6 mm). (8) : décocté 1h (d= 6 mm). (9) : solution aqueuse (d=
25mm).
1
2 3
4 5
6
7 8
9
Numéro du disque 1 2 3 4 5 6 7 8 9 10 11
Solvants Ether
de pétrole
Dichloro-
méthane Méthanol Ethanol Témoin DMSO
Marc 72h
Digeste 3h
Décocté 1h
Solution aqueuse Marc
24h
Décocté 15 min
Diamètre des zones d’inhibition pour chaque bactérie en (mm)
Escherichia coli
27 11 6 8 8 6 25 6 6 20 17
Staphylococcus
aureus
6 17 32 18 6 19 6 6 6 17 23
Pseudomonas
aeruginosa
16 20 6 6 6 19 19 19 25 15 28
Klebsiella
pneumoniae
6 28 18 6 6 18 6 6 6 27 25
L’histogramme 2 regroupe les différents diamètres des zones d'inhibition engendrées par les extraits de la plante Urtica dioica sur les différents germes.
D’après cet histogramme, on remarque que cette plante sous ces différents modes d’extractions exerce un effet important sur toutes les bactéries testées.
65
0 5 10 15 20 25 30 35
Bactéries
Diamètres des zones d'inhibition Ether de pétrole
Dichloro- méthane Méthanol
Ethanol Témoin DMSO Marc 72h Digeste 3h Décocté 1h Solution aqueuse Marc 24h Décocté 15 min Digeste 45min
Histogramme 2 : L’effet d’Urtica dioica sous différents modes de préparations sur les souches bactériennes représenté par le diamètre des zones d’inhibition
Les bactéries étaient sensibles aux extraits préparés par l'eau surtout ceux de courte durée; du marc de 24 h, du décodé de 15 min et du digeste de 45 min.
La bactérie la plus sensible à cette plante est Staphylococcus aureus. Cette dernière est largement sensible à l’extrait du méthanol.
II-8
-2-3 Etude de l’effet des extraits de Petroselinum Sativum a) Escherichia coli
Les photographies suivantes illustrent d’après les boites de pétri incubés 24 h à 37° C, l’effet des extraits de Petroselinum Sativum sur les bactéries avec leurs diamètres des zones d’inhibition (d).
La détermination du diamètre des zones d’inhibition a révélé que la souche E.coli est sensible à la majorité des extraits de cette plante. La plus importante zone enregistrée est celle du marc de 72 h de diamètre (d=35mm), suivi par celle de la solution aqueuse et du décocté de 15 min avec des diamètres des zones d’inhibition de 32 mm et 30mm respectivement.
Le diméthyle sulfoxide (DMSO) qui représente le témoin est resté sans effet.
b) Staphylococcus aureus
66
Photo 7 : l’effet des plus importants extraits de Petroselinum Sativum sur E. coli. (5) : témoin (d=
6mm). (6) : marc de 72 h (d= 35mm). (7) : digeste de 3h (d=17mm). (8) : décocté 1h (d=18 mm). (9) : solution aqueuse (d=32 mm). (10) : marc 24 h (d=25mm). (11) : décocté de 15min (d= 30 mm). (12) : digeste 45 min (d= 6mm).
12
Staphylococcus aureus est sensible à la majorité des extraits aqueux. Le plus important effet enregistré est celui du marc de 24 h (d= 35 mm), suivi de la solution aqueuse (d= 32 mm) et du marc de 72h (d= 30 mm).
c) Pseudomonas aeruginosa
Les extraits de cette plante ont exercé une activité antibactérienne moyenne vis-à-vis de cette bactérie par rapport aux autres plantes. L’extrait du dichlorométhane et que le décocté de 15 minutes ont provoqués les zones d’inhibitions les plus importantes avec un diamètre de 18 mm.
d) Klebsiella pneumoniae
Photo 9 : l’effet des plus importants extraits de Petroselinum Sativum sur Klebsiella pneumoniae.
67
(1) : l’extrait d’éther de pétrole (d=19mm). (2) : l’extrait de dichlorométhane(d= 6mm). (3) : méthanol (d= 6mm). (4) : l’extrait d’éthanol (d=22 mm). (9) solution aqueuse (d= 36 mm). (10) : marc de 24h (d=
6mm). (11) : décocté de 15 min (d= 6mm). (12) : digeste de 45 min (d=6mm).
12
Photo 8 : l’effet des plus importants extraits de Petroselinum Sativum sur S.aureus. (5) : témoin (d=6mm). (6) : marc de 72h (d=30mm). (7) : digeste de 3h (d=14 mm). (8) : décocté 1h (d=12mm). (9) : solution aqueuse (d=32mm). (10) : marc de 24 h d= (35 mm). (11) : décocté de 15 min (d= 6mm) (12) : digeste de 45 min (d= 6mm).
12
Cette bactérie est sensible surtout à la solution aqueuse avec un diamètre de 36 mm. Pour les extraits d’éthanol et d’éther de pétrole, les zones d’inhibition enregistrées sont respectivement de 22 mm et 19mm.
Pour pouvoir comparer l’effet de cette plante avec ces différents modes d’extraction sur les quatre souches étudiées, nous avons regroupé les diamètres des zones d’inhibition sur le tableau 19.
Tableau 19 : Effet des extraits de Petroselinum Sativum sur les bactéries, exprimé en diamètre des zones d’inhibition en mm.
Numéro du disque 1 2 3 4 5 6 7 8 9 10 11
Solvants
Ether de pétrole
Dichloro-
méthane Méthanol Ethanol Témoin DMSO
Marc 72h
Digeste 3h
Décocté 1h
Solution aqueuse Marc
24h
Décocté 15 min
Diamètre des zones d’inhibition pour chaque bactérie en (mm)
Escherichia coli
16 20 18 16 8 35 17 18 32 25 30
Staphylococcus
aureus
6 6 6 13 6 30 14 12 32 35 6
Pseudomonas
aeruginosa
16 18 16 15 8 12 13 15 17 15 18
Klebsiella
pneumoniae
19 8 10 22 6 6 6 6 36 6 6
Nous avons représenté sur l’histogramme 3, L’effet de Petroselinum Sativum sous différents modes de préparations sur les souches bactériennes exprimé par le diamètre des zones d’inhibition en mm.
68
La majorité des bactéries de l’infection sont sensibles aux extraits de Petroselinum Sativum.
Les souches les plus sensibles sont l’Escherichia Coli, le Staphylococcus aureus et le Klebsiella pneumoniae, qui ont marqué des diamètres des zones d’inhibition allant de 19 à 36mm.
II-8
-2-4 Etude de l’effet des extraits de Thymus vulgaris
a) Escerichia coli
69
0 5 10 15 20 25 30 35 40
Bactéries
Diamètres des zones d'inhibition
Ether de pétrole Dichloro- méthane Méthanol Ethanol Témoin DMSO Marc 72h Digeste 3h Décocté 1h Solution aqueuse Marc 24h Décocté 15 min Digeste 45min
Histogramme 3 : L’effet de Petroselinum Sativum sous différents modes de préparations sur les souches bactériennes exprimé par le diamètre des zones d’inhibition en mm
Cette souche est sensible à l’extrait de l’éther de pétrole et le décocté d’une heure avec des zones d’inhibition de 28mm et 18mm respectivement. L’effet de l’extrait de dichlorométhane n’est pas négligeable, le diamètre de la zone d’inhibition enregistré est de 17mm.
b) Staphylococcus aureus
Tous les extraits de cette plante n’exercent aucun effet antibactérien contre Staphylococcus aureus.
c) Pseudomonas aeruginosa.
La photographie ci-dessous illustre les zones d’inhibition de Pseudomonas aeruginosa engendrées par quelques extraits de Thymus vulgaris avec leurs diamètres (d).
70
Photo 10 : L’effet des plus importants extraits de Thymus vulgaris sur E.coli. (1) : l’extrait d’éther de pétrole (d=28mm). (2) : l’extrait du dichlorométhane (d= 17mm). (3) :l’extrait du méthanol (d= 6mm).
(4) : l’extrait d’éthanol (d= 6mm). (5) : témoin (d= 6mm). (6) : marc 72h (d= 6mm). (7) : digeste 3h (d=
6mm). (9) solution aqueuse (d= 6mm). (8) : décocté 1h (d=18 mm).
1
2 3
4 5
6
7 8
9
Photo 11 : L’effet des plus importants extraits de Thymus vulgaris sur pseudomonas aeruginosa. (1) : l’extrait d’éther de pétrole (d= 6mm). (2) : l’extrait du dichlorométhane (d=26mm). (3) :l’extrait du méthanol (d= 6mm). (4) : l’extrait d’éthanol (d= 6mm). (5) : témoin DMSO (d= 6mm).
1
2
3
4 5
L’extrait de dichlorométhane a provoqué une zone d’inhibition de Pseudomonas aeruginosa de 26 mm de diamètre. Cette souche résiste aux autres extraits.
d) Klebsiella pneumoniae
L'effet antibactérien de cette plante a été enregistré pour Klebsiella pneumoniae avec les solutions aqueuses : (décoction de 15 min, digestion de 45min, macération de 24 h et de 72 h), avec des zones d'inhibition allant jusqu’à 32 mm, de diamètre.
Nous avons regroupé sur le tableau 20, les diamètres des zones d’inhibition des différents extraits testés sur les bactéries.
Tableau 20 : l’effet des extraits de Thymus vulgaris sur les bactéries exprimé en diamètre des zones d’inhibition en mm
1 2 3 4 5 6 7 8 9 10 11
71
Photo 12 : L’effet des plus importants extraits de Thymus vulgaris sur Klebsiella pneumoniae (6) : marc de 72h (d= 18mm). (7) : digeste de 3h (d= 6mm). (8) : décocté 1h (d= 6mm). (9) : solution aqueuse (d= 6mm). (10) : marc de 24 h (d=23 mm). (11) : décocté de 15 min (d=32mm) (12) : digeste de 45 min (d=25mm).
6
7
8 9
1 0
1 1 1
2
Numéro du disque
Solvants Ether de pétrole
Dichloro-
méthane Méthanol Ethanol Témoin DMSO
Marc 72h
Digeste 3h
Décocté 1h
Solution aqueuse Marc
24h
Décocté 15 min
Diamètre des zones d’inhibition pour chaque bactérie en (mm)
Escherichia coli
28 17 6 6 6 6 6 18 6 6 6
Staphylococcus
aureus
6 6 6 6 6 6 6 6 6 6 6
Pseudomonas
aeruginosa
6 26 6 6 6 10 6 10 10 6 6
Klebsiella
pneumoniae
6 8 6 9 6 18 8 10 6 23 32
L’histogramme 4 représente les diamètres des zones d’inhibition de chaque bactérie.
D’après ces résultats, nous déduisons que l’effet du Thymus vulgaris, sur les bactéries est moins important par rapport aux autres plantes. On note une absence totale de l’activité inhibitrice pour la souche Staphyloccocus aureus.
II-8
-2-5 Etude de l’effet des extraits d’Hordeum vulgare
72
0 5 10 15 20 25 30 35
Bactéries
Diamètres des zones d'inhibition
Ether de pétrole Dichloro- méthane Méthanol
Ethanol Témoin DMSO Marc 72h Digeste 3h Décocté 1h Solution aqueuse Marc 24h Décocté 15 min Digeste 45min
Histogramme 4 : L’effet de Thymus vulgaris sous différents modes de préparations sur les souches bactériennes représenté par le diamètre des zones d’inhibition
Staphylococcus aureus, Pseudomonas aeruginosa et Klebsiella pneumoniae avec leurs diamètres des zones d’inhibition (d).
a)Escherichia coli
Parmi tous les extraits de cette plantes, seules, les extraits du dichlorométhane et le méthanol ont inhibés cette bactérie avec des zones d’inhibitions de 28mm et 24 mm respectivement.
b) Staphylococcus aureus
Le décocté de 1heure ainsi que le digeste de 3h de cette plante, ont exercé un effet inhibiteur, remarquable sur Staphylococcus aureus. Ces derniers ont permis l’obtention des zones d’inhibition de 35mm et 32mm respectivement. Cette souche résiste aux autres extraits.
c) Pseudomonas aeruginosa.
73
Photo 14 : L’effet des plus importants extraits d’ Hordeum vulgare sur Pseudomonas aeruginosa.
(10) : marc de 24 h (d= 6mm). (11) : décocté de 15 min (d=40mm). (12) : digeste de 45min (d= 6mm).
Photo 13 : L’effet des plus importants extraits d’ Hordeum vulgare sur Escherichia coli. (6) : marc de 72h (d= 6mm). (9) : solution aqueuse (d= 6mm). (7) : digeste de 3h (d=32mm). (8) : décocté 1h (d=35mm).
6
7 8
9
Concernant le Pseudomonas aerugenosa, c'est la décoction de 15 min qui a inhibé le plus ce germe avec une zone d’inhibition de 40mm de diamètre.
d) Klebsiella pneumoniae
Pour Klebsiella pneumoniae, ce sont les extraits préparés à base de solvants qui ont provoqué l’inhibition la plus importante surtout celui d’éthanol avec une zone d’inhibition de 35 mm de diamètre. Les extraits d’éther de pétrole et du méthanol ont donné aussi un effet important, traduit par des zones d’inhibition de 28mm et 20mm respectivement.
La mesure du diamètre des zones d’inhibition en présence des extraits d’Hordium vulgare a donné les résultats représentés sur le tableau 21.
Tableau 21: l’effet des extraits d’Hordium vulgare sur les bactéries exprimé en diamètre
des zones d’inhibition en mm74
Photo 15: L’effet des plus importants extraits d’ Hordeum vulgare sur Klebsiella pneumoniae. (1) : l’extrait d’éther de pétrole (d=28mm). (2) : l’extrait du dichlorométhane (d=12mm). (3) :l’extrait du méthanol (d=20mm). (4) : l’extrait d’éthanol (d=35mm).
.
1
2 3
4
Solvants Ether de pétrole
Dichloro-
méthane Méthanol Ethanol Témoin DMSO
Marc 72h
Digeste 3h
Décocté 1h
Solution aqueuse Marc
24h
Décocté 15 min
Diamètre des zones d’inhibition pour chaque bactérie en (mm)
Escherichia coli
6 28 24 6 6 6 6 6 6 6 6
Staphylococcus
aureus
25 32 6 15 6 6 32 35 6 6 6
Pseudomonas
aeruginosa
28 8 6 16 6 12 12 9 10 18 40
Klebsiella
pneumoniae
28 12 20 35 6 6 17 7 6 6 6
L’histogramme 5 représente les différents diamètres des zones d’inhibition en mm pour chaque bactérie.
Toutes les bactéries sont sensibles à au moins trois extraits de l’Hordium vulgare. L’activité antibactérienne de l’Hordeum vulgare, vis-à-vis d’Escherichia coli est moins importante, sauf pour
Les extraits 2 et 3 correspondants aux extraits de dichlorométhane et méthanol où on a enregistré des zones d’inhibition de 28mm et 24 mm de diamètre respectivement.
II-8
-2-6 Etude de l’effet des extraits de Nigella sativa a) Escherichia Coli
75
051015202530354045
Bactéries
Diamètres des zones d'inhibition
Ether de pétrole Dichloro- méthane Méthanol Ethanol Témoin DMSO Marc 72h Digeste 3h Décocté 1h Solution aqueuse Marc 24h Décocté 15 min Digeste 45min
Histogramme 5 : L’effet de l’Hordeum vulgare sous différents modes de préparations sur les souches bactériennes représenté par le diamètre des zones d’inhibition
Le décocté de 15 minutes, le marc de 24h, l’extrait de dichlorométhane ainsi que la solution aqueuse ont exercé un pouvoir inhibiteur important vis-à-vis d'Escherichia coli avec des zones d’inhibition respectivement de 27, 23, 22 et 21 mm de diamètre.
b) Staphylococcus aureus
76
Photo 16 : l’effet des plus importants extraits de Nigella sativa sur E. coli. (2) : L’extrait de dichlorométhane (d=22mm). (9) : la solution aqueuse (d= 21mm). (10) : marc de 24 h (d=
23 mm). (11) : décocté de 15 min (d= 27 mm).
12
Photo 17 : l’Effet des plus importants extraits de Nigella sativa sur Staphylococcus aureus. (1):
l’extrait d’éther de pétrole (d= 20mm). (2) : l’extrait de dichlorométhane (d= 17mm). (4) : l’extrait d’éthanol (d= 15 mm). (6): marc de 72 h (d= 22 mm).
Concernant le Staphylococcus aureus, seulement le marc de 72h, les extraits d’éther de pétrole et de dichlorométhane ont donné un effet inhibiteur significatif. Les diamètres des zones d’inhibition enregistrées sont 22, 20 et 17mm respectivement.
c) Pseudomons aeruginosa.
L’effet antibactérien des extraits de Nigella sativa sur Pseudomonas aeruginosa est représenté sur la photographie suivante avec les diamètres des zones d’inhibition (d).
Pour le Pseudomonas aeruginosa, le pouvoir inhibiteur exercé par cette plante est moins important pour la majorité des extraits, sauf pour le marc de 24h et l’extrait du dichlorométhane, où on a enregistré des zones d’inhibition de diamètre 18 mm et 17mm respectivement.
d) Klebsiella pneumoniae
77
Photo 18 : l’effet des plus importants extraits de Nigella sativa sur Pseudomonas aeruginosa. (9) : la solution aqueuse (d= 16mm). (10) : décocté de 15 min (d=18mm). (11) : décocté 15 min (d= 6mm).
(12) : digeste 45 min (d=6 mm).
12
Photo 19 : (1) : l’effet des plus importants extraits de Nigella sativa sur Klebsiella pneumoniae. (1) : l’extrait d’éther de pétrole (d=28mm). (2) : l’extrait du dichlorométhane (d=16mm). (3) : l’extrait du méthanol (d= 21mm). (4) : l’extrait d’éthanol (d= 6mm). (5) : témoin (d=6mm). (6) : marc de 72 h (d=
16mm). (7) : digeste de 3 h (d= 16 mm). (8) : décocté de 1h (d= 14 mm). (9) : solution aqueuse (d=
16mm).
Cette souche est sensible aux extraits d’éther de pétrole, de méthanol, de dichlorométhane, marc de 72h, digeste de 3h, décocté de 15 min et la solution aqueuse avec des diamètres des zones d’inhibition de 28 mm, 21 mm et 16 mm respectivement. L’effet le plus important est celui de l’extrait d’éther de pétrole (d=28 mm).
Le tableau 22 regroupe les diamètres des zones d’inhibition des différentes souches bactériennes provoquées par les extraits de Nigella sativa.
Numéro du disque 1 2 3 4 5 6 7 8 9 10 11
Solvants Ether
de pétrole
Dichloro-
méthane Méthanol Ethanol Témoin DMSO
Marc 72h
Digeste 3h
Décocté 1h
Solution aqueuse Marc
24h
Décocté 15 min
Diamètre des zones d’inhibition pour chaque bactérie en (mm)
Escherichia coli
19 22 15 16 8 6 6 17 21 23 27
Staphylococcus
aureus
20 17 6 15 6 22 6 6 6 10 6
Pseudomonas
aeruginosa
6 17 6 6 8 13 16 15 16 18 6
Klebsiella
pneumoniae
28 16 21 8 6 16 16 14 16 15 16
Tableau 22 : Effet des extraits de Nigella sativa sur les différentes bactéries
Les diamètres des zones d’inhibition des différentes souches bactériennes obtenus par les extraits de Nigella sativa, sont présentés sur l’histogramme 6.
78
0 5 10 15 20 25 30
Bactéries
Diamètres des zones d'inhibition
Ether de pétrole Dichloro- méthane Méthanol
Ethanol Témoin DMSO Marc 72h Digeste 3h Décocté 1h Solution aqueuse Marc 24h Décocté 15 min Digeste 45min
Histogramme 6 : L’effet de Nigella sativa sous différents modes de préparations sur les souches bactériennes représenté par le diamètre des zones d’inhibition.
Les extraits d’éther de pétrole, de dichlorométhane, la solution aqueuse, le marc de 24h ainsi que le décocté de 15 min ont exercé un pouvoir inhibiteur important vis-à-vis d'Escherichia coli avec des zones d’inhibition de diamètre de 27 mm, 23 mm, 22 mm, 21 mm et 19 mm respectivement. Concernant le Staphylococcus aureus, les extraits d’éther de pétrole, de dichlorométhane et le marc de 72h ont donné un effet inhibiteur significatif avec un diamètre supérieur à 17 mm.
les résultats des diamètres des zones d’inhibition enregistrés en présence des extraits des plantes sont regroupés dans le tableau 23.
79
Numéro du disque 1 2 3 4 5 6 7 8 9 10 11
Solvants
Ether de pétrole
Dichloro-
méthane Méthanol Ethanol Témoin DMSO
Marc 72h
Digeste 3h
Décocté 1h
Solution aqueuse Marc
24h
Décocté 15 min
Diamètre des zones d’inhibition pour chaque bactérie en (mm) Matricaria chamomilla
Escherichia coli 28 8 6 6 6 6 6 6 11 6 6
Staphylococcus aureus 28 16 18 16 6 25 6 18 6 30 6
Pseudomonas aeruginosa 7 7 6 6 6 16 16 18 6 6 6
Klebsiella pneumoniae 6 26 38 6 8 35 8 6 6 40 6
Urtica dioica
Escherichia coli 27 11 6 8 8 6 25 6 6 20 17
Staphylococcus aureus 6 17 32 18 6 19 6 6 6 17 23
Pseudomonas aeruginosa 16 20 6 6 6 19 19 19 25 15 28
Klebsiella pneumoniae 6 28 18 6 6 18 6 6 6 27 25
Petroselinum Sativum
Escherichia coli 16 20 18 16 8 35 17 18 32 25 30
Staphylococcus aureus 6 6 6 13 6 30 14 12 32 35 6
Pseudomonas aeruginosa 16 18 16 15 8 12 13 15 17 15 18
Klebsiella pneumoniae 19 8 10 22 6 6 6 6 36 6 6
Thymus vulgaris
Escherichia coli 28 17 6 6 6 6 6 18 6 6 6
Staphylococcus aureus 6 6 6 6 6 6 6 6 6 6 6
Pseudomonas aeruginosa 6 26 6 6 6 10 6 10 10 6 6
Klebsiella pneumoniae 6 8 6 9 6 18 8 10 6 23 32
Hordeum vulgare
80
Staphylococcus aureus 25 32 6 15 6 6 32 35 6 6 6
Pseudomonas aeruginosa 28 8 6 16 6 12 12 9 10 18 40
Klebsiella pneumoniae 28 12 20 35 6 6 17 7 6 6 6
Nigella sativa
Escherichia Coli 19 22 15 16 8 6 6 17 21 23 27
Staphylococcus aureus 20 17 6 15 6 22 6 6 6 10 6
Pseudomonas aeruginosa 6 17 6 6 8 13 16 15 16 18 6
Klebsiella pneumoniae 28 16 21 8 6 16 16 14 16 15 16
II-9 Discussion
La recherche d’activité bactérienne (tableau 23), menée sur une série de 6 espèces de plantes appartenant à 6 famille utilisées par la population Ouest algérien sur les souches bactériennes Escherichia Coli, Staphylococcus aureus, Pseudomonas aeruginosa, Klebsiella pneumoniae a donné des zones d’inhibition variant entre 7mm et 40mm. En supposant une activité positive (effective) à partir d’une zone d’inhibition de 8 mm de diamètre, 59,5% (157 tests positifs/264 extraits) des plantes ont un potentiel antibactérien.
TRAIJED et al [92] montrent que l’activité antibactérienne des plantes est considérée importante à partir d’un diamètre de la zone d’inhibition supérieure ou égale à 15 mm. Sur cette base, 43 % des extraits des plantes testés présentent une activité importante.
21,96 % des extraits ayant un diamètre des zones d’inhibition compris entre 15mm et 19mm.
Les zones comprises entre 20 mm et 29 mm de diamètre représentent 14,01 %.
7,5 % de l’ensemble des extraits de plantes possède le potentiel d’activité antimicrobienne le plus élevé (diamètre de la zone d’inhibition entre 30mm et 40mm).
L’effet de l’activité antibactérienne par nature d’extraction de la plante sur les souches microbiennes a montré que la décoction, surtout celle de courte durée (15 minutes) a eu l’effet le plus important avec la majorité des plantes.
Le tableau 24 regroupe les diamètres des zones d’inhibition des bactéries en (mm) pour les extraits les plus actifs de chaque plante.
Tableau 24: Diamètre des zones d’inhibition des bactéries en (mm) pour les extraits les plus actifs de chaque plante.
Diamètre des zones d’inhibition pour chaque bactérie en (mm) Plantes
Bactéries
Matricaria chamomilla
Urtica dioica
Petroselinum Sativum
Thymus vulgaris
Hordeum
vulgare Nigella sativa
81
Tableau 23: L’effet antibactérien des différents extraits des plantes testées représenté par lediamètre des zones d’inhibition en mm.
Escherichia coli 40
(12)27
(1)35
(6)- 28
(1)27
Staphylococcus aureus 30
(10)32
(3)35
(10)- 35
(8)22
Pseudomonas aeruginosa - 28
(11)- 26
(2)40
(11)Klebsiella pneumoniae 40
(10)28
(2)36
(9)32
(11)35
(4)28
Les différences dans l’activité antibactérienne des plantes testées sont de toute évidence liées à des différences dans leurs contenues en composés actifs [92]. La majorité des groupes chimiques présents dans les végétaux, comme les tanins, les saponosides, les flavonoïdes, les coumarines, les anthocyanosides et les mucilages, sont extractibles par l’eau [73]. Ce dernier semble être le meilleur solvant pour extraire la majorité des constituants chimiques responsables des différentes activités biologiques, ce qui démontre la pertinence de la forme traditionnelle d’utilisation.
Matricaria chamomilla
Cette plante préparée en digestion de 45 minutes et en macération de 24 heures a exercé un pouvoir inhibiteur très important vis-à-vis d’Escherichia Coli et Klebsiella pneumoniae respectivement, avec des zones d’inhibition de ces souches atteignant 40mm de diamètre.
Le diamètre enregistré pour Staphylococcus aureus avec le marc de 24 heures de la même plante n’est pas négligeable, il est de 30mm.
D’après les résultats de la phytochimie, Matricaria chamomilla est une plante riche en constituants polyphénoliques (acide phénolique, flavonoides, coumarines) et des huiles essentielles [81]. Ces dernières sont libérées dans les tisanes préparées à basse température.
D’après M. WICHTL [78], l’utilisation d’eau froide dans l’extraction permet la libération des huiles essentielles. Selon S.DUPONT [93], l’activité antibactérienne des extraits des feuilles de thé est limité, mais si celles ci sont associés à des huiles essentielles, cette activité devient plus importante.
Urtica dioica
Pour cette plante, l’extrait du méthanol a donné l’activité antibactérienne la plus importante avec Staphylococcus aureus.
Ceux d’éther de pétrole et dichlorométhane ont donné une moyenne activité antibactérienne sur Escherichia Coli et Klebsiella pneumoniae.
82
(1) : l’extrait d’éther de pétrole, (2) : l’extrait de dichlorométhane, (3) : l’extrait du méthanol, (4) : l’extrait d’éthanol, (6) : marc de 72 h, (8) : décocté de 1 heure, (10) : marc de 24 h, (11) : décocté de 15 minutes, (12) : digeste de 45 minutes.constituants, notamment les tanins et d'autres substances polyphénoliques [73]. De nombreux travaux ont mis en évidence l’activité antibactérienne des tanins [94-96].
La capacité d’une espèce végétale à résister à l’attaque des micro-organismes est souvent corrélée avec la teneur en composés phénoliques [97].
Petroselinum Sativum
Le marc ainsi que la solution aqueuse de cette plante semblent avoir la même activité antibactérienne, puisqu’ils présentent des zones d’inhibition respectives de 35 mm et 36mm avec Escherichia Coli, Staphylococcus aureus et Klebsiella pneumoniae. Ceci est du peut être à la richesse de cette plante en vitamine C qui ne supporte pas les températures élevées pour être pleinement efficace.
En parallèle, un criblage phytochimique a été effectué pour prospecter les différents composés secondaires caractérisant cette plante. Cette étude a montré la présence des coumarines, des terpènes, des saponines et des Alcaloïdes. Ceci renforce l’activité antibactérienne de cette plante.
Thymus vulgaris
Le décocté de 15 minutes de cette plante a agit le plus avec Klebsiella pneumoniae. Le deuxième pouvoir inhibiteur enregistré pour le Thymus vulgaris est celui de l’extrait de dichlorométhane avec Pseudomonas aeruginosa.
L’étude phytochimique a révélé que cette plante contient de 0,2 à 0,5 % d’huiles essentielles composées de thymol, de carvacrol qui en font un excellent vulnéraire et un puissant antiseptique. Elle contient aussi des flavonoïdes et des triterpènes [82]. Ces derniers ont été extraits préférentiellement par le dichlorométhane.
Unlu et al [98] ont indiqué que le thymol, le carvacrol et le borneol sont les principaux éléments de d'huile essentielle de cette plante. D’après N. Ameziane [99], un test de l’activité antibactérienne effectué avec des fractions d’huiles essentielles a montré que l'activité a été principalement observée dans les fractions contenant le thymol et le carvanol.
Hordeum vulgare
Le décocté de 15 minutes de cette plante est très actif vis-à-vis du Pseudomonas aeruginosa.
Cette dernière est connue comme une bactérie pathogène et résistante à la majorité des
83
antibiotiques. Le décocté d’une heure de la même plante a donné presque le même effet avec Staphylococcus aureus.
Ces propriétés antibactériennes pourraient être attribuées à la présence dans les graines de cette plante de pectine et d’acides organiques [100-102]. Selon M. WICHTL [78], l’eau bouillante (décoction) serait responsable de l’extraction de ce type de composés.
L’extrait d’éthanol de l’ Hordeum vulgare a été le plus actif contre Klebsiella pneumoniae.
Certaines molécules extraites préférentiellement par ce solvant pourraient être à l'origine de cette efficacité [70].
Nigella sativa
Cette plante semble avoir le même effet avec l’extrait d’éther de pétrole et le décocté de 15 minutes vis à vis d’Escherichia Coli et Klebsiella pneumoniae respectivement. L’éther de pétrole serait responsable de l’extraction des alcaloïdes, terpènes, coumarines et les acides gras. L’eau bouillante permet la libération de l’amidon et des pectines. L’étude phytochimique confirme la présence de ces composés dans cette plante. Toute cette richesse en métabolites secondaires peut expliquer l'inhibition de la croissance de ces bactéries en utilisant cette plante.
II-10 Détermination de la Concentration Minimale Inhibitrice en milieu liquide
Par définition, la Concentration Minimale Inhibitrice (CMI) est la plus faible concentration d’antibiotique (extrait) capable de provoquer une inhibition complète de la croissance d’une bactérie donnée, appréciable à l’œil nu, après une période d’incubation donnée [103].
II-10-1 Méthode de dilution
Les méthodes de dilution sont effectuées en milieu liquide. Elles consistent à mettre un inoculum bactérien standardisé au contact de concentrations croissantes d’antibiotiques (extraits) selon une progression géométrique de raison 2 par exemple 0,5 mg/l 1, 2, 4, 8, 16 (figure 9).
Figure 11 : détermination de la CMI par la méthode de
84
dilution en milieu liquide
La galerie ainsi préparée sera incubée à 37°C pendant 18 heures. Enfin elle sera examinée à l'œil nu et dans l'exemple ci-dessous, la CMI de l'antibiotique à tester est de 2mg/l.
II-10-2 Détermination de la Concentration Minimale Inhibitrice (CMI) des extraits de plantes étudiées
Chaque un des extraits des différentes plantes (10 mg/ml) est dilué dans le bouillon Mueller-Hinton de façon à avoir une concentration de départ de 0,25 mg/ml. Cette dilution est suivie par une série de dilutions selon une progression géométrique de raison 2. On ajoute dans chaque tube 100 µl de culture fraîche (préparé
eà partir d'une souche incubée 18 heures à 37 ° C) à une concentration de 10
6UFC /ml
-1. Les tubes de la gamme ont été incubés 24 heures à 37 ° C. La CMI en milieu liquide est définie comme la plus faible concentration en antibiotique (extrait) pour laquelle il n'y a pas de trouble visible [90].
Elle est réalisée seulement pour les extraits qui ont présentés une activité antibactérienne considérable dont le diamètre de la zone d’inhibition est supérieur à 15 mm. Les résultats de la CMI sont regroupés dans le tableau 25.
85
Plantes Extraits et CMI des différentes bactéries en mg/ml
Ether de pétrole Dichlorométhane Méthanol
Sa E.coli Pa Kp Sa E.coli Pa Kp Sa E.coli Pa Kp
Matricaria chamomilla 0.078 0.078 - - 0.312 - - 0.078 0.312 - - 0.039
Urtica dioica - 0.078 0.312 - 0.312 - 0.312 0.078 0.039 - - 0.312
Petroselinum sativum - 0.312 0.312 0.312 - 0.312 0.312 - - 0.312 0.312 -
Thymus vulgaris - 0.078 - - - 0.312 0.078 - - - - -
Hordeum Vulgaris 0.156 - 0.078 0.078 0.039 0.078 - - - 0.156 - 0.312
Nigella Sativa 0.312 0.312 - 0.078 0.312 0.156 0.312 0.312 - 0.625 - 0.156
Ethanol Solution aqueuse Macération 72H
Matricaria chamomilla 0.312 - - - 0.156 - 0.312 0.312
Urtica dioica - - - 0.312 - 0.312 -
Petroselinum sativum - 0.312 0.625 0.156 0.039 0.039 0.312 0.039 0.039 0.009 - 0.312
Thymus vulgaris - - - -
Hordeum Vulgaris 0.625 - 0.312 0.039 - - - 0.039
Nigella Sativa 0.625 0.312 - - - 0.156 0.312 0.312 0.156 - - 0.312
Digestion 3h Décoction 1h Macération 24h
Matricaria chamomilla - - 0.312 - 0.312 - 0.312 - 0.039 - - 0.009
Urtica dioica - 0.156 0.312 - - - 0.312 - 0.312 0.312 0.625 0.078
Petroselinum sativum - 0.312 - - - 0.312 0.312 - 0.039 0.156 0.625 -
Thymus vulgaris - - - 0.312 - - - 0.156
Hordeum Vulgaris 0.039 - - 0.312 0.039 - - - 0.312 -
Nigella Sativa - - 0.312 0.312 - 0.312 0.625 - - 0.156 0.312 0.625
Digestion 45 min Décoction 15 min
Matricaria chamomilla - - - 0.009 - -
Urtica dioica 0.312 0.312 0.156 0.312 0.156 0.312 0.078 0.078
Petroselinum sativum - - - 0.039 0.312 -
Thymus vulgaris - - - 0.156 - - - 0.039
Hordeum Vulgaris - - - 0.009 -
Nigella Sativa - - - 0.078 - 0.625
(-) : absence d’activité antibactérienne.
Sa: Staphylococcus Aureus, E.Coli: Escherichia Coli, Pa: Pseudomonas aeuriginosa, Kp: Klebsiella Pneumoniae.
Tableau 25: Concentration Minimale Inhibitrice (CMI) des extraits des plantes testées
86
d’une bactérie à une autre. Les valeurs des concentrations minimales inhibitrices obtenues dans cette étude des extraits des plantes, variaient entre 0,625 et 0,009 mg/ml.
Les plus faibles CMI, reflétant la haute sensibilité des bactéries aux extraits des plantes sont regroupés dans le tableau 26.
Tableau 26: Les plus importantes (CMI) des extraits des plantes testées pour chaque bactérie.
Extraits et CMI des différentes bactéries en mg/ml Matricaria
chamomilla Urtica dioica
Petroselinum sativum
Thymus
vulgaris Hordeum
Vulgare
Nigella Sativa
Escherichia coli0 ,009 (6) 0,078 (1) 0,039 (9,11) 0,078 (1) 0,078 (2) 0,078
Staphylococcus
aureus
0,039(10) 0,039 (3) 0,009 (6,10) - 0,039 (2, 7,8) 0,156Pseudomonas
aeruginosa
0,312 (6, 7, 9) 0,078 (11) 0,312(1, 2, 3, 8,11) 0,078(2) 0,009 (11) 0,312(2, 7, 9,10)Klebsiella
pneumoniae
0,009 (10) 0,078 (2, 10, 11) 0,039 (9) 0,039 (11) 0,039 (4, 6) 0,0781- Ether de pétrole 2- Dichlorométhane 3- Méthanol
4- Ethanol 5- Témoin 6- Macération 72h 7- Digestion 3h 8- Décoction 1h 9- Solution aqueuse 10- Macération 24 h 11- Décoction 15min 12- Digestion 45min

![Tableau 16 : les composés libérés par des solvants organiques lors d’une extraction [70,78].](https://thumb-eu.123doks.com/thumbv2/123doknet/13153740.389398/5.892.95.811.171.417/tableau-composés-libérés-solvants-organiques-extraction.webp)