THÈSE
Pour l'obtention du grade de
DOCTEUR DE L'UNIVERSITÉ DE POITIERS École nationale supérieure d'ingénieurs (Poitiers)
Pôle poitevin de recherche pour l'ingénieur en mécanique, matériaux et énergétique - PPRIMME (Poitiers) (Diplôme National - Arrêté du 25 mai 2016)
École doctorale : Sciences et ingénierie en matériaux, mécanique, énergétique et aéronautique -SIMMEA (Poitiers)
Secteur de recherche : Énergétique Cotutelle : Université de Bejaïa
Présentée par :
Radouane Maizia
Diagnostic des piles à combustible PEMFC par la mesure des bruits électrochimiques :
application à la gestion de l'eau
Directeur(s) de Thèse :
Sergueï Martemianov, Abdelhafid Dib Soutenue le 11 janvier 2018 devant le jury
Jury :
Président Boualem Saidani Professeur, Université de Béjaïa, Algérie Rapporteur Daniel Hissel Professeur, Université de Franche-Comté
Rapporteur Mohammed Hamour Maître de conférences, Université de Tizi-Ouzou, Algérie Membre Sergueï Martemianov Professeur, ENSIP, Université de Poitiers
Membre Abdelhafid Dib Maître de conférences, LECVE, Université de Béjaïa, Algérie Membre François Huet Professeur, LISE, CNRS-Sorbonne Université, Paris
Membre Anthony Thomas Maître de conférences, PPRIME, Université de Poitiers
Membre Hakim Lounici Professeur des Universités, BIOGEP, Université de Bouira, Algérie
Pour citer cette thèse :
Radouane Maizia. Diagnostic des piles à combustible PEMFC par la mesure des bruits électrochimiques :
application à la gestion de l'eau [En ligne]. Thèse Énergétique. Poitiers : Université de Poitiers, 2018. Disponible sur Internet <http://theses.univ-poitiers.fr>
Pour l’obtention du Grade de
DOCTEUR DE L’UNIVERSITE DE POITIERS (Faculté des Sciences Fondamentales et Appliquées)
(Diplôme National - Arrêté du 25 mai 2016) Ecole Doctorale : SI-MMEA
Secteurs de Recherche : Energétique Présentée par :
Radouane MAIZIA ************************
Diagnostic des piles à combustible PEMFC par la
mesure du bruit électrochimique : Application à la
gestion d'eau
************************
Directeur de Thèse : Sergueï MARTEMIANOV Co-directeur de Thèse : Abdelhafid DIB
Co-encadrant de thèse : Anthony THOMAS ************************ Soutenue le 11/01/2018
devant la Commission d’Examen ************************
JURY
Mr Daniel HISSEL Professeur, Université de Franche-Comté Rapporteur Mr Mohammed HAMOUR Maître de Conférences, Université de Tizi-Ouzou Rapporteur Mr François HUET Professeur, Université de UPMC Examinateur Mr Boualem SAIDANI Professeur, Université de Bejaia Examinateur Mr Hakim LOUNICI Professeur, Université de Bouira Examinateur Mr Serguei MARTEMIANOV Professeur, Université de Poitiers Examinateur Mr Abdelhafid DIB Professeur, Université.de Bejaia Examinateur Mr Anthony THOMAS Maitre de Conférences, Université de Poitiers Examinateur
Valorisation des Travaux de Recherche de la Thèse
Articles
1) R. Maizia, A. Dib, A. Thomas, S. Martemianov, « Proton exchange membrane fuel cell diagnosis by spectral caractérisation of the electrochemical noise », Journal of Power Sources, 342 (2017) 553-561.
2) R. Maizia, A. Dib, A. Thomas, S. Martemianov, « Statistical short time analysis of electrochemical noise generated within a proton exchange membrane fuel cell », Journal of solid state electrochemistry, (2017), DOI : 10.1007/s10008-017-3848-0.
Conférences
1) R. Maizia, A. Dib, A. Thomas, S. Martemianov, « Electrochemical Noise as a Diagnostic Tools for PEM Fuel Cell », Journée d’électrochimie, Bordeaux, Juin 2017.
2) R. Maizia, A. Dib, A. Thomas, S. Martemianov « New Methodology Based on Electrochemical Noise Analysis Applied to PEMFC », 6th Symposium on Hydrogen, Fuel Cells and Advanced Batteries, Juin 2017 Porto.
3) R. Maizia, A. Dib, A. Thomas, S. Martemianov « Diagnosis of Proton Exchange Membrane Fuel Cell by Electrochemical Noise », GDR HySPàC, Mai 2017, Limoges.
4) R. Maizia, A. Dib, A. Thomas, S. Martemianov « Proton Exchange Membrane Fuel Cell Diagnosis by Spectral Characterization of the Elechtrochemical Noise », Fundamentals and Développements of Fuel Cells, Stuttgart, Janvier 2017.
5) A. Thomas, R. Maizia, A. Dib, S. Martemianov « Advanced methodology developments applied to proton exchange membrane fuel cell », European Fuel cell Car workshop, Orléans, Mars 2017.
6) R. Maizia, A. Dib, A. Thomas, S. Martemianov « Proton Exchange Membrane Fuel Cell Diagnosis by Spectral Characterization of the Elechtrochemical Noise », International Discussion on Hydrogen energy and Application, Nantes, Novembre 2016.
cotutelle entre laboratoire d’Electrochimie, Chimie Corrosion et de Valorisation Energétique (LECVE) de l’Université de Béjaia (Algérie) et l’Institut Pprime de l’Université de Poitiers (France), sous financement de l’Université de Bejaia et d’une bourse ministérielle PNE.
J’exprime ma profonde gratitude et reconnaissance à mon directeur de thèse, Monsieur Serguei MARTEMIANOV Professeur à l’Université de Poitiers, pour l’accueil qu’il m’a réservé au sein de son équipe de recherche, pour la confiance qu’il m’a accordée, pour les moyens mis à ma disposition et pour les discussions scientifiques que nous avons eu pour le bon accomplissement de mes travaux de recherche.
Je tiens à remercier en deuxième lieu mon co-directeur de thèse, Monsieur Abdelhafid DIB Professeur à l’Université de Bejaia, d'avoir accepté de diriger mes travaux de recherche, de faire confiance à mes compétences et de m'offrir une grande autonomie. Je lui suis également reconnaissant pour le temps qu'il m'a accordé, ses qualités pédagogiques et scientifiques, sa franchise et sa sympathie. J'ai beaucoup appris à ses côtés. Son énergie et sa confiance ont été des éléments moteurs pour moi. J'ai pris un grand plaisir à travailler avec lui et je lui adresse ma gratitude pour tout cela.
Je tiens à exprimer toute ma gratitude et ma reconnaissance à mon Co-encadrant de thèse Monsieur Anthony THOMAS, Maître de conférence à l’université de Poitiers, pour, m’avoir aidé, sa disponibilité et ses conseils durant toutes ces années de thèse.
Je remercie chaleureusement Monsieur Boualem SAIDANI, Professeur et Recteur de l’université de Bejaia, pour m’avoir fait l’honneur de présider ce jury de thèse, qu’il trouve ici l’expression de mon profond respect et de toute ma gratitude.
Tous mes remerciements s’adressent à Monsieur Mohammed HAMOUR, Maître de conférence A à l’université Mouloud Mammeri Tizi Ouzou, Monsieur Daniel HISSEL, Professeur à l’Université de Belfort, Monsieur François HUET, Professeur à l’Université de Pairs VI et Monsieur Hakim LOUNICI, Professeur à l’Université de Bouira, pour avoir accepté de participer à ce jury de soutenance et de donner leur précieux temps pour examiner ce travail.
Mes plus sincères salutations vont à l’ensemble des permanents (techniciens, ingénieurs et enseignants) du LECVE et l’institut Pprime qui m’ont beaucoup apporté pour mener à terme mon travail.
Un grand merci également à mes amis et collègues doctorants, des deux rives, trop nombreux pour être cités pour leur soutien et bonne humeur constants durant mon travail de thèse.
Je remercie du fond du cœur, bien sur, mes parents ainsi que tous les membres de ma famille notamment mes frères « Said et Bachir », ma sœur « Fazia », mes neveux « Adem et Abdeljalil », mes belles-sœurs « Rahima et chafia », et mon beau-frère « Fateh », pour leur soutien et leur amour depuis ma naissance jusqu'à maintenant.
Enfin, je dédie ce manuscrit à la mémoire de mon cher frère « Salim ».
PAC Pile A Combustible. FCV Fuel Cell Vehicle.
PEMFC Proton Exchange Membrane Fuel Cell.
BE Bruit Electrochimique.
MP Mesure de Pression.
STD Standard Deviation.
SK Skewness.
FL Flatness.
FFT Fast Fourier Transform. PEM Porton Exchange Membrane. AFC Alkaline Fuel Cell.
PAFC Phosphoric Acid Fuel Cell. DMFC Direct Methanol Fuel Cell. SOFC Solid Oxide fuel Cell.
MCFC Molten Carbonate Fuel Cell.
EPACOP Expérimentation de Piles À Combustible de petite taille sur sites Opérationnels.
AME Assemblage Membrane Electrodes . PFSA PerFluoroSulfonic Acid.
PTFE Poly(TetraFluoroEthylène). GDL Gaz Diffusion Layer.
SIE Spectroscopie d’Impédance Électrochimique.
RMN Résonnance Magnétique Nucléaire. MEB Microscope Electronique à Balayage. MET Microscope Electronique à Transmission.
EA Emission Acoustique.
DSP Densité Spectrale de Puissance.
HF Haute Fréquence.
BF Basse Fréquence.
MPL Micro-Porous Layer.
fs Fréquence d’échantillonnage.
FC Fuel cell.
OCV Open Circuit Potentiel. PSD Power Spectral Density.
HR Humidité Relative.
QH2 Débit volumique de l’hydrogène. Qair Débit volumique de l’air.
Tcell Température de la cellule. RHc Relative Humidity cathodic. RHa Relative Humidity anodic. Panodique Pression à l’entrée de l’anode. Pcathode Pression à l’entrée de la cathode. STDpc Ecart type de la pression anodique. STDpc Ecart type de la pression cathodique.
Tables des matières
Introduction générale………...1
Chapitre 1 Etat de l’art sur les piles à combustible
1.1 Piles à combustibles ... 7
1.1.1 Différents types de piles à combustible. ... 8
1.1.2 Applications ... 13
1.2 Pile à combustible à membrane échangeuse de proton (PEMFC) ... 16
1.2.1 Principe de fonctionnement ... 16
1.2.2 La structure et les composants des PEMFC ... 17
1.3 Problématique scientifique liée à la gestion de l’eau ... 23
1.3.1 L’assèchement de la membrane ... 24
1.3.2 L’engorgement de la pile ... 26
1.4 Etat
de l’art des défaillances d’une pile à combustible ... 28
1.4.1 Introduction ... 28
1.4.2 Dégradations réversibles ... 28
1.4.3 Dégradations irréversibles ... 32
1.4.4 Les empoisonnements ... 35
1.4.5 Récapitulatif des défauts affectant les différents composants d’une pile PEMFC ... 36
1.4.6 Conclusion ... 38
1.5 Références bibliographiques ... 39
Chapitre 2 Méthodes de diagnostic et analyse des bruits électrochimiques
appliqués à une PEMFC
2.1 Définition de diagnostic ... 45
2.2 Différents outils de diagnostic... 45
2.2.1 Méthodes électrochimiques ... 46
2.2.1.1 Courbe de polarisation ... 46
2.2.1.3 Interruption de courant ... 50
2.2.1.4 Voltammétrie cyclique ... 51
2.2.2 Méthodes chimiques et physiques ... 53
2.2.2.1 Mesure de la pression ... 53
2.2.2.2 Mesure par émission acoustique. ... 53
2.2.2.3 Microscopie électronique à balayage ou à transmission ... 54
2.2.3 Diagnostic par la mesure du bruit électrochimique ... 54
2.2.3.1 Historique ... 55
2.2.3.2 Définition et principe de la méthode ... 56
2.2.3.3 Différentes méthodes de traitement du bruit électrochimique ... 56
2.2.3.4 Domaines d’applications du bruit électrochimique ... 60
2.3 Conclusion ... 61
2.4 Références bibliographique ... 61
Chapitre 3 Matériel et méthodes
3.1 Description du banc de test ... 72
3.2 Description de la mono-cellule utilisée ... 74
3.2.1 Assemblage Membrane-Electrodes (AMEs) ... 75
3.2.2 Couche de diffusion des gaz ... 76
3.2.3 Joint d’étanchéité ... 77
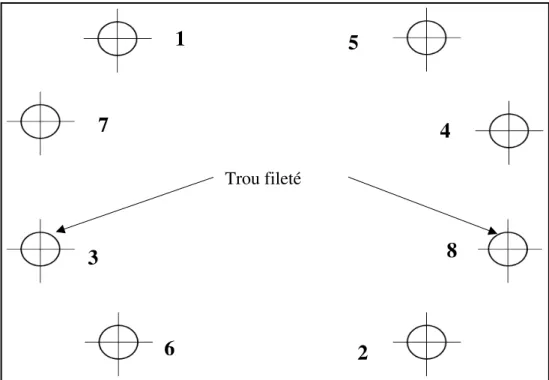
3.2.4 Plaques de distribution des gaz ... 77
3.2.5 Plaques collectrices du courant ... 79
3.2.6 Plaques supports (compression) ... 80
3.3 Protocole d’assemblage de la mono-cellule PEMFC ... 81
3.4 Conditionnement d
’assemblage membrane électrode ... 83
3.5 Les conditions expérimentales utilisées ... 84
3.6 Bruit électrochimique ... 85
3.6.1 Principe de la mesure des fluctuations de Potentiel ... 85
3.6.2. Carte d’acquisition ... 86
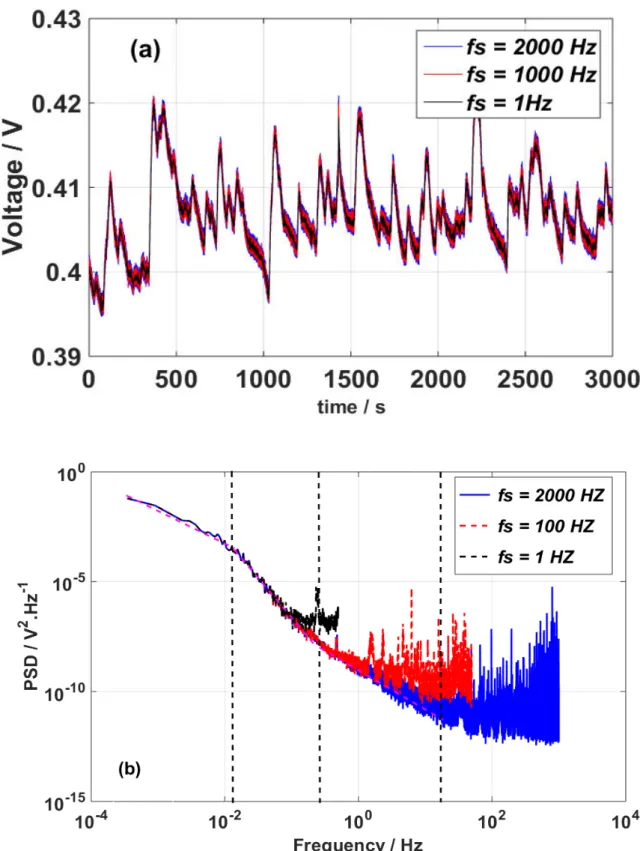
3.6.3. Choix de la Fréquence d’échantillonnage du signal ... 88
3.6.4. Bruit intrinsèque du montage expérimental ... 90
3.9 Références bibliographiques ... 94
Chapitre 4 Analyse spectrale du bruit électrochimique
4.1 Analyse spectrale par la méthode de Fourier (FFT) ... 96
4.2 Méthodologie de l’analyse spectrale ... 67
4.3 Résultats ... 103
4.3.1 Effet de l’humidité relative des gaz à l’entrée de la pile à combustible ... 103
4.3.2 Effet du courant ... 112
4.3.3 Effet de la température ... 118
4.3.4 Effet de l’humidité relative de la cathode (HRc) ... 124
4.3.5 Effet de l’humidité relative de l’anode ... 128
4.4 Conclusion ... 133
4.5 Références bibliographiques ... 136
Chapitre 5 Analyse statistique a court-terme du bruit électrochimique
5.1 Théorie de l’analyse statistique ... 139
5.1.1 Interprétation de l’écart type (STD) ... 139
5.1.2 Interprétation de Skewness (SK) ... 140
5.1.3 Interprétation de Flatness normalisé (FL) ... 140
5.2 Méthodologie de l’analyse statistique à court-terme ... 141
5.3 Résultats ... 146
5.3.1 Effet de l’humidité des gaz à l’entrée de la cellule de pile à combustible ... 146
5.3.2 Effet de la température de la cellule de la pile à combustible ... 160
5.4 Conclusion ... 167
Chapitre 6 Diagnostic de la PEMFC par analyse des fluctuations de
potentiel et de pression
6.1 Introduction ... 173
6.2 Résultats ... 174
6.2.1 Analyse direct des fluctuations de tension et de pression dans le domaine temporel ... 174
6.2.2 Analyse statistique des fluctuations de pression ... 184
6.2.3Analyse croisée des fluctuations de tension et de pression ... 189
6.3 Conclusion ... 192
6.3 Références bibliographiques ... 193
1
L’environnement est le patrimoine commun des êtres humains [1]. Depuis le début des années 2000, la lutte contre le réchauffement climatique est devenue une mission majeure de notre société. Cette mission passe en partie par la gestion de l’énergie. En effet, l’exploitation intensive des ressources énergétiques, fossiles notamment, depuis le début des années 70 est en grande partie responsable de la perturbation des écosystèmes par l’émission de gaz à effet de serre, responsable du réchauffement climatique. Or, avec l’utilisation, toujours croissante, de nouvelles technologies dans des domaines tels que l’industrie, le transport ou l’habitation ; l’humanité consomme plus d’énergie que les ressources et la production ne le permettent. De plus 87 % de cette production d’énergie provient de ressources fossiles [2]. Aujourd’hui la gestion énergétique mondiale s’imbrique dans un nouveau paradigme de développement durable qui comprend, au-delà de l’aspect écologique, un aspect social et économique. Ainsi, de nombreuses alternatives ont été développées ces dix dernières années afin de palier à cette possible pénurie d’énergie, notamment par l’utilisation d’énergies dites « renouvelables » telles que l’éolien, l’hydraulique, la géothermie ou encore le solaire [3]. Cependant, l’utilisation unique des énergies renouvelables ne permet pas de répondre aujourd’hui à la demande énergétique mondiale tant les rendements associés sont faibles. C’est ainsi que de nouvelles formes de transformation d’énergie apparaissent tels que les piles à combustible (PAC).
Technologies innovantes focalisées sur la production de puissance pour la cogénération d’électricité et de chaleur, elles se présentent comme un véritable levier économique et commercial. Révolutionnant le monde de l’énergie, les piles à combustibles ont commencé leur développement à grande échelle, par la création, par exemple: par Alstom en Allemagne d’un train à PAC, le Coradia. Elles se retrouvent également au Japon, par la fabrication de la voiture Toyota FCV (fuel cell vehicle) ou encore aux Etats-Unis, par la conception par Boeing et IHI d’un nouveau prototype d’avion [4]. En France, on retrouve cette technologie pour la mobilité de flottes captives avec la Poste (projet Moby Post) par exemple ou dans le domaine du naval comme le projet Energy Observer. Différents types de PAC sont ainsi actuellement en cours de développement. Parmi ces technologies, la pile à membrane échangeuse de protons (PEMFC) se voit être la candidate la plus prometteuse, soulignée notamment par la voiture Mirai conçue par Toyota. En outre, cette voiture à hydrogène, dont les performances sont comparables à celles d'une voiture à essence, dispose d'une autonomie d'environ 500 km, contrairement au véhicule électrique dont l’autonomie ne dépasse pas au mieux les 150 km, avec un plein d'hydrogène réalisé en 3 minutes [5].
Introduction générale
2
Les PEMFCs sont une technologie prometteuse de conversion de l’énergie chimique en énergie électrique et chaleur pour différentes applications tant mobiles (transport, électronique portable), que stationnaires (générateur auxiliaire, conversion/stockage de l’énergie). En dépit des progrès indéniables réalisés ces dernières décennies, des verrous technologiques restent encore à lever pour permettre un développement économiquement viable. Parmi les différentes pistes, actuellement en cours d’étude, nous pouvons citer la réduction des coûts de fabrication, l’augmentation de la fiabilité et de la durée de vie des systèmes ainsi que la mise en place d’outils de diagnostic et de contrôle [6]. La gestion de l’eau dans les cellules de pile à combustible reste aussi un des aspects déterminants à la fois d’un point de vue performances et longévité [7-9].
Pour répondre en partie à ces verrous, cette thèse est donc dédiée au développement d’une méthode originale de diagnostic des piles à combustible appliquée à la gestion d'eau dans un cœur de mono-cellule de PEMFC. Cette méthode non invasive est basée sur la mesure du bruit électrochimique (mesure des fluctuations de potentiel) et permet un diagnostic non perturbant de la pile, critère important notamment pour les applications industrielles. De plus, l’étude des bruits internes des systèmes électrochimiques est un challenge scientifique.
Pour aborder les objectifs mentionnés ci-dessus, nous avons concentré nos efforts sur les mesures des bruits électrochimiques dans des conditions bien contrôlées et sur le développement d’une méthodologie de génération des signatures spectrales et des descripteurs statistiques dans le domaine temporel en mettant l’accent sur la problématique de non-stationnarité éventuelle des signaux aléatoires.
La mesure du bruit électrochimique (BE) est une approche prometteuse qui nécessite une instrumentation assez simple pour permettre la surveillance des piles à combustible. En effet, la mesure de la tension électrique de la pile à combustible avec une fréquence d'acquisition de données assez importante est suffisante pour obtenir la signature stochastique du système. Les fluctuations de tension (bruit électrochimique) fournissent une information riche sur l'état d'une pile à combustible en fonctionnement par rapport à celles obtenues en utilisant des méthodes plus sophistiquées comme la spectroscopie d'impédance électrochimique (SIE) par exemple. Certainement, l'interprétation des mesures du BE est une question ouverte qui nécessite le développement d'approches appropriées, mais les mêmes difficultés sont aussi rencontrées avec la SIE. Le problème principal est lié à la connaissance limitée des phénomènes physico-chimiques couplés et des phénomènes de transfert qui
3
utilisées aujourd'hui pour la détection d‘un défaut de fonctionnement ou d’anomalies et permettre une meilleure compréhension des phénomènes physico-chimiques et de transfert de masse et de chaleur en cœur de pile.
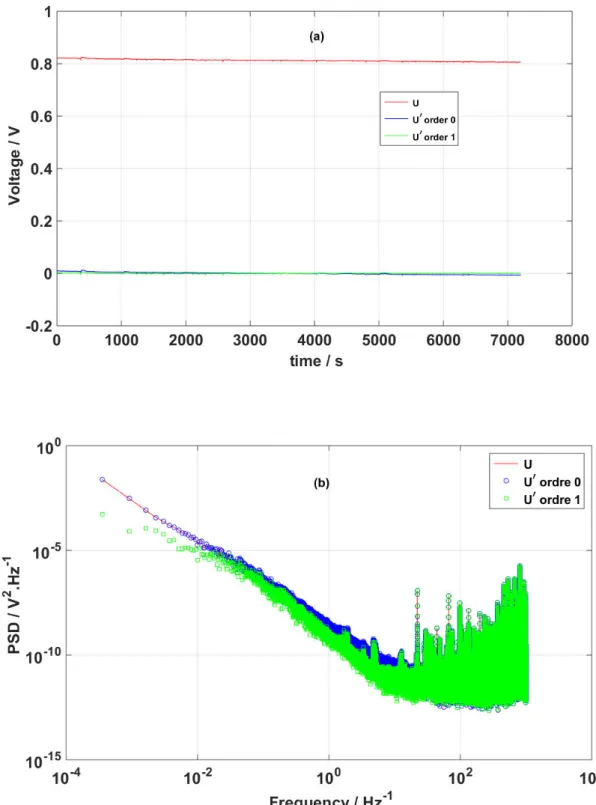
La façon traditionnelle de traiter les mesures du BE est basée sur la génération de descripteurs statistiques dans le domaine temporel (les moments : Standard deviation, Skewness, Flatness, …), sur l’analyse spectrale (spectres de Fourier) ou sur l’analyse tempo-fréquentielle (ondelettes, …). Cette thèse s’est limitée à la génération de descripteurs statistiques à court terme dans le domaine temporel et à l’analyse spectrale (spectres de Fourier) dans le domaine fréquentiel, qui convient mieux aux applications pratiques possibles. L'une des difficultés est liée à la dérive temporelle possible des signaux enregistrés (non-stationnarité des signaux du bruit électrochimique) qui nécessitent des développements de différentes procédures d’élimination de la dérive des signaux du bruit électrochimique. Dans ce présent manuscrit nous avons développés deux procédures qui peuvent résoudre ce problème.
La première procédure est basée sur l’analyse spectrale des signaux de tension. Notre méthodologie consiste à faire la distinction entre un signal quasi-stationnaire et non stationnaire par la comparaison des spectres après la procédure de detrending (d’élimination de la dérive). Par la suite l’analyse spectrale est appliquée uniquement aux signaux quasi-stationnaires.
La deuxième possibilité est d'appliquer une analyse statistique à court-terme. Cette approche est basée sur la séparation du signal total sur des petites fenêtres temporelles, et sur le calcul des descripteurs statistiques (les moments) dans ces fenêtres où le signal peut être traité comme quasi-stationnaire. De cette façon, des descripteurs statistiques peuvent être obtenus et utilisés pour la caractérisation de l'état d'une pile à combustible en cours d'exécution et pour détecter ses anomalies possibles.
De manière à compléter la méthode du bruit électrochimique, nous avons combiné les mesures des fluctuations de tension avec les mesures des fluctuations de pression de l’anode et de la cathode. Le couplage de ces deux techniques permettra l'analyse croisée des phénomènes liés à la mauvaise gestion de l’eau (assèchement de la membrane et noyage de pile).
Ce manuscrit est divisé en six chapitres. Dans le chapitre 1, nous présentons une étude bibliographique sur les PEMFC axée essentiellement sur la problématique scientifique liée à
Introduction générale
4
la gestion de l’eau (assèchement et noyage). Le chapitre 2 présente les différentes défaillances qui peuvent avoir lieu dans une PEMFC et les techniques de diagnostic associées. Dans le chapitre 3, nous avons décrit le matériel et les méthodes utilisées lors de nos travaux. Enfin, les chapitres 4, 5 et 6 rassemblent les travaux expérimentaux obtenus avec les techniques du BE et la MP. Le chapitre 4 présente la méthodologie et les résultats obtenus par l’analyse fréquentielle en appliquant la transformée de Fourier. Le chapitre 5 est consacré à l’analyse statistique à court terme par des moments d’ordre supérieurs dans le domaine temporel et le chapitre 6 est dédié à l’analyse croisée des signaux de tension et de pression.
Enfin, une conclusion générale faisant la synthèse des travaux réalisés au cours de cette thèse et des perspectives constituant plusieurs pistes de travail pour l’avenir sont présentées.
Références bibliographiques
[1] Charte de l'environnement 2004.
[2] B. Multon, « Production d’énergie électrique par sources renouvelables », Tech.
L’Ingénieur Traité Génie Electrique, 2003.
[3] G. Gerges, A. El Ali, N. Moubayed, et R. Outbib, « L’énergie éolienne au Liban: Bilan annuel, rendement et rentabilité », Proc SIELMEN, vol. 7, p. 361–366, 2007.
[4] L. Dos Santos, « Mécanisme de conduction protonique au sein de membranes hybrides pour piles à combustible », Université Pierre et Marie Curie-Paris VI, 2014.
[5] G. Porrometo, « Voiture à hydrogène : quels avantages et inconvénients par rapport aux voitures électriques ? - Tech », Numerama, 25-déc-2016.
[6] B. Legros, « Contribution à la gestion de l’eau dans les piles à combustible basse température par émission acoustique et bruit électrochimique », Grenoble, France, 2010. [7] R. Maizia, A. Dib, A. Thomas, et S. Martemianov, « Proton exchange membrane fuel cell
diagnosis by spectral characterization of the electrochemical noise », J. Power Sources, vol. 342, no Supplement C, p. 553‑561, févr. 2017.
[8] B. Legros, P.-X. Thivel, Y. Bultel, et R. P. Nogueira, « First results on PEMFC diagnosis by electrochemical noise », Electrochem. Commun., vol. 13, no 12, p. 1514‑1516, déc. 2011.
[9] R. Maizia, A. Dib, A. Thomas, et S. Martemianov, « Statistical short-time analysis of electrochemical noise generated within a proton exchange membrane fuel cell », J. Solid State
5
ETAT DE L’ART SUR LES PILES A COMBUSTIBLE
Sommaire
1.1 Les piles à combustible ... 7
1.1.1 Les Différents types de piles à combustible. ... 8
Alkaline Fuel Cell (AFC) : ... 9
Proton Exchange Membrane Fuel Cell (PEMFC) ... 9
Phosphoric Acid Fuel Cell (PAFC) ... 9
Direct Methanol Fuel Cell (DMFC) ... 10
Solid Oxide Fuel Cell (SOFC) ... 11
Molten Carbonate Fuel Cell (MCFC) ... 11
1.1.2 Applications ... 13
1.2 La Pile à combustible à membrane échangeuse de proton (PEMFC)
... 16
1.2.1 Principe de fonctionnement ... 16
1.2.2 La structure et les composants des PEMFC ... 17
1.3 Problématique scientifique liée à la gestion de l’eau ... 23
1.3.1 L’assèchement de la membrane ... 24
1.3.2 L’engorgement de la pile ... 25
1.4 Etat
de l’art des défaillances d’une pile à combustible ... 28
1.4.1. Introduction ... 28
1.4.2 Dégradations réversibles ... 28
1.4.3 Dégradations irréversibles ... 32
6
1.4.4 Les empoisonnements ... 35 1.4.5 Récapitulatif des défauts affectant les différents composants d’une pile PEMFC ... 36 1.4.6 Conclusion ... 38
7
1.1 Les piles à combustible
La découverte de la pile à combustible est attribuée à William Grove, avocat anglais et chercheur amateur en électrochimie en 1839. Il aurait d’abord effectué l’électrolyse de l’eau au moyen de deux électrodes en platine poreuses, d’une solution d’acide sulfurique et d’une source de courant conformément à l’expérience schématisée sur la figure (1.1a) [1], formant ainsi de l’hydrogène et l’oxygène. Il brancha ensuite un ampèremètre (figure 1.1b) et observa l’établissement d’un courant. Dans ce cas, le courant observé vient de la recombinaison de l’oxygène et l’hydrogène en eau. C’est le principe de base des piles à combustible.
Cette découverte est restée plus ou moins à l’abandon, à cette époque, tandis que se développaient en parallèle les moteurs à combustion, les accumulateurs et les piles électriques. Ce n’est qu’au début des années 1960 que la technologie des piles à combustibles a connue de grandes avancées, notamment pour ses applications dans le domaine spatial [1]. Ces piles, d’une puissance de quelques kilowatts ont servi de générateur électrique pour les véhicules spatiaux (programme Gemini).
Au cours des années 1970, les recherches menées sont essentiellement fondamentales et visent à améliorer les différents composants de la pile : électrodes, électrolyte, plaques bipolaires de distribution. DuPont®, dans le même temps, met au point la membrane Nafion®, Figure.1.1 : Expériences de William Grove : (a) Electrolyse de l’eau, (b) Pile à
Chapitre 1 Etat de l’art sur les piles à combustible
8
qui se retrouve actuellement dans la plupart des piles à combustible de type membrane échangeuse de protons (PEM).
Les piles restent toutefois couteuses, dans les années 1980, une trop faible durée de vie et une épaisseur trop importante ne permette pas de trouver une application commerciale. Les recherches et les travaux ralentissent dans la plupart des pays.
Dans les années 1990, les piles à combustible connaissent un regain d’intérêt en raison de :
L’aggravation des problèmes environnementaux liés à l’effet d’émission des gaz à effet de serre : les piles présentent un avantage en terme de pollution car les rejets sont beaucoup plus faibles voir nuls par rapport aux technologies concurrentes,
Les progrès technologiques (membranes, catalyseurs).
Le développement de nouveaux prototypes pour des applications spatiales. Aujourd’hui les piles à combustible ont de plus ou moins grande avancées sur le marché en fonction de leur technologie. Elles souffrent, comme beaucoup de systèmes, de devoir répondre au triptyque, coût, durabilité, performance, du choix de développements et d’appui financier de la part des industriels sur d’autres technologies, comme les batteries et les super capacités pour les sources électrochimique d’énergie par exemple, et d’énergies fossiles encore « peu chères » actuellement. L’association des différentes technologies des sources électrochimiques d’énergie, un besoin de stocker l’énergie électrique à plus grande échelle par le développement des renouvelables notamment, la raréfaction des énergies fossiles et leur impact sur l’environnement et la santé devrait permettre leur développement à plus grande échelle.
1.1.1 Les différents types de piles à combustible.
Les différentes recherches ont mené au développement de six technologies de piles à combustible classées selon la nature de leur électrolyte :
Solide : céramiques, polymères : Nafion, Dow ou Gore, …etc. Liquide : solution KOH, acide phosphorique …etc.
et/ou de la température de fonctionnement :
Basses températures qui englobent les technologies fonctionnant entre 60 et 220°C environ.
Hautes températures qui considèrent les piles fonctionnant entre 600 et 1000°C environ.
9 Alkaline Fuel Cell (AFC) :
Les piles alcalines fonctionnent à des températures variant de 60 à 80°C, sur un catalyseur en nickel, argent, platine-palladium ou platine-or, les réactions mises en jeu sont les suivantes [2]:
Oxydation anodique de l’hydrogène :
� + ��− → � � + �− (1)
Réduction cathodique d’oxygène :
� + � � + �− → ��− (2)
Pour ce type de pile, l’électrolyte utilisé est une solution aqueuse de KOH (30 à 40%). C’est un électrolyte conducteur d’ions hydroxyde (OH−) et un accélérateur de la réduction de l’oxygène. Cependant l’électrolyte peut réagir avec le dioxyde de carbone contenu dans l’air pour former un composé de carbonate, ce qui réduit énormément le rendement de la pile à combustible [2].
�� + ��− → �� −+ � � (3)
Proton Exchange Membrane Fuel Cell (PEMFC)
La PEMFC fonctionne à une température d’environ 80°C de façon à maintenir l’eau à l’état liquide dans la membrane [3].
Oxydation anodique de l’hydrogène :
� → �++ �− (4)
Réduction cathodique d’oxygène :
� + �++ �− → � � (5)
L’électrolyte est une membrane polymère mince qui assure le passage des protons (�+) de l’anode vers la cathode. Un catalyseur à base de platine est utilisé au niveau des électrodes. Du fait de son prix onéreux, de nombreuses recherche cherche à développer un catalyseur plus robuste et moins cher pour le substituer.
Phosphoric Acid Fuel Cell (PAFC)
La pile à combustible à acide phosphorique est le système le plus avancé dans le développement et la commercialisation. Elle est principalement utilisée pour des applications
Chapitre 1 Etat de l’art sur les piles à combustible
10
stationnaires, en tant que générateur électrique. Des centrales électriques de type PAFC, avec une puissance fournie comprise entre 5 et 20 MW, ont été installées dans différents endroits dans le monde pour fournir de l’électricité, du chauffage et de l’eau chaude à certains villages, usines ou hôpitaux [4].
Les avantages des PAFCs sont sa facilité de fabrication, sa stabilité thermique et chimique et son rendement énergétique proche de 80%. Les réactions qui se produisent dans une PAFC sont :
L’oxydation d’hydrogène (� ) à l’anode :
� → �++ e−, (6)
La réduction d’oxygène à la cathode :
� + �++ e− → � � (7)
La réaction globale :
� + � → � � (8)
Mise à part la nature de l’électrolyte, les composants de PAFC et PEMFC sont très semblables. Autrement dit, dans le cas des PAFCs l’électrolyte est une solution d’acide phosphorique, alors qu’il s’agit d'un polymère solide dans le cas de la PEMFC.
Direct Methanol Fuel Cell (DMFC)
La DMFC est une PEMFC utilisant du méthanol comme carburant. Le méthanol est fourni directement afin d’éviter le reformage catalytique compliqué et permet un stockage plus facile que l’hydrogène [5]. Les DMFC sont basées sur l'oxydation du méthanol sur une couche de catalyseur afin de former du dioxyde de carbone. De l'eau est consommée à l'anode et est produite à la cathode. Les protons (H+) sont transportés à travers la membrane échangeuse de
protons vers la cathode où ils réagissent avec de l'oxygène afin de produire de l'eau. Les électrons sont transportés via un circuit externe de l'anode vers la cathode, procurant ainsi de l'énergie aux équipements externes. Les demi-réactions sont :
L’oxydation anodique du méthanol :
�� �� + � � → �� + 6 �+ + 6e− (9)
La réduction cathodique de l’oxygène :
� + H+ + e− → 6 H O. (10)
La réaction globale :
11 Solid Oxide Fuel Cell (SOFC)
Le principe de fonctionnement d’une pile à oxyde solide (SOFC) est basé sur le mécanisme suivant : L’oxygène se dissocie en O2- à la cathode puis l’anion migre à travers l’électrolyte (conducteur ionique) à haute température et va se combiner à l’anode avec l’hydrogène pour former l’eau, selon le mécanisme ci-dessous [4] :
À la cathode, la réduction de l’oxygène :
� + �− → � −, (12)
À l’anode, l’oxydation de l’hydrogène :
� + � − → � � + �− (13)
On notera que le cermet de zirconium et le manganite de lanthane dopé au Strontium sont utilisés respectivement à l’anode et à la cathode comme catalyseur [5]. La caractéristique principale des SOFC réside dans leur température de fonctionnement relativement élevée (600 à 1000 °C), ce qui permet l’obtention d’une conductivité ionique suffisante de l’électrolyte céramique. En effet, cette température présente un double avantage [4]:
Elle permet d’abord l’utilisation directe d’hydrocarbures, sans passer par le reformage.
Elle produit d’autre part une chaleur élevée facilement exploitable en cogénération [4].
Pour ces raisons, la technologie SOFC se prête particulièrement bien à la production d’électricité décentralisée et à la cogénération (domaines couvrant des puissances allant de 1 kW à quelques dizaines de MW). Grâce à son fort rendement et sa capacité potentielle à fonctionner directement avec des hydrocarbures liquides [5].
Molten Carbonate Fuel Cell (MCFC)
Le développement des piles à combustible à carbonates fondus a débuté dans le milieu du vingtième siècle. Leurs avantages et inconvénients sont les mêmes que pour les SOFC. Une haute température améliore la cinétique de la réaction de réduction de l’oxygène et rend donc inutile l’utilisation de métaux nobles comme catalyseurs. Les réactions qui ont lieu dans ce type de piles sont les suivantes [5]:
Oxydation anodique de l’hydrogène en présence de chrome ou nickel-aluminium comme catalyseur :
Chapitre 1 Etat de l’art sur les piles à combustible
12
Réduction cathodique de dioxygène en présence d’un catalyseur d’oxyde de nickel :
� + �� + �− → �� − (15)
Ici, du dioxyde de carbone et l’oxygène sont consommés à la cathode et l’ion carbonate (CO32)
passe de la cathode à l’anode. L’électrolyte est fait d’un mélange de carbonates de métaux alcalins (carbonates de lithium, de potassium et de sodium) retenus par une matrice céramique d’oxyde d’aluminium et de lithium (����� ) [5].
Le tableau 1.1 récapitule et compare les différents types de piles à combustibles. Ce tableau rassemble les principales caractéristiques de chaque assemblage à savoir : la nature de l’électrolyte, les réactifs consommés et la température de fonctionnement. Les différents électrolytes utilisés nécessitent des architectures et des températures de fonctionnement variés. Les mêmes réactifs sont utilisés pour ces différentes applications : de l’hydrogène (pur ou réformé) et de l’oxygène pur (ou de l’air), à l’exception des piles DMFC qui utilisent la combustion directe du méthanol.
Tableau.1.1 : Comparaison des différents types de piles à combustible [6].
Type de Pile AFC PEMFC DMFC PAFC MCFC SOFC
Electrolyte Solution KOH Membrane polymère conductrice de proton Membrane polymère conductrice de proton Acide phoshorique Li CO et KCO fondu dans une matrice liAlO �� et � Ions dans l’élyctrolyte ��− �+ �+ �+ �� − � − Niveau de Temperature 60 - 80℃ 60 - 100℃ 60 - 100℃ 180 – 220℃ 600-660℃ 700 - 1000℃ Combustible � � (pur ou reformé) Méthanol � (pur ou reformé) � (pur ou reformé) � (pur ou reformé)
Oxydants � (pur) Air Air Air Air Air
Domaines d’applications Spacial Automobiles, Portable, Cogénération Maritime Portable Cogénération Cogénération Production Centralisée D’électricité, Maritime Cogénération Production Centralisée D’électricité, Maritime Automobile
13
1.1.2 Applications
Du fait de leur grande flexibilité en géométrie et en volume, les applications des piles à combustibles sont nombreuses. On retient généralement les applications stationnaires, transport et portables.
1.1.2.1 Applications stationnaires
Les piles à combustible semblent très prometteuses pour les applications stationnaires. Ceci parce qu’elles permettent une production d’énergie décentralisée associée à un haut rendement énergétique. De nombreux prototypes sont déjà en cours d’essai (figure 1.2). Les deux types de pile, « basses » et « hautes » températures, sont envisagés mais avec des objectifs différents [7].
Les piles « basses températures » conviennent pour des systèmes de faible puissance (quelques kilowatts). Leur temps de mise en marche étant beaucoup plus court que celui des piles « hautes températures », elles semblent adaptées pour des applications domestiques en cogénération (eau chaude, chauffage), pour des systèmes de secours ou de sécurité ainsi que pour une utilisation dans des lieux isolés.
Les piles « hautes températures » sont envisagées dans le cadre de la production d’énergie centralisée (en remplacement notamment de centrales thermiques trop polluantes) ou décentralisée de moyenne puissance (quelques centaines de kilowatts). Pour la production centralisée d’énergie, seules ces piles sont adaptées. En effet, la haute température des vapeurs peut être valorisée par l’utilisation d’une turbine à vapeur ou à gaz (voire les deux pour une SOFC). Dans ces conditions, elles produisent, ainsi, de l'électricité avec un rendement total très élevé qui pourrait avoisiner les 70%. Dans le cadre, d’une utilisation comme source de courant délocalisée, elles présentent également l’avantage de pouvoir fonctionner avec un grand nombre de combustibles (notamment le gaz naturel) et ainsi ne pas nécessiter de reformeurs externes, qui sont très coûteux et d’une durée de vie courte. La chaleur produite peut être valorisée par une utilisation directe (chauffage, refroidissement grâce à une pompe à chaleur, eau chaude). Un inconvénient de ces systèmes est le temps important nécessaire à leur mise en marche.
Deux améliorations majeures sont requises en vue de l’utilisation commerciale des piles pour les applications stationnaires : une durée de vie supérieure à 40000 heures de fonctionnement et une diminution de leur coût de production.
Chapitre 1 Etat de l’art sur les piles à combustible
14
Le projet EPACOP, débuté en 2003 pour une durée de deux ans, est un exemple d’une telle application visant à tester en conditions réelles l’utilisation de cinq piles à combustibles dans quatre villes (Dunkerque, Nancy, Limoges et Sofia-Antipolis). D’une puissance de 5 kW en électricité et 7 kW en chaleur, elles alimentent des bâtiments administratifs [7].
1.1.2.2 Transport
Le transport est le domaine d’application à l’origine du développement de la pile à combustible à partir des années 90. Le transport est un des secteurs les plus consommateurs en ressources énergétiques et la quasi-totalité de l’énergie est fournie par les hydrocarbures. Dans un souci environnemental et considérant la raréfaction des énergies fossiles, de nouvelles sources doivent être imaginées. C’est dans cette application que les PEMFC trouvent un regain d’intérêt, grâce à leur faible température de fonctionnement et leur "simplicité" de mise en œuvre. Cependant, un des problèmes majeurs des PEMFC reste l’approvisionnement en hydrogène. Pour le moment, il est surtout stocké soit sous forme gazeuse (haute pression : de 300 à 700 bars) ou liquide [7, 8].
Figure 1.2 : Photographie de la pile à combustible de type PEMFC. Limoges, projet EPACOP [7].
15 1.1.2.3 Portable
Le marché des appareils électroniques portatifs (téléphones, ordinateurs, caméscopes, agendas électroniques...etc.) en constante croissance peut également être alimenté par les piles à combustibles (figure 1.4). Ces appareils, d'une gamme de puissance comprise entre 0.1 et 10 W, souffrent actuellement de leur faible autonomie [6].
Figure 1.3 : Bus Mercedes Citaro fonctionnant avec une PEMFC [8].
Figure 1.4 : Système de pile à combustible de type PEM intégré
Chapitre 1 Etat de l’art sur les piles à combustible
16
L'autonomie d’une pile à combustible ne dépend que de la taille du réservoir de carburant (hydrogène ou méthanol). Leur modularité permet de créer des systèmes de petites puissances avec des cellules de faibles surfaces. Toutefois, la miniaturisation du système semble avoir ses limites. La création de micro piles passe par la miniaturisation de l'ensemble des composants (pile, pompe, convertisseur de courant.) [9].
1.2 La Pile à combustible à membrane échangeuse de proton (PEMFC)
La PEMFC (Proton Exchange Membrane Fuel Cell en anglais) est actuellement le type de pile à combustible le plus étudié. Cette pile fonctionne à basse température (<100°C) et utilise l’hydrogène comme combustible [3]. Les PEMFCs permettent d’envisager une technologie simplifiée qui peut assurer un démarrage rapide (son temps de mise en fonctionnement est quasi-instantané), une évacuation aisée de la chaleur, un rapport puissance /poids intéressant et une pollution quasi nulle. De ce fait et de part de la grande flexibilité dans leurs géométries et leurs volumes, les applications couvertes sont multiples, allant du domaine automobile à ceux du stationnaire et du portable.
1.2.1 Principe de fonctionnement
Le principe de fonctionnement de la pile à combustible à membrane échangeuse de protons est illustré dans la figure (1.5).
Figure 1.5 : Principe de fonctionnement d’une pile à combustible à membrane échangeuse de proton [12].
17
Une PEMFC utilise comme électrolyte une membrane solide à base d’un polymère perfluorosulfoné fonctionnalisé par des fonctions acides [3]. Généralement, le combustible utilisé est l’hydrogène et le comburant l’oxygène. L’hydrogène alimente l’anode où, en présence de catalyseur, il libère ses électrons (oxydation Eq.16) et se transforme en protons H+ selon la réaction suivante :
� → �++ e− (16)
La membrane est conductrice de protons (PEM) et permet aux ions H+ de la traverser pour atteindre la cathode. Par contre elle est électroniquement isolante. Les électrons sont conduits à travers un circuit extérieur (produisant l’énergie électrique) vers la cathode de la pile où ils vont participer à la réaction de réduction de l’oxygène (Eq.17).
�++ �−+ � → � � (17)
Les produits de réactions seront donc de l’eau et de l’énergie sous forme de chaleur. La réaction globale donne :
� + � → � � + ��� ��� é��� � � + �ℎ �� (18)
1.2.2 La structure et les composants des PEMFC
Une PEMFC est constituée en général d’un assemblage de plusieurs cellules élémentaires qui forment un « stack » (figure 1.6a). La taille et le nombre des cellules sont conditionnés ensuite par la puissance électrique du système. Une mono-cellule d’une pile PEMFC (Figure 1.6b) comprend généralement : l’assemblage membrane-électrodes (1), les joints d’étanchéité (2), les plaques bipolaires (3), collecteur de courant (4), et la plaque support (5).
Chapitre 1 Etat de l’art sur les piles à combustible
18 1.2.2.1 L’assemblage membrane-électrodes (AME)
L’assemblage membrane-électrodes représente l’élément primordial d’une pile à combustible sans lequel celle-ci ne pourrait pas fonctionner. On la surnomme aussi le cœur de la pile. L’AME est constitué des éléments suivants : une membrane (l'électrolyte), deux électrodes (une pour l’anode et une pour la cathode).
1.2.2.1.1 La membrane
La membrane, joue un rôle très important dans une PEMFC. D’une part, elle sépare l’anode de la cathode et ne laisse pas passer les électrons et les gaz, d’autre part elle assure la conduction des protons de l’anode vers la cathode. Les membranes les plus utilisées dans les PEMFC sont les membranes acide perfluorosulfonique (PFSA) [10]. En effet ces membranes ont une bonne stabilité chimique et possèdent une conductivité ionique assez grande lorsqu’elles sont bien hydratées : 0.1 S.cm-1 à 80 °C pour une humidité relative de 100% [11]. Ces membranes sont toutefois limitées à des températures inférieures à 100°C [12].
La structure chimique des membranes PFSA est illustrée en figure (1.7).
Il s’agit d’un polymère composé d’un squelette fluoro-carboné, dérivé du PTFE (Polytetrafluorethylene), aussi appelé Téflon ®, sur lequel sont greffées des chaines possédant une fonction sulfonate fortement hydrophile et conférant au polymère de bonnes propriétés de conduction ionique. Seuls les cations, et notamment les protons (H+), sont mobiles et libres d’être transportés par l’intermédiaire des groupements sulfonates. Le mouvement des protons, pouvant se solvater dans l’eau, est facilité par une bonne hydratation de la membrane.
19
Généralement l’épaisseur de ces membranes est comprise entre 18 et 180 µm. Ces membranes peuvent subir des dégradations mécaniques, thermiques et chimiques [13–15]. En effet, les membranes peuvent, par des effets de rétrécissement/gonflement dus aux conditions opératoires (∆P, T, HR), présenter des déchirures et fissures [16–20]. Cela entraine une augmentation de la perméation des gaz [15]. La déformation et décomposition de la membrane peu augmenter ce phénomène notamment par une température de fonctionnement élevée. Consécutivement au phénomène de perméation, la réaction exothermique de combustion de l’hydrogène produit des surchauffes locales accentuant la dégradation de la membrane et diminuant la conductivité protonique.
1.2.2.1.2 Les électrodes
Les lieux des demi-réactions d’oxydoréduction sont appelés les électrodes, ou couches actives. L’électrode doit permettre le transport des protons vers la membrane, celui électrons vers les collecteurs de courant et le transport des réactifs et des produits de réaction (l’eau et la chaleur). Les électrodes sont donc constituées d’une poudre de carbone, conductrice électriquement, sur lesquelles sont déposées des particules de platine [17]. Ces particules sont liées entre elles à l’aide du polymère assurant la conductivité protonique [21, 22]. Les électrodes forment donc des zones de « triple contact » composées des trois matériaux : le platine supporté par le carbone et le polymère (figure 1.8).
Le diamètre des particules de platine est nanométrique afin d’offrir une surface de réaction la plus grande possible, tout en diminuant la masse de platine employée. Ceci a pour but de réduire les coûts et la quantité de platine. En 1960, un chargement de 30 mg de platine par cm² était utilisé [23], contre cent fois moins, 0.3 mg.cm-2aujourd’hui. L’objectif annoncé par le DOE est
maintenant de 0.1 mg.cm-2. Le prix du platine a lui augmenté de 600% sur les 20 dernières
années [10]. La structuration des électrodes, notamment avec des nanofibres de carbone orientées afin d’augmenter les surfaces électrochimiques, d’améliorer la stabilité et de diminuer fortement le chargement en platine (< 0.03 mgPt.cm-2) sont en cours de développement [24].
Les électrodes subissent, de manière similaire à la membrane, des dégradations. Le platine peut être dissout à cause de conditions agressives (potentiel élevé, faible pH, présence de radicaux), redéposé en surface ou dans la membrane ou bien s’agglomérer [12, 17, 25–27], diminuant la surface spécifique du catalyseur. Un empoisonnement du catalyseur au CO notamment ou par des ions métalliques peut aussi avoir lieu [28– 31]. Le support carboné peut subir des dégradations par la formation de groupements oxygénés (carboxyle, carbonyle,
Chapitre 1 Etat de l’art sur les piles à combustible
20
hydroxyle, phénol) en surface du carbone [32, 33] puis par le dégagement éventuel de CO2 due
à la corrosion du carbone.
1.2.2.1.3 Les couches poreuses
Les couches poreuses ou couches de diffusion (GDL) ont pour fonction d’amener de manière homogène les gaz réactifs des canaux vers les électrodes, d’évacuer l’eau et la chaleur produite et d’assurer le transport des électrons jusqu’aux collecteurs de courant. Elles doivent être perméables aux réactifs et produits et garantir un excellent contact électrique et thermique entre les plaques bipolaires et l’AME [34]. Elles doivent aussi assurer une bonne tenue mécanique. Les couches poreuses sont généralement composées de papier ou de feutre de carbone tissé ayant une taille moyenne de pores de 10 à 50 µm.
Figure 1.8 : (a) Vue du support carboné avec une dispersion uniforme du platine (b) Zoom sur les particules de platine Pt en surface d’une sphère de carbone (c) Schéma de la composition d’une électrode [10].
21
Leur porosité varie entre 60 et 90% avec des épaisseurs comprises entre 50 et 450 µm. Lors du serrage, elles peuvent subir une diminution de 10 à 40% de leur épaisseur. L’hydrophobicité des couches poreuses est assurée par un traitement avec du PTFE (Téflon®) afin de faciliter l’évacuation de l’eau. Ce traitement est souvent réalisé par spray, ce qui implique une déposition en surface, le PTFE se loge ainsi plutôt dans les macropores que les micropores [35]. La quantité de PTFE varie entre 10 et 40% en massique et peut affecter les performances [36, 37].
Aujourd’hui, une couche microporeuse (MPL) est insérée entre les électrodes et la GDL (figure 1.9). Cette couche poreuse est composée de grain de carbone de taille de l’ordre de 10 à 100 nm. Un traitement PTFE est réalisé par spray ou à l’aide d’une encre [38, 39]. L’ajout de cette couche amène à une amélioration des performances [40–43] par un meilleur contact électrique et thermique entre les couches [44]. Les travaux de Hamour et al ont montré que, la compression optimale de la GDL améliore les performances de la pile à combustible [45, 46].
1.2.2.2 Les plaques d’alimentation
Dans une pile à combustible chaque AME et GDLs est situé entre deux plaques spécifiques appelées plaques d’alimentation ou plaques bipolaires. Physiquement, ces plaques représentent les frontières entre deux cellules. Elles assurent la tenue mécanique de la cellule, et permettent la séparation des réactifs entre chaque cellule. Elles assurent également la liaison électrique entre les cellules et le circuit externe, jouant le rôle de conducteur électronique entre Figure. 1.9 : Structure de la couche de diffusion MPL+GDL avec émission d’une
goutte au niveau du canal (CL : catalyst layer, PEM : proton exchange membrane, GC : gas channel) [37].
Chapitre 1 Etat de l’art sur les piles à combustible
22
l’anode productrice d’électrons et la cathode consommatrice d’électrons. De plus, elles doivent évacuer efficacement l’eau et les gaz non consommés. Ainsi que la chaleur libérée par les réactions.
Les matériaux utilisés pour la fabrication de plaques bipolaires doivent présenter certaines propriétés spécifiques, notamment : une bonne conductivité électrique et thermique, imperméabilité aux gaz, résistance à la corrosion, bonnes stabilités mécanique et chimique aux réactifs et produits de réactions. Le graphite est un matériau qui remplit les impératifs techniques cités précédemment lorsqu’il est imbibé ou enduit, par exemple, d’une résine appropriée réduisant considérablement sa porosité. Les plaques métalliques sont aussi envisagées en terme de compacité et coût mais un traitement spécifique est obligatoire pour assurer leur tenue à la corrosion.
Les plaques bipolaires présentent différentes géométries de canaux pour assurer un écoulement optimal des gaz et cette géométrie peut être différenciée entre l’anode et la cathode. Les directions d’écoulement sur les électrodes peuvent également être différentes les unes par rapport aux autres : mode co-courant ou contre-courant ou croisés. Le choix de la géométrie et l’optimisation des canaux d’écoulement des plaques bipolaires affectent fortement la performance des PEMFCs, particulièrement au travers de la gestion de l’eau et la distribution des gaz sur les électrodes.
On trouve dans la littérature trois principaux types de canaux illustrés sur la figure (1.10) : en parallèles (a), en serpentins (b) ou interdigités (c). Chaque géométrie a ses avantages et inconvénients. Par exemple la géométrie (a) permet d’avoir de faibles pertes de charges mais présente une capacité à évacuer l’eau faible. La géométrie (b) au contraire permet une bonne évacuation de l’eau mais génère des pertes de charge entre l’entrée et la sortie plus élevées [47]. L’intérêt de la dernière géométrie est de forcer le passage du gaz dans la GDL. Elle présente les meilleures performances en termes de gestion de l’eau. En contrepartie les pertes de charges générées par ce type d’écoulement sont largement supérieures [48].
La plaque bipolaire doit être légère afin de limiter le poids total de la pile. Par ailleurs, les canaux dont dépendent les performances de la pile doivent être usinés avec soin, d’où une fabrication délicate et des prix élevés. Les recherches se portent sur des matériaux composites carbone-polymère, ou organiques [49] ainsi que des aciers traités en surface contre la corrosion.
23
Les dégradations des plaques d’alimentation sont souvent dues à un endommagement mécanique et chimique entrainé par des pressions de serrage excessives, des températures et des conditions opératoires extrêmes.
1.3 Problématique scientifique liée à
la gestion de l’eau
Malgré leurs avantages indéniables par rapport aux autres types de pile à combustible, les piles à combustible à échangeuse de proton (PEMFC) posent de nombreux défis scientifiques et technologiques. Leurs électrolytes solides qui constituent un de leurs atouts principaux, sont paradoxalement sujets aux améliorations. Ces membranes, le plus souvent en Nafion®, ont un coût élevé et ne peuvent supporter des températures supérieures à 100°C, ce qui limite les possibilités de diminution de la teneur en platine (le catalyseur) au niveau des électrodes ou sont remplacement total. D’autre part, les performances des membranes en Nafion® ou à base de Nafion® en terme de conduction protonique sont conditionnées par leur teneur en eau. Une gestion rigoureuse de la quantité d’eau présente dans le cœur de pile est donc essentielle pour améliorer le comportement électrique du système.
La gestion de l’eau dans la pile à combustible fait intervenir de nombreux phénomènes couplés les uns aux autres et ayant lieu à différentes échelles. D’une importance cruciale pour les performances et la durabilité des piles à combustible à membrane échangeuses de protons elle s’articule autour d’axes opposés [47, 50, 51]: l’hydratation optimale de la membrane et l’évacuation de l’eau hors de l’AME de manière à éviter le noyage des électrodes. Un très grand nombre de travaux de recherche ont été effectués pour comprendre et maîtriser les différents aspects de la gestion de l’eau dans les PEMFC. Un nombre important d’articles ont été publiés sur les aspects de la gestion de l’eau [10]. D’autres sujets, comme le diagnostic du noyage et de
Chapitre 1 Etat de l’art sur les piles à combustible
24
l’assèchement dans les PEMFC [52, 53], le transport de l’eau dans l’AME [10, 54], les phénomènes de chute de tension liés à la gestion de l’eau [52], les différentes techniques de visualisation de l’eau dans les PEMFC [50] ou encore l’influence de la gestion de l’eau sur la durée de vie des AME sont également traités [55].
La gestion de l’eau est un challenge global qui se traite à l’échelle locale. Les spécificités des différents éléments d’une PEMFC doivent être étudiées individuellement de manière à appréhender au mieux les mécanismes responsables du transport de l’eau. Dans cette section, nous présenterons donc les causes et les conséquences de la mauvaise gestion de l’eau sur la durabilité et les performances de la PEMFC.
1.3.1
L’assèchement de la membrane
Le risque d’assèchement de l’électrolyte est particulièrement important en entrée de cellule, là où la quantité d’eau produite par la réduction de l’oxygène n’est pas suffisamment importante pour en assurer son hydratation.
1.3.1.1 Causes de l’assèchement :
L’assèchement de l’électrolyte est principalement dû à des conditions opératoires inadaptées :
L’arrivée de gaz secs en entrée de pile engendre un assèchement très rapide de l’électrolyte. Au contact de la membrane, les gaz secs vont absorber l’eau qu’elle contient. Ce phénomène est particulièrement marqué pour une membrane perfluorée de type Nafion dont le squelette hydrophobe en tétrafluoroethylène favorise la désorption de l’eau.
Une température de fonctionnement trop élevée accélère l’évaporation de l’eau aux interfaces de la membrane et provoque son assèchement, ce qui engendre des risques de fissuration comme le montre la figure (1.11). Une membrane fissurée n’assure plus l’étanchéité entre les deux électrodes. La combustion de l’hydrogène mis en contact avec de l’oxygène, augmente la température locale, accentuant le phénomène.
25 1.3.1.2 Conséquences de l’assèchement :
Outre le risque de fissuration de la membrane, son assèchement provoque une diminution de sa conductivité protonique [54]. La figure (1. 12) illustre l’importance de l’hydratation de la membrane.
L’augmentation de la résistance de l’électrolyte au niveau des zones actives (électrodes) peut également affecter les cinétiques de réduction de l’oxygène et d’oxydation de l’hydrogène. Ceci se caractérise par une augmentation des surtensions d’activation anodique et cathodique. Par des analyses de spectroscopie d'impédance, Springer et al [56] montré les effets négatifs d’une mauvaise hydratation des gaz sur la cinétique de réduction de l'oxygène et sur la conductivité protonique de la couche catalytique.
1.3.2
L’engorgement de la pile
Paradoxalement à l’assèchement, une quantité d’eau trop importante peut également nuire aux performances de la pile [57, 58]. L’accumulation d’eau liquide peut se produire soit au niveau de l’électrode soit dans la GDL (figure 1.13), soit dans les canaux de distribution des gaz (Figure 1.14).
Figure 1.12 : Evolution de la conductivité de la membrane en fonction de la teneur en eau [57].
Chapitre 1 Etat de l’art sur les piles à combustible
26 1.3.2.1 Causes de l’engorgement :
L’engorgement de la pile peut être dû à de mauvaises conditions opératoires :
Une température de fonctionnement trop faible favorise la condensation de l’eau. L’eau liquide peut engorger les sites catalytiques et les zones de diffusion des gaz.
L’arrivée de gaz trop humides en entrée de pile accélère son engorgement. Dès que les gaz sont saturés, leur capacité d’absorption de la vapeur d’eau devient nulle. L’eau produite par la pile ne pouvant s’évaporer dans le flux de gaz, reste sous forme liquide et encombre les zones catalytiques, les pores des différentes couches et les canaux de la pile. Ces phénomènes sont amplifiés par un mauvais choix des matériaux constituant le cœur de pile, induisant un problème d’évacuation de l’eau produite par la cathode :
Si la membrane est trop épaisse, le flux électro-osmotique (transport d’eau de l’anode vers la cathode dû au transport des ions) l’emporte sur le flux diffusif (transport de l’eau
Figure 1.14 : Accumulation d’eau liquide dans les canaux de distribution des gaz [58].
27
produite à la cathode vers l’anode dû à la différence de pression partielle en eau de part et d’autre de l’électrolyte). Ce déséquilibre entre les flux d’eau membranaires induit un assèchement du côté anodique et un engorgement du côté cathodique. Pour éviter ce problème, il est possible, soit de diminuer l’épaisseur de la membrane ou de changer sa nature pour augmenter son coefficient de diffusion, soit d’augmenter le gradient de pression entre l’anode et la cathode (en prenant garde à ne pas imposer de trop grandes contraintes mécaniques à l’électrolyte) [58].
1.3.2.2 Conséquences de l’engorgement :
L’accumulation d’eau liquide dans les canaux et au niveau des électrodes engendre une mauvaise diffusion des gaz réactifs vers les sites catalytiques. La cinétique globale des réactions électrochimiques est alors fortement ralentie. De plus, l’encombrement de l’accès aux électrodes crée des zones mortes ne produisant pas d'électricité. Ces hétérogénéités locales de fonctionnement sont très nuisibles à la durée de vie de la pile. L’accumulation d’eau liquide dans les canaux peut engendrer un écoulement diphasique de type bouchon, induisant des pertes de charge importantes et indirectement, un gradient de pression de part et d’autre de l’électrolyte susceptible d’entraîner ou d’accélérer sa détérioration.
Chapitre 1 Etat de l’art sur les piles à combustible
28
1.4
Etat de l’art des défaillances d’une pile à combustible
1.4.1. Introduction
Dans cette section, nous nous intéressons aux défaillances inhérentes aux piles à combustible à membranes échangeuses de protons (PEMFC), alimentées en H2/O2 ou H2/Air, et fonctionnant à des basses températures (< 100°C). Ces dysfonctionnements se séparent en deux catégories. Ceux dus à des causes internes ou externes. Les causes internes découlent du fonctionnement même de la pile à travers des dégradations dues au vieillissement, à une mauvaise gestion de l’eau et de la chaleur. Celles externes sont reliées aux polluants, amenés notamment par les gaz. On parlera ici d’empoisonnement. Ces dégradations peuvent être réversibles ou irréversibles. Une dégradation irréversible aura une constante de temps lente, et une dégradation réversible sera rapide.
Après cette bref introduction, nous présenterons donc les dégradations internes : Dégradations réversibles.
Dégradations irréversibles.
Ainsi que des dégradations externes : Les empoisonnements.
1.4.2 Dégradations réversibles
Les défaillances réversibles concernent des conditions de fonctionnement non optimales (températures de la pile, humidités relatives des gaz à l’entrée, débits des gaz, stœchiométrie des gaz, pression des gaz.) affectant les performances de la pile et pouvant amener à un arrêt temporaire du système. Il est donc important de les détecter et les corriger rapidement afin d’éviter l’arrêt total de la pile à combustible.
1.4.2.1 Dégradations liées à la gestion de l’eau
L’eau dans la PEMFC provient de deux voies essentielles, à savoir l’humidification des gaz (que ce soit le combustible du coté anodique ou le comburant du coté cathodique), ou bien l’eau produite au sein même de la couche active coté cathode [59]. La gestion de l’eau au cœur de la pile est primordiale pour son bon fonctionnement.
La figure (1.15) représente un schéma des différents mouvements d’eau au sein d’une cellule de pile à combustible de type PEM. L’eau est créée au sein de la couche active cathodique par la réaction de réduction d’oxygène (la quantité d’eau produite est
29
proportionnelle au courant demandé). L’eau produite par la réaction diffuse à travers la membrane par un gradient de concentration (diffusion) de la cathode vers l’anode. Par ailleurs, les protons produits par la réaction lors de la réaction d’oxydation d’hydrogène se déplaçant de
l’anode vers la cathode pour y être consommé, entrainent avec eux des molécules d’eau. Ce phénomène est appelé électro-osmose [60]. De plus, de l’eau peut être injecté en entrée de la pile avec les gaz afin d’hydrater la membrane. Enfin, l’eau est évacuée, sous forme vapeur et/ou liquide à l’extérieur de la pile [54, 60],
Une mauvaise gestion de l’eau peut donner lieu à deux types de défauts antagonistes : le noyage (engorgement) et l’asséchement.
Noyage
L’accumulation d’eau liquide au sein d’une PEMFC peut provoquer un noyage, ce qui entraine une perte importante du rendement de la pile. L’eau peut s’accumuler à différents niveaux dans la pile, soit :
Dans les canaux d’alimentation des gaz, ce qui provoque des problèmes d’écoulements et l’augmentation des pertes de charge liées au bouchon d’eau ce qui amène au blocage de la distribution des réactifs dans des secteurs entiers de la cellule.
Figure.1.16. Schéma représentant les différents mouvements d'eau au sein d'une cellule de pile à combustible [60].

![Figure 1.5 : Principe de fonctionnement d’une pile à combustible à membrane échangeuse de proton [12]](https://thumb-eu.123doks.com/thumbv2/123doknet/7791089.259908/27.892.164.823.723.1070/figure-principe-fonctionnement-pile-combustible-membrane-échangeuse-proton.webp)
![Figure 1.12 : Evolution de la conductivité de la membrane en fonction de la teneur en eau [57]](https://thumb-eu.123doks.com/thumbv2/123doknet/7791089.259908/36.892.133.736.477.835/figure-evolution-conductivité-membrane-fonction-teneur-eau.webp)
![Figure 2.1 : Courbe de polarisation typique d’une Pile à combustible de type PEM [13]](https://thumb-eu.123doks.com/thumbv2/123doknet/7791089.259908/58.892.149.733.294.705/figure-courbe-polarisation-typique-pile-combustible-type-pem.webp)
![Figure 2.2: Spectre d’impédance pour différentes valeurs du courant de fonctionnement [46]](https://thumb-eu.123doks.com/thumbv2/123doknet/7791089.259908/60.892.142.735.176.534/figure-spectre-impédance-valeurs-courant-fonctionnement.webp)
![Figure 2.5 : Détection de l’état d’une pile à combustible par l’analyse direct de du bruit électrochimique en potentiel : (a) Etat normal, (b)Etat Engorgé (c) Etat sec [96]](https://thumb-eu.123doks.com/thumbv2/123doknet/7791089.259908/67.892.173.697.228.1051/figure-détection-combustible-analyse-direct-électrochimique-potentiel-engorgé.webp)
![Figure 2.7 : Skewness et Kurtosis à court terme de la décharge d’une batterie Li-ion [107]](https://thumb-eu.123doks.com/thumbv2/123doknet/7791089.259908/68.892.257.674.510.967/figure-skewness-kurtosis-court-terme-décharge-batterie-li.webp)