HAL Id: tel-02193725
https://tel.archives-ouvertes.fr/tel-02193725
Submitted on 24 Jul 2019HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Géopolymérisation et activation alcaline des coulis
d’injection : structuration, micromécanique et résistance
aux sollicitations physico-chimiques
Anass Cherki El Idrissi
To cite this version:
Anass Cherki El Idrissi. Géopolymérisation et activation alcaline des coulis d’injection : structuration, micromécanique et résistance aux sollicitations physico-chimiques. Génie civil. École centrale de Nantes, 2016. Français. �NNT : 2016ECDN0015�. �tel-02193725�
Anass CHERKI EL IDRISSI
Mémoire présenté en vue de lʼobtentiondu grade de Docteur de lʼÉcole Centrale de Nantes sous le sceau de l’Université Bretagne Loire
École doctorale : Sciences pour l'Ingénieur, Géosciences, Architecture Discipline : Génie Civil
Unité de recherche : Institut de recherche en génie civil et mécanique UMR CNRS 6183 Soutenue le 14 décembre 2016
Géopolymérisation et activation alcaline des coulis
d’injection : structuration, micromécanique et
résistance aux sollicitations physico-chimiques
JURY
Président : Christophe LANOS, Professeur, Université de Rennes 1 Rapporteurs : Martin CYR, Professeur, Université Toulouse III Paul Sabatier
David BULTEEL, Professeur, Ecole des Mines de Douai Examinateur : Dimitri DENEELE, Directeur de Recherche, IFSTTAR Invitée : Sabine DARSON, Docteur, Soletanche Bachy
Directeur de Thèse : Ahmed LOUKILI, Professeur, Ecole Centrale de Nantes
i
Résumé
La nécessité de construire de manière durable, rationnelle et écologique incite à l’innovation et la recherche d’alternatives, telles que la géopolymérisation et l’alcali-activation, qui suscitent un intérêt croissant dans l’industrie de la construction. Dans ce sens, ces technologies permettent de valoriser des matières premières à plus faible impact environnemental pour le développement d’une nouvelle famille de matériaux. Cependant, ces mécanismes réactionnels sont complexes et il est encore nécessaire de lever plusieurs verrous avant leur implémentation : la confusion entre les deux processus, l’absence d’approches de formulation rationnelles, la méconnaissance de certaines vulnérabilités, etc.
La présente thèse s’intègre dans cette dynamique et a pour objectif une meilleure connaissance des géopolymères et des matériaux alcali-activés. Le cadre de travail est le développement de formulations de coulis d’injection et renforcement de sols. Un programme expérimental basé sur une sélection de compositions est établi afin de caractériser les principales propriétés de ces matériaux. Les différences entre les deux processus de structuration sont relevées à travers une étude physico-chimique (DRX, RMN) et liées aux évolutions macroscopiques au jeune âge. La géopolymérisation se traduit par la formation d’un réseau aluminosilicate amorphe, une stabilité volumique au cours du durcissement, piloté par un processus de polycondensation. L’alcali-activation du laitier présente des aspects similaires à l’hydratation du ciment : dissolution/précipitation, formation de gels CSH et retrait chimique. Un travail d’optimisation de formulation est mené afin de répondre à des critères d’application et définir les paramètres influençant le comportement rhéologique et mécanique des coulis. La substitution partielle du métakaolin ou du laitier par des cendres volantes permet la régulation du comportement à l’état frais et de la résistance du matériau. Une méthodologie basée sur l’analyse de la microstructure est mise en place pour lier la micromécanique aux propriétés macroscopiques. L’homogénéisation multi-échelles a permis d’évaluer le module élastique des matériaux et peut servir de plateforme pour une analyse globale du comportement mécanique. Enfin, une étude de durabilité de ces matériaux est entamée en évaluant la sensibilité au séchage et à la lixiviation en milieu acide. Elle révèle différents mécanismes de dégradation en fonction de la composition et de la sollicitation. Les matériaux sont sensibles au séchage mais les géopolymères étudiés sont apparus très stables en milieu acide.
ii
Abstract
The need for more durable, rational and ecological constructions encourages innovation and the search for alternatives, such as geopolymerization and alkali-activation, with a growing interest. These technologies allow the use of resources with a lower environmental impact in developing a new class of materials. However, both reaction mechanisms are complex and some issues need further investigation before a proper implementation: the confusion between these processes, the absence of a rational design approach, the lack of knowledge concerning some mechanisms of degradation, etc.
The present thesis joins this dynamic and aims at a better understanding of geopolymers and alkali-activated materials to design soil injection grouts. An experimental program has been established based on selected mix designs to study their main properties. The differences between both structuration processes were determined through a physicochemical study (XRD, NMR). They were correlated to the macroscopic phenomena observed at early age. An optimization of the mixtures was carried to satisfy the application criteria and define the parameters controlling the rheological and mechanical behavior of the grouts. Using a micromechanical characterization and multiscale homogenization, a methodology has been designed to determine the elastic modulus of the materials. This can be used as a first tool to analyze the global mechanical behavior. Finally, the sensitivity to drying and exposure to acid environments was assessed.
iii
Remerciements
Avant tout, je souhaite exprimer mes sincères remerciements à M. Christophe Lanos, Professeur à l’Université de Rennes, pour avoir accepté de présider mon jury de thèse. Ses conseils me seront très utiles pour la valorisation de ces travaux. Je voudrais ensuite remercier M. Martin Cyr, Professeur à l’Université de Toulouse III, et M. David Bulteel, Professeur à l’Ecole des Mines d’Alès, pour leurs précieux retours sur ce manuscrit et pour la discussion qui s’en suivit pendant la soutenance. Je souhaiterais aussi exprimer ma gratitude à M. Dimitri Deneele, Directeur de recherche à l’IFSTTAR Nantes, pour avoir fait partie de mon jury, sans oublier toute l’aide qu’il m’a fourni pendant toute ma thèse.
En plus de sa participation à mon jury, tout ce travail de thèse n’aurait pas eu lieu sans la confiance, l’initiative et le soutien de Mme Sabine Darson, Responsable du Laboratoire Matériaux de Soletanche Bachy. Pendant plus de trois ans, son support a été de taille et j’ai toujours pu et dû me tourner vers elle pour ses conseils et sa perspective.
Toute ma gratitude est également envers mon directeur de thèse M. Ahmed Loukili, Professeur à l’Ecole Centrale de Nantes, pour avoir cru en moi pour cette thèse et pour m’avoir orienté, aidé et défendu lors des trois ans.
Je voudrais aussi remercier mon co-encadrant M. Emmanuel Rozière, Maître de Conférences à l’Ecole Centrale de Nantes, pour sa disponibilité et son soutien. Il a été tout aussi investi que moi dans ce projet, en alimentant à chaque fois ma curiosité, tout en me permettant de mieux l’orienter vers les pistes les plus pertinentes.
Ensuite, je dois remercier M. Michael Paris, Ingénieur de Recherche à l’Institut des Matériaux Jean Rouxel, pour m’avoir introduit, accompagné et formé lors de ma découverte de la RMN du solide.
Je voudrais aussi remercier M. Frédéric Grondin, Professeur à l’Ecole Centrale de Nantes, pour son aide qui m’a permis d’introduire les aspects d’homogénéisation multi-échelle et encouragé à entreprendre l’étude micromécanique
Je souhaiterais également exprimer ma gratitude à M. Serge Borel et M. Jean-François Mosser, respectivement Directeurs Technique et R&D à Soletanche Bachy, pour m’avoir fait confiance, encouragé et pour les réunions intéressantes que nous avons pu avoir.
iv
Mes remerciements vont aussi aux membres du GeM qui m’ont ouvert leurs portes et aidé pendant mes travaux, j’en cite MM. Jean-Pierre Regoin, Patrick Denain, Vincent Wisniewski, Yannick Benoît et François Bertrand. Leur disponibilité et bonne humeur a permis de me faciliter les différents essais que j’ai eu à faire.
Je remercie également les autres personnes qui m’ont aidé pendant ces essais, à savoir Elodie Coudert, pour tout la caractérisation physico-chimique, ainsi qu’Alexis Charpentier-Süter, Jules Gibert, Melchior De Bourayne et Oussama Keddache pour l’apport qu’ils ont fourni pendant leurs stages.
Je voudrais remercier mes collègues et anciens collègues, qui m’ont largement aidé d’une façon ou d’une autre pendant ces années : Thibault, Hamza, Gildas, Zakaria, Benoît, Georges, Mounia, Younes, Menghuan, Ahmed, Siyimane, Reda, Abderrahmane, leur souhaitant une bonne continuation dans leurs carrières.
A mes autres amis, je souhaite exprimer la chance que j’ai eue de les avoir autour de moi. Merci à Ilham, Leila, Ayoub, Mehdi et tous les autres que j’aurais pu oublier de citer pour votre présence, humour et soutien pendant cette période de ma vie.
Enfin, je ne peux passer sans remercier ma famille ici à Nantes et au Maroc, pour leur aide inconditionnelle, leurs encouragements et la motivation. Je n’aurais jamais pu atteindre cette marque sans leur support qui m’a fourni l’environnement et les conditions nécessaires pour mener à bien cette aventure.
v
TABLE DES MATIERES
I
NTRODUCTIONG
ENERALE__________________________________________________ 1
1
C
ARACTERISTIQUES PHYSICO-
CHIMIQUES DES REACTIFS ET PRODUITS__________ 5
1.1 BIBLIOGRAPHIE _______________________________________________________ 81.1.1 Mécanismes de réaction ______________________________________________ 8 1.1.2 Matières premières et intérêt écologique _________________________________ 14 1.2 PRINCIPES DE FORMULATION _____________________________________________ 18
1.2.1 Système d’équations ________________________________________________ 18 1.2.2 Limites de formulation ______________________________________________ 21 1.3 MATERIAUX ________________________________________________________ 22
1.3.1 Solution de silicate alcaline ___________________________________________ 22 1.3.2 Précurseurs ______________________________________________________ 23 1.3.3 Programme expérimental ____________________________________________ 24 1.3.4 Méthodes d’observation _____________________________________________ 26 1.4 RESULTATS DE LA CARACTERISATION PHYSICO-CHIMIQUE _________________________ 32 1.4.1 Constituants _____________________________________________________ 32 1.4.2 Produits_________________________________________________________ 36 1.5 CINETIQUE DE REACTION ET STABILITE VOLUMIQUE _____________________________ 44
1.5.1 Méthodologie _____________________________________________________ 44 1.5.2 Influence du précurseur sur la cinétique de réaction _________________________ 46 1.5.3 Stabilité volumique des géopolymères ___________________________________ 47 1.5.4 Influence du précurseur sur les modules élastiques __________________________ 48 1.6 BILAN ____________________________________________________________ 50
vi
2
F
ORMULATION ETR
HEOLOGIE__________________________________________ 59
2.1 COULIS D’INJECTION ET CAHIER DES CHARGES ________________________________ 592.2 BIBLIOGRAPHIE :LEVIERS POUR LA FORMULATION ______________________________ 61
2.2.1 Rhéologie et prise _________________________________________________ 61 2.2.2 Contrôle de la stabilité______________________________________________ 63 2.2.3 Résistance mécanique ______________________________________________ 63 2.2.4 Adjuvantation des géopolymères ______________________________________ 66 2.3 PROGRAMME EXPERIMENTAL ET METHODES __________________________________ 70
2.3.1 Programme expérimental ____________________________________________ 70 2.3.2 Essais relatifs au cahier des charges _____________________________________ 74 2.3.3 Caractérisation rhéologique __________________________________________ 75 2.4 RESULTATS ET DISCUSSION _____________________________________________ 76 2.4.1 Résultats préliminaires ______________________________________________ 76 2.4.2 Etude des coulis binaires ____________________________________________ 79 2.5 BILAN ____________________________________________________________ 88
RÉFÉRENCES _____________________________________________________________ 89
3
E
TUDEM
ICROMECANIQUE ETH
OMOGENEISATION_________________________ 97
3.1 MICROSTRUCTURE DES GEOPOLYMERES ET AAM :DONNEES BIBLIOGRAPHIQUES _________ 973.1.1 Particularités de la microstructure _____________________________________ 97 3.1.2 Effet de la porosité sur les propriétés mécaniques __________________________ 99 3.2 PREVISION DES PROPRIETES ELASTIQUES PAR HOMOGENEISATION MULTI-ECHELLES _______ 100
3.2.1 Principes de la méthode ____________________________________________ 100 3.2.2 Applications aux matériaux cimentaires _________________________________ 102 3.2.3 Quelques résultats sur les géopolymères ________________________________ 103 3.3 STRATEGIE ET METHODES ______________________________________________ 104
3.3.1 Stratégie et programme expérimental __________________________________ 104 3.3.2 Méthodes de caractérisation microstructurale ____________________________ 105 3.4 RESULTATS ET DISCUSSION _____________________________________________ 112 3.4.1 Répartition des phases dans la microstructure ____________________________ 112 3.4.2 Caractérisation micromécanique ______________________________________ 118 3.4.3 Modélisation analytique et numérique __________________________________ 122 3.5 BILAN ___________________________________________________________ 126
vii
4
S
ENSIBILITE AUS
ECHAGE ET A LAL
IXIVIATION___________________________ 131
4.1 BIBLIOGRAPHIE : DURABILITE DES GEOPOLYMERES ET AAM _______________________ 1314.1.1 Retrait _________________________________________________________ 132 4.1.2 Autres actions environnementales _____________________________________ 137 4.1.3 Lixiviation et attaques acides _________________________________________ 138 4.1.4 Dégradation endogène (RAG) ________________________________________ 141 4.2 PROGRAMME EXPERIMENTAL ____________________________________________ 142 4.2.1 Formulations ____________________________________________________ 142 4.2.2 Méthodes expérimentales ___________________________________________ 142 4.3 RETRAIT DE SECHAGE _________________________________________________ 144 4.4 LIXIVIATION ACIDE __________________________________________________ 150 4.5 BILAN ___________________________________________________________ 159 RÉFÉRENCES ____________________________________________________________ 160
C
ONCLUSION ETP
ERSPECTIVES____________________________________________ 167
1
I
NTRODUCTION
G
ENERALE
L’évolution du contexte environnemental mondial a poussé l’industrie de la construction à reconsidérer certaines des pratiques adoptées pour le choix des matériaux. Le marché du ciment Portland est montré du doigt depuis la conférence de Kyoto comme étant responsable de 5 à 6 % des émissions mondiales de gaz à effet de serre. Pour relever ces défis, plusieurs alternatives s’offrent aux différents acteurs : une rationalisation du dimensionnement, le recyclage des déchets de déconstruction, l’utilisation d’additions en quantités plus importantes, etc. Ces dernières années, une autre option en pleine expansion vise la substitution complète du ciment. En plus de la problématique environnementale, ces efforts s’inscrivent dans une dynamique de développement de matériaux plus adaptés aux différentes contraintes d’utilisation liées notamment à la durabilité.
La géopolymérisation et l’activation alcaline des aluminosilicates constituent une alternative possible pour répondre à ces enjeux techniques et environnementaux. Ceci passe par l’exploitation de coproduits d’autres industries (cendres volantes, laitier de hauts fourneaux, etc.) et de matériaux à faible impact environnemental (métakaolin, pouzzolanes). Malgré leur relatif jeune âge, l’implémentation de ces nouveaux matériaux se concrétise à présent autour du monde à travers des applications diverses et innovantes. Outre le béton et matériaux de construction, leurs propriétés les rendent adaptés à l’utilisation dans l’isolation thermique, l’aéronautique, la céramique, les revêtements, etc. Après des débuts discrets dans les années 70-80, la recherche autour des géopolymères et liants alcali-activés s’accélère de façon soutenue, amenant une meilleure connaissance des spécificités de leur fabrication et utilisation. Le nombre de thèses, articles et brevets atteste de l’intérêt croissant pour ces matériaux parmi les chercheurs ainsi que les industriels, ce qui permet de pronostiquer un marché prometteur pour les années à venir.
Au sein de ce marché, des applications telles que l’injection et le renforcement des sols n’ont pas encore été suffisamment explorées. La transposition de ces technologies dans le contexte des travaux géotechniques permettrait de répondre à des problématiques techniques et de réduire l’impact environnemental de cette industrie. Ce domaine technologique est aussi bien placé pour profiter des propriétés des géopolymères liées à la résistance en milieu agressif et/ou pollué. La grande variété de matériaux possibles, liée à des matières premières tout aussi variées, permet des degrés de liberté supplémentaires en fonction des conditions du terrain.
2
Les géopolymères et matériaux alcali-activés représentent donc une alternative à considérer dans le but, non pas de remplacer totalement le ciment, mais d’élargir les possibilités disponibles au moment de la prise de décision.
Cette thèse vise ainsi à améliorer la compréhension des mécanismes et particularités de la géopolymérisation et de l’activation alcaline, dans le cadre du développement de coulis d’injection. Or, malgré la présence d’une composante industrielle parmi les objectifs, le but principal demeure la participation à élargir ce nouveau domaine des connaissances. Par conséquent, l’approche adoptée est celle d’une étude rationnelle des différents points liés à cette application. La finalité n’est en effet pas simplement de définir des compositions optimales, mais plutôt d’établir une base scientifique permettant une meilleure prise en main de ces matériaux.
Cependant, au début de l’étude, nous avons recensé un certain nombre de verrous scientifiques et technologiques à lever afin de permettre le développement de coulis géopolymères ou alcali-activés. Cette classe de matériaux est en effet relativement nouvelle. Il manque donc des données, des études scientifiques et des méthodes rationnelles pour relier la formulation aux propriétés mécaniques, à la durabilité, etc. Ce manque est en partie dû à la multiplication de brevets, difficiles à exploiter dans un cadre scientifique et technique. En outre, l’originalité de l’application visée, à savoir la formulation de coulis fluides, réduit considérablement le domaine de données pertinentes. Il faut également adapter les formulations, basées sur l’activation alcaline, aux prérequis de sécurité pour le déploiement sur le terrain en éliminant les risques liés à l’utilisation de produits caustiques. Enfin, les normes relatives au béton ne prévoient pas l’application de ces matériaux et demeurent fortement centrées autour du ciment Portland.
Au cours de la thèse, l’utilisation de la géopolymérisation et de l’activation alcaline afin de produire des coulis pour les applications souterraines a été étudiée. Devant la multitude d’approches envisageables, le choix a été fait de travailler avec des matières premières courantes. Ceci a l’avantage de réduire le fossé entre l’étude réalisée en laboratoire et l’utilisation pratique avec ses contraintes technologiques et économiques. L’utilisation systématique de matières premières de premier choix n’est en effet pas réaliste d’un point de vue géographique. Les conséquences de ce choix expérimental sont évidentes : la formulation et la caractérisation doivent prendre en considération les limitations de ces matériaux en termes d’homogénéité et de réactivité.
Une grande importance a donc été réservée à la caractérisation des matières premières et à la compréhension de leur influence sur les mécanismes réactionnels et la structuration du matériau durci. Le premier chapitre de ce manuscrit se focalise sur ces aspects, en soulignant les principales différences entre la géopolymérisation et l’activation alcaline des systèmes calciques. Pour ce faire, différentes techniques (diffraction des rayons X, résonance magnétique
3
nucléaire, calorimétrie, mesure des propriétés élastiques par ultrasons) ont été utilisées de façon synergique pour décrire et expliquer les évolutions macroscopiques au jeune âge. Ensuite, les principaux résultats obtenus sur le chemin de la formulation d’un coulis alternatif optimal sont présentés. Dans ce deuxième chapitre, l’accent est mis non seulement sur la réponse à un cahier des charges qui fait preuve de satisfaction sur le plan industriel à partir des différentes matières premières, mais aussi sur la corrélation entre les grandeurs mesurées et les propriétés physico-chimiques des matières premières et des mélanges. Les propriétés rhéologique et mécanique sont traitées en lien avec l’utilisation de mélanges binaires de précurseurs.Le chapitre suivant détaille la méthodologie suivie afin d’établir des liens entre la microstructure et le comportement mécanique du matériau. Une utilisation couplée de différentes techniques y est mise en place afin de comprendre les particularités de la microstructure. Elle est constituée d’une analyse de la microstructure des matériaux par MEB et EDX avec détection des phases, d’une caractérisation par micro-indentation et de l’utilisation de la micro-tomographie aux rayons X. Le but est d’effectuer une homogénéisation multi-échelles permettant de remonter au module élastique macroscopique.
Le quatrième et dernier chapitre présente les principaux résultats obtenus lors de l’évaluation de la résistance des coulis formulés face aux sollicitations physico-chimiques. En se focalisant sur la dégradation par l’exposition au séchage et à la lixiviation acide, la performance de formulations choisies est comparée à un matériau cimentaire suivant différents indicateurs de performance. L’objectif est de définir les principaux mécanismes de dégradation présents et de permettre la désignation des compositions les plus adaptées en fonction des conditions d’utilisation.
5
1 C
ARACTERISTIQUES PHYSICO
-
CHIMIQUES
DES REACTIFS ET PRODUITS
Les géopolymères seraient l’une des technologies antiques perdues et « redécouvertes » récemment. Des études y voient la technique utilisée pour la fabrication des blocs constitutifs de monuments de l’antiquité dont les pyramides égyptiennes [1], [2]. Ces théories ont été – et sont toujours – débattues avec ferveur dans les milieux archéologiques [3].
Le premier à avoir émis cette hypothèse, le professeur français Joseph Davidovits, est également le premier à avoir mis en place le mot géopolymère, dans les années 1970. Il l’utilise pour distinguer une classe de matériaux fabriqués en utilisant une solution alcaline et une source aluminosilicate [4], [5]. Ils ont été développés comme une alternative aux polymères organiques classiques, afin de mieux résister au feu et éviter les dangers associés aux incendies et aux fumées toxiques. Cependant, les géopolymères ont vite suscité l’intérêt en tant que liants alternatifs au ciment pour les matériaux de construction. Au début, les géopolymères étaient trop coûteux pour une telle application, nécessitant des matériaux de choix et une procédure de fabrication soignée. Il y a eu un changement après les travaux de Wastiels et al. qui ont démontré la possibilité d’obtenir des matériaux performants à partir de l’activation alcaline des cendres volantes, un déchet des centrales thermiques [6]. Ceci a eu pour effet de donner un nouvel élan aux géopolymères, les rendant économiquement et écologiquement attractifs. Pendant une longue période, les connaissances globales sur les géopolymères ont progressé lentement. Et pour cause, la majorité des informations présentes étaient sous la forme de brevets [7]. Les premiers travaux fondateurs sur les géopolymères au métakaolin ont été publiés dans les années 90 [8]–[11]. Ces études ont permis d’établir une base de connaissances autour de la chimie des géopolymères et de leurs processus réactionnels. Par la suite, la recherche sur les géopolymères s’est localisée dans quelques pays : la Nouvelle Zélande [12], [13], l’Australie [14]–[16], l’Espagne [17]–[19] et la France [20]–[22].
L’activation alcaline d’aluminosilicates comme alternative au ciment Portland usuel pour fabriquer des matériaux de construction n’est néanmoins pas récente. Les études se fondant principalement sur les laitiers à forte teneur en calcium remontent jusqu’à 1940 avec le travail de Purdon [23]. L’utilisation de tels matériaux était répandue en ex-URSS, et certains ouvrages réalisés avec du laitier à activation alcaline existent encore de nos jours en Ukraine et Russie [24]. Cette utilisation fait principalement suite aux travaux de Glukhovsky qui a donné à cette famille de matériaux le nom de « soil-silicate cements » [25]. L’activation alcaline a depuis fait le sujet de plusieurs études [26]–[28] et suscite un grand intérêt car cette technologie ouvre la
6
porte à l’exploitation de produits secondaires silico-alumineux pour l’obtention de matériaux hautement résistants et durables à moindre coût.
Cependant, une différence chimique majeure permet de distinguer les géopolymères des laitiers alcali-activés. Ceux-ci sont principalement composés d’un gel de silicate de calcium hydraté (CSH) avec des atomes Si en chaînes 1D [29], [30], des substitutions du silicium par l’aluminium et une intégration du magnésium avec le calcium [31]. Les géopolymères sont un réseau tridimensionnel d’aluminosilicate alcalin, présentant un caractère de gel amorphe [32]. La limite entre les géopolymères et les matériaux alcali-activés (AAM) est encore difficile à déterminer, mais elle est principalement fondée sur le taux de calcium dans le mélange et le rôle qu’il y joue. Un critère usuel est de parler de liants à fort taux de calcium (et donc d’AAM) lorsque le rapport Ca/(Si+Al) est supérieur ou égal à 1 [33].
L’application industrielle de notre étude est le développement de solutions alternatives au ciment qui remplissent un cahier de charges prédéfini. Cette approche orientée objectif implique de ne pas écarter a priori l’une des options disponibles. Ainsi, bien que le focus principal soit le géopolymère comme défini par Davidovits, les matériaux alcali activés ont aussi été étudiés. Cette décision a été prise afin de pouvoir exploiter leurs propriétés très intéressantes et d’obtenir un degré de liberté supplémentaire pour concilier les objectifs de coût et de performances rhéologiques, mécaniques et la durabilité. Par conséquent, cette bibliographie couvre les différents mécanismes de formation des géopolymères, mais porte également de l’intérêt aux matériaux activés, et plus particulièrement au laitier alcali-activé.
L’un des plus grands défis du développement des géopolymères est celui de la nomenclature. Encore en 2015, la première conférence internationale sur les géopolymères a connu, lors de son ouverture par Davidovits un débat soutenu sur ce que l’on peut qualifier de « géopolymère ». Alors que le mot géopolymère est de plus en plus courant dans le milieu scientifique, il n’y a pas encore de consensus sur les limites de son utilisation. Celui-ci est réservé par les pionniers du domaine aux matériaux dont la phase liante est formée d’un réseau tridimensionnel tétraédrique d’aluminium et silicium, amorphe et stable dans l’eau [34]. Néanmoins, étant simple d’utilisation, ce terme est parfois utilisé par abus pour qualifier des matériaux ne remplissant pas ces conditions, notamment des AAM à base de laitier ou de cendres volantes calciques, qui contiennent des CSH comme phase principale. Cependant, les géopolymères ne sont qu’une petite classe au sein des AAM [28], qui englobent d’autres types de matériaux (à base de sulfates, carbonates, …) (Figure 1.1).
Tout au long de ce travail, l’appellation ‘géopolymère’ est utilisée pour désigner les résultats de l’activation alcaline du métakaolin et des cendres volantes. Les matériaux ‘alcali-activés’ ou ‘à activation alcaline’ (Alkali Activated Materials ou AAM) font principalement référence au cas du laitier, ou du laitier avec substitutions, quel que soit l’activateur utilisé.
7
Figure 1.1 : Classification des liants selon [35]
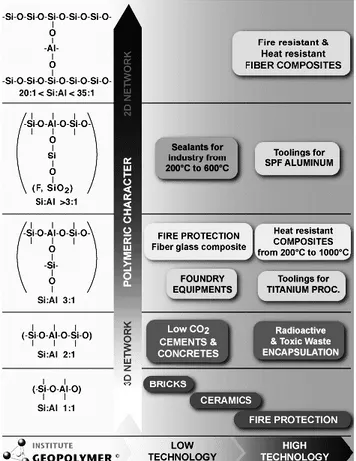
Davidovits a également proposé des termes spécifiques pour la description de la structure d’un réseau géopolymère : sialate (Si-O-Al), siloxo (Si-O-Si), … [4]. Ceci lui a permis de donner des dénominations aux différentes familles de réseaux, en fonction du rapport Si/Al : poly(sialate) [Si/Al =1], poly(sialate-siloxo) [Si/Al = 2], poly(sialate-disiloxo) [Si/Al = 3] et ainsi de suite. Il reprend cette même classification afin de spécifier des familles d’applications pour chaque type de réseau (Figure 1.2).
8
1.1 B
IBLIOGRAPHIE
1.1.1 Mécanismes de réaction
1.1.1.1 Géopolymérisation
Quand Davidovits a, pour la première fois, parlé de « géopolymère », le processus concerné était celui de l’activation du métakaolin par un hydroxyde alcalin et/ou silicate alcalin [5], [7], [36]. Ce processus a été étendu ensuite pour couvrir des matériaux produits à partir d’autres aluminosilicates comme les cendres volantes. Le géopolymère au métakaolin demeure en effet, jusqu’à aujourd’hui, un système modèle, permettant de comprendre les mécanismes de formation de ces matériaux, et de les transposer ensuite vers des aluminosilicates plus complexes.
L’utilisation du métakaolin pour former des matériaux aluminosilicates solides date de bien avant les « géopolymères ». Barrer et Mainwaring [37], [38] ont publié en 1972 une étude détaillée sur les « soil minerals », qui traite en partie de la transformation du métakaolin dans des milieux alcalins sous hautes températures. Ces processus forment différents types de zéolite, en fonction des conditions de la réaction. Un brevet pour la fabrication de zéolite à base de métakaolin et d’hydroxyde de sodium a même été déposé dès 1961 [39]. Mais, depuis l’étude de Palomo et Glasser [8], les travaux se sont intensifiés afin de mieux caractériser le déroulement de la géopolymérisation.
Provis et al. [40] ont résumé les étapes de la géopolymérisation comme suit :
1) Les aluminates et silicates du métakaolin sont libérés dans la solution, suite à l’attaque alcaline. L’aluminium de coordinence V et VI est alors converti en Al(IV) [41]. La dissolution de l’aluminium a lieu avant celle du silicium, ses liaisons étant les premières à être cassées [42]. Ceci est confirmé par la présence de particules de métakaolin résiduelles à plus faible teneur en aluminium [43].
2) Formation d’oligomères aluminosilicates à partir des espèces dissoutes et des silicates présentes dans la solution d’activation.
3) Lorsque la concentration en aluminates est suffisante pour déstabiliser la solution de silicates, un gel commence à se former par précipitation. En parallèle, la dissolution se poursuit, causant ainsi une concurrence entre les deux processus.
4) Au bout d’un certain temps, le mélange se solidifie suite à l’augmentation de concentration en gel. La durée de la prise dépend de la température, de la composition, ainsi que de la présence d’impuretés. Les réactions peuvent se poursuivre au-delà de la prise, avec un éventuel gain en résistance et le développement de cristaux de zéolite dans certains cas [44].
Le résultat de ce processus est ce que Davidovits appelle une structure géopolymère. Pour la décrire, il a utilisé des modèles basés sur les zéolites, qui dépendent du ratio Si/Al du mélange
9
et du type d’alcalin utilisé [5]. Rahier et al. [9]–[11] utilisent la terminologie des polymères en parlant de « verre polymère inorganique à basse température ». D’autres chercheurs ont parlé d’« hydrocéramiques » pour les géopolymères au métakaolin à hautes températures [45], [46]. Barbosa et al. [47] ont proposé un modèle (Figure 1.3(a)) basé sur celui de Davidovits (Figure 1.3(b)), qui situe l’eau et l’alcalin au sein du réseau. Ce modèle a été amélioré par Rowles et al. [48] grâce à des études RMN (Résonance Magnétique Nucléaire) du 29Si, de l’27Al, de l’1H et du 23Na, en essayant de détailler encore plus la position du sodium et son rôle dans le réseau.Figure 1.3 : (a) Structure semi-schématique d’un polysialate au sodium, proposée par Barbosa et al. [47], (b) Structure 3D basée sur un modèle de polysialate de Davidovits [49]
Malgré ces études, la nanostructure des géopolymères présente encore des zones d’ombre. Toutefois, certaines caractéristiques semblent désormais bien connues :
- La typologie de la structure locale est déterminée principalement par le ratio Si/Al et par la nature de l’alcalin utilisé [50].
(a)
10
- Le réseau géopolymère est équilibré électriquement : La charge des sites d’aluminium tétraédrique est équilibrée par le cation alcalin, associé à un ou plusieurs atomes d’oxygènes qui l’entourent.
- L’ordre local ressemble à celui des zéolites et autres minéraux aluminosilicates. Cependant, cet ordre n’est pas suffisamment étendu dans l’espace, en faisant un matériau globalement amorphe.
- Les atomes d’oxygènes présents dans le géopolymère sont généralement pontants, donnant lieu à un réseau complètement connecté. Ceci peut être altéré par un excès d’alcalin ou une cure insuffisante du géopolymère.
- L’une des plus grandes différences entre le géopolymère et les silicates de calcium hydratés, constituants principaux des matériaux cimentaires classiques, est que l’eau n’est pas liée à la matrice. Elle est en grande majorité présente dans les pores du matériau, vu la quasi absence d’hydroxyles liés. Ces pores varient du nanopore au macropore, et leur distribution dépend de la chimie du matériau ainsi que de ses conditions de mise en œuvre.
- L’aluminium est généralement entouré de 4 voisins silicium, cette caractéristique importante permet l’identification de réseaux géopolymère par RMN de l’27Al.
Ce qui a été dit ci-dessus est principalement fondé sur les études de la géopolymérisation du métakaolin. Plusieurs principes de la réaction et de la structure finale sont applicables aux cendres volantes. Cependant, vu la complexité de la matière première, les systèmes aux cendres ont leurs propres spécificités. Ainsi, les auteurs ont tendance à utiliser une description différente par rapport au métakaolin, se basant principalement sur la terminologie de la structure N-A-S-H. Cet acronyme renvoie à un aluminosilicate alcalin amorphe hydraté avec une unité de base sous la forme : (Mn-(SiO2)-(AlO2)n.wH2O) dont les tétraèdres de silicium et
d’aluminium sont distribués aléatoirement dans un squelette 3D (Figure 1.4). La réaction forme également des produits secondaires tels que l’hydroxysodalite, la zéolite P, la chabazite-Na, la zéolite Y et la faujasite [51]–[53].
Cette description du réseau d’aluminosilicate alcali-activé, appliquée aux matériaux à faible taux de calcium, n’est autre qu’une manifestation du débat en cours. L’appellation N-A-S-H, préférée par les chercheurs provenant du domaine des matériaux cimentaires, est clairement dérivée de celle des C-S-H, produits familiers pour le monde du génie civil. Les chimistes – tels que Davidovits, MacKenzie, Rahier et autres – préfèrent parler de géopolymères ou de polymères inorganiques, pour insister sur la polymérisation et ses mécanismes réactionnels. Là où les premiers parlent de nucléation et de précipitation, les derniers parlent d’oligomères et de polycondensation. Cette confusion complique parfois les discussions autour d’une seule et même structure [54], et il n’y a pour l’instant pas d’approche dominante.
11
Figure 1.4 : Structure du gel N-A-S-H (d’après [55])
1.1.1.2 Activation alcaline du laitier
Pour l’activation alcaline du laitier, il y a une sorte de consensus sur la terminologie utilisée pour la description du système et de ses produits. Etant donné que le laitier alcali-activé est utilisé en premier lieu comme un substitut des liants cimentaires classiques, une description issue du domaine du ciment s’est imposée au cours des études.
L’une des premières études détaillées sur l’activation alcaline du laitier a été réalisée par Purdon en 1940 [23]. Il y analyse l’utilisation d’hydroxydes et de carbonates alcalins pour activer un laitier de haut fourneau, avec différents taux d’activateur. Ensuite, Glukhovsky [25], [56] a étudié les mécanismes réactionnels qui ont lieu lors de l’activation alcaline du laitier. Ces étapes, reprises ensuite par Krivenko [57], consistent en une dissolution des particules vitreuses du précurseur, suivie d’une nucléation des phases solides initiales, puis d’interactions et liaisons mécaniques aux frontières de ces phases. Les réactions se poursuivent par diffusion des espèces réactives avec le temps, donnant lieu à un matériau évolutif [58]. Dans ce processus, le cation alcalin joue principalement le rôle d’un catalyseur, dont le rôle est d’accélérer une réaction d’hydratation qui nécessiterait une durée bien plus longue dans un système laitier + eau [59].
Au niveau des produits formés, il y a un accord sur la présence majoritaire d’un gel aluminosilicate de calcium hydraté, C-A-S-H [29], [30], [60]. Ce gel, de rapport C/S plus faible (0,9-1,2) [61], diffère cependant des C-S-H présents dans les liants Portland. L’alcalin, en plus de son rôle catalyseur, affecte les propriétés du gel formé et sa structure [62]. Les cations alcalins (Na ou K) sont intégrés au gel C-A-S-H lorsque leur concentration est suffisamment élevée et que le rapport Ca/Si est faible. Suite à la dissolution progressive des particules de laitier, le ratio Ca/Si peut être amené à augmenter. Par conséquent, les alcalins sont remplacés par le calcium et sont relâchés dans la solution interstitielle [63]. D’ailleurs, la lixiviation de ces alcalins est rapide, et leurs liaisons dans le système sont assez faibles, prouvant leur rôle
12
principal comme catalyseur de la réaction d’hydratation. Ainsi, on retrouve parfois la notation C-(N,K)-A-S-H, signifiant une substitution partielle du calcium par le sodium ou le potassium. Cette substitution est plus rare dans le laitier activé à la soude NaOH, comparé au laitier activé au silicate de sodium, où le rapport Ca/Si est plus faible à cause du silicium apporté par la solution d’activation. Le gel formé dans le laitier activé au silicate a été assimilé à des phases tobermorite par Puertas et al. [64]. Ce modèle a été ensuite développé par Myers et al. pour prendre en compte les contraintes des structures réticulées et non-réticulées d’unités assimilées à la tobermorite, permettant ainsi de mieux décrire le degré de réticulation et la longueur des chaînes de la structure [31]. Ce modèle, baptisé CSTM pour « Cross-linked Substituted Tobermorite Model » ou modèle réticulé substitué de tobermorite, permet de mieux agglomérer les différents résultats actuels sur la structure des laitiers alcali-activés au silicate de sodium.
Figure 1.5 : Illustration du modèle CSTM, incluant les hypothèses et contraintes prises en compte [31]
Le modèle CSTM prend également en compte la formation de produits secondaires dans le matériau. Ces produits résultent de l’abondance en aluminium et magnésium dans le laitier [65], [66]. Ces éléments ne pouvant être tous intégrés dans la structure du gel C-A-S-H, l’excédent forme deux principaux produits secondaires : des phases AFm (Alumino-Ferrite de calcium hydraté monosubstituée) et des phases hydrotalcite (hydroxydes double lamellaire de magnésium et d’aluminium de formule analogue à Mg6Al2CO3(OH)16·4(H2O)). Les phases AFm ne sont toutefois pas toujours détectables par diffraction des rayons X, car elles peuvent être intégrées à l’échelle du nanomètre à la structure C-A-S-H [67].
Les processus réactionnels des géopolymères (activation alcaline d’aluminosilicates à faible teneur en calcium) et des AAM (activation alcaline d’aluminosilicates calciques) sont bien résumés par Provis et Bernal dans la Figure 1.6 [33]. Et les différents produits de ces réactions sont rappelés dans le Tableau 1.1.
13
Figure 1.6 : Schéma des processus de géopolymérisation et d'activation alcaline (traduit de [33]) Tableau 1.1 : Produits des réactions d'activation alcaline et de géopolymérisation comparés au ciment [55]
Type du liant
Ciment Portland
Liant alcali activé
(Na,K)2O-CaO-Al2O3-SiO2-H2O (Na,K)2O-Al2O3-SiO2-H2O Pro du it de réact ion
Primaire C-S-H C-A-S-H N-A-S-H
Secondaire Ca(OH)2 AFm AFt Hydrotalcite C4AH13 CASH8 C4AcH11 C8Ac2H24 Zeolites : hydroxysodalite, zéolite P, chabazite Na, zéolite Y, faujasite
C = CaO, S = SiO2, A = Al2O3, N = Na2O, H = H2O, c = CO2
Dissolution d’une source
aluminosilicate solide la solution d’activation Espèces silicates dans
Réarrangement et échange des espèces dissoutes Nucléation du gel Solidification, durcissement et développement de résistance Hydroxydes
doubles lamellaires Gel C-A-S-H
Forte teneur en calcium (Magnésium moyen-élevé) (Magnésium faible) Pauvre en calcium Gel N-A-S-(H) Zéolites cristallisées
14
1.1.2 Matières premières et intérêt écologique
1.1.2.1 Hydroxydes alcalins
L’hydroxyde alcalin le plus souvent utilisé est l’hydroxyde de sodium (NaOH), alors que les hydroxydes de potassium, lithium, rubidium ou césium sont réservés à des applications particulières [68]. Ces hydroxydes, lorsqu’ils sont utilisés pour l’activation alcaline des cendres volantes ou du laitier, conduisent à des problèmes d’efflorescence. En effet, la réaction est stoppée par le durcissement rapide du matériau. Il en résulte une microstructure poreuse où la solution interstitielle est alcaline et très mobile [69]. En outre, pour l’activation d’aluminosilicates, et notamment ceux à faibles teneurs en calcium, les concentration et quantité d’hydroxyde de sodium peuvent être élevées, et nécessitent souvent une cure thermique (à 60°C usuellement). Ceci induit des risques à la production en masse vu la corrosivité des solutions concentrées de soude et limite leur emploi à des unités de préfabrication où l’environnement est plus facilement contrôlable [21]. Néanmoins, les solutions de NaOH ont l’avantage d’être plus fluides et ainsi de produire des matériaux plus maniables, comparées aux solutions de silicate.
Les hydroxydes alcalins sont majoritairement obtenus par un traitement électrolytique de sels chlorures. Cette méthode n’est pas sans impact sur l’environnement du fait de la consommation d’énergie et de la production de déchets de mercure [70], et d’autres polluants [71]. Cependant, vu que le procédé chlore-alcali produit également du dichlore (Cl2), un calcul d’allocation d’impact environnemental est à prendre en compte [72].
1.1.2.2 Silicates alcalins
Les silicates alcalins les plus utilisés sont, comme pour les hydroxydes, à base de sodium et moins fréquemment de potassium. Ils sont produits à partir de sels carbonates et de silice (sable), qui sont fondus à haute température avant d’être dissous à haute pression dans de l’eau, formant ainsi une solution visqueuse appelée également verre liquide. C’est à ce moment qu’est fixé le rapport molaire SiO2:M2O (module de la solution, avec M=Na, K, etc. ), ainsi que la concentration. En fonction de ces deux paramètres, la chimie de la solution va varier. Un module faible implique l’augmentation d’espèces monomères Q0 [Si(OH)4], qui sont les plus réactives. Cependant, en dessous d’un certain seuil (~ 1,7), la solution est instable et y a lieu une précipitation des éléments dissous. La présence d’oligomères (chaînes de plusieurs atomes Si) cause une diminution de la réactivité, ainsi qu’une augmentation de la viscosité, vu la taille plus importante des molécules [73].
Le type de cation affecte également les propriétés de la solution. En effet, les silicates de potassium sont sensiblement plus fluides que les silicates de sodium, parce que les atomes de sodium mobilisent plus de molécules d’eau pour leur hydratation que les atomes de potassium. L’eau est ainsi beaucoup moins mobile d’où une augmentation importante de la viscosité. La
15
même logique est respectée pour le mélange avec le précurseur, où les silicates dissous vont augmenter le module du produit et, de ce fait, sa viscosité.La production des silicates par la méthode mentionnée ci-dessus (dite au four) n’est pas sans impact sur l’environnement. La décarbonatation des sels carbonates utilisés ainsi que l’énergie nécessaire pour leur fusion sont des sources non négligeables d’émissions de CO2 (suivant l’équation Na2CO3 + xSiO2 xSiO2 : Na2O + CO2) et d’autres gaz à effet de serre, dont une quantification a été réalisée par Fawer et al. [74]. Par exemple, la production d’une tonne d’une solution typique de silicate de sodium (concentrée à 37%) consomme 4623 MJ et émet 424 kg de dioxyde de carbone. D’autres déchets nuisibles sont également rejetés dans l’eau, dont des chlorures et autres sels et acides.
1.1.2.3 Métakaolin
Le métakaolin est le produit de la calcination de la kaolinite, une argile naturelle, à une température autour de 700°C [75], [76]. Celle-ci dépend de la pureté du kaolin et du degré de cristallisation de la kaolinite. A ces températures, la kaolinite se déshydroxyle et se transforme en une phase amorphe et très réactive en milieux basiques [77], [78]. Ceci en a fait, en plus de son rôle comme précurseur de choix pour les géopolymères [5], [8], [47] une addition qui suscite de plus en plus d’intérêt pour les matériaux cimentaires [79]–[81]. La procédure de fabrication classique en usine du métakaolin passe par un broyage du kaolin, une calcination en four rotatif pendant quelques heures, avant une dernière étape de broyage du produit calciné.
Récemment, le procédé de calcination flash a été adapté pour la production du métakaolin et breveté par l’entreprise Demeter Technologies [82]. Il permet la calcination très rapide (quelques secondes) du kaolin, tout en éliminant la nécessité d’une étape de broyage à la fin. San Nicolas et al. ont montré que le métakaolin produit par calcination flash ne comporte aucune différence aux niveaux chimique et minéralogique par rapport au métakaolin obtenu par la méthode classique (four rotatif) [83]. Il permet en plus d’améliorer l’ouvrabilité des mélanges produits car il contient plus de particules sphériques et une surface spécifique plus faible. Le métakaolin reste pourtant une addition à surface spécifique élevée et dont les performances dépendent largement de la pureté du kaolin originel [79].
La calcination flash du métakaolin présente également un intérêt économique et écologique. Comparé au ciment, le métakaolin flash permet une consommation d’énergie 4 fois inférieure au ciment CEM I et 10 fois moins d’émissions de CO2 [84]. Ceci est dû à l’absence de réactions de décarbonatation (si le kaolin brut ne contient pas de calcaire) et à la température de réaction plus faible (700°C au lieu de 1450°C pour la production du clinker).
16
1.1.2.4 Cendres volantes
Les cendres volantes proviennent de la combustion du charbon dans les centrales thermiques pour la production de l’électricité. A la suite de cette combustion, les gouttelettes d’aluminosilicates fondues refroidissent rapidement et forment des phases amorphes ou, si le refroidissement n’est pas rapide, semi-cristallines, et notamment de la mullite (3Al2O3,2SiO2) [85]. La morphologie et granulométrie des particules dépend des conditions de refroidissement et de récupération des cendres, alors que la chimie dépend principalement du charbon et des impuretés qu’il contient. Ainsi, on peut y retrouver des oxydes de fer, de titane, de soufre, d’alcalins ou de calcium. Cette teneur en chaux est justement utilisée pour classifier les cendres en cendres calciques et siliceuses/silico-alumineuses, selon la norme NF EN 197-1.
Ces cendres volantes silico-alumineuses sont composées de phases siliceuses et alumineuses en partie amorphes qui génèrent, dans un milieu basique comme celui du ciment, une réaction pouzzolanique. Ceci permet d’augmenter la résistance du béton et d’améliorer sa durabilité, notamment en affinant la porosité du matériau [86]–[89]. Dans les géopolymères à base de cendres volantes, le résultat dépend largement de la provenance et des caractéristiques chimiques et physiques des cendres [90]. En effet, l’évaluation de la quantité réactive dans le matériau n’est pas facile et nécessite l’emploi de plusieurs techniques [91]. Il existe toutefois un consensus, comme pour le métakaolin, de ne pas comptabiliser les phases cristallines (comme le quartz, la mullite, etc.) vu leur stabilité dans ce type de milieux [92].
Les cendres calciques pouvant être hydratées grâce à leur teneur en chaux, elles sont assimilées au laitier dans leur processus d’activation alcaline et sont utilisées également en substitution partielle du clinker dans les ciments recomposés. En France, les cendres volantes produites encore aujourd’hui sont du type silico-alumineux (type F fly ash) [93]. Ces cendres, dont une grande quantité provient de décharges temporaires, sont valorisées principalement dans le domaine du béton et de la restauration des mines [94]. Un grand potentiel existe en effet pour la réintégration de cette matière abondante, peu chère et qui confère plusieurs propriétés intéressantes au géopolymère : gain de résistance dans le temps [95], [96], ouvrabilité [97], [98] et durabilité [19], [99].
1.1.2.5 Laitier de haut fourneau
Le laitier de haut fourneau est un coproduit du traitement du minerai de fer pour l’obtention de la fonte. A l’issue d’un refroidissement rapide, le matériau aluminosilicate formé, très riche en calcium, présente des phases peu cristallisées sous une forme de verre dépolymérisé [100]. Ce résidu solide est alors broyé afin de produire une poudre fine, très réactive, et dont les caractéristiques et la composition varient en fonction du minerai de base et du type de traitement. Les facteurs clés influençant la performance du laitier sont sa granulométrie, sa teneur en calcium par rapport au silicium, ainsi que les cations tels que Mg2+ et Fe2+.
17
Le laitier de haut fourneau est le précurseur de référence pour l’activation alcaline dans des systèmes riches en calcium. Cependant, ce matériau est en forte demande pour l’utilisation dans les ciments recomposés, où le taux de substitution du ciment Portland peut atteindre jusqu’à 95% (NF EN 197-1). L’utilisation du laitier dans ce type de contexte s’approche de son activation alcaline, dans la mesure où le ciment fournit au laitier un milieu suffisamment basique pour accélérer son processus d’hydratation et la formation de gels C-S-H/C-A-S-H [101]. Ce type de ciments permet de viser de très bonnes résistances mécaniques en plus d’une durabilité élevée face aux attaques acides et sulfatiques [102], [103]. En activation alcaline, le laitier a été largement étudié et utilisé depuis les travaux de Purdon [23] et jusqu’aux études plus récentes [29], [30], [69], [104], [105].1.1.2.6 Intérêt écologique des géopolymères et AAM
L’un des avantages majeurs de l’utilisation des géopolymères et des AAM serait la réduction de l’impact environnemental des produits. Davidovits [106] indiquait une réduction pouvant atteindre 80 à 90 % pour les émissions de CO2 et une baisse conséquente de la facture énergétique. Le ciment constitue environ 5% de l’ensemble des émissions anthropogéniques de dioxyde de carbone [107]. Par conséquent, ces matériaux suscitent beaucoup d’intérêt en tant qu’alternatives envisageables. Cependant, l’évaluation de l’impact écologique des géopolymères s’avère plus compliquée. Celle-ci dépend de plusieurs facteurs dont la disponibilité des matières premières, leur traitement, la quantité de liant pour une résistance équivalente, etc. En ce qui concerne les émissions de CO2, il apparaît que les matériaux à activation alcaline ont en effet un impact généralement inférieur au ciment Portland, mais les gains ne sont pas aussi importants que ce qui est souvent annoncé. Une exception est celle des « one-part binders », qui se composent d’un mélange de laitier et de cendres volantes mélangés à un activateur sec à base de carbonate, hydroxyde et d’albite thermo-activée [108], [109]. Cette innovation, brevetée par Zeobond®, permet la fabrication d’un liant auquel seul l’ajout d’eau est nécessaire. L’impact lié aux silicates ou autres activateurs polluants est éliminé et conduit à une réduction des émissions carbone allant de 71 % à 93 % par rapport à un ciment équivalent, comme l’indiquent les calculs effectués par Ouellet-Plamondon et Habert [110].
Par ailleurs, Habert et al. [22] ont souligné les limites d’une analyse basée uniquement sur les émissions carbone. D’autres catégories d’impact (10 au total) sont prises en compte dans une analyse de cycle de vie. Ainsi, même si les géopolymères étudiés ont bien un potentiel de réchauffement global inférieur au ciment, ils ont un effet particulièrement négatif du côté d’autres facteurs comme l’épuisement des ressources non renouvelables, l’acidification ou l’écotoxicité marine. Ces effets sont attribués principalement aux silicates alcalins et leur analyse signale la nécessité d’améliorer les méthodes de formulation pour rendre les géopolymères écologiquement plus intéressants. L’étude de Weil et al. [111], moins exhaustive, offre des conclusions similaires. Un autre facteur non négligeable, lié au transport des matières
18
premières, a été étudié par McLellan et al. [112]. Ils concluent sur une grande variabilité de l’impact environnemental et du coût, en fonction de la proximité des différents fournisseurs. A la lumière de ces données, il ne se dégage pas une conclusion générale sur l’intérêt écologique des géopolymères. Les gains sont à évaluer au cas par cas, en fonction des différents paramètres géographiques, économiques et réglementaires liés à l’application envisagée. Il y a également un choix à faire au niveau des indicateurs à étudier, afin d’effectuer une analyse de cycle de vie qui soit complète et pertinente.
1.2 P
RINCIPES DE FORMULATION
1.2.1 Système d’équations
L’étape de formulation des géopolymères nécessite des choix sur les critères à remplir. Si la formulation des matériaux cimentaires est fondée sur des matières premières normalisées (types de ciments, coefficients d’activité des additions, etc.), des paramètres bien définis (E/C, volume de pâte) et des principes techniques et empiriques bien établis. Ce n’est pas encore le cas pour les géopolymères. En effet, on ne dispose pas encore des outils nécessaires pour procéder de la sorte. Il n’est pas envisageable de définir des relations – théoriques ou empiriques – entre les propriétés du matériau final et sa composition. Ceci est dû à plusieurs facteurs :
- La variété des matières premières : Comme détaillé précédemment, les géopolymères peuvent être obtenus à partir de différents types de matières premières. Les carrières du kaolin, les modes de calcination et les différentes centrales thermiques contribuent à faire varier la pureté, la composition et la réactivité de la source aluminosilicate. Une méthode de formulation exhaustive devrait donc englober toutes ces nuances.
- La variété des procédés de fabrication : Pour une source aluminosilicate donnée, les méthodes de préparation d’un géopolymère peuvent être variées. Solution alcaline au silicate de sodium/potassium, utilisation de la soude/potasse, ordre d’introduction des composants, cure thermique, etc. Cette diversité de choix, induite par la diversité des applications, conditionne les résultats obtenus au niveau du géopolymère.
- L’insuffisance des études effectuées : La jeunesse des géopolymères, relativement aux matériaux cimentaires, fait que les recherches n’ont pas fourni suffisamment de données pour faire ressortir des liens entre les paramètres de formulation et les propriétés rhéologiques, mécaniques, ou microstructurales des géopolymères. Des années de travail sont encore nécessaires afin de pouvoir agglomérer tous les résultats et fournir des conclusions pratiques.
Néanmoins, afin de mieux classer les géopolymères confectionnés, il faudra parvenir à les distinguer sur la base de critères bien définis liés à la formulation. Deux courants se distinguent : l’utilisation des rapports massiques ou volumiques (activateur/aluminosilicate,
19
eau/solide, soude/silicate, etc.) ou de rapports atomiques/moléculaires (Si/Al, SiO2/Al2O3, Al/Na, H2O/Na2O, etc.). Le premier choix est limité par la variabilité des matières premières, le deuxième par la difficulté de caractériser avec précision les compositions atomiques réelles de ces matières premières. Dans notre étude, le deuxième choix a été retenu, sur la base de la connaissance des analyses chimiques des matières premières. Ceci a conduit à la définition d’équations basées sur les rapports molaires des éléments chimiques (Équation 1) :𝑋 𝑌
⁄ =
𝑛(𝑋)
𝑛(𝑌)
=
𝑚(𝑋)
𝑀(𝑋)
𝑚(𝑌)
𝑀(𝑌)
Équation 1 : exemple de calcul du rapport molaire
X et Y étant les éléments choisis, n(X) et n(Y) leurs quantités de matière respectives dans le mélange, m(X), m(Y) leurs masses et M(X) et M(Y) leurs masses molaires.
Ainsi, on obtient :
𝑆𝑖 𝐴𝑙
⁄
=
𝑛(𝑆𝑖𝑂
2)
2. 𝑛(𝐴𝑙
2𝑂
3)
=
𝛼
𝑆𝑖𝑂2×𝑚
𝑠𝑜𝑢𝑟𝑐𝑒𝑀(𝑆𝑖𝑂
2)
+
𝑅𝑀×𝑆
𝑠𝑖𝑙×𝑚
𝑠𝑖𝑙×𝑀(𝑆𝑖𝑂
2)
[𝑅𝑀×𝑀(𝑆𝑖𝑂
2) + 𝑀(𝑀𝑒
2𝑂)]
2
𝛼
𝐴𝑙2𝑂3×𝑚
𝑠𝑜𝑢𝑟𝑐𝑒𝑀(𝐴𝑙
2𝑂
3)
Équation 2 : calcul du rapport Si/Al
𝐴𝑙 𝑀𝑒
⁄
=
2. 𝑛(𝐴𝑙
2𝑂
3)
𝑛(𝑀𝑒𝑂𝐻) + 2. 𝑛(𝑀𝑒
2𝑂)
=
2
𝛼
𝐴𝑙2𝑂3×𝑚
𝑠𝑜𝑢𝑟𝑐𝑒𝑀(𝐴𝑙
2𝑂
3)
𝑚
𝐻×(1 − (1 −
𝐶
𝜌
𝐻 𝐻)×𝛿
𝐻)
𝑀(𝑀𝑒𝑂𝐻)
+
2×𝑆
𝑠𝑖𝑙×𝑚
𝑠𝑖𝑙[𝑅𝑀×𝑀(𝑆𝑖𝑂
2) + 𝑀(𝑀𝑒
2𝑂)]
20
𝐻
2𝑂 𝑀𝑒
⁄
2𝑂
=
𝑛(𝐻
2𝑂)
𝑛(𝑀𝑒𝑂𝐻)
2
+ 𝑛(𝑀𝑒
2𝑂)
=
𝑚
𝑒+ (1 − 𝑆
𝑠𝑖𝑙)×𝑚
𝑠𝑖𝑙+ 𝛿
𝐻× (1 −
𝐶
𝜌
𝐻 𝐻) ×𝑚
𝐻𝑀(𝐻
2𝑂)
𝑚
𝐻×(1 − (1 −
𝐶
𝜌
𝐻 𝐻)×𝛿
𝐻)
2×𝑀(𝑀𝑒𝑂𝐻)
+
𝑆
𝑠𝑖𝑙×𝑚
𝑠𝑖𝑙[𝑅𝑀×𝑀(𝑆𝑖𝑂
2) + 𝑀(𝑀𝑒
2𝑂)]
Équation 4 : calcul du rapport H2O/Me2O
Avec :
𝑚𝑋 : masse du composant X (g)
𝑆𝑠𝑖𝑙 : masse sèche de silicate (%)
𝜌𝑋 : densité du composant X
𝐶𝑋 : concentration molaire de la solution X
𝛼𝑋 : pourcentage de la molécule X dans la source aluminosilicate (%)
𝑅𝑀 : ratio molaire SiO2:Me2O 𝑀𝑒 : Sodium (Na) ou Potassium (K)
𝐻 : (en indice) hydroxyde de sodium (Na) ou potassium (K) 𝑒 : (en indice) eau ajoutée
𝛿𝐻 : variable booléenne, valant 1 si l’hydroxyde est utilisé sous forme de solution, 0 sinon
Ces trois équations, rajoutées à l’équation de compatibilité des volumes, nous donnent le système suivant, avec comme inconnues les masses des 4 constituants de base :
{
𝑚
𝑠𝑜𝑢𝑟𝑐𝑒𝜌
𝑠𝑜𝑢𝑟𝑐𝑒+
𝑚
𝑠𝑖𝑙𝜌
𝑠𝑖𝑙+
𝑚
𝐻𝜌
𝐻+
𝑚
𝑒𝜌
𝑒= 1000
________________________________________
𝑆𝑖 𝐴𝑙
⁄
= 𝑥
________________________________________
𝐴𝑙 𝑀𝑒
⁄
= 𝑦
_________________________________________
𝐻
2𝑂 𝑀𝑒
⁄
2𝑂
= 𝑧
La résolution de ce système permet la définition d’une solution unique en fixant les scalaires (x,y,z). La définition des rapports Si/Al et Al/Me définit principalement les composants actifs du mélange. La partie solide du matériau se retrouve donc intégralement définie par ses deux ratios. Le troisième, H2O/Me2O, définit la concentration du mélange. Il est directement lié à la
21
quantité d’eau ajoutée qui, nous devons le rappeler, n’est pas un réactif de la géopolymérisation. Ce rapport est donc déterminé par l’application visée et pourrait être lié à un autre rapport, Eau/Solide, qui peut être apparenté au rapport E/C dans les matériaux cimentaires. Il n’a toutefois pas les mêmes implications que celui-ci. Son calcul se présente comme suit :𝐸𝑎𝑢 𝑆𝑜𝑙𝑖𝑑𝑒
⁄
=
𝑚
𝑒+ (1 − 𝑆
𝑠𝑖𝑙)×𝑚
𝑠𝑖𝑙+ 𝛿
𝐻× (1 −
𝐶
𝜌
𝐻 𝐻) ×𝑚
𝐻𝑚
𝑠𝑜𝑢𝑟𝑐𝑒+ 𝑆
𝑠𝑖𝑙×𝑚
𝑠𝑖𝑙+ 𝑚
𝐻×(1 − (1 −
𝐶
𝜌
𝐻 𝐻)×𝛿
𝐻)
Équation 5 : Calcul du rapport massique Eau/Solide (E/S)
Il est bien visible d’après l’équation 5 que le rapport Eau/Solide est défini entre l’eau totale du mélange (y compris celle provenant des silicates ou éventuellement de la soude) et la fraction solide restante. A l’instar du rapport E/C, le rapport massique Eau/Solide (ci-après noté E/S) est un paramètre primordial qui conditionne les propriétés du matériau aux états frais et durci, malgré la non implication de l’eau dans les réactions chimiques.
1.2.2 Limites de formulation
Soit une formulation définie par les données suivantes :
Si
Al
=x,
Al
Me
=1
,
E
S
=z,
comme définis plus haut.Une façon de résoudre le système est d’écrire toutes les masses en fonction de la masse de la source aluminosilicate. Celle-ci étant fixée en premier, les ratios définis nous permettent d’en déduire les masses des autres composants. La masse de silicate à utiliser est définie par une équation de la forme :
𝑚
𝑠𝑖𝑙= (𝑥 −
𝑆𝑖
𝐴𝑙
𝑠𝑜𝑢𝑟𝑐𝑒)×𝑓(𝑅𝑀, 𝑆
𝑠𝑖𝑙, 𝛼
𝐴𝑙2𝑂3)×𝑚
𝑠𝑜𝑢𝑟𝑐𝑒Équation 6 : Limite sur le rapport Si/Al
De cette équation, ressort une limite sur le rapport Si/Al. En effet, sauf à rajouter des aluminates dans le mélange, il existe une limite basse sur ce ratio, qui est celui de la source aluminosilicate. Dans le cas du métakaolin pur par exemple, de formule chimique Al2O3(SiO2)2, nous avons un rapport molaire minimal Si/Al égal à 1. Par contre, il n’existe aucune limite haute théorique à ce rapport. Ici, f, fonction du ratio molaire et masse sèche du silicate, ainsi que de la quantité d’aluminium dans la source, définit la quantité à rajouter. Plus la solution silicatée est diluée, plus il faudra augmenter sa quantité pour atteindre le ratio x.
La solution de silicate alcalin nous a donc permis de fixer le rapport Si/Al. Elle introduit par la même occasion, dans le mélange, les oxydes alcalins et l’eau. L’alcalin introduit, nécessaire
22
comme exposé plus haut pour équilibrer les charges acquises par l’aluminium, est parfois insuffisant, et doit être suppléé par des hydroxydes alcalins. Le ratio Al/Me est donc, en général, fixé à 1 pour notre famille d’applications, et il n’y a pas de grand intérêt à le faire varier [41]. A ce stade de la formulation, les masses de la source aluminosilicate, du silicate alcalin et – éventuellement – de l’hydroxyde alcalin ont été fixées. Ceci conduit le mélange à contenir par défaut une certaine quantité d’eau. Afin d’atteindre le rapport E/S désiré, il faut éventuellement ajouter une masse d’eau
m
e donnée par l’Équation 7 :𝑚
𝑒= (𝑧 −
𝐸
𝑆
𝑠𝑜𝑢𝑟𝑐𝑒+𝑠𝑖𝑙+ℎ𝑦𝑑)×𝑚
𝑠𝑜𝑙𝑖𝑑𝑒𝑠Équation 7 : limite sur le rapport E/S
D’après l’équation, on voit que le rapport E/S ne peut passer en deçà du rapport E/S induit par l’eau des silicates. Afin d’étendre le domaine de formulation, il convient donc d’utiliser des solutions de silicate alcalin relativement concentrées. Pour un contrôle absolu de tous les paramètres, il est également possible d’opter pour du silicate soluble et d’utiliser des additions d’aluminates. La Figure 1.7 illustre un exemple de limitation qui existe pour le domaine de formulation d’un coulis au métakaolin avec un silicate de sodium classique.
Figure 1.7 : Exemple de limites de formulation pour un coulis au métakaolin et silicate ordinaire avec un rapport Al/Na=1
1.3 M
ATERIAUX
1.3.1 Solution de silicate alcaline
La solution alcaline utilisée dans notre étude est composée d’un silicate de sodium en solution, ajusté par de l’hydroxyde de sodium en pastilles et de l’eau déminéralisée. La solution de silicate de sodium est fournie par WOELLNER® et fait partie de leur gamme GEOSIL®,




![Figure 2.6 : Effet des sels Ca et Mg sur le temps de prise de formulations géopolymères (Lee et van Deventer [91])](https://thumb-eu.123doks.com/thumbv2/123doknet/7963598.266820/79.892.274.663.201.506/figure-effet-sels-temps-prise-formulations-géopolymères-deventer.webp)
![Figure 2.8 : Viscosimètre proposé par Marsh [103] et méthode d'évaluation de la ressuée](https://thumb-eu.123doks.com/thumbv2/123doknet/7963598.266820/85.892.227.723.84.444/figure-viscosimètre-proposé-marsh-méthode-évaluation-ressuée.webp)