Évolution des ressources et des coûts directs à la suite
d'un infarctus du myocarde au Québec – Une étude
longitudinale de 1992 à 2018
Mémoire
Tania Villeneuve
Maîtrise en épidémiologie - avec mémoire
Maître ès sciences (M. Sc.)
Québec, Canada
Évolution des ressources et des coûts directs à la suite d'un
infarctus du myocarde au Québec – Une étude longitudinale de
1992 à 2018
Mémoire
Maîtrise en épidémiologie
Maître ès sciences (M.Sc.)
Tania Villeneuve
Sous la direction de :
Jason Robert Guertin, directeur de recherche
Xavier Trudel, codirecteur de recherche
ii
Résumé
Problématique : Les maladies cardiovasculaires constituent la deuxième source du fardeau économique
des soins de santé au Canada. Selon une étude réalisée en Alberta, les coûts d’hospitalisation pour un infarctus du myocarde (IM) seraient en diminution. Par ailleurs, au Québec, on en sait peu sur les coûts reliés aux IM et leur évolution, à travers le temps.
Objectifs : Cette étude estime les coûts directs d’une première hospitalisation pour un IM, dans le contexte
québécois. L’objectif secondaire analysera l’évolution des différentes catégories de coûts (séjours hospitaliers, réclamations médicales et services d’urgence), entre 1992 et 2018.
Méthodologie : Le devis utilisé est une analyse de coûts longitudinale de 26 ans, basée sur une cohorte
québécoise. Les bases de données médico-administratives québécoises (RAMQ et MED-ECHO) ont été utilisées afin de retrouver les cas incidents d’IM, à l’aide des codes diagnostiques issus de la classification internationale des maladies (CIM-9 et CIM-10). Tous les coûts ont été convertis en dollar canadien de 2018. Les intervalles de confiance (IC) des moyennes de coûts ont été estimés par bootstrap non paramétrique. Les tendances temporelles des coûts ont été examinées grâce aux régressions linéaires généralisées.
Résultats : L’échantillon est composé de 310 patients hospitalisés pour un premier IM. L’âge médian des
patients est de 59 ans et 17% sont des femmes. Le coût moyen des 310 hospitalisations est de 9 073$ [IC 95% 8 246$-10 027$]. On observe une diminution du coût de l’hospitalisation entre 1992 et 2018 (11 456$ vs 8 487$, valeur p=0.0123). D’importantes variations par catégorie de coûts sont observées, notamment une diminution de 49% des frais de séjours hospitaliers.
Conclusion : Les résultats indiquent une baisse de 35% du coût des hospitalisations sur la période
observée. De futures études pourront explorer les fluctuations de pratique clinique et leurs impacts économiques.
iii
Abstract
Background: Cardiovascular disease is the second-largest source of economic burden of healthcare in
Canada. According to an Alberta study, hospital costs for myocardial infarction (MI) are decreasing. Unfortunately, in Quebec, little is known about the costs associated with MI and their evolution over time.
Objectives: The main objective of this study is to estimate the direct costs of first hospitalization for MI in
the Quebec context. The secondary objective will analyze the evolution of different cost categories (hospital stays, practitioner claims and emergency services), between 1992 and 2018.
Methodology: The study design used is a 26-year longitudinal cost analysis, based on a Quebec cohort.
Quebec medico-administrative databases (RAMQ and MED-ECHO) were used to find incident MI cases using diagnostic codes, from the international classification of diseases (ICD-9 and ICD-10). All costs were converted to 2018 Canadian dollars. The confidence intervals (CI) of cost averages were estimated by nonparametric bootstraps. Temporal trends cost were examined using generalized linear regressions.
Results: The sample consisted of 310 patients hospitalized for a first MI. The median age of the patients
was 59 years, and 17% were women. The average hospitalization cost of the 310 cases was $ 9,073 [95% CI $ 8246-$ 10,027]. There was a decrease in the hospitalization cost between 1992 and 2018 ($ 11,456 vs $ 8,487, p value=0.0123). Significant variations in cost categories are observed, including a 49% decrease in hospital stay costs. Conversely, the practitioner claims cost increased by 746% between 1992 and 2018 ($ 320 vs $ 2,709, p value = <0.001).
Conclusion: Our results indicate a drop of 35% in hospitalizations cost over the period observed. Large
variations are observed within the different cost categories. To measure the economic impact, future studies should consider clinical practice fluctuations before combining the available data.
iv
Tables des matières
ÉVOLUTION DES RESSOURCES ET DES COÛTS DIRECTS À LA SUITE D'UN INFARCTUS DU MYOCARDE AU
QUÉBEC –UNE ÉTUDE LONGITUDINALE DE 1992 À 2018 ... 1
RÉSUMÉ ... II ABSTRACT ... III TABLES DES MATIÈRES ... IV LISTE DES TABLEAUX ... VI LISTE DES FORMULES ... VII LISTE DES FIGURES ... VIII LISTE DES ABRÉVIATIONS, SIGLES, ACRONYMES... IX REMERCIEMENTS ... X AVANT-PROPOS ... XI INTRODUCTION ... 1
Problématique ... 1
I.RECENSION DES ÉCRITS ... 3
1.1 L’infarctus du myocarde ... 3
1.1.1 Physiopathologie ... 3
1.1.2 Profil épidémiologique ... 4
1.1.3 Facteurs de risques ... 5
1.1.3.1 Facteurs modifiables ... 5
1.1.3.1.1 Évolution des facteurs de risque modifiables ... 7
1.1.3.2 Facteurs non modifiables ... 8
1.2 Économie en santé ... 8 1.2.1 Mise en contexte ... 8 1.2.2 Évaluation économique ... 9 1.2.3 Étude de coûts ... 11 1.2.3.1 Horizon temporel ... 13 1.2.3.2 Perspectives ... 13 1.2.3.3 Type de coûts ... 15
1.2.3.4 Contexte temporel des coûts ... 15
1.3. Aspects économiques de l’IM... 16
1.3.1 Interventions thérapeutiques... 17
1.3.1.1 Aspect économique ... 17
1.3.1.2 Évolution des recommandations de traitement de l’IM ... 18
1.3.2 Influence du type d’infarctus ... 19
1.3.3 Durée de séjour ... 20
1.3.4 Coûts de la prise en charge de l’IM ... 20
II.OBJECTIFS DE RECHERCHE ... 23
2.1 Objectifs ... 23
2.2 Hypothèse ... 23
III.MÉTHODE ... 24
3.1 Population étudiée ... 24
3.2 Source des données ... 24
3.3 Critères d’inclusion et d’exclusion ... 26
3.3.1 Critères d’inclusions ... 26
3.3.2 Critère d’exclusion ... 26
v
3.4 Variables indépendantes ... 27
3.4.1 Identification des issues cliniques ... 27
3.4.1.1 Comorbidités ... 28
3.4.1.2 Type d’infarctus ... 28
3.4.1.3 Type d’intervention ... 28
3.5 Variables dépendantes ... 31
3.5.1 Identification des issues économiques ... 31
3.5.1.1 Utilisation des ressources ... 31
3.5.1.2 Coûts ... 31
3.6 Analyse statistique ... 32
3.6.1 Catégorie d’année ... 33
3.6.2 Analyse des ressources ... 33
3.6.3 Analyse des coûts... 34
3.7 Aspects éthiques ... 34
IV.CHAPITRE I ... 36
4.1 Résumé ... 37
4.2 Abstract ... 38
V.ANALYSES SUPPLÉMENTAIRES ... 57
5.1 Analyses stratifiées selon le sous-type d’IM ... 57
5.2 Analyses stratifiées selon le sexe ... 60
VI.DISCUSSION GÉNÉRALE ... 62
6.1 Résumé de l’étude ... 62
6.2 Comparaison avec la littérature... 62
6.3 Forces et limites de l’étude ... 63
6.3.1 Limites de l’étude ... 63
6.3.1.1 Validité interne ... 64
6.3.1.2 Validité externe ... 66
6.3.2 Forces de l’étude ... 67
6.4 Importance des résultats ... 67
6.5 Possibilités de recherche futures ... 68
CONCLUSION ... 70
BIBLIOGRAPHIE ... 71
ANNEXE A :ORGANIGRAMME DE SUIVI DES PARTICIPANTS DE LA COHORTE PROSPECTIVE QUÉBEC (PROQ) SUR LE TRAVAIL ET LA SANTÉ ... 76
ANNEXE B :CODES DIAGNOSTIQUES UTILISÉES LORS DE L’EXTRACTION DES DONNÉES POUR RETROUVER LES CAS INCIDENTS ... 78
ANNEXE CALGORITHME DE CODIFICATIONS DES COMORBIDITÉS UTILISÉES ... 79
ANNEXE D :CODES UTILISÉS DE LA CLASSIFICATION CANADIENNE DES ACTES DIAGNOSTIQUES, THÉRAPEUTIQUES ET CHIRURGICAUX (CCADTC) ... 81
ANNEXE E :CODES UTILISÉS DE LA CLASSIFICATION CANADIENNE DES INTERVENTIONS (CCI) ... 82
ANNEXE F :CODES D’ENTENTE DE FACTURATION DE LA DEMANDE DE PAIEMENT DE LA FÉDÉRATION DES MÉDECINS OMNIPRATICIENS DE QUÉBEC (FMOQ) ... 86
ANNEXE G :CODES D’ENTENTE DE FACTURATION DE LA DEMANDE DE PAIEMENT DE LA FÉDÉRATION DES MÉDECINS SPÉCIALISTES DE QUÉBEC (FMSQ) ... 87
vi
Liste des tableaux
Tableau 1 : Facteurs de risque de survenue d’un premier infarctus du myocarde ... 5
Tableau 2: Perspectives économiques en santé ... 14
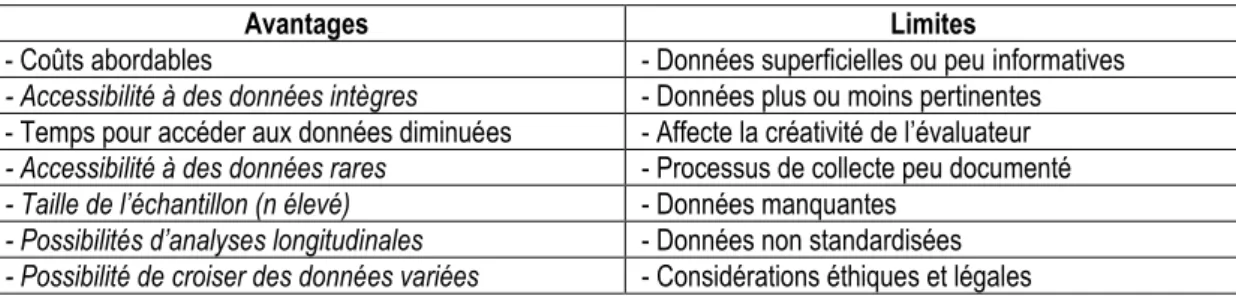
Tableau 3: Principaux avantages et limites de l'analyse de données secondaires ... 27
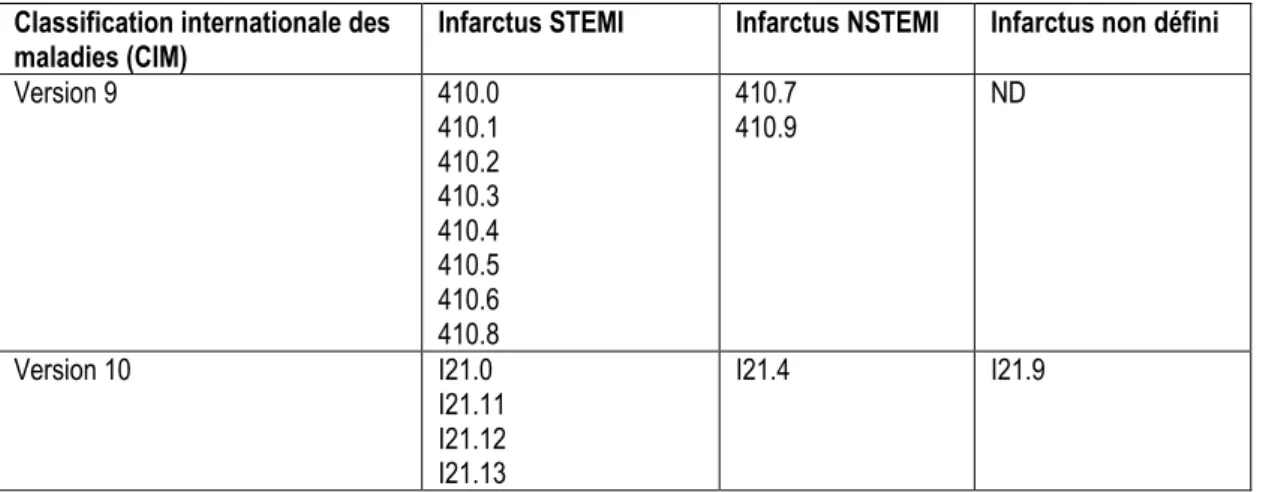
Tableau 4: Algorithme d'identification des codes diagnostiques reliés aux infarctus STEMI, NSTEMI et non-définis. ... 28
Tableau 5: Classifications des codes diagnostics et d'intervention ... 29
Tables 6: Sociodemographics characteristics of the study sample ... 48
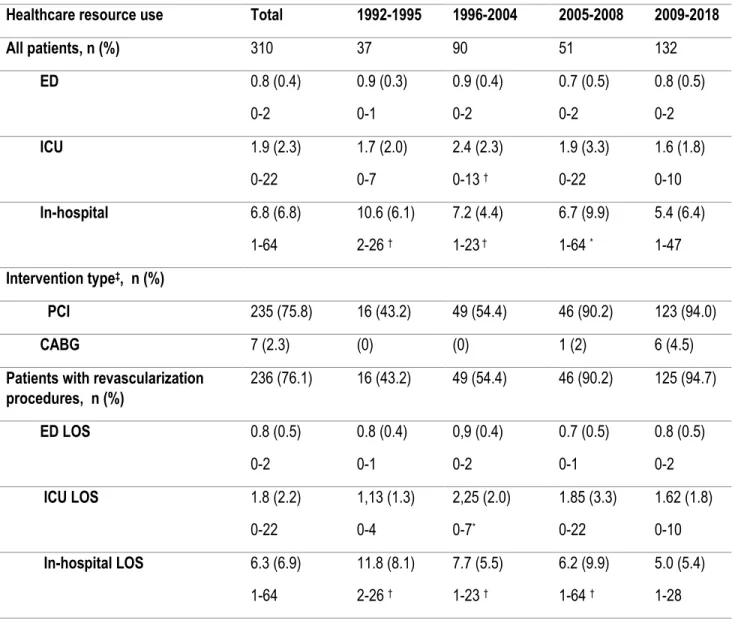
Tableau 7: Healthcare resources used by time categories and stratified in function of the presence or absence of a revascularization procedure. ... 50
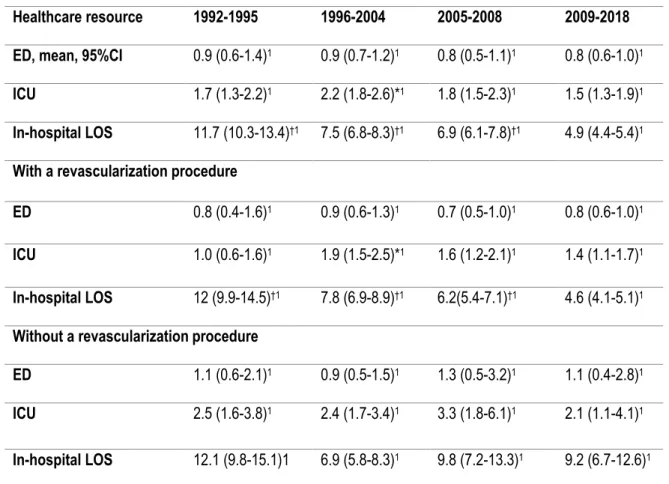
Tableau 8: Adjusted healthcare resources used by time categories and in function of the presence or absence of a revascularization procedure. ... 52
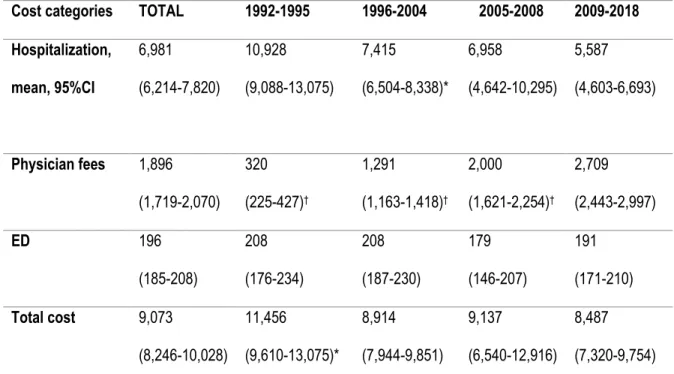
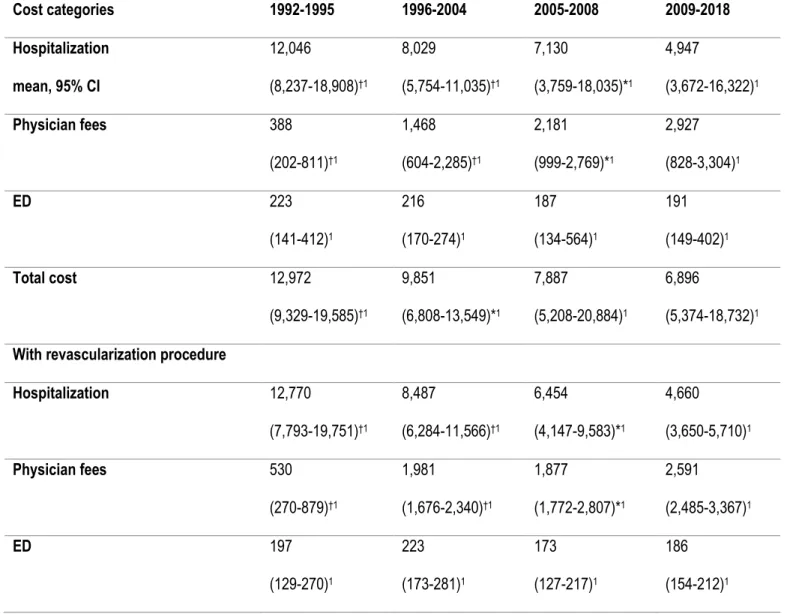
Tableau 9: Myocardial infarction cost, by cost categories over time and in function of the presence or absence of revascularization procedures. ... 53
Tableau 10: Utilisation des ressources et des coûts directs engendrés par un premier épisode de soins, stratifié selon le sous-type d'IM (STEMI, NSTEMI, non-définis) ... 58
Tableau 11 : Utilisation des ressources et des coûts directs engendrés par un premier épisode de soins à la suite d’un IM, stratifié selon le sexe ... 60
Tableau 12: Codes used to find incident myocardial infarction in ICD-9. ... 78
Tableau 13: Codes used to find incident myocardial infarction in ICD-10. ... 78
Tableau 14: Algorithme de codification des comorbidités selon ICD-9 et ICD-10 ... 79
Tableau 15: Codes utilisés de la CCADTC pour retracer les ICP ... 81
Tableau 16: Codes utilisés de la CCADTCC pour retracer les PAC ... 81
Tableau 17: Codes used with the CCI to retrace PCI ... 82
Tableau 18: Codes used in the CCI to retrace CABG ... 85
Tableau 19: Codes utilisés pour retracer les ICP et PAC avec le FMOQ. ... 86
vii
Liste des formules
Équation 1: Formule permettant d'obtenir un rapport de coût-efficacité incrémentiel entre deux
interventions en santé. ... 10 Équation 2: Formule permettant de déterminer quelle intervention favoriser dans une analyse coût-bénéfice. ... 11 Équation 3: Formule permettant d'obtenir une valeur actuelle, selon une valeur passée. ... 16
viii
Liste des figures
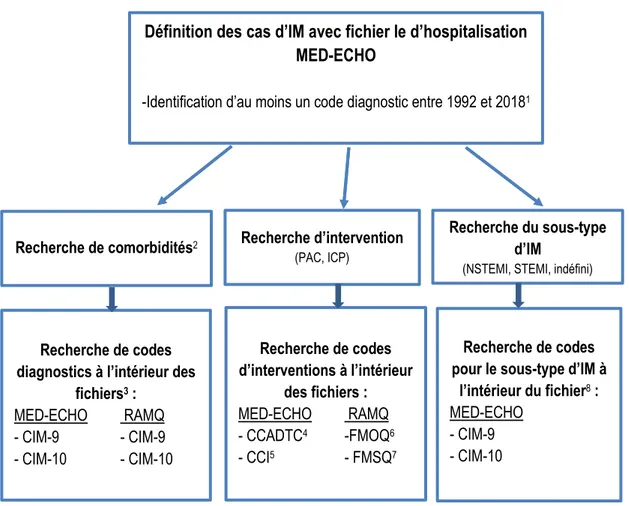
Figure 1 : Algorithme d'identification des cas d'infarctus du myocarde et différentes caractéristiques à partir des bases de données médico administratives du Québec……….………….30 Figure 2 : Flowchart of the PROspective Quebec (PROQ) Study on Work and Health……….….76
ix
Liste des abréviations, sigles, acronymes
Français :
ACMTS : Agence canadienne des médicaments et des technologies en santé AVAQ : Années de vie ajustée selon la qualité
AVCI : Année de vie corrigée pour incapacité ECG : Électrocardiogramme
CCADTC : Classification canadienne des actes diagnostiques, thérapeutiques et chirurgicaux CCI : Classification canadienne des interventions
CIM : Classification internationale des maladies
FMOQ : Fédération des médecins omnipraticiens du Québec FMSQ : Fédération des médecins spécialistes du Québec IC : Intervalle de confiance
ICP : Intervention coronarienne percutanée IPC : Indice des prix à la consommation IM : Infarctus du myocarde
IMC : Indice de masse corporelle MCV : maladies cardiovasculaires
OCDE : Organisation de coopération et de développement économique OMS : Organisation Mondiale de la Santé
RAMQ : Régie de l’assurance maladie du Québec
MED-ECHO : Maintenance et exploitation des données pour l’étude de la clientèle hospitalière MSSS : Ministère de la Santé et des Services sociaux
SCC : Société canadienne de cardiologie
Anglais :
CABG : Coronary artery bypass grafting
CADTH : Canadian agency for drugs and technologies in health CCI: Canadian Classification of intervention
DALY: Disability Adjusted Life Years CI : Confidence interval
CVD : Cardiovascular disease
ICD : International classification of diseases MI : Myocardial infarction
QALY: Quality Adjusted Life Years CCS : Canadian Cardiovascular society
x
Remerciements
Je tiens à offrir de profonds et sincères remerciements à mon directeur de recherche Jason Robert Guertin, Ph. D. qui a cru en moi dès notre première rencontre. Son appui, son temps et son dévouement envers les étudiants qu’il dirige se doivent d’être soulignés. Son soutien dans mon projet de retour aux études m’a permis de franchir une nouvelle étape de ma vie professionnelle et de dépasser mes limites. L’univers auquel le Dr Guertin m’a initiée est fascinant, et avec ce nouveau bagage accumulé durant mon parcours de maîtrise, je suis prête pour de nouveaux défis professionnels. Je tiens à remercier Xavier Trudel, en tant que co-directeur de recherche pour son appui et son soutien ainsi que tous les membres de l’équipe de recherche de la Dre Chantal Brisson, qui m’ont accueilli parmi eux et qui m’ont soutenu durant ce processus académique.
Je tiens à souligner le travail fabuleux de l’ensemble du corps professoral de la maîtrise et du doctorat en épidémiologie de l’Université Laval. L’implication et le dévouement de tous auprès des étudiants rendent la qualité de l’enseignement exceptionnelle. Merci à tous de transmettre aux étudiants votre passion avec autant d’énergie et de plaisir que vous le faites.
Ce projet de maîtrise en épidémiologie était pour moi une vieille ambition. Ce fut notamment possible grâce au soutien sans égal de mon entourage. Merci à mon conjoint qui malgré la distance imposée par ce projet a su m’épauler et m’encourager dans cette aventure. Sans son soutien sans faille, il m’aurait été d’autant plus difficile d’y parvenir.
Alors que je m’éloignais, physiquement du moins, de mon conjoint resté en Suisse, j’ai eu le plaisir de retrouver et recréer des liens forts avec ma famille, au Québec. Leur soutien et réconfort pendant ces deux années m’ont permis d’apaiser les moments difficiles et de partager ceux de bonheur. Leur confiance m’a permis d’y croire. Pendant cette période, des amitiés se sont renforcées alors que d’autres sont nés, grâce à elles, j’ai pu partager.
Merci aux organismes subventionnaires desquels j’ai obtenu du soutien financier, le Réseau québécois de recherche sur les médicaments (RQRM) et centre de recherche du centre hospitalier universitaire de Québec. Avec votre soutien financier, j’ai pu consacrer mon temps à la poursuite de mes études sans devoir concilier avec un second travail. Sans cette aide, ce projet se serait révélé d’autant plus laborieux. Merci de votre intérêt envers mon projet.
xi
Avant-propos
Ce mémoire est l’aboutissement d’un travail de collaboration mené sous la direction de Dr Jason Robert Guertin, professeur au Département de médecine sociale et préventive de l’Université Laval et la co-direction de Dr Xavier Trudel, également professeur au Département de médecine sociale et préventive. Pour les besoins de la réalisation de ce projet de recherche, j’ai eu accès aux banques de données d’une cohorte de travailleurs de la ville de Québec. Ce projet a été financé par le réseau québécois sur la recherche des médicaments (RQRM).
Je suis l’auteure principale de l’article scientifique intégré dans ce mémoire. J’ai ainsi eu la possibilité de réaliser toutes les étapes de ce projet de recherche à savoir, la revue de la littérature, la rédaction du protocole de recherche, la formulation des objectifs, les analyses statistiques, l’interprétation des résultats ainsi que la rédaction de ce mémoire. Les co-auteurs ont contribué à la préparation du manuscrit à divers degrés. Dr Jason Guertin et Dr Xavier Trudel m’ont assisté dans la réalisation de l’ensemble des étapes de la recherche.
Le projet de recherche a été réalisé à l’Hôpital du Saint-Sacrement à Québec, siège de l’Axe santé des populations et pratiques optimales en santé du centre de recherche du centre hospitalier universitaire de Québec. Ce mémoire est composé d’un article, qui occupe la section des résultats du mémoire. L’article fait état des coûts de prise en charge hospitalière d’un infarctus du myocarde au Québec. Plus spécifiquement, il traite des coûts directs engendrés par l’hospitalisation des patients ayant subi un premier infarctus du myocarde.
Les résultats de ce projet ont été présentés à diverses rencontres scientifiques :
▪ Présentation par affiche : 6e Journée de la recherche des étudiants SP-POS, 7 juin 2019,
Université Laval à Québec.
▪ Présentation par affiche : Journée de la recherche 30 et 31 mai 2019, Pavillon Ferdinand-Vandry, Université Laval.
▪ Présentation par affiche : 28e Congrès scientifique annuel de la Société québécoise
d’hypertension artérielle (SQHA), Montréal, 24-25 janvier 2020.
▪ Présentation par affiche : Symposium agence canadienne des médicaments et des technologies en santé (ACMTS), résumé accepté pour présentation par affiche, conférence annulée.
À noter que la crise sanitaire du COVID-19 a apporté d’importants délais et complication à la finalisation de ce projet. De plus, l’annulation de plusieurs rencontres scientifiques auxquelles devait être présenté ce projet a nui à sa visibilité. Plusieurs éléments de ce projet, notamment au niveau méthodologique, ont dû être revus afin de pouvoir terminer à l’échéance prévue.
Enfin, il est prévu que l’article scientifique inséré dans ce mémoire soit soumis au Canadian Journal of Cardiology pour publication durant l’automne 2020.
1
Introduction
Problématique
Le profil épidémiologique des maladies cardiovasculaires (MCV) a subi de profondes modifications, au niveau mondial, au cours des trois dernières décennies (1). Alors que le taux de mortalité a diminué de moitié dans les pays les plus développés, la tendance est tout autre dans les pays à revenu faible et moyen. Le taux de mortalité dans ces pays est stable, voire en augmentation (1). Malgré une forte baisse du taux de mortalité dans les pays à revenu élevé, il s’agit malgré tout de la première cause de décès dans le monde depuis plus de 16 ans (2). À elles seules, les MCV sont responsables de plus de 17,3 millions de décès annuellement (3). En 2015, l’Organisation Mondiale de la Santé (OMS) a affirmé que 42% des décès liés aux MCV étaient attribuables aux cardiopathies ischémiques, dont fait partie l’infarctus du myocarde (IM) (3). L’IM se caractérise par l’obstruction partielle ou complète d’une ou de plusieurs artères coronaires en plus d'entraîner une ischémie et une nécrose cellulaire qui peut s’avérer irréversible (4). Au Canada, environ 2,4 millions de personnes de plus de 20 ans vivent avec une cardiopathie ischémique. En 2012-2013, 62 300 personnes ont eu un premier IM, correspondant à une incidence de 2,3 pour 1000-personnes-année (5).
D’autre part, les MCV sont la deuxième source du fardeau économique des soins de santé au Canada (6). En 2002, cette charge économique était estimée à 22,3 milliards de dollars par an. Les coûts directs, définis comme étant les ressources consommées directement pour traiter un problème de santé, représentent 34,7% de ces coûts. Cette responsabilité financière additionnée aux conséquences à court et long terme de l’IM ont incité les gouvernements à intensifier la prévention des facteurs de risque des MCV (7). Des progrès majeurs ont été réalisés sur la prévention et la cessation du tabagisme, le traitement précoce de l’hypercholestérolémie et du diabète de type II. Les innovations technologiques au niveau de la prise en charge thérapeutique des patients sont également à noter. Un diagnostic précoce et la mise en place de plateaux techniques permettent des interventions thérapeutiques plus rapides (8). Au fil du temps, à la fois, le profil des patients atteints d’IM et la prise en charge thérapeutique se sont profondément modifiés. Au Canada, entre 1979 et 2007, la baisse de la prévalence des MCV et du taux de mortalité qui y est associé a permis d’augmenter de trois ans l’espérance de vie, chez les gens âgés de 65 et 85 ans, et ce autant chez les hommes que chez les femmes (9). Sachant que les patients qui souffrent aujourd’hui d’un IM sont différents de ceux qui ont subi un IM il y a trente ans, que savons-nous sur l’utilisation des ressources en santé et les coûts engendrés par ces patients, durant cette période?
Propre à chaque législation selon l’organisation et le système de soins de santé en vigueur dans chaque pays, il est difficile d’extrapoler les résultats d’une étude de coûts hors du pays dont elle est issue. L’American Heart Association prévoit, aux États-Unis, une hausse des coûts de prise en charge des cardiopathies ischémiques (10). Une étude italienne (11) observe une augmentation des coûts de prise en
2
charge des patients à la suite d’un premier IM. Au Canada, une étude de coûts réalisée en Alberta (12) a estimé le coût engendré par la prise en charge médicale de l’IM. Selon la conclusion des auteurs, entre 2004 et 2013, le fardeau économique du coût annuel de prise en charge d’un IM, tend à diminuer, de manière significative. Les coûts de prise en charge hospitalière représentent la plus grande part des coûts (63,1%), suivie des médicaments (21,1%). Des différences de coûts ont pu être observées, entre le type d’infarctus et la prise en charge médicale privilégiée. De plus, des nuances au niveau du coût des soins ont été observées entre les hommes et les femmes. L’horizon temporel de cette étude était limité à neuf ans, soit de 2004 à 2013.
Au Québec, des chercheurs ont projeté jusqu’en 2050 les dépenses publiques en hospitalisations et en consultations médicales selon divers scénarios d’évolution de la présence des MCV. Un scénario plausible ont amené les chercheurs, à émettre l’hypothèse qu’une diminution de 30% de l’incidence des MCV grâce à la prévention des facteurs de risque auprès de la population pourrait générer 21 milliards de dollars d’économies (13). Cette étude permet de croire que les dépenses en santé pour traiter les MCV pourraient diminuer dans un proche avenir. En ce qui concerne l’IM, aucun projet de recherche ne s’est intéressé à l’évolution de ses coûts directs et des ressources de soins de santé engendrés, au cours des trois dernières décennies. Ainsi une étude rétrospective sur un horizon temporel à plus long terme permettra d’observer les tendances des coûts et de l’utilisation des ressources en soins de santé sur les cas incidents d’IM. L’incidence des IM n’étant pas nulle, étudier les coûts de prise en charge des patients souffrant d’un premier IM permettra de prévoir l’impact économique d’un premier événement d’IM dans les années à venir. La présente étude vise à estimer les coûts de prise en charge hospitalière reliés à un premier IM au Québec. Dans un second temps, cette étude examinera l’évolution des parts relatives des différentes composantes de coûts. Ce projet permettra de déterminer quelles catégories de coûts ont le plus d’impact, sur l’ensemble de la prise en charge. Les catégories de coûts varient-elles en fonction du temps? De plus, ce projet permettra de comparer les coûts selon le type de prise en charge médicale privilégiée ainsi que d’évaluer l’impact de l’âge et du sexe sur les coûts de prise en charge. Cette étude permettra de décrire les tendances dans l’utilisation des soins de santé et permettra de prévoir l’impact du fardeau économique, causé par l’IM.
3
I.
Recension des écrits
1.1 L’infarctus du myocarde
1.1.1 PhysiopathologieL’infarctus du myocarde est une pathologie due à l’ischémie du muscle cardiaque (14). Le myocarde est irrigué par un réseau d’artères coronaires complexe qui permet l’apport en oxygène nécessaire au bon fonctionnement du muscle. À la suite de l’obstruction d’une artère par un phénomène biologique tel que l’angine ou un thrombus causé par le détachement d’une plaque d’athérosclérose, le myocarde est privé d’apport en oxygène et un processus avec une issue irréversible se déclenche; l’ischémie du myocarde. L’ischémie cause la mort des cellules et engendre un processus de nécrose au niveau du muscle. Ce phénomène causant la mort des cellules n’est pas instantané, mais nécessite entre quatre et six heures (14).
Les manifestations cliniques présentées par les patients peuvent s'apparenter aux symptômes suivants: douleur épigastrique, douleur thoracique, sensation d’essoufflement, douleur au niveau du bras gauche avec ou sans irradiation dorsale ou de la mâchoire. Rapidement, un diagnostic objectif doit être posé. Le diagnostic médical de l’IM se confirme à l’aide de l’observation d’une élévation des marqueurs biochimiques, des techniques d’imagerie et l’activité électrique du cœur enregistrée grâce à l’électrocardiogramme (ECG). L’ECG permet de confirmer la présence d’une ischémie au niveau du myocarde. Les changements électriques enregistrés permettent de catégoriser l’infarctus. Afin de faciliter les références aux formulations anglophones, le terme STEMI (ST elevation myocardial infarction) et NSTEMI (Non-ST elevation myocardial infarction) seront utilisés (8, 14). Les lettres ST font référence au segment ST, retrouvé sur le tracé de l’électrocardiogramme.
1) L’infarctus de type STEMI correspond à une obstruction complète d’une artère coronaire. Ce type d’IM est celui nécessitant le plus haut niveau de priorité de prise en charge. Comme son nom l’indique, le STEMI est reconnaissable à l'ECG par une nouvelle élévation du segment ST (ou onde Q de nécrose).
2) L’infarctus de type NSTEMI représente une obstruction partielle de l’artère coronaire et ne présente pas de surélévation du segment ST, à l’ECG. Au contraire, ce dernier peut parfois montrer une dépression du segment ST, des changements de l’onde T, ou simplement un tracé ECG sans présence d’anomalie et d’onde Q de nécrose (14).
À la suite de la privation d’oxygène causée par l’ischémie, une nécrose myocardique se développe et amène des conséquences irréversibles. Lors d’un infarctus de type STEMI, une prise en charge d’urgence est
4
nécessaire. Les patients qui ne sont pas traités dans les délais prescrits par la Société canadienne de cardiologie sont deux fois plus à risque de décéder, dans les 30 jours suivant un infarctus du myocarde (15). L’intervention coronarienne percutanée (ICP) est l’option de choix afin de déterminer le type, le lieu et la gravité de la lésion sur la ou les artères coronaires affectées par l’ischémie (16). Lorsque le traitement de la lésion ischémique n’est pas possible par angioplastie, le pontage aortocoronarien (PAC) s’avère la meilleure option de traitement. Le traitement de l’infarctus NSTEMI ne nécessite pas d’emblée une reperfusion rapide, puisque le muscle myocardique n’est, à priori, pas complètement privé d’apport en oxygène (4).
1.1.2 Profil épidémiologique
Les maladies cardiovasculaires sont la première cause de mortalité dans le monde. D’autre part, l’évolution du taux de mortalité en lien avec les cardiopathies ischémiques s’est profondément modifiée, au cours des dernières décennies (17). Les tendances temporelles des cardiopathies ischémiques dans 21 régions du monde, observées entre 1980 et 2010, démontrent qu’il existe d’importantes disparités régionales en matière de taux de mortalité (18). Un déclin de la mortalité a été observé depuis les années 1970, en Amérique du Nord. Entre 1980 et 2010, le taux de mortalité à l’échelle mondiale a diminué. Au niveau international, plusieurs disparités existent. Certaines régions telles que les Amériques, l’Océanie, la Chine et l’Europe de l’Ouest, ont des taux de mortalité standardisés par âge en 2010 qui oscille entre 36 et 100 décès par 100 000 personnes. En Europe de l’Est et en Asie centrale ce taux se situe entre 155 et 313 décès par 100 000 personnes (18).
Au Canada le taux de mortalité standardisé par âge à la suite d’un IM a diminué de 38,1%, entre 1994 et 2004 (19). Pour la même période, le taux d’admission dans un hôpital pour IM a diminué de seulement 9,2%. Par contre, le taux de décès intrahospitalier des cas d’IM a diminué de 33,1%, entre 1994 et 2004. Le contraste entre la forte diminution du taux de mortalité à la suite d’un IM et la diminution beaucoup plus modeste du taux d’admission est dû à deux facteurs antagonistes (19). D’abord, un diagnostic et un traitement plus précoce favorisent une diminution de mortalité intrahospitalière et le taux de mortalité général. Deuxièmement, puisque l’âge est un facteur de risque majeur des cardiopathies ischémiques, le vieillissement de la population entraîne un plus grand nombre de personnes âgées à être admis dans un centre hospitalier pour un IM. Les facteurs sous-jacents à ces changements sont dus à une diminution de l’exposition à des facteurs de risques majeurs des cardiopathies ischémiques. Une diminution de consommation de tabac, une augmentation d’exercice physique et un meilleur contrôle de l’hypertension artérielle sont documentés en Europe de l’Ouest et en Amérique du Nord. Malgré les efforts de prévention, les facteurs de risques sont d’autant plus prévalents chez les jeunes ayant un niveau socio-économique faible (20).
5
Au Québec, le profil épidémiologique des cardiopathies ischémiques a également fortement évolué. Entre 1981 et 2013, le taux de mortalité ajusté pour l’âge a diminué chez les hommes de 74,6% et de 63,6% chez les femmes (21). En observant les décès toutes causes confondues sur trois décennies, la proportion qu’occupaient les cardiopathies ischémiques représentait 33,4% de tous les décès en 1982, alors qu’elles étaient responsables de 18,1% des décès, en 2012. La prévalence, ajustée pour l’âge, des cardiopathies ischémiques était de 7,8%, au Québec, en 2011-2012 et de 8,1% au Canada, pour la même période (22). La prévalence a légèrement augmenté entre les années 2000 et 2006, pour ensuite se stabiliser autour de 8%. Par ailleurs, en 2011-2012, il existait toujours une différence de prévalence entre les deux sexes. La prévalence observée chez les hommes était de 9,9% et de 6,0%, chez les femmes. Entre 2000 et 2012, le taux d’incidence au Québec a diminué de 44% passant de 12,7% à 7,1%, durant cette période (22). De manière similaire à la prévalence, le taux d’incidence annuel, c’est-à-dire le nombre d’apparitions de nouveaux cas sur une période d'une année, a diminué. En 2011-2012, le taux d’incidence rencontré chez les femmes était de 5,5%, alors qu’il était de 9,1% chez les hommes.
1.1.3 Facteurs de risques
Il a été démontré que neuf facteurs de risque modifiables sont fortement associés, à la survenue d’un IM (23). Avec l’adoption de cinq bonnes habitudes de vie : un poids santé, la pratique d’activité physique régulière, l’absence de consommation de tabac et d’alcool avec modération, ainsi qu’une alimentation équilibrée, pourraient prévenir jusqu’à 79%, des cas d’IM (24). En contrepartie, certains facteurs de risque sont dits non modifiables puisqu’il est impossible de modifier leur impact. Il s’agit de l’âge, des antécédents familiaux et du sexe. Les facteurs de risques modifiables et non modifiables discutés dans cette section sont énumérés ci-dessous, dans le tableau 1.
Tableau 1 : Facteurs de risque de survenue d’un premier infarctus du myocarde Facteur de risques modifiables Facteur de risques non modifiables Alimentation Consommation d’alcool Diabète Dyslipidémies Hypertension Obésité Sédentarité Stress Tabac Âge Antécédents familiaux Sexe 1.1.3.1 Facteurs modifiables
Alimentation : Une consommation de trois portions ou plus de fruits et légumes par jour montre un effet protecteur de 19% du risque d’IM (25). La consommation de viande transformée, dans laquelle on retrouve
6
des ajouts d’agents de conservation alimentaire, représente un risque 42% plus élevé de survenue de maladies cardiovasculaires. Le risque associé à la consommation de viande transformée est effectif, à partir d'une consommation de celle-ci, supérieure à 50 grammes, quotidiennement (26).
Consommation d’alcool : certaines études suggèrent qu'une consommation faible à modérée (maximum 1-2/jours) d’alcool a un effet protecteur, sur la santé cardiovasculaire. Cette influence positive sur la santé démontre une diminution de 25% du taux incidence, des cardiopathies ischémiques (27). Au Québec, en 2002, il a été estimé que la proportion des décès de cardiopathie ischémiques attribuables à l’alcool était de -4,9% chez les femmes et de -9,3% chez les hommes. Ces pourcentages négatifs démontrent l’association protectrice d’une consommation d’alcool faible à modérer, sur la santé cardiovasculaire. À l’inverse, une étude génétique démontre qu’une réduction de la consommation d’alcool, même chez les gens ayant une consommation faible à modérer d’alcool, réduit le risque de maladie coronarienne (28). Diabète : Les évidences scientifiques ont établi depuis longtemps une association positive, entre le diabète et le de risque de cardiopathies ischémiques. Les diabétiques sont de deux, à quatre fois plus à risque de mourir d’une maladie cardiovasculaire. Environ 50% d’entre eux décéderont d’une maladie cardiovasculaire (29, 30). Une revue systématique et méta-analyse, publiée en 2016, a démontré que les diabétiques ont 50% plus de risque, de mourir des complications d’IM, comparativement à des personnes non-diabétiques (31).
Dyslipidémie : Le cholestérol sanguin et plus particulièrement les triglycérides, montrent une tendance linéaire positive entre l’incidence du risque de maladies ischémiques, lorsqu’elles se retrouvent en plus grande concentration dans le sang, et ce, chez les hommes et les femmes (32). Les deux tiers de la population ayant un taux de cholestérol à faible densité de lipoprotéines, ou en anglais low-density lipoproteins (LDL), le plus élevé est 1,7 fois plus à risque de subir un événement cardiovasculaire que le tiers de la population, ayant un taux plus faible (33).
Hypertension artérielle : Au Québec en 2003, la prévalence des MCV chez les hommes et chez les femmes hypertendus était de 12,8%. Chez les gens avec une tension artérielle normale, la prévalence est estimée à 2,7% (22). L’impact de l’hypertension artérielle sur les artères est insidieux, puisqu’il est rarement symptomatique. En effet, l’hypertension artérielle ne provoque souvent aucun symptôme, malgré qu’avec les années, son impact sur les artères soit un facteur de risque majeur des MCV. Une réduction de 10 mm de Hg de la pression systolique, chez les gens hypertendus, amène un effet protecteur de 17% sur le risque de survenue d’IM (34).
Obésité: Au Québec, la prévalence des maladies cardiovasculaires est près de deux fois plus élevée, chez les gens obèses, que chez les gens ayant un indice de masse corporelle (IMC) < 25 (22). Le surplus de poids corporel et la mesure de l’IMC qui y est associé ont longtemps été reconnus comme un excellent
7
indicateur en prévention de santé cardiovasculaire. Cependant, les évidences scientifiques démontrent que le ratio taille-hanche s’avère un meilleur indicateur du risque de la survenue d’IM (35).
Sédentarité : Le manque d’activité physique est considéré comme le quatrième facteur de risque de décès au monde. Il est estimé que la sédentarité soit la cause principale, d’environ 30%, des cas de cardiopathie ischémique (36). L’activité physique, peu importe le type, pratiquée de manière récréative ou non a un effet protecteur sur la santé cardiovasculaire. Il est démontré que l’activité physique diminue le risque de mortalité par événement cardiovasculaire aigüe (37).
Stress : Le stress est un facteur de risque bien connu des maladies cardiovasculaires. En s’intéressant à l’association entre la récurrence d’événement cardiovasculaire et les gens ayant déjà fait un événement cardiaque, lorsqu’exposés au stress au travail, il a été démontré que ceux-ci ont deux fois plus de chance de subir un deuxième événement cardiovasculaire que ceux non exposés au stress au travail (38). Tabac : Les effets néfastes du tabac sur la santé et les maladies du cœur sont bien connus et documentés, dans la littérature scientifique (39). Les fumeurs ont une espérance de vie de 5,5 années inférieures, à celles des non-fumeurs. À lui seul, au Québec, le tabagisme est responsable d'une utilisation excédentaire de 32,6% des dépenses totales actuellement encourues, pour les jours d’hospitalisation (40). En observant les coûts directs attribuables au tabagisme pour les soins hospitaliers, il est estimé que le tabagisme est responsable de 8,1% des ressources utilisées pour les soins et le diagnostic des patients, atteints de cardiopathies ischémiques (40).
1.1.3.1.1 Évolution des facteurs de risque modifiables
Au Canada, un outil a été développé afin d’observer la prévalence des facteurs de risques modifiables de la santé cardiovasculaire de la population (41). Cet outil, nommé Cardiovascular Health in Ambulatory Care Research (CANHEART) est basé sur une enquête sur la santé de la population canadienne. Les chercheurs ont examiné la prévalence de six facteurs de risque cardiovasculaires. Ils ont défini des critères pour chacun des six facteurs de risque. Additionnées ensemble, les mesures des indicateurs permettent d’obtenir un score de santé cardiovasculaire entre 0 (très mauvais) et 6 (idéal). Les données récoltées, entre 2003 et 2011, ont permis de démontrer que la prévalence de certains facteurs favorables à une bonne santé cardiovasculaire est en progression. Notamment, l'augmentation de consommation de fruits et légumes, ainsi que l'accroissement de la pratique d’activité physique. Une diminution d’usagers du tabac a pu être observée. Par contre, une augmentation de la prévalence des personnes en surpoids, de l’hypertension et du diabète a été constatée. Selon cet outil, seulement 9,4% des Canadiens ont une santé cardiovasculaire optimale, soit un score de 6 sur l’échelle CANHEART. Des efforts de promotion de la santé sont encore nécessaires.
8
1.1.3.2 Facteurs non modifiables
Alors que les facteurs de risque modifiables sont des éléments sur lesquels les individus ont un certain pouvoir, il n’en est pas de même pour les facteurs de risque non modifiables. Ceux-ci sont indépendants de la volonté et du pouvoir des individus d’influer sur eux.
Âge : Les cardiopathies ischémiques sont étroitement reliées à l’âge. Le vieillissement biologique du corps humain le prédispose au risque de souffrir d’hypertension artérielle et du diabète qui sont notamment des facteurs de risque majeurs des cardiopathies ischémiques. Au Québec, à partir de 45 ans, la prévalence des cardiopathies ischémiques augmente de manière fulgurante. En 2012, la prévalence chez les hommes âgés de 45 à 49 ans était de 3,9% alors qu’elle est de 54,1% chez les personnes âgées de 85 ans et plus. Chez les femmes, la prévalence était de 2,0% chez les 45 à 49 ans, pour augmenter à 43,2% chez les 85 ans et plus (22).
Antécédents familiaux : Du point de vue clinique, les antécédents familiaux sont un facteur de risque majeur des maladies cardiovasculaires. Ainsi, les hommes, dont un des parents est décédé de manière prématurée d’une maladie cardiovasculaire ont deux fois plus de risque, de souffrir de maladies cardiovasculaires, ce risque est de 1,7 fois chez les femmes (42).
Sexe : Les hommes sont encore aujourd’hui les plus touchés par les cardiopathies ischémiques. Au Canada, en 2012-2013 la prévalence des cardiopathies ischémiques chez les plus de 20 ans était de 10% chez les hommes, alors qu’elle était de 6,3% chez les femmes (5). En ce qui concerne l’IM, pour la même période, la prévalence était de 2,9% chez les hommes et de 1,1% chez les femmes. Les femmes ont en moyenne leur premier événement cardiovasculaire, neuf ans plus tard que les hommes. L’âge médian est de 65 ans chez les femmes et de 56 ans chez les hommes (23). En plus des pistes hormonales qui semblent être en cause, cette différence est explicable par le fait que les hommes sont exposés plus longtemps que les femmes à des facteurs de risque de niveau élevé, tels que l’hypertension et le tabac.
1.2 Économie en santé
Puisque ce projet de recherche s’intéresse à l’IM, sous un angle économique, en estimant les coûts de prise en charge hospitalière, une présentation des concepts clefs de l’économie en santé et des principes qui la soutiennent sont importants. Ceux-ci seront abordés dans la section suivante.
1.2.1 Mise en contexte
L’économie est une science qui s’intéresse aux choix. Elle se définit comme l’utilisation des ressources dans un contexte de rareté (43). Appliquée au contexte de la santé, l’économie se définit de la même manière. Elle correspond à l’allocation et la distribution des ressources, toujours dans un contexte où les ressources
9
sont insuffisantes, à combler tous les besoins (44). Le système de santé est soumis aux mêmes pressions que la loi de l’offre et la demande. Les demandes et besoins en soins de santé sont infinis, alors que les ressources, elles, sont limitées. L’intérêt des scientifiques envers l’économie en santé est un phénomène qui prend son envol dans les années 1960. Un des pionniers de cette branche de l’économie est le théoricien Kenneth J. Arrow, lauréat du Prix Nobel (43). En observant le PIB, la part des dépenses de santé dans les pays membres de l’organisation de coopération de développement économique (OCDE) a doublé, entre 1960 et 1990 (45). D’où l’intérêt de s’assurer que les ressources mises à dispositions sont bien utilisées avec le meilleur rendement possible pour la société. Dans une juridiction comme celle du Canada, où le gouvernement couvre la plupart des coûts en soins de santé, les personnes atteintes de maladies sont peu confrontées aux questions telles que : quel est le coût d'une journée d’hospitalisation? Quel est le coût d’une intervention? De quelle manière, les ressources consommées en soins de santé auraient-elles pu être autrement distribuées? Par différents champs d’intérêt, l’économie en santé tente de répondre à ces questions. L’économie en santé s’oriente autour de quatre axes : le développement de la santé, l’activité économique et le système de soins, la régulation du système de soins et l’évaluation économique (45). Une attention particulière sera portée à cette dernière, dans la section suivante, puisqu’elle est requise pour répondre aux objectifs du projet.
1.2.2 Évaluation économique
L’évaluation économique permet de comparer le coût et les effets sur la santé, de différentes interventions. Elle permet d’outiller les décideurs en soins de santé et d’éclairer leurs décisions concernant l’allocation des ressources de santé. Au Canada, deux entités ont pour mission de fournir des lignes directrices sur l’évaluation des coûts et l’allocation des ressources en soins de santé. Dans toutes les provinces canadiennes, sauf au Québec, l’Agence canadienne des médicaments et des technologies en santé (ACMTS) remplit ce rôle. Au Québec, l’Institut national d’excellence en santé et en services sociaux (INESSS) a la mission de promouvoir l’utilisation efficace des ressources dans le secteur de la santé et des services sociaux. L'INESSS publie des lignes directrices et conduit des études sur les coûts et l’utilisation de ressources en santé. Afin de répondre aux questions soulevées par l’évaluation économique, quatre types d’études sont utilisés : analyse de minimisation de coûts, analyse coût-efficacité, analyse coût-utilité, et l'analyse coût-bénéfice. Chacune d’elle est décrite dans les paragraphes suivants (46).
L’analyse de minimisation des coûts : s’intéresse à deux technologies dont les effets et conséquences connus sont identiques, en tout point. On compare seulement les coûts entre deux technologies. Ce devis est peu utilisé, car il est difficile de faire le postulat que deux technologies ont à la fois les mêmes effets et que l'ensemble de leurs conséquences sont identiques. L’application de ce type d’étude est souvent
10
réservée aux produits pharmaceutiques quand on s’intéresse à un produit générique, versus une version brevetée.
L’analyse coût-efficacité : mesure l’impact marginal de deux interventions. Elle s’intéresse à une seule conséquence commune des interventions ou technologies étudiées. Le résultat de cette analyse se résume à un ratio, où le numérateur est la différence de coûts, entre les deux interventions. Ce type d’étude mesure l’impact marginal d’un choix sur les coûts et la santé. Le numérateur est déterminé à la suite de la mesure de la différence d’une conséquence entre les interventions, en termes de valeur naturelle (les années de vies gagnées, les jours d’hospitalisation sauvés, nombre d’années de vie, etc.). Le dénominateur est une estimation de la différence de coûts attendus entre les deux interventions. Le résultat se traduit par un rapport de coût-efficacité incrémentiel, mieux connu sous le terme anglais de Incremental cost-effectiveness ratio (ICER). L’équation 1 montre la formule à utiliser.
𝐼𝐶𝐸𝑅 = ∆ 𝐶 ∆ 𝐸 =
𝐶𝑜û𝑡 ($) 𝐼𝑛𝑡𝑒𝑟𝑣𝑒𝑛𝑡𝑖𝑜𝑛 𝐵 − 𝐶𝑜û𝑡 ($) 𝐼𝑛𝑡𝑒𝑟𝑣𝑒𝑛𝑡𝑖𝑜𝑛 𝐴 𝐸𝑓𝑓𝑖𝑐𝑎𝑐𝑖𝑡é 𝐼𝑛𝑡𝑒𝑟𝑣𝑒𝑛𝑡𝑖𝑜𝑛 𝐵 − 𝐸𝑓𝑓𝑖𝑐𝑎𝑐𝑖𝑡é 𝐼𝑛𝑡𝑒𝑟𝑣𝑒𝑛𝑡𝑖𝑜𝑛 𝐴 Équation 1: Formule permettant d'obtenir un rapport de coût-efficacité incrémentiel entre deux interventions en santé.
L’analyse coût-utilité : contrairement aux devis présentés précédemment, celui-ci a la particularité de pouvoir comparer une ou plusieurs conséquences pouvant être différentes, entre les interventions. Pour ce faire, elle utilise une mesure agrégée permettant de prendre en compte une dimension de durée et une seconde dimension regardant la préférence du patient pour son état de santé. À l’aide de questionnaire validé, la préférence des participants pour l'état de santé est mesurée et on y attribue un score entre 0 et 1, nommé score d’utilité. Le chiffre obtenu est multiplié par le temps passé dans cet état et on obtient une mesure correspondant au nombre d’années de vie ajustée selon la qualité (AVAQ). Ce terme est plus fréquemment retrouvé dans la littérature selon l’appellation anglophone Quality Ajusted Life-Years (QALY). L’avantage du QALY est qu’il tient compte de la durée et de la qualité de vie. Ainsi l’analyse coût-utilité utilise un ratio avec au numérateur la différence de coûts rencontrés entre deux interventions et au dénominateur la différence de QALY rencontré. Un autre concept retrouvé dans la littérature est celui de l’année de vie corrigée pour l’incapacité (AVCI), ou encore sous son appellation anglophone Disability Adjusted Life Years (DALY). Le DALY cherche à mesurer le nombre d’années engendrées par une maladie, un handicap ou la mortalité prématurée. Ce concept est plus fréquemment utilisé, dans le domaine de la santé publique au Canada et en santé internationale. Notamment par l’OMS pour l’évaluation des systèmes de soin qui l’utilise, ainsi que plusieurs autres indicateurs, pour mesurer le niveau de santé général d’une population.
L’analyse coût-bénéfice : ce type d’étude présente les effets et les conséquences des interventions en valeur monétaire. Cette méthode implique que les conséquences positives tout comme négatives sont
11
converties en valeur monétaire, à l’aide de différentes méthodes (47). Les interventions sont comparées selon leur bénéfice net et l’alternative la moins onéreuse sera préférée. Dans cette analyse, les mesures des coûts et des conséquences en santé sont rapportées en valeur courante d'une devise. L’équation 2 montre la formule à utiliser et la manière d’interpréter les résultats en fonction de l’intervention.
𝐵é𝑛é𝑓𝑖𝑐𝑒 𝑖𝑛𝑐𝑟é𝑚𝑒𝑛𝑡𝑖𝑒𝑙 = 𝑏é𝑛é𝑓𝑖𝑐𝑒𝑠 (𝐵 − 𝐴) − 𝑐𝑜û𝑡𝑠 𝑑′𝑖𝑛𝑡𝑒𝑟𝑣𝑒𝑛𝑡𝑖𝑜𝑛 (𝐵 − 𝐴) o Si le bénéfice incrémentiel de l’intervention B est > que celui de l’intervention A, on recommande l’intervention B. o Si le bénéfice incrémentiel de l’intervention B est < que celui de l’intervention A, on recommande l’intervention A. Équation 2: Formule permettant de déterminer quelle intervention favoriser dans une analyse coût-bénéfice.
L’analyse coût-bénéfice implique de donner un coût à la santé, ce qui s’avère souvent un coût dont la validité est subjective. De plus, ce concept est controversé sur le plan éthique. Il s’agit d’une limite de ce type d’étude. Les individus sont naturellement récalcitrants à donner une valeur monétaire à un état de santé. De plus, dans une juridiction telle que celle du Canada les soins de santé sont majoritairement assurés par le gouvernement. Les individus sont peu enclins à donner une valeur à la santé ou à une vie humaine.
1.2.3 Étude de coûts
Alors que l’évaluation économique permet d’éclairer les choix des décideurs en soins de santé, les analyses de coûts sont nécessaires afin de déterminer la valeur monétaire d’une intervention, d’estimer le fardeau d’une maladie ou afin de répondre à des analyses d’impact budgétaires. L’étude des coûts d’une maladie ou d’une intervention représente une forme d’évaluation économique partielle. Puisqu’elle ne s’intéresse qu’à une intervention. Fréquemment utilisé en économie de la santé (48), le but ultime des analyses de coût est de quantifier le nombre de ressources utilisées. En quantifiant les ressources, il est par la suite possible d’attribuer un coût unitaire à celles-ci. Une étude de coûts doit être entreprise selon les ressources disponibles; budget d’étude, temps à disposition, données disponibles, celles-ci guideront l’approche à utiliser.Un des défis de l’étude de coût est qu’il peut s’avérer difficile de choisir entre la précision dans l’estimation des coûts et la quantité d’information à capturer. Deux principes doivent être appliqués; premièrement : plus la ressource utilisée est d’une grande valeur monétaire, plus elle doit être incluse dans l’analyse de coût. Deuxièmement, plus la ressource que l’on souhaite quantifier est utilisée fréquemment, plus sa valeur d’information est grande et on doit s’assurer de saisir cette information pour l’intégrer à notre analyse (47). Bien entendu, on devrait toujours chercher à obtenir l’estimation des coûts la plus précise possible, mais le niveau de précision dépend de l’information disponible et surtout de la facilité d’accès à cette information, ainsi que du budget disponible.
12
L’estimation des coûts en santé représente un défi majeur. L’objectif est de déterminer un coût unitaire pour une ressource donnée. Afin de guider les chercheurs qui entreprennent ce type d'analyse, l’ACMTS suggère une série d’étapes à suivre permettant de réaliser adéquatement une analyse de coût (49). Celles-ci sont résumées dans les lignes suivantes.
Étapes à suivre pour réaliser une étude de coûts :
1. Définir le problème : la définition de la question de recherche permet de s’assurer que tous les coûts et ressources qui doivent être inclus dans l’étude sont identifiés. Définir des éléments tels que le contexte où se situe l’analyse de coût et la population cible permettent de déterminer ce qu’il est nécessaire d’inclure dans l’étude. D’autres éléments tels que la perspective choisie et l’horizon de temps doivent être déterminés. Ceux-ci seront discutés dans les sections suivantes. 2. Identifier les ressources à inclure dans l’analyse : les chercheurs doivent s’assurer que toutes les
ressources nécessaires selon la perspective de l’analyse sont identifiées. Exemple de catégories de ressources : pharmaceutiques, facturations médicales, services hospitaliers, services de facturation médicaux pour examens, etc.
3. La mesure des ressources : il existe deux types principaux de mesure de ressources, primaire et secondaires. Les mesures primaires sont celles qui sont collectées dans le cadre d’un essai clinique, ou d’une étude observationnelle. Les ressources mesurées de manière secondaire sont capturées à l’aide de données administratives, ou encore de bases de données cliniques. 4. La valeur des ressources : les ressources sont mesurées à l’aide de la monnaie en vigueur. Le
coût est la valeur multipliée par la quantité. Le prix est la valeur attribuée à un produit pour la production de celui-ci. Par exemple le coût d'un service ou d'une intervention. Les frais sont les montants chargés pour avoir droit à un service.
5. Identifier la variabilité, l’incertitude et les biais : la variabilité des résultats devrait être explorée dans le cadre d’analyses de sensibilités. L’incertitude reliée aux coûts peut prendre différentes formes, mais dans une analyse de coût l’emphase est mise sur l’incertitude des paramètres. Plus l’impact d’un paramètre de coûts est grand, plus l’estimation de celui-ci doit être précise. La présence de biais sur les mesures de coûts doit être mentionnée.
6. Rapporter les coûts : l’ACMTS a émis trois principes généraux permettant de guider le report des coûts et la mesure des ressources utilisées (49). Dans un premier temps, chaque composante de coût devrait être reportée séparément. Ensuite, les composantes doivent être agrégées, afin de déterminer un coût total. Dernièrement, les sources d’information devraient être fournies afin de
13
permettre au lecteur de vérifier et valider l’information des analyses. Ce dernier principe permet d’assurer la transparence des informations.
Dans la littérature l’analyse de coûts se décline sous trois grandes familles (47). La première est l’évaluation des coûts liés à un épisode de soins. Cette méthode cherche à évaluer de manière précise le coût des items et ressources utilisées. Ce sera cette approche qui sera favorisée pour réaliser ce projet de recherche. La deuxième méthode est celle qui tente d’évaluer le fardeau économique de la maladie. Elle cherche à estimer quel est l’impact économique d’une maladie sur la société. Ces deux méthodes ont le même objectif : quantifier le nombre de ressources utilisées selon leurs échelles respectives; le coût d’un épisode de soins mesure une prise en charge d’un problème de santé de manière ponctuel alors que l’estimation du fardeau économique d’une maladie mesure en terme économique un aspect chronique de la maladie. La troisième méthode, lorsqu’elle compare deux interventions, est une des formes d’évaluation économique; l’analyse de minimisation de coûts, précédemment discutée. Dans une analyse de coûts, tout comme dans toute étude reliée à l’économie en santé, plusieurs éléments doivent être précisés, ceux-ci sont discutés dans les sections suivantes.
1.2.3.1 Horizon temporel
Un élément important à préciser dans une étude de coût est l’horizon temporel de l’analyse. Celui-ci peut être court de quelques jours à quelques semaines, par exemple la durée d’un séjour hospitalier. Ou encore, il peut être long, p. ex., 5 ou 10 ans ou s’étendre à la durée de vie du patient. L’horizon temporel à privilégier sera influencé par l’histoire naturelle de la maladie. La durée de la maladie, son temps de traitement, les conséquences et les effets délétères à long terme, doivent être pris en compte. L’essentiel est que l’horizon temporel couvre la période nécessaire afin de capturer tous les coûts et conséquences, ainsi que les bénéfices du sujet d’étude. Dans ce projet, l’horizon temporel de cette analyse de coût est la durée d’hospitalisation pour un premier événement d’IM. Cette période permet de répondre à l’objectif de l’étude.
1.2.3.2 Perspectives
Lors de la conduite d’une étude à caractère économique, il est nécessaire de déterminer la perspective à utiliser. Celle-ci permet de définir quels coûts et conséquences seront nécessaires d’être couverts par l’étude. Il existe plusieurs perspectives différentes, mais trois d’entre elles sont plus souvent retrouvées dans la littérature; celle du patient, celle du système de santé et la perspective sociétale (47). Ces perspectives varient selon les législations particulières à chaque pays. Comme son nom l’indique, la perspective économique du patient fait référence aux coûts encourus et pris en charge par le patient, pour ses soins de santé. Elle prend en compte les frais encourus par le patient lui-même afin de bénéficier de soins de santé. Les études en économie de la santé se limitent rarement à la perspective du patient quoique
14
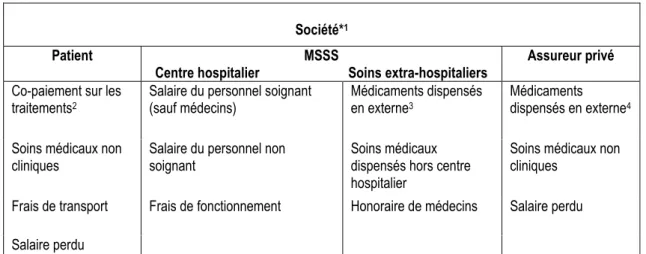
les frais encourus par celui-ci ne soient pas négligeables. Ces coûts sont variables, personnels à chaque individu et difficiles à capturer de manière macroéconomique, puisqu’ils ne sont pas archivés de manière systématique et nécessitent généralement de questionner directement les individus à ce sujet. La perspective du système de santé fait référence à tous les coûts et frais pris en charge par les gouvernements fédéraux et provinciaux. Au Canada, la perspective du système de santé est vaste en raison de l’étendue du rôle de l’état dans la gestion des services de soins de santé. La plupart des frais de soins de santé sont couverts par l’assurance maladie universelle offerte aux résidents canadiens. Au Québec, on fait référence aux coûts des ressources en soins de santé pris en charge par le ministère de la Santé et des Services sociaux (MSSS). Dans un cadre plus englobant, la perspective économique sociétale englobe tous les coûts associés à la prise en charge d’une maladie; ceux du patient, ceux du MSSS et ceux défrayés par les assurances privées. De plus, la perspective sociétale se doit de prendre en compte les coûts indirects, encourus par la perte de productivité reliée au travail, ceux-ci seront discutés ci-dessous.
La raison majeure de l’importance de déterminer une perspective lorsqu’une analyse de coût est entreprise est qu’un élément peut être un coût selon une perspective, mais pas selon une autre. La perspective économique utilisée permet de poser le périmètre de l’ensemble des catégories de coûts qui devront être inclus dans l’étude, selon leurs disponibilités. Par exemple, les frais de transport pris en charge par un patient pour avoir accès à un soin de santé sont un coût nécessaire à inclure lorsque la perspective adoptée est celle du patient, ou encore la perspective sociétale. Lorsque la perspective du système de santé est adoptée, il ne s’agit pas d’un coût à inclure dans l’analyse. Le tableau 2 fournit un rappel de différentes perspectives ainsi que des exemples de catégories de coûts incluses par celles-ci.
Tableau 2: Perspectives économiques en santé
Société*1
Patient MSSS
Centre hospitalier Soins extra-hospitaliers Assureur privé Co-paiement sur les
traitements2
Salaire du personnel soignant
(sauf médecins) Médicaments dispensés en externe3
Médicaments dispensés en externe4
Soins médicaux non
cliniques Salaire du personnel non soignant Soins médicaux dispensés hors centre hospitalier
Soins médicaux non cliniques
Frais de transport Frais de fonctionnement Honoraire de médecins Salaire perdu Salaire perdu
* Autorisation de reproduction accordée par Jason Robert Guertin, tableau tiré du cours Évaluation économique en santé : théories et application, SAP-7017, hiver 2019.
MSSS : Ministère de la Santé et des Services sociaux. 1. Inclus tous les coûts engendrés.
2. La liste d’items inclus dans chaque catégorie n’est pas exhaustive, elle est donnée à tire indicative. 3. Si assurance au public (moins le co-paiement fait par le patient).
15
1.2.3.3 Type de coûts
Tel que discuté préalablement, l’analyse poursuivie doit déterminer quels coûts doivent être comptabilisés et le niveau de précision nécessaire. D’autre part, il est nécessaire de discuter des types de coûts rencontrés. Il existe trois types de coûts en économie en santé (47). Les coûts directs seront ceux qui seront estimés dans ce projet d’étude. Ils font référence aux coûts spécifiques des ressources utilisées par les soins de santé, soit la valeur économique des ressources utilisées dans le traitement des individus. Dans la littérature, les coûts directs sont parfois séparés en deux sous-catégories : cliniques ou non cliniques. Les coûts directs cliniques sont ceux utilisés de manière spécifique aux ressources utilisées par l’événement de santé et les coûts directs non cliniques réfèrent aux coûts nécessaires pour avoir accès aux soins de santé. Des exemples de coût non clinique sont les frais de stationnement et les frais de transport interhospitalier. La seconde catégorie de coûts est celle des coûts indirects. Ils représentent l’aspect économique de la maladie par l’individu en regard des pertes de revenus encourus. Les coûts indirects sont souvent associés àla perte de productivité au travail engendrée par un problème de santé. Une autre composante des coûts indirects réfère au concept que tout le temps d’un individu est monnayable. Ainsi la valeur du temps durant lequel, en raison de la maladie, un individu ne peut s'adonner à ses activités usuelles a également une valeur à laquelle on peut attribuer un prix. Lorsqu'une étude utilise la perspective sociétale, il est important de prendre en compte les coûts indirects associés à cette perspective. Puisque l'on s'intéresse au fardeau économique d'une maladie sur la société, il est nécessaire de prendre en considération tous les coûts engendrés par celle-ci. Les coûts indirects associés à la perte de productivité, p. ex., pertes de salaire, prestations d’assurance chômage ou prestations d’invalidité représentent un aspect économique important à considérer dans le cadre d’une étude avec une perspective sociétale. Si les coûts indirects ne sont pas rapportés, il s’agit d’une limitation majeure de l’étude. Les coûts intangibles comme son nom l’indique sont difficiles à comptabiliser. Ils regroupent l’ensemble de conséquences négatives vécues à la suite d’une maladie. Les coûts intangibles ont tendance à être subjectifs et personnel à chacun. Il est difficile de leur attribuer une valeur, car ils sont souvent impondérables, par exemple : la douleur.
1.2.3.4 Contexte temporel des coûts
Le coût d’un soin aujourd’hui est différent de celui de demain tout comme il est également différent de celui d’hier. Il est important dans une étude sur les coûts de prendre en compte ce contexte particulier. Idéalement, une analyse de coût doit être entreprise avec une monnaie à valeur constante, selon une année prédéterminée (47). En santé, les études sont souvent rétrospectives ou encore prospectives avec des horizons de temps parfois très long, tel que ce projet de recherche, où la période d’étude s’étend sur 26 ans. Il devient alors primordial d’utiliser une unité de mesure fixe, afin que tous les coûts pris en compte soient rapportés à la même valeur. Des méthodes ont été développées, afin de respecter le postulat de l’année et
16
de la valeur de référence. Afin d’obtenir la valeur courante d’un bien pour lequel on a uniquement le coût passé, il est nécessaire de faire subir à ce coût une inflation. Au Canada, l’utilisation de l’indice de prix à la consommation (IPC) est un outil utile et disponible grâce à la Banque du Canada (50). L’IPC est basé sur l’estimation de l’évolution du coût de la vie au Canada (51). Cet indice représente les variations de prix tel qu’expérimenté par les consommateurs canadiens. En utilisant le coût d’un panier fixe de biens et services, il mesure les variations de prix au fil du temps. Afin de rapporter en valeur courante un prix passé, il faut multiplier un coût par le taux d’inflation correspondant à l’année de référence souhaitée. L’équation 3 décrit la procédure à utiliser.
$ 𝑃𝑎𝑠𝑠é
𝑃𝑜𝑢𝑣𝑜𝑖𝑟 𝑑′𝑎𝑐ℎ𝑎𝑡 𝑝𝑎𝑠𝑠é × 𝑃𝑜𝑢𝑣𝑜𝑖𝑟 𝑑
′𝑎𝑐ℎ𝑎𝑡 𝑎𝑐𝑡𝑢𝑒𝑙 = $ 𝐴𝑐𝑡𝑢𝑒𝑙
Équation 3: Formule permettant d'obtenir une valeur actuelle, selon une valeur passée.
Le contexte s’applique également quand il s’agit d’estimer la valeur d’un bien futur en valeur actuelle, c’est ce qu’on appelle l’actualisation des coûts. Il s’agit du coût de dépréciation comptabilisé dans le futur. La logique du taux d’actualisation suit le concept que les gens préfèrent bénéficier d’un service maintenant que plus tard. L’incertitude dont est fait demain amène les gens à vouloir bénéficier de privilèges dans l’immédiat, plutôt que dans le futur. D’où l’importance en économie en santé d’accorder une dépréciation aux événements futurs. Plus le taux d’actualisation est grand, plus la valeur actuelle d’un coût futur sera faible (47). Au Canada, depuis mars 2017, l’ACMTS recommande un taux d’actualisation de 1,5% par année. Dans le cadre de ce projet, l’utilisation du taux d’inflation sera nécessaire afin de ramener en valeur courante des valeurs passées, mais nous ne ferons pas de projection, donc le taux d’actualisation est seulement discuté, à titre informatif.
1.3. Aspects économiques de l’IM
Les maladies cardiovasculaires sont un problème de santé publique majeur, en plus d’être une source de fardeau économique lourde de conséquences sur les systèmes de santé (52, 53). Au Canada en 2003, 33% de tous les décès étaient imputables aux MCV. Connaître l’impact de ce poids économique et des catégories de coûts les plus onéreuses permet de discerner où il peut s’avérer judicieux d'anticiper des stratégies de contentions de coût en plus de permettre d’anticiper les prévisions budgétaires en santé. Néanmoins, il y a une limite majeure aux prévisions budgétaires en santé, dans ce domaine les tendances peuvent s’avérer trompeuses. Le développement technologique rapide peut apporter des changements majeurs, au niveau de la planification budgétaire. La plupart de ces changements entraînent une hausse des coûts. La situation inverse s'avère rare. Parallèlement au développement technologique à visée thérapeutique, les méthodes d’analyses de coûts reliées à l’IM ont fortement évoluées. Les technologies de l’information et les progrès