Universit6 du Qu6bec
Institut National de la Recherche Scientifique Centre Eau Terre Environnement
DfvELoppEMENT D'uN pRocftf n'oxvDATIoN pHoroflfcrRocATAlyrreuE
INNOVANT UTILISANT DES TILECTRODES NANOSTRUCTUREES DE Ti/TiO2 POUR LE TRAITEMENT DES EFFLUENTS CONTAMINNS P.tN DES RfSIDUS MfDICAMENTEUX
Par Rimeh DAGHRIR
Thdse pr6sent6e pour l'obtention du grade de philosophiae doctor (Ph.D.) en sciences de I'eau
Jury d'6valuation Examinateur externe Examinateur externe Examinateur interne Directeur de Recherche Co-directeurs de Recherche Trong-On Do Universit6 Laval Manuel J. Rodriguez Universit6 Laval Satinder Kaur Brar
INRS- ETE Patrick Drogui INRS-ETE My Ali El Khakani INRS-EMT Didier Robert Universit6 De Lorraine
REMERCIEMENTS
Ce travail a 6td effectu6 au Laboratoire d'Electro-technologies Environnementales et Proc6d6s
Oxydatifs (LEEPO) de I'INRS-ETE. Je tiens dr exprimer, en premier lieu, ir mon directeur de
recherche, Monsieur le Professeur Patrick Drogui, ma profonde gratitude et mes
remerciements les plus sincdres pour son infaillible et stimulant encadrement, pour son
inestimable aide et ses conseils pr6cieux. Je ne peux ignorer ses qualit6s humaines et ne pas
6tre reconnaissante au savoir qu'il m'a prodigud, la confiance qu'il m'a accord6e et le grand
soutien moral apport6 de sa part grdce d quoi j'ai pu accomplir mon travail.
Je tiens aussi d t6moigner mes vifs remerciements au professeur My Ali El-Khakani qui a eu
l'amabilite de bien vouloir m'accueillir au sein de son 6quipe de recherche d I'INRS-EMT
pour r6aliser la majeure partie des exp6riences sur le simulateur solaire. Ma reconnaissance et
mes remerciements pour sa disponibilit6, son soutien, ses conseils judicieux, mais aussi pour la confiance qu'il m'a accordde au cours de ces ann6es de thdse.
Je remercie 6norm6ment, Monsieur le Professeur Didier Robert, pour ses pr6cieux conseils et
sa disponibilitd, mais aussi pour le grand interdt qu'il a portd d ce travail.
Je suis particulidrement reconnaissante et honor6e de l'int6r6t qu'ont port6 d cette thdse en
acceptant d'en 6tre les rapporteurs, Messieurs les Professeurs Trong-On Do de l'Universitd
Laval, Manuel J. Rodriguez de I'Universit6 Laval et Madame le Professeur Satinder Kaur
Brar de I'INRS-ETE.
Je remercie vivement l'ensemble des membres du LEEPO pour leur aide pr6cieuse lors de
mes travaux de recherche. Je remercie 6galement celles et ceux qui ont tant fait pour moi: Dr
Brahima Seyhi pour son pr6cieux coup de main et ses conseils judicieux, Dr Lea Rosine
Je n'oublie pas de citer mes trois stagiaires : Aicha Dimboukou-Mpira, Asmaa Errachidi et
Lorene Igounet pour leur contribution, leur investissement et leur collaboration dans ce projet
de recherche.
Je suis particuli6rement reconnaissante envers le personnel des laboratoires de I'INRS-ETE
Mesdames et Messieurs: St6phane Pr6mont, Lise Rancourt, Pauline Fournier, Jean-Frangois
Dutil, Stephane Moise et Julie Perreault pour leur expertise et leurs conseils techniques, leur pr6sence et leur aide.
Tous mes respects et sincdres remerciements i tous les professeurs de I'INRS-ETE pour la qualit6 de la formation qu'ils m'ont fournis tout au long de mon cursus universitaire d
I'TNRS-ETE.
Ma gratitude s'adresse aussi d mes coll6gues de I'INRS-ETE pour leurs conseils, leurs
encouragements et leur aide inestimable.
Enfin, si j'ai r6sist6 durant ces anndes d'6tudes, avec des hauts et des bas, c'est bien grdce d
mes proches, qui ont 6t6 constamment d mes c6t6s. Mes pens6es vont tout particulidrement d papa et maman, qui ont toujours su m'entourer de leur affection et soutenu dans la rdalisation
de mes prdets. Je vous remercie pour votre patience, votre compr6hension et votre grande
confiance. Un grand merci d mes deux frdres, d ma belle scur et d ma nidce pour leur soutien
dans les moments difficiles, leurs conseils, les 6motions partagdes et leur pr6sence. Cette
thdse, aboutissement de longues anndes d'6tudes, je la dois beaucoup d mes deux fr6res et d
mes parents exceptionnels avec qui j'ai vdcu dans un climat toujours serein, d l'abri de tous
soucis affectifs. Il m'est impossible de trouver les mots pour dire d quel point je suis fidre
d'eux, et d quel point je les aime.
Je suis incapable de terminer ceffe liste de remerciement sans exprimer mon 6stimation du
Kim Huong, Ahmadi Kingumbi, Shedly Baya, Sheyma Bourourou et Magdouli Sarra. Merci
d'avoir souvent penser d moi et i mon bonheur, merci pour les ann6es de soutien, merci pour
vos encouragements. Je garderai le souvenir de votre sincdre amiti6.
AVANT.PROPOS
L'objectif principal de ce projet de thdse est de d6velopper et optimiser un proc6d6
d'oxydation photo6lectrocatalytique utilisant une dlectrode nanostructurde de Ti/TiO2 pour le
traitement d'effluents contaminds par des micropolluants organiques r6fractaires tels que la
chlorot6tracycline et la carbamazlpine. Le d6veloppement d'un procddd d'oxydation
photo6lectrocatalytique mettant en synergie les proc6d6s 6lectrochimiques et les techniques
photocatalytiques pourrait constituer une avenue potentielle pour le traitement d grande
6chelle des compos6s organiques persistants. Cette 6tude se compose de dix chapitres.
Le premier chapitre correspond d la synthdse de ce travail, laquelle comprend la revue de
litt6rature relative d la probl6matique des polluants organiques r6fractaires et des diff6rents proc6d6s de traitement existant afin d'y rem6dier, ainsi que les objectifs et la d6marche
m6thodologique employ6e et, enfin un bilan g6n6ral des r6sultats obtenus.
Parmi tous les contaminants 6mergents refractaires ddtectds dans l'environnement, les rdsidus
m6dicamenteux de type antibiotique sont souvent cit6s parmi les compos6s les plus probl6matiques. De ce point de vue, le second chapitre traite de la pr6sence des t6tracyclines
dans les cours d'eaux et de leur devenir dans I'environnement, lequel a fait I'objet d'un article
synthdse publi6 dans Environmental Chemistry Letters, DOI 10.1007/sl031l-013-0404-8:
Rimeh Daghrir, Patrick Drogui (2013) Tetracycline antibiotics in the environment: a
review.
Vue les exigences de plus en plus strictes afin d'assurer une bonne gestion des eaux
contamin6es par des r6sidus medicamenteux, les spdcialistes s'orientent vers la recherche de
technologies de traitement plus avanc6es. C'est dans cette optique que la technique de
photo6lectrocatalyse a 6t6 propos6e afin d'am6liorer I'efficacit6 6puratoire lors du traitement
photo6lectrocatalytique et ses principales applications environnementales, lequel a fait
dgalement l'objet d'un article synthdse publi6 dans Journal of photochemistry and
photobiologt A : Chemistry 238:41-52: Rimeh Daghrir, Patrick Drogui, Didier Robert
(2012) Photoelectrocatalytic technologies for environmental applications.
En tenant compte de ces propri6t6s physico-chimiques, le TiOz est le photocatalyseur le plus
souvent utilisd comme photoanode dans un procdd6 d'oxydation photo6lectrocatalytique. Il a
une bande interdite de 3.2 eV et est capable d'absorber les photons UV. Le d6veloppement de
telles photoanodes qui absorberaient dans la partie visible du spectre solaire peut constituer un
avantage majeur pour pouvoir appliquer le procddd d'oxydation photodlectrocatalytique d
l'6chelle rdelle. Ainsi, le quatridme chapitre pr6sente les diff6rentes approches utilis6es pour
6tendre la r6ponse spectrale de TiOz vers la r6gion du visible ainsi que ses differentes
applications environmentales. Cette synthdse bibliographique a fait l'objet d'un article publid
dans Industrial & Engineering Chemistry Research, 52: 3581-3599: Rimeh Daghrir, Patrick
Drogui, Didier Robert (2013) modified TiOz for environmental photocatalytic applications : a review.
Le TiOz utilis6 comme photoanode dans un tel procddd d'oxydation photo6lectrocatalytique a
6t6 synth6tis6 et int6gr6 dans une cellule photo6lectrocatalytique afin d'dvaluer leur capacitd
de production d'6spdces oxydantes ndcessaires d l'oxydation des micropolluants rdfrcataires.
La mise en 6vidence de ces 6sp6ces oxyg6n6es r6actives a 6t6 r6alis6e en utilisant une
m6thode indirecte utilisant le p- nitrosodimethylaniline. Le cinquidme chapitre correspond d
l'6tude portant sur le blanchissement du p- nitrosodimethylaniline par oxydation photo6lectrocatalytique utilisant le Ti/TiO2 nanostructur6 comme photoanode. Ce chapitre a
fait I'objet d'un article publi6 dans Journal of Applied Electrochemistry 43 (4) : 467-479 :
Rimeh Daghrir, Patrick Drogui, Ibrahima Ka, My Ali El Khakani and Didier Robert
(2013) Photoelectrocatalytic bleaching of p-nitrosodimethylaniline using TiiTiOz
nanostructured electrodes deposited by means of a pulsed laser deposition process.
Ces rdsultats pr6c6dents ont permi5 d'exploiter ult6rieurement le procdd6 d'oxydation
photodlectrocatalytique pour le traitement d'une solution synth6tique contaminde par un
polluant organique persistant tel que la chlortetracycline. L'6tude relative d la ddgradation du
chlorotdtracycline par un procddd d'oxydation photodlectrocatalytique utilisant une 6lectrode
nanostructurde pr6par6e par la m6thode de d6position par ablation laser est pr6sent6e en d6tail
dans le sixidme chapitre. Les r6sultats issus de ces travaux ont 6t6 valorisds sous forme
d'article publid dans Journal of Hazardous Materials 199-200: 15-24: Rimeh Daghriro
Patrick Drogui, Ibrahima Ka, My Ali El Khakani Q0l2) Photoelectrocatalytic
degradation of chlortetracycline using Ti/TiOz nanostructured electrodes deposited by
means of a Pulsed Laser Deposition process.
L'dfficacitd d'oxydation photo6lectrocatalytique de la chlortetracycline sous radiation UV
pourrait 6tre am6lior6 en utilisant une cathode appropride pour la g6n6ration simulatn6e d'un
accepteur d'dlectron tel que le HzOz. De ce point de vue, le septidme chapitre porte sur la
d6gradation photo6lectrocatalytique du chlorot6tracycline en utilisant le TilTiOz comme photoanode avec une production simultande du peroxyde d'hydrogdne. Cette partie des
travaux a 6t6 publi6 dans Electrochimica Acta,87: 18-31 : Rimeh Daghrir, Patrick Drogui,
My Ali El Khakani (2013) Photoelectrocatalytic oxidation of chlortetracycline using
Ti/TiO2 photo anode with simultaneous H2O2 production.
L'exploitation des raditaions solaires lors de l'application du procddd d'oxydation
photo6lectrocatalytique constitue un avantage majeur qui pourrait contribuer dr r6duire les
c6uts du traitement. De ce point de vue, le huitidme chapitre traite de l'oxydation
photo6lectrocatalytique du chlorot6tracycline sous radiation solaire en utilisant le TiO2
nanostructur6 dopd dl'azote. Cette 6tude a fait I'objet d'un article acceptf dans la revle Water
Research WRI0I66 (accept6 le 10 Septembre 2013) : Rimeh Daghrir, Patrick Drogui,
Nazar Delegan, My Ali El Khakani (2013), Electrochemical degradation of
chlortetracycline using N-doped Ti/TiOz photoanode under sunlight irradiations.
En tenant compte des rdsultats du huitidme chapitre, les meilleures conditions de traitement
ont 6t6 par la suite appliqu6es sur un effluent r6el de type municipal artifrciellement
contamind par la chlortetracycline. Les r6sultats de cette 6tude sont pr6sent6s dans le
neuvidme chapitre qui porte sur I'application du proc6dd d'oxydation photo6lectrocatalytique pour le traitement tertiaire d'un effluent de type municipal artificiellement contamind par la
chlorot6tracycline. Cette 6tude a fait I'objet d'un article publi6 dans la revre Science of the
total Environment, 466-467 : 300-305 : Rimeh Daghrir, Patrick Droguio Nazar Delegan,
My Ali El Khakani Q0l4) Removal of chlortetracycline from spiked municipal
wastewater using a photoelectrocatalytic process under sunlight irradiations.
Dans l'optique d'6tendre son spectre d'activitd, le procddd photodlectrocatalytique a 6tE t1st6 pour la ddgrdation d'une autre polluant de type pharmaceutique tel que la carbamaz5pine
couramment rencontr6e dans les eaux r6siduaires. Les r6sultats de cette 6tude ont 6t6
synth6tis6s dans le dixidme chapitre. Ce chapitre fait rdference d l'6tude sur la d6gradation d'un antid6pressif, carbamazlpine par le proc6d6 d'oxydation photodlectrocatalytique, lequel
a 6t6 optimis6 par la m6thodologie des plans d'expdriences en utilisant l'6lectrode Ti/liOz
nanostructurd comme photoanode. Ces rdsultats ont fait l'objet d'un article accept6 dans la
revue Chemosphere CHEM 14256 (accept6le 17 Septembre2013): Rimeh Daghrir, Patrick
Drogui, Aicha Dimboukou-Mpira, My Ali El Khakani (2013) Photoelectrocatalytic
degradation of carbamazepine using Ti/TiOz nanostructured electrodes deposited by
means of a pulsed Laser deposition process.
RESUME
Depuis un certain nombre d'anndes, une attention scientifique particulidre est portde sur
l'dmergence et le devenir dans I'environnement de composds organiques persistants d'origine
urbaine et industrielle. Ces compos6s ne sont pas g6n6ralement 6limin6s dans les filidres
conventionnelles de traitement des eaux usdes et s'accumulent ainsi dans le milieu rdcepteur.
Ils provoquent des bouleversements significatifs sur la faune et la flore ainsi que sur la sant6
humaine. Plusieurs espdces animales et v6g6tales sont en voie de disparition d cause des
composds nocifs prdsents dans l'environnement. Au cours de ces demidres ann6es, de
nombreuses technologies ont 6td d6veloppdes pour faire face d ces polluants d'intdr6t
6mergent. De ce point de vue, les procddds d'oxydation photo6lectrocatalytique sont particulidrement intdressants. L'int6r0t de ces techniques r6side dans leur aspect non polluant
et leur facilit6 d' automatisation.
L'objectif de ce projet est d'dvaluer I'efficacitd de l'oxydation photo6lectrocatalytique
utilisant une 6lectrode nanostrrctur6e de TilTiOz dans le traitement des effluents contenant
des compos6s organiques persistants tel que la chlorotetracycline et la carbam azfipine. Le
ddveloppement d'un proc6dd d'oxydation photo6lectrocatalytique mettant en synergie les proc6d6s 6lectrochimiques et les techniques photocatalytiques pourrait constituer une avenue
potentielle de traitement des compos6s organiques persistants. Le proc6d6 photocatalytique
est une technologie basde sur I'irradiation d'un catalyseur, en g6n6ral un semi-conducteur
(TiO2) qui peut 6tre photoexcit6 pour former des sites 6lectro-donneurs (h-) et des sites
6lectro-accepteurs d'dlectrons (e-) induisant ainsi des rdactions d'oxydo-r6duction.
L'application des radiations UV ayant une dnergie supdrieure au gap d'dnergie entre la bande
de valence et la bande de conduction favorise le passage des 6lectrons de la bande de valence
d la bande de conduction crdant ainsi des pairs d'6lectron-trou (e-lh-). La dur6e de vie de ces paires d'6lectron-trous (e-Ar*) est de l'ordre de nanoseconde. Le potentiel externe appliqu6
dans un proc6d6 photo6lectrocatalytique constitue un facteur cl6 puisqu'il est capable de
retarder la recombinaison d'dlectron-trou e-lh- photog6n6r6. Cet effet de synergie permet de
produire in situ des espdces oxyg6n6es r6actives trds puissantes telles que les radicaux
hydroxyles ayant la capacitl de d6grader efficacement les composds organiques jusqu'd sa
min6ralisation. Le TiOz est le semi-conducteur le plus utilis6 comme photoanode dans les
r6actions photocatalytiques. N6anmoins, cette activit6 photo-catalytique de TiOz se limite
souvent d l'utilisation des rayonnements ultra-violets (1" < 384 nm) qui repr6sentent seulement
3 it 5% des radiations solaires. L'exploitation des radiations visibles en prdsence de TiOz dop6
d I'azote serait une alternative pour l'application du procddd d'oxydation photo6lectrocatalytique d grande 6chelle. Le mat6riel photodlectrocatalytique utilis6 afin de
r6aliser cette 6tude est composd d'une cellule photo6lectrocatalytique d 6lectrode
rectangulaire de TilTiOz (dop6 ou non-dop6 dl'azote) et alimentd par des radiations UV (ou
des radiations visibles), ce qui a permis d l'dchelle du laboratoire, d'dvaluer et d'optimiser le proc6d6.
Les travaux pr6liminaires ont d'abord consistd d dvaluer le potentiel d'oxydation d'un proc6dd photo6lectrocatalytique. Pour ce faire, la p-nitrosodimethylaniline (RNO) a 6t6 utilis6 pour
dvaluer la capacitl de production des espdces oxyg6n6es r6actives telles que l'ozone et les
radicaux hydroxyles. Un taux de blanchissement de RNO allant jusqu'ir22.6 10-3 mM hl a 6t6
obtenu en appliquant une intensit6 de courant de 0.1 A sous irradiation UV-254 nm et en
utilisant la forme anatase de TiOz comme photoanode et le carbone vitreux ir la cathode. Ces
r6sultats permettront ultdrieurement d'exploiter cette technique pour le traitement d'une
solution synthetique contamin6e par un polluant organique persistant tel que la
chlorot6tracycline, puis pour le traitement des effluents r6els artificiellement contamin6s par
la chlorot6tracycline. A titre de comparaison, la carbamazepine aEt6 6tudi6. L'6valuation de
us6es synth6tiques contamin6es par la CTC a 6td bas6e sur une s6rie d'optimisation de
certains paramdtres op6rationnels. Les diff6rents paramdtres inh6rents d ce proc6d6 tels que
l'intensit6 de courant, le temps de traitement, la structure cristallographique de TiOz, le type
de cathode, le pH et la concentration initiale du polluant ont 6t6 6valu6es en termes
d'efficacitd de d6gradation du polluant et de co0t dnergdtique. Le recours d l'utilisation d'un
logiciel de plan d'exp6rience en premier lieu a permis de d6crire les diff6rents processus de
ddgradation et d'dvaluer les effets propres d chaque paramdtres ainsi que les interactions
6ventuelles. Cette 6tude a permis 6galement d partir des moddles math6matiques issus du plan
d'exp6rience de ddterminer les conditions opdratoires optimales. L'6tude de la d6gradation de
la chlorot6tracycline par un procddd d'oxydation photo6lectrocatalytique a permis de mettre
en dvidence I'effet de chaque paramdtre et de mieux comprendre les m6canismes de
d6gradation mis en jeu. Des taux de d6gradation de la chlorot6tracycline de 99.6Yo et des taux
d'6limination de 92.5Yofr.26% et de 90.3o/o+l.loh de carbone organique total et d'azote totale
ont respectivement 6t6 enregistr6s, aprds 180 min du temps de traitement, sous radiation
visible, en imposant une intensit6 de 0.6 A et en utilisant le TiOz dopd d 3.4 at.%o d'azote et en prdsence d'une cathode de carbone vitreux. L'analyse des sous-produits de d6gradation de la
chlorotdtracycline a permis de proposer un mdcanisme rdactionnel de d6gradation. Une fois
les conditions optimales de ddgradation du chlorot6tracycline d6termin6es, celles-ci ont 6t6
appliqudes pour le traitement d'effluents rdels issus de station d'6puration et artificiellement
contamin6s par ce polluant. Un rendement de degradation totale de la chlorot6tracycline (99.1%+0.1%) a 6td enregistr6 aprds 180 min du traitement photo6lectrocatalytique utilisant le
TiO2 dopd dl'azote et une intensit6 de courant de 0.6 A. Des taux d'dlimination de 85.4o/o
+3.6oh, 87.4%+3.I% ainsi que de 55.7% + 2904 ont respectivement 6t6 enregistr6s pour le
carbone organique total, pour l'azote total et pour l'azote ammoniacal. Une meilleure
efficacit6 de d6sinfection (94.8%; abatement >1.2-log units) a 6t6 6galement obtenue dans les
conditions optimales du traitement d'oxydation photodlectrocatalltique. Le co0t de traitement
TABLE DES MATIERES
t . SYNTHESE. ...3
Introduction..
Synthdse bibliographigue... ...4 Propri6t6s physico-chimiques et impacts environnementaux des eaux us6es r6siduaires.... ...4 Polluants organiques d'int6r€t 6mergent retrouv6s dans les eaux us6es r6siduaires ...7 Stratdgies de traitement des eaux r6siduaires contaminees par les r6sidus m6dicamenteux de type
a n t i b i o t i q u e . . . . . . 1 7 P r o c d d 6 d ' o x y d a t i o n P E C . . . . . . 3 5 Hypothdses de travail et objectifs de recherche ...5-t I . I 1 . 2 r . 2 . 1 t.2.2 t . 2 . 3 1 . 3 t . 2 . 4 1.4 Objectifs de recherche. ...56 1 . 4 . 1 O b j e c t i f G 1 o b a 1 e . . . . . . 5 6 1 . 4 . 2 O b j e c t i f s s p 6 c i h q u e s . . . . . . . 5 6 1.5 Originalitd de I'dtude ...57 1 . 6 D d m a r c h e m d t h o d o l o g i q u e . . . . . . 5 8 1.6.1 Polluants
1.6.2 Pr6paration de solutions synth6tiques ...62 1.6.3 Echantillonnage et caracterisation des eaux rdelles ...62 1.6.4 Pr6paration de la photoanode TilTiO2... ...65 1 . 6 ' 5 P r 6 p a r a t i o n d e 1 a p h o t o a n o d e T i / T i o : d o p 6 i r 1 , a z o t e
1.6.6 Pr6paration des 6lectrodes de carbone amorphe... ...67 1.6.7 Montage et caract6ristiques des cellules d'oxydation PEC... ...68
1.6.8 Fonctionnement de I'unit6 expdrimentale ...70
1.6.9 M6thodologie de plan d'exp6rience. ...73
1 . 6 . 1 0 M 6 t h o d e s a n a 1 y i q u e s . . . . . . 7 4 1.7 Principaux nisultats et discussion g'lndra\e... ...81
1.7.1 Production in-situ des EORs: Application de la m6thode de blanchissement du RNO (Chapitre 5) 8 l 1.7.2 Oxydation PEC du CTC utilisant une 6lectrode nanostructu6e de TilTiO2 comme
photo-anode prepar6e par la m6thode de d6position par ablation laser: Application de la m6thodologie de plan d'exp6riences (Chapitre 6)... ...82 1.7.3 Oxydation PEC du CTC utilisant une 6lectrode nanostructur6e de Ti/TiO2 comme photo-anode
avec une production simultanee duH2O2 (Chapitre 7) ... ...84 1.1 .4 D6gradation PEC du CTC utilisant une photoanode nanostructur6e de TilTiOz dop6 ir l'azote
( C h a p i t r e 8 ) . . . . . . 8 8 1.7.5 Traitement des eaux us6es municipales contamin6es par la CTC en utilisant un proc6dd PEC sous
irradiation solaire (Chapitre 9). ... ...90 1.7 .6 Mdthodologie de plans d'expdriences appliqu6e d I'oxydation PEC du CBZ utilisant une dlectrode
nano-structurde de Ti/TiO2 comme photo-anode (Chapitre l0)... ...92 1 . 8 C o n c l w i o n s G d n d r a l e s . . . . . . - . . . 9 5 1 . 9
r.t0
CHAPITRE 2 ... 129
7 TETRACYCLINE ANTIBIOTICS IN THE ENVIRONMENT. A REVIEW...13I
Abstract ... I 31
2 . 1 2.2
z . J
Keywords...
Worldwide usage of tetracycline antibiotics... lntroduction
2 . 4
XlV
2 . 5 2 . 6
Occurrence of tetracycline antibiotics in the environment... ...140
2.6.1 Effects of tetracycline antibiotics on aquatic species... ...146
2.6.2 Effects of tetracycline antibiotics on terrestrial organisms ...147
2.6.3 Estrogenic effects of tetracycline antibiotics ...148
2.7 Treatment of tetracycline antibiotics in waters ...149
2 . 7 . 1 M e m b r a n e p r o c e s s e s . . . . . . 1 5 0 2.7.2 Adsorption processes ...150
2.7.3 Photochemical processes... ...151
2.7.4 Electrochemical process... ...154
2.7.5 Photocatalytic and photoelectrocatalytic processes ...155
2 . 1 1 CHAPITRE 3... 3 . PHOTOELECTROCATALYTIC TECHNOLOGIES FOR ENVIRONMENTAL APPLTCATIONS ... 3 . 1 3 . 2 K e y w o r d s . . . . . . 1 8 9 3 . 3 3.4 Mechanism of the photoelectrocatalytic process... ....-,...192
3.5 Parameters affecting the photoelectrocatalytic process... ...197
3.5.1 Effect of extemal potential applied on TiOz or effect of current intensity... ...197
189
3.5.2 Effect of light intensity ...199
3 . 5 . 3 3.5.4 Effect of dissolved oxygen... ...201
3.5.5 Effect ofelectrolytes... ...203
3.5.6 Effect of counter electrode (or cathode electrode)...:... ...204
3.5.7 Effect of temperature... ...204
3.5.8 Effect of mass transfer ...205
3.6 TiO2 electrodes: characteristics and specificities ... ...206
3.6.1 Preparation of TiO2 electrodes... ...206
3.6.2 Characteristics and specificities of TiO2 electrodes... ...207
3.6.3 UV radiation of TiO2 electrodes ...212
3 . 1 2 4. MODIFIED TIO' FOR ENVIRONMENTAL PHOTOCATALYTIC APPLICATIONS: A REVIEW... 3 . 7 3.8 3 . 9 4 . 1 ,1 ) 4.3 4.4 Photoelectrocatalytic reactors ...2 I 4 Application of photoelectrocatalytic processes (PECPs) ...218
Current andfuture development of PECPs ...224
4 . 5 D o p i n g T i O 2 . . . . . . 2 5 3
4.5.1 Cations doping of TiO2 ...253
4.5.2 Drawbacks of cations doping of titanium dioxide... ...261
4.5.3 Anions doped TiO2.... ...262
4.6 Coupled semiconductor photocatalysts... ...270
4.6.1 Photosenitization of TiO2 by M*S, nanoparticles ...273
4.6.2 Coupling TiO2 by M*O, nanoparticles... ...276
4.7 Others photosensitization of TiO2... ...282
4.8 Future trends of TiO2for environmental applicatiolls... ...283
4 . 8 . 1 P r e p a r a t i o n a s p e c t o f T i O 2 . . . . . . 2 8 5 4 . 8 . 2 A p p l i c a t i o n a s p e c t o f T i O 2 . . . . . . 2 8 6 4.8.3 Toxicity aspect... ...289 4.9 4 . 1 0 A c k n o w l e d g m e n t s . . . . . . 2 9 1 4 . 1 1 cHAPITRE 5 ... ...321
PHOTOELECTROCATALYTIC BLEACHING OF P-NITROSODIMETHYLANILINE USING TI/TIO2 NANOSTRUCTURED ELECTRODES DEPOSITED BY MEANS OF A PULSED LASER DEPOSITION PROCESS ...323
5.2 5 . 3 5.4 Mateials andMethods. ...327
5.4.1 Ti/TiO2 electrode preparation ...;...327
5.4.2 Preparation of the synthetic solution... ...328 xvll
5.5.1 Characterisation of the TilTiO, electrode ...332 5 . 5 . 2 B l e a c h i n g o f R N O . . . . . . 3 3 6 5.5.3 Effect of the crystallographic structure... ...340 5.5.4 Effect of external potential.... ...343 5.5.5 Effect of light intensity ...344 5 . 5 . 6
5.5.7 Effect of H2O2 produced at the cathode electrode... ...348 5.5.8 Effect of ozone production.. ...352 5.6
5 . 7 5.8
PHOTOELECTROCATALYTIC DEGRADATION OF' CHLORTETRACYCLINE USING TI/TIO2 NANOSTRUCTURED ELECTRODES DEPOSITED BY MEANS OF A PULSED
LASER DEPOSITION PROCESS ...36s
6.1
6 . 2 K e y w o r d s . . . . . . 3 6 5 6.3
6 . 4 M a t e r i a l s a n d m e t h o d s . . . . . 3 6 8 6.4.1 TiiTiO2 electrode preparation.... ...368 6.4.2 Preparation of the synthetic solution... ...368
6.4.3 Experimental devices ...371
6.4.4 Experimental desigrr... ...372 6 . 4 . 5 A n a l y t i c a l d e t a i l s . . . . . . 3 7 3 6 . 4 . 6 E c o n o m i c a s p e c t . . . . . . 3 7 4
6.5 Results anddiscussion ...374
6.5.1 Characterization of the TiiTiO? electrode ...374 6.5.2 Preliminary investigation of CTC degradation ...376 6.5.3 Effect of the experiment parameters on the CTC degradation using the experimental factorial
(
design methodology ... ...380 6.5.4 Optimization conditions for CTC degradation using central composite design (CCD) methodology
. . . 3 8 6 6.6
6 . 7 6.8
7. PHOTOELECTROCATALYTICOXIDATIONOFCHLORTETRACYCLINEUSING TI/TIO2 PHOTO ANODE WITH SIMULTANEOUS H2O2 PRODUCTION
7.4.6 Analytical techniques... ...414 7 . 4 . 7 E c o n o m i c a s p e c t . . . . . . 4 1 . 6
7.5 Results and discussion ...417
7.5.1 Ch.araclerizalion of the TilTiO, electrode ...417 7.5.2 Characterization of the carbon electrode... ...420 7.5.3 Effect of the Ti/TiO2 crystallographic structure.... ...422 7.5.4 Effect of the cathode material ...-...424 7.5.5 Effect of the initial concentration of CTC ...429 7.5.6 Effect of the initial pH on CTC degradation... ...431 7.5.7 Kinetic study of CTC degradation by PECO process ...435 7.5.8 By-products identification and proposed mechanism of CTC degradation.... ...440 7.5.9 Aquatic toxicity studies... ...443 7.6
7 . 7 7.8
CHAPITRE 8 ....4s3
ELECTROCHEMICAL DEGRADATION OF CHLORTETRACYCLINE USING N-DOPED TI/TIO2 PHOTOANODE UNDER SUNLIGHT IRRADIATIONS ....455
8 . 2 K e y w o r d s . . . . . . 4 5 5 8.3 Introduction..
8 . 4 M a t e r i a l a n d m e t h o d s . . . . . . 4 5 9 8.4.1 N-doped TiO2 Photoanodes preparation ... ...459 8.4.2 Synthetic solution preparation
8.4.3 Photoelectrocatalvtic cell ... ...461 8 . 4 . 4 E x p e r i m e n t a l s e t u p . . . . . . 4 6 1 8.4.5 Experimental procedure ...462 8.4.6 Analytical technique ... ...463 8 . 4 . 7 E c o n o m i c a s p e c t . . . . . . 4 6 4 8.5 Results and Discussion... ...464
8.5.1 Photoanode characterization ...464 8.5.2 Effect ofnitrogen content on the photoelectrocatalytic properties ofN-doped TiO2 photoanodes
. . . 4 6 8 8.5.3 Effect of current intensity ...473 8.5.4 Effect of treatment time ...474 8.5.5 By-products identification and proposed mechanism of CTC degradation... ...477 8.6 Conclusion....
8 . 7 A c k n o w l e d g m e n t s . . . . . . 4 8 1 8.8
9. REMOVAL OF CHLORTETRACYCLINE FROM SPIKED MUNICIPAL WASTEWATER USING A PHOTOELECTROCATALYTIC PROCESS OPERATED UNDER SUNLIGHT
IRRADIATIONS ... ...491 9.1
9 . 2 K e y w o r d s . . . . . . 4 9 1 9.3 Introduction..
9.4 Materials and methods ...493 9.4.1 Preparation of the synthetic solution... ...493 9.4.2 Wastewater CTC-spiking. ...494
9.4.3 Photoelectrocatalytic cell ... ...494 9 . 4 . 4 E x p e r i m e n t a l s e t u p . . . . . . 4 9 5 9.4.5 Experimental procedure... ...496
9.4.6 Analytical technique ...497
9 . 4 . 7
9.5 Results and discussions ...498 9.5.1 Preliminary investigations of CTC degradation... ...498 9.5.2 Photoelectrocatalytic treatment of MWW contaminated by CTC... ...502 9.6
9 . 7 9.8
10. PHOTOELECTROCATALYTICDEGRADATIONOFCARBAMAZEPINEUSINGTI/TIO2 NANOSTRUCTURED ELECTRODES DEPOSITED BY MEANS OF A PULSED LASER
DEPOSTTION PROCESS . . . 5 1 1
10.2 1 0 . 3
1 0 . 4 M a t e r i a l s a n d m e t h o d s . . . . 5 1 5 10.4.1 Preparation of the TilTiO2 electrode ...515 10.4.2 Preparation of the amorphous carbon e1ectrode... ...516 10.4.3 Preparation of the synthetic solutions ...516 1 0 . 4 . 4 E x p e r i m e n t a l d e v i c e s . . . . . . 5 1 7 1 0 . 4 . 5 E x p e r i m e n t a l d e s i g n . . . . . . 5 1 8
10.4.6 Analytical details ...519
10.4.7 Economic aspect ...520 10.5 Results and discussions -...---...520
10.5.1 Characterization of the Ti/TiO' electrode ...520 10.5.2 Characterization of the nanostructured carbon electrode... ...524 10.5.3 Efficacy of the PECO process in removing CBZ using different types of cathode electrodes ...525 10.5.4 Effect of the experiment parameters on the CBZ degradation using the experimental factorial
design methodology ... ...528 10.5.5 Optimization conditions for CBZ degradation using central composite design (CCD) methodology
. . . 5 3 4 10.5.6 By-products formation and proposed mechanism of CBZ degradation... ...539 10.5.7 Kinetics study of CBZ degradation by PECO process... ...541 1 0 . 6
1 0 . 7 A c k n o w l e d g m e n t s . . . . . . 5 4 4 10.8
Tableau 1-1 Tableau 1-2 Tableau 1-3 Tableau 1-4 Tableau 1-5 Tableau 1-6 Tableau 1-7 Tableau 1-8 Tableau 1-9 Tableau 1-10 Tableau 2-l Tableat2-2 Tableau 2-3 TabIeau2-4 Tableau 2-5 Tableau 2-6 Tableau2-7 Tableau 3-1 Tableau 3-2 Tableau 3-3 Tableau 3-4
LISTE DES TABLEAUX
Composition typique des EUD (Bitton, 2005)... ... 6 Structure mol6culaire et caract6ristique de certains produits chimiques. ... 10 Concentrations des antibiotiques ddtectds dans I'environnement... ...14 Les constantes de biod6gradation de cretains antibiotiques dans un systdme de
traitement biologique. ... 19
Performances des POAs pour la d6gradation des antibiotiques ... ...32 Performances des POAs pour la d6gradation des antibiotiques (suite)... 33 Performances des POAs pour la d6gradation des antibiotiques ... ...34 Les semi-conducteurs utilis6s dans un proc6dd PEC ... 35 Charact6ristiques des deux formes cristallographiques de TiOz : Anatase et
R u t i l e . . . 4 8
Propri6t6s physico-chimique des polluants 6tudies... ...62 Chemical properties of tetracycline antibiotics ... ... 137 Variation of the residual concentration of tetracvcline antibiotics with animal
t y p e . . . . . . I 4 4
Removal of tetracycline antibiotics using different treatment processes... 159 Removal of tetracycline antibiotics using different treatment processes... 160 Removal of tetracycline antibiotics using different treatment processes... 161 Removal of tetracycline antibiotics using different treatment processes... ...162 Removal of tetracycline antibiotics using different treatment processes... 163 The role and the effect of UV iradiation and current intensity in
photoelectrocatalylic mechanism ... 193
Redox potential of oxidants used for water treatment... ... 195 Characteristics of the anatase and rutile forms of TiO2... ...209 Removal of different types of organic pollutants in aqueous solutions using
P E C P s . . . 2 2 2
Tableau 3-5 Tableau 4-1 Tableat4-2 Tableau 4-3 Tablea'u4-4 Tableau 5-1 Tableau 6-l Tableat6-2 Tableau 6-3 Tableau 6-4 Tableau 6-5 Tableau 6-6 Tableau6-7 Tableau 7-l TableauT-2 Tableau 7-3 TableauT-4 Tableau 7-5 Tableau 7-6
Removal of dye and microbial pollutants using PECPs... ...223 Commonsemiconductorusedinphoto-catalysisprocess ...248 Removal of organic pollutants in aqueous solution using different tlpe of
cations doped TiO2... ...268
Removal of organic pollutants in aqueous solution using different type of
a n i o n s d o p e d T i O 2 . . . . . . 2 6 9 Removal of organic pollutants in aqueous solution using photosensitization
system(TiO2A4*OyorTiOz/IV1"Sr)... . . ...281
Effect of crystallographic structure on the rate of RNO removal. ...342 Chemical properties of Chlortetracycline hydrochloride. ... 370 Different processes used for degradation of CTC... ...377 Chlortetracycline hydrochloride removal under various experimental
conditions.. ...379
Data for optimization operation: experimental range and levels of
independent process variables.... ... 380
Experimental factorial matrix in the 2a design. . . ... . . .. .. 382 ANOVA results for the response surface quadratic for CTC degradation...39I Determination of optimum operating conditions proposed by Desigu-Expert @ Program Software....
Chemical properties of Chlortetracycline hydrochloride. ... 411 Effect of TiOz phase structure on the removal rate of CTC ...424 Effect of cathode materials on CTC degradation and mineralization... 428 Influence of the initial concentrations of pollutant on the photoelectrocatalytic oxidation of CTC (TilTiO2 (anatase): anode and VC: cathode)... 430
Kinetic parameters for CTC degradation ...437
Toxicity measurements before and after PECO treatment in optimal
conditions.. ...444
Physico-chemical properties of Chlortetracycline hydrochloride... ... 460 Tableau 8-l
Tableau 9-1 Tableau 10-1 Tableau 10-2
Tableau 10-3 Tableau 10-4
Different processes used for CTC degradatron... ... 501
Effect of cathode materials onCBZ degradation ...527
Experimental region and experimental results from Factorial Design matrix
( 2 0 ) . . . . . . s 3 3
Central composite matrix and experimental results .... 536
ANOVA results for CBZ desradation ...537
Figure l-1 Figure l-2 Figure 1-3 Figure 1-4 Figure 1-5 Figure 1-6 Figure 1-7 Figure 1-8 Figure l-9 Figure 1-10 Figure l-11 Figure l-12 Figure l-13 Figure l-14 Figure 1-15 Figure 1-16 Figure 2-1
LISTE DES FIGURES
Source et devenir des rdsidues d'antibiotiques dans l'environnement...21.
Organigramme de diff6rentes techniques pouvant 6tre utilis6es pour l'dlimination des r6sidus d'antibiotiques prdsents dans les effluents
m6dicamenteux. ... ...22
Les r6actions d'oxydordduction qui se produisent d la surface d'un
photocatalyseur. ... ... 31
M6canisme du proc6d6 d'oxydation PEC utilisant le TiO2 comme
p h o t o a n o d e . . . 3 7
R6gion UV pour la photo-activit6e de TiO2... ... 46 Repr6sentation sch6matique de la maille cristalline a) Rutile et b) Anatase...47 Structure sch6matique du niveau d'dnergie de TiOz dopd i l'a2ote... 50 Description schdmatique de la d6marche m6thodologique suivie... 59
Filidre de traitement des eaux us6es de la station d'dpuration de la ville de
Qu6bec (Secteur Est), Canada... ... 64 Description schdmatique de la ddposition d'un rev6tement de TiO2 par
a b l a t i o n 1 a s e r . . . . . . 6 6 Description sch6matique de la technique de pulv6risation magnetron d haute
fr6quence... ...67
Structure sch6matique de la cellule d'oxydation PEC C1 ... 68 Structure sch6matique de la cellule d'oxydation PEC C2... ...69 Structure schdmatique de I'unit6 expdrimentaleU2. ...72 Spectromdtre UV/visible utilisd pour l'analyse de la CTC et laCBZ. ...77 Chromatographie liquide coupl6e ir deux spectromdtries de masses utilis6es
pour I'analyse du CTC et du CBZ.. ... 78
Variation of the total amounts (tons) of tetracycline antibiotics used for
veterinary purposes around the world. ... t40
Figwe2-2 Figure 3-1 Figure 3-2 Figure 3-3 Figure 3-4 Figure 3-5 Figure 4-1 Figwe 4-2 Figure 4-3 Figure 4-4 Figure 4-5 Figure 4-6 Figwe 4-7 Figure 5-1 Figure 5-2 Figure 5-3 Figure 5-4 Figure 5-5
Possible sources and pathways for the occurrence of TCAs in the
environment ...145
Mechanism of photoelectrocatalytic process using TiO2 photocatalyst and the reactions that occur at the surface. ... ... 197 Coupling of two different semiconductor configurations. ... ...212 Photoreactor equipped with t'wo electrodes: TtlTiO2 as anode and platinum electrode as cathode (adapted from Li et a1.,2007) .... 214 Photoreactor equipped with three electrodes used for photoelectrocatalylic
oxidation process (adapted from Xie and Li (2006). ...215 Rectangular qtariz photoreacteur used for photoelectrocatalytic process
(adapted from Quan et a1.,2007) ...216
Band gap and redox potential for different semiconductors using the normal
hydrogen electrode (NHE)... ...250
UV region for photoactivity of TiO2... ...252 Schematic energy level of iron doping TiOz. ... ....259 Schematic energy level of nitrogen doping TiO2... ...265 Vectorial transfer of electrons-holes (e-lh-) in coupled semiconductor system.272 TiOz/SnOz photocatalyst configuration... ...279 Future trends of modifred TiOz for environmental applications... ...284 Schematic diagram of the photoelectrocatalytic reactor: (1) DC power supply (2) qtartz window (3) UV lamp (4) photometer (5) photoanode (6) cathode (7) stirring bar (8) magnetic stirrer... ... 330 SEM views of PLD TiOz films deposited on Si at different deposition
t e m p e r a t u r e s . . . . . . 3 3 2 SEM views of PLD TiO2 films deposited on silicon. ... 333 X-ray diffraction patterns of TiO2 film coated at (a) 600"C and 400oC; (b) on
Si substrates and; (c) Ti grids. ... 335
Bleaching of RNO using different processes ...337
Figure 5-6 Figure 5-7 Figure 5-8 Figure 5-9 Figure 5-10 Figure 6-1 Figure 6-2 Figure 6-3 Figure 6-4 Figure 6-5 Figure 6-6 Figore 6-7 Figure 7-1 Figure 7-2
Kinetic studies of bleaching of RNO using (a) DP (b) PC (c) EO and (d)
PECO processes. ... 340
Bleaching of RNO using the PECO process under different current intensities (Effect of extemal potential) (at254nm and using TilTiO2 anatase). ...344
Bleaching of RNO using the PECO process (at 0.1 A and using Ti/TiO2
anatase) under different light intensities... ...346 Bleaching of RNO using the PECO process (at 0.1 A under 254 nm using
TlTiO2 anatase) at different pH... ... 348 H2O2 production during electrolysis at 0.1 A and under 254 nm. ...352
Schematic diagram of the photoelectrocatalytic reactor: (1) DC po'\Mer supply (2) quarrz window (3) IJV lamp (4) photometer (5) photoanode (6) cathode
(7) stirring bar (8) magnetic stirrer... ...372
SEM images of the surface morphology of the TiOz film deposited at 600'C. 375 X-ray diffraction patterns of TiOz film coated on Ti grids and on Si substrates
a t 6 0 0 " C . . . . 3 7 6
Graphical Pareto analysis of the effect of current intensity, treatrnent time, Pollutant concentration and UV lamp position on CTC degradation ... 383 Interaction X13 between current intensity and pollutant concentration... 386
The effect of current intensity (A) and pollutant concenbation (mg L-r) on CTC removal (application time: 90 min) three-dimensional plot; results
obtained from central composite matrix; Internal UV lamp position. ... 389 Comparison between actual and predicted values for CTC degradation. ... 390 Schematic diagram of the photoelectrocatalytic reactor: (1) DC power supply (2) qtartz window (3) UV lamp (4) photometer (5) photoanode (6) cathode (7) stirring bar (8) magnetic stirrer... ... 413 SEM views of PLD TiO2 films deposited on Si at different deposition
t e m p e r a t u r e s . . . . . . 4 1 7 SEM views of PLD TiO2 films deposited. ... 418
xxxi Figure 7-3
Figure 7-9
Figure 7-10 (a) LCA{SA4S chromatogram presented with (b) individual MS spectra of Figure 7-4 Figure 7-5 Figure 7-6 Figare 7 -7 Figure 7-8 Figure 7-11 Figure 8-1 Figure 8-2 Figure 8-3 Figure 8-4
X-ray diffraction pattems of TiO2 film coated on titanium grids and on silicon
substrates at 600oC and 400oC.. ... 420
SEM views of PLD amorphous carbon deposited on titanium at20"C...42I Hydrogen peroxide production using different cathode materials (at 0.39 A of current intensity and under 254 rm of UV irradiation). ... 426 Effect of the initial pH value on the oxidation and the mineralization of CTC (TilTiOz; VC; 0.39 A of current intensity; 254rmr; [CTC]0 :32 ttgfiy... +ll Chemical structure of CTC and the three distinct moieties (I)
tricarbonylamide, (If phenolic diketone and (III) dimethylamine...435 (a) Variation of the initial rate of CTC degradation versus different intial
concentration and (b) the linear variation of the plot l/re versus l/Co in the Langmuir-Hinshelwood kinetic model (TilTiO2; VC; 0.39 A of current
intensity; 254nrnof UV light). ...439
possible by-products of CTC by PECO process. ... 442
The chemical structure and the proposed photoelectrocatalytic degradation
pathways of CTC... ...443
Schematic diagram of the experimental setup: (1) PVC tank, (2) peristaltic recycling pump, (3) photoelectrocatalytic reactor, (4) N-doped TiO2 photocatalyst, (5) and (6) vitreous carbon, (7) in let, (8) out let, (9) Solar simulator.
X-ray diffraction patterns of pure TiOz and N-doped TiO2 coatings prepared at 65OoC, by means of a magnetron sputtering process. ... 465 Typical SEM micrograph of the sputter-deposited N-doped TiOz films. ... 466 [IV-Vis absorbance spectra of the N-doped TiOz films with various nitrogen contents (indicated by the arrows). The inset shows the variation of the
optical bandgap of the N-doped TiO2 films as a function of their N content... 468 Effect of nitrogen content doped TiO2 photoanode on the oxidation and the mineralization of CTC (VC as cathode; 0.39 A of current intensity; visible
i n a d i a t i o n ; [ C T C ] " : 1 0 0 p g L - ' ) . . . . . . . 4 7 2 Figure 8-5
Figure 8-6 Figure 8-7 Figure 8-8 Figure 9-l Figure 9-2 Figure l0-l Figure 10-2 Figure 10-3 Figure 10-4 Figure 10-5 Figure 10-6 Figure 10-7 Figure 10-8 Figure 10-9
Effect of current intensity on CTC degradation and mineralization using PECO process (3.4 at.% N-doped TiO2 photoanode; treatrnent time:120 min; [ C T C ] ' : 1 0 0 p g L - ' ) . . . . 4 7 4 Effect of treatrnent time on CTC degradation and mineralization using PECO process (N-doped TiO2 photoanode with a N content of 3.4 at.oh; Cvrent
i n t e n s i t y : 0 . 6 A ; [CTC]' : 100 pg L-r). . . . 4 7 7
Proposed photoelectrocatal5rtic degradation pathways of CTC under visible irradiation using 3.4 at.% N-doped TiOz photoanode ...,.... 480 Schematic diagram of the experimental setup: (1) PVC tank, (2) peristaltic recycling pump, (3) photoelectrocatalytic reactor, (4) N-doped TiO2 photocatalyst, (5) and (6) vitreous carbon, (7) in let, (8) out let, (9) Solar
simulator. ...496
Photoelectrocatalytic treatment of municipal wastewater contaminated by CTC under visible irradiation ([CTC]' : 100 pg L-1; [TOC]' : 18.7+1.2 mg L-1; [TN]" : lg.8+2.1mg L-1; [NH4l' :12.7+0.5 mg L-1; [NO2-+NO3-].:
1 . 6 8 + 0 . 0 5 m g L t ) . . . . . . . 5 0 3 Schematic diagram of the photoelectrocatalytic reactor: (1) DC power supply (2) qurartz window (3) IJV lamp (4) photometer (5) photoanode (6) cathode (7) stirring bar (8) magnetic stirrer... ... 518
SEM image of the surface morphology of the TiOz frlm deposited at 400"C.. 52I SEM views of PLD TiOz frlms deposited on silicon. ...52I X-ray diffraction patterns of TiOz film coated on silicon substrates and on
titanium grids at 400"C... ...524
SEM views of PLD amorphous carbon deposited on Ti at 20 "C. ... 525 Graphical Pareto analysis of the effect of current intensity, treatrnent time,
pollutant concentration and cathode material. ...529
Interaction Xr+ between current intensity and cathode material. ... 532 Interaction X3a between pollutant concentration and cathode material ... 532 The effect of current intensity (A) and pollutant concentration (mg L-r) on
CBZremoval (application time: 90 min); VC as cathode. ... 535
Figure 10-10 Comparison between actual and predicted values for CBZ degradation ... 539 Figure 10-11 Reaction mechanism proposed for the photoelectrocatalytic degradation of
c 8 2 . . .
. . . 5 4 r
LISTES DES EQUATIONS
E q u a t i o n 1 - 1 H z O + M - - - + M [OH'] + H* + e-... . . . 2 6
Equation 1-2 R + M [OH"] --+ M + RO + If+ e ... ...26
Equation 1-3 2SOa,2' + 2t -+ HzSzOs * 2e- ... ...26
Equation 1-4 Cl- + 2H2O ---+ HCIO * H3O* + 2e- ... ...26 Equation 1-5 O2(dirror,r) + 2lF^* + 2e' + HzOz ... ...26
Equation 1-6 HzOz* hv ---+ 2OH" ... 28
Equation 1-7 03 + H2O + hv ---+ 2OHo * O2... ...29
Equation 1-8 Fe2* + HzOz+ Fe3n + OH- + OHo... ... 30
Equation 1-9 Fe3* + H2o + hv --- Fe2* + H+ +c)Ho ... 30
Equation l-10 Formation des pairs 6lectrons-trous TiOz *hv ---+e sc * h*sv ... 36 Equation 1-11 Oxydation de polluant adsorb6 R par les phototrous h*sv * R ads+ n... :O Equation 1-12 Formation de radicaux hydroxyles h+sy *H2Q_+OH. + It'... 36 Equation 1-13 Formation de radicaux superoxyde e-sc * Oz-Ozo-.... ...37 Equation 1-14 Formation du peroxyde d'hydrog6ne 02 * 2H* + 2e s6+I{2O2... ...37
Equation
1-15 lncl - lQ-Ot"a
r' -l
k"
Equation 1-16 Equation 1-17 Equation 1-18 Equation l-19 Equation 1-20 Equation 1-21 Equationl-22 Equation 1-23 Equationl-2440
xxxvEquation 1-25 Equation 1-26 Equationl-27 Equation 1-28 Equation 1-29 Equation l-30 Equation 3-1 Equation 3-2 Equation 3-3 Equation 3-4 Equation 3-5 Equation 3-6 Equation 3-7 Equation 3-8 Equation 3-9 Equation 3-10 Equation 3-11 Equation 3-12 Equation 3-13 Equation 3-14 Equation 3-15 Equation 3-16
lncl, =
k , )
a - ( t
l )
k r ) R [ 2 , T , )r99
(I-a-)I,A kD Equation3-17 Ln XXXVIEquation 3-18 Equation 3-19 Equation 4-1 Equation4-2 Equation 4-3 Equation 4-4 .4 ,Equatlon )-l Equation 5-2 Equation 5-3 Equation 5-4 ,a Equatton )-)
Equation 5-7 RNO1.4 + H-<+RNOH-(.q)... ...347
Equation 5-8 e- * Oz(ads) + Oz"-... ... 350
Equation 5-9 Ouo- * H* -HO2o. ... 350
Equation 5-10 2HO2"---+HzOz+Oz ... 350
Equation 5-11 Ozo- * HO2o ---+ 02 + HO2- ... 350
Equationl-L2 HO2- + H* ---' H2O2... ... 350
Equation 5-13 02 + 26gs + 2H* --- HzOz ... 350
Equation 5-14 2H2O + 2h+vs'I{2Oz + 2H+uq ... 350
Equation 5-15 HzOz+ hv - 2OH' ... 350
E q u a t i o n 5 - 1 6 3 H z O + O r * 6 H * + 6 e - . . . . : . . . . . . 3 5 3
Equation 5-17 03 + hv -1Oz+ Oo... ... 353
Equation 5-18 Equation 5-19 Equation 6-1 Equation 6-2 Equation 6-3 Oo *H2O+ 2OH"
3s3
b r o X . , X o + b ^ X , X . t b r o X , X o + b r o X . X n Y = 5 0 . 8 5 + 7 2 . 0 6 X , + 5 . 6 5 ) { 2 - 2 . 7 3 X 3 - 2 . 1 8 X 4 - 0 . 3 6 X r X , + l . l l X r X 3 + 0 . 8 1 X , X o + 0 . 3 5 X 2 X 3 - 0 . 5 5 X 2 X 4 + 0 . 6 0 X , X o( n ? )
4 =l i,, l*1oo
(i + o)
...
383
\L"i )B : ( x r x ) - t
x t y . . .
. . .
3 8 7
u i - u i 0 a u i . . .
. . . 3 8 7
Y r = - 2 3 - 0 8 0 7 + 1 9 3 . 2 3 5 X , + 0 , 7 4 6 2 X , - 0 . 3 7 8 8 X 3 - 0 . 0 9 6 6 X l X 2 . . . 3 9 7 0 . 7 1 2 x l x 3 + 0 . 0 0 0 9 3 3 X r X , - 1 7 4 . 9 6 7 X 1 , - 0 . 0 0 3 0 9 5 x r ' - 0 . 0 0 2 1 6 x , ' Y t = - 3 4 . 9 3 0 7 7 + 2 0 4 . 2 0 0 3 0 X r + 0 . 7 6 6 5 8 X 2 - 0 . 3 4 3 2 5 X 3 - 0.0966 X r X 2 . . . 388 0.712X1X3 + 0.000933 XzXt -174.g67X,2 - O.OO:OIS X22 -0.002t6X320.9 1
D _ 3 8 1 Equation 7-1 EquationT-2 Equation 7-3 EqurationT-4 r = - - = dC k , A = clt k , K C . . . . 4 3 6 l + K C '- = koppt K,KCOEquation
6-4 Y : br+
D,.x,* 1-,u,,.r',
*
4 1 ,ur",",
te,
...
386
t:1
Equation 6-5 Equation 6-6
Equation 6-7
Equation 6-8
Equation 7-5 , = -oFl =k,KC =koppC
Equation 7-6
t.rQ
C EquiationT-7 f o = l+ KCo xxxvlrr 438Equation 7-8 Equation 8-1 Equation 8-2 534
Equation
l0-l p: - J2J-
...
s22
A(20)cos0 E q u a t i o n l 0 - 2 Y = b o + b t X l + b . x 2 + b 3 x i + b 4 x o r b n x r x . + b B x t x 3 + b u X l X o I b T X r X , + b r o X r X o * b y X 3 X 4 E q u a t i o n l 0 - 3 Y = 3 6 . 1 5 + 0 . 7 9 x 1 + 7 . 6 5 x , - 4 . 4 0 x 3 - 1 . 4 1 x 4 - 0 . 0 8 8 X , X , + 0 . 0 3 7 X , X , - 1 . 5 3 X r X 4 - 0 . 8 0 X r X 3 - 0 . 5 4 X r X n + 1 . 2 9 X r X n 528 . . . 5 2 8 k k kEquation
l0-5 Y = bo
+>b{t +>biixiz +>>\X,X,
+ e
.... 534
i=l i=l , Y 2 = 5 . 2 6 1 7 3 - 3 2 . 5 9 8 4 9 X 1 + 0 . 5 8 3 1 l X , + 0 . 7 0 8 7 1 X : . - 0 . 0 8 1 2 5 X r X r + 0 . 3 8 7 5 0 X r X ,Equation 10-7 -6.3?510 'x,X^+r2r.86609x,1-t.tzostto-' x|-o.ozssqzx'. """' 534
Equation 10-9
, v1 = 2.28525 - 54.02954 X t + 0.57154X, +l.01299 X, -0.08125 XL + 0.38750XrX, Equation 10-6 -6.37510-3 xrXr+r2r.8660gxi -r.r2o8n0 3 x2'z -0.039642x:
a-c
AL BV BC CBZ CEAEQ CF COT CTC CV DBO DCO DRX EO EORs ERU EUD EUI Gr LC-MS-MS MEB NT OTC PC PCC PD PE PEC PF PM POAs PPs PPCLISTE DES ABREVIATIONS
Carbone amorpheAblation laser Bande de valence Bande de conduction Carbamaz6pine
Centre d'expertise en analyse environnementale du Qu6bec Coliformes f6caux
Carbone organique totale Chlortehacycline Carbone vitreux
Demande biologique en oxygdne Demande chimique en oxygdne Diffraction des rayons X
Electro-oxydation
Espdces oxydantes r6actives Effluents r6siduaires urbains Eaux us6es domestiques Eaux us6es industrielles Graphite
Liquid chromato gtaphy-Mas s spectro scopy-Mass spectro scopy Microscopie 6lectronique d balayage
Azote totale Oxytetracycline Photocatalytique Plan central composite Photolyse directe Perturbateur endocrinien Photo 6lectrocatalytique Plan factoriel
Pulv6risation magn6tron
Procddds d' oxydations avancdes Produits pharmaceutiques
Proc6d6 de photocatalyse conventionnel
PPSPs PSR RNO TCs TC
Produits pharmaceutiques et de soins personnels Plan de surfce de r6ponse
p-nitro sodimethylaniline Tetracyclines
CHAPITRE l
l .
1.1
SYNTHDSE
Introduction
Dds le d6but du XX sidcle, I'utilisation de l'eau par l'€tre humain dans plusieurs activitds s'est
intensifi6e. Cependant, son usage varie selon les pays car elle d6pend du climat, du mode
d'agriculture, du niveau d'industrialisation du pays ainsi que du niveau d'accds d I'eau potable. D'une fagon g6ndrale, le secteur agricole consomme d lui seule prds de 70%o del'eau
disponible, le secteur industriel consomme prds de 20o/o alors que 10% de l'eau disponible est
destin6 pour des utilisations domestiques (Schwarzenbach et al., 2006). L'urbanisation
croissante et I'industrialisation intensive entraine une hausse de la consommation en eau et
une d6gradation de la qualit6 des ressources naturelles (eaux de surfaces et eaux souteraines).
De nombreux compos6s chimiques sont utilis6s pour des applications industrielles,
domestiques et agricoles. La pollution de l'environnement par des contaminants r6fractaires et
persistants est un d6fi majeur auquel doivent faire face les scientifiques et les gestionnaires.
Ces eaux us6es contiennent de nombreuses substances organiques et inorganiques
susceptibles de nuire gravement d I'environnement (Schwarzenbach et at,2006). En raison de leur toxicit6 et de leur persistance dans l'environnement, ces contaminants ne sont pas
g6ndralement 6limin6s dans les frlidres conventionnelles de traitement des eaux us6es
(Watkinson et a1., 2007). Certains de ces compos6s r6fractaires sont trds stables et par
cons6quent difficile d ddgrader. D'autres parviennent d se ddgrader partiellement et des
compos6s interm6diaires plus stables et plus toxiques que le polluant de d6part peuvent se
former (Watkinson et a1.,2007; Heberer, 2002). Ainsi, le rejet de ces contaminants dits
bio-rdcalcitrantes dans l'environnement peuvent engendrer des bouleversements significatifs, tels
que I'eutrophisation, la sous-oxyg6nation des lacs et des rividres et par consdquent un impact
cancdrigdnes, mutagdnes ou susceptibles d'interfdrer avec le systdme hormonal des Otres
vivants (Pal et al., 2010 ; Lai et al., 2009; Kolok et al., 2007). Pour faire face d ce probldme,
un fort dynamisme des recherches actuelles s'orientent de plus en plus vers le ddveloppement
des technologies simples, efficaces et plus adapt6s pour le traitement de ces contaminants afin
de pr6server les ressources en eaux et rdpondre ir une r6glementation de plus en plus
contraignante.
De ce point de vue, les proc6dds d'oxydation photodlectrocatalltique sont particulidrement
int6ressants. L'intdr€t de ces techniques rdside dans leur aspect non polluant, leur facilit6 de
mise en Guvre, leur faible co0t et surtout en raison de leur grande efficacitd sur les polluants
refractaires.
L.2 Synthisebibliographique
L.2.1 Propri6t6s physico-chimiques et impacts environnementaux des eaux us6es
r6siduaires
1.2.1.1 Gindralitis
Compte tenu de la pr6occupation mondiale face au probldme de plus en plus important de la pollution de l'environnement aquatique et terrestre, la question du traitement et du devenir des
eaux us6es a regu une importance croissante au cours de ces dernidres ann6es. Les eaux us6es
r6siduaires d'origine industrielle, domestique, agricole et mdme urbaine contiennent des
quantit6s non n6gligeables et vari6es de polluants organiques, inorganiques et bact6riens et ne
peuvent ainsi €tre rejetdes dans l'environnement aquatique sans traitement pr6alables. Le rejet
de ces polluants dans l'environnement sont l'une des causes principales de I'apport des
composds perturbateurs endocriniens dans I'environnement et perturbent le fragile dquilibre
des systdmes biologiques. Ainsi, il est n6cessaire de connaitre les constituants majeurs qui
que les techniques de traitement pr6alables qui peuvent 6tre utilis6es pour enlever ces
polluants afin de prot6ger la santd publique et l'environnement.
1.2.1.2 Eaux risiduaires domestiques
D'une fagon gdndrale, les eaux usdes domestiques (EUD) comprennent les eaux de m6nage
qui proviennent des salles de bains, des douches, des cuisines et des buanderies. Les EUD
sont une combinaison de plusieurs polluants provenant de plusieurs sources d'activit6s
humaines. La composition de ces eaux varie significativement selon l'endroit et la saison. Elle
ddpend principalement du nombre d'habitant install6s dans la ville, de leur niveau de vie ainsi que de la nature d'alimentation consom mde (Henze et a1.,2002). Les principales constituantes
des EUD sont les protdines (40-60%),les carbohydrates (25-50%),les d6tergents, les acides
humiques et fluviques, les huiles et les graisses (10%),la lignine et les tannins, ainsi que
d'autres polluants organiques et inorganiques (phosphore et azote) dissous (Rebhun et Mank4
1971; Manka et al, 1974). Par exemple, les eaux de cuisine sont trds riches en matidre en
suspensions et des matidres organiques provenant des d6chets v6g6taux et animaux. Les eaux
us6es provenant de la salle de bain sont trds particulidres. Misd d part les matidres en
suspension, elles renferment des d6tergents ainsi que des concentrations r6siduelles de produits pharmaceutiques et de soins personnels. En se basant sur les donn6es pr6sent6es par
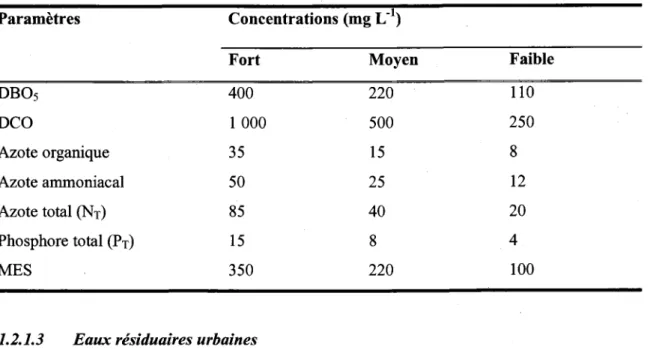
Tableau 1-1 Composition typique des EUD (Bitton,2005)
Paramitres Concentrations (mg L-r)
Fort Moyen Faible
DBOs DCO Azote organique Azote ammoniacal Azote total (N1) Phosphore total (P1) MES
400
I 000
3 5
50
8 5
1 5
3 5 0
220
s00
1 1 0 250 8 l 2 20 4 100 l 5 25 40 8 2201.2.1.3 Eaux risiduaires urbaines
Les effluents r6siduaires urbains (ERU) sont un m6lange complexe de plusieurs types de polluants. La composition de cet effluent varie principalement selon la taille de la
communaut6 urbaine ainsi que les habitudes alimentaires et d'hygidne des individus. En plus des effluents domestiques et des effluents industriels, les ERU comprennent 6galement des
effluents issus des institutions, des commerces, des hdpitaux, des casernes ainsi que les eaux
pluviales. Vue leur grande diversit6 et complexitd, ces ERU peuvent 0tre d l'origine de
l'apport des contaminants 6mergents rdfractaires dans l'environnement.
1.2.1.4 Eauxrisiduaiyesindustrielles
Les eaux us6es industrielles (EUI) sont diff6rentes des EUD et ses caract6ristiques varient
d'une industrie d l'autre. En plus des matidres organiques et des compos6s azotds et
phosphor6es, les EUI peuvent contenir 6galement des produits toxiques, des m6taux lourds,
des hydrocarbures ainsi que des micropolluants organiques. Ndanmoins, une classification des
effluents industriels doit 6tre dtablie selon qu'il renferme ou non des substances toxiques
classification permet de distinguer les polluants organiques non biod6gradables ainsi que les
polluants min6raux qui inhi-bent les processus de d6gradation biologique (Matin, 1982).
Certaines industries telles que les abattoirs, les fromageries, les cartonneries, les sucreries pr6sentent souvent des eaux us6es r6siduaires pouvant €tre trait6es par voie biologique. En
revanche, certaines industries telles que les industries pharmaceutiques g6ndrent des
composes toxiques (des antibiotiques, des solvants, des substances bact6ricides, etc)
susceptibles d'inhiber I'activit6 biologique de d6gradation des polluants organiques dans les
stations d'6puration des eaux usdes rdsiduaires (Adams et al., 2002 ; Snyder et al., 2003). Pour
minimiser l'impact de ces polluants sur les traitements subsdquents (ex. traitement
biologique), un prdtraitement est g6n6ralement requis avant leur rejet dans les r6seaux
collectifs.
1.2.2 Polluants organiques d'int6r6t 6mergent retrouv6s dans les eaux us6es r6siduaires
1.2.2.1 Origines etpropriitis physico-chimiques
Depuis le 20'sidcle, une industrialisation intense et incontrOlable se d6veloppe dans plusieurs pays du monde, et ce dans differents secteurs d'activitds : industries pharmaceutiques,
agroalimentaires, cosm6tiques, p6trolidres, chimiques, etc. Au nombre de ces polluants
couramment d6cel6s dans les rejets industriels et urbains, se trouvent les produits
pharmaceutiques ej de soins personnels (PPSPs), les pesticides, les produits chimiques
industriels et domestiques, les surfactants, les m6taux, etc (Tableau 1-2). Un grand nombre de
ces substances rentrent dans la cat6gorie des polluants 6mergents appel6s perturbateurs
endocriniens (Chang et a1.,2009). Un perturbateur endocrinien (PE) se d6finit comme 6tant
une substance exogdne qui altdre ou inhibe le fonctionnement du systdme endocrinien et, par
cons6quent, cause des effets n6gatifs sur un organisme intact, ou ilr sa prog6niture ou sa
population (Lister et Van Der Kraak, 2,OOI; Esplugas et al., 2007). Ces substances
faune aquatique (f6minisation et disparition de la faune aquatique) et sur la sant6 humaine
(occurrence de certains cancers, malformation des organes g6nitaux, alt6ration des thyroides,
baisse du quotient intellectuel, etc.) (Kumar et a1., 20ll ; Yoon et al., 2007). Quan et al.
(2007) ont signal6s que 38.000 substances chimiques ont une action sur le systdme
endocrinien, alors que l'agence de la protection environnementale (USEPA) prdvoit que
87.000 compos6s chimiques doivent €tre test6s pour d6terminer leurs effets sur le systdme
endocrinien (Kumar et al., 2011).
Les rejets issus des stations d'dpuration sont I'une des causes principales de I'apport de ces
contaminants dans I'environnement aquatique et terrestre incluant les eaux de surface, les
eaux souterraines, les s6diments et les boues (Kolpin et a1.,200L). Des concentrations allant jusqu'd 100 ng L-l peuvent €tre d6tect6 dans les eaux us6es r6siduaires (Servos et aL,2005;
Auriol eta1.,2007), alors que des concentrations trds faibles (0.1 ng L-r) peuvent induire des
effets oestrog6niques chez les organismes aquatiques (Auriol et a1.,2007). Ces composds sont
souvent prdsents dl'fitatde trace, c'est-d-dire d des concentrations allant du ng L-l d quelques dizaines de pg L'1, et ils ne participent globalement qu'd une trds faible proportion de la
matidre organique dissoute (Huang et Sedlak, 2001). Cependant, leur pr6sence dans les eaux
est d prendre en considdration en raison de la toxicitd potentielle pour I'homme et les espdces aquatiques. Ces compos6s organiques r6fractaires sont nombreux et 6chappent pour la plupart
d l'dpuration classique des eaux usdes, comprenant un prdtraitement physico-chimique suivi
d'un traitement biologique par biomasse en suspension (boue activ6e) ou biomasse fix6e (biofrltration, lit bact6rien) (Auriol et al., 2006). La pollution de l'environnement par ces
contaminants organiques persistants constitue aujourd'hui une des probldmatiques
6mergeantes associ6es au traitement des eaux us6es.
Parmi tous les produits chimiques complexes, une vari6t6 de PPSPs administr6s aux hommes
lacs, etc). Mdme si leurs concentrations 6taient dans certains cas ddtectables d l'6tat de trace
(des concentrations allant du ng L-l vers le pg L-l), ces polluants organiques sont persistiants
dans l'environnement et sont par consdquent reconnus comme une menace potentielle pour la
sant6 humaine et les 6cosystdmes. Les PPSPs sont des micropolluants d'intdr€t dmergents
couramment ddcelds dans les effluents rdsiduaires de type industriel et urbain. Une
description plus d6taill6e des produits pharmaceutiques (PPs) sera pr6sent6e dans les
Tableau 1-2 Structure mol6culaire et caract6ristique de certains produits chimiques.
Classe Produit chimique Structure chimique
Pharmaceutique (antibiotique)
Pharmaceutique (analg6sique)
Produit de soins de personnel (6cran solaire)
Pesticide Produits chimiques industriels ( Surfactant) Produits chimique industriel (Plastique) Sous-produits de combustion Sulfam6thazine
(sMZ)
Acdtaminophen Oxybenzone Atrazine Nonyl-ph6nol Bisph6nol A DioxinrJ'{ox{r
H " N # |fi-->-*Y
F|o+-? o c l, "A"
-J--*A*-AruA/\a\,'*
i l l HO/v C H a -,o4 \--)-Z \)-on \:/ c"rv":u)ry":
1.2.2.2 Rdsidus midicamenteux de type antihiotique
Les compos6s pharmaceutiques appel6s dgalement les PPSPs sont des substances issues de la
chimie fine de synthdse, regroupant une trds grande vari6t6 de produits tels que les
m6dicaments, les parfums, les produits cosm6tiques, les savons, les d6odorants, etc. Ces
compos6s sont des polluants d'intdr€t dmergent. Plusieurs 6tudes rapportent que les PPSPs ne
sont pas compldtement dliminds dans les stations d'dpurations des eaux usdes
conventionnelles (Clara et a1.,2005; Zuehlke et a1.,2006; Cirja et a1.,2008). Du fait de leur
caractdre trds persistant, ces compos6s pharmaceutiques ont 6t6 d6tect6s dans les eaux de
surface, les eaux souterraines, les eaux potables, et les eaux us6es de plusieurs pays,
notamment au Canada, aux Etats-Unis, au Br6sil, en Allemagne et dans d'autres pays (Heberer, 2002; Kummerer, 2009). Dans les eaux de surface, des concentrations entre 10 et
500 ng L-r ont 6td d6tect6es (Ternes, 1998), alors que des concentrations r6siduelles allant du
ng L-r au pg L-r ont 6t6 mesur6es dans les eaux us6es municipales. Les PPSPs sont des
substances trds stables et trds solubles dans l'eau compards aux autres composds organiques.
Etant donnd la grande diversitd de ce type de compos6s, il est difficile d'dtablir clairement et
sp6cifiquement leur toxicit6. Plusieurs recherches (Andreozzi et al. 2004; Fent et al. 2006)
pr6voient que I'exposition d long terme et d faible dose aux PPs dans l'environnement
conduit d des effets n6fastes sur la sant6 humaine et sur les espdces aquatiques.
Parmi ces produits, les m6dicaments constituent un groupe important et diversifi6 de
compos6s organiques utilis6s en grande quantitd d travers le monde (Kummerer, 2001). Dans
les pays d6velopp6s, la consommation de m6dicaments progresse d'une ann6e d une autre.
Les m6dicaments les plus couramment d6tect6s dans l'environnement sont les antibiotiques,
les antid6presseurs, la caf6ine, les antalgiques, les m6dicaments contre le cholest6rol, etc. Les
antibiotiques sont souvent cit6s parmi les compos6s les plus probl6matiques (Homem and
Santos, 201 l; Gao et a1.,2012; Onal, 2011; Pan et al, 2011). Les antibiotiques sont largement
utilis6s pour traiter et pr6venir les maladies dans la m6decine humaine et animale, ainsi que
pour augmenter I'efficacitd alimentaire et am6liorer le taux de croissance chez les b6tails et
les volailles (Gao et al. 2012; Pan et al. 2011; Sarmah et al. 2006; Chen et al. 2011). Tel que
mentionn6 par Martinez et al. (2011) et Halling-Sorensen et al. (1998), le volume de
production annuelle de mddicaments a 6t6 estim6 dr plusieurs centaines de tonnes, alors que
son utilisation a 6t6 globalement estim6e entre 100.000 et 200.000 tonnes (Kummerer,2003).
Par exemple, Ia capacit6 de production annuelle des antibiotiques en Chine est d'environ
210.000 tonnes (85% est utilis6 pour l'6levage et la m6decine), tandis que le rapport annuel de
production d'antibiotiques au Japon est d'environ 2.200 tonnes (30% sont utilis6s pour les
humains et 600/o sont utilis6s pour le b6tail) (Luo et al. 201l; Miyata et al. 2011). Aux
Etats-Unis, environ 9200 tonnes d'antibiotiques ont 6t6 produites en 2003 pour des applications
agricoles (AHI, 2005). Au cours de leur utilisation, les antibiotiques ne peuvent pas 6tre
absorb6s ou m6tabolis6s entidrement in vivo et une fraction importante (30 d 90%) est
excrdt6e sous forme de m6tabolites dans l'environnement via l'urine (Zhol et a1.,2012;Hu et
al., 2010a, b; Bound and Voulvoulis, 2004). Aprds utilisation, ces substances chimiques
persistent et peuvent contaminer les eaux de surface, les eaux souterraines et mdme les eaux
potables (Lopez-Penalver et al. 2010; Kim and Tanaka 2009; Bautitz and Nogueira 2007). Le
Tableau 1-3 prdsente les diff6rentes concenffations des antibiotiques d6tect6es dans l'environnement. Ces compos6s peuvent se trouver dans l'environnement aquatique d travers
le rejet direct des eaux us6es issues de fermes ou le rejet d'effluents des usines de traitement
des eaux us6es de type municipal ou industriel. L'application de fumier de ferme d'dlevage sur les terres agricoles contribue 6galement ir introduire les antibiotiques dans I'environnement
(Shelver et al.2010; Chen et al.2011). L'infiltration de ces substances dans l'environnement
peut ainsi causer des probldmes environnementaux y compris les risques 6cologiques et des
dommages de la sant6 humaine.
Le groupe de t6tracycline (oxyt6tracycline (OTC), chlorot6tracycline (CTC) et t6tracycline (TC)) est l'un des premiers groupes d'antibiotiques utilisds en thdrapie dans la m6decine
humaine et comme additif alimentaire dans le secteur agricole (Li et al., 2011; Ding et Mou,
2000). En raison de leur plus faible cofit et de leur plus grande activit6 antimicrobienne, le
groupe de t6tracycline a 6t6 largement utilis6 comme m6dicament dans la m6decine
v6t6rinaire pour la pr6vention et le traitement des animaux de ferme et pour gudrir plusieurs
maladies infectieuses (Onal, 201I ; Chen et al., 2011). Ce groupe d'antibiotique a dt6