UNIVERSITÉ DE SHERBROOKE Faculté de génie
Département de génie chimique et biotechnologique
ÉTUDE DE LA FORMATION ET DU COMPORTEMENT
D’UN DÉPÔT DE BOUE AU CENTRE DE LA CUVE À
L’INTERFACE CATHODIQUE
Thèse de doctorat Spécialité: génie chimique
Marc-André COULOMBE
Jury : Gervais SOUCY (directeur) Ryan GOSSELIN
Marie-Josée CHOLLIER Laszlo KISS
À ma femme Sophie À mes enfants Évangéline, Rosalie et Raphaël À mon Père, ma Mère, mon Frère
i
RÉSUMÉ
L’augmentation du rendement énergétique des cuves est un des objectifs principaux de la recherche sur l’électrolyse de l’alumine. Les objectifs de la thèse sont d’étudier les propriétés des dépôts, leurs facteurs de formation et leur effet sur la dégradation du bloc cathodique, notamment la chute de voltage cathodique (CVD).
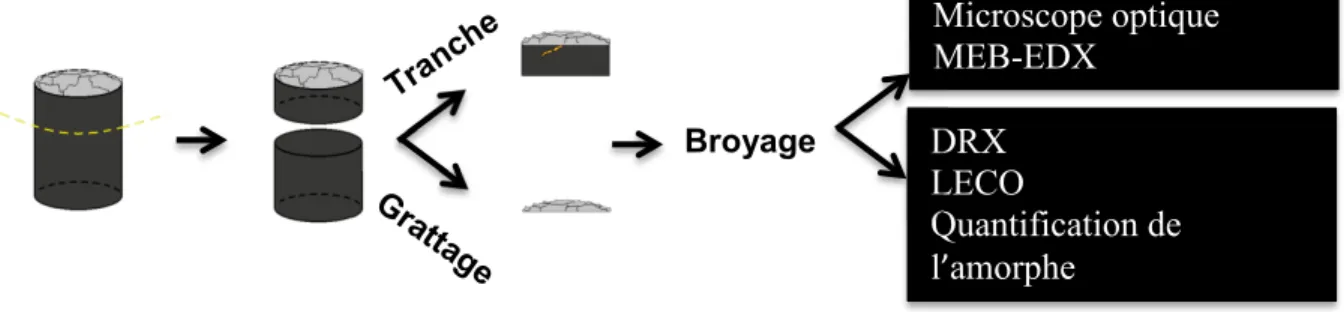
Une première phase des travaux a permis le développement d’une méthode de caractérisation des dépôts par le calcul de l’amorphe, l’estimation de l’alumine totale par un bilan sur l’oxygène LECO et une quantification plus précise des espèces contenant du calcium par mesure fluorescence X (XRF). L’étude d’échantillons bloc cathodique/dépôt par microscopie à balayage couplée avec la spectroscopie de la dispersion des rayons X (MEB-EDX) a aussi amené une meilleure compréhension de l’épaisseur de la couche de carbure à l’interface et de la taille des particules d’alumine dans la matrice de dépôt. Le développement d’un banc d’essai a permis de mesurer la CVD et de simuler les conditions d’électrolyse d’un bloc industriel en contrôlant l’alimentation alumine d’un côté et le refroidissement de l’autre côté. Une analyse statistique préliminaire a aidé à discerner des tendances dans la composition chimique des dépôts ainsi que des zones de dépôt précises. Des calculs thermodynamiques ont été utilisés pour obtenir la température de précipitation de la cryolite et de l’alumine et ainsi estimer la concentration solide/liquide dans les dépôts à température d’opération. Ces données ont ensuite permis l’estimation des propriétés de densité et de conductivité électrique des dépôts. Un bref exposé théorique de la formation des carbures et des oxycarbures a présenté le lien entre les travaux précédants sur l’imagerie XPS et l’effet des dépôts sur la dégradation du bloc cathodique.
Plusieurs phénomènes peuvent expliquer la formation de dépôt au fond de la cuve. La dissolution incomplète de l’alumine d’alimentation et la chute du matériel de couverture d’anode amènent une fraction significative de dépôt en dessous de la nappe d’aluminium jusqu’à la surface du bloc cathodique. L’importance de l’un ou l’autre des phénomènes peut être expliquée par les propriétés de l’alumine d’alimentation, le design et l’opération de la cuve. Une fois passé l’interface aluminium/bain, le dépôt peut s’accumuler en dessous des points d’alimentation, le long du couloir central entre les anodes ou s’étendre sur l’ensemble de la surface du bloc cathodique. L’étude de quatre cuves de deux différentes technologies a montré qu’il existe une corrélation entre la formation d’un mince film, sa sursaturation en alumine, le taux de dissolution partielle de l’alumine d’alimentation, la longueur du pied de talus et la CVD. En plus de la sursaturation en alumine, le mince film conduit à l’épaississement de la couche de carbure ce qui amène une hausse de la CVD. Des expériences laboratoires ont démontré que la dissolution partielle de l’alumine produit des dépôts d’une concentration massique d’alumine en deçà de 30 % et que ces dépôts riches en alumine peuvent interagir avec le pied de talus pour former un « dépôt » liquide qui remonte dans le bain électrolytique. Les résultats laboratoires ont aussi confirmé la corrélation entre l’épaisseur du dépôt et de la couche de carbure.
L’effet de la résistivité du film mince sur l’ensemble de la surface du bloc cathodique et de la longueur du pied de talus sur la CVD a été évalué à l’aide d’un modèle purement électrique. Trois types de films minces ayant une résistivité différente ont été modélisés selon des observations de composition chimique et de morphologie précédentes. Les données du
ii modèle correspondent aux données de CVD mesurées dans des cuves industrielles, et ce, pour deux types de technologies. Le modèle montre que l’effet combiné entre le pied de talus et la présence d’un mince film résistif amène une hausse significative de la densité de courant au centre de la cuve. Ce résultat pourrait conduire à une conclusion différente sur l’effet de la présence de dépôt au centre sur la CVD. Des expériences laboratoires ont montré que la simulation d’un pied de talus par l’ajout d’une plaque d’alumine produit une hausse de la CVD mesurable. La formation d’un dépôt épais produit une hausse encore plus grande de la CVD. Toutefois, des efforts demeurent pour augmenter la précision de la mesure afin d’évaluer l’impact d’un mince film sur la CVD.
L’étude d’une deuxième technologie a démontré un enrichissement du pied de talus en alumine ainsi qu’une corrélation entre la composition des dépôts au centre de la cuve et du pied de talus. Une étude approfondie des mouvements MHD supporte aussi l’existence d’une interaction entre dépôt centre et pied de talus. Il semblerait toutefois que le transport de matière net soit du centre de la cuve vers le pied de talus. L’étude de la densité des dépôts de pied de talus par tranche verticale a montré un phénomène de cristallisation des particules solides par le bas de l’échantillon ainsi que la formation d’un cœur liquide et moins dense que le reste de l’échantillon.
Mots-clés :
Électrolyse de l’alumine, formation de dépôt, interface cathodique, film mince, carbure d’aluminium, chute de voltage cathodique (CVD), étude thermodynamique.
iii
REMERCIEMENTS
Je tiens tout d’abord à remercier mon directeur de recherche Gervais Soucy avec qui j’ai pu débattre de mes idées et recevoir conseils et éclaircissements. Je voudrais aussi remercier Martin Désilets pour ces judicieux conseils et son aide avec la modélisation de la CVD. Pour ces beaux moments passés avec François Allard avec qui j’ai étroitement collaboré à développer notre montage laboratoire et passé des heures devant le LECO, merci. Je suis de plus reconnaissant pour tous les partages avec mes autres collègues et amis en l’occurrence Martin Brassard, Alexandra Shoucri, Pascal Lamontagne, Martin Lebeuf ainsi qu’avec Aliréza Hekmat, Sanaz Safa, Behnam Noorizadeh, Ali et Yasaman Shaverdi, Salaam. Pour le soutien à la caractérisation, je ne voudrais pas oublier de remercier Sonia Blais, Irène Kelsey, Stéphane Gutierrez, Carl St-Louis et Charles Bertrand ni pour le soutien technique André Bilodeau et Serge Gagnon. Pour le soutien dans mon projet de recherche des gens très occupés de l’industrie, un grand merci à Loïg Rivoaland, Didier Lombard, Jean-François Bilodeau, Alexandre Blais et Claude Gilbert. Pour le très apprécié soutien financier sans lequel ce projet n’aurait pas eu lieu, je voudrais remercier Rio Tinto Alcan, au Conseil de recherches en sciences naturelles et en génie du Canada (CRSNG) et le Fonds de recherche Nature et technologies du gouvernement du Québec (FQRNT).
Finalement, à toute ma famille, l’Église, ma famille dans la foi (je ne vous nommerai pas tous, car vous êtes trop nombreux) avec qui j’ai trouvé la force de persévérer jusqu’au bout, un grand merci. (Marc-André Coulombe)
iv
Table des Matières
LISTE DES FIGURES 7
LISTE DES TABLEAUX 10
LEXIQUE 11
LISTE DES ACRONYMES 13
CHAPITRE 1 INTRODUCTION 1
1.1 Objectifs du projet de recherche 3
1.2 Contributions originales 4
1.3 Plan du document 5
CHAPITRE 2 ÉTAT DE L’ART 7
2.1 Définition actuelle de la boue 8
2.1.1 Propriétés de la boue 8
2.1.2 Propriétés de la croûte/boue durcie (Muck/Bottom crust) 11
2.1.3 Propriétés des autres matériaux électrolytiques 14
2.2 Formation de la boue 15
2.2.1 Dissolution et agglomération de l’alumine 15
2.2.2 Accumulation de la boue sur la nappe de métal 22
2.2.3 Répartition de l’alumine à l’intérieur d’une cuve 23
2.2.4 Réalimentation de la boue vers le bain électrolytique 24
2.3 Dégradation du bloc cathodique 25
2.3.1 Abrasion physique par la boue 25
2.3.2 Interaction de la boue avec l’Al4C3 26
2.3.3 Formation des oxycarbures (Al4O4C et Al2OC/AlN) 27
2.3.4 Formation de la croûte à la surface de la cathode 27
2.3.5 Chute de voltage cathodique due à la présence des dépôts de surface 29
2.3.6 Méthode de mesure de la conductivité de la boue 31
CHAPITRE 3 MÉTHODOLOGIE 34
3.1 Analyse post mortem des cuves industrielles 34
3.1.1 Description des technologies et des principaux paramètres 34
3.1.2 Méthodes d’échantillonnage 37
3.2 Tests de laboratoire 38
3.2.1 Description du montage 38
3.2.2 Conditions d’opération et des paramètres 43
3.2.3 Plan expérimental et méthodes d’échantillonnage 45
3.2.4 Méthodes d’échantillonnage 45
3.3 Méthodes d’analyses des échantillons 47
3.3.1 Microscopie optique 47
3.3.2 Microscopie à balayage électronique et spectroscopie par dispersion d’énergie 47
3.3.3 Imagerie par spectrométrie photoélectronique X (XPS) 47
3.3.4 Diffraction rayons X et détection du calcium par un module de fluorescence X 48
3.3.5 Analyse élémentaire de l’oxygène 48
3.4 Traitement des données de composition chimique 49
3.4.1 Quantification de l’amorphe 49
v
3.4.3 Calculs des concentrations à partir des échantillons dopés au quartz et non dopés 50 3.4.4 Normalisation des concentrations d’Al2O3 avec les données LECO 52 3.4.5 Calculs des concentrations équivalentes pour simulation FactSageTM 53
CHAPITRE 4 ASPECTS THÉORIQUES 54
4.1 Analyse par composantes principales 55
4.1.1 Analyse globale des cuves et des tests laboratoires 55
4.1.2 Analyse des groupes d’échantillons 57
4.2 Calculs thermodynamiques 60
4.2.1 Simulation thermodynamique 60
4.3 Estimation des propriétés physico électriques 70
4.3.1 Calculs de la masse volumique des dépôts 70
4.3.2 Calculs de la résistivité des dépôts 70
4.4 Aspect théorique de la dégradation du bloc cathodique 72
4.4.1 Théorie sur la formation des carbures 72
4.4.2 Théorie sur la formation des oxycarbures 73
4.4.3 Observation en laboratoire des oxycarbures 73
4.4.4 Implication des résultats pour l’industrie 76
CHAPITRE 5 FORMATION DES DÉPÔTS 77
5.1 Avant-propos 77
5.2 Article scientifique 78
5.2.1 Abstract 78
5.2.2 Introduction 79
5.2.3 Electrolysis conditions and parameters 81
5.2.4 Results 86
5.2.5 Discussion on the deposit formation 104
5.2.6 Summary and conclusions 111
5.2.7 Acknowledgments 113
5.2.8 References 113
CHAPITRE 6 EFFET DES DÉPÔTS SUR LA CVD 115
6.1 Avant-propos 115
6.2 Article Scientifique 116
6.2.1 Abstract 116
6.2.2 Introduction 117
6.2.3 Methodology 118
6.2.4 Aluminium electrolysis experiments 123
6.2.5 Numerical simulation 127 6.2.6 Results 130 6.2.7 Discussion 135 6.2.8 Conclusions 137 6.2.9 Future works 137 6.2.10 Acknowledgements 137 6.2.11 References 138
CHAPITRE 7 INTERACTION AVEC LE PIED DE TALUS 139
7.1 Enrichissement en alumine 139
7.2 Formation d’un dépôt liquide 142
7.3 Cristallisation du dépôt 145
vi
CHAPITRE 8 CONCLUSION 151
ANNEXE A COMPOSITION CHIMIQUE PARTICULIÈRE 156
ANNEXE B PARTICULARITÉ DU MONTAGE LABORATOIRE 157
ANNEXE C ÉTUDE DÉTAILLÉE DES ÉCHANTILLONS INDUSTRIELS 158
Annexe C.1 : Position des échantillons dans les cuves industrielles c et d. 158 Annexe C.2 : Étude détaillée de l’échantillon e-1 159 Annexe C.3 : Étude détaillée de l’échantillon e-2 161
vii
LISTE DES FIGURES
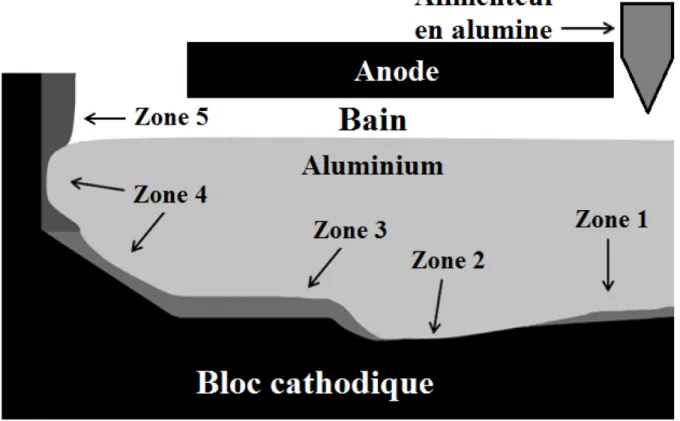
Figure 1.1 Schéma d’une cuve Hall-Héroult avec les différents types de dépôt. Traduit de [Coulombe et
coll., 2015]. ... 1
Figure 2.1 Masse volumique de la boue en fonction de la température pour différentes compositions (%masse d'Al2O3; ligne pointillée et fraction volumique d'alumine solide; ligne pleine). La masse volumique de l'aluminium est aussi donnée. Adapté de [Thonstad et coll., 1980]. ... 10
Figure 2.2 Montage d’un creuset pour étudier la croissance de la croûte à la surface du bloc cathodique ... 12
Figure 2.3 Croûte formée à partir de la boue. ... 13
Figure 2.4 Influence des additifs sur le taux de dissolution de l'alumine [Gerlach et Winkhaus, 1985]. ... 16
Figure 2.5 Courbe typique de la concentration d'alumine dissoute en fonction du temps accompagnée de l'impact sur la diminution de la température de l'électrolyte [Welch et Kuschel, 2007]. ... 18
Figure 2.6 Taille critique des agglomérats pouvant être accumulés à la surface de la nappe de métal [Keller, 1984]. ... 22
Figure 2.7 Transfert de l’alumine de la boue vers le bain au travers d’une couche d’aluminium intermédiaire. Courbe typique pour une épaisseur de 2,5, 4,0 et 5,5 cm. Taux d’agitation : 40 rpm [Thonstad et coll., 1980]. ... 24
Figure 2.8 Schéma du diagramme de phase du système Na3AlF6-Al2O3. [Thonstad et coll., 1982]. ... 28
Figure 2.9 Schéma démontrant l'effet de la hauteur de la boue sur la résistance électrique à la surface du bloc cathodique. Adapté de Geay et coll., 2001. ... 30
Figure 2.10 a) Montage physique, b) Schéma de l'arrangement électrique pour la mesure de la conductivité électrique de la boue [Geay et coll., 2001]. ... 31
Figure 2.11 Mesure de la rupture du voltage d'un appareil IGBT [Geay et coll., 2001]. ... 32
Figure 3.1 Positions des dépôts pris dans les cuves d’électrolyse a, b, c et d. ... 35
Figure 3.2 Surface du bloc cathodique d’une cuve de la technologie I. ... 36
Figure 3.3 Surface du bloc cathodique d’une cuve de la technologie II. ... 36
Figure 3.4 Préparation d’un échantillon prélevé à l’aide d’une carotteuse. ... 37
Figure 3.5 Préparation d’un bloc de carbone et de son interface. ... 38
Figure 3.6 Préparation d’un dépôt à l’interface cathodique. ... 38
Figure 3.7 Montage expérimental avant le démarrage. ... 39
Figure 3.8 Couvercle du creuset d’Inconel©. ... 40
Figure 3.9 Voltmètre et tige de mesure de la CVD. ... 40
Figure 3.10 Cellule d’électrolyse expérimentale et tube de refroidissement. ... 41
Figure 3.11 Nouvelle configuration de la cellule d’électrolyse expérimentale. ... 42
Figure 3.12 Correction du dosage d’alumine. ... 43
Figure 3.13 Schéma de la première coupe (verticale). ... 45
Figure 3.14 Aspect visuel typique de l’intérieur d’une cellule d’électrolyse laboratoire (coupe verticale). ... 46
Figure 3.15 Schéma de la deuxième coupe (horizontale). ... 46
Figure 3.16 Aspect visuel typique de l’intérieur d’une cellule d’électrolyse laboratoire (coupe horizontale). . 46
Figure 3.17 Pente de l'équation pour le calcul de la partie amorphe en fonction de la quantité de standards ajoutée et de la fraction amorphe réelle [Westphal et coll., 2009]. ... 50
Figure 4.1 Analyse par composantes principales des divers dépôts provenant de sept cuves industrielles et d’un test laboratoire (Classification par cuve – Voir Tableau 3.1). ... 56
Figure 4.2 Analyse par composantes principales (Séparation par classe d'échantillon)... 57
Figure 4.3 Diagramme de phase typique du groupe 1. ... 62
Figure 4.4 Diagramme de phase typique du groupe 2. ... 63
Figure 4.5 Diagramme de phase typique du groupe 3. ... 64
Figure 4.6 Diagramme de phase typique du groupe 4. ... 65
Figure 4.7 Diagramme de phase typique du groupe 5. ... 65
Figure 4.8 Diagramme de phase en fonction de l’AlF3. ... 66
Figure 4.9 Diagramme de phase typique du groupe 6. ... 67
Figure 4.10 Diagramme de phase typique du groupe 7. ... 68
Figure 4.11 Diagramme de phase typique du groupe 8. ... 69
Figure 4.12 Ratio du spectre de masse du signal 28 sur le signal 14. ... 75
Figure 4.13 Présence de fissures dans la bille d’aluminium. ... 75
viii
Figure 5.2 Front view of the electrolysis cell. ...82
Figure 5.3 Top view of the electrolysis cell. ...83
Figure 5.4 Lower part of cathode with (1) smaller part for the study of the deposit morphology and (2) larger part for chemical composition analysis. ...85
Figure 5.5 Schematic view of the measured deposit formation and sampling position (a-1 to a-6 and 1 to b-3) along with the simulated velocity profile based on the work of Renaudier et al. [16] in the metal for a typical cell of Technology I. The modelled velocity profile is calculated without deposit. Circular shapes - feeding point. Grey Zone 1 – whitish deposits under the SGA feeder. Yellow Zone 2 – thin film. Grey Zone 3 – ledge toe. ...88
Figure 5.6 Schematic view of the measured deposit formation and sampling position (c-1 to c-5 and 1 to d-2) for a typical cell of Technology II. Small circular shapes - feeding point. Larger circular shapes – velocity profile based on the work of Renaudier et al. [16]. The modelled velocity profile is calculated without deposit. Dark Zone 1 – thick deposits along the central channel. Yellow Zone 2 – thin film. Grey Zone 3 – ledge toe. ...89
Figure 5.7 MEB-EDX analysis of the dark thin layer under the thick sludge deposit at the center of the cell. ...91
Figure 5.8 MEB-EDX analysis of the a) yellowish and b) greyish thin film in the intermediate zone. ...94
Figure 5.9 Top view and front view of the deposit in a) Test A and b) Test B. ...97
Figure 5.10 Typical SEM-EDX microstructure of the ledge toe (B-2 and B-3) and the thin film (B-4 and B-5). ...98
Figure 5.11 Top view and front view of the deposit in Test C. ...99
Figure 5.12 Top view and front view of the deposit in a) Test D and b) Test E. ...101
Figure 5.13 Top view and front view of the deposit in Test F. ...102
Figure 5.14 Typical SEM-EDX microstructure of the thick deposit (Test F). ...103
Figure 6.1 Schematic top view of the deposit formation for an aluminium electrolysis cell. Grey zone – thick deposits. Yellow zone – thin film. Dark zone – thick deposit at the centre of the cell. Circular shapes - feeding points. ...118
Figure 6.2 Untypical deposit sample showing two types of frozen layer microstructure (left) and the element mapping (figures at the right) within the first 300 µm. ...122
Figure 6.3 Front view and side view of the electrolysis cell in the Inconel crucible inside the circular furnace. ...124
Figure 6.4 Summary of the CVD measurement. ...125
Figure 6.5 Schematic of the cathode block assembly along with the meshing and boundary limits (blue = carbide layer; green = sludge layer; brown = aluminium layer; orange = triangular shape). ...128
Figure 6.6 Zoom in showing the effect of specific mesh ratio of 3:1. ...130
Figure 6.7 Effect of the ledge toe length (X-axis) and the conductivity of the thin film models on the CVD. ...131
Figure 6.8 Centre cut view of the current density and of the distribution of the voltage in the block for the second thin film model and 30% of ledge toe covering. ...132
Figure 6.9 Local current density along the centre cut view at the cathode/block interface for different ledge toe covering. ...132
Figure 6.10 Effect of the technology on the modelled CVD within measured ledge toe covering area. ...133
Figure 6.11 Measured CVD for industrial cells from two technologies with both a typically low and a typically high CVD. ...134
Figure 7.1 Régime transitoire entre la surface de particules et la partie liquide [Yalin, 1977]. ...140
Figure 7.2 Mouvements à l’interface métal/bain causés par la tension de surface et les gaz produits à l’anode dans une cuve d’électrolyse [Utigard et Toguri, 1991]. ...141
Figure 7.3 Vue en coupe verticale d’une cellule d’électrolyse. ...142
Figure 7.4 Schéma du diagramme de phase du système Na3AlF6-Al2O3 (6% CaF2 -11% AlF3). Lignes pointillées : Mesures DSC. Ligne pleine : Valeurs thermodynamiques. ...143
Figure 7.5 Schéma d’une cuve Hall-Héroult avec les différentes zones couplées avec le profil de température selon l’axe de la cuve. ...144
Figure A.1 Graphique DRX démontrant la présence majoritaire d’aluminium dans les particules de plus de 250 µm dans les échantillons de dépôts de surface. ...156
Figure B.1 Fidélité de la mesure de l’alimenteur d’alumine. ...157
ix
Figure C.2 Photos de l'échantillon e-1 a) du côté A, b) du côté B et c) de côté. ... 159 Figure C.3 Particule de FexOy dans une matrice de bain électrolytique. ... 160 Figure C.4 Particule de fer, nickel, chrome en présence d'oxygène. ... 160 Figure C.5 Photographie de l’échantillon e-2 a) dessous, b) dessus, c) côté et d) interface du dépôt épais
(Microscopie optique). ... 161 Figure C.6 Analyse élémentaire et microstructurale du dépôt épais e-2 près de l’interface cathodique. Un
agrandissement de la figure de gauche révèle la morphologie des couches superposées dans les 100 premiers microns. ... 162 Figure C.7 Croissance de cristaux d’alumine dans une matrice riche en sodium et en fluor de l’échantillon
e-2. ... 163 Figure C.8 Analyse élémentaire et microstructurale typique au centre du dépôt épais e-2. ... 163
x
LISTE DES TABLEAUX
Tableau 2.1 Composition typique de la boue [Geay et coll., 2001] ... 9
Tableau 2.2 Propriétés de l’alumine primaire. Traduit de [Welch et Kuschel, 2007] ...19
Tableau 2.3 Comparaison de la CVD causée par la formation de pied de talus et de boue durcie, 350kA, espacement = 125 mm, V [Jie et coll., 2007] ...31
Tableau 3.1 Informations sur les cuves analysées ...34
Tableau 3.2 Conditions expérimentales ...44
Tableau 3.3 Paramètres étudiés ...44
Tableau 4.1 Liste des variables de concentration pour le modèle PCA ...55
Tableau 4.2 Moyenne et écart type de la composition des groupes 1 à 5 ...58
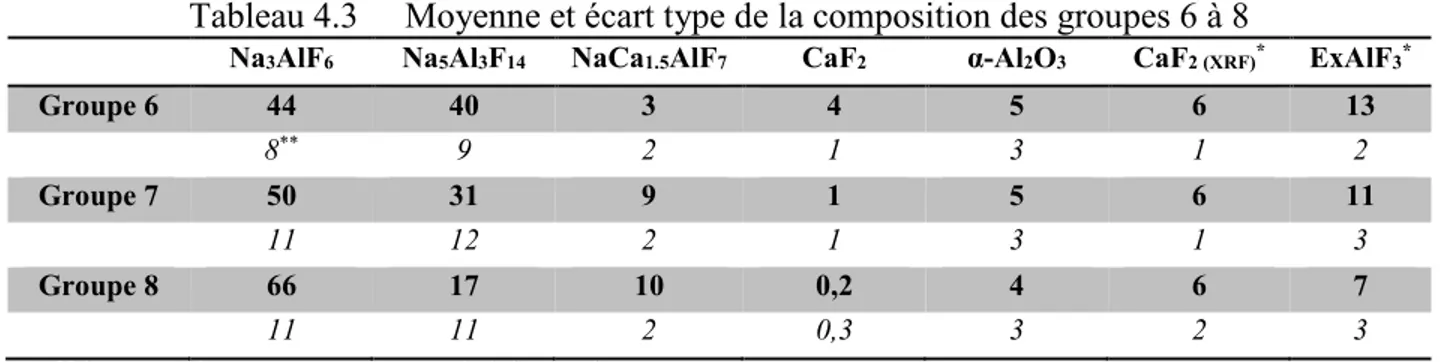
Tableau 4.3 Moyenne et écart type de la composition des groupes 6 à 8 ...59
Tableau 4.4 Moyenne et écart type des concentrations équivalentes pour le calcul des huit (8) diagrammes de phase typiques ...61
Table 5.1 Experimental electrolysis parameters ...84
Table 5.2 Industrial cell characteristics ...87
Table 5.3 Chemical composition of deposit found in Zone 1 at the center of industrial cells ...92
Table 5.4 Chemical composition of deposit in Zone 2 (intermediate zone) ...95
Table 5.5 Temperature gradient between the two walls depending of the electrolysis parameters ...96
Table 5.6 Summary of the chemical composition of the deposit found in the laboratory experiments ...103
Table 5.7 Comparison of the liquid aluminum and the samples c-3 and c3-S4 in function of the temperature ...105
Table 6.1 Summary of the conductivities used for the CVD model ...122
Table 6.2 Summary of the compositions and electrical conductivities for all three thin film models ...123
Table 6.3 Experimental Electrolysis Parameters ...124
Table 6.4 Summary of the ledge toe covering area and thin film aspect for the four industrial autopsied cells ...135
Tableau 7,1 Ensemble des données de pied de talus des cuves c et d ...139
Tableau 7.2 Étude par tranche de l’échantillon a-7 au bout du pied de talus en aval entre les points d’injection d’alumine ...146
Tableau 7.3 Étude par tranche de l’échantillon d-3 au bout du pied de talus en amont entre les deux points d’injection d’alumine centraux ...147
Tableau 7.4 Étude par tranche de l’échantillon e-1 en aval vis-à-vis un point d’injection d’alumine ...147
Tableau 7.5 Comparaison de la masse volumique relative à l’aluminium liquide des tranches de l’échantillon e-1 en fonction de la température ...148
Tableau 7.6 Étude par tranche de l’échantillon e-2 au bout du pied de talus en aval entre les points d’injection d’alumine centraux ...148
Tableau 7.7 Comparaison de la masse volumique relative à l’aluminium liquide des tranches de l’échantillon e-2 en fonction de la température ...150
xi
LEXIQUE
Terme technique Définition
Alumine Oxyde d’aluminium (Al2O3). Matière première utilisée pour produire
l’aluminium. Bain
électrolytique (Bath)
Liquide à base de sels fluorés dans lequel l’alumine est dissoute pour former l’aluminium par électrolyse.
Boue (Sludge) Dépôt mobile se formant sur le bloc cathodique. Sa position varie selon les cuves d’électrolyse, mais généralement située au centre de la cuve d’électrolyse. La boue est composée de bain électrolytique liquide et d’alumine solide en suspension à température d’opération. La boue peut contenir de l’aluminium et des impuretés en faible quantité.
Cathode Bloc de carbone sur lequel reposent l’aluminium liquide et le bain électrolytique. D'un point de vue électrochimique, la cathode est en réalité l'aluminium métallique liquide qui se trouve sur ce bloc de carbone
Chute de voltage
cathodique Perte d’énergie par effet d’Ohm à la cathode.
Croûte (Crust) Dépôt constitué majoritairement d’alumine (autour de 80 %). Il se comporte comme un solide lors de l’opération.
Cryolite ou
Cryolithe Fluorure de sodium et d’aluminium (Naélectrolytique. 3AlF6). Composé principal du bain Dépôt (Deposit) Terme générique pour décrire les phases présentes sur une surface. Le
dépôt peut être mobile ou solide à température d’opération
Film de bain Couche complètement liquide circulant entre l’aluminium et le bloc cathodique ou la gelée
Film mince (Thin
film) Dépôt se formant entre l’aluminium et le bloc cathodique. Il s’agit d’un film de bain sursaturé en alumine qui peut circuler à la surface du bloc cathodique. Ce dépôt a été observé lors dans la zone intermédiaire entre les dépôts au centre de la cuve et le pied de talus.
Efficacité de
courant Quantité d’aluminium produit par la cellule d’électrolyse divisée par la quantité calculée par la loi de Faraday. Gelée Terme générique pour décrire un dépôt solide à température d’opération.
On le distinguera généralement de la croûte en ce que le dépôt sera composé majoritairement de cryolite solide plutôt que d’alumine solide. Gelée de fond de
cuve (Bottom
freeze)
Dépôt se formant sur le bloc cathodique. À la différence de la croûte, il est constitué de bain solidifié et de peu d’alumine. Il se forme lorsque la surchauffe du bain est trop faible ou par refroidissement.
xii Nid-de-poule
(Pothole) Érosion localisée de la surface du bloc cathodique. Pied de talus
(Ledge toe) Dépôt se formant sous le talus et sur le bloc cathodique. La position horizontale du pied de talus part de la paroi latérale jusqu’au début de la zone érodé du bloc cathodique. Le pied de talus est formé généralement par refroidissement.
Ratio de cryolite
(Cryolite ratio) Composition chimique du bain électrolytique. Son composé est principalement la cryolite (Na3AlF6) qui équivaut à 3 moles de fluorure de
sodium (NaF) et 1 mole de fluorure d’aluminium (AIF3). Le ratio de
cryolite est donc de 3 pour de la cryolite pure. Un bain avec un ratio de cryolite < 3 est considéré acide, un ratio de 3 est neutre tandis qu'un ratio de > 3 est considéré comme basique ou alcalin.
Talus ou gelée
(Side ledge) Dépôt se formant sur la paroi latérale (Side wall). Il est constitué principalement de bain solidifié. Il se forme par refroidissement par le côté de la cuve. L’industrie de l’aluminium emploie le terme gelée ou talus. Dans le présent document, le terme talus sera utilisé.
Zone
solide/liquide (Mushy zone)
Section du bain qui est sous la température de liquidus et au-dessus de la température de solidus. On suppose cette zone assez fluide dans certaines conditions pour couler et former le pied de talus.
xiii
LISTE DES ACRONYMES
Acronyme Définition
ACM Matériel de couverture d’anode (Anode
Covering Material)
CR Ratio de cryolite molaire ou NaF/AlF3
(Cryolite Ratio)
CVD Chute de voltage cathodique (Cathode
Voltage Drop)
DRX (XRD) Diffraction des rayons X (X-Ray
Diffraction)
EDS Analyse dispersive en énergie
(Energy-Dispersive X-ray Spectroscopy)
LECO Laboratory Equipment COrporation
MEB (SEM) Microscopie électronique à balayage
(Scanning Electron Microscope)
MHD Magnétohydrodynamique
PCA Analyse par composantes principales
(Principal Component Analysis)
SGA Alumine de grade industriel (Smelter
Grade Alumina)
XPS Spectrométrie photoelectronique X
(X-Ray Photoelectron Spectroscopy)
XRF Spectrométrie de fluorescence X (X-Ray
1
CHAPITRE 1
INTRODUCTION
L’électrolyse de l’alumine est une part importante de l’économie québécoise. À cause de la compétition féroce qui existe à l’intérieur de cette industrie mondiale, celle-ci doit constamment améliorer son efficacité et réduire ses coûts. Le procédé, connu sous le nom de Hall-Héroult, est constitué d’un caisson d’acier, une anode et un bloc cathodique contenant l’électrolyte appelé bain.
La recherche sur l’électrolyse de l’alumine est triple : 1) augmenter le rendement énergétique des cuves, 2) augmenter leur productivité par le biais de l’augmentation du courant et 3) augmenter leur durée de vie. La stratégie employée est de développer des cathodes composées de matériaux plus performants sur la base des trois objectifs précédents.
Toutefois, la conception de nouveaux matériaux n’est rendue possible que si une meilleure compréhension des phénomènes de dégradation est obtenue. Par exemple, il est connu qu’environ 10% de la chute de potentiel est trouvée à la cathode et que cette résistance électrique augmente avec le temps [Lombard et al, 1998].
Figure 1.1 Schéma d’une cuve Hall-Héroult avec les différents types de dépôt. Traduit de [Coulombe et coll., 2015].
2 La résistance électrique à la cathode peut être divisée en quatre sections : 1) la barre collectrice, incluant les 2 contacts au scellement, 2) le contact entre la barre et le bloc cathodique, 3) le bloc lui-même et 4) le contact entre le bloc et l’aluminium (présence de dépôts). Le dernier contact constitue le point central du projet de recherche et plus particulièrement les différents types de dépôts qui se forment à cette interface.
Les études de la formation du pied de talus et du dépôt de fond cathodique sont rares et de nature très préliminaire. Les dépôts au fond de la cuve peuvent se former par une suralimentation d’alumine due à une lacune dans le contrôle de l’alimentation [Lillebuen et coll., 1992] ou à cause de la chute de matériel de couverture d’anode [Eick et coll., 2010]. On peut aussi avoir de l’accumulation d’alumine (cratère inversé) qui finit par sombrer dans la cuve. Lorsqu’une quantité trop importante d’alumine est ajoutée dans la cuve, celle-ci descend sous la couche d’aluminium, emportant avec elle une quantité donnée de bain cryolitique.
Le phénomène de formation du pied de talus n’est pas bien connu, car l’écoulement d’un film du bain vers le bas de la cathode est sérieusement mis en cause [Solheim, 2006]. Au contraire, la pression de la nappe d’aluminium force le mouvement d’un film potentiel entre le talus et l’aluminium vers le bain. L’hypothèse d’un flux de masse causé par la tension de surface (effet de Marangoni) [Utigard et Toguri, 1991] doit elle aussi être abandonnée. En effet, la présence d’un dépôt plus acide que le bain au bout du pied de talus, nécessaire pour favoriser un mouvement du haut vers le bas, n’a jamais été observée en industrie. Au contraire, la tension de surface devrait plutôt favoriser le mouvement du film du bas vers le haut. Il faut donc que la source du film provienne du bas. Quoi qu’il en soit, à mesure que l’on s’approche du centre du plancher cathodique, le pied de talus diminue en épaisseur et l’interaction de l’aluminium métal avec le plancher cathodique augmente subitement. C’est à cet endroit qu’une érosion marquée débute et que le pied de talus se termine.
La formation de dépôts de surface devient problématique lorsque ces dépôts ne sont pas réalimentés, durcissent et créent une barrière au courant électrique [Geay et coll., 2001; Keller, 2005; Thonstad et coll., 1982; Gerlach et Winkhaus, 1985]. Ainsi, sous certaines conditions, le mélange, sursaturé en alumine et isolé du bain cryolitique, pourrait ne plus ou
3 presque plus se dissoudre. La présence d’alumine en suspension dans le bain d’électrolyse se trouvant à la surface du plancher du bloc cathodique se nomme boue. Cette boue, ressemblant à un mélange d’eau et de sable, peut se solidifier et devenir très dense. Ce phénomène est connu sous le nom de plaquage. À cet effet, il est aussi connu que la cristallisation due à un sous-refroidissement cause le durcissement des dépôts au fond de la cuve [Thonstad et coll., 1982]. Les dépôts de pied de talus deviendront problématiques dans la mesure où ils peuvent s’étendre jusque sous l’anode et créer des perturbations du courant. Ils peuvent aussi engendrer des changements dans le bilan thermique de la cuve. Les besoins de l’industrie sont donc de contrôler les bilans massique et thermique dans la cuve et de connaître les conditions d’opération auxquelles les dépôts deviennent problématiques.
Ainsi, le sujet de recherche proposé est : « Quels sont les effets des dépôts à l’interface du bloc cathodique? » L’étude s’est réalisée dans un contexte industriel où le recensement de données d’usine a servi à bâtir un plan d’expérimentation pour expliquer le lien entre les phénomènes se produisant à l’interface aluminium/bloc cathodique et la chute de potentiel cathodique. Les travaux ont été partagés entre la présente thèse et un mémoire [Allard, 2014c], centré sur l’explication de l’effet de la composition chimique du bain et l’étude spécifique des dépôts de pied de talus dans les cuves industrielles.
1.1 Objectifs du projet de recherche
Afin de répondre à la question de recherche, quatre objectifs fondamentaux ont été relevés : 1. Étudier les propriétés des dépôts de surface d’un bloc cathodique par l’analyse
d’échantillons industriels et laboratoires et se concentrer sur les dépôts au centre de la cuve ;
2. Étudier les facteurs de formation des dépôts à la surface du bloc cathodique en fonction des matériaux cathodiques, des conditions d’opération et particulièrement des transferts thermiques dans les cuves d’électrolyse ;
3. Étudier la dégradation de l’interface aluminium/bloc cathodique due à la présence des dépôts de surface ;
4
1.2 Contributions originales
Les travaux de recherche dans le cadre du doctorat ont été conduits depuis mai 2011. Ils font suite à un passage direct de la maîtrise au doctorat et à plusieurs travaux préliminaires de mise en place de techniques de caractérisation. Entre janvier 2010 et avril 2011, les travaux de recherche ont consisté au développement d’un banc d’essai sur l’électrolyse de l’alumine. Un chargeur de poudre d’alumine a été programmé et a été calibré afin de permettre les essais d’électrolyse de longue durée.
Les travaux de recherche sur le développement de phénomènes de réactivité de surface des blocs cathodiques se sont étendus à plusieurs autres techniques. L’étude de la composition élémentaire ainsi que l’imagerie élémentaire ont été rendues possibles par la maîtrise de la technique MEB-EDS (Microscopie à balayage couplé à la spectroscopie de la dispersion des énergies). Un développement de la technique de la microtomographie à rayon X à angle unique a permis d’observer et d’évaluer rapidement la vitesse de pénétration du bain dans les creusets de carbone. Ces travaux ont conduit à la rédaction de deux actes de conférence ainsi qu’à une présentation internationale à San Diego, États-Unis dans le cadre de la conférence 2011 « The Minerals, Metals & Materials Society ».
Le développement d’une méthodologie de mesure du contenu amorphe dans les dépôts, l’estimation de leur conductivité électrique, leur densité et leur fraction solide/liquide ont permis d’affiner l’interprétation des résultats de composition chimique. Le développement d’un montage laboratoire capable de contrôler l’alimentation en alumine, le taux de refroidissement sur un côté de la cellule et de mesurer la CVD aidera à développer des solutions concrètes et réalistes pour réduire la formation des dépôts dans les cuves Hall-Héroult.
Des efforts substantiels ont été déployés dans le développement de la technique d’analyse XPS et particulièrement celui de l’imagerie des énergies de liaison XPS. Une collaboration internationale avec une sommité dans le domaine de l’analyse des spectres XPS, Neal Fairley, a permis de pousser l’analyse de la réactivité du carbone à l’interface de blocs de carbone cathodique générés par les essais laboratoires d’une manière exceptionnelle et innovatrice. Les résultats et le développement de la technique ont conduit à produire un
5 article intitulé : « Cryolitic vein imaging from an industrial grade carbon » dans la revue « Electron Spectroscopy and Related Phenomena ».
L’étude de la formation des dépôts au centre de la cuve a mené pour la première fois à la caractérisation approfondie d’une couche de dépôt mince située dans une zone intermédiaire entre le pied de talus et les dépôts épais au centre de la cuve. Cette couche mince n’était jusqu’à présent pas prise en compte dans les modèles thermoélectriques des cuves Hall-Héroult. Une corrélation entre les caractéristiques isolantes, la longueur du pied de talus et la chute de voltage cathodique dans les cuves industrielles a été déterminée. Ces phénomènes ont été appuyés par des expériences laboratoires sous conditions contrôlées. L’étude de la formation d’un surnageant à la surface des dépôts épais et la croissance d’une couche de carbure sous la couche mince, ont conduit à la publication d’un article intitulé : « Factors leading to the formation of a resistive thin film at the bottom of aluminum electrolysis cells » dans la revue « Metallurgical Transaction B ». Ces travaux soulèvent un questionnement important sur l’effet indirect de la formation des dépôts au centre de la cuve sur l’augmentation de la chute de voltage cathodique.
Le développement de travaux précédents sur des modèles thermoélectriques [Blais et coll., 2013 et Dupuis et Bojarevics, 2005], par la simplification à la partie électrique seulement et par l’ajout d’un dépôt mince à la surface du bloc cathodique a permis de prédire de manière précise la chute de voltage cathodique en connaissant la longueur du pied de talus et la conductivité électrique moyenne du dépôt mince. Ces travaux qui permettront de quantifier les gains énergétiques causés par la réduction de la résistivité électrique du dépôt mince ont été résumés dans l’article : « The effect of ledge toe and thin film formation on cathode voltage drop in aluminum electrolysis cells » et soumis dans « Canadian Metallurgical Quaterly »
1.3 Plan du document
Incluant le chapitre d’introduction et de conclusion, la thèse est divisée en huit (8) chapitres dont les deux chapitres principaux correspondent à deux articles soumis dans des revues scientifiques. Le chapitre 2 expose de façon systématique l’état de l’art sur les caractéristiques des dépôts, les phénomènes connus entourant leur formation, les facteurs de
6 dégradation des cuves reliés à leur présence dans les cuves industrielles et un sommaire des travaux sur leur conductivité électrique. Le chapitre 3 présente la méthodologie employée, les analyses post mortem, les expériences laboratoires, les appareils de caractérisation et le traitement des données. Au chapitre 4, les aspects théoriques du projet, soient l’analyse par composante principale, les calculs thermodynamiques, l’estimation des propriétés physico électriques ainsi qu’un résumé de la théorie sur la formation des carbures et des oxycarbures sont abordés. Le chapitre 5 traite de la formation des dépôts à la surface cathodique et met l’accent sur les dépôts du centre de la cuve. Les phénomènes entourant la formation d’un mince film résistif entre les dépôts épais au centre de la cuve et le pied de talus constituent le cœur du chapitre. Le chapitre 6 décrit le modèle de résistivité électrique servant à mesurer la chute de voltage cathodique attendue en fonction de la longueur du pied de talus et la conductivité électrique du film mince. Le chapitre 7 traite des résultats complémentaires au projet de recherche touchant l’interaction entre le pied de talus et les dépôts au centre. Finalement, un chapitre de conclusion présente une synthèse des travaux effectués, met l’accent sur les contributions originales de la thèse et ouvre sur des travaux futurs pouvant ultimement résoudre de nouvelles questions qui ont été soulevées par la rédaction de cette thèse.
7
CHAPITRE 2
ÉTAT DE L’ART
Depuis plusieurs années, la présence de boue dans l’industrie de l’aluminium est problématique comme en témoignent les études sur le sujet [Geay et coll., 2001; Keller, 2005; Keller, 1984; Kheiri et coll., 1987 et Wang, 2009]. Tel que montré à la figure 1.1, les dépôts de boue peuvent se trouver à plusieurs endroits dans la cuve d’électrolyse de l’alumine. La présence de boue ne serait fondamentalement pas un problème dans l’industrie si son comportement était bien géré [Kalgraf et Tørklep, 1998]. L’alimentation de la cuve par la boue a même été suggérée comme un moyen permettant d’opérer à une concentration d’oxyde plus élevée que celle atteignable par une opération conventionnelle. De plus, une faible quantité de boue pourrait même passer inaperçue tant et aussi longtemps que le mélange ne forme pas une croûte cohérente [Thonstad et coll., 1982]. Pour que cette croûte se forme, un gradient de température d’au moins 15-20 °C doit exister entre la température de liquidus et la température réelle dans le dépôt de boue.
Les moyens dont l’industrie dispose pour contrôler, réduire voire éliminer certains phénomènes indésirables associés à la présence de la boue sont reliés au design, aux matériaux et à la construction des cuves d’électrolyse, aux méthodes de démarrage, aux paramètres d’opération, et aux additifs utilisés [Sørlie et coll., 1992].
Le phénomène général accepté menant à la formation de la boue est la dissolution partielle de l’alumine, la sédimentation subséquente à la surface de la couche de métal et une accumulation suffisamment importante pour vaincre la tension de surface et s’accumuler à l’interface du bloc cathodique. Ainsi, lorsque l’on parle de formation de boue, il est généralement question d’un mélange d’alumine et de bain électrolytique au fond de la cuve. Toutefois, on admet aussi la possibilité d’un durcissement structurel qui conduit au plaquage [Geay et coll., 2001].
Les raisons pour lesquelles la présence de la boue à l’interface cathodique est ou n’est pas problématique ne sont pas toujours claires. Une revue de la littérature sera effectuée pour
8 explorer la nature de la boue, la formation et la dégradation du bloc cathodique afin de mieux diriger les efforts de recherche sur cette question. Une attention particulière sera portée sur l’effet de la présence des dépôts sur la chute de voltage cathodique.
2.1 Définition actuelle de la boue
La boue est un terme générique pour parler d’un mélange de bain électrolytique sursaturé en alumine. La boue proprement dite est connue comme la formation d’un dépôt d’alumine qui vainc la tension de surface de la couche d’aluminium et s’accumule à l’interface cathodique. Une fois rendu à la surface du bloc, et si les conditions le permettent, la boue peut se durcir et former une croûte communément appelée corindon. À partir du moment où la boue subit un durcissement structurel, elle ne devrait plus porter l’appellation de boue. Dans la littérature, le mot boue, sludge, est de ce fait parfois mal utilisé.
Le corindon est, quant à lui, un autre abus de langage. En fait, le durcissement structurel de la boue ne peut être appelé corindon que si la croûte est constituée à 100 % de corindon. En effet, le corindon est la phase la plus stable de l’alumine et est aussi identifié comme étant de l’alumine α. La croûte est donc un état intermédiaire entre un mélange de particules d’alumine dispersées dans une matrice de bain électrolytique (boue) et une matrice solide constituée à 100 % de α-Al2O3 (corindon), soit un dépôt dur formé du corindon.
Toutes ces matrices devraient être différentiées de l’alumine d’alimentation, de l’alumine provenant des calcinateurs, du bain électrolytique, de la gelée, du matériel de couverture d’anode et du pied de talus. Dans la réalité toutefois, il n’est pas toujours évident de tracer la limite entre toutes ces matrices. Elles pourront être définies, entre autres, par leur composition chimique, leur microstructure et leurs propriétés électrophysicochimiques.
2.1.1 Propriétés de la boue
Composition
Des campagnes d’échantillonnage ont été effectuées à l’usine de Comalco, Tomago et St-Jean [Geay et coll., 2001] afin d’obtenir la composition typique de la boue. Le Tableau 2.1 résume la variation typique.
9 Tableau 2.1 Composition typique de la boue [Geay et coll., 2001]
Composé Concentration du
bain (%masse) Concentration de la boue (%masse)
Alumine (α-Al2O3) 2-6 38-50
Fluorure d’aluminium (AlF3)
7-13 0-3
Fluorure de calcium (CaF2) 4-5 2-3
Carbure d’aluminium (Al4C3)
Trace 0-2
Carbone (solide) Trace Trace
Aluminium (gouttelette) Trace Trace
Impuretés métalliques (fer,
nickel, chrome, vanadium) Trace Trace
Impureté (Silicium,
phosphore) Trace Trace
Cryolite (Na3AlF6) Balance Balance
Il est consistant de voir que le ratio de cryolite est plus basique dans la boue qu’au sein de la cuve. En effet, il est postulé que la boue est en équilibre avec le bain à la surface de l’aluminium, lui-même enrichi en sodium [Keller et coll., 1988]. Une autre valeur avancée pour la composition de la boue est 40 %m/m et 60 %m/m de bain électrolytique [Thonstad et coll., 1982].
Une deuxième étude d’échantillonnage de deux cuves industrielles [Allard et coll., 2014b] a montré la présence d’un enrichissement de la concentration massique de l’alumine au bout du pied de talus typiquement long [50 %-68 %] en comparaison de la partie plus près du mur de la cuve [1,7 %-4,7 %]. Dans le cas de l’étude d’un bloc où le pied de talus était typiquement court, l’effet était inversé, mais comprenait tout de même une zone du pied de talus chargé en alumine [30 %-54 %] comparé à 4,8 % pour le bout du pied de talus.
Microstructure
Quelques études [Keller, 1984 et Østbø, 2002] ont associé la microstructure trouvée dans les agglomérats d’alumine alimentée et celle retrouvée dans la boue après qu’elle ait vaincu la
10 tension superficielle de la nappe de métal. Cependant, aucune observation directe n’a été faite et l’effet du contact avec l’aluminium plutôt qu’avec le bain électrolytique n’a pas été commenté.
Propriétés électrophysicochimiques
Les propriétés électrophysicochimiques de la boue n’ont pas été étudiées en profondeur. Toutefois, la plupart des auteurs les ont estimées en considérant le mélange de boue comme étant composé de bain et d’alumine.
Densité
Une étude visant à montrer la densité relative de la boue a été accomplie [Thonstad et coll., 1980] en mélangeant l’alumine avec de l’air, de l’eau et de la cryolite. La figure 2.1 suggère qu’une boue contenant moins de 30 %m/m d’alumine aura tendance à remonter vers le bain à moins d’une force d’attraction quelconque. Elle est obtenue à partir d’un bain de 2,05 g/cm3
saturé à 12 %m/m d’alumine ayant une masse volumique de 3,75 g/cm3 qui correspond à
20 % vol/vol.
Figure 2.1 Masse volumique de la boue en fonction de la température pour différentes compositions (%masse d'Al2O3; ligne pointillée et fraction volumique d'alumine solide; ligne
pleine). La masse volumique de l'aluminium est aussi donnée. Adapté de [Thonstad et coll., 1980]. 30wt% Alumine 35wt% Alumine 40%alumine 45wt% Alumine 2,25 2,30 2,35 2,40 2,45 2,50 2,55 960 970 980 990 1000 1010 1020 1030 M as ee v ol umi qu e ( g/ cm3 ) Température (°C) 30wt% Alumine 35wt% Alumine 40wt% Alumine 45wt% Alumine 22vol% Air (déposé) 25vol% Eau
27vol% Air (compacté) Aluminium
11
Conductivité électrique
La résistance électrique n’est pas donnée avec précision dans la littérature, mais une valeur approximative de 2 fois la résistivité du bain [Keller, 1984] et 1S/m [Geay et coll., 2001] a été proposée.
Viscosité apparente
La boue peut se décrire un peu comme du sable gorgé d’eau. Ce bain est très fluide et la boue qui semble visqueuse l'est effectivement à cause de la friction des particules l’une contre l’autre et non à cause de la viscosité du fluide. Si la viscosité du bain n’excède pas 5 mPa.s, le mélange d’alumine et de bain peut, quant à lui atteindre quelque 105 Pa.s [Kalgraf et
Tørklep, 1998]. Ainsi, cette meilleure compréhension de la nature de la viscosité de la boue permet de mieux appréhender la notion répandue de boue très peu dense. Les grains d’oxyde décanteront très rapidement (0,6 m/s) et le surnageant, soit le bain, devrait monter presque instantanément à l’interface métal/bain dû à sa densité plus faible que le métal.
2.1.2 Propriétés de la croûte/boue durcie (Muck/Bottom crust)
Composition
Il a été tenté de reproduire la croûte qui se forme à la surface du bloc cathodique d’une cuve industrielle [Thonstad et coll., 1982]. Des expériences laboratoires ont été effectuées, dans un premier temps, en trempant un cylindre de graphite dans une solution de bain électrolytique saturée en alumine durant 6 heures à 5 jours. Ce cylindre, monté sur un tube d’inconel, a été maintenu à basse température en contrôlant le débit d’air dans le tube. Dans certaines expériences, de l’aluminium a été ajouté dans le creuset. Dans d’autres expériences, le cylindre de graphite a été polarisé cathodiquement. Le schéma expérimental correspond à la figure 2.2a.
Dans un deuxième temps, un gradient de température a été imposé en dessous d’un creuset de graphite rempli de boue et de bain électrolytique durant 3 à 5 jours.
12 Figure 2.2 Montage d’un creuset pour étudier la croissance de la croûte à la surface du
bloc cathodique
(a) Cellule d’électrolyse avec un doigt froid. A – Thermocouples, B – Tube d’acier, C – Tube d’inconel permettant la circulation d’air, D – cylindre de graphite, E – creuset de graphite, F
– croûte solide, G – mélange de cryolite et d’alumine fondue, H – excès d’alumine. (b) Cellule d’électrolyse avec un système de refroidissement par le bas. A – Creuset de graphite,
B – mélange de cryolite et d’alumine fondue, C – Boue, D – croûte solide, E – Thermocouples, F – Assemblage en acier et en inconel pour le refroidissement et le support
du montage [Thonstad et coll., 1982].
Les échantillons de croûte produite étaient composés de 65-85 %m/m d’alumine. Après une journée, la croûte contenait 70 %m/m d’alumine et après quatre jours 80-85 %m/m d’alumine. Deux échantillons industriels de croûte ont démontré des teneurs en alumine de 65 et 74 %m/m d’alumine.
Microstructure
Dans les expériences avec le cylindre de graphite comme dans celle avec le creuset de graphite, la croûte formée à la surface refroidie ainsi que la boue, formée de particules d’alumine dispersées, contenait des cristaux d’alumine. En comparant l’image de microscopie à balayage (MEB) de la figure 2.3a avec l’image MEB de la figure 2.7, on peut associer les deux types de microstructures à des formes variées de plaquettes d’alumine encastrées dans une matrice de bain électrolytique. On parle aussi de plaquettes « plate-like
13 crystals » normalement non colorées et transparentes en absence d’aluminium ou de polarisation [Thonstad et coll., 1982].
Dans les expériences de cylindres refroidis, les cristaux produits peuvent atteindre jusqu’à 15 mm. Dans les expériences de creusets refroidis, une coupe transversale de la croûte formée montre des endroits où les particules d’alumine sont recristallisées et d’autres endroits où la microstructure est encore similaire à celle de la boue. La taille des particules peut atteindre 1 mm et 4 mm avec et sans présence d’aluminium respectivement.
Figure 2.3 Croûte formée à partir de la boue.
L’échantillon est traité avec une solution d’AlCl3 pour dissoudre les fluorures. (a) Grandes
particules recristallisées. (b) Particules similaires à la boue. Microscopie électronique à balayage [Thonstad et coll., 1982].
De façon similaire aux expériences laboratoires en présence d’aluminium, une couleur jaunâtre a été observée dans certains cristaux provenant de cuves industrielles. La distribution de la taille des particules a été étudiée en broyant les agglomérats de >100 µm. Une étude Coulter Counter a permis d’identifier l’intervalle 40-80 µm comme étant prédominant. L’analyse visuelle de plusieurs photographies ont permis d’identifier que la majorité des grains avaient une taille entre 10 et 400 µm et que quelques grains avec une taille entre 3 et 4 mm.
14 Propriétés électrophysicochimiques
Densité
La croûte possède une masse volumique d’environ 3200-3700 kg/m3 et s’approche de celle
du corindon (3500-4000 kg/m3). La porosité peut varier de 1 à 20% [Verenaki et coll., 1973].
2.1.3 Propriétés des autres matériaux électrolytiques
Propriété de l’alumine d’alimentation « SGA (Smelter grade alumina) »
L’alumine d’alimentation contient 80-95% alumine de transition (γ, γ’, θ- Al2O3) et un faible
contenu en corindon (α-Al2O3). L’alumine de transition se transforme en corindon à environ
1200 °C dans les calcinateurs. Toutefois, en présence de fluorure, cette conversion se produit à plus faible température [Taylor, 2007; Ødegård et coll., 1985b et Groutso et coll., 2009]. Propriétés de la couverture d’anode « ACM (Anode covering material) »
La croûte qui se forme au-dessus du bain contient, en plus de l’alumine, environ 50 % m/m des phases présentent dans le bain [Thonstad et coll., 2001]. Le durcissement de la croûte d’alumine au-dessus du bain est le résultat de la transformation de l’alumine de transition en un réseau de plaquettes hexagonales de corindon [Groutso et coll., 2009]. L’électrolyte fondu pénètre cette matrice et joue un rôle majeur dans la formation de la croûte. Si l’ACM possède un contenu élevé de SGA, la croûte sera moins dure.
Propriétés du bain électrolytique
Au moins une étude s’est penchée sur le lien entre la composition de l’électrolyte et la composition de la boue [Geay et coll., 2001]. Après étude de deux cuves, il a été conclu qu’il n’y avait pas de corrélation entre l’excès d’AlF3 dans l’électrolyte et la boue, mais qu’il y
avait corrélation entre la concentration d’Al2O3 et la concentration de CaF2, selon l’équation :
%𝐶𝐶𝐶𝐶𝐹𝐹2 (𝑑𝑑𝑑𝑑𝑑𝑑𝑑𝑑 𝑏𝑏𝑏𝑏𝑏𝑏𝑏𝑏) = −6,3 ∗ 10−2�% 𝐴𝐴𝐴𝐴2𝑂𝑂3 (𝑑𝑑𝑑𝑑𝑑𝑑𝑑𝑑 𝑏𝑏𝑏𝑏𝑏𝑏𝑏𝑏)� + 5,4 (2.1)
Toutefois, il ne semble pas qu’aucune étude ne se soit penchée sur des corrélations possibles entre la composition du bain et la probabilité de formation de la boue.
15
2.2 Formation de la boue
2.2.1 Dissolution et agglomération de l’alumine
L’étude de la dissolution et de l’agglomération de l’alumine a constitué l’ouvrage ou une partie de l’ouvrage de plusieurs ouvrages [Østbø, 2002; Kuschel et Welch, 1990a; Haverkamp, 1992; Walker, 1996 et Paglia, 2004, Dassylva-Raymond et coll., 2015].
L’objectif ici n’étant pas la description de tels phénomènes, il est donc évident que cette section de revue de littérature fera un survol très léger du sujet. Il est tout de même important de relever les grandes lignes de ces ouvrages afin de faire le pont entre la nature de l’agglomération de l’alumine dans le bain électrolytique et la fraction résiduelle non dissoute qui atteint l’interface du bloc cathodique, sa nature et ses propriétés.
Alimentation de l’alumine
Les conditions d’opération d’une cuve d’électrolyse comprennent la température, la quantité et la composition chimique de l’électrolyte ainsi que la densité de courant et la distance entre l’anode et la cathode. Elles sont ajustées, entre autres, pour maintenir le bilan thermique tout en travaillant à de faibles températures d’opération. Cette réduction de la température d’opération amène par le fait même la réduction de la solubilité de l’alumine, mais ne serait plus aussi critique avec le contrôle de la concentration d’alumine dans la cuve [Thonstad et coll., 2001].
Le design d’un appareil d’alimentation automatique « point feeder » a permis d’améliorer considérablement le contrôle de la quantité de l’alumine introduite dans la cuve [Hove et Kvande, 1982]. Depuis cette invention, l’angle, la fréquence ainsi que le nombre de points d’alimentation ont été optimisés. Les cuves d’électrolyse optimales opéreraient à une température entre 955 et 970°C et la composition chimique de l’électrolyte doit être de 9 à 13 %m/m pour l’AlF3, 4 à 7 %m/m pour le CaF2 et 2 à 4 %m/m pour l’Al2O3 [Utigard, 1999].
Quoique la valeur économique de la présence de LiF reste incertaine, une concentration de 2 %m/m de cet additif abaisserait de 10°C la température optimale d’opération.
16 Cinétique de dissolution
Le phénomène de dissolution partielle de l’alumine est central dans la formation de la boue. Une compréhension minimale des taux de dissolution est nécessaire pour comprendre quelle fraction de l’alumine alimentée se rend à la surface du bloc cathodique.
Le taux de dissolution a été mesuré en considérant l’effet de la présence d’Al2O3, d’AlF3, du
CaF2, du MgF2, du LiF et de la température [Gerlach et Winkhaus, 1985]. Alors que l’AlF3
n’a aucune influence sur le taux de dissolution de l’alumine, les autres additifs abaissent son taux comme le montre la figure 2.5. Les paramètres les plus critiques pour le taux de dissolution sont toutefois la concentration initiale d’Al2O3 ajouté dans le bain électrolytique
et la température du bain.
Figure 2.4 Influence des additifs sur le taux de dissolution de l'alumine [Gerlach et Winkhaus, 1985].
17 L’intégration en 1999 [Qiu et coll., 1999] d’une caméra vidéo dans un montage laboratoire a grandement amélioré la précision de la mesure du taux de dissolution de l’alumine. L’expérience a été divisée en trois parties : La fonte de 150 g de cryolite solide (∼80 min), l’addition et la dissolution de 1,5 g d’alumine (∼15min) et l’addition et la dissolution d’une portion supplémentaire de 1,5 g d’alumine (∼15 min). Lors de cette expérience particulière, deux types d’alumine ont été comparés soient l’alumine « sandy » et un intermédiaire entre l’alumine « sandy » et l’alumine « floury ». L’alumine « sandy » est calcinée à basse température, est constituée de gros grains et possède un faible contenu en corindon. L’alumine « floury » est, à l’opposé, calcinée à plus haute température, est constituée de particules plus fines et un contenu en alpha plus élevé. La cryolite était composée de 2 % masse d’Al2O3, 3 % masse de CaF2 et de 1 % masse de LiF. Bien que l’alumine
« sandy » prenne plus de temps à quitter la surface du bain, elle se dissout toutefois plus rapidement que l’alumine intermédiaire. Une critique importante de cette méthode est la surestimation de la dissolution de l’alumine. En effet, l’index de réfraction de l’alumine étant similaire à celle du bain cryolitique, il est difficile de déterminer si l’alumine dispersée est réellement dissoute et ainsi de déterminer avec certitude la cinétique de réaction.
Avec les nouveaux paramètres d’opération (volume de bain électrolytique réduit/kA et une surchauffe minimale de l’électrolyte), la dissolution est de plus en plus limitée par le transfert de chaleur [Welch et Kuschel, 2007]. En effet, l’addition de 1 % masse d’Al2O3 requiert
entre 90 et 112 kJ/mol pour se dissoudre. Cette opération peut faire diminuer la température locale du bain de 15°C, soit plus d’énergie qu’une cuve moderne peut fournir. Aussi, il a été déterminé que le taux de dissolution n’est pas constant pour un même lot d’alumine. Le processus de dissolution est majoritairement endothermique, mais possède deux petites phases exothermiques. La figure 2.6 présente le processus typique de dissolution de l’alumine ainsi que la diminution de la température de l’électrolyte associé.
18 Figure 2.5 Courbe typique de la concentration d'alumine dissoute en fonction du temps
accompagnée de l'impact sur la diminution de la température de l'électrolyte [Welch et Kuschel, 2007].
D’autres paramètres contrôlant le taux de dissolution sont considérés. La vitesse et l’angle auxquels l’alumine touche la surface du bain deviennent des paramètres importants, car ces derniers amènent une dispersion plus ou moins grande de l’alumine et altèrent ainsi son taux de dissolution [Wang, 2009].
Effet des propriétés de l’alumine sur la cinétique de dissolution
Les propriétés de l’alumine primaire peuvent avoir un impact sur l’opération des cuves d’électrolyse. Leurs impacts sont résumés dans le Tableau 2.2.
19 Tableau 2.2 Propriétés de l’alumine primaire. Traduit de [Welch et Kuschel, 2007] Propriétés Rôle / Importance de la propriété
Pureté Na et Ca pour la consommation de l’AlF3, autres contaminants métalliques
Perte au feu 0°C to 300°C–volatiles adsorbés (peuvent former des « volcans » pour l’alimentation par points)
300°C to 1,000 °C–principalement des composés Al-O-H qui sont les contributeurs majeurs pour la formation du HF
Densité apparente Précision de la corrélation entre l’alimentation volumique et la masse supposée
Angle de repose Qualité de la couverture d’anode si de l’Al2O3 seulement est utilisée,
fluidité, capacité à remplir les réservoirs de stockage Distribution de la
taille des particules Cohérence des propriétés, tendance à produire de la poussière, impact sur la solubilité apparente (vitesse de dissolution–grosses particules) B.E.T. aire de
surface Capacité potentielle d’adsorber l’HF gazeux
Contenu en alpha. Mesure de la conversion du précipité Al(OH)3 « trihydrates» vers la forme
d’alumine la plus stable; une mesure secondaire de l’aire de surface pour une méthode de calcination donnée; tendance à former une croûte
Indice d’attrition Tendance du matériel polycristallin à se dégrader en particules plus petites Test d’écoulement Fluidité de l’alumine
Indice de poussière Évaluation qualitative de l’habileté à rester suspendu dans l’atmosphère au-dessus de la cuve et de ne pas être alimenté
L’effet individuel des paramètres de l’alumine est difficilement mesurable, car ils sont interreliés. La distinction entre l’alumine sandy et floury s’avère utile, mais une classification plus exhaustive serait essentielle pour la suite de l’étude de la dissolution de l’alumine dans le bain cryolitique.
Comportement de l’alumine dans le bain électrolytique
Une fois alimentée, l’alumine ne descend pas immédiatement dans le bain électrolytique. Elle réagit plutôt avec le bain pour former des radeaux et/ou des agglomérats. Les différences de comportement dans la dissolution des types d’alumine pourraient être reliées à leur tendance à former ces agglomérats [Rolseth et coll., 1994; Kobbeltvedt et coll., 1996; Thonstad et coll., 1972; Bagshaw et Welch, 1986; Kuschel et Welch, 1990b, Dassylva-Raymond et coll., 2015].
Il est connu que l’alumine a tendance à s’agglomérer lorsqu’elle est alimentée dans le bain d’électrolyse [Keller, 1984; Abd El All et coll., 1980 et Damoui et coll., 1982]. Une partie de l’alumine se disperse et se dissout rapidement. Le reste de l’alumine forme des agrégats et se
20 dissout beaucoup plus lentement [Østbø, 2002]. La connaissance de la microstructure présente dans les agglomérats peut être utilisée dans la compréhension du comportement du dépôt de boue par exemple dans le taux de dissolution.
L’agglomération de l’alumine serait causée par deux phénomènes [Townsend et Boxall, 1984] :
- La formation d’une couche de cryolite gelée autour de l’agglomérat
- La transformation γ α de l’alumine, la forme gamma sous-entend ici toute forme transitoire de l’alumine.
L’alumine alimentée aura premièrement tendance à former une croûte à la surface du bain électrolytique appelé « raft » [Keller, 2005; Qiu et coll., 1999]. Dépendamment du type d’alumine, la croûte produite aura tendance à être plus ou moins dure [Østbø, 2002].
La quantité d’ACM (Anode covering material) qui tombe au fond de la cuve à cause de toute sorte de manipulations des anodes est non-négligeable devant l’alimentation en alumine. Ainsi, le mouvement des anodes et le type de matériel qui les recouvre [Eick, I. et al, 2010] peuvent influencer la quantité et la composition de la boue. De plus, dépendamment de la composition en chiolite et de la position des isothermes, il arrive que le matériel puisse tomber au fond de la cuve [Gudmundsson, 2009]et participe à la formation de la boue. Une expérience laboratoire a été développée afin de mesurer l’impact de la qualité de l’alumine sur le type de croûte qui se forme à la surface du bain. Une définition en 5 parties du comportement de la croûte est proposée [Townsend et Boxall, 1984] :
1) Croûte sans cohésion. Quelques petits radeaux flottent à la surface et coulent à l’intérieur d’une minute. Forme de la boue et se dissout rapidement.
2) Croûte avec cohésion, mais très mince. La surface demeure poudreuse et n’est pas aisément mouillée par le bain. Coule à l’intérieur d’une minute. Forme de la boue et se dissout rapidement.
![Figure 1.1 Schéma d’une cuve Hall-Héroult avec les différents types de dépôt. Traduit de [Coulombe et coll., 2015]](https://thumb-eu.123doks.com/thumbv2/123doknet/3303455.95086/19.918.230.723.684.989/figure-schéma-hall-héroult-types-dépôt-traduit-coulombe.webp)
![Figure 2.4 Influence des additifs sur le taux de dissolution de l'alumine [Gerlach et Winkhaus, 1985]](https://thumb-eu.123doks.com/thumbv2/123doknet/3303455.95086/34.918.257.679.467.981/figure-influence-additifs-taux-dissolution-alumine-gerlach-winkhaus.webp)
![Figure 2.6 Taille critique des agglomérats pouvant être accumulés à la surface de la nappe de métal [Keller, 1984]](https://thumb-eu.123doks.com/thumbv2/123doknet/3303455.95086/40.918.109.645.646.930/figure-taille-critique-agglomérats-pouvant-accumulés-surface-keller.webp)
![Figure 2.10 a) Montage physique, b) Schéma de l'arrangement électrique pour la mesure de la conductivité électrique de la boue [Geay et coll., 2001]](https://thumb-eu.123doks.com/thumbv2/123doknet/3303455.95086/49.918.160.784.633.961/figure-montage-physique-schéma-arrangement-électrique-conductivité-électrique.webp)