Implication de l’infirmière dans la mise en œuvre du
bilan comparatif des médicaments à l’unité de
cardiologie d’un centre hospitalier québécois
Mémoire
Marie-Pier Mailhot
Maîtrise en sciences infirmières
Maître ès sciences (M. Sc.)
Québec, Canada
© Marie-Pier Mailhot, 2015
Résumé
Le bilan comparatif des médicaments (BCM) constitue une pratique organisationnelle requise par Agrément Canada. Alors que la contribution des médecins et pharmaciens est bien définie, celle des infirmières demeure à préciser. But : Décrire l’implication infirmière dans la mise en œuvre du BCM auprès d’une clientèle atteinte de problèmes cardiaques admise à l’unité de cardiologie d’un centre hospitalier. Méthode : Étude de cas unique avec entretiens (N = 6) (infirmières, médecins, pharmaciens), revue qualitative de dossiers patients (N = 22) et sources documentaires (N =15), s’appuyant sur un cadre de référence intégrateur. Résultats : L’implication infirmière va au-delà des attentes relatives à la seule gestion du formulaire. L’implication effective se traduit par quatre catégories : propre et distinctive, mobilisation nuancée, filet de sûreté et activités contributives. Conclusion : L’accompagnement des patients et la mobilisation des autres professionnels révèlent une implication de l’infirmière dans le BCM qui gagne à être reconnue.
Abstract
Medication reconciliation (MedRec) is a formal process. While doctors’ and pharmacists’ contribution is clearly spelled out, nurses’ involvement remains to be clarified. Goal: Describe nurses’ involvement in implementing MedRec among cardiorespiratory patients admitted to a hospital centre’s cardiology department. Framework: Meleis theory, Reason model. Method: Single case study. Three data sources: interviews (N = 6) (nurses, doctors and pharmacists); a qualitative review of patient files (N = 22), and documentation (N =15).
Results: While nurses are indeed expected to manage forms in the various phases of
transition of care, their involvement extends well beyond this task and falls into four main categories: distinct involvement; nuanced mobilization; safety net, and; contributive activities. Results show that the accompaniment of patients and their loved ones is learned through teaching, screening high-risk patients and collaborating in a way that supports the mobilization of the other professionals involved to ensure patient safety during transitions.
Table des matières
Résumé ... iii
Abstract ... v
Table des matières ... vii
Liste des tableaux ... xi
Liste des figures ... xiii
Remerciements ... xv
Introduction ... 1
1. Problématique ... 3
1.1 Mise en contexte de la problématique ... 3
1.1.1 La sécurité des patients et la prévalence des erreurs de médicaments ... 3
1.1.2 Les divergences médicamenteuses ... 4
1.1.3 Moyens de prévention des erreurs de médicaments ... 5
1.1.4 La gestion sécuritaire des médicaments ... 5
1.1.5 Le bilan comparatif des médicaments ... 7
1.2 Urgence d’agir en contexte infirmier ... 8
1.2.1 Enjeux de la mise en œuvre du BCM ... 9
1.2.2 Cadre législatif et professionnel ... 10
1.2.3 La clientèle de cardiologie ... 11
1.3 But et objectifs de l’étude ... 12
2. Recension des écrits ... 15
2.1 Les fondements conceptuels ... 15
2.1.1 Concept de réconciliation médicamenteuse ... 15
2.1.1.1 Définition opérationnelle de la réconciliation médicamenteuse ... 16
2.1.1.2 Distinction entre la revue des médicaments et la réconciliation médicamenteuse ... 17
2.1.1.3 Composante de la réconciliation médicamenteuse : MSTP ... 17
2.1.2 Efficacité de la réconciliation médicamenteuse... 19
2.1.2.1 Éviter les réadmissions et les visites aux urgences ... 19
2.1.2.2 Identifier les divergences et les erreurs de médicaments ... 20
2.1.2.3 Diminution des coûts ... 23
2.2 État des connaissances sur l’implication des différents acteurs dans la mise en œuvre du bilan comparatif du médicament ... 24
2.2.1 Implication du pharmacien ... 24
2.2.2 Implication du médecin ... 26
2.2.3 Implication de l’infirmière ... 27
2.3 Récapitulatif de l’état des connaissances sur le bilan comparatif des médicaments ... 30
3. Cadre de référence ... 33
3.1.2 La métaphore du fromage suisse ... 33
3.1.3 Approche système et barrières de défense ... 35
3.2 Le modèle théorique de la transition ... 36
3.2.1 Pour accompagner la transition dans le bilan comparatif du médicament ... 37
3.3 Présentation du cadre de référence ... 38
4. Méthode de recherche ... 39
4.1 Devis de recherche ... 39
4.2 Contexte de l’étude ... 41
4.3 Sources d’information et échantillons ... 41
4.4 Sélection des sources d’information et déroulement de la collecte ... 42
4.4.1 Sélection et recrutement des informateurs aux entretiens ... 43
4.4.1.1 Critères de sélection des informateurs clés pour les entretiens ... 43
4.4.1.2 Modalités de recrutement pour les entretiens ... 43
4.4.2 Critères et modalités de sélection des dossiers patients ... 44
4.4.2.1 Modalités de sélection des dossiers patients ... 44
4.4.3 Critères et modalités de sélection des sources documentaires ... 45
4.4.3.1 Modalités de sélection des sources documentaires ... 45
4.5 Outils de collecte de données ... 46
4.5.1 Guide d’entretien semi-dirigé ... 47
4.5.2 Grille d’extraction de données ... 47
4.5.2.1 Développement d’une grille préliminaire ... 48
4.5.2.2 Construction d’un guide d’utilisation de la grille d’extraction de données .. 48
4.5.2.3 Avis d’experts sur le contenu et la forme de la grille ... 49
4.5.2.4 Pré-test de la grille d’extraction de données ... 50
4.6 Analyse des données ... 51
4.6.1 Analyse des données issues des entretiens ... 51
4.6.2 Analyse des données extraites des dossiers patients ... 52
4.6.3 Analyse de la documentation ... 53
4.6.4 L’élaboration et la vérification des conclusions ... 53
4.7 Rigueur scientifique ... 54
4.8 Les aspects éthiques ... 55
5. Présentation des résultats de recherche ... 57
5.1 Contexte ... 57
5.2 Description du cas ... 60
5.2.1 Implication attendue de l’infirmière dans le bilan comparatif des médicaments ... 60
5.2.1.1 Implication transversale qui est attendue de l’infirmière aux phases d’admission, de transfert et de congé ... 61
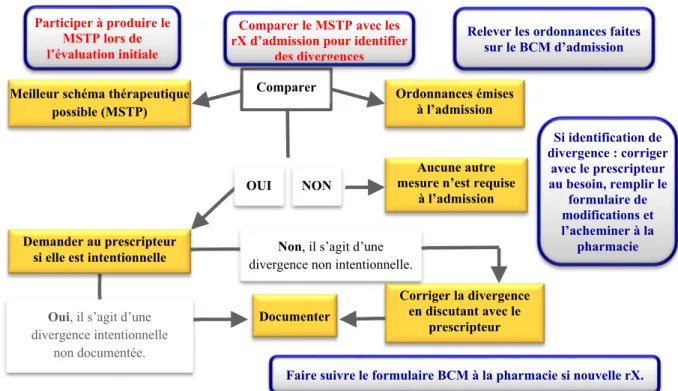
5.2.1.2 Comparer le MSTP avec les prescriptions d’admission pour identifier des divergences et les corriger avec le prescripteur ... 61
5.2.1.3 Enseignement sur les médicaments ... 63
5.2.1.4 Évaluation du processus de mise en œuvre ... 64
5.2.1.5 Enseignement sur la médication ... 64
5.2.2.1 Implication que devrait avoir l’infirmière à l’admission ... 65
5.2.2.2 Effectuer le relevé des ordonnances ... 66
5.2.2.3 Faire suivre le formulaire du bilan comparatif au département de pharmacie .. ... 66
5.2.2.4 Participer à produire le MSTP lors de la collecte de données initiale ... 67
5.2.2.5 Nuances des acteurs quant à l’implication de l’infirmière à l’admission ... 68
5.2.3 Implication attendue de l’infirmière au transfert ... 69
5.2.3.2 S’assurer que le médecin utilise le formulaire ... 70
5.2.3.3 Inscrire des éléments de suivi ... 71
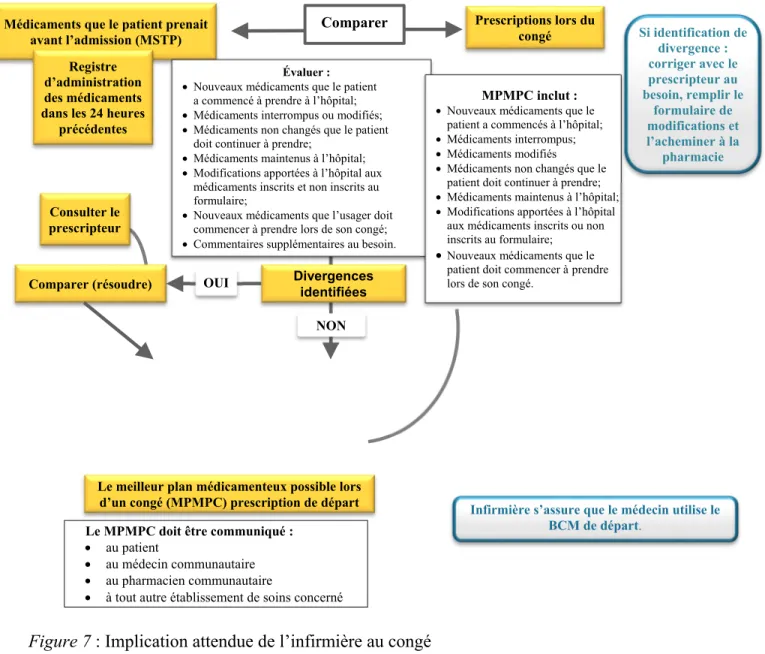
5.2.4 Implication attendue de l’infirmière au congé ... 71
5.2.4.1 L’infirmière s’assure que le médecin utilise le BCM de congé ... 72
5.2.5 L’implication attendue de l’infirmière dans la mise en œuvre du bilan comparatif des médicaments ... 73
5.3 Implication effective de l’infirmière dans la mise en œuvre du BCM ... 74
5.3.1 Implication propre et distinctive ... 75
5.3.1.1 Relever les ordonnances médicamenteuses ... 75
5.3.1.2 Enseigner lors de l’administration des médicaments ... 76
5.3.1.3 Aider lors des transitions médicamenteuses ... 76
5.3.2 Mobilisation nuancée ... 77
5.3.2.1 Coordonner la documentation requise ... 77
5.3.2.2 Communiquer les divergences médicamenteuses ... 78
5.3.2.3 Rappeler au médecin de remplir le BCM ... 81
5.3.3 Filet de sécurité ... 84
5.3.3.1 Vérifier le processus effectué ... 84
5.3.3.2 Vérifier le BCM avec la FADM ... 84
5.3.3.3 Identifier des cas à risque par rapport à la médication ... 85
5.3.4 Activités contributives ... 86
5 3.4.1 Documenter l’évaluation initiale ... 86
5.3.4.2 Enseigner à l’admission et au départ ... 87
5 3.4.3 Effectuer la surveillance clinique ... 88
6. Discussion ... 91
6.1 Discussion des résultats par rapport aux écrits ... 91
6.1.1 Implication de l’infirmière ... 91
6.1.1.1 Implication attendue et effective de l’infirmière ... 92
6.1.2 Implication auprès d’une clientèle adulte de cardiologie ... 95
6.1.3 Implication de l’infirmière en collaboration avec le pharmacien et le médecin 95 6.2 Discussion des résultats par rapport aux écrits théoriques ... 95
6.3 Limites de l’étude ... 96
6.3.1 Le recrutement et l’analyse ... 97
6.3.2 Entretiens limités et de courte durée ... 98
6.4.1 Recommandations pour la pratique ... 99
6.4.2 Recommandations pour la gestion des soins infirmiers ... 100
6.4.3 Recommandations pour la recherche en sciences infirmières ... 101
6.4.4 Recommandations pour l’enseignement ... 102
Conclusion ... 103
Références ... 105
Annexe 1 – Guide d’entretien semi-dirigé ... 111
Annexe 2 – Guide d’utilisation de la grille revue de dossiers patients ... 113
Annexe 3 – Avis d’experts – Élaboration grille de revue de dossiers patients ... 115
Annexe 4 – Grille de revue de dossiers patients ... 117
Annexe 5 – Grille d’extraction des données ... 121
Annexe 6 – Affiche – Recherche de participants ... 126
Annexe 7 – Formulaire de consentement ... 127
Liste des tableaux
1. Le circuit du médicament et les problèmes principaux associés ... 7
2. Détails des dossiers exclus ... 45
3. Présentation de l’échantillon selon les sources de données ... 46
4. Sommaire des sources documentaires retenues ... 46
5. Résumé des mesures employées pour assurer la qualité des données d’une étude de cas ... 54
Liste des figures
1. Illustration de la métaphore du fromage suisse ... 35
2. Le modèle de Reason, la théorie de la transition de Meleis et le bilan comparatif des médicaments. ... 38
3. Représentation schématique de l’étude de cas selon Rosenberg et Yates (2007) ... 39
4. Ligne du temps, déroulement de la collecte de données ... 42
5. Implication attendue de l’infirmière à la phase d’admission ... 66
6. Implication attendue de l’infirmière à la phase de transfert. ... 70
7. Implication attendue à la phase de congé ... 72
8. Implication effective de l’infirmière : catégories dégagées ... 74
Remerciements
Je désire transmettre mes plus sincères remerciements et exprimer ma reconnaissance et ma gratitude à ma directrice de recherche, madame Geneviève Roch, infirmière Ph. D., professeure à la Faculté des sciences infirmières de l’Université Laval. Sa patience, son savoir, sa rigueur scientifique, son approche rigoureuse et ses conseils m’ont permis de me dépasser au point de vue scientifique, personnel et professionnel, et de mener à terme ce projet de recherche.
Je désire également exprimer ma reconnaissance à madame Nathalie Thibault, qui a été pour moi un exemple professionnel ainsi qu’une personne clé dans la réussite de ce projet, par sa contribution à la collecte d’information, ses liens professionnels, ses conseils ainsi que son écoute.
Mes remerciements s’adressent également au CSSS Drummond pour le soutien offert, particulièrement à madame Élise Leclair, directrice des soins infirmiers, pour son appui personnel à ma réussite ainsi que sa présence inconditionnelle dans tous les moments, et qui est pour moi un modèle de réussite et une inspiration. De plus, je tiens à remercier monsieur Alain Bureau, chef du département de pharmacie, qui contribue à alimenter ma passion pour l’amélioration continue de la sécurité du circuit du médicament.
Par ailleurs, la réalisation de ce mémoire a été facilitée par le soutien financier de la compagnie Conseil en immobilisation & management inc. (CIM).
Finalement, je désire remercier spécialement Jacinthe et Denys; vous avez cru en moi et m’avez soutenu dans mes études. Sans vous, je n’y serais pas parvenue. Mes derniers remerciements s’adressent également à Katie, Stéphanie, Jessica, Isabelle et Geneviève pour votre patience, votre compréhension, votre écoute dans les moments difficiles et surtout votre indéfectible soutien. Merci tout le monde! Sans oublier tous ceux que je ne peux nommer.
Introduction
Le bilan comparatif des médicaments (BCM) est reconnu comme une pratique permettant d’éviter les divergences médicamenteuses non intentionnelles aux points de transition des patients, visant ainsi à éviter des erreurs pouvant causer des préjudices (Cornish et al., 2005). Le BCM peut être implanté de différentes façons selon les politiques, les procédures et les ressources disponibles dans les établissements (Institut pour l’utilisation sécuritaire des médicaments [ISMP], 2011). Pourtant, il existe peu de données sur l’implication des infirmières dans la mise en œuvre du BCM dans les milieux de soins. Dès lors, il apparaît nécessaire de documenter l’implication de l’infirmière dans la mise en œuvre du BCM. La présente étude vise à décrire l’implication de l’infirmière dans la mise en œuvre du BCM auprès d’une clientèle atteinte de problèmes cardiaques (insuffisance cardiaque, infarctus, angine) dans un centre hospitalier québécois.
Le premier chapitre décrit la problématique qui permet d’identifier les éléments de fond qui ont mené à établir le but de cette étude ainsi que les deux (2) objectifs de la recherche. Ceux-ci sont présentés à la fin de ce chapitre. Le deuxième chapitre permet de situer le concept de réconciliation médicamenteuse à la base du BCM. Il met aussi en relief ce que l’on sait de l’implication attendue et effective de l’infirmière dans la mise en œuvre du BCM. Le cadre de référence développé en vue de situer les concepts et les liens à l’étude, en regard du but et des objectifs poursuivis, est présenté dans le troisième chapitre. Le devis de recherche et la démarche méthodologique utilisée sont justifiés et exposés dans le quatrième chapitre. Le cinquième chapitre consiste à présenter les résultats en réponse au but et aux deux (2) objectifs poursuivis en présentant l’implication attendue et l’implication réalisée en référence aux quatre (4) catégories principales qui émergent des analyses.
La discussion des résultats suit, en mettant en relief la contribution de cette étude au développement des connaissances dans le domaine pratique de l’administration des services infirmiers, de l’enseignement et de la recherche. Les forces et les limites ainsi que les avenues de recherche futures sont aussi exposées. Finalement, la conclusion permet de reconnaître les retombées potentielles de cette étude.
1. Problématique
1.1 Mise en contexte de la problématique
Il est reconnu que les erreurs d’administration des médicaments constituent l’un des évènements indésirables les plus fréquents dans les services de santé (Aspden, 2007; Rozich et al., 2004). En contexte hospitalier, ce type d’erreurs est plus susceptible de se produire lorsque la prise de médicaments est interrompue ou modifiée, ou encore lorsque les médicaments sont changés à la suite de nouvelles prescriptions (Aspden, 2007). Un rapport américain de l’Institute of Medecine To Err is Human : Building a Safer Health System attribue plusieurs milliers de morts aux erreurs d’administration des médicaments (Khon, Corrigan, & Donaldson, 2000). Les organisations se doivent d’implanter des pratiques sécuritaires en matière de gestion du médicament (Khon et al., 2000). Au Canada, une étude démontre que les erreurs de médicaments aux points de transition (admission, transfert, congé) ont de multiples conséquences, telles que l’augmentation des coûts d’hospitalisation, d’autres problèmes de santé modérés à graves et même la mort (Baker et al., 2004). Au Québec, les incidents et accidents liés aux médicaments arrivent au deuxième rang (MSSS, 2014). En raison de leur présence auprès du patient, on reconnaît aux infirmières un rôle central dans la prévention des erreurs d’administration des médicaments (Brady, Malone, & Flemming, 2009; OIIQ, 2011). Lorsqu’il est question de processus de prévention organisationnels, leur implication demeure hautement imprécise, voire ignorée. Il est alors important de présenter : 1) la sécurité des patients et la prévalence des erreurs de médicaments; 2) les divergences médicamenteuses; 3) les moyens de prévention des erreurs de médicaments; 4) la gestion sécuritaire des médicaments et 5) le bilan comparatif des médicaments.
1.1.1 La sécurité des patients et la prévalence des erreurs de
médicaments
Selon Khon et al. (2000), la sécurité des patients se définit comme l’absence de blessures accidentelles. Selon Baker et al. (2004), les évènements indésirables sont des complications ou des blessures qui sont causées par les prestations des soins plutôt que par la maladie ou le problème de santé sous-jacent. Les évènements indésirables les plus fréquents reliés aux soins de santé sont les erreurs de médicaments (Khon et al., 2000). Au Québec, en 2013,
selon le Rapport semestriel des incidents et accidents survenus lors de la prestation des soins et des services de santé au Québec du 1er octobre 2012 au 31 mars 2013, les erreurs
de médicaments se sont classées au deuxième rang, ce qui représente 32,5 % des évènements déclarés. Par ailleurs, selon une étude canadienne, les erreurs de médicaments et de solutés arrivent au deuxième rang des évènements indésirables dans les milieux de soins (Baker et al., 2004). Parmi les conséquences des évènements indésirables pour les patients, notons qu’il peut survenir une augmentation de la durée du séjour, une incapacité et même la mort (Baker et al., 2004). De plus, dans une étude canadienne, après avoir reçu leur congé d’un service de médecine interne d’un hôpital, 23 % des 328 patients ont subi des évènements indésirables (Forster, Murff, Peterson, Gandhi, & Bates, 2003). Les trois quarts de ces évènements indésirables étaient reliés à la médication (Forster et al., 2003).
1.1.2 Les divergences médicamenteuses
Une divergence médicamenteuse est une différence entre les médicaments pris par le patient par rapport aux prescriptions. Cette différence est parfois désirée, mais parfois elle n’est pas intentionnelle et peut mener à une erreur de médicaments pouvant engendrer des conséquences sur la santé du patient. Selon l’étude de Cornish et al. (2005) il y a eu une divergence entre la médication qui était prise à la maison et celle prescrite lors de l’admission dans une unité de médecine interne pour 53,6 % des patients de leur échantillon. Pour participer à l’étude, le patient admis en médecine interne devait prendre au moins quatre (4) médicaments réguliers à la maison. Dans cette même étude, la divergence d’omission était la plus fréquente des types de divergences et représentait 46,4 % de celles recensées (Cornish et al., 2005). Une omission est en fait la non-represcription d’un médicament pris par le patient à la maison (Cornish et al., 2005). En effet, il y a quelques types de divergences qui sont reconnues, soit par des erreurs de dosage, d’addition de médicaments, de changements de médicaments et d’omission (Andreoli et al., 2014; Cornish et al., 2005; Lingard et al., 2004). Mentionnons également que, selon la recension des écrits de (Tam et al., 2005), basée sur 22 études (n = 3 755 usagers), il en ressort que 67 % des patients ont présenté des divergences entre les médicaments à l’admission et ceux à domicile devant être poursuivis. De plus, de 10 % à 61 % d’entre eux avaient été l’objet d’au moins une erreur d’omission au cours de leur
épisode de soins (Tam et al., 2005). De plus, aux États-Unis, on estime que 1,5 million d’erreurs de médicaments par année peuvent être prévenues, et ce, en excluant les erreurs d’omission (Aspden, 2007).
On remarque donc qu’il ne faut pas sous-estimer les erreurs de médicaments dans les milieux de soins, car elles sont bien présentes et peuvent survenir aux points de transition d’un patient. Cela nécessite de revoir et d’assurer la mise en œuvre de pratiques organisationnelles visant à assurer une gestion sécuritaire du médicament.
1.1.3 Moyens de prévention des erreurs de médicaments
Il existe plusieurs facteurs contribuant aux erreurs de médicaments sur lesquels l’infirmière peut intervenir. Il y a le système de distribution des médicaments, la divulgation des erreurs de médicaments, les déviances procédurales, les connaissances sur la médication et la réconciliation de l’histoire de santé et des prescriptions (Brady et al., 2009). De plus, selon Aspden (2007), pour améliorer la sécurité des médicaments, les intervenants impliqués (médecin, pharmacien et infirmière) doivent, avec le patient :
Revoir la liste de médicaments du patient à l’admission et aux points de transition; Expliquer les différentes options de traitement;
Revoir les noms des médicaments et le but de leur utilisation; Définir quand la médication doit être prise;
Discuter des effets indésirables importants et des actions à poser en présence d’effets indésirables;
Discuter des interactions avec les autres médicaments, avec la nourriture et avec d’autres maladies;
Revoir comment le patient peut s’impliquer dans la gestion sécuritaire;
Revoir le rôle de la médication par rapport au contexte dans lequel celle-ci est utilisée.
1.1.4 La gestion sécuritaire des médicaments
Il est important de bien situer la gestion sécuritaire des médicaments. La gestion sécuritaire du médicament est une démarche qui s’impose pour diminuer les erreurs de médicaments. Cette démarche comprend le système et les processus qu’une organisation adopte pour la pharmacothérapie. La gestion sécuritaire du médicament est multidisciplinaire et comprend les efforts coordonnés des intervenants vers les processus efficaces dans la conception,
l’implantation, l’amélioration de la sélection, l’approvisionnement et l’entreposage. Des actions concertées doivent être mises en œuvre pour sécuriser le système qu’est le circuit du médicament qui, lui, comprend : la prescription, la transcription, la distribution, la préparation/administration et la surveillance de la thérapie médicamenteuse (Aspden, 2007). La gestion sécuritaire du médicament implique l’éducation du patient, des membres de sa famille ou du soignant au sujet de l’utilisation de la médication, de l’administration, des effets attendus et des effets secondaires à surveiller (Joint Commission on Accreditation of Healthcare organizations [JCAHO], 2006). Agrément Canada (2014) inclut, dans les normes sur la gestion des médicaments, les actions suivantes : 1) planifier le mécanisme de gestion des médicaments, 2) assurer la formation et l’évaluation des compétences, 3) accéder aux renseignements sur le patient et les médicaments, 4) sélectionner et se procurer des médicaments, 5) entreposer les médicaments à la pharmacie et dans les unités de soins, 6) prescrire des médicaments et émettre des ordonnances, 7) préparer les médicaments, 8) étiqueter et emballer les médicaments, 9) délivrer et administrer les médicaments, 10) surveiller le patient et 11) évaluer le mécanisme de gestion des médicaments.
Le tableau qui suit résume les problèmes principaux du circuit du médicament relevés par Aspden (2007) et associés à l’étape de gestion des médicaments.
Tableau 1
Le circuit du médicament et les problèmes principaux associés Éléments du circuit du
médicament Problèmes principaux pouvant mener à l’erreur
Prescription
Prescripteur qui manque de connaissances;
Connaissances insuffisantes concernant les bénéfices du traitement par opposition aux risques associés au traitement;
Information incomplète concernant le patient;
Mauvaise évaluation initiale de la prise de médication et autres produits;
Manque de communication entre les différents intervenants;
Responsabilité du pharmacien insuffisante dans le processus de prescription.
Transcription Mauvaise communication entre les intervenants (erreurs lors de transcription). Préparation et distribution
Problème avec les médicaments ayant des noms semblables ou des emballages semblables;
Environnement stressant et distractions.
Administration et surveillance
Manque de temps pour avoir accès à l’information avant de procéder aux soins ou à l’administration des médicaments;
Manque de connaissances, oubli ou non-adhérence aux bonnes pratiques;
Mauvais dosage;
Environnement stressant et distractions. Divulgation Culture incriminante.
Auto-soins
Demande d’antibiotiques pour une condition qui ne le justifie pas (ex. : un rhume);
Non-adhérence au traitement;
Manque d’attention aux interactions avec les autres médicaments; Mauvaise surveillance des bons effets et des effets secondaires; Mauvaise connaissance de la gestion des effets secondaires. (Tiré d’Aspen, 2007)
1.1.5 Le bilan comparatif des médicaments
Comme le BCM peut être implanté de différentes façons, selon les politiques et les procédures de l’établissement, et pour que cette pratique soit efficace et que les retombées attendues par le BCM soient maximisées, il est important de connaître la contribution de chacun des professionnels et des intervenants de la santé impliqués dans la mise en œuvre de cette pratique organisationnelle, qui sera dorénavant exigée pour tous les établissements de santé canadiens qui doivent se conformer aux exigences d’Agrément Canada (ISMP, 2011; Niclyn, 2013). De plus, il est essentiel de connaître la façon dont l’infirmière s’implique dans la mise en œuvre du BCM. Alors que les attentes envers cette nouvelle pratique organisationnelle sont relativement claires à l’endroit des médecins et des pharmaciens par la présence de guides cliniques soutenant cette pratique, il semble qu’il en soit autrement par rapport à l’infirmière (Blais et al., 2009; Liang et al., 2008).
Un des facteurs favorisant l’implantation du BCM est la mise en place d’une politique désignant les intervenants responsables de celui-ci (ISMP, 2011). Une approche de collaboration interprofessionnelle est aussi un aspect à considérer pour la réussite de l’implantation du BCM (ISMP, 2011). Cependant, il est difficile de déterminer comment optimiser le partage des implications des différents intervenants dans la mise en œuvre du BCM (ISMP, 2011). Déterminer l’implication de l’infirmière au regard du BCM peut s’avérer un enjeu du point de vue de la sécurité des patients, particulièrement en ce qui a trait à la gestion sécuritaire du médicament. Même si le pharmacien peut effectuer l’histoire médicamenteuse d’un patient, une étude américaine révèle qu’elle n’est effectuée par celui-ci que pour 5 % des patients dans la plupart des hôpitaux (Sullivan, Gleason, Rooney, Groszek, & Barnard, 2005).
1.2 Urgence d’agir en contexte infirmier
Le problème provient particulièrement de l’urgence de mettre en place le bilan comparatif du médicament afin de diminuer les erreurs. Cette nécessité d’agir est présentée dans ce qui suit.
En 2011, devant l’urgence d’agir à l’échelle nationale, un sommet pancanadien a eu lieu pour adopter des stratégies visant à favoriser la mise en place du bilan comparatif du médicament (BCM), une pratique organisationnelle requise par Agrément Canada qui permet d’effectuer la réconciliation médicamenteuse de l’histoire du patient avec les prescriptions aux points de transition (admission, transfert, congé) afin de diminuer les erreurs de médicaments en identifiant les divergences médicamenteuses (ISMP, 2011). Il importe de renforcer les pratiques organisationnelles qui visent à réduire les erreurs de médicaments pour que la sécurité des patients soit assurée, de la prescription de la médication à l’administration de celle-ci (Aspden, 2007).
Il est important de définir le contexte infirmier dans lequel le bilan comparatif des médicaments s’inscrit. Ce contexte est divisé en trois aspects : 1) les enjeux de la mise en œuvre du BCM, 2) le cadre législatif et professionnel et 3) la clientèle de cardiologie.
1.2.1 Enjeux de la mise en œuvre du BCM
Il y a des guides de pratique sur la mise en œuvre du BCM pour les médecins et les pharmaciens (Liang, 2008; ISMP, 2011), mais il n’en n’existe pas pour les infirmières. De plus, il y a de nombreux écrits concernant les erreurs d’administration des médicaments faites par les infirmières. L’administration des médicaments étant complexe, plusieurs facteurs peuvent contribuer aux erreurs, tels que l’interruption et les distractions lors de l’administration, la charge de travail, les heures supplémentaires et l’expérience professionnelle (Biron, 2009; Lisby, Nielsen, & Mainz, 2005). Or, selon Brady et al. (2009), les facteurs reliés aux erreurs de médicaments sont nombreux et incluent des facteurs individuels et organisationnels. De plus, l’administration de la médication est seulement une partie du processus de gestion du médicament (Fijn et al., 2002).
Peu de recherches portent sur la mise en œuvre du BCM en contexte infirmier. Étant présente 24 heures sur 24 auprès de la clientèle hospitalisée, l’infirmière exerce un rôle de premier plan dans la continuité des services associés au circuit du médicament. Dans ce contexte, l’infirmière peut participer à prévenir les erreurs de médicaments (Brady et al., 2009). Elle est donc un acteur important pour éviter les évènements indésirables et s’assurer d’un suivi adéquat auprès des patients et des autres professionnels impliqués. Certains écrits qualifient d’ailleurs le service infirmier de « filet de sécurité », puisqu’il peut rattraper plusieurs erreurs avant qu’elles ne causent préjudice au patient (Tucker, 2004). Seulement, même si son rôle et ses implications au regard de la sécurité des patients apparaissent implicites, il importe de les rendre explicites par rapport à la mise en œuvre du BCM. En effet, l’infirmière a le potentiel de réduire les erreurs de médicaments susceptibles de se produire aux points de transition des patients.
À cause des contacts fréquents de l’infirmière avec le patient durant le processus d’utilisation de la médication, celle-ci peut améliorer significativement la qualité du processus lié à la gestion sécuritaire du médicament en suivant les protocoles, en participant au développement de nouveaux projets et en favorisant le succès de tous les
efforts pour améliorer la sécurité des patients reliée à l’utilisation des médicaments (Anderson, 2007).
Certains milieux de soins ont donc donné une place à l’infirmière dans la mise en œuvre du BCM (Pronovost et al., 2003; Sullivan et al., 2005). Par contre, les écrits traduisent une importante variabilité de l’implication de l’infirmière dans la mise en œuvre du BCM (Murphy, Oxencis, Klauck, Meyer, & Zimmerman, 2009; Sullivan et al., 2005; Walker-Cillo & Fowler, 2008; Young, 2008).
1.2.2 Cadre législatif et professionnel
Au Québec, l’article 107.1 de la Loi sur les services de santé et les services sociaux (LSSSS) stipule que « tout établissement doit obtenir l’agrément des services de santé et des services sociaux qu’il dispense auprès d’un organisme d’accréditation reconnu » (LRQ, c. S-4.2). Agrément Canada fait partie des organismes pouvant émettre des accréditations de soins et de services de santé pour les établissements de soins au Québec. Comme il y a beaucoup d’erreur de médicaments au Canada et que les divergences médicamenteuses aux points de transition d’un patient dans un continuum de soins ne sont pas sans risques. Dans un but de protection des patients, Agrément Canada oblige les établissements de santé à mettre en place une procédure de BCM. Les exigences sont similaires aux États-Unis. The Joint Commission on Accreditation of Healthcare Organizations, organisme américain comparable à Agrément Canada, demande à ce qu’un processus de réconciliation médicamenteuse soit en place pour l’obtention de l’accréditation des soins de santé offerts dans les établissements de soins américains.
Au Québec, par rapport aux lois qui régissent la pratique infirmière, l’implication de celle-ci dans la mise en œuvre du BCM n’est pas explicelle-cite. En effet, la Loi sur les infirmières et infirmiers définit l’exercice infirmier comme suit : « L’exercice infirmier consiste à évaluer l’état de santé d’une personne, à déterminer et à assurer la réalisation du plan de soins et de traitements infirmiers, à prodiguer les soins et les traitements infirmiers et médicaux dans le but de maintenir et de rétablir la santé de l’être humain en interaction avec son
environnement et de prévenir la maladie ainsi qu’à fournir les soins palliatifs. » (article 36, Loi sur les infirmières et les infirmiers) Il y a une activité professionnelle plus spécifique reliée à la médication : « Administrer et ajuster des médicaments ou d’autres substances, lorsqu’ils font l’objet d’une ordonnance. » Cette activité concède ainsi à l’infirmière un rôle clé dans l’administration médicamenteuse, mais sous-tend aussi l’importance de son implication dans toutes les pratiques visant la gestion sécuritaire des médicaments. L’Ordre des infirmières et infirmiers du Québec (OIIQ) a produit un guide clinique de vigilance de l’infirmière en pharmacothérapie où les activités de l’infirmière en lien avec les médicaments sont présentées (OIIQ, 2011). Les infirmières évaluent l’état de santé du patient, prennent la décision d’administrer ou non un médicament, ajustent la médication, complètent au besoin la préparation d’un médicament et vérifient les interactions médicamenteuses avant de les administrer. Leur implication se poursuit par l’administration de la médication, par la rédaction des données au dossier du patient sur la médication administrée et par la surveillance clinique du patient quant à l’effet escompté. Lorsqu’il y a apparition d’effets secondaires indésirables, elles corrigent la situation en effectuant, si nécessaire, un suivi avec le prescripteur. C’est aussi l’infirmière qui inscrit, au plan thérapeutique infirmier, toutes particularités relatives aux médicaments ou à d’autres substances afin de favoriser les effets thérapeutiques. Enfin, elle contribue à l’enseignement sur l’autogestion des médicaments (OIIQ, 2011). Bien que ce guide clinique ne fasse pas explicitement référence au BCM, on comprend que l’ajustement de la médication aux points de transition du patient fait partie de la pratique infirmière.
1.2.3 La clientèle de cardiologie
La clientèle de cardiologie est une clientèle particulièrement à risque de subir des erreurs de médicaments. Selon Fijn et al. (2002), les médicaments analgésiques, cardiovasculaires et gastro-intestinaux sont souvent impliqués dans les erreurs de prescriptions. Les personnes atteintes d’insuffisance cardiaque sont souvent âgées et la comorbidité, la polypharmacie et l’invalidité compliquent souvent les soins de ces personnes (Wong et al., 2008). Wong et al. (2008) ont étudié les données d’un sondage intitulé National Health and Nutrition Examination Survey (NHANES) afin de décrire la population américaine atteinte d’insuffisance cardiaque. Les périodes examinées sont 1988-1994, 1999-2002 et
2003-2008. Dans cette étude, 1 395 participants avec une insuffisance cardiaque ont été identifiés (n = 581; 1988-1994), (n = 280; 1999-2002), (n = 534; 2003-2008). L’âge moyen des participants était de 67,7 ans. Il est démontré que la consommation de médicaments a augmenté dans les deux dernières décennies, passant d’une moyenne de 4,1 médicaments à 6,4 médicaments (Wong et al., 2008). De plus, selon l’étude descriptive de Cowie et al. (2002), les patients atteints d’un nouveau diagnostic d’insuffisance cardiaque sont à risque d’hospitalisation durant le premier mois suivant le diagnostic. Sur un échantillon de 332 nouveaux cas d’insuffisance cardiaque, 294 cas ont été classés à risque d’hospitalisation. Durant la période de l’étude, 59 % des 294 cas ont été hospitalisés (Cowie et al., 2002). Dans l’étude de Fang, Alderman, Keenan, & Ayala (2010) aux États-Unis, le taux d’hospitalisation pour un infarctus du myocarde a été établi à 242 pour 100 000 personnes en 2003-2005. Ce taux a été calculé à l’aide du National Hospital Discharge Survey et la population civile de 1979 à 2005. Selon l’Agence de la santé publique du Canada (2009), en 2005-2006, 160 323 hospitalisations ont été reliées à une maladie cardiaque ischémique, 60 996 pour infarctus et 54 333 pour insuffisance cardiaque. En somme, la population atteinte de problèmes cardiaques consomme souvent plus d’un médicament, peut faire face à des hospitalisations fréquentes et nécessiter des ajustements de médicaments qui peuvent rendre le patient vulnérable à des erreurs.
1.3 But et objectifs de l’étude
Considérant que pour améliorer la qualité des soins de santé, les organisations doivent avoir une définition claire des rôles de chacun des acteurs (O'Rourke, 2003), cette étude vise à décrire l’implication de l’infirmière dans la mise en œuvre du BCM auprès d’une clientèle atteinte de problèmes cardiaques (insuffisance cardiaque, infarctus, angine) admise dans une unité de cardiologie d’un centre hospitalier québécois. Le choix de cette population s’explique par une prévalence ajustée de cardiopathies ischémiques qui ne va pas en diminuant au Québec mais qui tend à rester stable (Sauvé, 2014), mais aussi et surtout par la multiplication du nombre de changements ou d’ajustements médicamenteux lors d’un séjour hospitalier pour les types de problèmes cardiaques retenus. Pour atteindre ce but, deux objectifs de recherche sont poursuivis :
1) Documenter l’implication que l’infirmière devrait avoir dans la mise en œuvre du BCM auprès de patients admis à l’unité de cardiologie d’un centre hospitalier québécois à partir des guides de pratique internes et externes, et des principaux acteurs impliqués.
2) Décrire comment l’infirmière s’implique dans la mise en œuvre du BCM auprès de patients hospitalisés à l’unité de cardiologie d’un centre hospitalier québécois à partir des principaux acteurs impliqués.
2. Recension des écrits
Le présent chapitre présente les écrits recensés aux fins de cette recherche. Dans un premier temps, les bases conceptuelles du BCM sont présentées à partir du concept de réconciliation médicamenteuse qui sous-tend son opérationnalisation. Par la suite, les résultats d’écrits présentant l’implantation du BCM dans différents milieux de soins de courte durée sont proposés de manière à positionner les connaissances actuelles par rapport à l’implication des différents acteurs qui interviennent dans sa mise en œuvre.
2.1 Les fondements conceptuels
Le concept du BCM sera défini conceptuellement et opérationnellement, tel qu’il est compris à même la mise en œuvre du BCM. Les concepts apparentés et les composantes, tels que la revue des médicaments et le meilleur schéma thérapeutique possible, seront aussi conceptuellement situés, avant que ne soit présenté l’état des connaissances sur l’efficacité de la réconciliation médicamenteuse et sur l’implication des différents acteurs qui interviennent dans la mise en œuvre du BCM.
2.1.1 Concept de réconciliation médicamenteuse
La réconciliation médicamenteuse sert d’assise conceptuelle à la pratique organisationnelle requise nommée Bilan comparatif des médicaments par Agrément Canada. La réconciliation médicamenteuse se définit comme « la vérification systématique de l’histoire médicamenteuse et des ordonnances aux différents points de transition tels l’admission, le transfert et le congé qui sont des moments à risque d’erreurs » (Sullivan et al., 2005). Schwarz & Wyskiel (2006) utilisent une définition similaire. Murphy et al. (2009) amènent la notion de communication dans leur définition de réconciliation médicamenteuse : « La réconciliation médicamenteuse consiste à vérifier et à communiquer la médication d’un patient aux points de transition de soins à partir de l’histoire médicamenteuse du patient obtenue à l’admission. » (traduction libre, p. 2126) L’Institute for Healthcare Improvement insiste sur l’établissement et le maintien d’une liste complète de médicaments utilisés par le patient et la comparaison de cette liste avec les prescriptions du médecin à l’admission, au transfert et au congé (Berwick, Calkins, McCannon, & Hackbarth, 2006). Les erreurs
pouvant être évitées par la réconciliation médicamenteuse sont les erreurs d’omission, de duplication et de mauvais médicaments ou dosages (Berwick et al., 2006). Finalement, Rozich et al. (2004) mettent l’accent sur l’importance de corriger ou d’annoter les erreurs ou divergences médicamenteuses au dossier médical du patient.
2.1.1.1 Définition opérationnelle de la réconciliation médicamenteuse
La réconciliation médicamenteuse est le concept qui sous-tend la pratique organisationnelle requise d’Agrément Canada qu’est le BCM. Afin de bien comprendre la portée de la réconciliation médicamenteuse, soit le BCM, voici quelques définitions opérationnelles retenues s’y rattachant et recensées dans les écrits.
Selon Agrément Canada (2013), la pratique organisationnelle du BCM se définit ainsi : « Le BCM est un processus structuré et partagé dans le cadre duquel l’équipe de soins : 1. Collabore avec le patient, la famille et les soignants (selon le cas) et au moins une autre
source d’information pour produire le meilleur schéma thérapeutique possible (MSTP). Un MSTP est une liste de tous les médicaments d’ordonnance et en vente libre, les remèdes traditionnels, holistiques et à base de plantes médicinales, les vitamines et les suppléments;
2. Décèle et clarifie les différences (écarts) entre le MSTP et les médicaments prescrits aux points de transition;
3. Consigne des renseignements à jour sur les médicaments des patients et leur communique cette information (ainsi que le nom du prochain prestataire de services s’il y a lieu). »
L’ISMP (2011) y va avec une définition semblable en ajoutant la notion de gestion des médicaments et de moyens de communication : « Il s’agit d’un processus formel au cours duquel les professionnels de la santé travaillent de concert avec les patients, leur famille et les autres prestataires de soins de santé dans le but de s’assurer que les renseignements précis et exhaustifs sur les médicaments soient systématiquement communiqués à travers les interfaces de soins. Le BCM nécessite une analyse systématique et exhaustive de tous les médicaments pris par le patient pour s’assurer que les médicaments ajoutés, modifiés ou cessés soient évalués attentivement. Il représente une des composantes de la gestion des médicaments et permettra de fournir les renseignements permettant aux prescripteurs de prendre des décisions adéquates pour le patient (p.6). »
L’Association des pharmaciens des établissements de santé du Québec (2009) ajoute la notion d’adhésion du patient au traitement médicamenteux lors de l’établissement du meilleur schéma thérapeutique possible : « Le BCM consiste, dans un premier temps, en un processus formel de comparaison entre la liste des médicaments/produits (médicaments prescrits, ceux en vente libre et produits naturels) pris par le patient avant son admission dans l’établissement de santé et les ordonnances émises ainsi que celles valides au moment critique évalué d’un épisode de soins (admission, transfert, congé), et ce, en lien avec l’adhésion thérapeutique du patient. Dans un deuxième temps, ce processus permet d’identifier les divergences existantes entre les ordonnances de ces deux (2) listes afin que les interventions soient effectuées en vue d’éviter des erreurs de prescription (p. 11). »
2.1.1.2 Distinction entre la revue des médicaments et la réconciliation médicamenteuse
Il est important de bien distinguer la réconciliation médicamenteuse de la revue médicamenteuse. Le concept de la revue de la médication, en anglais la medication review, se définit « comme l’évaluation systématique de la pharmacothérapie d’un individu ayant pour but d’évaluer et d’optimiser la médication du patient par le changement ou la recommandation d’un changement dans les prescriptions » (Christensen & Lundh, 2013) (traduction libre, p. 1). Selon Christensen et Lundh (2013), c’est un concept qui implique « d’évaluer l’effet thérapeutique et la dangerosité de la médication tout en faisant le lien avec la condition clinique du patient. D’autres questions telles que l’adhérence, les interactions, le monitorage et la compréhension que le patient a de sa condition et de son traitement sont à inclure lorsque nécessaires » (traduction libre, p. 1). Le relevé des médicaments se veut aussi un élément important pour améliorer la qualité des prescriptions afin de prévenir la survenance d’évènements.
2.1.1.3 Composante de la réconciliation médicamenteuse : MSTP
Dans le cadre de la présente recherche, le meilleur schéma thérapeutique possible (MSTP), une composante de la réconciliation médicamenteuse, est la liste complète des médicaments constituée « de tous les médicaments d’ordonnance et en vente libre, des remèdes
traditionnels, holistiques et à base de plantes médicinales ainsi que la liste de toutes les vitamines et de tous les suppléments que le patient prend actuellement. Il indique également le nom, la dose, la fréquence et la voie d’administration de chacun d’entre eux » (Agrément Canada, 2014, p. 11). De plus, on retrouve quelques définitions dans les écrits. Penformis et al. (2012) mentionnent que le BCM « englobe la production d’une liste complète de tous les médicaments que le patient prenait avant l’admission, c’est-à-dire le meilleur schéma thérapeutique possible. Cette liste est établie grâce à diverses sources et comprend des renseignements sur les médicaments d’ordonnance, les médicaments en vente libre, les vitamines, les suppléments, ainsi que le nom du médicament, la dose, la fréquence et la voie d’administration » (p. 216). Cependant, la définition de l’ISMP (2015) est plus précise et comprend 1) les sources de renseignements utilisées pour indiquer tous les antécédents; 2) les renseignements complets sur chaque médicament; 2) l’indication selon laquelle la prise effective correspond à l’usage prescrit; 3) le nom et le numéro de la pharmacie communautaire; 4) les détails sur la gestion des médicaments à la maison et 5) l’utilisation de plaquettes calendriers.
Le MSTP ne comprend pas la notion d’évaluation des médicaments avec la condition clinique telle que présentée dans le concept de revue des médicaments, mais comprend l’établissement de la liste exhaustive des médicaments d’un patient qui est nécessaire pour effectuer la réconciliation médicamenteuse aux points de transition, c’est-à-dire qu’il inclut la comparaison de médicaments pris par le patient à l’admission, au transfert et au congé.
Cependant, l’établissement du meilleur schéma thérapeutique possible comporte des éléments qui rejoignent le concept de revue de la médication principalement pour Phan-Dang et Poulin (2009), pour qui la réalisation du BCM n’est pas terminée avec l’obtention de la liste des médicaments. À cette étape, la liste obtenue est examinée pour l’identification des problèmes associés à la pharmacothérapie et l’établissement d’un traitement pharmacologique optimal pour le patient.
2.1.2 Efficacité de la réconciliation médicamenteuse
Plusieurs études présentent l’implantation ou l’étude d’un groupement d’interventions pour démontrer l’efficacité de la réconciliation médicamenteuse (Varkey et al., 2007; Murphy, 2009; Schnipper, 2009). Les interventions présentées dans ces études sont la réconciliation médicamenteuse, la revue appropriée des médicaments, la communication avec un prestataire de soins externe et l’enseignement au patient. Certaines de ces études utilisent un groupe contrôle réparti au hasard. De plus, d’autres études sont plutôt des écrits pour améliorer des processus internes de qualité. Voici quelques écrits qui supportent la présence de la réconciliation médicamenteuse comme étant un des éléments efficaces pour diminuer 1) les réadmissions, 2) les divergences et 3) les coûts.
2.1.2.1 Éviter les réadmissions et les visites aux urgences
Une étude suédoise quasi expérimentale effectuée avec un groupe contrôle réparti au hasard a démontré une diminution de 80 % des réadmissions à l’Urgence liées aux médicaments dans les 12 mois suivant le congé du patient (Gillespie et al., 2009). Le groupe avec interventions a bénéficié d’un pharmacien attitré à l’unité d’hospitalisation pour effectuer la réconciliation médicamenteuse. Celui-ci effectuait le meilleur schéma thérapeutique possible du patient et s’assurait que les médicaments prescrits à l’admission à l’unité étaient adéquats. D’autres interventions étaient aussi mises en place telles que la transmission de l’information concernant les médicaments au prochain prestataire de soins concernant les changements de médicaments et un appel au patient à la maison deux mois après l’hospitalisation. À l’inverse, le groupe contrôle n’avait pas de pharmacien attitré à l’unité pour faire cela, et celui-ci recevait des soins usuels (clientèle de 80 ans et plus hospitalisée sur deux unités de médecine interne).
Une autre étude américaine quasi expérimentale utilisant aussi un groupe contrôle réparti au hasard a démontré une diminution des réadmissions de 38,1 % chez le groupe recevant des interventions contre 10 % chez le groupe contrôle recevant les soins usuels (Koehler et al., 2009). Dans cette étude, les interventions incluaient la réconciliation médicamenteuse par un pharmacien, l’éducation spécifique par rapport à sa condition, la planification du congé par un coordonnateur de soins et un suivi téléphonique après le congé.
Finalement, Grimes et al. (2010) ont démontré que de ne pas effectuer un processus de réconciliation médicamenteuse au congé pouvait être dangereux pour la sécurité des patients. Cette étude descriptive menée en Irlande a été effectuée à partir d’une revue de dossiers patients dans deux hôpitaux publics d’enseignement totalisant 900 lits. Un total de 9 569 prescriptions pour 1 245 épisodes de soins a été étudié. Au moins un médicament n’était pas réconcilié (erreur de prescription au départ ou changement de médicaments non documenté) dans 50,1 % des cas (n = 624). Pour 100 cas sélectionnés de façon aléatoire, l’impact des médicaments qui n’étaient pas réconciliés a été évalué. Certaines omissions de réconciliation avaient le potentiel de causer des problèmes modérés à sérieux auprès de 2 % des patients, et pour 1 % d’entre eux, une réadmission non planifiée dans les trois (3) mois suivant l’hospitalisation a été observée. Pour le reste des médicaments non réconciliés, 63 % avaient un potentiel de dangerosité modéré et 35 % présentaient un potentiel de dangerosité mineur, tandis que 37 % avaient un taux potentiel de réadmission non planifiée modéré et 62 % avaient un potentiel de réadmission non planifiée faible.
2.1.2.2 Identifier les divergences et les erreurs de médicaments
Il est important de bien comprendre les types de divergences pouvant être identifiés à l’aide de la réconciliation médicamenteuse. Selon l’ISMP (2011), la divergence intentionnelle « survient lorsque le prescripteur a consciemment pris la décision d’ajouter, de modifier ou de cesser un médicament et que sa décision est clairement documentée » (traduction libre, p. 6). Cette divergence peut ne pas être documentée; elle est alors considérée comme une divergence intentionnelle non documentée. L’ISMP (2011) définit aussi la divergence non
intentionnelle comme suit : « Elle survient lorsque le prescripteur a modifié, ajouté ou
omis involontairement de prescrire un médicament que le patient prenait à l’admission. » (traduction libre, p. 6) Ce type de divergence entraîne des erreurs de médicaments pouvant avoir de graves conséquences pour un patient, soit des évènements indésirables potentiels évitables liés aux médicaments. De plus, plusieurs écrits utilisent le terme erreurs de
médicaments lorsqu’une divergence identifiée a mené à un changement de prescriptions
Une étude quasi expérimentale auprès d’une clientèle cardiaque avec groupe contrôle réparti au hasard a démontré un taux de divergences médicamenteuses de 39 % pour le groupe avec intervention contre 68 % pour le groupe sans intervention recevant des soins usuels (Eggink, Lenderink, Widdershoven, & Bemt, 2010). L’intervention de réconciliation médicamenteuse consistait en l’implication d’un pharmacien pour communiquer les erreurs de prescriptions de congé au cardiologue, l’enseignement et la transmission de l’information à la pharmacie du secteur privé (Eggink et al., 2010).
Un rapport d’implantation de la réconciliation médicamenteuse démontre la diminution de
divergences de médicaments au congé en post-implantation d’une intervention de
réconciliation médicamenteuse (Murphy et al., 2009). Les divergences non
intentionnelles sont ainsi passées de 90 % à 47 % (95 % IC, 42-53 %; p < 0,001) en
chirurgie et de 57 % à 33 % (95 % IC, 28-38 %; p < 0,001) en médecine. Dans une autre étude, l’implantation d’un processus structuré de réconciliation médicamenteuse incluant le meilleur schéma thérapeutique possible (chez une population âgée de 65 ans et plus) a permis une diminution des divergences médicamenteuses non intentionnelles de 62 % pour le groupe contrôle et de 32 % pour le groupe avec l’implantation de la réconciliation médicamenteuse à l’admission par du personnel de la pharmacie (Bemt et al., 2013).
Dans une revue de dossiers patients de Gleason et al. (2004), l’implantation d’une réconciliation médicamenteuse a été démontrée efficace pour identifier des divergences
médicamenteuses pouvant causer des préjudices au patient. Cette étude consistait à
identifier le type, la fréquence et la sévérité des divergences à l’admission. Un échantillon de convenance de 204 dossiers de patients a été utilisé lors de cette étude. Les critères de sélection des patients nécessitaient d’être en mesure de donner leur histoire médicamenteuse et d’être admis directement dans une unité de médecine-chirurgie. La mise en place de la réconciliation médicamenteuse visait à comparer l’histoire médicamenteuse avec les prescriptions d’admission au dossier du patient. Au total, 241 divergences ont ainsi été identifiées par le processus de réconciliation médicamenteuse. Dans une autre étude avec un groupe contrôle non réparti au hasard et un groupe où la réconciliation médicamenteuse avait lieu à l’admission, la réconciliation médicamenteuse a permis de
diminuer de 43 % les évènements indésirables causés par des changements de prescriptions (Boockvar et al., 2011). Par ailleurs, lors d’une autre étude descriptive d’implantation d’un processus de réconciliation médicamenteuse de Rozich et al. (2004), la réconciliation médicamenteuse a permis de faire passer un taux d’évènements indésirables liés aux
médicaments de 76 par 10 000 doses de médicaments à 31 par 10 000 doses.
Dans une autre étude de Varkey et al. (2007) présentant un projet pilote d’implantation d’une réconciliation médicamenteuse à l’admission et au congé, la réconciliation médicamenteuse a été démontrée efficace pour diminuer l’occurrence des divergences. Ce projet pilote mené dans une unité de médecine familiale d’un hôpital américain comportait deux phases. En phase 1, il y a eu intégration de la réconciliation médicamenteuse à l’admission entre les médicaments pris à la maison par le patient et les médicaments prescrits à l’admission. En phase 2, la liste de réconciliations médicamenteuses d’admission et de congé a été incluse dans le sommaire d’hospitalisation. Ce projet pilote a permis, en phase 1, pour 51 patients avec des caractéristiques comparables, de diminuer le taux de 0,5 divergence par patient à 0 divergence par patient en post-implantation. Au congé, le taux de divergences est passé de 3,3 par patient à 1,8 par patient en post-implantation.
Au Québec, l’étude de Blanchet (2010), menée en centre hospitalier québécois, a démontré que le BCM était efficace pour identifier les divergences médicamenteuses aux points de transition. Cette étude descriptive transversale a été effectuée à la suite de deux projets pilotes visant l’implantation du BCM (Blanchet, 2010). Lors du premier projet pilote, un groupe de personnes impliquées dans la mise en œuvre du BCM a été sollicité pour commenter deux formulaires permettant la mise en œuvre du BCM. Lors de ce premier projet pilote, 465 bilans comparatifs du médicament ont été évalués : 1055 divergences ont été décelées, dont 68 % étaient intentionnelles et documentées par un médecin, et 717 divergences ont été documentées par un pharmacien, dont 47 % étaient non intentionnelles. Dans ce premier projet pilote, le taux de divergences s’élevait à 1,5 par patient. Le deuxième projet pilote a permis d’apporter des modifications sur le formulaire Bilan comparatif du médicament à la suite du premier projet pilote. Lors du deuxième projet pilote, 110 bilans comparatifs du médicament ont été révisés : 254 divergences ont
été décelées, dont 47 % étaient intentionnelles, 53 % non intentionnelles et 19 % liées à de la médication cardiaque nécessaire au traitement du patient. De plus, 4 % des divergences non intentionnelles ont engendré des effets sérieux. Ces effets sérieux sont définis comme ayant entraîné des signes et symptômes associés à un risque élevé, ne causant pas la mort, mais pouvant avoir causé une altération des activités journalières du patient. Dans ce deuxième projet pilote, le taux moyen de divergences était de 1,9 par patient (Blanchet, 2010).
Remarquons que, dans les écrits recensés, aucun ne traitait spécifiquement de l’efficacité de la réconciliation médicamenteuse à la phase de transfert, se concentrant principalement sur les phases de congé et d’admission. Or la clientèle de cardiologie, concernée par la présente étude, peut faire face à la phase de transfert, par exemple lors du passage des soins intensifs, en phase aiguë d’un épisode d’infarctus, à l’unité de soins régulière. Également, peu d’études portent spécifiquement sur la clientèle de cardiologie. De plus, la plupart des études parlent de l’implication des pharmaciens.
2.1.2.3 Diminution des coûts
Voici quelques écrits démontrant que la réconciliation médicamenteuse engendre une diminution des coûts pour les établissements de soins. Une étude effectuée aux Pays-Bas démontre que la prévention des erreurs engendrées par la réconciliation médicamenteuse effectuée au congé d’une unité de pneumologie amène une diminution des coûts (Karapinar-Çarkit et al., 2012). De plus, Karnon et al. (2009) ont effectué une analyse de coûts liés à l’efficacité du BCM effectué par un pharmacien à l’admission en milieu hospitalier qui a permis de confirmer la rentabilité du BCM par la diminution des erreurs de médicaments engendrée par la réconciliation médicamenteuse. Finalement, dans l’étude de Kilcup, Schultz, Carlson, et Wilson (2013), la comparaison d’un groupe contrôle sans intervention du pharmacien pour effectuer la réconciliation médicamenteuse et un suivi téléphonique après le congé à un groupe ayant reçu ces interventions, a démontré une économie de 35 000 $ pour 100 patients ayant un haut risque de réadmission. Aucun écrit recensé visant l’évaluation de la réduction des coûts associée à l’utilisation de l’infirmière
dans la mise en œuvre de la réconciliation médicamenteuse n’a été relevé dans le cadre de cette étude.
2.2 État des connaissances sur l’implication des différents
acteurs dans la mise en œuvre du bilan comparatif du
médicament
Il est important de bien situer comment se met en œuvre le BCM dans les milieux de soins. De plus, il est important de savoir quels sont les acteurs impliqués. Il y a une grande variabilité dans les façons de mettre en application le BCM. Il est clair que chaque organisation de soins doit trouver une façon de faire selon les ressources disponibles (Young, 2008). L’ISMP (2011) et Agrément Canada (2013) soulignent toutefois que les professionnels, particulièrement les médecins, les pharmaciens et les infirmières, doivent être impliqués dans la mise en œuvre du BCM. L’Association des pharmaciens des établissements de santé du Québec (2009) souligne que l’histoire médicamenteuse permettant l’établissement du meilleur schéma thérapeutique possible doit être effectuée par du personnel ayant une bonne connaissance de la médication afin de diminuer les évènements indésirables liés aux médicaments. Cependant, l’implication des professionnels n’est pas définie de façon statutaire. Il revient aux organisations de santé de déterminer l’implication des différents professionnels et non-professionnels impliqués dans la gestion médicamenteuse. Selon l’ISMP (2011), la personne qui recueille les renseignements relatifs au meilleur schéma thérapeutique possible devrait être un professionnel de la santé (médecin, pharmacien, infirmière, infirmière praticienne) dont le champ de pratique comprend cette activité. De plus, cette personne doit avoir une formation sur la façon de réaliser le MSTP : suivre une démarche systématique d’entrevue pour obtenir le meilleur schéma thérapeutique possible et être consciencieuse, responsable et imputable d’effectuer le meilleur schéma thérapeutique possible.
2.2.1 Implication du pharmacien
Certains écrits démontrent que le fait d’impliquer le pharmacien dans le processus de réconciliation médicamenteuse est efficace pour la diminution des réadmissions, l’identification de divergences médicamenteuses et pour la réduction des coûts (Karnon et
al., 2009; Kilcup et al., 2013). De ce fait, le pharmacien est impliqué pour établir le MSTP lors de la collecte de données initiale et pour l’identification des divergences (Gleason et al., 2004; Murphy et al., 2009; Varkey et al., 2007). Au Québec, un guide clinique d’implantation de la pratique organisationnelle requise par Agrément Canada, en lien avec la mise en place du BCM dans les milieux de soins québécois, est disponible pour les pharmaciens afin de connaître leur implication dans cette pratique (Association des pharmaciens des établissements de santé du Québec, 2009). Dans ce document, il est présenté que le pharmacien peut être impliqué lors de l’élaboration des outils de documentation liés à la mise en œuvre du BCM, soit le formulaire servant à compléter la collecte de données initiale sur la prise des médicaments du patient. De plus, il peut participer à la formation de non-professionnels, par exemple l’assistant technique en pharmacie, sur la collecte de données. Le pharmacien peut prendre également une ordonnance verbale dans le but de corriger une divergence médicamenteuse. Par ailleurs, le pharmacien peut procéder à l’analyse d’une divergence médicamenteuse.
L’étude de Murphy et al. (2009) présente une approche multidisciplinaire médecin, pharmacien et infirmière visant l’intégration de la réconciliation médicamenteuse dans un centre hospitalier américain à vocation d’enseignement. Dans cette approche, un pharmacien a été intégré pour faire la collecte de données initiale de la médication prise à la maison, soit l’établissement du MSTP. Par la suite, il y a la comparaison des ordonnances d’admission avec la liste de médicaments pris par le patient à la maison et obtenue par le pharmacien.
Selon Varkey et al. (2007), c’est aussi une approche multidisciplinaire de réconciliation. Dans ce projet pilote mené dans un hôpital américain, un médecin, un pharmacien et une infirmière ont participé à la mise en œuvre de la réconciliation. Ce projet comportait deux phases. En phase 1, il y a eu intégration de la réconciliation médicamenteuse à l’admission entre les médicaments pris à la maison par le patient et les médicaments prescrits à l’admission. Une fois à l’unité, le pharmacien attitré regardait le formulaire de réconciliations médicamenteuses et identifiait les divergences entre les médicaments pris à la maison par le patient et les médicaments prescrits à l’admission. Les divergences étaient
ensuite transmises au résident responsable du patient. Lors du congé, la médication de la liste sommaire d’hospitalisation était comparée avec les médicaments pris par le patient à la maison, le profil de médicaments utilisé en cours d’hospitalisation et les prescriptions médicamenteuses au congé. En phase 2, le personnel impliqué dans la réconciliation médicamenteuse a été formé pour inclure la liste de réconciliations médicamenteuses d’admission et de congé dans le sommaire d’hospitalisation.
Il est à retenir que le pharmacien peut être impliqué à plusieurs étapes de la mise en œuvre du BCM, autant dans la formation du personnel qui doit le mettre en œuvre que dans l’établissement du MSTP et la comparaison de celui-ci avec les prescriptions du patient.
2.2.2 Implication du médecin
Mentionnons que selon l’Association des pharmaciens des établissements de santé du Québec (2009), le Collège des médecins ne semble pas avoir pris position spécifiquement sur l’implication du médecin dans la mise en œuvre du BCM. Il n’y a pas de loi qui oblige un médecin à être responsable de tous les médicaments au congé. Cependant, le Collège des médecins reconnaît l’importance d’outils de gestion permettant de diminuer les évènements indésirables reliés aux médicaments (Association des pharmaciens des établissements de santé du Québec, 2009). Aux États-Unis, un guide clinique a été rédigé à l’attention du médecin concernant son implication dans la mise en œuvre du BCM (Liang et al., 2008). Selon Liang et al. (2008), le médecin est un leader dans le processus du BCM et peut agir, entre autres, dans l’établissement du MSTP, dans l’identification de divergences médicamenteuses et dans la correction des divergences médicamenteuses par la rédaction des ordonnances. Certaines études soulignent aussi l’implication du médecin pour la correction des divergences médicamenteuses et pour l’établissement du MSTP (Gleason et al., 2004; Rozich et al., 2004). Le médecin effectue également les prescriptions au congé (Murphy et al., 2009).