HAL Id: hal-02758775
https://hal.inrae.fr/hal-02758775
Submitted on 4 Jun 2020
HAL is a multi-disciplinary open access
archive for the deposit and dissemination of
sci-entific research documents, whether they are
pub-lished or not. The documents may come from
teaching and research institutions in France or
abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est
destinée au dépôt et à la diffusion de documents
scientifiques de niveau recherche, publiés ou non,
émanant des établissements d’enseignement et de
recherche français ou étrangers, des laboratoires
publics ou privés.
Transfert du diuron et de l’oryzalin en lysimètres dans
trois sols viticoles non perturbés (Vosne-Romanée, 21)
David Landry, Sylvie Dousset, Francis Andreux
To cite this version:
David Landry, Sylvie Dousset, Francis Andreux. Transfert du diuron et de l’oryzalin en lysimètres
dans trois sols viticoles non perturbés (Vosne-Romanée, 21). 31. Congrès du Groupe Français des
Pesticides, May 2001, Lyon, France. �hal-02758775�
229
Transfert du diuron et de l’oryzalin en
lysimètres dans trois sols viticoles non
perturbés (Vosne-Romanée, 21)
Leaching of diuron and oryzalin in undisturbed lysimeters
of three vineyard soils (Vosne-Romanée, 21)
D. LANDRY, S. DOUSSET, F. ANDREUX
UMR INRA A111 Microbiologie des Sols - GéoSol
Université de Bourgogne, Centre des Sciences de la Terre 6, boulevard Gabriel, 21000 Dijon, FRANCE
Tel : 03 80 39 37 24 - Fax : 03 80 39 63 87 E-mail : david.landry@u-bourgogne.fr
Résumé : La mobilité du diuron et de l’oryzalin a été étudiée en colonnes de sol non perturbé au laboratoire. Les sols étudiés sont trois sols viticoles de la région Bourgogne (Vosne-Romanée, 21) et ont été prélevés selon une topolithoséquence. Leurs teneurs en carbone organique sont respectivement de 1,2 %, 1,7 % et 2,2 % pour le sol brun calcaire de mi-pente (SBC MP), le sol brun calcaire de bas de pente (SBC BP) et la rendzine. Après une hauteur de pluie simulée de 845 mm, les percolats respectifs de la rendzine, du SBC MP et du SBC BP contiennent des quantités plus importantes de diuron (3,2 %, 11,8 % et 18,8 %), que d’oryzalin (0,2 %, 4,9 % et 3,7 % des quantités appliquées). Dans les colonnes de sol, les quantités extractibles de résidus herbicides sont plus élevées pour le diuron (48,7 %, 31,1 % et 35,6 %) que pour l’oryzalin (12,7 %, 11,9 % et 15,5 %) dans la rendzine, le SBC MB et le SBC BP respectivement. La distribution des deux herbicides au sein des colonnes de sol et les quantités percolées semblent en relation avec la teneur en matière organique du sol en surface et avec la structure du sol en profondeur.
Abstract : Mobility of diuron and oryzalin were studied in undisturbed soil columns in laboratory. Soils studied were three vineyard soils from Burgundy (Vosne-Romanée) and were chosen from a topolihoséquence. Organic carbon contents of this soils were 1,2 %, 1,7 % et 2,2 % for SBC MP, SBC BP and rendzine, respectively. After 845 mm of water applied, leachates of rendzine, SBC MP and SBC BP showed greater amounts of diuron (3,2 %, 11,8 % and 18,8 %) than oryzalin (0,2 %, 3,9 % and 4,7 % of applied) respectively. In soil columns, more residues were extractable for diuron (48,7 %, 31,1 % et 35,6 %) than for oryzalin (12,7 %, 11,9 % et 15,5 %) from the rendzine, SBC MB and SBC BP, respectively. Mobility of this two herbicides seems in relation to organic matter content in surface soils and to structure of the soils deeper.
Mots clés : diuron, oryzalin, lysimètre, sol structuré, sol viticole, lessivage
230
Introduction
La viticulture est l’une des activités majeures de l’économie bourguignonne. La facilité d’emploi de produits phytosanitaires, dans un vignoble de coteau à la topographie difficile, a favorisé un développement rapide des techniques de désherbage chimique dans les années 70. Ces produits phytosanitaires ont constitué un progrès essentiel pour la production viticole en assurant des rendements réguliers et la nécessaire qualité des produits. Mais un usage intensif de ces molécules a engendré, dans certaines situations, la présence de résidus de pesticides dans les eaux destinées à la consommation humaine. Ainsi, depuis 1992, le suivi des analyses d'eau réalisé par la DDASS dans le captage en eau potable de Vosne-Romanée montre la présence de produits phytosanitaires (notamment de diuron) à des concentrations supérieures à la norme Européenne de 0,1 µg.l-1 (Vey, 1998). L'oryzalin, utilisé abondamment par les viticulteurs de Vosne-Romanée, n'a jamais été retrouvé dans ces eaux. Lors de la contamination des eaux souterraines, et plus particulièrement des eaux de captage par les produits phytosanitaires, l’origine et les temps de résidence de ces molécules peuvent être déterminés en évaluant leur mode de transfert et leur réactivité. Le processus de transfert dépend des caractéristiques physico-chimiques du sol, des propriétés de la molécule et des facteurs climatiques tels que pluviométrie et température (Dousset et al., 1995). Le périmètre de protection éloigné du captage d'eau potable de Vosne-Romanée couvre une surface de 240 ha, dont 144 ha sont aujourd’hui plantés en vignes. Ce secteur a été choisi compte tenu de l'importance de la culture de la vigne dans cette région, de la présence de molécules herbicides dans les eaux du captage et de la volonté conjuguée du syndicat viticole et du syndicat des eaux de reconquérir la qualité de l'eau du captage de Vosne-Romanée. Les objectifs de ce travail sont donc d’étudier au moyen de lysimètres, dans le bassin-versant viticole de Vosne-Romanée, l’influence du type de sol sur le transfert du diuron et de l'oryzalin, et de déterminer les molécules herbicides présentant le moins de risque de contamination des nappes phréatiques. Ces résultats sont nécessaires pour la mise en place au terrain, de plans d'action compatibles avec les impératifs de la culture de la vigne et le respect de la qualité des eaux souterraines.
1. Matériel et méthode
1.1
Molécules
Le diuron [3-(3,4-dichlorophenyl)-1,1-dimethylurée], ses métabolites majeurs le DCPMU [N'-3,4-dichlorophenyl-N-methylurée], le DCPU [3,4-dichlorophenylurée] et le 3,4-DCA [3,4-dichloroaniline], (Dalton et al., 1966) ainsi que l’oryzalin [4-(dipropylamino)-3,5-dinitrobenzenesulphonamide] ont respectivement des puretés chimiques de 98,8 %, 99,9 %, 98,0 %, 99,0 % et 99,0 % (C.I.L., Bordeaux). Les caractéristiques chimiques de ces molécules sont présentées dans le tableau 1.
231
diuron oryzalin
Famille Phénylurées substituées Dinitroanilines Formule chimique C12H18N4O6S C9H10Cl2N2O
Koc ml.g
-1 400 700-1100
Solubilité (eau, 25°C) mg.l-1 36,4 2,6
T1/2 vie 4 à 8 mois 1,2 mois
Tableau n° 1 : Propriétés chimiques des molécules herbicides (d'après Tomlin et al., 1997)
1.2
Sols étudiés
Les trois sols Bourguignons (Vosne-Romanée (21), France) ont été prélevés dans la couche 0-20 cm, sur une topolithoséquence. Les caractéristiques principales de ces sols figurent dans le tableau 2. Sur le terrain, des monolithes de sol ont été isolés, en prenant soin de ne pas altérer la structure naturelle des sols. Des tubes en PVC (25 cm de long, 20 cm de diamètre interne) sont disposés autour de ces monolithes. Le vide existant entre le sol et le tube en PVC a été comblé par de la mousse expansée, afin de réduire les phénomènes d’écoulement préférentiel le long de la paroi interne des tubes. Les colonnes sont ensuite dégagées du sol et ramenées au laboratoire. sols > 2 mm a (%) pH eau Sables b (%) Limons b (%) Argiles b (%) C.O. c (%) rendzine 43,6 8,1 36,6 36,5 24,9 2,2 SBC MP 30,4 8,2 23,8 41,2 35,0 1,2 SBC BP 24,2 8,1 19,1 41,5 39,4 1,7
Tableau n° 2 : Propriétés physico-chimiques des sols étudiés
a >2 mm : fraction grossière des sols supérieure à 2 mm (en % du poids de sol sec) b Analyses granulométriques, en pourcentage du poids de la fraction < 2 mm c C.O. : teneur en carbone organique
1.3
Mise en place du dispositif
Au laboratoire, les colonnes sont placées sur un dispositif vertical conçu à cet effet. La base des colonnes repose sur une plaque en PVC perforée de trous de 2 mm de diamètre. Une toile à bluter (105 µm d'ouverture des mailles) est placée à la base de chacune afin d'empêcher les particules fines d'être entraînées par l'eau. Pour chaque modalité de traitement, une colonne par type de sol a été utilisée. L’aspersion des colonnes est assurée par une pompe péristaltique (ISMATEC MP 25) à un débit de 1,3 cm.h-1. Le volume d'eau total apporté en tête de colonne (845 mm) correspond à la pluviométrie annuelle (moyenne des 20 dernières années)
232
sur Vosne-Romanée. Un filtre en fibre de verre est placé sur la surface des sols, assurant une répartition homogène de l’eau à la surface de la colonne. Les percolats sont fractionnés et récupérés dans des flacons en polyéthylène toutes les 24 heures pendant les 15 jours de percolation.
1.4 Doses d'herbicides appliquées
Trente ml d’une solution méthanolique à 63,4 mg.l-1 de diuron (équivalant à une dose de 3,6 kg.ha-1) ou à 13,70 mg.l-1 d'oryzalin (équivalant à une dose de 7,7 kg.ha-1) sont uniformément appliqués à la surface du sol de chaque colonne. Les deux herbicides restent en contact pendant 48 heures avec le sol sec, avant d'appliquer la pluie simulée.
1.5 Collecte et analyse des percolats
Les percolats sont récupérés toutes les 24 heures. Les flacons sont pesés pour déterminer les volumes des échantillons. Ces derniers sont filtrés à 0,45 µm (filtres Millipore en nitrate de cellulose) et extraits en phase solide à l’aide de cartouches LC-18 (Supelclean). Les cartouches sont conditionnées par addition de 10 ml de méthanol puis de 10 ml d’eau distillée. Les résidus d’herbicides fixés par ces cartouches sont élués par 3 ml de méthanol puis évaporés à sec à l'aide d'un évaporateur rotatif à 30°C. Les résidus sont ensuite récupérés dans 3 ml de méthanol. Les molécules sont dosées en HPLC avec détection à barrettes de diodes. Les conditions analytiques sont les suivantes : colonne C18 en phase
inverse (15 cm x 4,6 mm), phase mobile composée d’acétonitrile et d’eau (70:30, v/v; débit de 0,8 ml.min-1) pour l'analyse des phénylurées et (50:50, v/v; débit de 1,2 ml.min-1) pour l’analyse de l'oryzalin. La détection UV est réalisée à 251 nm
pour le diuron, le DCPMU et le DCA, à 247 nm pour le DCPU (Field et al., 1997) et à 254 nm pour l'oryzalin (Kennedy, 1977). Les détections limites sont de 0,04 µg.l-1 pour le diuron, de 0,06 µg.l-1 pour le DCPMU,de 0,05µg.l-1 pour le DCPU, le DCA et l'oryzalin.
1.6 Extraction des sols et analyses
A la fin de la percolation, les colonnes de sol sont découpées en 4 niveaux de 5 cm de hauteur, séchées à l’air et tamisées à 2 mm. 50 g de sol sont extraits par 100 ml d'un mélange de méthanol/eau (80/20, v/v). Les échantillons sont agités pendant 10 heures à l'aide d'un agitateur rotatif, puis centrifugés pendant 20 minutes à 5500 rpm. Trois extractions successives sont effectuées. L'ensemble de ces extractions est mélangé puis évaporé à sec à l'aide d'un évaporateur rotatif (30°C). Les résidus sont repris dans 3 ml de méthanol et dosés par HPLC dans les conditions décrites précédemment.
233
2. Résultats et discussion
2.1 Teneur en résidus herbicides dans les percolats
Les quantités éluées cumulées des herbicides sont représentées en fonction des hauteurs éluées cumulées des percolats des colonnes (figure 1).
Fig. n° 1 : Quantités éluées cumulées d'herbicides (en % des quantités appliquées) en fonction de la hauteur d'eau éluée cumulée (mm)
Dans les percolats de la rendzine, du SBC MP et du SBC BP, le diuron est détecté à partir de 217 mm, 110 mm et 55 mm d’eau éluée respectivement. En fin d’expérience, soit pour une hauteur moyenne d’eau éluée de 773,8 ± 4,8 mm, les
hauteur d'eau éluée cumulée (mm)
200 400 600 800 C /C o de di ur on pe rc ol é 0 5 10 15 20
hauteur d'eau éluée cumulée (mm)
200 400 600 800 C /C o d'o ry zal in p erc ol é 0 5 10 15 20 rendzine SBC MP SBC BP oryzalin diuron rendzine SBC MP SBC BP dcpmu
234
percolats de la rendzine, du SBC MP et du SBC BP contiennent respectivement 3,2 %, 11,8 % et 18,8 % du diuron appliqué.
Le DCPU et le DCA ne sont retrouvés dans aucun des percolats. Le DCPMU n’est pas détecté dans les percolats de la rendzine mais dans ceux des deux SBC. Le DCPMU apparaît 7 jours après l’application du diuron dans le SBC MP, soit après 310 mm d’eau éluée et 4 jours après l’application du diuron, soit après 172 mm d’eau éluée, dans le SBC BP. Les quantités cumulées de DCPMU sont de 0,6 % et de 0,8 % du diuron appliqué dans les percolats respectifs du SBC MP et du SBC BP.
L'oryzalin est détecté dans les percolats des SBC MP et SBC BP pour des hauteurs d'eau éluées cumulées respectives de 114 mm et de 57 mm. L'oryzalin n'est détecté que dans 50 % des percolats de la rendzine. En fin de percolation, soit pour une hauteur moyenne d’eau éluée de 766,5 ± 2,7 mm, les pourcentages totaux d'oryzalin récupérés sont de 0,2 %, 4,9 % et 3,7 % dans les percolats respectifs de la rendzine, du SBC MP et du SBC BP.
2.2 Distribution des herbicides dans les sols
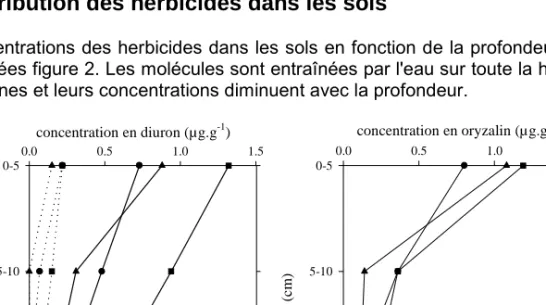
Les concentrations des herbicides dans les sols en fonction de la profondeur sont représentées figure 2. Les molécules sont entraînées par l'eau sur toute la hauteur des colonnes et leurs concentrations diminuent avec la profondeur.
Fig. n°2 : Concentration en herbicide (µg.g-1) dans les différents niveaux de sols
concentration en oryzalin (µg.g-1) 0.0 0.5 1.0 1.5 pr of o ndeu r ( c m ) 0-5 5-10 10-15 15-20 concentration en diuron (µg.g-1) 0.0 0.5 1.0 1.5 pr of o ndeu r ( c m ) 0-5 5-10 10-15 15-20 rendzine SBC MP SBC BP diuron dcpmu rendzine SBC MP SBC BP
235
Les concentrations en diuron dans le niveau 0-5 cm sont de 1,32 µg.g-1 dans la rendzine, de 0,88 µg.g-1 dans le SBC MP et de 0,73 µg.g-1 dans le SBC BP. Dans les niveaux 5-20 cm, les concentrations en diuron sont plus élevées dans la rendzine que dans les SBC. Les concentrations en diuron sont plus élevées dans le SBC MP que dans le SBC BP dans les niveaux 5-20 cm. Parmi les métabolites du diuron, le DCPMU et le DCA n'ont pas été retrouvés dans les sols. Dans la rendzine, le DCPMU migre le plus profondément à des concentrations variant de 0,22 µg.g-1 dans l’horizon 0-5 cm à 0,07 µg.g-1 dans l’horizon 10-15cm. Dans le SBC MP, le DCPMU est présent dans la couche 0-5 cm, à une concentration de 0,22 µg.g-1 et dans la couche 5-10 cm, à une concentration de 0,07µg.g-1. Dans le SBC BP, le DCPMU est uniquement détecté dans l’horizon 0-5 cm, à une concentration de 0,15 µg.g-1.
Les concentrations en oryzalin dans l’horizon de surface 0-5 cm des sols sont de 1,19 µg.g-1 dans la rendzine, de 0,8 µg.g-1 dans le SBC MP et de 1,08 µg.g-1 dans le SBC BP. En profondeur, les concentrations en oryzalin sont plus élevées dans la rendzine que dans les deux SBC. Elles sont également plus élevées dans le SBC MP que dans le SBC BP.
Dans l'horizon de surface (0-5 cm), la rétention des herbicides est en relation avec la teneur en carbone organique des sols. En effet, les concentrations en diuron et en oryzalin sont les plus élevées dans la rendzine à 2,2 % de carbone organique et sont les plus faibles dans le SBC MP à 1,2 % de carbone organique. La teneur en matère organique des sols serait la première responsable de l’adsorption de l’oryzalin (Fourie, 1992 ; 1993) et du diuron (Madhun et Freed, 1987). En profondeur, un autre facteur interviendrait sur la mobilité des herbicides : la rendzine présente une fraction grossière de 43,6 % et contient plus de sables et moins d'argiles et de limons que les deux SBC. Ces caractères peuvent se traduire par une meilleure stabilité de la structure du sol, accordant un meilleur potentiel pour la migration des herbicides (Monnier, 1994 ; Futch et Singh, 1999). Le SBC MP présente une fraction grossière de 30,4 % et le SBC BP de 24,2 %. Cette différence peut également être à l'origine d'une plus grande mobilité des molécules dans le SBC MP en profondeur.
2.3 Bilan de masse
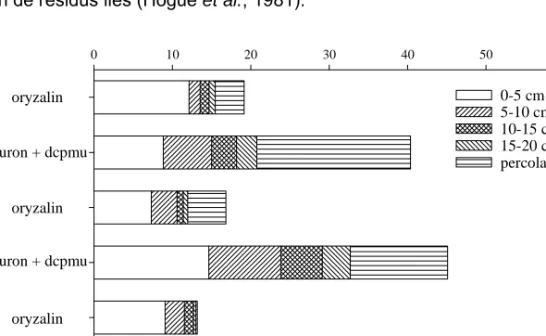
La figure 3 représente les quantités totales de résidus d'herbicides retrouvés dans les percolats et dans les sols. Ces pourcentages sont, respectivement dans la rendzine, le SBC MP et le SBC BP, de 51,85 %, 43,53 % et 55,23 % pour le diuron et de 13,19%, 16,82 % et 19,13 % pour l’oryzalin. Les faibles quantités d’oryzalin retrouvées pourraient s’expliquer par des processus de dégradation (Golab et al., 1975 ; Fourie, 1992 ; 1993). L’absence d'étalons de métabolites de l'oryzalin n'a pas permis de quantifier ces résidus. La formation de résidus liés, réduisant rapidement les quantités disponibles pour la percolation, pourrait également être à l’origine des faibles quantités d’oryzalin retrouvées (Golab et al., 1975). Les quantités d'oryzalin sont majoritairement retrouvées à la surface des sols.
236
Pour le diuron, 45 % à 55 % du diuron appliqué a disparu. Ce phénomène pourrait s'expliquer par une perte par photodécomposition et volatilisation de la molécule (Khan et al., 1976), par la minéralisation du diuron (Khan et al., 1976) ou par la formation de résidus liés (Hogue et al., 1981).
Fig. n° 3 : Quantités totales de résidus herbicides retrouvées en fonction des quantités appliquées
Conclusion
La distribution des deux herbicides dans les sols confirme leur relative mobilité dans les percolats. Au même taux d'application d'eau, la migration du diuron est supérieure à celle de l'oryzalin pour chacun des sols. Ces travaux confirment ceux de Futch et Singh (1999) quant à la mobilité plus grande du diuron par rapport à l'oryzalin. La rétention des molécules semblerait fortement liée à la teneur en carbone organique dans les horizons de surface des sols. En profondeur, la différence de structure des sols pourrait expliquer la plus forte mobilité des herbicides dans la rendzine comparée aux SBC. Des conditions expérimentales de l'étude, le lessivage au travers des trois sols viticoles, donc le risque potentiel de transfert vers les nappes phréatiques, s'avère plus important pour le diuron que pour l'oryzalin. % d'herbicide retrouvé 0 10 20 30 40 50 60 0 10 20 30 40 50 60 diuron + dcpmu diuron + dcpmu diuron + dcpmu oryzalin oryzalin oryzalin REN D ZI NE SBC BP SBC MP 0-5 cm 5-10 cm 10-15 cm 15-20 cm percolat
237
Références
Dalton R.L., Evans A.W., Rhodes R.C., 1966 -Disappearance of diuron from cotton field soils, Weeds, 14, p. 31-33.
Dousset S., Mouvet C., Schiavon, M., 1995 -Leaching of atrzine and some of its metabolites in undisturbed field lysimeters of three type soils, Chemosphere, 30
(3), p. 511-524.
European Community, 1980 -Council Directive on the quality of water for human consumption, Official Journal of the EC, 80/778 EEC L229, p. 11-29.
Field A.J., Reed R.L., Sawyer T.E., Martinez M., 1997 -Diuron and its metabolites in surface water and ground water by solid phase extraction and in-vial elution,
J. Agric. Food Chem., 45, p. 3897-3902.
Fourie J.C., 1992 -Herbigation in a vineyard :persistence of four pre-emergence herbicides in a sandy loam soil, S. Afr. J. Enol. Vitic., 62 (2), p. 64-68.
Fourie J.C., 1993 -Herbigation in a vineyard :persistence of five pre-emergence herbicides in a sandy soil, S. Afr. J. Enol. Vitic., 14 (1), p. 3-10.
Futch S.H., Singh M., 1999 -Herbicide mobility using soil leaching columns, Bull.
Environ. Contam. Toxico., 62, p. 520-529.
Golab T., Bishop C.E., Donoho A.L., Manthey J.A., Zornes L.L., 1975 -Behaviour of
14C oryzalin in soil and plants, Pest. Biochem. and Physiol., 5, p. 196-204.
Hogue E.J., Khan S.U., Gaunce A., 1981 -Leaching of four orchard herbicides in soils columns, Can. J. Soil Sci., 61, p. 401-407.
Kennedy JH., 1977 -High pressure liquid chromatographic analysis of oryzalin and other selected herbicides, Journal of chromatographic science, 15, p. 79-81. Khan S.U., Marriage P.B., Saidak W.J., 1976 -Persistence and movement of diuron
and 3,4-Dichloroaniline in an Orchard soil, Weed Science, 24, p. 583-586. Madhun Y.A., Freed V.H., 1987 -Degradation of the herbicides bromacil, diuron
and chloroluron in soil, Chemosphere, 16, p. 1003-1011.
Monnier G., 1994 -Assemblage et organisation physique des particules, In
Bonneau M., Souchier B., Constituants et propriétés du sol, 2nde édition, p. 324-345.
Tomlin C.D.S., 1997-The pesticide manual, BCPC, UK.
Vey F., 1998 -Eau et produits phytosanitaires : diagnostic et plan d'action pour la reconquête de la qualité de l'eau du captage de Vosne-Romanée, Rapport