HAL Id: hal-02165227
https://hal.archives-ouvertes.fr/hal-02165227
Submitted on 25 Jun 2019
HAL is a multi-disciplinary open access
archive for the deposit and dissemination of
sci-entific research documents, whether they are
pub-lished or not. The documents may come from
teaching and research institutions in France or
abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est
destinée au dépôt et à la diffusion de documents
scientifiques de niveau recherche, publiés ou non,
émanant des établissements d’enseignement et de
recherche français ou étrangers, des laboratoires
publics ou privés.
Contrôle de la vectorisation des xénobiotiques chez les
plantes : une nouvelle manière d’aborder le ciblage des
parasites afin de réduire les impacts environnementaux
Hanxiang Wu, Sophie Marhadour, Zhiwei Lei, Cécile Marivingt-Mounir, Rémi
Lemoine, Jean-Louis Bonnemain, Jean-François Chollet
To cite this version:
Hanxiang Wu, Sophie Marhadour, Zhiwei Lei, Cécile Marivingt-Mounir, Rémi Lemoine, et al..
Con-trôle de la vectorisation des xénobiotiques chez les plantes : une nouvelle manière d’aborder le ciblage
des parasites afin de réduire les impacts environnementaux. Métrologie des pesticides et évaluation des
risques pour l’Homme et pour les milieux naturels, Editions du GFP, pp.25-26, 2019. �hal-02165227�
Contrôle de la vectorisation des xénobiotiques chez les plantes :
une nouvelle manière d’aborder le ciblage des parasites afin de
réduire les impacts environnementaux
Hanxiang Wu
(1), Sophie Marhadour
(1), Zhiwei Lei
(2), Cécile Marivingt-Mounir
(1), Rémi
Lemoine
(3), Jean-Louis Bonnemain
(3), Jean-François Chollet
(1)(1) IC2MP (Institut de Chimie des Milieux et des Matériaux de Poitiers), UMR CNRS 7285, Université de
Poitiers, 4 rue Michel Brunet, TSA 51106, F-86073 Poitiers Cedex 9, France
(2) Guizhou Tea Reasearch Institute, Guizhou Academy of Agricultural Science, Guiyang, Guizhou 550009,
China.
(3) Laboratoire EBI (Écologie et Biologie des Interactions), UMR CNRS 7267, Équipe SEVE (Sucres, Échanges
Végétaux, Environnement), Université de Poitiers, 3 rue Jacques Fort, TSA 51106, F-86073 Poitiers Cedex 9, France
Avec l’intérêt croissant de la société contemporaine pour les sujets ayant trait à la santé humaine et à l'environnement, on observe une nette volonté pour réduire l'utilisation des pesticides dans le monde entier. Cependant, réduire l'utilisation des composés phytopharmaceutiques sans affecter la quantité et la qualité des produits est devenu l'un des grands défis du XXIe siècle. Pour concilier la demande de réduire les doses avec
celle de maintenir une efficacité optimum des produits phytosanitaires, un meilleur ciblage des parasites est devenu l’une des priorités du développement agrochimique. De ce point de vue, les produits agrochimiques et pharmaceutiques modernes ont les mêmes exigences de développement. Tout comme les médicaments, les pesticides nécessitent une administration ciblée pour assurer une concentration élevée sur le site d'action, ceci tout en limitant la toxicité dans les organes ou organismes non ciblés. Ainsi, certaines stratégies de libération ciblée de médicaments sont également applicables à la recherche et au développement de produits agrochimiques pour améliorer la biodisponibilité de nouveaux ingrédients actifs.
La stratégie de prodrogue (Fig. 1) s'est révélée être un moyen efficace pour améliorer les propriétés physico-chimiques ou biologiques de la molécule médicamenteuse de manière à améliorer sa biodisponibilité [1]. L'une des approches attrayantes pour la conception de prodrogues est de conjuguer un médicament avec des substrats endogènes, les molécules résultantes pouvant être reconnues et transportées par des transporteurs membranaires [2-4]. Les transporteurs de médicaments sont maintenant largement reconnus comme des déterminants importants régissant leur absorption, leur excrétion et, dans de nombreux cas, l'ampleur de leur entrée dans les organes cibles [5]. Les transporteurs de médicaments fréquemment exploités comprennent des transporteurs d'acides aminés et de glucose.
48 congrès du Groupe Français des Pesticides, 30 mai – 1 juin 2018, LIMOGES
Cette stratégie utilisant un mécanisme de transport actif fournit également une nouvelle voie possible pour la vectorisation de produits phytopharmaceutiques, ce qui peut conduire à une translocation et à une distribution vers des sites cibles en utilisant des transporteurs de la membrane plasmique végétale. Au cours des deux dernières décennies, quelques travaux ont été réalisés pour améliorer la mobilité ou la translocation phloémienne de pesticides vers le système racinaire en utilisant des transporteurs de sucre ou d'acides aminés de la membrane plasmique (Fig. 2) [7-9]. Le développement d'insecticides et
Figure 2. Transporteurs possiblement impliqués dans le
chargement de xénobiotiques par le tissu phloémien (d’après Réf. [8]) de fongicides phloème-mobiles est une nécessité avérée depuis longtemps. Par exemple, les fongicides systémiques phloémiens pourraient être appliqués sur le feuillage pour contrôler des maladies vasculaires ou racinaires, là où les fongicides actuellement commercialisés sont incapables de le faire.
De même, cette stratégie de prodrogue a été explorée quant à la prise en charge de composés phytopharmaceutiques par un transporteur de nutriments, le but de cette étude étant d'exploiter la possibilité de développer des profongicides phloème-mobiles pour contrôler les maladies vasculaires. Le fenpiclonil, fongicide de contact de la famille des phénylpyrroles, a été choisi comme composé modèle. Selon la stratégie de prodrogue, les molécules profongicides souhaitées ont été obtenues en introduisant soit un acide aminé, soit du glucose. L'effet de l'acide aminé ou du glucose sur le transport phloémien des conjugués synthétisés a été étudié comparativement en utilisant des plantules de Ricinus
communis (Fig. 3) et le mécanisme de transport actif
impliqué dans la translocation des différents conjugués a été examiné.
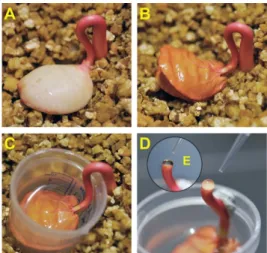
Figure 3. Le modèle Ricin utilisé pour
l’évaluation de la systémie des conjugués synthétisés
Dans une première partie [10], notre objectif était de sélectionner un groupement/nutriment optimal
pour mener à bien une stratégie de vectorisation des produits phytopharmaceutiques, celle-ci étant basée sur un mécanisme de transport actif via les systèmes de transport des nutriments chez les plantes. Le fenpiclonil, un fongicide non systémique de la famille des phénylpyrroles, a été choisi comme molécule modèle parent pour tester notre stratégie de vectorisation et, en premier lieu, pour comparer la capacité des systèmes de transport d'acides aminés et de sucres à prendre en charge des xénobiotiques chlorés volumineux. La méthode dite de “click chemistry” a été utilisée pour synthétiser trois conjugués (Fig. 4A) combinant le fenpiclonil au glucose ou à l'acide glutamique, ceci en introduisant un espaceur contenant un cycle triazole. Dans les tests de systémie, la mobilité phloémienne des conjugués associant l'acide L-glutamique ou le D-glucose et le fenpiclonil a été
comparée en utilisant des plantules de Ricinus communis. La concentration du conjugué L-aminoacide/fenpiclonil dans la sève phloémienne est environ 20 fois plus élevée que celle observée avec le conjugué D-glucose/fenpiclonil (Fig. 4B, C), suggérant qu’un acide aminé est nettement plus favorable à la mobilité phloémienne que le glucose. Une étude plus poussée du mécanisme de transport actif a révélé que la systémie du conjugué avec l’acide L-glutamique dépend du pH et est presque complètement inhibée par le protonophore carbonylcyanure m-chlorophénylhydrazone (CCCP). En outre, en considérant que la concentration dans la sève phloémienne du conjugué obtenu avec l’acide L-glutamique est cinq fois plus élevée que celle obtenue avec le dérivé de la série D (Fig. 4B), nous avons conclu que le transport phloémien du conjugué acide L-glutamique/fenpiclonil est régi par un système de transport d’acide aminé stéréospécifique énergisé par la force proton-motrice.
Figure 4. Structures et comparaison de la mobilité phloémienne de conjugués associant le
fenpiclonil à un nutriment. A : Structure du conjugué avec le D-glucose (12), d’un conjugué avec l’acide L-glutamique (L-13) et d’un conjugué avec l’acide D-glutamique (D-13). B : Comparaison de la mobilité phloémienne de L-13 et D-13. C : Mobilité phloémienne de 12 à 100 et 500 µM.
Dans un second temps [11], nous avons étudié les limites de notre stratégie de vectorisation avec le
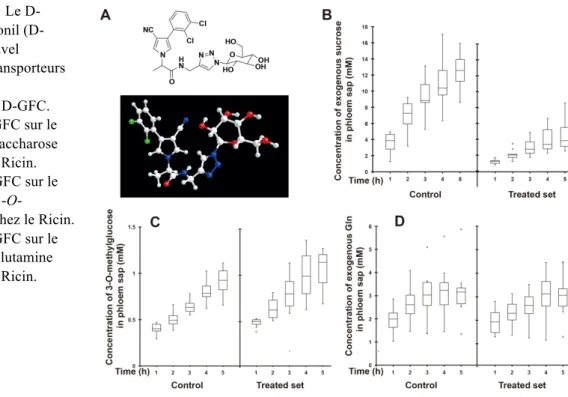
conjugué D-glucose/fenpiclonil (D-GFC) qui présente une très faible mobilité phloémienne contrairement au conjugué fenpiclonil/acide L-glutamique (L-13). Nous avons émis l'hypothèse que le D-GFC peut être reconnu par les transporteurs de saccharose, mais la taille (Mr = 551.38) et la structure amphiphile (Fig. 5A) du conjugué sont complètement inappropriées pour la translocation compte tenu des exigences structurales moléculaires requises pour l'activité du transporteur de saccharose. L'effet du D-GFC à une concentration de 0,5 mM sur l’absorption du saccharose-[14C] (Suc), du 3-O-méthylglucose-[3H] et de la glutamine-[3H] a été étudié en
utilisant des plantules de R. communis. Les résultats ont montré que le D-GFC inhibe fortement l'absorption et le transport phloémien du Suc-[14C] comme l'acide p-chloromercuribenzènesulfonique (PCMBS) utilisé à la même
concentration (Fig. 5B). Mais, contrairement au PCMBS qui se lie aux groupes sulfhydryle de nombreuses protéines membranaires, aucun effet inhibiteur du D-GFC n’est noté chez le ricin sur l’absorption du 3-O-méthyl-D-glucose (Fig. 5C) et de la glutamine (Fig. 5D), ainsi que sur l'activité PM-H+-ATPase. De même, le D-GFC 0,5 mM inhibe d'environ 80 % le transport actif de Suc par les tissus foliaires de Vicia faba et par les cellules de Saccharomyces cerevisiae transformées avec AtSUC2, un gène impliqué dans le chargement phloémien de Suc dans Arabidopsis. Les données indiquent que le D-GFC est un puissant inhibiteur de l'absorption de Suc par les cotylédons et du chargement phloémien de Suc. C'est ainsi le premier produit chimique connu à présenter une telle spécificité. En conséquence, le D-GFC a été utilisé comme nouvel outil en phloémologie pour étudier et quantifier les diverses voies de chargement en Suc endogène du phloème chez le Ricin.
48 congrès du Groupe Français des Pesticides, 30 mai – 1 juin 2018, LIMOGES Figure 5. Le
D-Glucose/fenpiclonil (D-GFC) est un nouvel inhibiteur des transporteurs de saccharose.
A : Structure du D-GFC. B : Effet du D-GFC sur le
chargement de saccharose exogène chez le Ricin.
C : Effet du D-GFC sur le
chargement du
3-O-méthylglucose chez le Ricin.
D : Effet du D-GFC sur le
chargement de glutamine exogène chez le Ricin.
Dans une dernière partie [12], notre objectif était d'améliorer la stratégie utilisant la conjugaison avec
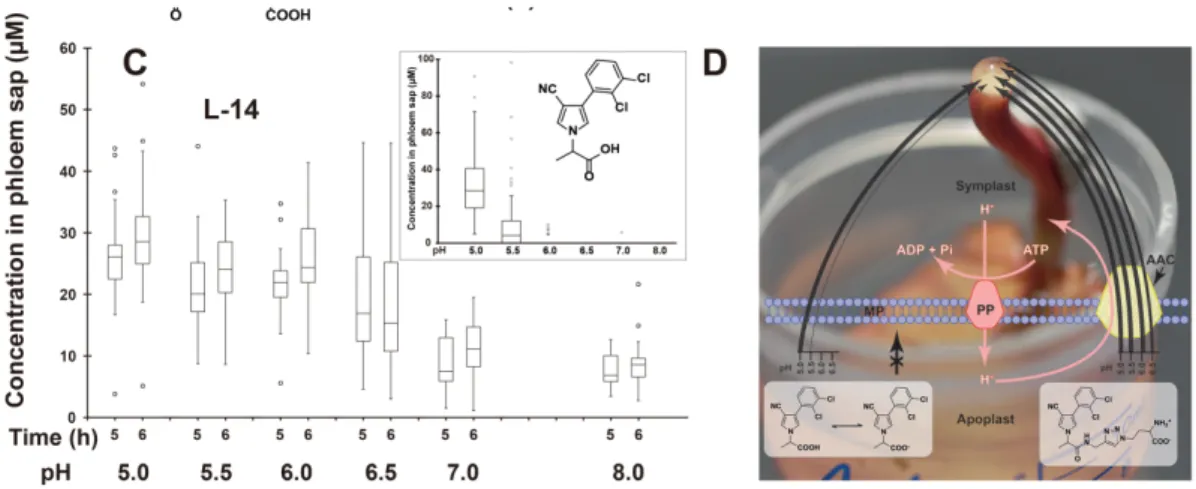
des acides aminés. Des variations structurales ont été réalisées en introduisant différents espaceurs entre le fenpiclonil et la fonction acide α-aminé. Trois nouveaux conjugués d'acides aminés ont ainsi été synthétisés (Fig. 6A) et leur mobilité phloémienne a été testée chez le ricin pour étudier l'effet de la structure de l’espaceur sur la reconnaissance et le transport par le transporteur. Le conjugué L-14, qui contient un cycle triazole avec la chaîne d'acides aminés la plus courte, montre la plus forte concentration dans la sève phloémienne parmi les quatre conjugués testés (Fig. 6B), indiquant que la longueur de la chaîne entre le cycle triazole et la fonction L-α-aminoacide conduit à une amélioration de la mobilité phloémienne. En revanche, l'élimination du cycle triazole dans le bras espaceur n'a pas amélioré la systémie, bien que les propriétés physico-chimiques soient plus favorables à la diffusion à travers la membrane plasmique (Fig. 6B).
Figure 6. Optimisation de la mobilité phloémienne des conjugués intégrant une fonction α-aminoacide
en variant la structure de l’espaceur. A : Structure des conjugués étudiés. B : Comparaison de leur mobilité phloémienne chez le ricin.
Par ailleurs, le conjugué L-14 présente une systémie phloémienne à toutes les valeurs de pH de l'apoplaste foliaire (pH de 5,0 à 6,5) rapportées dans la littérature, tandis que les dérivés acides du fenpiclonil ne sont mobiles qu'à des valeurs proches de pH 5,0 (Figs. 6C, D).
Figure 6. Optimisation de la mobilité phloémienne des conjugués intégrant une fonction
α-aminoacide en variant la structure de l’espaceur. C, D : Effet du pH sur la mobilité phloémienne chez le ricin d’un conjugué du fenpiclonil avec un α-aminoacide et d’un dérivé acide du fenpiclonil.
Conclusion : La stratégie de prodrogue a été considérée comme un concept important dans la recherche
de produits agrochimiques modernes compatibles avec une efficacité optimale, la sécurité environnementale et la facilité d’utilisation [13]. Les profongicides peuvent offrir de nouvelles opportunités dans le contrôle de maladies racinaires et vasculaires en véhiculant les matières actives via le phloème. Cependant, la conception des profongicides est encore à un stade précoce de développement, en particulier lorsqu’un processus de transport actif est mis en jeu. D’un point de vue général, nos résultats ont fourni des informations sur les relations entre la structure et la mobilité, ceci afin d’optimiser la conception de profongicides pris en charge par un système de transport actif, ceci en choisissant le meilleur vecteur et en optimisant la structure de l’espaceur.
Remerciements : Les auteurs remercient FranceAgriMer, InterLoire et JAS Hennessy & Co. pour le
support financier de ces travaux.
Mots-clés : « click chemistry », conjugués phénylpyrrole-nutriment, vectorisation, mobilité phloémienne, inhibiteur transport saccharose
Références bibliographiques
1. Stella, V. J., Borchardt, R. T., Hageman, M. J., Oliyai, R., Maag, H., and Tilley, J. W., Prodrugs:
Challenges and Rewards. 2007: Springer Science & Business Media.
2. Gynther, M., Laine, K., Ropponen, J., Leppanen, J., Mannila, A., Nevalainen, T., Savolainen, J.,
Jarvinen, T. T., and Rautio, J., Large Neutral Amino Acid Transporter Enables Brain Drug Delivery Via
Prodrugs. Journal of Medicinal Chemistry, 2008. 51(4): p. 932-936.
3. Fan, W., Wu, Y., Li, X. K., Yao, N., Li, X., Yu, Y. G., and Hai, L., Design, Synthesis and Biological
Evaluation of Brain-Specific Glucosyl Thiamine Disulfide Prodrugs of Naproxen. European Journal of
Medicinal Chemistry, 2011. 46(9): p. 3651-3661.
4. Sugano, K., Kansy, M., Artursson, P., Avdeef, A., Bendels, S., Di, L., Ecker, G. F., Faller, B.,
Fischer, H., Gerebtzoff, G., Lennernaes, H., and Senner, F., Coexistence of Passive and Carrier-Mediated
48 congrès du Groupe Français des Pesticides, 30 mai – 1 juin 2018, LIMOGES
5. DeGorter, M. K., Xia, C. Q., Yang, J. J., and Kim, R. B., Drug Transporters in Drug Efficacy and
Toxicity, in Annual Review of Pharmacology and Toxicology, Vol 52, Insel, P. A., Amara, S. G., and Blaschke,
T. F., Editors. 2012, Annual Reviews: Palo Alto. p. 249-273.
6. Rautio, J., Laine, K., Gynther, M., and Savolainen, J., Prodrug Approaches for Cns Delivery. Aaps Journal, 2008. 10(1): p. 92-102.
7. Dufaud, A., Chollet, J. F., Rudelle, J., Miginiac, L., and Bonnemain, J. L., Derivatives of Pesticides
with an Alpha-Amino-Acid Function - Synthesis and Effect on Threonine Uptake. Pesticide Science, 1994. 41(4):
p. 297-304.
8. Deletage-Grandon, C., Chollet, J. F., Faucher, M., Rocher, F., Komor, E., and Bonnemain, J. L.,
Carrier-Mediated Uptake and Phloem Systemy of a 350-Dalton Chlorinated Xenobiotic with an Alpha-Amino Acid Function. Plant physiology, 2001. 125(4): p. 1620-1632.
9. Wu, H. X., Yang, W., Zhang, Z. X., Huang, T., Yao, G. K., and Xu, H. H., Uptake and Phloem
Transport of Glucose-Fipronil Conjugate in Ricinus Communis Involve a Carrier-Mediated Mechanism. Journal
of Agricultural and Food Chemistry, 2012. 60(24): p. 6088-6094.
10. Wu H., Marhadour S., Lei Z.W., Yang W., Marivingt-Mounir C., Bonnemain J. L., and Chollet J.
F., Vectorization of agrochemicals: amino acid carriers are more efficient than sugar carriers to translocate
phenylpyrrole conjugates in the Ricinus system. Environmental Science and Pollution Research, 2018. 25: p.
14336-14349.
11. Wu H., Marhadour S., Lei Z.W., Dugaro E., Gaillard C., Porcheron B., Marivingt-Mounir C.,
Lemoine R., Chollet J. F. and Bonnemain J. L., Use of D-glucose-fenpiclonil conjugate as a potent and
specific inhibitor of sucrose carriers. J. Exp. Bot. 68: p. 5599-5613.
12. Marhadour S., Wu H., Yang W., Marivingt-Mounir C., Bonnemain J. L. and Chollet J. F.,
Vectorisation of agrochemicals via amino acid carriers: influence of the spacer arm structure on the phloem mobility of phenylpyrrole conjugates in the Ricinus system. Pest Manage. Sci., 2017. 73: p. 1972-1982
13. Jeschke, P., Propesticides and Their Use as Agrochemicals. Pest Management Science, 2016. 72(2): p. 210-225.
![Figure 1. Illustration du concept de prodrogue (modifié d’après Rautio et al. [6]).](https://thumb-eu.123doks.com/thumbv2/123doknet/14608225.545034/2.892.261.686.877.1050/figure-illustration-concept-prodrogue-modifié-rautio-al.webp)