Je Dédie ce Travail
A la mémoire de mon Père
Nulle dédicace ne peut exprimer ce que je lui dois pour ses efforts et
ses sacrifices.
Il a toujours été à mes cotés dans les bons moments et les rudes
épreuves, éclairant mon chemin par ses conseils et ses directives.
Je ne saurais exprimer ma tristesse en son absence.
Puisse Dieu lui accorder sa clémence et sa miséricorde et puisse ce
travail être une prière pour son âme.
A ma très chère Mère
Autant de mots aussi expressifs soient- ils ne sauraient montrer le
degré d’amour, d’affection, d’estime et de dévouement que j’ai pour
vous.
Vous m’avez comblé par votre tendresse et votre affection tout au
long de mon parcours.
Ce travail est le résultat d’énormes efforts et sacrifices que vous avez
consenti pour mon éducation.
Que dieu vous garde et vous procure longévité et santé ; puisse-t-il
m’aider pour ne jamais vous décevoir.
A mes Frères Sidi Mohammed
et Sidi Ahmed
A ma Sœur Khadija
A toute ma Famille
A ma très chère amie Hafsa El Ouzzani
A tous les résidents de radiologie
A NOTRE MAÎTRE ET PRESIDENTE DE THÈSE
Madame le Professeur T. AMIL
Professeur de radiologie à l’ HMIM V de Rabat
V
ous nous faites un grand honneur en acceptant de présider le jury de thèse.
C
e travail est une occasion pour nous d’apprécier vos qualités humaines et
professionnelles, ainsi que la richesse de vos connaissances.
V
euillez agréer cher maître nos sincères remerciements et toute la reconnaissance que
nous vous témoignons.
A NOTRE MAÎTRE ET RAPPORTEUR DE THÈSE
Monsieur le professeur J. EL FENNI
Professeur de radiologie à l’HMIM V de Rabat
N
ous avons eu l’honneur et le privilège d’élaborer ce travail sous votre précieux
encadrement. C’est grâce à vos conseils éclairés et à vos remarques que nous avons pu
mener ce travail jusqu’au bout.
N
ous avons pu apprécier la rigueur de votre enseignement et vos remarquables qualités
humaines et professionnelles.
V
ous avez fait preuve par votre patience, compréhension et modestie de la signification
morale de notre profession.
Q
ue ce travail, si modeste soit-il, puisse être le message de mes sentiments les plus
respectueux et de ma sincère reconnaissance.
A NOTRE MAÎTRE ET JUGE DE THÈSE
Monsieur le professeur M. JIDAL
Professeur de radiologie à l’HMIM V de Rabat
N
ous sommes particulièrement reconnaissants pour l’honneur que vous nous faites en
acceptant de siéger parmi les membres du jury.
V
otre enseignement rigoureux, vos qualités humaines, votre modestie n’ont cessé de
susciter notre grande admiration.
V
euillez trouver à travers ce travail le témoignage de notre profonde reconnaissance et
respect.
A NOTRE MAÎTRE ET JUGE DE THÈSE
Monsieur le Professeur A. ABID
Professeur de pneumologie à l’HMIM V de Rabat
C
’est pour nous un immense plaisir de vous voir siéger parmi les membres du jury de
notre thèse.
V
euillez nous permettre de vous formuler l’assurance de notre haute considération et
sincère reconnaissance.
A NOTRE MAÎTRE ET JUGE DE THÈSE
Monsieur le Professeur E. KABIRI
Professeur de chirurgie thoracique à l’HMIM V de Rabat
N
ous vous remercions vivement pour l’honneur que vous nous faites en acceptant de
juger ce travail.
N
otre gratitude est grande pour l’intérêt que vous avez montré à l’encontre de notre
travail.
A MONSIEUR LE DR. D. Bassou
Professeur assistant au service de radiologie à l’HMIM V de RABAT
A MONSIEUR LE DR. T. ZIADI
ABRÉVIATIONS
KB : Kyste bronchogénique TDM : Tomodensitométrie
IRM : Imagerie par résonance magnétique VCI : Veine cave inférieure
VCS : Veine cave supérieure UH : Unité Hounsfield ECG : Eléctrocardiogramme LCR : Liquide céphalo-rachidien Fig : Figure MHZ : Méga-Heirtz Cm : Centimètre Mm : Millimètre ml : millilitre
INTRODUCTION ...1
RAPPELS ………4
Rappel de l’embryogenèse pulmonaire ... 5
a)-Stade embryonnaire ... 5 b)-Stade fœtal ... 6 b-1)- Stade pseudoglandulaire... 6 b-2)- Stade canaliculaire ... 7 b-3)- Stade sacculaire ... 7 b-4)- Stade alvéolaire ... 7 Ethiopathogénie ... 9
a)-Théorie de fractionnement REKTOZIK ... 9
b)-Théorie du bourgeon accessoire ELLIS ... 9
c)-Théorie vasculaire de PRYCE ... 10
Anatomie du médiastin ... 10
a)- Limites et communications ... 10
b)- Contenu ... 10
c)- La division du médiastin ... 11
Classification des kystes bronchogéniques ... 14
a)-Les kystes bronchogéniques médiastinaux ... 14
b)-Les kystes bronchogéniques pulmonaires ... 14
c)-Autres localisations ectopiques... 14
Imagerie ... 15
I) Radiographie du thorax ... 15
3)- Radiographie numérisée ... 17
B)- Radio-anatomie normale sur les clichés standard ... 18
1)- Médiastin sur le cliché de face ... 18
a)- Les bords du médiastin ... 18
b)- Les lignes médiastinales ... 19
2)- Sur le cliché de profil ... 22
C)- La topographie de la lésion ... 23
a)- Signe de la silhouette ... 23
b)- Signe cervico-thoracique ... 23
c)- Signe de convergence du hile ... 24
d)- Signe de recouvrement du hile ... 25
e)- Signe de l’iceberg ... 26
II) La TDM ... 27 A)- La technique ... 27 B)- La radio-anatomie normale ... 30 III)- L’IRM ... 37 A)- La technique ... 37 B)- La caractérisation tissulaire ... 39 IV)- L’échographie ... 41
MATERIEL ET METHODES ...43
RESULTATS ...70
DISCUSSION ...77
I)- Epidémiologie ... 78II)- Etude clinique ... 78
C)- Biologie ... 83 D)- Diagnostic radiologique ... 83 1)- Radiographie du thorax ... 83 2)- La TDM ... 84 a)- Apport de la TDM ... 84 b)- Résultats ... 85 c)- Limites de la TDM ... 86 3)- L’ IRM ... 87
a)- Apport de l’IRM ... 87
b)- Résultats ... 88
4)- L’échographie ... 89
a)- Apport de l’échographie ... 89
b)- Résultats ... 91
E)- Autres examens complémentaires ... 93
III)- Diagnostic différentiel ... 94
IV)- Particularités topographiques ... 95
V)- Etude anatomopathologique ... 96 VI)- Traitement ... 101 VII)- Evolution ... 103
CONCLUSION ... 104
RESUME………..106
BIBLIOGRAPHIE………..109
Les kystes bronchogéniques sont des tumeurs kystiques bénignes d’origine embryonnaire (dysembryome homoplastique), qui se présentent comme des structures arrondies ou ovalaires, de taille variable, et dont la paroi est de type bronchique sécrétant ce qui explique le contenu liquide [1,2,3 ].
Les kystes bronchogéniques résultent d’une anomalie de développement d’un bourgeon aberrant issu de l’intestin primitif antérieur, ou de l’ébauche trachéo-bronchique et n’ayant pas abouti à la différenciation alvéolaire [4,5].
Il semble toutefois qu’ils sont dûs à un accident tératogène pouvant survenir à toutes les étapes de développement de l’intestin primitif antérieur [2].
En d’autres termes, il s’agit d’une anomalie congénitale issue d’une malformation embryonnaire.
Leur topographie est principalement médiastinale dans 36 à 90% des cas, cependant, ils peuvent siéger au niveau du parenchyme pulmonaire. D’autres localisations ectopiques plus rares ont été rapportées [6, 7, 8, 9, 10, 11, 12, 13].
Le plus souvent, les kystes bronchogéniques sont de découverte fortuite lors d’un examen radiologique systématique, ce qui prouve l’intérêt de l’imagerie dans leur exploration [3].
L’efficacité du diagnostic radiologique a été complètement transformée par le développement de l’imagerie médicale.
En effet, si la radiographie standard permet de détecter ces lésions, la tomodensitométrie joue un rôle essentiel en précisant leurs caractères densitométriques, leur topographie exacte, ainsi que leurs rapports avec les structures anatomiques de voisinage [14, 15].
L’IRM est une technique également très évolutive, mais elle reste un complément de la TDM, et ses apports sont limités à quelques indications particulières [2].
Ceci permet une approche diagnostique performante, mais le diagnostic de certitude est anatomopathologique reposant sur deux critères histologiques à savoir : la présence au niveau de la paroi kystique d’un ou de plusieurs tissus de l’arbre trachéo-bronchique, et la présence d’autre part d’un épithélium respiratoire [2, 16, 17, 18, 19].
L’objectif de ce travail est de définir une bonne stratégie diagnostique des kystes bronchogéniques médiastinaux en tenant compte de l’apport respectif des différentes techniques en imagerie à propos d’une série de 5 cas, colligée dans le service de radiologie de l’hôpital militaire d’instruction MOHAMMED V de Rabat sur une période de 9 ans allant de l’année 2000 à 2008.
RAPPEL DE L’EMBRYOGENESE PULMONAIRE
[4] (Fig.1)
Le terme d’embryologie ne s’applique qu’à une partie du développement de l’appareil respiratoire puisque celui-ci se poursuit bien après la naissance, ainsi on divise la formation des poumons en deux étapes : embryonnaire et fœtale. Le stade embryonnaire marque le début du bourgeonnement du diverticule respiratoire et la formation des voies aériennes hautes (trachée, bronches souches et lobaires).
Le stade fœtal comporte quatre étapes : pseudo-glandulaire, canaliculaire, sacculaire, alvéolaire.
a) Stade embryonnaire : (22è jour - 6è semaine)
C’est une période d’une grande complexité puisque plusieurs phénomènes fondamentaux évoluent parallèlement : développement de l’arbre respiratoire, cloisonnement trachéo-oesophagien, mise en place de la vascularisation pulmonaire.
L’ébauche respiratoire naît d’une gouttière apparaissant à la face ventrale de l’intestin primitif antérieur postéro-pharyngé vers le 22è- 24è jour.
Cette gouttière se prolonge caudalement par un diverticule (diverticule trachéal, respiratoire, bourgeon pulmonaire).
Le diverticule respiratoire se divise rapidement (26-28j) pour former les bourgeons bronchiques droit et gauche.
Le bourgeon bronchique droit se divise en trois bourgeons bronchiques secondaires (bronches lobaires), et le bourgeon bronchique gauche en deux bourgeons bronchiques secondaires (bronches lobaires).
Après division des bronches secondaires, se forment alors dix bronches tertiaires à droite et à gauche (bronches segmentaires), qu’elles mêmes donnent naissance aux bronches sous segmentaires.
Cette évolution est concomitante du cloisonnement trachéo-oesophagien. Ce cloisonnement est lié en grande partie à l’apparition au 26è jour, à la partie caudale de la gouttière trachéo-bronchique, des crêtes latérales se dirigeant médialement pour se réunir sur la ligne médiane séparant ainsi la trachée en avant, et l’œsophage en arrière.
Le développement de la circulation pulmonaire est contemporain à ce stade, la vascularisation artérielle initialement systémique, forme des plexus qui sont rejoints vers le 30è jour par les artères pulmonaires. La vascularisation pulmonaire devient prédominante au 2è mois.
Le retour veineux pulmonaire subit d’importantes modifications : initialement assuré par un plexus splanchnique se drainant vers le système des veines cardinales supérieures, se jetant dans le sinus veineux par l’intermédiaire des canaux de CUVIER.
La partie pulmonaire de ce plexus est rejointe dès le 30è jour par des veines pulmonaires issues du tronc veineux pulmonaire primitif.
b) Stade fœtal
b-1) Stade pseudo glandulaire (6 à 16 semaines)
La dichotomisation des bronches se poursuit pour aboutir aux divisions bronchiques pré-acinaires (bronchiole terminale). L’épithélium est columnique et renferme des cellules ciliées, non ciliées (pré-Clara), caliciformes et quelques cellules neuro-endocrines.
Le mésenchyme péri épithélial se différencie pour former les fibres musculaires lisses, cartilage, tissu élastique.
b-2)-Stade canaliculaire (17 à 24 semaines)
C’est une phase capitale marquant l’apparition de la fonction respiratoire. Chaque bronchiole terminale se divise en deux ou plusieurs bronchioles respiratoires.
L’acinus apparaît et avec lui, la barrière alvéolo-capillaire.
L’épithélium se différencie avec apparition du glycogène dans le cytoplasme des cellules épithéliales, apparition des premières cellules sécrétoires, pneumocytes type II et cellules de Clara.
L’évolution des capillaires du mésenchyme est simultanée, marquée par un processus de maturation des septas inter-alvéolaires.
b-3)-Stade sacculaire
La poursuite de l’arborisation respiratoire conduit à la naissance des canaux et des sacs alvéolaires.
Les cellules épithéliales acquièrent une différenciation proche de celle du nouveau-né.
Le mésenchyme se réduit du fait de l’augmentation des espaces aériens.
b-4) Stade alvéolaire (de 36 semaines de gestation à 18 mois ou 2 ans postnatal)
Des sacs terminaux continuent à s’ajouter et parallèlement apparaissent les alvéoles définitives.
L’alvéolisation marque ce stade et est liée à la subdivision des sacs alvéolaires par la naissance et la croissance des septas secondaires.
ETHIOPATHOGENIE
Les kystes bronchogéniques médiastinaux peuvent être considérés comme des dérivés des bourgeons aberrants issus de l’intestin primitif antérieur ou de l’ébauche trachéo-bronchique, et n’ayant pas abouti à la différenciation
alvéolaire [5].
La séparation de cette lésion dysplasique se produit à un moment précoce de l’embryogenèse pour les kystes médiastinaux, environ le 30è jour [5, 21, 22, 23].
Ainsi, les kystes bronchogéniques peuvent être considérés comme des séquestrations extra-lobaires [4, 5, 21].
La pathogénie de ce groupe de malformation en particulier celle de séquestrations reste mal étudiée. On peut rappeler trois théories émises.
a)- Théorie de fractionnement REKTOZIK
Une partie du territoire bronchique isolée par suite de la fermeture prématurée du canal pleuro-peritonéal, continue d’évoluer de façon autonome. Le fractionnement étant précoce, la vascularisation de ce territoire ne peut être captée par le système pulmonaire et sa vascularisation reste systémique [24].
b)- Théorie du bourgeon accessoire ELLIS
Un bourgeon supplémentaire naît de l’intestin respiratoire, qui peut se trouver plus ou moins inclus dans le territoire pulmonaire, et garde parfois une connexion avec le tube digestif, sa vascularisation demeurant systémique [24]. En effet, l’existence de bourgeons accessoires a été démontrée chez l’embryon humain.
c)- Théorie vasculaire de PRYCE
La vascularisation persistante d’un territoire pulmonaire, par un rameau aortique postérieur, qui altère ce territoire, le sépare et le séquestre du reste du poumon. Cette théorie a été reprise et même étendue par plusieurs auteurs notamment DELARUE et collaborateurs en 1959 [24, 25, 26].
ANATOMIE DU MEDIASTIN [27]
(fig.2)Le médiastin est constitué par l’ensemble des organes intra-thoraciques de l’espace extra-pleural, entre les deux loges pleuro-pulmonaires.
Il a une forme de pyramide tronquée, aplatie dans le sens transversal.
a)-
Limites et communications
En avant, il répond au sternum et les articulations chondro-costales. En arrière, il est limité par la saillie des corps vertébraux thoraciques
et les gouttières costo-vertébrales.
En haut, il est limité par l’orifice cervico-médiastinal, ainsi il communique largement avec le cou et les creux sus-claviculaires. En bas, il repose sur le diaphragme, et communique avec la cavité
péritonéale à travers l’orifice rétro-costo-xiphoïdien et l’orifice hiatal. Latéralement, il est limité par les plèvres médiastines et communique
avec les axes broncho-vasculaires intra-parenchymateux au niveau des hiles.
b)- Contenu
Le médiastin contient dans un espace cellulo-graisseux :
La trachée et sa bifurcation en bronches souches droite et gauche, qui constituent les éléments centraux des pédicules pulmonaires.
L’œsophage : en arrière et à gauche de la trachée puis derrière le cœur. Les lymphatiques du médiastin et le canal thoracique.
Le thymus : développé chez l’enfant, subit une involution graisseuse avec l’âge.
Les nerfs du médiastin : nerf pneumogastrique, nerf récurrent gauche, nerf phrénique, et chaînes sympathiques.
c)-La division du médiastin (fig.3)
La division du médiastin, la plus classique et la plus utilisée, est une division en trois compartiments et en trois étages permettant d’obtenir neuf régions anatomiques.
Le compartiment antérieur est situé en avant d’un plan passant par la face antérieure de l’arbre trachéo-bronchique et derrière le cœur. Ce compartiment contient le cœur, les gros vaisseaux, le thymus et les chaînes lymphatiques antérieures.
Le compartiment moyen, situé derrière le plan précédent, et devant un plan passant par la face antérieure des corps vertébraux.
Ce compartiment contient la trachée, les bronches souches, l’œsophage et les chaînes lymphatiques voisines.
Le compartiment postérieur est essentiellement constitué des gouttières costo-vertébrales, dans lesquelles cheminent les nerfs sympathiques, et chez le sujet âgé l’aorte déroulée.
Ces trois compartiments sont divisés en trois étages :
L’étage supérieur est situé au dessus du toit de l’aorte horizontal. L’étage inférieur est situé au dessous du plan passant par la carène. L’étage moyen est situé entre ces deux plans.
4) CLASSIFICATION DES KYSTES BRONCHOGENIQUES
On peut distinguer [23] :Les kystes médiastinaux
Les kystes intra-parenchymateux et les kystes ectopiques.
a)- Les kystes bronchogéniques médiastinaux
On peut en s’inspirant de la classification de Maier et Herbert, séparer les kystes bronchogéniques médiastinaux en [1, 29, 30] :
Kystes para trachéaux Kystes carinaires
Kystes hilaires ou pédiculaires (pré, ou plus fréquemment rétro- pédiculaires, à droite comme à gauche)
Kystes du ligament triangulaire
Kystes para-oesophagiens extra- ou intra-muraux
Kystes de localisations plus rares, comme les gouttières costo-vertébrales.
b) Kystes bronchogéniques pulmonaires
Ils représentent 15 à 25% de l’ensemble des kystes bronchogéniques [8, 31, 32]. Solitaires en général, ils peuvent aussi être multiples ou bilatéraux [21]. Ils sont situés le plus souvent dans les régions péri-hilaires (intra-lobulaires) ou rarement dans le poumon périphérique avec une prédilection pour les lobes inférieurs [11, 31, 33, 34, 35].
c) Autres localisations
Kystes bronchogéniques intra-myocardiques [37, 38, 39, 40, 41, 42] Kystes de la région cervicale [30, 43, 44, 45]
Kystes intra-pleuraux [46].
D’autres localisations ectopiques ont été rapportées: intra-diaphragmatique, intra- murale digestive, rétro-péritonéale sus-rénale [47, 48, 49, 50, 51, 52, 53]. Un cas de kyste bronchogénique rétro-pharyngé a été décrit [54].
IMAGERIE :
L’imagerie du médiastin repose en premier lieu sur la radiographie conventionnelle du thorax ; l
a
radiographie standard a été progressivement remplacée par la technique numérisée, qui à performance égale offre des possibilités de traitement, de transfert et de stockage des images [55, 56].
La TDM est l’examen de référence, bénéficie actuellement d’évolution technologique importante permettant des acquisitions de plus en plus fines et rapides, avec des possibilités de reconstructions de meilleure qualité [14].
L’IRM représente une technique très évolutive, mais reste un complément de la TDM. Ses apports sont limités à quelques indications particulières [2].
Les autres techniques sont d’indications ciblées.
LA RADIOGRAPHIE DU THORAX
A) Technique [28, 55, 56]
1) Cliché de face :
C’est l’incidence de base. Elle est réalisée en apnée et en inspiration profonde, chez un patient en position debout ou demi-assise.
Si l’état du patient ne permet pas une telle position, le cliché de face peut être effectué en position couchée ou demi-assise.
Il est indispensable d’avoir un cliché de bonne qualité, nécessitant la haute tension (120-140KV), une grille anti- diffusante, un temps de pause le plus court possible et l’apnée après inspiration profonde.
Les critères de bonne qualité d’un cliché de face :
- La situation médiane de l’apophyse épineuse de D3, se projetant à mi chemin des articulations sterno-claviculaires.
- La projection des bords internes des omoplates en dehors des côtes, ou juste au niveau de leur bord externe.
- La visibilité du larynx et des culs de sac costo-diaphragmatiques.
- Inspiration suffisante : le dôme diaphragmatique doit se projeter au dessus de l’arc postérieur de la sixième côte.
- L’absence de flou cinétique, en particulier cardiaque, indiquant un temps de pose court.
- visibilité suffisante des vaisseaux en périphérie du poumon, éliminant une surexposition.
2) Cliché de profil
Le cliché est pris en inspiration profonde, chez un patient en position debout, demi assise, ou couchée.
Le rayon directeur est centré 10 cm au dessous de l’aisselle.
Cette incidence permet de préciser les caractères d’une image anormale (topographie, dimensions, nature), peut également être indiquée pour étudier certaines régions du thorax mal individualisées sur le cliché de face : régions retrosternale, retrocardiaque, sous-hilaire.
- Visibilité de l’ensemble des champs pulmonaires
- Absence de rotation du thorax, visible par la superposition des bords des côtes droites et gauches.
- Absence de projection des bras sur les structures pulmonaires.
- Absence de surexposition (bonne visibilité des vaisseaux pulmonaires dans l’espace retrocardiaque).
- Absence de sous-exposition (visibilité des gros vaisseaux pulmonaires à travers le cœur).
D’autres incidences complémentaires (cliché en expiration, obliques) peuvent être indiquées, mais de moins en moins réalisées avec l’avènement de la TDM.
3) Radiographie numérisée :
En radiologie conventionnelle, le cliché est la représentation de l’absorption d’un faisceau de rayons X après la traversée du corps examiné.
En radiologie numérisée, l’absorption des rayons X est indiquée par des nombres, ainsi on aura une représentation numérique de l’information.
Face à l’image analogique de l’écran secondaire de l’amplificateur de brillance, existe un convertisseur analogique / numérique qui va affecter à chaque point de l’image un chiffre réalisant ainsi une image numérique.
Cette image est stockée dans une mémoire magnétique.
B)- Radio anatomie normale sur les clichés standard
1)- Le médiastin sur le cliché de faceLes contours externes du médiastin définissent deux bords, formés par la projection des structures cardiovasculaires de topographie antérieure.
D’autres éléments de siège plus postérieur sont analysés grâce aux replis de la plèvre médiastinale qui leur est accolée, et définissent les lignes médiastinales [15].
a) Les bords du médiastin [15] (fig. 4)
a-1) Le bord droit : est constitué par les structures veineuses qui sont de haut en bas :
Tronc veineux brachio-céphalique. Veine cave supérieure souvent invisible.
L’oreillette droite, convexe vers la droite, réalise le bord droit de la silhouette cardiaque.
VCI, oblique en haut et en dedans.
a-2) Le bord gauche : se compose de haut en bas des structures artérielles qui sont :
L’artère sous clavière gauche Bouton aortique
Le bord gauche du tronc de l’artère pulmonaire et l’auricule gauche forment l’arc moyen
b) Les lignes médiastinales [15, 57] (fig.4)
Représentent les contours externes du médiastin qui sont moulés par les clartés pulmonaires.
Elles ne sont visibles que lorsqu’elles sont tangentes au rayonnement incident, et leur analyse nécessite des clichés de haute tension, suffisamment pénétrés.
Leur non visualisation peut être liée à une conformation particulière du sujet ou à une incidence non tangentielle à l’interface médiastino-pulmonaire.
En revanche leur refoulement ou leur déformation sont pathologiques, et permettent de déceler et de localiser un éventuel processus pathologique.
Les principales lignes médiastinales sont :
Ligne médiastinale antérieure : elle réalise une ligne pré-vertébrale souvent oblique en bas et à gauche. Elle se projette en regard des 2è et 3è cartilages costaux.
En haut, au niveau de la convergence des troncs veineux brachio- céphaliques, elle a la forme d’un V.
Caudalement, elle ne dépasse pas le 4è cartilage costal.
Bien qu’elle constitue un bon critère de normalité du médiastin antéro- postérieur, son intérêt reste limité par la fréquence de ses variations physiologiques.
Ligne médiastinale postérieure : réalise une ligne pré-vertébrale pratiquement médiane au niveau des 1è et 2è cartilages costaux.
Au dessus du manubrium sternal, elle dessine un V ouvert en haut. Caudalement, elle se termine à la hauteur de l’arc aortique.
Retrouvée dans 60% des radiographies thoraciques de l’adulte.
Ligne para-trachéale droite : visible dans 65% des cas chez l’adulte, formée par la réflexion de la plèvre médiastine sur le bord droit de la trachée, son épaisseur normale est de 5 mm.
Ligne para-vertébrale droite : visible dans 39% des cas, formée par la réflexion de la plèvre sur les tissus mous para-vertébraux.
Elle dessine une ligne distante d’environ 2 à 4 mm du bord du rachis et peut être refoulée par une grosse veine azygos.
Ligne para-vertébrale gauche : correspond à la réflexion du poumon gauche et de la plèvre sur les tissus mous para-vertébraux, elle est habituellement visible du bouton aortique à T10- T11 où elle rejoint la ligne para-aortique. Elle reste solidaire de l’aorte et la suit dans ses sinuosités.
Ligne para-aortique : toujours visible, déterminée par la tangence entre le bord externe de l’aorte thoracique et le poumon gauche.
Ligne para-azygo-oesophagienne : visible dans 88% des cas, représente la limite gauche du recessus inter-azygo-oesophagien. Elle décrit une ligne se projetant sur le rachis en forme de S allongée, dont le 1/3 supérieur est concave et le 1/3 inférieur convexe à droite.
En haut elle se continue avec le bouton azygos et se prolonge avec la ligne médiastinale postérieure.
La ligne para-aortique droite peut lui faire suite lorsque le recessus inter- azygo-oesophagien vient mouler le bord droit de l’aorte.
La ligne aorto-pulmonaire : relie le bord externe du bouton aortique et le bord supérieur de l’artère pulmonaire.
La ligne aortico-veineuse : elle relie le bouton aortique au bord supérieur de la veine pulmonaire supérieure gauche.
Fig. 4 : Bords et principales lignes du médiastin [15].
1. Tronc veineux brachio-céphalique ; 2. VCS ; 3. Oreillette droite ; 4. VCI ; 5. Artère sous clavière gauche ; 6. Bouton aortique ; 7. Tronc de l’artère pulmonaire et auricule gauche ; 8. Ventricule gauche ; 9. Ligne médiastinale postérieure ; 10. Ligne médiastinale antérieure ; 11. Ligne paratrachéale droite ; 12. Ligne para-vertébrale droite ; 13. Ligne para-para-vertébrale gauche ; 14. Ligne para-aortique gauche ; 15. Ligne para-azygo-oesophagienne ; 16. Ligne aortico-pulmonaire.
2) Sur le cliché de profil [15] (fig. 5) Cette incidence permet d’individualiser :
La silhouette cardiaque dont le bord antérieur est constitué par le ventricule droit, le bord postérieur par l’oreillette gauche et le ventricule gauche.
L’aorte est habituellement visible au niveau de la partie inférieure de la crosse, lorsqu’elle est déroulée, elle peut être entièrement visible.
La trachée est oblique en bas et en arrière.
Fig.5 : Médiastin de profil [15].
1. Médiastin antérieur ; 2. Médiastin moyen ; 3. Médiastin postérieur ; 4. Trachée ; 5. Aorte ; 6. Artère pulmonaire ; 7. VCI ; 8. Tronc artériel brachio-céphalique ; 9. Ventricule droit ; 10. ventricule gauche.
C) Topographie de la lésion
La topographie médiastinale d’une lésion se traduit [15] : Soit par un déplacement d’une ligne médiastinale.
Soit par un déplacement ou une anomalie du contour externe du médiastin ;
La localisation de la lésion dans l’un des compartiments antérieur, moyen ou postérieur du médiastin repose sur :
- Le cliché de profil qui aide à situer l’opacité d’avant en arrière [58, 59]. - L’identification d’un certains nombres de signes propres au médiastin. Les principaux signes [60, 61, 62, 63, 64, 65] :
a) Signe de la silhouette : précise le siège de la lésion qui se situe dans le même plan que la structure dont la silhouette a disparu.
b) Signe cervico-thoracique (fig. 6 et 7) : localise sur une radiographie de face, une opacité du défilé cervico-thoracique.
Lorsque son bord externe est visible au dessus de la clavicule, cette opacité est de topographie postérieure.
A l’inverse, si elle est de topographie antérieure, noyée dans la graisse du creux sus-claviculaire, son bord externe n’est pas visible au dessus de la clavicule.
Fig. 6 : L’opacité disparaît au Fig. 7 : L’opacité dépasse la clavicule vers
dessus de la clavicule Le haut
c) Signe de convergence du hile (fig. 8 et 9) : permet de différencier une masse médiastinale d’une grosse artère pulmonaire.
En effet devant une opacité hilaire, si les branches artérielles pulmonaires convergent vers elle et perdent leur silhouette sur son bord externe, il s’agit d’une artère pulmonaire.
A l’inverse, si les vaisseaux restent visibles à travers l’opacité, il s’agit d’une masse médiastinale.
Fig.8 : Convergence des vaisseaux : Fig.9 : Pas de convergence des
d) Signe de recouvrement du hile (fig.10 et 11) : permet de différencier une masse médiastinale antérieure d’une cardiomégalie ou d’une péricardite.
L’artère pulmonaire gauche ou le point de convergence de ses premières divisions (hile radiologique) est située en général en dehors du bord du médiastin parfois au ras du médiastin, plus rarement légèrement en dedans. Si le hile est situé à plus de 1 cm en dedans du médiastin, il s’agit d’une tumeur médiastinale antérieure.
Fig. 10 : Hile recouvert. Fig. 11 : Hile non recouvert [66]. L’opacité siège en avant du hile [66].
e) Signe de l’iceberg (fig. 12 et 13): une masse médiastinale inférieure est thoraco-abdominale si son contour externe croise le diaphragme en s’écartant du rachis.
En revanche, si son contour inféro-externe rejoint le rachis, elle est sus- diaphragmatique.
Fig.12 : Le contour inférieur rejoint Fig. 13 : Le contour externe s’éloigne du rachis
le rachis. L’opacité est thoraco-abdominale [66].
LA TDM
L’examen tomodensitométrique est l’examen morphologique de référence pour l’analyse du thorax [14].
En effet, si la radiographie standard permet la détection de ces lésions, la tomodensitométrie, qui associe une bonne résolution spatiale et une haute sensibilité en contraste, joue un rôle essentiel en étudiant la topographie, la densité et les rapports de la lésion avec les autres structures du médiastin [14,15].
A) La technique
[14]Le principe de l’examen tomodensitométrique repose sur la mesure de l’absorption par l’organisme de rayons X. L’utilisation de multiples détecteurs de rayons X assemblés sur une couronne circulaire permet d’obtenir un très grand nombre de coefficients d’absorption qui sont reconstruits pour attribuer à chacun des pixels une valeur d’atténuation. Ces coefficients d’atténuation sont exprimés en unités Hounsfield (UH).
Le coefficient d’atténuation est étalonné entre une valeur de – 1000 pour l’air et une valeur de + 1000 pour les structures les plus denses, telle que la corticale osseuse. Le niveau 0 de l’échelle de Hounsfield correspond à l’eau pure, la graisse a un coefficient d’atténuation qui varie entre – 100 et – 140UH.
La majorité des tissus de l’organisme sont caractérisés par des coefficients d’atténuation qui varient entre 10 et 100UH, ce chiffre étant rehaussé lors de l’injection du produit de contraste.
Les cœfficients Hounsfield sont transformés en niveau de gris, les points les plus sombres correspondant aux pixels aux UH les plus basses, les points les plus clairs correspondant aux pixels aux UH les plus hautes.
Tomodensitométrie conventionnelle : cette technique a été quasiment abondonnée au profit de l’acquisition spiralée. Elle consiste à réaliser un balayage incrémenté du corps examiné. Ainsi, chaque acquisition est séparée de l’acquisition suivante par un déplacement incrémenté du lit sur lequel le malade est placé. Entre les acquisitions le malade respire normalement et à chacune des acquisitions successives on lui demande de réaliser une apnée.
Les limites de l’acquisition incrémentée :
L’apnée réalisée par le patient n’est pas toujours au même niveau que l’inspiration. On risque de réaliser deux fois le même niveau de coupe et au contraire de ne pas acquérir un niveau donné ;
L’ensemble des acquisitions qui sont séparées par un intervalle de temps incompressible, dure relativement longtemps et rend difficile l’optimisation de l’injection du produit de contraste.
Acquisition spiralée ou hélicoïdale : permet de coupler l’acquisition des images par la rotation continue du tube à rayons X au déplacement linéaire de la table d’examen. Il devient ainsi possible d’acquérir l’ensemble du volume pulmonaire en une seule acquisition qui dure 10 à 20 secondes. Le nombre de coupe réalisable dépend des caractéristiques intrinsèques de la machine. Les machines de dernières générations utilisent actuellement une technique multi-barrettes (4, 8,16 voire 64 rangées de détecteurs) permettant l’acquisition de plusieurs coupes à la fois.
Les avantages principaux du mode d’acquisition volumique sont :
L’acquisition d’un volume entier sans risque de ne pas visualiser un niveau de coupe ;
L’amélioration de la résolution en contraste, puisqu’il devient possible de réaliser des reconstructions intercalées ;
Enfin, la possibilité de réaliser des reconstructions multiplanaires et tridimensionnelles.
On se sert généralement pour l’analyse tomodensitométrique du thorax de deux fenêtres :
Une fenêtre médiastinale ou tissulaire avec une largeur de 300UH et un niveau de 50UH. Ce niveau correspond à l’absorption moyenne de la plupart des tissus de l’organisme. Ainsi, toute les structures dont le coefficient d’atténuation est inférieur à – 100UH seront reproduites en noir, alors que les structures dont le coefficient d’atténuation est supérieur à 200UH seront reproduites en blanc. Cette fenêtre médiastinale est adaptée à l’analyse des tissus et notamment du médiastin où elle permet de faire la différence entre les densités tissulaires relativement proches.
Une fenêtre parenchymateuse dont le niveau est de l’ordre de – 600UH et la largeur de l’ordre de 1600UH permet, d’analyser correctement le parenchyme pulmonaire.
La qualité de l’image est définie principalement par la résolution en contraste, c'est-à-dire la possibilité de différencier deux tissus de coefficient différent et par la résolution spatiale qui correspond à la possibilité de différencier deux points proches l’un de l’autre.
L’utilisation de produit de contraste permet d’améliorer la résolution en contraste de l’image. Cette injection de produit de contraste permet de mieux repérer les vaisseaux, mais également de différencier les tissus en fonction de leur mode de vascularisation.
Du point de vue pratique, on réalise dans un premier temps un examen complet du thorax en contraste spontané, secondairement on réalise des acquisitions après injection du produit de contraste iodé.
La technique classique d’exploration comporte la réalisation de coupes jointives de 5 mm depuis l’orifice cervico-médiastinal jusqu’ aux culs de sac pleuraux postéro-inférieurs.
Des coupes plus fines de 3 mm voire parfois millimétriques sont parfois utiles pour une analyse plus précise de l’extension et des rapports de la lésion.
B) Radio anatomie normale sur la TDM
[15]Elle fournit une analyse topographique beaucoup plus précise selon HEITZMAN.
Elle distingue neufs territoires topographiques :
L’orifice cervico-médiastinal (fig.14) limité par :
- En avant, le manibrium sternal et les articulations sterno- claviculaires.
- En arrière, le corps vertébral de T1. - Latéralement, les apex pulmonaires. Il contient au sein du tissu cellulo-graisseux :
- L’axe aéro-digestif représenté par la trachée et l’œsophage. - Les axes vasculaires jugulo-carotidiens.
- Les structures nerveuses - Le canal thoracique.
L’espace rétro-sternal pré-aortico-cave (fig.15) limité par : - En avant, la paroi sterno-costale
- Latéralement, les plèvres médiastines.
- En arrière, le tronc veineux brachio-céphalique, la veine cave supérieure et l’aorte.
Angles cardio-phréniques antérieurs (fig. 16) délimités par : - En avant, la paroi sterno-chondro-costale
- En arrière et en dedans, le péricarde recouvrant l’oreillette droite et la pointe du coeur
- En bas, la portion antérieure horizontale du diaphragme. L’angle cardio-phrénique postérieur (fig.17) limité par :
- En avant, le bord postérieur du cœur et la VCI.
- En arrière, la veine grande azygos, l’aorte, le canal thoracique. - Latéralement, la plèvre médiastinale et les ligaments triangulaires. - En haut, il est en relation avec l’oreillette gauche et les veines
pulmonaires inférieures et se poursuit avec la région sous et rétro-carinaire.
- En bas, il est en relation avec l’orifice hiatal et l’espace infra-médiastinal postérieur.
L’espace para-trachéo-oesophagien, il s’agit d’une zone centrée par l’axe aéro-digestif limité par :
- En haut, l’orifice cervico-médiastinal - En bas, l’orifice hiatal
- Latéralement, les plèvres médiastinales et les ligaments triangulaires.
Gouttières costo-vertébrales (fig.18): situées entre le rachis et la plèvre médiastinale, sur toute la hauteur du médiastin.
Elles contiennent l’aorte descendante, la veine grande azygos, les veines hémi-azygos, les chaînes ganglionnaires et le canal thoracique. L’espace sous et rétro-carinaire (fig.19) : limité par l’artère pulmonaire en avant ; en arrière et à droite par le recessus para-azygo-oesophagien du poumon droit ; à droite le tronc intermédiaire ; à gauche
l’œsophage et l’aorte descendante ; en haut la crosse de l’azygos ; en bas il est en continuité avec l’angle cardio-phrénique postérieur en arrière de l’oreillette gauche.
L’espace infra-médiastinal postérieur ou espace rétro-aural (fig.20) : il est limité par les piliers du diaphragme en avant et en dehors, en arrière le corps vertébral.
Il contient l’aorte, les racines des veines azygos, le canal thoracique, la partie inférieure des chaînes ganglionnaires médiastinales postérieures. Médiastin para-orificiel :
Le bilan d’une lésion se développant aux limites du médiastin doit faire rechercher une extension ou une origine extra-médiastinale.
Ainsi l’analyse doit porter également sur le cou, l’abdomen pour les angles cardio-phréniques antérieurs, postérieurs, l’espace infra- médiastinal postérieur, et le hile pour la région para-trachéo-oesophagienne.
Le canal vertébral pour les gouttières costo-vertébrales.
Les lignes médiastinales visibles sur le cliché thoracique sont par ailleurs mieux analysées sur la TDM.
Fig. 14 : Coupe transversale passant par le corps thyroïde [15].
1. Corps de T1 ; 2. Apex pulmonaire ; 3. Trachée ; 4.Oesophage ; 5. Thyroïde ; 6. Carotide primitive ; 7. Artère sous clavière ; 8.Veine jugulaire interne ; 9. Chaîne sympathique ; 10. Nerf récurrent ; 11. Nerf pneumogastrique ; 12. Canal thoracique.
Fig. 15 : Coupe transversale passant par la crosse de l’aorte [15]
1. Sternum ; 2. VCS ; 3.Aorte ; 4.Trachée ; 5.Thymus ; 6.Nerf phrénique ; 7. Pédicule mammaire interne ; 8. Chaîne ganglionnaire médiastinale antérieure droite ; 9. Chaîne ganglionnaire médiastinale antérieure gauche ; 10. Nerf pneumogastrique ; 11. Nerf récurrent gauche.
Fig. 16 : Coupe transversale passant par les cavités cardiaques [15].
1. Appendice xiphoïde ; 2. Oreillette droite, 3. Ventricule droit ; 4.Artère mammaire interne ; 5. VCI ; 6. Nerf phrénique droit ; 7. Ganglion du groupe diaphragmatique latéro-péricardique ; 8. Ganglion du groupe diaphragmatique antérieur ; 9. Muscle triangulaire du sternum.
Fig. 17 : Coupe transversale passant par l’angle cardio-phrénique postérieur [15].
1. VCI ; 2. Veine grande azygos ; 3. Canal thoracique ; 4. Aorte descendante ; 5. Ligament triangulaire ; 6. Œsophage ; 7. Nerf pneumogastrique gauche ; 8. Nerf pneumogastrique droit ; 9. Nerf phrénique droit ; 10. Ganglion périœsophagien ; 11. Ganglion du groupe diaphragmatique latéropéricardique.
Fig. 18 : Coupe transversale passant par les gouttières costo-vertébrales [15].
2. Veine grande azygos ; 3. Canal thoracique ; 6. Œsophage ; 7. Nerf pneumogastrique gauche ; 8. Nerf pneumogastrique droit ; 16. Plèvre médiastinale ; 17. Veine hemiazygos ; 18. Chaîne sympathique.
Fig. 19 : Coupe transversale passant par l’espace sous et rétro-carinaire [15].
2. Veine grande azygos ; 3. Canal thoracique ; 4. Aorte descendante ; 6. Œsophage ; 7. Nerf pneumogastrique gauche ; 8. Nerf pneumogastrique droit ; 10. Ganglion périoesophagien ; 12.Artère pulmonaire droite ; 13. Tronc intermédiaire ; 14. Recessus interazygo-oesophagien ; 15. Ganglion sous-carinaire.
Fig.20 : Coupe transversale passant par l’espace infra-médiastinal postérieur [15].
1. VCI ; 3. Canal thoracique ; 4. Aorte descendante ; 18. Chaîne sympathique ; 19. Rachis ; 20. Pilier du diaphragme ; 21. Racines interne et externe de la veine grande azygos ; 22. Racines interne et externe de la veine hemiazygos ; 23. Ganglions lymphatiques ; 24. Languette pulmonaire.
L’IRM
A) Technique
[67]Une bonne exploration IRM du thorax doit répondre à plusieurs objectifs : obtenir un bon rapport signal sur bruit, éviter les artefacts liés aux mouvements cardiaques et à ceux de la cage thoracique lors de la respiration, avoir une bonne résolution spatiale et temporelle pour l’étude cardio-vasculaire et éviter si possible d’autres explorations plus agressives ou invasives.
Imagerie anatomique
a) Séquences sans apnéeQuand l’information anatomique prime sur l’information fonctionnelle, les séquences en écho de spin ou en turbo-écho de spin sont les séquences de choix. Les séquences en écho de spin pondérées en T1 avec un asservissement à l’ECG permettent en quelques minutes l’obtention d’images morphologiques de grande qualité pour l’étude du médiastin, des vaisseaux et des cavités cardiaques.
Les artefacts liés aux mouvements respiratoires et à une mauvaise synchronisation à l’ECG peuvent gêner l’interprétation.
Le rapport signal / bruit peut être augmenté avec l’utilisation des antennes type (phased-array) au prix d’artefacts générés par la graisse de la paroi thoracique antérieure.
b) Séquences en apnée
Il est possible actuellement d’acquérir des images anatomiques au cours d’une apnée de 15 à 20 secondes ce qui permet d’éliminer les artefacts respiratoires.
La réalisation de telles séquences est possible en acquérant réellement une partie de l’information et en interpolant une partie de l’information non acquise pour obtenir une image complète.
Une qualité des images identique à celle acquises en écho de spin pondérée T1 peut être obtenue avec ces séquences asservies à l’ECG dont l’acquisition est segmentée en utilisant la technique turbo ou fast-écho de spin.
Le rapport signal/ bruit est augmenté par l’utilisation impérative des antennes de surface type (phased – array).
c)- Angiographie par résonance magnétique
L’aorte et les artères pulmonaires peuvent être visualisées soit avec les séquences précédemment décrites soit par une séquence d’angiographie par résonance magnétique, sans injection du produit de contraste, basée sur le phénomène de temps de vol ou le contraste de phase. Actuellement, l’angiographie par résonance magnétique avec injection de chélate de gadolinium est devenue possible grâce aux progrès réalisés dans la rapidité d’acquisition des séquences.
d) Imagerie fonctionnelle Ciné-RM :
Il s’agit de séquences utilisant la technique d’écho de gradient. Le sang circulant apparaît en blanc (signal élevé) du fait de l’entrée des protons non saturés dans le plan de coupe. Ceci permet d’obtenir des images correspondant à un temps donné du cycle cardiaque, ainsi l’acquisition en apnée de 8 à 12 images dites multiphases permet d’explorer la totalité du cycle cardiaque. La mise en boucle de ces images réalise le mode ciné.
Imagerie de perfusion :
Elle permet l’étude de la vascularisation pulmonaire et myocardique.
La séquence utilisée est une séquence turbo-flash pondérée en T1 au cours de l’injection d’un bolus de gadolinium permettant une résolution temporelle de l’ordre de la seconde au dépend d’une épaisseur de coupe de 15 à 20mm. On obtient ainsi une opacification successive des cavités cardiaques droites, des artères pulmonaires, du parenchyme pulmonaire, des veines pulmonaires, des cavités cardiaques gauches puis de l’aorte. En soustrayant une image sans opacification à une image avec injection de contraste on obtient au temps capillaire une parenchymographie pulmonaire en coupes tomographiques, jugée de qualité supérieure à la scintigraphie.
Elle permet une bonne étude des rapports vasculaires. Imagerie de ventilation :
C’est encore actuellement une imagerie qui est du domaine de la recherche. Cette imagerie est basée sur l’utilisation de gaz nobles hyperpolarisés tel que l’Hélium et le Xénon.
B) Caractérisation tissulaire
[15, 67]La caractérisation tissulaire nécessite la comparaison du signal en séquence spin-écho pondérée en T1, T2, et en T1 après injection de gadolinium.
Une formation liquidienne peut être affirmée sur l’hypo-signal en T1 et l’hyper- signal franc en T2. L’hypo-signal en T1 peut être remplacé par un hyper-signal, en cas de liquide riche en protéines ou présentant des remaniements hémorragiques.
Après injection du produit de contraste, la paroi du kyste peut être rehaussée alors que le signal à l’intérieur du kyste ne se modifie pas.
Les lésions charnues ont un signal intermédiaire, voisin de celui du muscle sur les séquences pondérées en T1, et un signal supérieur au muscle et parfois proche de celui de la graisse sur les séquences pondérées en T2. Ces lésions se rehaussent après injection du produit de contraste.
Le contenu graisseux d’un tissu peut être affirmé par son signal caractéristique à savoir un hyper-signal T1, une diminution de cet hyper-signal en T2 et sa disparition en T1 avec suppression de graisse.
La mise en évidence d’une hémorragie ou d’un saignement se fera sur l’existence d’un hyper-signal en T1 et d’un hyper-signal en T2 sauf en cas de présence d’hémosidérine qui donnera un hypo-signal en T2.
Un tissu fibreux au stade tardif peut être différencié d’une tumeur par son hypo- signal en T1 et en T2.
Les calcifications sont de détection moins aisée qu’en TDM. Si elles sont volumineuses, elles sont visibles sous forme d’une zone d’hypo-signal T1 et T2.
L’ECHOGRAPHIE
A) Technique
- L’échographie transpariétale est un examen de faible coût, d’accès facile mais reste une technique accessoire en pathologie thoracique médiastinale [15].
Le médiastin de l’adulte se prête mal à l’exploration ultrasonore par voie externe, en raison de l’étroitesse des fenêtres acoustiques. Cependant, dans certaines situations cliniques, le recours à un examen ultrasonore avec des sondes de 3.5 ou 5MHZ est utile. Le médiastin est abordé par trois grandes voies : La voie sus-sternale permet l’exploration en coupes frontales et sagittales du médiastin supérieur ; les voies para-sternales droite et gauche associées au décubitus latéral permettent d’explorer la loge médiastinale antérieure et le cœur ; la voie abdominale récurrente sous-costale permet une exploration trans- diaphragmatique utile pour l’exploration des masses des angles cardio-phréniques [57].
L’échographie est très sensible dans la détection des masses médiastinales antérieures où elle supplante largement la radiographie de face et profil. En revanche, la sensibilité reste mauvaise pour le dépistage des masses du médiastin moyen et postérieur. Elle apparaît moins performante que la TDM mais demeure très supérieure aux clichés simples dans l’exploration de la région pré-vasculaire (en avant de la veine cave supérieure et de l’aorte ascendante) et de la région para-trachéale droite [15].
-La visualisation d’une lésion dépend de son échostructure, de sa taille, et de la forme de la fenêtre acoustique. La distance qui la sépare de la sonde intervient également, une masse profonde étant moins bien décelée qu’une masse
- Les informations fournies concernent la taille, la morphologie, la topographie, l’échostructure de la lésion, ainsi que les rapports avec les structures anatomiques de voisinage [15].
- Chez le petit enfant, l’étude des masses médiastinales est faite par échographie. Chez le jeune enfant, le couple d’examens utiles est la radiographie thoracique et l’échographie alors que chez l’adulte, le couple est fait de la radiographie thoracique et de la TDM [57].
- L’échographie peut aussi être réalisée par voie endo-oesophagienne, couplée à une fibroscopie. Il s’agit d’une technique nouvellement apparue dans l’arsenal des examens disponibles pour étudier les tumeurs du médiastin moyen [2, 15].
PREMIERE OBSERVATION
Il s’agit de madame D.B., âgée de 40 ans, asymptomatique, ayant bénéficié d’une radiographie pulmonaire systématique lors d’un bilan préopératoire pour vésicule biliaire lithiasique.
Examen clinique est sans particularités. Le bilan biologique est normal.
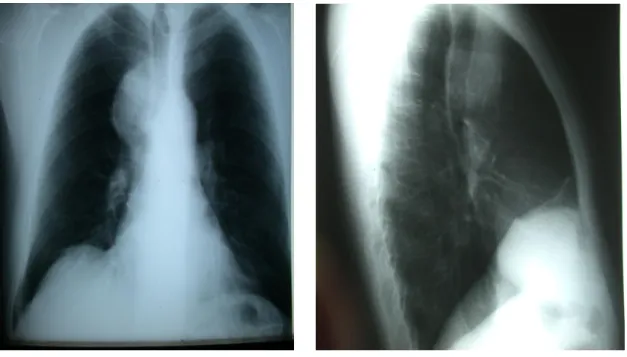
1/ La radiographie thoracique face et profil (fig. 21et 22)
Présence d’une opacité de tonalité hydrique, de l’angle cardio-phrénique droit, ovalaire, homogène, bien limitée, à contours nets et réguliers, dont le bord externe est convexe vers le poumon et le bord interne est noyé dans le médiastin. Cette opacité se raccorde en pente douce avec le médiastin.
Par application du signe de la silhouette, cette opacité n’efface pas le bord droit du cœur, donc elle est rétro-cardiaque ; et par application du signe thoraco-abdominal, le bord externe de cette opacité rejoint le rachis donc elle est de siège thoracique.
Le profil montre le siège médiastinal moyen de la lésion.
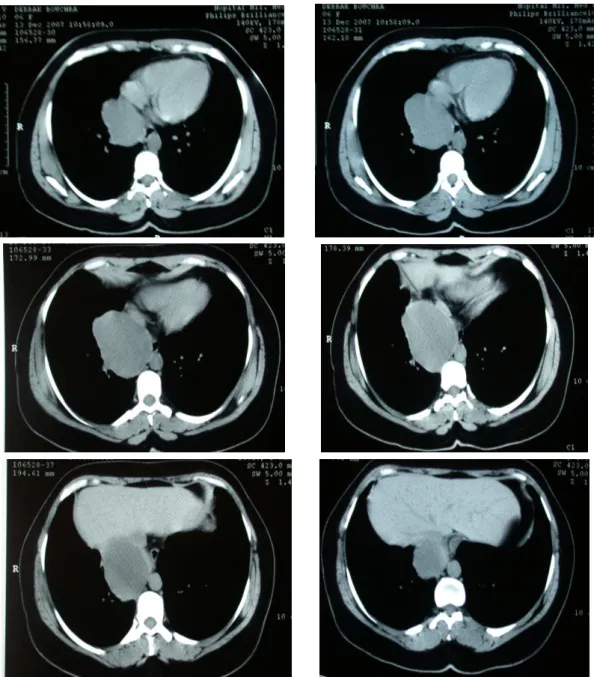
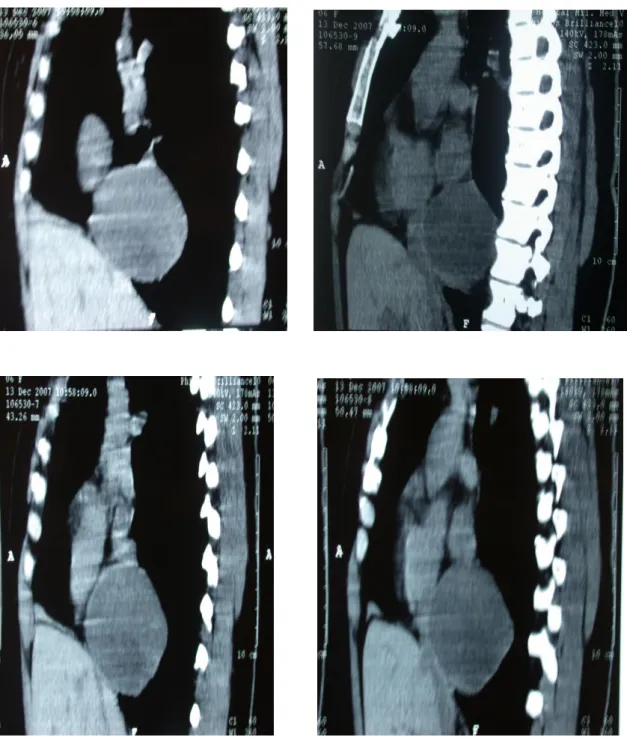
2/ la TDM thoracique (fig.23 et 24)
Masse médiastinale moyenne et inférieure droite de densité liquidienne, homogène, mesurant 8×6.5×7 cm, arrondie, bien limitée, à paroi fine. Cette masse arrive au contacte de l’oreillette droite et du flanc droit de l’aorte descendante.
Elle refoule la VCI en avant. Il n’existe pas d’envahissement endo-vasculaire spontanément décelable.
Elle a des rapports étroits avec le bord droit de l’œsophage sans anomalies de ce dernier. La partie inférieure de cette lésion repose sur le diaphragme.
Il n’existe pas de rapports avec l’axe trachéo-bronchique. Absence d’adénomégalies médiastinales.
Absence de lésions pleuro-parenchymateuses.
Fig. 23 : Coupes axiales de 5mm avant l’injection du produit de contraste.
DEUXIEME OBSERVATION
Il s’agit de madame L.F., âgée de 43 ans, ayant présenté comme symptomatologie une dyspnée.
L’examen clinique est sans particularités. Le bilan biologique est normal.
1) Radiographie thoracique face et profil (fig. 25et 26)
Opacité médiastinale sus-hilaire droite de tonalité hydrique, arrondie, bien limitée, homogène, dont le bord externe est net et convexe vers le poumon, alors que le bord interne est non visible noyé dans le médiastin.
Elle se raccorde en pente douce avec les bords du médiastin.
Par application du signe cervico-thoracique, le bord externe de cette masse ne dépasse pas la clavicule donc elle est de siège antérieur.
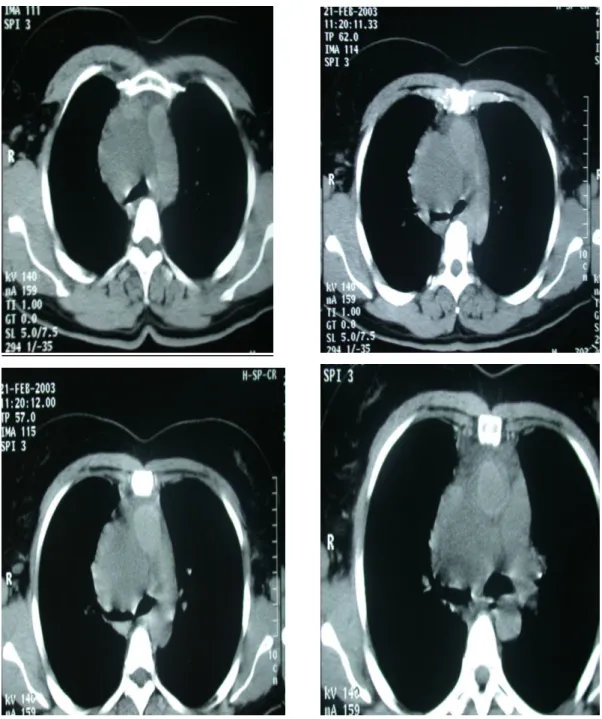
2) La TDM thoracique (fig. 27 et 28)
Masse médiastinale antérieure de densité liquidienne, mesurant 6×5×5.5 cm arrondie, bien limitée, homogène, à paroi fine, non modifiée par l’injection intraveineuse du produit de contraste.
Cette masse siège dans la loge de BARETY, refoule la VCS en avant, la crosse de l’azygos vers l’avant et en dehors et arrive au contact du flanc droit de l’aorte ascendante. Elle arrive également au contact de l’artère pulmonaire droite.
Absence de signes d’envahissement endo-vasculaire.
Cette lésion comprime la trachée, la carène, et les bronches souches droite et gauche, sans envahissement endoluminal, ni troubles de la ventilation.
Cette lésion ne présente pas de rapports avec l’œsophage. Absence de lésions pleuro-parenchymateuses.
3) IRM thoracique (fig. 29, 30, 31et 32)
Masse médiastinale antérieure en situation latéro-trachéale droite de signal liquidien, hyposignalT1, hypersignalT2, arrondie, homogène, bien limitée, non modifiée par l’injection intraveineuse de gadolinium.
L’IRM permet de confirmer l’absence d’envahissement vasculaire (VCS, crosse de l’azygos, aorte ascendante) grâce à sa meilleure résolution en contraste.
Fig.31 : Coupes coronales pondérées T2.
Les figures 33 et 34 représentent les aspects per-opératoires de ce kyste bronchogénique.
Fig. 33 : Aspect per-opératoire du kyste bronchogénique.
(Photo due à l’obligeance du Pr. E. Kabiri - Service de chirurgie thoracique de l’ HIM. Med V)
Fig. 34 : Aspiration per-opératoire du kyste bronchogénique.
TROISIEME OBSERVATION
Il s’agit de madame F.E., âgée de 50 ans, asymptomatique, ayant bénéficié d’une radiographie pulmonaire systématique lors d’un bilan préopératoire pour cataracte.
L’examen clinique est normal.
Le bilan biologique est sans particularités.
1) Radiographie thoracique face et profil (fig. 35 et 36)
Masse médiastinale moyenne et inférieure rétro-cardiaque gauche, de tonalité hydrique, arrondie, bien limitée, homogène. Son bord externe est convexe vers le poumon, alors que son bord interne est invisible car noyé dans le médiastin. Cette masse est solidaire de l’œsophage et arrive au contact de la ligne para-aortique.
Par application du signe thoraco-abdominal, le contour externe de cette masse rejoint le rachis donc elle est de siège thoracique.
2) TDM thoracique (fig. 37, 38 et 39)
Masse rétro-cardiaque gauche, de densité liquidienne, mesurant 6.5×5×4 cm, arrondie, homogène, bien limitée, à paroi fine, siégeant dans le médiastin moyen, non modifiée par l’injection du produit de contraste. Cette masse déborde légèrement sur le médiastin postérieur.
Elle présente des rapports étroits avec le bord gauche de l’œsophage et le flanc gauche de l’aorte descendante.
Elle arrive au contact de l’aorte et du ventricule gauche avec respect du liseré graisseux témoignant de l’absence d’envahissement.
QUATRIEME OBSERVATION
Patiente âgée de 65 ans, asymptomatique. Cette patiente a bénéficié d’une radiographie pulmonaire systématique pour le pélerinage.
L’examen clinique est normal.
Le bilan biologique est sans particularités.
1) Radiographie thoracique face et profil
(fig. 40 et 41)Opacité médiastinale de tonalité hydrique, en situation hilaire et sus-hilaire droite, homogène, arrondie, se raccordant en pente douce avec le médiastin, bien limitée, à bord externe net régulier convexe vers le poumon , et à bord interne noyé dans le médiastin.
Le cliché de profil montre le siège médiastinal antérieur de la lésion.
2) TDM thoracique
(fig. 42 et 43)Masse médiastinale antérieure, de densité liquidienne, mesurant 7×7.5×6 cm, arrondie, homogène, bien limitée, à paroi fine, non rehaussée après injection du produit de contraste. Cette masse siège dans la loge de Barety. Elle refoule la VCS vers l’avant, la crosse de l’azygos vers l’avant et en dehors, et arrive au contact de l’artère pulmonaire droite et du flanc droit de l’aorte ascendante. Absence de signes d’envahissement endo-vasculaire.
Cette lésion est solidaire de l’axe trachéo-bronchique sans signes d’envahissement endoluminal.
CINQUIEME OBSERVATION :
Il s’agit de monsieur B.M., âgée de 45 ans, présentant une toux chronique. L’examen clinique est sans particularités.
Le bilan biologique est normal.
1) Radiographie thoracique face et profil
(fig. 44 et 45)Volumineuse opacité de tonalité hydrique, homogène, siégeant au niveau du médiastin moyen à son étage inférieur, para-cardiaque droite remontant jusqu’au hile droit, bien limitée, à bord externe net et convexe vers le poumon, alors que le bord interne est noyé dans le médiastin.
Epanchement pleural droit.
Le profil montre le siège médiastinal moyen et postérieur de la lésion.
Fig. 44 : Radiographie thoracique de face Fig. 45 : Radiographie thoracique de profil
2) TDM thoracique
(fig. 46 et 47)Volumineuse masse médiastinale moyenne étendue au médiastin postérieur, mesurant 13×8×6 cm, discrètement hyperdense comportant des calcifications intra-lésionnelles, non rehaussée après injection du produit de contraste.
Cette masse englobe le tronc bronchique intermédiaire avec atélectasie lobaire inférieure.
Compte tenu de son siège sous-carinaire, elle refoule l’artère pulmonaire droite et arrive au contact du bord postérieur de l’aorte ascendante. Aussi elle arrive au contact des veines pulmonaires inférieures droites, et refoule l’oreillette gauche.
Absence d’envahissement endo-vasculaire ou cardiaque.
Par ailleurs, cette lésion présente également des rapports avec le bord droit de l’œsophage.
Absence de lésions pleuro-parenchymateuses. Epanchement pleural droit.
Tous nos patients ont été opérés et l’étude anatomopathologique a confirmé le diagnostic de kyste bronchogénique médiastinal.
Age :
age en années 0 10 20 30 40 50 60 70 cas n°1 cas n° 2 cas n° 3 cas n°4 cas n°5 age en annéesFig. 48 : Histogramme de la répartition d’âge.
Dans notre série, la moyenne d’âge est de 48.6 ans.
Sexe :
On note une nette prédominance féminine : 4 femmes pour un homme.
Circonstances de découverte :
0 0,5 1 1,5 2 2,5 3 d ys p n é e to u x a u tr e s sy m p to m e s symptomatique asymptomatique nombre de cas nombre de casFig. 49 : Histogramme montrant les circonstances de découverte des kystes bronchogéniques.
Trois patients étaient asymptomatiques.
Deux patients étaient symptomatiques, l’un avait une dyspnée (observation 2), l’autre avait une toux chronique (observation 5).
Topographie de la lésion :
1) Compartiment : 0 0,5 1 1,5 2 2,5 3 Médiastin antérieur Médiastin moyen Médiastin postérieurFig.50 : Histogramme montrant la répartition des kystes bronchogéniques en fonction des compartiments
Trois patients ont présenté une localisation médiastinale moyenne (observations 1 ; 3 et 5).
Deux patients avaient une localisation médiastinale antérieure (observations 2 et 4).
![Figure 1 : Bourgeon pulmonaire en coupe sagittale [20].](https://thumb-eu.123doks.com/thumbv2/123doknet/15059413.698243/23.892.244.670.114.965/figure-bourgeon-pulmonaire-coupe-sagittale.webp)
![Figure 2 : Vue latérale gauche du médiastin [27].](https://thumb-eu.123doks.com/thumbv2/123doknet/15059413.698243/27.892.142.803.311.927/figure-vue-latérale-gauche-médiastin.webp)
![Figure 3 : Division du médiastin [28].](https://thumb-eu.123doks.com/thumbv2/123doknet/15059413.698243/28.892.187.731.316.734/figure-division-du-médiastin.webp)
![Fig. 4 : Bords et principales lignes du médiastin [15].](https://thumb-eu.123doks.com/thumbv2/123doknet/15059413.698243/36.892.187.739.158.699/fig-bords-principales-lignes-médiastin.webp)
![Fig. 14 : Coupe transversale passant par le corps thyroïde [15].](https://thumb-eu.123doks.com/thumbv2/123doknet/15059413.698243/48.892.288.649.229.496/fig-coupe-transversale-passant-corps-thyroïde.webp)
![Fig. 19 : Coupe transversale passant par l’espace sous et rétro-carinaire [15].](https://thumb-eu.123doks.com/thumbv2/123doknet/15059413.698243/50.892.296.641.546.824/fig-coupe-transversale-passant-l-espace-rétro-carinaire.webp)