31
FACULTE DE MEDECINE ET DE PHARMACIE - RABAT DOYENS HONORAIRES :
1962 – 1969 : Professeur Abdelmalek FARAJ 1969 – 1974 : Professeur Abdellatif BERBICH
1974 – 1981 : Professeur Bachir LAZRAK 1981 – 1989 : Professeur Taieb CH
KILI
1989 – 1997 : Professeur Mohamed Tahar ALAOUI 1997 – 2003 : Professeur Abdelmajid BELMAHI
2003 – 2013 : Professeur Najia HAJJAJ - HASSOUNI
ADMINISTRATION :
Doyen : Professeur Mohamed ADNAOUI
Vice Doyen chargé des Affaires Académiques et estudiantines Professeur Mohammed AHALLAT
Vice Doyen chargé de la Recherche et de la Coopération Professeur Taoufiq DAKKA
Vice Doyen chargé des Affaires Spécifiques à la Pharmacie Professeur Jamal TAOUFIK
Secrétaire Général : Mr. El Hassane AHALLAT
1- ENSEIGNANTS-CHERCHEURS MEDECINS ET
PHARMACIENS
PROFESSEURS :
Mai et Octobre 1981
Pr. MAAZOUZI Ahmed Wajih Chirurgie Cardio-Vasculaire
Pr. TAOBANE Hamid* Chirurgie Thoracique
Mai et Novembre 1982
Pr. BENOSMAN Abdellatif Chirurgie Thoracique
Novembre 1983
Pr. HAJJAJ Najia ép. HASSOUNI Rhumatologie
Décembre 1984
Pr. MAAOUNI Abdelaziz Médecine Interne – Clinique Royale Pr. MAAZOUZI Ahmed Wajdi Anesthésie -Réanimation
Pr. SETTAF Abdellatif pathologie Chirurgicale
Novembre et Décembre 1985
Pr. BENJELLOUN Halima Cardiologie
Pr. BENSAID Younes Pathologie Chirurgicale Pr. EL ALAOUI Faris Moulay El Mostafa Neurologie
Pr. EL YAACOUBI Moradh Traumatologie Orthopédie Pr. ESSAID EL FEYDI Abdellah Gastro-Entérologie
Pr. LACHKAR Hassan Médecine Interne
Pr. YAHYAOUI Mohamed Neurologie
Décembre 1988
Pr. BENHAMAMOUCH Mohamed Najib Chirurgie Pédiatrique
Pr. DAFIRI Rachida Radiologie
Pr. HERMAS Mohamed Traumatologie Orthopédie
Décembre 1989
Pr. ADNAOUI Mohamed Médecine Interne –Doyen de la FMPR Pr. BOUKILI MAKHOUKHI Abdelali* Cardiologie
Pr. CHAD Bouziane Pathologie Chirurgicale Pr. OUAZZANI Taïbi Mohamed Réda Neurologie
Janvier et Novembre 1990
Pr. CHKOFF Rachid Pathologie Chirurgicale Pr. HACHIM Mohammed* Médecine-Interne
Pr. KHARBACH Aîcha Gynécologie -Obstétrique
Pr. MANSOURI Fatima Anatomie-Pathologique
Pr. TAZI Saoud Anas Anesthésie Réanimation
Février Avril Juillet et Décembre 1991
Pr. AL HAMANY Zaîtounia Anatomie-Pathologique
Pr. AZZOUZI Abderrahim Anesthésie Réanimation –Doyen de la FMPO
Pr. BAYAHIA Rabéa Néphrologie
Pr. BELKOUCHI Abdelkader Chirurgie Générale Pr. BENCHEKROUN Belabbes Abdellatif Chirurgie Générale
Pr. BENSOUDA Yahia Pharmacie galénique
Pr. BERRAHO Amina Ophtalmologie
Pr. BEZZAD Rachid Gynécologie Obstétrique Pr. CHABRAOUI Layachi Biochimie et Chimie
Pr. CHERRAH Yahia Pharmacologie
Pr. CHOKAIRI Omar Histologie Embryologie
Pr. KHATTAB Mohamed Pédiatrie
Pr. SOULAYMANI Rachida Pharmacologie – Dir. du Centre National PV
Pr. TAOUFIK Jamal Chimie thérapeutique
Décembre 1992
Pr. AHALLAT Mohamed Chirurgie Générale
Pr. BENSOUDA Adil Anesthésie Réanimation
Pr. BOUJIDA Mohamed Najib Radiologie
Pr. CHAHED OUAZZANI Laaziza Gastro-Entérologie Pr. CHRAIBI Chafiq Gynécologie Obstétrique
Pr. DAOUDI Rajae Ophtalmologie
Pr. DEHAYNI Mohamed* Gynécologie Obstétrique Pr. EL OUAHABI Abdessamad Neurochirurgie
Pr. TAGHY Ahmed Chirurgie Générale
Pr. ZOUHDI Mimoun Microbiologie
Mars 1994
Pr. BENJAAFAR Noureddine Radiothérapie
Pr. BEN RAIS Nozha Biophysique
Pr. CAOUI Malika Biophysique
Pr. CHRAIBI Abdelmjid Endocrinologie et Maladies Métaboliques Pr. EL AMRANI Sabah Gynécologie Obstétrique
Pr. EL AOUAD Rajae Immunologie
Pr. EL BARDOUNI Ahmed Traumato-Orthopédie Pr. EL HASSANI My Rachid Radiologie
Pr. ERROUGANI Abdelkader Chirurgie Générale- Directeur CHIS
Pr. ESSAKALI Malika Immunologie
Pr. ETTAYEBI Fouad Chirurgie Pédiatrique
Pr. HADRI Larbi* Médecine Interne
Pr. HASSAM Badredine Dermatologie
Pr. IFRINE Lahssan Chirurgie Générale
Pr. JELTHI Ahmed Anatomie Pathologique
Pr. MAHFOUD Mustapha Traumatologie – Orthopédie
Pr. MOUDENE Ahmed* Traumatologie- Orthopédie Inspecteur du SS
Pr. RHRAB Brahim Gynécologie –Obstétrique
Pr. SENOUCI Karima Dermatologie
Mars 1994
Pr. ABBAR Mohamed* Urologie
Pr. ABDELHAK M’barek Chirurgie – Pédiatrique
Pr. BELAIDI Halima Neurologie
Pr. BRAHMI Rida Slimane Gynécologie Obstétrique Pr. BENTAHILA Abdelali Pédiatrie
Pr. BENYAHIA Mohammed Ali Gynécologie – Obstétrique Pr. BERRADA Mohamed Saleh Traumatologie – Orthopédie
Pr. CHAMI Ilham Radiologie
Pr. CHERKAOUI Lalla Ouafae Ophtalmologie
Pr. EL ABBADI Najia Neurochirurgie
Pr. HANINE Ahmed* Radiologie
Pr. JALIL Abdelouahed Chirurgie Générale
Pr. LAKHDAR Amina Gynécologie Obstétrique
Pr. MOUANE Nezha Pédiatrie
Mars 1995
Pr. ABOUQUAL Redouane Réanimation Médicale
Pr. AMRAOUI Mohamed Chirurgie Générale
Pr. BAIDADA Abdelaziz Gynécologie Obstétrique
Pr. BARGACH Samir Gynécologie Obstétrique
Pr. CHAARI Jilali* Médecine Interne
Pr. DIMOU M’barek* Anesthésie Réanimation – Dir. HMIM Pr. DRISSI KAMILI Med Nordine* Anesthésie Réanimation
Pr. OUAZZANI CHAHDI Bahia Ophtalmologie
Pr. SEFIANI Abdelaziz Génétique
Pr. ZEGGWAGH Amine Ali Réanimation Médicale
Décembre 1996
Pr. AMIL Touriya* Radiologie
Pr. BELKACEM Rachid Chirurgie Pédiatrie Pr. BOULANOUAR Abdelkrim Ophtalmologie Pr. EL ALAMI EL FARICHA EL Hassan Chirurgie Générale
Pr. GAOUZI Ahmed Pédiatrie
Pr. MAHFOUDI M’barek* Radiologie
Pr. MOHAMMADI Mohamed Médecine Interne
Pr. OUADGHIRI Mohamed Traumatologie-Orthopédie
Pr. OUZEDDOUN Naima Néphrologie
Pr. ZBIR EL Mehdi* Cardiologie
Novembre 1997
Pr. ALAMI Mohamed Hassan Gynécologie-Obstétrique Pr. BEN SLIMANE Lounis Urologie
Pr. BIROUK Nazha Neurologie
Pr. CHAOUIR Souad* Radiologie
Pr. ERREIMI Naima Pédiatrie
Pr. FELLAT Nadia Cardiologie
Pr. HAIMEUR Charki* Anesthésie Réanimation
Pr. KADDOURI Noureddine Chirurgie Pédiatrique
Pr. KOUTANI Abdellatif Urologie
Pr. LAHLOU Mohamed Khalid Chirurgie Générale
Pr. MAHRAOUI CHAFIQ Pédiatrie
Pr. OUAHABI Hamid* Neurologie
Pr. TAOUFIQ Jallal Psychiatrie
Pr. YOUSFI MALKI Mounia Gynécologie Obstétrique
Novembre 1998
Pr. AFIFI RAJAA Gastro-Entérologie
Pr. BENOMAR ALI Neurologie – Doyen Abulcassis Pr. BOUGTAB Abdesslam Chirurgie Générale
Pr. ER RIHANI Hassan Oncologie Médicale Pr. EZZAITOUNI Fatima Néphrologie
Pr. LAZRAK Khalid * Traumatologie Orthopédie
Pr. BENKIRANE Majid* Hématologie
Pr. KHATOURI ALI* Cardiologie
Pr. LABRAIMI Ahmed* Anatomie Pathologique
Pr. BENJELLOUN Dakhama Badr.Sououd Pédiatrie
Pr. BOURKADI Jamal-Eddine Pneumo-phtisiologie Pr. CHARIF CHEFCHAOUNI Al Montacer Chirurgie Générale Pr. ECHARRAB El Mahjoub Chirurgie Générale Pr. EL FTOUH Mustapha Pneumo-phtisiologie Pr. EL MOSTARCHID Brahim* Neurochirurgie
Pr. ISMAILI Hassane* Traumatologie Orthopédie Pr. MAHMOUDI Abdelkrim* Anesthésie-Réanimation Pr. TACHINANTE Rajae Anesthésie-Réanimation Pr. TAZI MEZALEK Zoubida Médecine Interne
Novembre 2000
Pr. AIDI Saadia Neurologie
Pr. AIT OURHROUI Mohamed Dermatologie Pr. AJANA Fatima Zohra Gastro-Entérologie
Pr. BENAMR Said Chirurgie Générale
Pr. CHERTI Mohammed Cardiologie
Pr. ECH-CHERIF EL KETTANI Selma Anesthésie-Réanimation
Pr. EL HASSANI Amine Pédiatrie
Pr. EL KHADER Khalid Urologie
Pr. EL MAGHRAOUI Abdellah* Rhumatologie
Pr. GHARBI Mohamed El Hassan Endocrinologie et Maladies Métaboliques
Pr. HSSAIDA Rachid* Anesthésie-Réanimation
Pr. LAHLOU Abdou Traumatologie Orthopédie
Pr. MAFTAH Mohamed* Neurochirurgie
Pr. MAHASSINI Najat Anatomie Pathologique
Pr. MDAGHRI ALAOUI Asmae Pédiatrie
Pr. NASSIH Mohamed* Stomatologie Et Chirurgie Maxillo-Faciale
Pr. ROUIMI Abdelhadi* Neurologie
Décembre 2000
Pr. ZOHAIR ABDELAH* ORL
Décembre 2001
Pr. ABABOU Adil Anesthésie-Réanimation
Pr. BALKHI Hicham* Anesthésie-Réanimation
Pr. BENABDELJLIL Maria Neurologie
Pr. BENAMAR Loubna Néphrologie
Pr. BENAMOR Jouda Pneumo-phtisiologie
Pr. BENELBARHDADI Imane Gastro-Entérologie
Pr. BENNANI Rajae Cardiologie
Pr. BENOUACHANE Thami Pédiatrie
Pr. BEZZA Ahmed* Rhumatologie
Pr. BOUCHIKHI IDRISSI Med Larbi Anatomie Pr. BOUMDIN El Hassane* Radiologie
Pr. CHAT Latifa Radiologie
Pr. EL MADHI Tarik Chirurgie-Pédiatrique Pr. EL OUNANI Mohamed Chirurgie Générale
Pr. ETTAIR Said Pédiatrie
Pr. GAZZAZ Miloudi* Neuro-Chirurgie
Pr. HRORA Abdelmalek Chirurgie Générale
Pr. KABBAJ Saad Anesthésie-Réanimation
Pr. KABIRI EL Hassane* Chirurgie Thoracique Pr. LAMRANI Moulay Omar Traumatologie Orthopédie
Pr. LEKEHAL Brahim Chirurgie Vasculaire Périphérique Pr. MAHASSIN Fattouma* Médecine Interne
Pr. MEDARHRI Jalil Chirurgie Générale
Pr. MIKDAME Mohammed* Hématologie Clinique
Pr. MOHSINE Raouf Chirurgie Générale
Pr. NOUINI Yassine Urologie
Pr. SABBAH Farid Chirurgie Générale
Pr. SEFIANI Yasser Chirurgie Vasculaire Périphérique Pr. TAOUFIQ BENCHEKROUN Soumia Pédiatrie
Décembre 2002
Pr. AL BOUZIDI Abderrahmane* Anatomie Pathologique
Pr. AMEUR Ahmed * Urologie
Pr. AMRI Rachida Cardiologie
Pr. AOURARH Aziz* Gastro-Entérologie
Pr. BAMOU Youssef * Biochimie-Chimie
Pr. BELMEJDOUB Ghizlene* Endocrinologie et Maladies Métaboliques
Pr. BENZEKRI Laila Dermatologie
Pr. BENZZOUBEIR Nadia Gastro-Entérologie Pr. BERNOUSSI Zakiya Anatomie Pathologique Pr. BICHRA Mohamed Zakariya* Psychiatrie
Pr. CHOHO Abdelkrim * Chirurgie Générale
Pr. CHKIRATE Bouchra Pédiatrie
Pr. EL ALAMI EL FELLOUS Sidi Zouhair Chirurgie Pédiatrique Pr. EL HAOURI Mohamed * Dermatologie
Pr. EL MANSARI Omar* Chirurgie Générale Pr. FILALI ADIB Abdelhai Gynécologie Obstétrique
Pr. HAJJI Zakia Ophtalmologie
Pr. IKEN Ali Urologie
Pr. JAAFAR Abdeloihab* Traumatologie Orthopédie
Pr. KRIOUILE Yamina Pédiatrie
Pr. LAGHMARI Mina Ophtalmologie
Pr. MABROUK Hfid* Traumatologie Orthopédie
Pr. MOUSSAOUI RAHALI Driss* Gynécologie Obstétrique Pr. MOUSTAGHFIR Abdelhamid* Cardiologie
Pr. NAITLHO Abdelhamid* Médecine Interne
Pr. OUJILAL Abdelilah Oto-Rhino-Laryngologie Pr. RACHID Khalid * Traumatologie Orthopédie
Pr. SIAH Samir * Anesthésie Réanimation
Pr. THIMOU Amal Pédiatrie
Pr. ZENTAR Aziz* Chirurgie Générale
Janvier 2004
Pr. ABDELLAH El Hassan Ophtalmologie
Pr. AMRANI Mariam Anatomie Pathologique
Pr. BENBOUZID Mohammed Anas Oto-Rhino-Laryngologie Pr. BENKIRANE Ahmed* Gastro-Entérologie Pr. BOUGHALEM Mohamed* Anesthésie Réanimation
Pr. BOULAADAS Malik Stomatologie et Chirurgie Maxillo-faciale
Pr. BOURAZZA Ahmed* Neurologie
Pr. CHAGAR Belkacem* Traumatologie Orthopédie
Pr. CHERRADI Nadia Anatomie Pathologique
Pr. EL FENNI Jamal* Radiologie
Pr. EL HANCHI ZAKI Gynécologie Obstétrique Pr. EL KHORASSANI Mohamed Pédiatrie
Pr. EL YOUNASSI Badreddine* Cardiologie
Pr. HACHI Hafid Chirurgie Générale
Pr. JABOUIRIK Fatima Pédiatrie
Pr. KHABOUZE Samira Gynécologie Obstétrique Pr. KHARMAZ Mohamed Traumatologie Orthopédie
Pr. LEZREK Mohammed* Urologie
Pr. MOUGHIL Said Chirurgie Cardio-Vasculaire Pr. OUBAAZ Abdelbarre* Ophtalmologie
Pr. TARIB Abdelilah* Pharmacie Clinique Pr. TIJAMI Fouad Chirurgie Générale
Pr. ZARZUR Jamila Cardiologie
Janvier 2005
Pr. ABBASSI Abdellah Chirurgie Réparatrice et Plastique Pr. AL KANDRY Sif Eddine* Chirurgie Générale
Pr. ALAOUI Ahmed Essaid Microbiologie
Pr. ALLALI Fadoua Rhumatologie
Pr. AMAZOUZI Abdellah Ophtalmologie
Pr. AZIZ Noureddine* Radiologie
Pr. BAHIRI Rachid Rhumatologie
Pr. BARKAT Amina Pédiatrie
Pr. BENHALIMA Hanane Stomatologie et Chirurgie Maxillo Faciale
Pr. BENYASS Aatif Cardiologie
Pr. BERNOUSSI Abdelghani Ophtalmologie Pr. CHARIF CHEFCHAOUNI Mohamed Ophtalmologie
Pr. DOUDOUH Abderrahim* Biophysique
Pr. EL HAMZAOUI Sakina* Microbiologie
Pr. HAJJI Leila Cardiologie (mise en disponibilité)
Pr. HESSISSEN Leila Pédiatrie
Pr. JIDAL Mohamed* Radiologie
Pr. SBIHI Souad Histo-Embryologie Cytogénétique Pr. ZERAIDI Najia Gynécologie Obstétrique
Décembre 2005
Pr. CHANI Mohamed Anesthésie Réanimation
Avril 2006
Pr. ACHEMLAL Lahsen* Rhumatologie
Pr. AKJOUJ Said* Radiologie
Pr. BELMEKKI Abdelkader* Hématologie
Pr. BENCHEIKH Razika O.R.L
Pr. BIYI Abdelhamid* Biophysique
Pr. BOUHAFS Mohamed El Amine Chirurgie - Pédiatrique Pr. BOULAHYA Abdellatif* Chirurgie Cardio – Vasculaire Pr. CHENGUETI ANSARI Anas Gynécologie Obstétrique
Pr. DOGHMI Nawal Cardiologie
Pr. ESSAMRI Wafaa Gastro-entérologie
Pr. FELLAT Ibtissam Cardiologie
Pr. FAROUDY Mamoun Anesthésie Réanimation
Pr. GHADOUANE Mohammed* Urologie
Pr. HARMOUCHE Hicham Médecine Interne Pr. HANAFI Sidi Mohamed* Anesthésie Réanimation Pr. IDRISS LAHLOU Amine* Microbiologie
Pr. JROUNDI Laila Radiologie
Pr. KARMOUNI Tariq Urologie
Pr. KILI Amina Pédiatrie
Pr. KISRA Hassan Psychiatrie
Pr. KISRA Mounir Chirurgie – Pédiatrique
Pr. LAATIRIS Abdelkader* Pharmacie Galénique Pr. LMIMOUNI Badreddine* Parasitologie
Pr. MANSOURI Hamid* Radiothérapie
Pr. OUANASS Abderrazzak Psychiatrie
Pr. SAFI Soumaya* Endocrinologie
Pr. SEKKAT Fatima Zahra Psychiatrie
Pr. SOUALHI Mouna Pneumo – Phtisiologie
Pr. TELLAL Saida* Biochimie
Pr. ZAHRAOUI Rachida Pneumo – Phtisiologie
Octobre 2007
Pr. ABIDI Khalid Réanimation médicale
Pr. ACHACHI Leila Pneumo phtisiologie
Pr. ACHOUR Abdessamad* Chirurgie générale
Pr. AIT HOUSSA Mahdi* Chirurgie cardio vasculaire Pr. AMHAJJI Larbi* Traumatologie orthopédie
Pr. AMMAR Haddou* ORL
Pr. AOUFI Sarra Parasitologie
Pr. BOUTIMZINE Nourdine Ophtalmologie Pr. CHARKAOUI Naoual* Pharmacie galénique Pr. EHIRCHIOU Abdelkader* Chirurgie générale
Pr. ELABSI Mohamed Chirurgie générale
Pr. EL MOUSSAOUI Rachid Anesthésie réanimation
Pr. EL OMARI Fatima Psychiatrie
Pr. GANA Rachid Neuro chirurgie
Pr. GHARIB Noureddine Chirurgie plastique et réparatrice
Pr. HADADI Khalid* Radiothérapie
Pr. ICHOU Mohamed* Oncologie médicale
Pr. ISMAILI Nadia Dermatologie
Pr. KEBDANI Tayeb Radiothérapie
Pr. LALAOUI SALIM Jaafar* Anesthésie réanimation
Pr. LOUZI Lhoussain* Microbiologie
Pr. MADANI Naoufel Réanimation médicale
Pr. MAHI Mohamed* Radiologie
Pr. MARC Karima Pneumo phtisiologie
Pr. MASRAR Azlarab Hématologique
Pr. MOUTAJ Redouane * Parasitologie
Pr. MRABET Mustapha* Médecine préventive santé publique et hygiène
Pr. MRANI Saad* Virologie
Pr. OUZZIF Ez zohra* Biochimie-chimie
Pr. RABHI Monsef* Médecine interne
Pr. RADOUANE Bouchaib* Radiologie
Pr. SEFFAR Myriame Microbiologie
Pr. SEKHSOKH Yessine* Microbiologie
Pr. SIFAT Hassan* Radiothérapie
Pr. TABERKANET Mustafa* Chirurgie vasculaire périphérique
Pr. TACHFOUTI Samira Ophtalmologie
Pr. TAJDINE Mohammed Tariq* Chirurgie générale
Pr. TANANE Mansour* Traumatologie orthopédie
Pr. TLIGUI Houssain Parasitologie
Pr. TOUATI Zakia Cardiologie
Décembre 2007
Pr. DOUHAL ABDERRAHMAN Ophtalmologie
Décembre 2008
Pr ZOUBIR Mohamed* Anesthésie Réanimation Pr TAHIRI My El Hassan* Chirurgie Générale
Mars 2009
Pr. ABOUZAHIR Ali* Médecine interne
Pr. ALLALI Nazik Radiologie
Pr. AMAHZOUNE Brahim* Chirurgie Cardio-vasculaire
Pr. AMINE Bouchra Rhumatologie
Pr. ARKHA Yassir Neuro-chirurgie
Pr. AZENDOUR Hicham* Anesthésie Réanimation Pr. BELYAMANI Lahcen* Anesthésie Réanimation
Pr. BJIJOU Younes Anatomie
Pr. BOUHSAIN Sanae* Biochimie-chimie
Pr. BOUI Mohammed* Dermatologie
Pr. BOUNAIM Ahmed* Chirurgie Générale
Pr. BOUSSOUGA Mostapha* Traumatologie orthopédique Pr. CHAKOUR Mohammed * Hématologie biologique
Pr. CHTATA Hassan Toufik* Chirurgie vasculaire périphérique
Pr. DOGHMI Kamal* Hématologie clinique
Pr. EL MALKI Hadj Omar Chirurgie Générale Pr. EL OUENNASS Mostapha* Microbiologie
Pr. ENNIBI Khalid* Médecine interne
Pr. FATHI Khalid Gynécologie obstétrique
Pr. HASSIKOU Hasna * Rhumatologie
Pr. KABBAJ Nawal Gastro-entérologie
Pr. KABIRI Meryem Pédiatrie
Pr. KARBOUBI Lamya Pédiatrie
Pr. L’KASSIMI Hachemi* Microbiologie
Pr. LAMSAOURI Jamal* Chimie Thérapeutique Pr. MARMADE Lahcen Chirurgie Cardio-vasculaire
Pr. MESKINI Toufik Pédiatrie
Pr. MESSAOUDI Nezha * Hématologie biologique
Pr. MSSROURI Rahal Chirurgie Générale
Pr. NASSAR Ittimade Radiologie
Pr. OUKERRAJ Latifa Cardiologie
Pr. RHORFI Ismail Abderrahmani * Pneumo-phtisiologie
Pr. ZOUHAIR Said* Microbiologie
PROFESSEURS AGREGES :
Octobre 2010
Pr. ALILOU Mustapha Anesthésie réanimation
Pr. AMEZIANE Taoufiq* Médecine interne
Pr. BELAGUID Abdelaziz Physiologie
Pr. BOUAITY Brahim* ORL
Pr. CHADLI Mariama* Microbiologie
Pr. CHEMSI Mohamed* Médecine aéronautique
Pr. DAMI Abdellah* Biochimie chimie
Pr. DARBI Abdellatif* Radiologie
Pr. DENDANE Mohammed Anouar Chirurgie pédiatrique
Pr. EL HAFIDI Naima Pédiatrie
Pr. LAMALMI Najat Anatomie pathologique
Pr. LEZREK Mounir Ophtalmologie
Pr. MALIH Mohamed* Pédiatrie
Pr. MOSADIK Ahlam Anesthésie Réanimation
Pr. MOUJAHID Mountassir* Chirurgie générale
Pr. NAZIH Mouna* Hématologie
Pr. ZOUAIDIA Fouad Anatomie pathologique
Mai 2012
Pr. AMRANI Abdelouahed Chirurgie Pédiatrique Pr. ABOUELALAA Khalil* Anesthésie Réanimation
Pr. BELAIZI Mohamed* Psychiatrie
Pr. BENCHEBBA Driss* Traumatologie Orthopédique
Pr. DRISSI Mohamed* Anesthésie Réanimation
Pr. EL ALAOUI MHAMDI Mouna Chirurgie Générale Pr. EL KHATTABI Abdessadek* Médecine Interne Pr. EL OUAZZANI Hanane* Pneumophtisiologie Pr. ER-RAJI Mounir Chirurgie Pédiatrique
Pr. JAHID Ahmed Anatomie pathologique
Pr. MEHSSANI Jamal* Psychiatrie
Pr. RAISSOUNI Maha* Cardiologie
Février 2013
Pr. AHID Samir Pharmacologie – Chimie
Pr. AIT EL CADI Mina Toxicologie
Pr. AMRANI HANCHI Laila Gastro-Entérologie
Pr. AMOUR Mourad Anesthésie Réanimation
Pr. AWAB Almahdi Anesthésie Réanimation
Pr. BELAYACHI Jihane Réanimation Médicale Pr. BELKHADIR Zakaria Houssain Anesthésie Réanimation Pr. BENCHEKROUN Laila Biochimie-Chimie
Pr. BENKIRANE Souad Hématologie
Pr. BENNANA Ahmed* Informatique Pharmaceutique
Pr. BENSEFFAJ Nadia Immunologie
Pr. BENSGHIR Mustapha* Anesthésie Réanimation
Pr. BENYAHIA Mohammed* Néphrologie
Pr. BOUATIA Mustapha Chimie Analytique
Pr. BOUABID Ahmed Salim* Traumatologie Orthopédie
Pr. BOUTARBOUCH Mahjouba Anatomie
Pr. CHAIB Ali* Cardiologie
Pr. DENDANE Tarek Réanimation Médicale
Pr. DINI Nouzha* Pédiatrie
Pr. ECH-CHERIF EL KETTANI Mohamed Ali Anesthésie Réanimation Pr. ECH-CHERIF EL KETTANI Najwa Radiologie
Pr. EL KABABRI Maria Pédiatrie
Pr. EL KHANNOUSSI Basma Anatomie Pathologie
Pr. EL KHLOUFI Samir Anatomie
Pr. EL KORAICHI Alae Anesthésie Réanimation Pr. EN-NOUALI Hassane* Radiologie
Pr. ERRGUIG Laila Physiologie
Pr. FIKRI Meryim Radiologie
Pr. GHANIMI Zineb Pédiatrie
Pr. GHFIR Imade Médecine Nucléaire
Pr. IMANE Zineb Pédiatrie
Pr. IRAQI Hind Endocrinologie et maladies métaboliques
Pr. KABBAJ Hakima Microbiologie
Pr. KADIRI Mohamed* Psychiatrie
Pr. LATIB Rachida Radiologie
Pr. MAAMAR Mouna Fatima Zahra Médecine Interne
Pr. MEDDAH Bouchra Pharmacologie
Pr. MELHAOUI Adyl Neuro-chirurgie
Pr. MRABTI Hind Oncologie Médicale
Pr. NEJJARI Rachid Pharmacognosie
Pr. OUBEJJA Houda Chirurgie Pédiatrique Pr. OUKABLI Mohamed* Anatomie Pathologique
Pr. RAHALI Younes Pharmacie Galénique
Pr. RATBI Ilham Génétique
Pr. RAHMANI Mounia Neurologie
Pr. REDA Karim* Ophtalmologie
Pr. REGRAGUI Wafa Neurologie
Pr. RKAIN Hanan Physiologie
Pr. ROSTOM Samira Rhumatologie
Pr. ROUAS Lamiaa Anatomie Pathologique
Pr. ROUIBAA Fedoua* Gastro-Entérologie
Pr. SALIHOUN Mouna Gastro-Entérologie
Pr. SAYAH Rochde Chirurgie Cardio-Vasculaire
Pr. SEDDIK Hassan* Gastro-Entérologie
Pr. ZERHOUNI Hicham Chirurgie Pédiatrique
Pr. ZINE Ali* Traumatologie Orthopédie
Avril 2013
Pr. EL KHATIB Mohamed Karim* Stomatologie et Chirurgie Maxillo-faciale
Pr. GHOUNDALE Omar* Urologie
PROFESSEURS / PRs. HABILITES
Pr. ABOUDRAR Saadia Physiologie
Pr. ALAMI OUHABI Naima Biochimie – chimie
Pr. ALAOUI KATIM Pharmacologie
Pr. ALAOUI SLIMANI Lalla Naïma Histologie-Embryologie
Pr. ANSAR M’hammed Chimie Organique et Pharmacie Chimique
Pr. BOUHOUCHE Ahmed Génétique Humaine
Pr. BOUKLOUZE Abdelaziz Applications Pharmaceutiques
Pr. BOURJOUANE Mohamed Microbiologie
Pr. BARKYOU Malika Histologie-Embryologie
Pr. CHAHED OUAZZANI Lalla Chadia Biochimie – chimie
Pr. DAKKA Taoufiq Physiologie
Pr. DRAOUI Mustapha Chimie Analytique
Pr. EL GUESSABI Lahcen Pharmacognosie
Pr. ETTAIB Abdelkader Zootechnie
Pr. FAOUZI Moulay El Abbes Pharmacologie
Pr. HAMZAOUI Laila Biophysique
Pr. HMAMOUCHI Mohamed Chimie Organique
Pr. IBRAHIMI Azeddine Biologie moléculaire Pr. KHANFRI Jamal Eddine Biologie
Pr. OULAD BOUYAHYA IDRISSI Med Chimie Organique
Pr. REDHA Ahlam Chimie
Pr. TOUATI Driss Pharmacognosie
Pr. ZAHIDI Ahmed Pharmacologie
Pr. ZELLOU Amina Chimie Organique
Mise à jour le 09/01/2015 par le Service des Ressources Humaines
ACM : Artère cérébrale moyenne.
AVP : Accident de la voie publique.
CMRglucose : consommation cérébrale en glucose.
CMRO2 : Extraction cérébrale moyenne en oxygène
DSC : Débit sanguin cérébral.
DTC : Doppler transcrânien.
EDTC : Echo doppler transcrânien.
GCS : Glasgow Coma Scale.
HITS : High Intensity Transient Signals.
HTIC : Hypertension intracrânienne.
IP : Indice de pulsatilité ou indice de Gosling.
IR : Indice de résistance ou indice de Pourcelot.
IRM : Imagerie par résonance magnétique.
LCR : Liquide céphalo-rachidien.
LIC : Lésions intracérébrales.
MES : Micro Emboli Signal.
NAA : Acétyl Amino-Succinate.
PIC : Pression intracrânienne.
PICA : Artères cérébelleuses postéro-inférieures.
PPC : Pression de perfusion cérébrale.
Q : Débit.
S : Section.
SAUV : Salle d’accueil des urgences vitales.
TC : Traumatisme crânien.
TCG : traumatisme crânien grave.
TDM : tomodensitométrie.
UH : Unité Hounsfield.
V : Vélocité.
VM : Vélocité moyenne.
VSM : Vélocité systolique maximale.
A mes parents
Aucun hommage ne saurait être à la hauteur de vos sacrifices, de
l’amour et du soutien dont vous n’avez cessé de m’entourer.
Vous avez toujours été présents, dans les moments les plus difficiles,
prodiguant inlassablement amour, conseils et encouragements.
Comme à l’accoutumée, votre participation active à ce travail n’a pas
A ma sœur Najoua
Merci d’avoir été l’exemple idéal de la sœur aînée.
Tellement semblables mais si différentes, tu es ma meilleure amie, ma
confidente, mon modèle.
A mon frère amine
En témoignage de l’amour qui nous unit, je te dédie mon travail et ma
réussite.
Dans l’espoir de te retrouver bientôt parmi nous, je te souhaite bonne
chance
A Marouan et Maryam
Merci d’être présents, je vous aime
A ma princesse Sofia et mes petits bijoux Jad et Mehdi
Que dieu vous garde et vous protège
Tata vous aime.
A nos beaux souvenirs, à tous ces moments passés ensembles qui
restent gravés dans la mémoire, à notre complicité et à notre attachement.
A Adnane
A nos meilleurs souvenirs, à nos moments de folie, à nos rires et
sourires, et à nos années de jeunesse…..
Tu m’as toujours soutenu, compris et réconforté, tu es et tu resteras
toujours ma source d’inspiration.
Puisse dieu nous préserver du mal, nous combler de santé, de bonheur
et nous procurer une longue vie pour le service de dieu… ..
A la mémoire de ma grand-mère Hajja Charafa
Dont l’absence se fait cruellement sentir
A ma grand-mère Hajja fettouma
Que dieu vous garde pour nous
A la mémoire de mes grands parents
Qui nous ont quitté trop tôt
A tous mes oncles et tantes, à toute ma famille
A nos souvenirs heureux
A mes amis
En témoignage de l’amitié qui nous unit, je vous dédie ce travail.
A tous ceux qui ont contribué, de près ou
de loin, à la réalisation de ce travail.
A notre maître, rapporteur et président de thèse
Monsieur le professeur M.Faroudy
Professeur de l’enseignement supérieur d’anesthésie-réanimation
CHU Ibn Sina- Rabat
Vous m’avez honoré par votre confiance en me confiant cet excellent
sujet de travail.
Les conseils fructueux que vous nous avez prodigué ont été très
précieux, nous vous en remercions.
Vous êtes un homme de science et un médecin attentif au bien-être de
ses patients.
C’est avec sincérité que nous vous exprimons notre admiration pour le
professeur, mais aussi pour la personne que vous êtes.
Nous avons pu, au cours des stages passés sous votre direction,
apprécier vos qualités humaines, votre savoir-faire
et vos compétences scientifiques.
Veuillez trouver ici, l’assurance de notre
reconnaissance et notre admiration.
A notre maître et juge de thèse
Madame le Professeur N.El Abbadi
Professeur de l’enseignement supérieur de neurochirurgie
CHU Ibn Sina- Rabat
Vous nous avez accordé un grand honneur en acceptant de juger nôtre
travail.
Nous avons eu la chance et le privilège de profiter de votre culture
scientifique, vos compétences professionnelles incontestables ainsi que vos
qualités humaines qui vous valent l’admiration et le respect.
Veuillez Madame, trouver dans ce modeste travail l’expression de
A notre maître et juge de thèse
Madame le professeur I. Nassar
Professeur agrégé de radiologie
CHU Ibn Sina- Rabat
Nous sommes particulièrement touchés par la gentillesse avec laquelle
vous avez bien voulu accepter de juger ce travail.
Votre parcours professionnel, votre compétence incontestable, votre
charisme inspirent une grande admiration et un profond respect.
Permettez-moi, cher maître de vous exprimer notre profond respect et
notre sincère gratitude.
A notre maître et juge de thèse
Monsieur le professeur A.Kettani
Professeur agrégé d’anesthésie-réanimation
CHU Ibn Sina- Rabat
Nous vous remercions pour l’honneur que vous nous faîtes en
acceptant de juger ce travail.
Votre bonté, votre modestie, votre compréhension, ainsi que vos
qualités professionnelles ne peuvent que susciter notre grand estime et
profond respect.
Veuillez trouver dans ce travail, cher maître, l’expression de notre
estime et notre considération.
A notre maître et juge de thèse
Monsieur le professeur A. EL koraichi
Professeur agrégé d’anesthésie-réanimation
CHU Ibn Sina- Rabat
Nous vous remercions de la spontanéité et de la simplicité avec
lesquelles vous avez accepté de juger ce travail
Nous espérons être dignes de votre confiance, et nous prions, cher
maître, d’accepter notre profonde reconnaissance et notre haute
considération.
INTRODUCTION ... 1 RAPPEL ANATOMIQUE ... 5 RAPPEL PHYSIOLOGIQUE ... 10 I/ METABOLISME CEREBRAL ... 11 II. DEBIT SANGUIN CEREBRAL ... 11 A/ débit sanguin cérébral normal ... 11 B/ variation physiologique du DSC, Autorégulation du débit sanguin cérébral ... 11 1/ L’âge ... 11 2/ Pression artérielle moyenne ... 12 3/ l’hématocrite ... 14 4/ La température ... 14 5/ L’hypoxie ... 15 6/ Pression partielle en CO2 (PaCO2) ... 15 7/ Débit cardiaque ... 16 III/ COUPLAGE DEBIT-METABOLISME... 16 IMAGERIE CONVENTIONNELLE DES LESIONS CEREBRALES POST TRAUMATIQUES ... 19 I/ LESIONS EXTRAPARENCHYMATEUSES ... 22 A/ L’hématome extradural ... 22 B/ L’hématome sous-dural ... 23 C/ L’hémorragie méningée ... 23
F/ La dissection vasculaire ... 24 II/ LESIONS INTRAPARENCHYMATEUSES PRIMAIRES ... 25 A/ L’œdème cérébral ... 25 B/ Les contusions hémorragiques ... 25 C/ Lésions axonales diffuses ... 27 III/ LESIONS INTRAPARENCHYMATEUSES SECONDAIRES ... 30 LE DOPPLER TRANSCRANIEN ... 31 I/ HISTORIQUE ... 32 II/ PRINCIPE ... 32 III/ MATERIEL UTILISE ... 36 IV/ TECHNIQUE DE REALISATION ... 37 V/ LES FENETRES ACOUSTIQUES ... 37 A/ Fenêtre temporale ... 38 1/ Repères mode B ... 38 2/ Le système carotidien en fenêtre temporale ... 40 3/ Le système vertébro-basilaire en fenêtre temporale ... 40 B/ Fenêtre orbitaire ... 41 C/ Fenêtre sous occipitale ... 42 VI/ LES PARAMETRES EVALUES... 42 VII/ INTERPRETATION DES RESULTATS ... 44
CRANIEN ... 48 A/ L’hémorragie méningée anévrismale: ... 48 B/ Les sténoses et les occlusions intracrâniennes ... 49 C/ Détection des embols asymptomatiques _HITS ... 49 D/ Bilan de suppléances ... 50 E/ Diagnostic de mort cérébrale ... 50 F/ Imagerie vasculaire morphologique ; anévrysmes intracrâniens ... 52 IX/ DTC ET TRAUMATISME CRANIEN GRAVE ... 53 MATERIEL ET METHODES ... 55 I/ Matériel ... 56 A/ Type de l’étude ... 56 B/ Population de l’étude ... 56 1/ Critères d’inclusion ... 56 2/ Critères d’exclusion ... 56 II/ Méthode... 57 RESULTATS ... 59 I/ DONNEES EPIDEMIOLOGIQUES... 60 A/ SEXE ... 60 B/ Age ... 60 C/ Antécédents ... 60 D/ Circonstances de survenue ... 61 E/ Délai d’admission ... 61
B/ Diagnostics cliniques ... 62 III/ DONNEES RADIOLOGIQUES INITIALES ... 63 A/ Scanner cérébral initial ... 63 B/ Doppler transcrânien ... 65 IV/ THERAPEUTIQUE CHIRURGICALE INITIALE ... 66 V/ IMAGERIE DE CONTROLE ... 66 A/ TDM de contrôle systématique à H48 ... 66 B/ TDM réalisées pour DTC pathologiques ... 67 VI/ Modifications thérapeutiques sur la base de l’imagerie de contrôle ... 68 A/ TDM de contrôle systématique à H48 ... 68 B/ Doppler transcrânien ... 68 VII/ Evolution ... 70 DISCUSSION ... 73 CONCLUSION... 86 RESUME ... 88 ANNEXES ... 92 REFERENCES ... 99
Les traumatismes crâniens (TC) représentent la principale cause de décès et d’handicap majeur avant 45 ans. Il s’agit d’un problème de santé publique mondial. Les accidents de la voie publique (AVP) représentent la cause principale de cette pathologie. L’incidence annuelle en France des traumatisés crâniens est estimée entre 150000 et 300000 hospitalisations par an. Près de 80% de ces patients sont admis aux urgences pour TC mineurs (15-14) ou modérés (13-9) [1]. Ente 8 et 10% d’entre eux peuvent avoir des lésions intracérébrales avec recours à la chirurgie dans 1% des cas [2]. Néanmoins, le risque d’aggravation neurologique chez ces patients à la phase aigüe est réel (1-30%) [3].
Au niveau national, le nombre de tués lors d’AVP oscille aux alentours de 4000/an, les blessés graves près de 12000/an. L’absence de système de recueil systématique des cas de TC quelle qu’en soit le mécanisme explique l’absence de données nationales.
La surveillance neurologique représente le pilier principal de la prise en charge des (TC) à la phase aigüe. Elle a pour objectif majeur de dépister précocement une aggravation neurologique réversible par des mesures thérapeutiques médicales ou curables chirurgicalement.
Cette surveillance neurologique s’avère plus simple pour les TC mineurs et modérés et est basée sur l’évaluation de l’état de conscience suivant le score de Glasgow (GCS).
Le chiffre exact de GCS à l’admission ne doit pas être retenu pour définir le TC grave, car l’évolution des lésions entraine systématiquement une aggravation secondaire de l’état neurologique.
Ces TC sévères nécessitent rarement un geste chirurgical à l’admission. En revanche, ils imposent toujours une réanimation rapide et bien conduite. Cette réanimation est basée sur la connaissance des mécanismes physiologiques de la circulation cérébrale et ses modifications au cours de l’agression encéphalique. La prise en charge médicale ne vise pas à traiter les lésions primaires directement causées par le traumatisme mais à éviter les lésions d’agression cérébrale secondaire responsables de l’ischémie cérébrale.
La sédation-analgésie thérapeutique, représente un volet fondamental dans la prise en charge médicale à la phase aigüe du TC, mais rend l’évaluation neurologique clinique impossible.
En traumatologie crânienne, la TDM cérébrale est l’examen de référence pour déceler les lésions intra et ou extra-parenchymateuses. Mais elle est prise en défaut pour prédire le risque d’aggravation surtout lorsqu’elle est normale ou peu contributive [3].La crainte d’une indication chirurgicale restant la justification la plus fréquemment mise en avant lors de la demande d’examen tomodensitométrique.
C’est dans ce contexte que le doppler transcrânien (DTC), réalisé à l’admission, puis répété, permet de dépister d’une façon précoce les patients à risque d’aggravation. Il s’agit d’un examen rapide, non invasif, qui permet l’étude de l’hémodynamique cérébrale au lit du malade et dont l’emploi est largement répandu en réanimation [3].
L’objectif principal de cette étude, est de démontrer l’intérêt du DTC dans la hiérarchisation des autres examens complémentaires, en l’occurrence la TDM cérébrale. Les objectifs secondaires sont l’étude des aspects lésionnels des
traumatisés crâniens admis durant la période de l’étude ainsi que l’évaluation de l’impact du DTC sur les pratiques de réanimation visant à optimisant la circulation cérébrale.
Les artères du cerveau proviennent de quatre troncs artériels : deux artères vertébrales constituant le courant artériel postérieur et deux artères carotides internes représentant le courant artériel antérieur.
Les artères vertébrales pénètrent dans le crâne par le trou occipital, contournent la face latérale du bulbe et se réunissent en avant de lui, sur la ligne médiane, à la hauteur du sillon bulbo-protubérantielle, pour former le tronc basilaire. Celui-ci repose sur la gouttière basilaire et dans la gouttière protubérantielle médiane située sur la face antérieure de la protubérance. Le tronc basilaire donne, à ce niveau, des collatérales ; il se divise au niveau du sillon ponto-pédonculaire en deux branches, ce sont les artères cérébrales postérieures.
Les deux artères carotides internes débouchent, dans la cavité crânienne, au niveau de l’extrémité antérieure du sinus caverneux. Chaque artère donne aussitôt une collatérale, l’artère ophtalmique. Les artères carotides internes arrivent verticalement à la base du cerveau où elles se divisent, en dehors du chiasma optique, en quatre branches terminales ; ce sont les artères : cérébrale antérieure, en avant et en dedans ; communicante postérieure, en arrière ; choroïdienne antérieure, en arrière et en dehors, et l’artère cérébrale moyenne (ACM), en dehors.
A : l’artère cérébrale antérieure se dirige en avant, passe au-dessus du nerf optique et s’unit, en avant du chiasma optique, à celle du côté opposé par une courte anastomose transversale, appelée artère communicante antérieure. Elle s’élève ensuite vers la scissure inter hémisphérique et chemine le long du bec du corps calleux. Elle abandonne des branches variables, rejoignant la face
inférieure du lobe frontal et le bulbe olfactif ; les autres branches s’épanouissent à la face médiale de l’hémisphère cérébral.
B : l’artère communicante postérieure se dirige en arrière, croise la face inférieure de la bandelette optique et s’anastomose avec l’artère cérébrale postérieure, branche du tronc basilaire.
C : l’artère choroïdienne antérieure chemine le long de la bandelette optique jusqu’au plexus choroïde du ventricule latéral. Les collatérales de cette artère vascularisent la bandelette optique, la partie temporale des radiations optiques, l’hippocampe, la queue du noyau caudé et le noyau amygdalien.
D : l’artère cérébrale moyenne se dirige vers le dehors et se place dans le fond de la fosse sylvienne où elle se divise en plusieurs branches : les artères insulaires, pour le cortex de l’insula, et les artères corticales qui émergent du fond de la fosse sylvienne pour se répartir à la face latérale de l’hémisphère. Ces branches naissent perpendiculairement à la direction de l’artère carotide interne et sont situées dans un plan horizontal par rapport à la face inférieure du cerveau. Toutes les artères cérébrales amènent avec elles, dans leurs adventices, des rameaux sympathiques issus, soit du plexus carotidien, soit du plexus de l’artère vertébrale. Le courant artériel carotidien est plus important que le courant artériel vertébral, dans un rapport de deux à un. Ainsi, malgré tous les systèmes de suppléance par des anastomoses intracérébrales, l’impact d’une ligature carotidienne est sérieux.
L'ACM peut être divisée en quatre segments successifs. Le segment M1 ou sphénoïdal (parfois horizontal) passe à proximité de l'os sphénoïde, d'où son nom. Il a une direction horizontale, parfois descendante et donne les artères
lenticulostriées à destination des ganglions de la base. Le segment M2 ou insulaire est située devant de l'insula. Il donne deux ou trois branches qui se terminent dans le cortex. Le segment M3 ou operculaire est situé entre l'insula et le cortex. Il est parfois regroupé avec le segment M2 sous le nom de segment sylvien. Le segment M4 ou cortical va de la partie externe du sillon latéral au cortex. Ce segment terminal irrigue le cortex. Le flux de l’ACM est estimé à 70 % de la circulation hémisphérique homolatérale.
L’os temporal, encore appelé fenêtre temporale, est une zone privilégiée de passage du signal Doppler pour l’ACM. À ce niveau, cette artère est particulièrement accessible sur une grande profondeur avec un angle le plus faible possible entre la sonde et l’artère. L’ACM est donc l’artère la plus souvent étudiée.
Les artères issues du tronc basilaire et des artères carotides internes constituent le cercle artériel de la base du cerveau. Celui-ci est représenté, en arrière, par les artères cérébrales postérieures, latéralement, par les artères communicantes postérieures reliant les artères carotides internes aux artères cérébrales postérieures et, en avant, par les artères cérébrales antérieures. Ces dernières sont unies entre elles par une courte anastomose transversale, appelée artère communicante antérieure.
Ce cercle artériel est aussi appelé polygone de Willis. Il est situé, dans l’espace sous-arachnoïdien, dans deux loges : l’une, antérieure ou lac opto-chiasmatique, où se trouvent les artères communicantes postérieures ; l’autre, postérieure ou lac basilaire avec les artères cérébrales postérieures. Le polygone artériel encercle la selle turcique ; il est en rapport avec les insertions de la
dure-mère sur les apophyses clinoïdes antérieures et postérieures ; il encadre le losange opto-pédonculaire avec les tubercules mamillaires, le tuber et le chiasma optique.
RAPPEL
I/ METABOLISME CEREBRAL
Le poids d’un cerveau adulte est compris entre 1400 et 1600g, c'est-à-dire environ 2% du poids du corps, mais consomme 20% de l’oxygène de l’organisme (CMRO2 3à5ml/100g/min). En l’absence de jeûne prolongé, le glucose est la seule source d’énergie du cerveau. Ceci nécessite un débit sanguin de 750 ml/min environ, soit 15% du débit cardiaque. Le cerveau n’a pratiquement pas de réserve énergétique bien que l’extraction cérébrale moyenne en oxygène soit seulement de 25à30%. Cette extraction est bien plus marquée au niveau du cortex.
II. DEBIT SANGUIN CEREBRAL A/ débit sanguin cérébral normal :
Le débit sanguin cérébral (DSC) normal est d’environ 50ml / 100g/min (tableau 1). Chaque carotide contribue pour 40% du DSC et le tronc basilaire pour 20%.
B/ variation physiologique du DSC, Autorégulation du débit sanguin cérébral :
1/ L’âge :
Chez l’adulte, le DSC diminue avec l’âge d’environ 3ml/min/an à partir de 60ans. Mais lorsque le DSC est ramené au poids du cerveau, le DSC est constant, ce qui montre que le débit reste adapté au métabolisme cellulaire. Chez les sujets âgés, des variations considérables du DSC peuvent exister en fonction de l’existence d’une artériopathie touchant les vaisseaux cérébraux. Chez l’enfant, le DSC atteint une valeur maximale vers l’âge de 10ans. Le doppler
transcrânien (DTC) a permis de montrer qu’entre la naissance et la troisième semaine de vie, le DSC augmente rapidement. Par la suite, l’augmentation est beaucoup plus lente, puis le DSC décroît à partir de l’adolescence.
2/ Pression artérielle moyenne
La stabilité du DSC (50ml/100g/min) pour un intervalle important de valeurs de pression artérielle est la caractéristique la plus connue du DSC, et correspond à l’autorégulation du DSC. On considère que le DSC est constant pour des valeurs de pression artérielle moyenne (PAM) comprises entre 50 et 150mmHg, correspondant au plateau d’autorégulation (figure2). Ceci ne tient pas compte de la pression intracrânienne. Lorsqu’elle n’est pas négligeable, la pression à prendre en compte est la pression de perfusion cérébrale (PPC) qui est la différence entre la PAM et la pression intracrânienne (PIC). En dessous du seuil inférieur d’autorégulation, le DSC diminue de manière linéaire avec la PCC. Au-dessus du seuil supérieur d’autorégulation (hypertension artérielle maligne), il existe une vasodilatation cérébrale passive et le DSC augmente. La capacité à maintenir un DSC constant lors des variations de pression artérielle est liée à la vasomotricité des artérioles cérébrales. L’autorégulation dépend donc du tonus artériolaire basal. L’ensemble des facteurs qui agissent sur la vasomotricité cérébrale agit donc sur les capacités d’autorégulation.
Figure 2 : Variations du débit sanguin cérébral en fonction de la pression de perfusion cérébrale
Par exemple, lors d’une hypercapnie sévère la vasodilatation artériolaire est maximale. La capacité d’adaptation aux variations de PAM devient nulle et l’autorégulation est complètement abolie. A l’inverse, en hypocapnie, il existe une vasoconstriction cérébrale qui accroît les possibilités d’adaptation à l’hypotension (vasodilatation) et augmente la largeur du plateau d’autorégulation. L’autorégulation est donc un phénomène à interpréter en fonction des conditions circulatoires et métaboliques cérébrales. Ce n’est pas un phénomène immédiat. Lors d’une diminution brutale de la PAM, le DSC chute et revient à sa valeur antérieure en une vingtaine de secondes. La rapidité du retour du DSC à sa valeur antérieure est explorée dans les tests d’autorégulation dynamique. En pratique clinique, la manière la plus simple d’évaluer l’autorégulation statique, c’est-à-dire entre deux états d’équilibre pour la pression artérielle, est d’utiliser le doppler transcrânien. Cette technique mesure la vitesse du flux sanguin dans les artères cérébrales. La vitesse est proportionnelle au DSC et inversement proportionnelle au diamètre artériel.
3/ l’hématocrite :
L’hémodilution augmente le DSC. L’augmentation est d’environ de 2% pour une diminution de l’hématocrite, de 1% entre 40% et 30% d’hématocrite. Cette augmentation du DSC vise à maintenir un transport en oxygène cérébral constant. Elle est la conséquence de deux facteurs : d’une part la diminution de la viscosité sanguine, d’autre part la diminution du contenu artériel en oxygène.
La vasodilatation artériolaire lors de l’hémodilution est liée à la valeur de l’hématocrite, à la viscosité sanguine, au contenu artériel en oxygène, à la taille du vaisseau et au métabolisme énergétique local. En dessous de 20% d’hématocrite, les capacités d’adaptation du DSC à la diminution du contenu artériel en oxygène sont dépassées. Le DSC varie alors dans le même sens que la viscosité sanguine.
4/ La température :
Le métabolisme énergétique et le DSC diminuent de manière proportionnelle à la diminution de la température. La CMRO2 diminue d’environ 7% pour une diminution de 1°C de la température cérébrale, mais la relation CMRO2/température n’est pas linéaire.
La manière dont la pression partielle en CO2(PaCO2) est calculée en hypothermie (corrigée ou non) joue un rôle majeur sur le DSC. Le CO2 étant plus soluble dans le sang en hypothermie, la PaCO2 diminue avec la température. Les gaz du sang étant toujours mesurés à 37°C, il faut corriger la valeur de PaCO2 pour avoir la valeur réelle à la température du patient.
5/ L’hypoxie :
Dans la limite physiologique, le contenu artériel en oxygène n’a aucune influence sur le DSC (figure 1). Cependant, l’hypoxémie est un puissant stimulant de la vasodilatation artériolaire cérébrale. En situation d’hypoxie, l’augmentation du DSC vise à rétablir un apport normal en oxygène au tissu cérébral.
6/ Pression partielle en CO2 (PaCO2) :
Le facteur physiologique le plus important de variation du DSC est la PaCO2. Il existe une relation linéaire entre la PaCO2 et le DSC pour des valeurs comprises entre 20 et80 mmHg (figure1). Chez le sujet sain, le DSC varie de 3% à5% par mmHg de PaCO2. Le DSC diminue de moitié lorsque la PaCO2 diminue de 40à80 mmHg. La réponse à l’hypocapnie dépend de l’état vasculaire basal. Elle est amplifiée lorsqu’il existe une vasodilatation artériolaire. Il n’y a pas de modification de la CMRO2 lors des variations de la PaCO2 dans les limites physiologiques. Les variations de volume sanguin cérébral sont plus faibles que celles du DSC en hypocapnie, comprises entre 0,3% et 0,5% par mmHg, ce qui explique que le traitement d’une hypertension intracrânienne par l’hyperventilation comporte un risque élevé d’ischémie cérébrale.
Figure 3 : Variations du débit sanguin cérébral en fonction des pressions d’02 et de CO2 dans le sang artériel
7/ Débit cardiaque :
Au cours de l’insuffisance cardiaque sévère, le DSC est légèrement diminué. A l’inverse, dans d’autres situations cliniques comme le réveil de l’anesthésie ou chez les traumatisés crâniens, il n’existe pas de relation entre le DSC et le débit cardiaque, que l’autorégulation soit préservée ou altérée.
III/ COUPLAGE DEBIT-METABOLISME
Les réserves énergétiques du cerveau ne permettent que 3 minutes de fonctionnement au maximum en l’absence de débit, la circulation cérébrale doit être ajustée précisément au métabolisme cérébral. L’extraction cérébrale en oxygène est basse mais il existe des variations considérables de débit et de métabolisme cérébral d’une zone à l’autre du cerveau. Le débit sanguin s’adapte donc à la demande métabolique locale assurant l’extraction en oxygène uniforme dans l’ensemble des hémisphères cérébraux. Lors de taches cognitives, les variations locales du DSC ne dépassent pas 5%. Pour qu’une souffrance
ischémique liée à une insuffisance du débit sanguin cérébral apparaisse, celui-ci doit diminuer de plus de 40%, soit en dessous de 22ml/100g/min. L’excès d’oxygène présent à l’état basal pour le cerveau apparait encore plus significatif lors de l’activation d’une zone cérébrale. Alors que l’utilisation du glucose paraît être proportionnelle à l’augmentation du DSC lors de l’activation cérébrale, la CMRO2 augmente beaucoup moins que le DSC. L’augmentation de l’apport en oxygène dans la zone d’activation cérébrale ne serait donc qu’une conséquence et non la cause de l’augmentation du DSC.
Dans le modèle proposé par Zonta et al. , l’élément responsable du couplage débit/ métabolisme est le glutamate. Lors d’une activité synaptique intense, le glutamate libéré de la terminaison axonale diffuse dans les membranes astrocytaires proches de la fente synaptique et active les récepteurs métabotropiques au glutamate. Ceci provoque la propagation d’un signal calcique qui diffuse à l’extrémité astrocytaire en contact avec les artérioles. L’augmentation du calcium intracellulaire provoque la libération d’un agent vasodilatateur, responsable de l’augmentation du flux sanguin qui serait une prostaglandine. L’astrocyte est donc au centre du métabolisme cérébral, en fournissant au neurone une énergie de manière rapide et en adaptant le débit à l’activité métabolique neuronale.
Tableau1 : valeurs normales des principaux paramètres physiologiques
Paramètre Valeurs normales
DSC 50ml/100g/min CMRO2 3-5ml/100g/min CMRglucose 31µmol/100g/min Réactivité CO2 3-5%/mmHg PIC <15mmhg Volume LCR 140ml
CMRO2 : consommation en oxygène cérébrale ; CMRglucose : consommation en glucose cérébral ; réactivité CO2 : pourcentage de variation du DSC par mmHg de PaCO2 ; PIC : pression intracrânienne ; LCR : liquide céphalorachidien.
IMAGERIE
CONVENTIONNELLE DES
LESIONS CEREBRALES POST
Le scanner est une méthode de diagnostic radiologique basé sur la mesure du coefficient d'atténuation du faisceau de rayons X au cours de la traversée d'un segment du corps. Le coefficient d’atténuation est exprimé en unités Hounsfield (HU)sur une échelle. Par convention, le coefficient d’atténuation de l’eau est 0 UH et celui de l’air -1000 UH. Le coefficient d’atténuation des composants physiologiques du contenu de la boite crânien est compris entre 12 UH (liquide céphalorachidien) et 60 UH (sang) pour une valeur moyenne de 33,5 UH chez le sujet sain.
L'image de la coupe d'un objet irradié par un faisceau fin de rayons X, est reconstituée à partir d'un grand nombre de mesures du coefficient d'atténuation, effectuées selon diverses incidences. On recueille ainsi toutes les données, qui proviennent des volumes élémentaires de matière, grâce aux détecteurs. A l'aide d'un calculateur, on attribue aux surfaces élémentaires de l'image reconstruite à partir des données projetées sur une matrice de reconstruction, une tonalité plus ou moins importante en fonction des coefficients d’atténuation. Il est possible de réaliser des reconstructions tridimensionnelles, par exemple pour étudier les déplacements dans les fractures du massif facial ou pour étudier les vaisseaux (angioscanner).
Le scanner cérébral représente l’examen de choix à réaliser en première intention après un traumatisme crânien et doit systématiquement être effectué en urgence en cas de score de Glasgow inférieur à 15, de la présence d’une fracture du crâne, de signe clinique évoquant une fracture de la base du crâne, d’une crise convulsive, de signe neurologique de localisation, ou de céphalées persistantes [6]. La grande disponibilité de cette technique, la rapidité de son
acquisition, sa reproductibilité et son coût modéré expliquent la place conquise par la tomodensitométrie dans l’évaluation du patient traumatisé crânien. Le scanner cérébral permet dans ce contexte la détection d’un hématome intra- ou extra-parenchymateux, d’un œdème cérébral, d’une contusion cérébrale, d’un effet de masse, d’une pneumocéphalie. Chez les patients les plus graves, sa réalisation doit être la plus rapide possible afin d’évaluer la nécessité d’une intervention chirurgicale ou d’un monitorage de la pression intracrânienne. Le développement et la diffusion récente de scanner multicapteurs offre la possibilité d’étendre le champ d’exploration aux structures osseuses fines (recherche d’une fracture du rachis cervical) et vasculaires (angioscanner à la recherche d’une dissection des vaisseaux du cou ou d’une dissection intracrânienne). Par ailleurs, les machines récentes permettent de réaliser la totalité de l’examen en un temps restreint, ce qui améliore la sécurité de patients souvent sous assistance respiratoire et support hémodynamique.
Une attention toute particulière doit être apportée aux explorations scanographiques effectuées précocement dans les trois premières heures suivant un traumatisme crânien grave (TCG); une imagerie normale à ce stade n’exclut pas la survenue ultérieure de lésions cérébrales [7] et en particulier la constitution retardée d’un hématome extradural après un intervalle libre de quelques heures ou l’aggravation majeure d’une contusion cérébrale. Dans le cadre du traumatisme crânien grave, la première question à laquelle l’imagerie précoce doit répondre est celle de l’existence d’une urgence neurochirurgicale. L’équipe médico-chirurgicale doit confronter les conditions de survenue du traumatisme et l’état clinique du patient aux données scanographiques pour prendre sa décision. A la phase aiguë, les urgences neurochirurgicales
traumatiques sont dominées par les hématomes extra- et sous-duraux avec déviations de la ligne médiane et par les embarrures ouvertes ou parfois fermées. Dans un second temps les contusions temporales avec disparition de la citerne et anisocorie homolatérale, les contusions frontales avec hypertension intracrânienne (HTIC) incontrôlable et l’existence d’un œdème massif avec HTIC incontrôlable peuvent exceptionnellement faire l’objet d’un traitement chirurgical sous forme d’un volet large.
I/ LESIONS EXTRAPARENCHYMATEUSES A/ L’hématome extradural
Résulte de la constitution d’une collection sanguine comprise entre la boite crânienne et la dure-mère et est le plus souvent associé à une fracture du crâne en regard. Il est la conséquence d’une lésion d’une artère ou veine méningée, plus rarement de la rupture d’un sinus veineux. Son diagnostic est scanographique et sa présentation est celle d’une lentille biconvexe spontanément hyperdense bien limitée accompagnée d’un effet de masse sur le parenchyme adjacent. En cas de constitution très récente et/ou très rapide, son aspect peut-être celui d’une collection isodense ou hétérogène avec coexistence de plages hypo et hyperdenses traduisant l’existence de sang collecté et de sang encore liquide. La possibilité d’une apparition retardée de cette lésion impose une interprétation prudente des images et le renouvellement de l’examen lorsque la réalisation de celui-ci est précoce.
B/ L’hématome sous-dural :
Il se constitue entre l’arachnoïde et la dure-mère et résulte de lésions de petites veines traversant l’espace sous-arachnoïdien. Cette collection se situe le plus souvent au niveau de la grande convexité de la boite crânienne. L’association d’un hématome sous dural et d’une contusion parenchymateuse sous-jacente est fréquente rendent le pronostic de l’hématome sous-dural aigu plus sévère que celui des hématomes extraduraux à volume égal. Son diagnostic repose sur la réalisation d’un scanner cérébral sans injection de produit de contraste révélant une lame hyperdense homogène étalée en croissant à limite interne concave.
C/ L’hémorragie méningée :
La représentation scanographique de l’hémorragie méningée est celle d’une hyperdensité spontanée homogène des espaces sous-arachnoïdiens. Elle est retrouvée dans environ 35 % des cas de traumatismes crâniens et constitue un facteur indépendant de mauvais pronostic.
D/ L’hémorragie intra-ventriculaire :
Correspond à la présence de sang au sein du système ventriculaire et se traduit par une hyperdensité spontanée au sein du liquide céphalorachidien ventriculaire. Souvent secondaire à l’extension d’une contusion hémorragique, l’hémorragie ventriculaire est rare et expose au risque d’hydrocéphalie par blocage des voies d’écoulement du LCR.
E/ La pneumocéphalie :
Une pneumocéphalie est suspectée devant la présence de bulles d’air hypodenses au sein de la boîte crânienne. Elle traduit l’existence d’une fracture de la base du crâne ou du sinus frontal ou d’une brèche dure-mérienne associée à une fracture ouverte.
F/ La dissection vasculaire :
La présence d’une lésion ischémique systématisée dans un territoire artériel doit faire évoquer l’existence d’une dissection vasculaire. Celle-ci peut intéresser une artère carotide dans sa portion extra ou intracrânienne ou bien une artère vertébrale. Sa mise en évidence repose sur la réalisation d’un angioscanner, d’une angio-IRM ou (exceptionnellement) d’une artériographie. Cette atteinte doit être systématiquement dépistée en cas de fracture de la base du crâne ou de lésion du rachis cervical.
II/ LESIONS INTRAPARENCHYMATEUSES PRIMAIRES : A/ L’œdème cérébral :
L’œdème cérébral post-traumatique se développe dans les heures et jours suivant le traumatisme. Qu’il soit vasogénique ou ischémique (cytotoxique) il expose au risque de déplacement et d’engagement des structures cérébrales, d’hypertension intracrânienne, d’hypoperfusion cérébrale et d’ischémie. Sa présentation scanographique associe une disparition des citernes de la base, une diminution de la taille des ventricules, une disparition des sillons corticaux, et une dédifférenciation cortico-sous-corticale.
B/ Les contusions hémorragiques :
Les contusions hémorragiques représentent des zones de destructions cérébrales résultant du choc direct de l’encéphale contre des zones saillantes de la structure osseuse de la boite crânienne. Pour cette raison, elles se constituent le plus souvent au niveau des lobes frontaux et temporaux. Elles sont souvent associées à des lésions de contrecoup. Les contusions hémorragiques sont constituées d’un noyau central hémorragique, hyperdense, entouré d’une zone de tissu cérébral hypoperfusé à risque ischémique, hypodense. Dans les heures et jours suivant le traumatisme se forme un halo œdémateux péricontusionnel de mécanisme vasogénique et parfois ischémique/cytotoxique. Au sein des contusions, la destruction du parenchyme cérébral s’accompagne d’une augmentation accrue de la perméabilité de la barrière hémato-encéphalique, notamment aux produits de contraste [8, 9]. Dans ces conditions l’utilisation agressive de thérapeutiques osmotiquement actives doit être réfléchie en cas de zones contuses étendues [10]. L’hématome évolue ensuite vers la résorption,
laissant au final une cicatrice nettement plus petite que la lésion initiale, visible sous la forme d’une hypodensité au scanner et d’un hyposignal T2* à l’imagerie par résonance magnétique (IRM). La présentation de ces contusions en imagerie est variable en fonction des patients, du traumatisme et du temps. La figure 4 illustre les modifications d’aspect et de taille des contusions hémorragiques à la phase initiale du traumatisme.
Figure 4 : Evolution temporelle d’une contusion hémorragique entre h2 (A) et h16 (B) post-traumatique
C/ Lésions axonales diffuses :
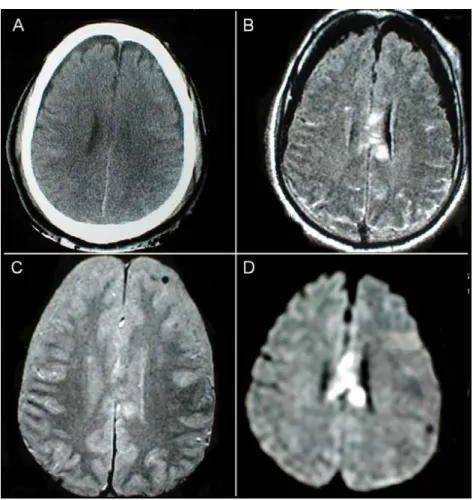
Les forces d’accélération-décélération et de rotation appliquées à l’encéphale lors du traumatisme se traduisent par des lésions de cisaillements des fibres nerveuses. Ces lésions de la substance blanches appelées lésions axonales diffuses sont localisées aux zones de jonctions de tissus de densités ou de masses différentes, elles peuvent être hémorragiques ou ischémiques. Elles siègent préférentiellement à la jonction entre la substance grise et substance blanche des lobes frontaux et temporaux, au niveau du corps calleux, des ganglions de la base et du mésencéphale. A la phase aiguë, la tomodensitométrie (TDM) peut révéler la présence de lésions axonales diffuses sous la forme de petites pétéchies punctiformes. Néanmoins, le scanner cérébral est très peu sensible, et sous-estime la quantité et la taille de ces lésions. L’IRM est le meilleur examen pour détecter les lésions axonales diffuses et doit être réalisée chez tous les patients présentant peu de lésions au scanner cérébral contrastant avec un coma profond. Les lésions axonales diffuses de type hémorragiques, non détectées par le scanner cérébral, sont visibles sur les séquences en écho de gradient en pondération T2*. Elles apparaissent sous la forme d’un hyposignal et traduisent la présence de désoxyhémoglobine paramagnétique (figure 5). Le nombre de lésions en T2* et leurs localisations seraient corrélés à la gravité clinique du patient et à son pronostic à moyen terme [11].
Figure 5 : Lésions axonales diffuses hémorragiques du corps calleux visibles sous la forme d’hyposignaux en séquences pondérées T2
L’IRM permet également de détecter des lésions axonales diffuses non hémorragiques [12]. Ces lésions peuvent expliquer les troubles de la conscience observés après traumatisme crânien malgré un aspect normal au scanner cérébral. Typiquement, il s’agit de lésions en hypersignal FLAIR, s’accompagnant d’hypersignaux en diffusion (diminution du coefficient de diffusion) sans anomalies en T2* [13]. Ces lésions sont le plus souvent situées au niveau du corps calleux, des noyaux gris centraux, du mésencéphale et de la protubérance (figure 6). L’IRM spectroscopique peut aider à la détection des lésions axonales diffuses. Les données de travaux expérimentaux [14] et cliniques [15, 16, 17] ont mis en évidence une diminution de l’acétyl-amino succinate (NAA) secondaire à une souffrance neuronale et une augmentation de