Le
Séminaire
International
sur
L'Hydrogéologie
et
I'Environnement
5 - 7
Novembre
2013,Ouârglâ (Algérie)
Elimination
de
la
Tyrosine par Adsorption sur Différents
Matériaux
et
Effet
de
la
Minéralisation
des
Eaux
Bouchemal
Fattoum(r),Achour
Samia(2) (rr (2)Laboratoire de Recherche en Hydraulique Soutenaine et de Surlace-LARHYSS Faculté des Sciences
et
Sciences de l'Ingénieur.Univelsité de
Biska,
BP
145 RP, 07000,Biska,
Algérie E-mail:
bouchemalhydro@yahoo.fr
;
sâmiâ.âchour@Larhyss.net
AbstruclThe objective
of
this
work
is
to
studythe
possibilitiesof
tyrosin retention onto various adsorbents (granular activated carbon and powdered activated carbon, âctivated bentonite, activated alumina,). The literature review has presented the mâin characteristicsof
natural organic mâtter and
more particularly amino acids of which tyrosiir. The most current techniques of depollution were described while insisting on the process ofadsorption on va.ious materials.During the experimentâl study, the tests carried out on static system and allowed to follow the tyrosin kinetics adsorption on various materials tested on distilled wâter
or
minerâlized waters. kinetics led to various removal efliciencies oftyrosin.I.
INTRoDUCTIoNLa
coloration intense
et
la
formation
de
composés orga.nohalogénéspotentiellement toxiques
sont
des problèmesqui
dégradentla
qualité
des eaux
potables.L'origine
de
ces problèmes est essentiellementliée
à
laprésence
de
la
matière organique
laquelle
découled'origines
diverses
dans les eaux
de
surface
pour
yconstituer
un
milieu très
hétérogène
(Achou
etMoussaoui,
1993).
Parmi
les
cômposés
organiquesd'origine
naturelle, les acides aminéslibres et
combinésconstituent
une
source
de
substrat carboné
pour
les biomasseslibres
et
fixées présentes dans les réseaux dedistribution (Hueiki
etal.,
1996).En particulier, la tyrosine est un acide aminé aromatique,
polaire. Elle
paxticipeà la
synthèse des catécholamines.Elle
peut être
synthétisée, dansle
corps,à partù
de
la phénylalanine(Biochimie, 2007).
Plusieurs procédés de îraitement ont eu pour butl'élimination
de la matièreThe influence
of
reactionâl parameters such as thÊ mass of adsorbent, for a constant mass ofadsorbeît, theThe best results were obtained for actiÿated carbon, Removal is improved when the medium of
dilution
is mineralized. An increasein
removal
is
also not€d when
the
massesof
adsorbents increase, depending horryever on the limitationsof
these.
Key
words-Tyrosin, removal efficiencies , retention, adsorbents, kinetics.
organique
dont
l'adsorption.
Elle
est
un
traitementparticulièrement
efficace
pour
enleyer
la
matière organique naturelle.L'utilisation
de
l'adsorption
sur
charbon
actif
pourl'élimination de micro-polluants
dans l'eau destinéeà
laconsommation
est
de
plus en plus
fréquente,
et
lalittératue
est
abondante
sur
la
mise
en
æuwe,
lesparamèfes
de
fonctionnement
ou
les
mécanismesd'interactions soluté-matériau
dans
le
cas
d'une alimentation parfaitement connue.D'autres matériaux poreux tels que les argiles sont aussi utilisés comme solulions allemalives.
L'objectif
de notre étude est donc de testerI'efficacité
de
rétention de la tyrosine sur quelques matédaux poreux (charbonactif,
bentonite activée, alumine activée). Nous tenterons,en
comparantleurs
différentes efficacités, de mettreen
évidencel'intérêt
que présente chacunde
cesLe
Sêminaire
International
sur
adsorbants. Nos essais expérimentaux ont eu
pour
but desuiwe
les cinétiquesd'adsorption
de la
ryrosineen
eaudistillée et en eaux minéralisées.
N.
MATERIELS
ETMETHODES
II.l.
Préparation des solutionsLa
solution mère de la 6.rosine est préparée àpartir
de 100 mg, quel'on
dissout dansun
litre
d'eaudistillée
ou eaux minéralisées. L'eau distillée aune
conductivitéde
2à 5
(ps.cm-') etun
pH
comprisente
4.66 et
6.36et
les eaux minéralisées présentent des conductivités et des pH différents(7,48
1pH17,17
et 439<
conductivité<
1990 ps.cm-').fI.2.
Dosage de la tyrosineLes
concentrations résiduelles
en
tyrosine
sont déterminéesà
partir
de
l'absorbarce
en U.V,
à
une iongueur d'onde ), = 270 nm,sw
un spectrophotomète de q,pe(JENWAY
6405UV/^/IS).
Les courbes d'étalonnage Absorbance(A)
: f
(concentration
en
tyrosine)
sont établies avant chaque série d'essais.II.3.
Caractéristiques des adsorbants utiliséesLes adsorbants testés sont
le
charbonactif
en grainsDARCO,
charbonactif
en poudre mésoporeux, l'alumineactivée faiblement acide
et la
bentonite activée
à
untemps
d'activation
d'une heure
et
un
taux
massique H?SO&/bentonite = 0,2(Youcefet
Achour, 2004).fI.4.
Description des essais d'adsorptionLes
essais
d'adsorption sont réalisés
en
réacteur statique en adoptant diflerentes conditions opératoires. Les cinétiquesd'élimination de la
t),rosine sur différents matériaux poreux sont réaliséessur
des solutions de 20 (mg.l-r) en tyrosine en eau distillée ou eaux minéralisées et auxquelles nousrajoutons
I
g d'adsorbant.Les
solutionssont
agitées pendant6
heuressur
des agitateurs électromagnétiques puis filtées.
L'Hydrogéologie
et
I'Environnement
5 - 7
Novembre
2013,Ouargla (Algêrie)
Les
doses optimales d'adsorbant correspondentalors
au rendementd'élimination le plus
élevé avecle
rendement défini par R% =((Co
C)/Co) x
100Co : Concentration initiale de la
tyrosine
(mg.l-r).C:
Concentration
résiduelle
de
la
tyrosine
en solution (mg.1-1).III.
RESULTATS
ET DISCUSSION 1II.1. Cinétiques des essais d'adsorptionde la tyrosine en eau distillée
L'évolution
des rendementsd'élimination
de la tyrosineen fonction du
temps
de
contact
est suivie pour
une concentration initiale de tyrosine de 20 (mg.l-r), une masse de I'adsorbant d'un gramme.Les
résultats obtenus(figures
I
et
2)
montrentque
les rendementsd'élimination
de la tyrosine sur charbonactif
(en grains
et
en
poudre)
augmententavec
le
temps d'agitation des solutions aqueuses et atteignent desvaleus
maximales del'ordre
de 66 à 81 %.Le
rendementmaximal d'élimination
de la
Otosine
surl'alumine
activée en eaudistillée
est seulement de26
%(figure
3) et
pourrait
s'expliquer
par
la
structurede
la tyrosine.Concemant
la
rétention
de la
6.rosine
sul la
bentonite activée, elle ne dépasse pas un rendement del8
% (figure4)
après une agitationd'une
heure.L'affinité
serait ainsipeu
importante
entre
la
structure
de
la
ÿosine
et
la surface de cette argile, même activée.Au
w
de
ces
résultats,
nous
pouvons
égalementconstater
que
les
cinétiques
présentent
deux
étapesdistinctes.
La
première
étapeest
rapide tandis
que
la deuxième estlente-Au
coursde la
première étape,il
y
a
une augmentation rapidejusqu'à environ
I
à 2 heures pourle
charbonactif
en grain,
seulementaprès
3
minutes
en utilisant
le charbonactif
en
poudrec'est l'étape
qui
correspond au transfert dela
masse exteme.Le
Séminaire
International
sur
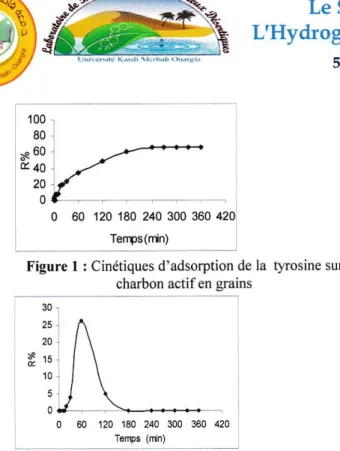
Figure
I
: Cinétiques d'adsorption dela
tyrosine sur charbonactifen
grains30 25 20
§,u
10 5 0 120 180 240 300 Tenps (mrn)Figure
3 : Cinétiques d'adsorption dela
6'rosine sur l'alumine activëeLa
forte adsor?tion dela
ryrosine surle
charbonactif
en poudre est due probablement à la dimension des pores dufait
que
le
charbon
actif en
poudre est
mésoporeux(Kifuani Kia
Mayeko et al., 2004).Cecirejoint
les travauxde Le
Cloirec (1985)
qui
montrent que les
composées aromatiques s'adsorbent bien sw charbon actif.1I.2.
Cinétiques des essais d'adsorption de la q.Tosine eneaux minéralisées
Les
résultats obtenus montrent
que les
rendements d'élimination de latyrosine
sur le charbonactif
engains
augmentent aufur et
à
mest]Ieque
le
temps d'agitation augmente,le
temps
d'équilibre atteint
5heureset
30 minutes, sur l'eau du Chetma, donne un rendement de 83,72 yo.Pü confe,
le tempsd'équilibre
est de 4 heures avec un rendement de 88,33 ÿo sur l'eaud'Ifri.
30 25 20
Ë,s
10 5 0L'Hydrogéologie
et
I'Environnement
5 - 7
Novembre
2013,Ouargla (Algérie)
60
120 180 240 300 360Tenps(nin)
Figure
2 : Cinéliques d'adsorption de la tyrosine sur charbon actif en poudre12A 1AO 240 300 360 420
Figure
4:
Cinétiques d'adsorption de la tyrosine sue la bentonite activéeLes rendements
d'élimination
de laÿosine
sur le charbonactif
en poudre sont quasiment identiquespour
les deuxmilieux de dilution.
Ils
sont
pratiquement constants aucours
de Ia
majorité
de
l'essai,
meilleurs
qu'avec
le charbonactifen
grains car proches de 1000/0.De
mêmequ'en
eau
distillée
la
forte
adsorptionde
latyrosine sur
le
charbon
actif
en
poudre
est
observée lorsque le milieu est minéralisé.Nous
avonspu
également observerque
le
processus d'adsorption de la ô.Tosine sur le charbonactif
se déroule en deux étapes distinctes aussi bien pourle
charbonactif
en
grainsqu'en
poudre, dela
même manière qu'en eau distillée.Le
rendementd'élimination
de la tyrosine sur l'alumine activée, estmeilleur
sur I'eau de Chetma 61,9%
au boutde
15minutes
que sur l'eaud'llli
11,20 %o au bout de 3heures.
0
60
120'180 240 300 360 100 80s40
20 0L'Hydrogéologie
et
I'Environnement
Le
Séminaire
International
sur
La capacité adsorbarte de la bentonite activée sur I'eau de Chetma
estde65,ll
yo aqès 2 heures d'agitation. Par confie. l'eaud'Ifri
dome
un rendement de 25,89%
dans lesl5
premières minutes.Nous
constatons
une
certaine amélioration
des rendements sur I'eaud'lfri,
mais une grande amélioration est observéepour l'eau
de Chetma en comparaison avec les rendements en eau distillée.Cette amélioration
pounait
être due à l'augmentation de la teneur en sels minétaux dans l'eau et au pH tamponné des eaux souterraines utilisées.Ceci avait déjà
étémis
en
évidencelors de
l'étude
de l'adsorption de substances humiques sur bentonite en eauxde
minémlisation
variable (Seghairi
et
al
,2004).
Enparticulier, les ions constitutifs
de la
dureté(calcium
etmagnésium)
pourraient
avoir
un rôle
bénéfique
et promoteur de la rétention de divers composés organiques sur les matériaux testés.Par contre, d'autres ions minéraux tels que les sulfates ou les phosphates pounaient avoir un rôle inhibiteur au cours de l'adsorption.
IV.
CONCLUSIONLes travaux réalisés dans cette étude on eu pour
objectif
l'application du
procédéd'adsorption de
la
tyrosine
sur des matériaux poreux (charbonactif,
bentonite activée etalumine
activée).Nous
avons déterminé
les
cinétiquesd'adsorption
de la
tyrosine
sur les
matériaux précédemment cités.Les
cinétiques
d'adsorption
se
déroulent
sur
deuxétapes,
la
première étape
est
rapide
correspond
au transfertde
la
masse exteme.Tandis que
la
deuxième étape est plus lente.Les essais réalisés nous ont permis de conclure que les pourcentages
d'élimination
dela
tyrosine sont importantslorsqu'il s'agit
du charbonactif.
Les rendements obtenusen utilisant
le
charbon
actif en
poudre sont
nettement5 - 7
Novembre
2013,Ouargla (Algérie)
supérieurs
à
ceux
obtenuspar
charbonactif en
grains. Ce matériaupourait
âussi êtreutilisé
cornrne adjuvant au lieu de mettre unlit
filtrant
sur charbonactifen $ains.
En eaux minéralisées. les rendements
difËrent
selon lemilieu
dedilution. En
eaud'Ilïi
oir la
minéralisation estfaible,
les
rendementsd'élimination
de la
tyrosine
sont assezfaibles
et
ne
dépassent pas 26Yoen utilisant
labentonite activée
ou
l'alumine
activée.Par contre,
cesrendements sont
plus
élevésen
eaude
Chetmadont
la minéralisation est importante.REFERENCES
.
ACHOUR, S., MOUSSAOUI, K. (1993), Etret de Ia chloration sur quelques types d'eaux en Algérie. Tribune de l'Eau. 564, 3l_34..
BIOCHIMIE. (2007),.Cours de Biochimie, polycopié, chapitre 11,lJniversité de Jussieu- Paris.
.
HUREÏKr. 1., GAUTHIER, C., PREVOST, M. (1996), Etude de l'évolution des acides aminés totaux dans deux filières de raitementd'eau potable. Rev.Sci.Eau. 9,
l.
297-318..
KIFUANI. K,M,, MUKANA, W,M,, NOKI, V,, MUSIBONO. E,,NZUZI, P.. PUNGI, P., et KUNYIMA, B. (2004), Adsorption de bleu de méthylène en solution âqueuse sur charbon actif obtenu a
partir des sciures végétales
,
préparation et caractérisation du charbon actif. Rev .Sci.20,l 12,215-224..
LE CLOIREC. P. (1985), Etude des interactions soluté-
charbonactif. Modélisation
de
réactions biotiques et abiotiques. thèse de docteur Es- Sciences Physiques, ENSCR, Llniversité de Rennes, France..
SEGHAIRI,N., KOUSSA,M,, ACHOUR,S,(2004),EffCt
dEI'activation chimique de la bentonite sur l'adsorption de substances
humiques en eaux de minérâlisation variable- Laihyss Joumal, 3,
87-98.
,
YOUCEF.L.. ACHOUR. S.(2004). Etude de l'éliminatjon desfluorures des eaux de boisson par adsorption sur bentonite. Larhyss Joumal,3, 129-142.