Développement et caractérisation de films
biodégradables à base d’acide polylactique et de
chitosane
Mémoire
Fatma Ben Dhieb
Maîtrise en génie chimique
Maître ès sciences (M.Sc.)
Québec, Canada
iii
Résumé
Une des meilleures alternatives actuellement pour réduire les déchets d’emballage est le recours aux polymères biodégradables.
C’est dans cette optique qu’on a essayé dans le cadre de ce travail d’élaborer un film d’emballage à base d’acide polylactique (PLA) et de chitosane (CS) vu leurs propriétés complémentaires et l’activité bactériostatique du CS.
Le PLA et le CS ont été compatibilisés avec le polycaprolactone et plastifiés avec le Polyéthylène glycol, selon deux procédés, le mélange en solution (casting) et par voie fondue au mélangeur interne.
La caractérisation des films par spectroscopie IR-TF, DSC et MEB, a révélé que les films obtenus par la méthode casting avait de meilleures propriétés. En effet, l’ajout du PCL et du PEG a pu améliorer les propriétés mécaniques et la perméabilité à la vapeur d’eau et à l’oxygène des films du CS/PLA.
v
Abstract
One of the best alternatives to reduce current packaging waste is the use of biodegradable polymers. It is in this context that we have tried, in this work, to develop a packaging film based on polylactic acid (PLA) and chitosane (CS) given their complementary properties and the bacteriostatic activity of CS. PLA and CS were compatiblized with polycaprolactone and plasticized with polyethylene glycol by two methods, the solution mixture (casting) and by hot melting in the internal mixer. Characterization of films by FTIR spectroscopy, DSC and SEM showed that the films obtained by casting method exhibited better properties. Indeed, the addition of PCL and PEG improved the mechanical properties and the water vapor and oxygen permeability of the CS/PLA films.
vii
Table des matières
Résumé………iii
Abstract……….v
Table des matières ... vii
Liste des tableaux ... xi
Liste des figures ... xiii
Liste des abréviations ... xv
Introduction ... 1
Chapitre I – Étude bibliographique ... 3
I- Polymères biodégradables ... 4
1) Définition ... 4
2) Classification ... 4
II- L’acide polylactique (PLA) ... 6
1) Production ... 6 2) Propriétés du PLA ... 8 3) Caractéristiques et applications ... 11 III- Le chitosane ... 13 1) Production ... 13 2) Caractéristiques du chitosane ... 15 3) Propriétés ... 17 4) Applications ... 18
5) Application dans l’emballage alimentaire ... 21
IV- Le mélange PLA /CS ... 23
1) Généralités sur les mélanges ... 23
2) Compatibilisation ... 27
3) Plastification ... 28
4) Méthodes d`élaboration des mélanges ... 30
V- Objectif du projet ... 32
Chapitre II- Matériels et méthodes ... 33
I- Matières premières ... 34
1) Matériaux ... 34
viii
II- Méthodes expérimentales ... 34
1) Synthèse des films par ‘casting’ ... 34
2) Synthèse des films au mélangeur interne ... 35
3) Méthodes de caractérisation ... 36
3.1) Caractérisation de la perméabilité ... 36
3.2) Évaluation des propriétés mécaniques ... 38
3.3) Absorption d’humidité ... 38
3.4) Teneur en eau ... 39
4) Caractérisation des films ... 39
4.1) Caractérisation des films par spectroscopie IR-TF ... 39
4.2) Analyse thermique différentielle (DSC) ... 40
4.3) Microscopie électronique à balayage (MEB) ... 42
Chapitre III- Résultats et discussion ... 43
Partie I- Étude des films synthétisés par mélange en solution ... 44
I- Caractérisation ... 44
1) Analyse par calorimétrie différentielle à balayage (DSC) ... 44
2) Analyse par spectroscopie IR-TF ... 47
3) Analyse par microscopie électronique à balayage (MEB) ... 49
II- Évaluation de la perméabilité des films ... 50
1) Perméabilité à l’oxygène ... 51
2) Perméabilité à la vapeur d’eau ... 52
III- Propriétés mécaniques ... 54
1) Effet du compatibilisant sur les propriétés mécaniques ... 54
2) Effet du plastifiant sur les propriétés mécaniques ... 57
IV- Absorption d’humidité ... 59
Partie II- Étude du mélange synthétisé par voie fondue ... 61
I- Caractérisation ... 61
1) Caractérisation par spectroscopie IR-TF ... 61
2) Analyse par microscopie électronique à balayage (MEB) ... 64
3) Analyse thermique différentielle (DSC) ... 64
II- Propriétés mécaniques ... 68
III- Perméabilité ... 69
ix
Comparaison des deux méthodes de synthèse... 75
Conclusion et perspectives ... 78
Références ... 79
xi
Liste des tableaux
Tableau 3.1 Propriétés thermiques des films du mélange CS/PLA/PCL/PEG
Tableau 3.2 Principales bandes dans le spectre IR-TF du mélange PLA/PCL/PEG/CS Tableau 3.3 Composition des films pour les essais de perméabilité
Tableau 3.4 Propriétés des plastiques les plus utilisés en emballage Tableau 3.5 Les propriétés mécaniques des mélanges non plastifiés Tableau 3.6 Contrainte et élongation à la rupture des films plastifiés Tableau 3.7 Compositions des mélanges étudiés
xiii
Liste des figures
Chapitre -1
Figure1.1 Les monomères optiques de l’acide lactique Figure1.2 Étapes de la synthèse du PLA
Figure1.3 Structure chimique de la chitine (a) et du chitosane (b).
Chapitre-2
Figure2.1 Schéma illustrant le principe de mesure de la perméabilité des films à l’oxygène et la vapeur d’eau
Chapitre-3
Figure3.1 Thermogrammes du premier chauffage du meilleur film obtenu et des polymères utilisés
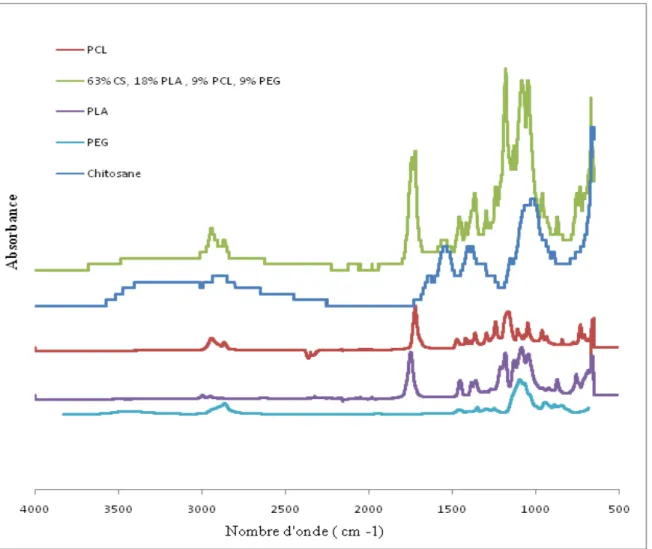
Figure3.2 Spectres IR-TF du film avec 63% de CS, 18% PLA, 9% PCL et 9% PEG (1) et des polymères purs le composant
Figure3.3 Micrographes MEB des films du mélange CS/PCL/PLA/PEG Figure3.4 Perméabilité à l’oxygène en fonction du PLA
Figure 3.5 Perméabilité à l’oxygène en fonction du PCL Figure3.6 Perméabilité à la vapeur d’eau en fonction du % de PCL Figure3.7 Perméabilité à la vapeur d’eau en fonction du % de PLA
Figure3.8 Élongation à la rupture des films en fonctions du pourcentage du chitosane dans le mélange pour les films avec et sans PCL Figure3.9 Contrainte à la rupture des films en fonction du pourcentage du
chitosane dans le mélange pour les films avec et sans PCL Figure3.10 Contrainte à la rupture des films en fonction du pourcentage de
chitosane dans le mélange.
Figure3.11 Élongation à la rupture des films en fonction du pourcentage de chitosane dans le mélange
Figure3.12 Absorption de l’humidité en fonction du pourcentage du chitosane Figure3.13 Spectres IR-TF des films de PLA/PCL/CS avec différents
pourcentages de PEG
Figure3.14 Spectres IR-TF du film de PLA/CS/PCL et des polymères purs Figure3.15 Micrographies MEB de la coupe transversale des films de
PLA/CS/PCL/PEG
Figure3.16 Thermogrammes d’un mélange PLA/ PCL/CS élaboré au mélangeur interne et des polymères purs
Figure3.17 Thermogrammes d’un mélange plastifié PLA/PCL/CS/PEG élaboré au mélangeur interne et des polymères purs
xiv
Figure3.18 Évolution de la cristallinité du PCL en fonction de son pourcentage dans le mélange
Figure3.19 Perméabilité à la vapeur d’eau en fonction du % de PCL pour les films synthétisés par casting et par voie fondue
Figure3.20 Perméabilité à l’oxygène en fonction du % du PCL pour les films synthétisés par casting et par voie fondue
Figure3.21 Cinétique de l’absorption de l’humidité des différents films
Figure3.22 Absorption de l’humidité en fonction du pourcentage du PCL dans le mélange de PLA/CS/PCL
Figure3.23 Absorption de l’humidité en fonction du pourcentage du PEG dans le mélange PLA/PCL/PEG/CS
Figure3.24 Perméabilité à la vapeur d’eau en fonction du % de PCL pour les films synthétisés par casting et par voie fondue. Figure3.25 Perméabilité à l’oxygène en fonction du % du PCL pour les films
xv
Liste des abréviations
AA Acide acétique
DA Degré d’acétylation
DD Degré de déacétylation
DMTA Analyse thermique dynamique DSC Calorimétrie différentielle
E Module d’Young
CHL Chloroforme
CS Chitosane
HCl Acide chlorhydrique
HDPE Polyéthylène de haute densité HLB Balance hydrophile-lipophile
HR Humidité relative
IR-TF Infra Rouge à Transformée de Fourier LDPE Polyéthylène de basse densité
MDI 4,4'-méthylène-bis-(phénylisocyanate) MEB Microscopie électronique à balayage OPC Coefficient de perméabilité de l’oxygène OTR Vitesse de transmission de l’oxygène o-LA Oligomère d’acide lactique
PA Polyamide
PCL Poly (ε-caprolactone) PDLA Acide poly (DL-lactide) PEG Polyéthylène glycol
PEHD Polyéthylène de Haute Densité PET Polyéthylène Téréphtalate PHB Poly β-hydroxy Butyrate PHV Poly Hydroxy Valérate PLA Acide polylactique PLLA Acide poly (L-lactique)
PP Polypropylène
PS Polystyrène
PVA Alcool polyvinylique PVC Polychlorure de vinyle
ROP Polymérisation par ouverture de cycle
TE Teneur en eau
WVPC Coefficient de perméabilité à la vapeur d'eau WVTR Vitesse de transmission de la vapeur d'eau
xvi Unités et symboles φ Fraction volumique ε Allongement à la rupture σ Contrainte à la rupture h Heure j Jour min Minutes s Secondes
Tdeg Température de dégradation thermique
Tf Température de fusion
Tg Température de transition vitreuse
Mw Poids moléculaire
1
Introduction
Avec la demande mondiale croissante en matière plastique qui a dépassé les 250 millions de tonnes en 2012
[1],
le prix alarmant du pétrole et les préoccupations environnementales, les matières plastiques biodégradables se positionnent parmi les meilleures alternatives.Dans le secteur de l’emballage, premier secteur demandeur en plastique [2] [1], l’emballage alimentaire est celui qui présente la croissance la plus élevée [3]. C’est de là que découle notre intérêt pour le développement d’un nouvel emballage alimentaire biodégradable. On a choisi de synthétiser ce dernier à partir des deux polymères, l’acide polylactique (PLA) et le chitosane (CS), vu leur disponibilité, leurs coûts, leur biodégradabilité et surtout leurs propriétés complémentaires.
Le PLA est le polymère le plus largement utilisé. C’est un thermoplastique produit par fermentation à partir de ressources renouvelables. Il peut également être synthétisé soit par polymérisation par condensation d'acide lactique ou par polymérisation par ouverture de cycle du lactide en présence d'un catalyseur [4]. Le chitosane a des propriétés intéressantes, telles que son caractère filmogène, sa non toxicité et ses propriétés antimicrobiennes, capables d'inhiber la croissance d'une large gamme de pathogènes alimentaires [5].
Malgré l’incompatibilité du PLA et du CS, leur mélange est d’un grand intérêt pour les chercheurs vu ses différentes propriétés telles la biodégradabilité, la biocompatibilité, l’activité anti microbienne, les propriétés mécaniques, etc. Les efforts ne cessent d’être déployés pour synthétiser le mélange de PLA et de CS selon différentes techniques, dépendamment de l’application visée. Ce type de mélange a déjà été étudié en utilisant plusieurs procédés tels que le mélange en solution ou casting [6], l’émulsification [7], l’électrofilage [8], la précipitation [9], le greffage [10, 11], ou encore par modification du chitosane pour le rendre plus hydrophobe [12].
2
Leur propriétés sont complémentaires mais ils ne sont pas miscibles et ils manquent tous les deux de ductilité, d’où notre recours à un compatibilisant, le polycaprolactone (PCL) qui a pour rôle d’augmenter l’adhésion des deux polymères. L’ajout d’un plastifiant, le polyéthylène glycol (PEG), aura aussi pour rôle d’améliorer le module d’élongation des films.
Dans une première partie de ce mémoire, on a fait une étude bibliographique sur les polymères biodégradables en général et nos polymères de base en particulier, ainsi que sur les méthodes de synthèses des systèmes PLA/CS.
Dans une deuxième partie, on a exposé le matériel et méthodes utilisés pour réaliser les films de PLA/CS et les caractériser, pour finir avec une partie d’interprétation de nos résultats ainsi qu’une proposition de certaines perspectives.
3
4
I-
Polymères biodégradables
1) DéfinitionSelon American Society for Testing and Material (société américaine pour les essais et les matériaux), un plastique dégradable est conçu pour subir un changement important dans sa structure chimiques sous des conditions environnementales résultant en une perte de certaines propriétés qui peuvent varier telles que mesurées par des essais normalisés appropriés.
Les plastiques peuvent être désignés comme photodégradables (dû à l’action des rayons UV et des radicaux libres), dégradables chimiquement par hydrolyse ou par oxydation et dégradables mécaniquement par cisaillement et coupure des chaînes (par exemple le broyage) [13]. Entre Octobre 1990 et Juin 1992, une confusion quant à la véritable définition de «biodégradable» conduit à des procès concernant la publicité environnementale trompeuse. Ainsi, il est devenu évident à la ASTM et à ISO que des méthodes de test communes et des protocoles pour les plastiques dégradables soient nécessaires [14]. La biodégradation correspond à la destruction d’un produit par des agents biologiques. Étant donné que la biodégradabilité peut s’effectuer n’importe où (sol, eau, milieu de compostage ou de décharge), un consensus s’est dégagé autour de la notion d’impact sur l’environnement. C’est ainsi que la définition suivante a été adoptée: La biodégradation correspond à la défragmentation, par l’action de micro‐organismes, avec perte des propriétés mécaniques ou avec modification chimique. La structure du matériau se simplifie pour finalement se convertir en H20, CO2, CH4 et/ou en une biomasse nouvelle
et éventuellement un résidu non toxique pour l’homme et l’environnement. La biodégradation est donc une dégradation catalysée par des micro‐organismes [15].
2) Classification
Le développement des bioplastiques est encore à son début, il représente approximativement 5 à 10 % du marché du plastique qui est de 200 millions de tonnes par an [16]. Les matières plastiques ou matériaux biodégradables peuvent avoir deux origines: l'industrie pétrochimique ou les ressources renouvelables.
5 2.1) Polymères biodégradables issus de la pétrochimie
Ces polymères peuvent être divisés en quatre sous-groupes :
- Les polyesters aliphatiques, comme l’acide polyglycolique, le polybutylène succinate et le polycaprolactone.
- Les polyesters aromatiques ou mélanges de polyesters aliphatiques et aromatiques, tel que le butylène succinate téréphtalate.
- Les alcools polyvinyliques.
- Les polyoléfines (comme le polyéthylène ou le polypropylène) modifiés avec des agents spécifiques sensibles à la température ou à la lumière.
2.2) Polymères biodégradables issus des ressources renouvelables Ils sont généralement classés en trois sous-groupes :
- Les polymères naturels.
- Les polymères d’origine bactérienne.
- les polymères synthétiques.
2.2.1) Les polymères naturels ou biopolymères
Les biopolymères sont synthétisés par les végétaux, les animaux ou les microorganismes et sont souvent divisés en trois sous-groupes : les polysaccharides, les protéines et les élastomères hydrocarbonés.
- Les polysaccharides : Ils constituent les biopolymères les plus utilisés et les plus répandus. Parmi ces polymères, on cite l’amidon de maïs, la cellulose et le chitosane.
- Les protéines : elles peuvent être extraites des plantes (caféine, gluten de blé) ou des tissus animaux (collagène, gélatine) et produits animaux (caséine).
6
2.2.2) Les polymères d’origine bactérienne
Ces polymères sont synthétisés à l’intérieur des bactéries lors de la fermentation et sont accumulés dans le cytoplasme. La fermentation a souvent comme matière première les sucres et l’amidon et donne des polymères tels le PHV (Poly hydroxy valérate et le PHB (Poly hydroxy butyrate).
2.2.3) Les polymères synthétiques
Les monomères dans ce cas sont obtenus par fermentation bactérienne et sont ensuite polymérisés par polycondensation (par chauffage). L’un des exemples les plus connus de ces polymères est l’acide polylactique (PLA).
II-
L’acide polylactique (PLA)
1) ProductionL’acide polylactique (PLA) est un polyester aliphatique, linéaire et biodégradable, produit à partir d'acide lactique (monomère de base). Ce monomère a deux isomères optiques L et D.
Figure 1.1 : Les monomères optiques de l’acide lactique [17]
L’acide lactique peut être dérivé de la fermentation de différents polysaccharides naturels, principalement le glucose extrait de l’amidon de maïs. Il peut aussi être obtenu par voie pétrochimique. Cependant, la fermentation est plus respectueuse de l'environnement, d’où sa large utilisation depuis les années 1990 [17]. L’acide lactique dérivé de la fermentation existe presque exclusivement sous la forme l (99.5% de l'isomère l et 0.5% de l'isomère d) [18].
7 Il existe deux principales voies pour produire le PLA à partir de l'acide lactique:
- Polymérisation directe par condensation de l'acide lactique :
Elle consiste en l’élimination de l'eau, l'utilisation de solvant sous vide et à température élevée. En plus de cela, elle nécessite des réacteurs relativement grands et conduit à une coloration et une racémisation accrue. Elle ne peut produire que des polymères de bas ou moyen poids moléculaire (Mw∼2–10kDa [19]).
- Polymérisation par ouverture de cycle en utilisant un intermédiaire lactide:
Un prépolymère de faible poids moléculaire est d'abord produit par élimination de l'eau dans des conditions douces et sans utilisation de solvant. Un dimère cyclique intermédiaire, le lactide, est alors produit par dépolymérisation catalytique de ce prépolymère. Le monomère lactide est en outre soumis à une polymérisation par ouverture de cycle en absence de solvant pour produire le PLA.
En règle générale, le PLA à un faible poids moléculaire et possède des propriétés mécaniques médiocres [18], d’où la polymérisation par ouverture de cycle est la méthode favorisée [17].
8
Il est à mentionner qu’un processus biologique complet pour la production du PLA et de ses copolymères à partir de ressources renouvelables a été récemment développé par fermentation directe grâce à des bactéries. Si Jae Park et al. ont examiné les progrès récents dans la production de lactate contenant des homo-et co-polyesters par des bactéries métaboliquement modifiées [20,21]. Ce procédé n’est toutefois pas encore appliqué à l’échelle industrielle.
2) Propriétés du PLA
2.1) Stéréochimie du PLA
L’acide lactide a trois stéréoisomères : L -lactide, D-Lactide et méso lactide. La composition stéréochimique du PLA a un effet significatif sur son point de fusion, la vitesse de cristallisation, l’étendue de sa cristallinité et ses propriétés mécaniques [22]. Le poly (D-lactide) ou poly (L-lactide) purs sont un point de fusion à l’équilibre cristallin à 207°C [23,24]. Or la présence de cristallites imparfaits, d’impuretés et de faible racémisation fait que le point de fusion typiques du PLA varie entre 170 et 180°C [19]. Un mélange en quantités égales de poly (L-lactide) et poly (D-lactide) purs a une température de fusion plus élevée (230˚C) et de meilleures propriétés mécaniques que les deux polymères purs. La résistance à la traction du stéréocomplexe est de 50 MPa tandis que celle du poly (L-lactide) pur est de 31 MPa [19,25,26]. La composition stéréochimique n’a par contre pas d’effet sur la température de transition vitreuse qui se situe entre 55 et 60˚C pour le poly (L-lactide) ayant une Mv de 23-66 kDa et entre 49 et 52˚C pour le poly
(D, L-lactide) ayant une Mv de 47.5-114 kDa [27]. Étant donné que la stéréochimie affecte
le taux de cristallinité et que ce dernier influence la vitesse de dégradation et les propriétés mécaniques [27,28], la stéréochimie a donc un impact sur ces deux propriétés.
Parmi les travaux qui se sont intéressés à relier les propriétés mécaniques à la stéréochimie, on cite celui de Bigg [29] qui a observé une augmentation notable du pourcentage d’élongation et de la contrainte à la rupture du PLA avec différents ratios du L-lactide et du D, lactide selon une orientation biaxiale. Pour un copolymère avec un ratio 80/20 de
L-9 lactide/D, L-lactide, l’élongation à la rupture a augmenté de 5.7 à 18.2 % et la contrainte à la rupture de 51.7 à 84.1 MPa pour une orientation biaxiale à 85˚C.
2.2) Propriétés thermiques
Les propriétés physiques du polylactide sont liées à la pureté enantiomérique des stéréo-copolymères de l’acide lactique. L’homo-PLA est une macromolécule linéaire ayant une architecture moléculaire qui est déterminée par sa composition stéréochimique. Le PLA peut être produit totalement amorphe ou cristallin. Les résines PLA contenant plus de 93% d'acide L-lactique sont semi-cristallines. Mais, le PLA avec 50-93% d’acide L-lactique est complètement amorphe. Par conséquent, le rapport L/D induit ou réduit la cristallinité du polymère. Les deux méso -et D-lactide induisent des torsions dans une architecture très régulière du poly (L-lactide). Les imperfections macromoléculaires sont responsables de la diminution à la fois du taux et de l'étendue de la cristallisation du PLLA. Pratiquement la majorité du PLA est constituée de copolymères L et D, L-lactide puisque sa production contient souvent des impuretés méso-lactide [30].
Dépendamment des conditions de préparation, le poly (L-lactide) cristallise en différentes formes [31]. La forme α présente un diagramme de diffraction bien définie. Cette structure est plus stable que la structure β et possède une température de fusion de 185˚C par rapport à 175˚C pour la structure β. Cette dernière peut être formée avec un rapport d'étirage élevé et à haute température d'étirage [32]. La forme γ est obtenue par cristallisation épitaxiale. Il a été observé qu'un mélange en quantités égales de PLLA et de PDLA donne une stéréo-complexation (cristallite racémique) des deux polymères. Ce stéréo complexe a des propriétés mécaniques meilleures que celles de PLLA ou PDLA purs et une température de fusion égale à 230˚C [30].
On trouve dans la littérature, différentes densités de PLA. Principalement, les phases cristallines donnent une densité de 1.29 contre 1.25 pour le matériau amorphe. Le PLA est un polymère qui cristallise lentement comme le PET. Sa cinétique de cristallisation a été largement étudiée. Comme le PET, le PLA peut être orienté par le traitement. L’orientation de la chaîne augmente la résistance mécanique du PLLA. Si l'orientation est effectuée à basse température, elle mène à un PLLA ayant un meilleur module sans avoir une
10
augmentation significative de la cristallinité. Pour déterminer le taux de cristallinité par DSC, la valeur la plus souvent mentionnée dans la littérature concernant l’enthalpie de fusion du PLA 100% de cristallin est de 93 J/g [33].
La cristallisation du PLA thermiquement cristallisable mais amorphe, peut être initiée par un recuit à des températures comprises entre 75°C et la température de fusion. Le recuit de copolymères de PLA cristallisables produit souvent deux pics de fusion. Différentes hypothèses ont été présentées. Certains auteurs [34] ont trouvé des points de fusion doubles dans les polymères PLLA et les ont attribués à la lenteur de cristallisation et de recristallisation.
La température de transition vitreuse, Tg, typique du PLA varie de 50 à 80˚C, tandis que la température de fusion, Tf, varie de 130 à 180˚C. Par exemple, le PLA énantiomériquement
pur est un polymère semi-cristallin ayant une Tg de 55˚C et une Tf de 180˚C. Pour le PLA
semi-cristallin, la Tf dépend des différents paramètres du procédé utilisé et de la structure
initiale du PLA. La Tf augmente avec le poids moléculaire (MW) jusqu'à une valeur
maximale. En outre, la cristallinité diminue avec l'augmentation de MW. La Tg est
également déterminée par la proportion des différents types de lactide. La Tf dépend de la
présence de méso-lactide dans la structure, laquelle réduit la Tf [31]. Le PLA peut être
plastifié en utilisant un oligomère d’acide lactique (ola) [33], de l’ester citrique [35], ou le polyéthylène glycol de faible poids moléculaire (PEG) [33,36-38].
La plastification augmente la mobilité des chaînes et favorise l'organisation du PLA et la cristallisation. Après la plastification, une cristallinité comprise entre 20 et 30% est obtenue [30].
2.3) Propriétés mécaniques
Les propriétés mécaniques du PLA, qui ont été largement étudiées, sont dépendantes de son processus de production et de son état amorphe ou semi-cristallin. Le PLA amorphe présente un module de traction entre 2.05 et 3.25 GPa [33,39], sauf selon Murariu et al. [40] qui ont montré un PLA avec un module de traction de 1.02 GPa. Cette gamme considérable de propriétés est due à la vitesse d'essai de traction qui varie de 1 à 50
11 mm/min pour les différentes études. La contrainte à la rupture et l’élasticité varient entre 32 et 68 MPa et entre 3 et 20%, respectivement [35, 39,40].
La cristallisation du PLA pur modifie légèrement les propriétés mécaniques. Selon Kulinski et al. [41], la cristallisation à froid induit une légère diminution de la limite d'élasticité et de la contrainte à la rupture. Cependant, Perego et al. [27] n'ont pas remarqué cette modification dans la contrainte et la déformation. Cependant, ils ont montré une augmentation
du module d'élasticité et de la résistance à l'impact, probablement en raison des effets de réticulation des domaines cristallins.
Perego et al. [27] ont également montré une influence de la masse molaire du polymère amorphe sur la résistance aux chocs et la flexion qui est multipliée par 1.5 à 2 lorsque la masse moléculaire a été portée de 23000 à 66000 g/mol. Ces évolutions sont les mêmes lorsque les échantillons sont recuits. La comparaison des deux grades de PDLLA, un pour un usage général, et l'autre pour l’injection, a montré une différence dans le module qui peut être due à une différence de masse moléculaire. En outre, la comparaison des propriétés mécaniques des films orientés et non orientés montre une augmentation de l'allongement à la rupture avec l'orientation.
À la température ambiante, les propriétés mécaniques du PLA sont proches de celle du PS mais inférieures à celle du PET. Les polyoléfines présentent une résistance à la traction inférieure à celle du PLA mais la déformation à la rupture de LDPE et HDPE sont beaucoup plus élevées que celle du PLA. En comparaison à un autre polymère d'origine naturelle, le poly (hydroxybutyrate) (PHB), le PLA présente de meilleures propriétés mécaniques (le module d'élasticité et la résistance à la traction) [42].
3) Caractéristiques et applications
Les caractéristiques du PLA font de lui un polymère très demandé et employé dans divers domaines. Parmi ses caractéristiques :
12
- Écologique: il est biodégradable, recyclable et compostable [43,22] et sa production consomme du dioxyde de carbone [44].
- Biocompatible: les produits de sa dégradation ne sont pas toxiques [45].
- Processabilité: le PLA peut être traité par divers procédés tels que l’injection moulage, l’extrusion, le thermoformage, etc.
- Économie d’énergie: sa production nécessite 25-55% moins d’énergie que les polymères issus de la pétrochimie et peut être encore réduite de 10% [18].
Grâce à sa biorésorbabilité et sa biocompatibilité dans le corps humain, le PLA a été utilisé pour les sutures résorbables et les appareils prostatiques [46]. Son application est surtout remarquable dans le domaine de l’emballage, car la majorité des procédés classiques de mise
en forme peuvent être utilisés [47].
Différentes compagnies comme Mitsui Chemicals (Japan), Mitsubishi (Japan), Shimadzu (Japan), Futerro (Total/ Galactic—Belgium), Purac (Netherland), Teijin (Japan), et Zhejiang HisunBiomaterials (China) produisent des produits PLA avec une large gamme de ratio L/D.
Cargill ((NatureWorks) [48,49]) a développé un procédé utilisant le maïs et autre matières premières pour obtenir différents grades de PLA. La production de cette compagnie est estimée à 140.000 tonnes/an. Présentement, c’est la production de polyester biodégradable qui est la plus élevée et son prix est estimé à 2€/kg.
La consommation du PLA est seulement aux alentours de 200.000 tonnes/an. Présentement, uniquement 30% d’acide lactique est utilisé pour la production du PLA. Par conséquent, ce biopolymère a un fort potentiel de développement. Disponible commercialement, on peut trouver le PLLA ayant une cristallinité très élevée (C-PLA) ainsi que les copolymères du PLLA, le poly (D, L-acide lactique) (PDLLA) qui sont plutôt amorphes (A-PLA) [27,49, 50].
Dannon et McDonald’s (Allemagne) ont été les pionniers dans l’utilisation du PLA comme matériau d’emballage pour les pots de yaourt et les couverts [46].
13
III- Le chitosane
1) Production
Le chitosane est un polymère naturel, non toxique, comestible et biodégradable. Il est obtenu par déacétylation de la chitine et il est considéré comme étant le biopolymère le plus abondant dans la nature après la cellulose.
La chitine peut être extraite des végétaux, comme les champignons, et des insectes, mais elle est surtout extraite des carapaces des crustacés vu qu’elle représente 20-30% de leur poids sec [51]. Elle est insoluble dans les solvants usuels, y compris les acides faibles ou les bases fortes. Elle possède une faible réactivité chimique et est un polysaccharide azoté dur, blanc et inélastique [52]. En moyenne, son poids moléculaire varie entre 1.03 et 2.5 x 106 Da, mais avec une N-déacétylation, il est réduit à une valeur de 1 à 5 x 105 Da
[53].
Le chitosane, contrairement à la chitine, n’est pas abondant dans la nature. On peut le trouver dans certains champignons (zygote fungi) et la paroi abdominale de la reine termite.
La chitine et le chitosane ont une structure chimique similaire (Figure 1.3). Ils sont formés de chaînes linéaires des groupes acétyle glucosamine, la seule différence est dans le nombre de groupements acétyles qui est inférieur pour le chitosane.
14
En effet le chitosane est obtenu industriellement selon le procédé de déacétylation de la chitine selon ces étapes :
- La déminéralisation
Cette étape est généralement réalisée à l’aide d’une extraction avec l’acide hydrochlorique diluée (10%) à température ambiante et avec une agitation pour dissoudre le carbonate de calcium sous forme de chlorure de calcium. Une déminéralisation optimale est obtenue avec une agitation constante des carapaces séchées et broyées avec du HCl 1N pendant 30 min à la température ambiante et à un ratio solide/solvant de 1:15 (w/v) [55].
- La déprotéinisation
Certaines protéines peuvent être extraites par des méthodes douces d’autres nécessitent un traitement plus poussé ce qui laisse à supposer la formation de fortes liaisons covalentes avec la chitine [56].
Les carapaces de crustacés sont habituellement broyées et traités avec une solution diluée d’hydroxyde de sodium à haute température (65-100°C) afin de dissoudre les protéines. Le temps de réaction est généralement de 0.5 à 12 h dépendamment des méthodes de préparation. Des conditions optimales impliquent le traitement de ces carapaces avec une solution de NaOH à 3.5 % (w/w) pendant 2h à 65°C avec une agitation continue et un ratio solide/solvant de 1 :10 (w/v) [55].
- La décoloration
Pour obtenir une chitine blanche, l’extraction avec l’acétone a été utilisée, la chitine a ensuite été séchée à température ambiante pendant 2 h. Le blanchissement est effectué avec 0.315% (v/v) d’une solution d’hypochlorure de sodium pendant 5 min avec un ratio solide/solvant de 1 :10 (w/v) (basé sur le poids sec) [55].
15 - La déacétylation
Cette étape consiste à éliminer une partie des groupements acétyle de la chitine et nécessite l’utilisation de l’hydroxyde de sodium ou potassium concentré à la température ambiante pendant 72h [57] ou à 100°C pendant au moins 30 min [54].
Une autre alternative, est une méthode douce et contrôlée qui consiste à utiliser une enzyme, la chitine déacétylase, qui catalyse la déacétylation des résidus N-acétyle-D-glucosamine de la chitine en des résidus D-N-acétyle-D-glucosamine chitosane [58,59]. Une fois que le degré de déacétylation (DD) de la chitine atteint approximativement 60 à 70%, on parle alors de chitosane [60, 61].
Plusieurs paramètres peuvent néanmoins affecter la production de chitosane. On peut citer la température de déacétylation [62,63], le temps de déacétylation et la concentration alcaline [64], l’atmosphère avec laquelle on travaille (air ou azote) [64,62], etc.
2) Caractéristiques du chitosane
- Degré de déacétylation
Suite au procédé de déacétylation, le chitosane devient riche en groupements amine hautement réactifs, ceci fait du degré de déacétylation un paramètre important vu qu’il affecte les propriétés physicochimiques, et donc détermine les applications du chitosane [65]. La déacétylation affecte aussi la biodégradabilité et l’activité immunologique [66].
La déacétylation donne au chitosane deux avantages par rapport à la chitine. Pour pouvoir dissoudre la chitine, il faut utiliser des solvants très toxiques tels le chlorure de lithium, tandis que le chitosane se dissout dans les acides dilués. Le deuxième avantage est que le chitosane possède des groupements amine libres qui sont des sites actifs dans les réactions chimiques [67]. Le degré de déacétylation du chitosane varie entre 56 et 99% avec une moyenne de 80%, dépendamment des espèces de crustacés et des méthodes de préparation [68].
16
Plusieurs méthodes ont été utilisées pour déterminer le degré de déacétylation, on en cite le test de ninhydrine, le titrage potentiométrique linéaire, la spectroscopie infra rouge et proche infrarouge et la spectroscopie RMN [69].
- Poids moléculaire
Le chitosane commercial a un poids moléculaire variant entre 100.000 et 1.200.000 Da [70]. En général, à une température élevée, de l’oxygène dissout et la contrainte de cisaillement peuvent dégrader le chitosane. Par exemple, au-delà de 280°C, il y une dégradation thermique du chitosane, les chaînes de polymères se rompent ce qui réduit le poids moléculaire [65].
La chromatographie [64], diffraction de la lumière [52] et la viscosimétrie [71] sont des méthodes utilisées pour déterminer le poids moléculaire.
- Viscosité
Étant donné que les propriétés fonctionnelles du chitosane dépendent de sa viscosité et de son poids moléculaire [72], plusieurs chercheurs se sont intéressés à l’influence des paramètres employés dans le procédé de fabrication sur la viscosité du chitosane. Il s’est avéré que la viscosité diminue suite à la variation de plusieurs paramètres, tels que l’augmentation du temps de déminéralisation, l’élimination de l’étape de déminéralisation avec une déprotéinisation à l’aide d’une solution de NaOH à 3% [64] ou encore avoir recours au blanchissement [73]. Autre que ces paramètres, les traitements physiques et chimiques [74] ainsi que la taille des particules [62] affectent aussi la viscosité.
- Solubilité
Le chitosane est soluble dans les acides dilués tels que l’acide acétique. Les solutions d’acides concentrées à haute température peuvent dépolymériser le chitosane [75]. Au-delà d’un pH 7, la stabilité de la solubilité du chitosane devient faible. À des pH élevés, le chitosane a tendance à précipiter et former un gel [76]. La solubilité est par
17 contre contrôlée par le degré de déacétylation et il est estimé que le degré de déacétylation soit au moins de 85% pour pouvoir atteindre la solubilité désirée [68].
- Caractère filmogène
Ce caractère traduit la capacité du chitosane à former un film continu en durcissant, ce qui fait de lui un polymère adéquat pour l’emballage alimentaire. Il peut être utilisé pour emballer les viandes avec une atmosphère modifiée [77] ou être employé comme agent de revêtement pour la préservation des fruits [78].
- Propriétés antimicrobiennes
Cette propriété est l’une parmi les plus importantes du chitosane vu que le pouvoir d’inhiber l’activité des bactéries fait du chitosane un polymère très convoité pour l’emballage alimentaire.
Le chitosane s’est montré plus efficace avec les bactéries à gram-positif (Listeria monocytogenes, Bacillus megaterium, B. cereus, Staphylococcus aureus, Lactobacillus plantarum, L. brevis, et L. bulgaris) que celles à gram-négatif (E. coli, Pseudomonas fluorescens, Salmonella typhymurium, et Vibrio parahaemolyticus) [79].
- Pouvoir émulsionnant
Même si le chitosane ne peut pas produire des émulsions, il peut améliorer la capacité émulsionnante des composés tels que le jaune d’œuf [80], l’huile de tournesol pour laquelle le degré de déacétylation optimal était de 81 [81] et de 89 [65].
3) Propriétés
Les films de chitosane sont biodégradables, biocompatibles, flexibles, durables, solides, résistants et difficiles à briser. Ils ont des valeurs modérées de perméabilité à l'eau et à l'oxygène, ils diminuent la fréquence respiratoire des aliments et inhibent la croissance microbienne [82].
La plupart des propriétés mécaniques des films de chitosane sont comparables à celles des polymères commerciaux de force moyenne, tels la cellulose [83]. La perméabilité ainsi que les propriétés mécaniques de ces films peuvent être contrôlées par le choix du poids
18
moléculaire et du solvant [84] ainsi que par l’ajout d’agent plastifiant et d’un compatibilisant [85,86,87]; par contre la présence de ces composés peut affecter l’activité antimicrobienne des films de chitosane [88].
4) Applications
- Purification de l’eau usée
La plus large utilisation du chitosane est dans la clarification des eaux usées et des effluents. La prise de conscience des problèmes écologiques et sanitaires liés aux métaux lourds et les pesticides, et leur accumulation dans la chaîne alimentaire a incité la nécessité d'une purification rigoureuse de l'eau industrielle avant sa décharge pour l’utilisation [89,90].
La capacité des groupements NH2 libres du chitosane à former des liaisons covalentes/de
coordination avec les ions métalliques est d’un grand intérêt [91].
La poudre de chitosane et/ou les films séchés de chitosane sont d’une utilité considérable dans la complexation des ions métalliques vu que le chitosane a la majorité de ses groupements amines libres au-delà de la valeur du pKa. L’utilisation du chitosane pour la purification de l’eau potable a été approuvé par l’agence américaine de protection de l’environnement (USEPA), jusqu’à un maximum de 10 ppm [89].
Le chitosane, le carboxyméthyle chitosane et le chitosane réticulé se sont montrés efficaces dans l’élimination du Cd2+, Cu2+, Hg2+ et le Zn2+ de l’eau usée et des effluents industriels
[52,92].
Grâce à sa structure moléculaire unique, le chitosane a une affinité élevée pour certaines classes de colorants, y compris les colorants sulfurés et les colorants à base de naphtol [93]. Il est aussi utilisé dans la séparation des colloïdes et les particules dispersées dans les déchets de transformation d’aliments [94,95].
- Additif pour papier
Le chitosane confère une résistance à l'état humide au papier [96]. L’hydroxyméthyle chitine et autres dérivés solubles dans l'eau sont des additifs finaux utiles dans la fabrication du papier. L'utilisation de chitosane donne aussi de meilleures caractéristiques de finition de papier [53].
19
- En agriculture
Le chitosane et ses dérivés ont des propriétés antifongiques et protectrices des plantes, déclenchant un mécanisme de défense chez les plantes contre les infections et les attaques de parasites, même à de très faibles concentrations. Il est utilisé sous forme de solution ou de revêtement de la semence. Il agit à différents niveaux, en renforçant le système racinaire et en épaississant la tige. Il agit aussi tel un fertilisant en accélérant la germination et la croissance des plantes [53].
- Domaine pharmaceutique
Son caractère polymérique cationique et ses groupements fonctionnels potentiellement réactifs (un groupe amine en position C-2 et deux groups hydroxyles aux positions C-3 et C-6) lui confèrent la possibilité d’être utilisé dans la thérapie de libération contrôlée de médicaments [97,98].
L’hydrogel de chitosane ioniquement réticulé offre plus de possibilités en tant que système de transport de médicaments, même s’il manque de stabilité mécanique [53,99].
Le chitosane possède toutes les caractéristiques requises pour fabriquer des lentilles de contact idéales, avec une clarté optique, une stabilité mécanique et une correction optique suffisantes. Des lentilles de contact ont été fabriquées à partir de chitosane issu de plume calmar partiellement dépolymérisée et purifiée, et sont claires, dures et ont de bonnes résistances à la traction et à la déchirure [100].
Grâce à sa biocompatibilité avec le tissu du corps humain, le chitosane s’est montré efficace pour toutes les formes de pansement de la peau, les fils de suture en chirurgie, les implants ou les gommes de cicatrisation pour la réparation des os ou la chirurgie dentaire [101,102].
Dans les crèmes dentaires, il prolonge la durée de conservation de pâte et contribue également à la régénération de gencives défectueuses [103].
20
- Clarification et désacidification des jus de fruits
Les sels de chitosane, chargés positivement, ont été utilisés pour contrôler l’acidité dans les jus de fruits [104]. Le chitosane s’est avéré être un bon agent clarifiant pour les jus de raisins et de pommes que ce soit avec ou sans traitement à la pectinase, ce qui donne des produits ayant une turbidité nulle [105].
- Contrôle du brunissement enzymatique des fruits
Les composés phénoliques et l’activité du polyphénol oxydase sont responsables du brunissement qui affecte la couleur, le goût et la valeur nutritive des fruits et légumes [106 ,107].
L’application d’un film ou d’un revêtement de chitosane aux fruits de litchi a retardé le brunissement enzymatique, modifiant ainsi le contenu des anthocyanes, les flavonoïdes et les phénoliques totaux [108]. Elle a aussi retardé l’augmentation de l’activité du polyphénol oxydase et a inhibé partiellement l’accroissement de l’activité de la peroxydase [109].
- Les cosmétiques
Le chitosane est utilisé dans les crèmes et les lotions et quelques-uns de ses dérivés sont aussi utilisés dans la préparation des vernis à ongles [110]. Le chitosane dépolymérisé et la carboxyméthyle chitine ont été utilisés comme éléments actifs dans des produits tels que le shampoing et le revitalisant vu la viscosité de leurs solutions aqueuses, leur caractère filmogène, leur capacité de rétention d’humidité et leur adoucissement de la peau et des cheveux [111].
- Batteries à l’état solide
Les batteries à l’état solide conductrices de proton ont besoin d’un polymère conducteur de protons. Le chitosane est un biopolymère qui peut donner une conductivité ionique une fois dissout dans l’acide acétique. La conductivité est due à la présence de protons dans la solution d’acide acétique. Le transport de ces protons est pensé se produire à travers
21 nombreux micro-vides dans le polymère vu que les constantes diélectriques sont faibles selon les études piézoélectriques [112].
5) Application dans l’emballage alimentaire
5.1) Les films de chitosane
En 1936, Rigby avait obtenu un brevet pour avoir fabriqué des films de chitosane et un deuxième brevet pour l’élaboration de fibres de chitosane. Les films obtenus étaient décrits comme flexibles, durs, transparent et incolore avec une résistance à la traction de 6210 kPa [113].
L’utilisation des films de chitosane pour prolonger la durée de vie et améliorer la qualité des aliments frais et congelés a été examinée [114,115], vu les excellents propriétés de ces films.
L’utilisation des films de N, O- carboxyméthyle chitosane pour préserver les films pour une longue période a été approuvée au Canada et aux USA [116]. Grâce à sa capacité de former des films semi-perméables, le chitosane devrait pouvoir modifier l’atmosphère interne, réduire les pertes dues à la transpiration et retarder la maturation des fruits [117,118].
Les propriétés mécaniques, la perméabilité, le point de décomposition thermique, la stabilité chimique, etc., sont des paramètres vitaux pour la sélection du film adéquat pour les applications spécifiques [119]. Les films de chitosane sont préparés en dissolvant le chitosane dans l’acide dilué et en l’étalant ensuite sur une surface plane pour le laisser sécher à la température ambiante. Les films peuvent aussi être séchés à 60°C dans un four en étalant la solution sur du plexiglas [120,121]. Ces procédés sont par contre demandeurs en temps.
Les films à base de chitosane peuvent aussi être fabriqués par ‘casting’ suivi d’un séchage à l’infra rouge (IR) [122], lequel est plus rapide que les méthodes conventionnelles. Ces films n’ont pas de différences significatives dans les propriétés mécaniques et barrières par rapport aux films obtenus avec les méthodes conventionnelles de séchage [123].
22
5.2) Pouvoir antimicrobien
Ces dernières années, les activités antimicrobiennes et antifongiques du chitosane et ses produits de dégradation comme les chito-oligomères et les chitosanes de faible poids moléculaire ont fait l’objet de plusieurs études [109, 124,125] en mettant l’accent sur leurs capacités à préserver les aliments [126].
Le chitosane a été approuvé en tant qu’additif alimentaire en Corée du Sud et au Japon depuis 1995 et 1983, respectivement [127,128]. Son pouvoir antimicrobien est dû à la présence de groupement NH2+ libres à la position C-2, ce qui le rend plus soluble et plus
cationique que la chitine. Le mécanisme précis de son activité antimicrobienne reste inconnu [113]. L’inhibition de la croissance et l’inactivation de la moisissure et des levures semblent dépendre en la concentration du chitosane, le pH, et la température [65].
Cuero [129] a trouvé que l’action antimicrobienne du chitosane est influencée par des facteurs intrinsèques et extrinsèques tels que le type du chitosane (brut ou dérivé), le degré de polymérisation, la nature des aliments, la composition chimique du substrat et/ou de l’aliment, et les conditions environnementales telles que l’activité du substrat dans l’eau. Dans une étude plus poussée [130] sur l’activité antimicrobienne du chitosane contre l’E.coli, il a été trouvé qu’une température élevée et un pH acide des aliments augmentaient l’effet antimicrobien du chitosane. Les auteurs ont aussi expliqué le mécanisme de l’action antimicrobienne du chitosane par une interaction entre le chitosane et les anions de la surface bactérienne engendrant un changement dans la perméabilité de la membrane.
L’activité antibactérienne élevée du chitosane à faible pH suggère que l’addition du chitosane à des aliments ayant un pH acide améliore son efficacité en tant qu’agent de conservation naturel [124]. Le chitosane à faible poids moléculaire possède une meilleure inhibition contre les phytopathogènes que celui à haut poids moléculaire [131].
Le revêtement de chitosane retarde significativement l’altération ou la décomposition des fruits et légumes tels que les tomates, les fraises, etc., à différentes températures. Les fruits revêtus de chitosane étaient non seulement plus fermes et avec une acidité plus élevée,
23 mais étaient aussi lents à se décomposer et avaient moins de pigmentation que les échantillons sans chitosane à la fin du stockage [132].
Wang [133] a observé que le chitosane pouvait rendre les S. aureus et L. monocytogènes inactifs à un pH 5.5 ou 6.5. L’effet d’inhibition de la L. monocytogènes a pu durer pour au moins 8 semaines [134]. Chang et al. [135] ont trouvé que des concentrations de 0.005% étaient suffisantes pour inactiver le S.aureus.
Un des dérivés du chitosane, le N-carboxybutyle chitosane, a été testé sur 298 cultures de différents microorganismes pathogènes et l’examen par microscopie électronique a montré une altération morphologique de ces microorganismes [136].
Le chitosane reste coûteux (≈ $15.5/kg), comparé aux films plastiques d’emballage (≈ $2/kg), alors même que les biopolymères sont beaucoup moins chers (l’amidon de maïs et la cellulose par exemple sont à ∼0.8 – 1.0$/kg). Néanmoins, pour le revêtement alimentaire et les applications pharmaceutiques, un tel prix est toléré, mais ce cout reste élevé pour l’emballage usuel [113].
IV- Le mélange PLA /CS
Les méthodes de synthèse du mélange de chitosane et du PLA sont très variées, dépendamment des applications ciblées. En effet ce mélange est utilisé dans le domaine médical comme vecteur de substance active vu sa biocompatibilité dans l’industrie textile et dans l’emballage.
Les propriétés du mélange obtenu varient selon plusieurs critères: la méthode de synthèse utilisée, la composition du PLA et du chitosane, la présence ou non d’un compatibilisant et d’un plastifiant.
1) Généralités sur les mélanges
L’élaboration des mélanges a généralement pour but d’améliorer les caractéristiques d’un polymère dédié à une certaine application. Ceci peut être en améliorant les propriétés
24
mécaniques [137,138], comme la résistance à l’impact [139,140,141], en réduisant la sensibilité à l’eau [140, 142,143] ou simplement en réduisant le coût [144,145,146].
Parmi les propriétés les plus étudiées des mélanges de biopolymères, il y a les propriétés thermiques, surtout la température de transition vitreuse, Tg, et les propriétés mécaniques comme la rigidité [147,148,149], la résistance [148,150,151], la flexibilité et la déformabilité [150,152,153,154]. Moins fréquemment, d’autres propriétés sont discutées comme les caractéristiques optiques [150,155], la biodégradabilité [156,157], l’inflammabilité [158] et le prix [137-146].
1.1) Types de mélanges
On distingue trois types de mélanges [159] : - Les mélanges totalement miscibles
Pour ces mélanges, ΔH<0 vu l’existence d’interactions spécifiques. L’homogénéité est observée à l’échelle nanométrique au moins, si ce n’est à l’échelle moléculaire.
- Les mélanges partiellement miscibles
Dans ces mélanges, une partie d’un composé est dissoute dans l’autre. Ce genre de mélange a une bonne morphologie des phases et des propriétés satisfaisantes, et sont donc considérés compatibles. Les deux phases du mélange (l’une riche en polymère 1 et l’autre en polymère 2) sont homogènes, et ont leurs propres Tg qui sont déplacées de la Tg du composé pur vers la Tg de l’autre composé.
- Les mélanges entièrement immiscibles
Les plupart des mélanges appartiennent à cette catégorie. Ils ont une morphologie de phase grossière, l’interface est nette, et l’adhésion entre les deux phases (chacune ayant la Tg du composé pur) est faible, ce mélange est donc inutile sans compatibilisant. Il faut toutefois faire une distinction entre ‘miscibilité’ et ‘compatibilité ’.
La miscibilité est un terme thermodynamique qui, à l’aide d’un modèle approprié, décrit le comportement d’une paire de polymère en spécifiant le nombre de phases qui se forment
25 dans le mélange et leur composition. Le modèle le plus fréquemment utilisé à cet effet est celui de Flory-Huggins [160,161].
D’un autre côté, la compatibilité est un terme technique définissant le profil de propriété du mélange en vue d’une certaine application [159]. Un mélange est dit compatible s’il a des propriétés désirées et utiles, d’un point de vue commercial, que ce soit par une miscibilité totale ou partielle, ou par l’utilisation d’une technique de compatibilisation adéquate [159]. La compatibilité des polymères est généralement modifiée par des moyens physiques (compatibilisants, les blocs de copolymères) ou chimiques (comme le traitement réactif) [162].
1.2) Thermodynamique des mélanges
La thermodynamique aide à prédire la miscibilité d’un mélange.
La relation la plus importante qui gouverne le malaxage de deux composés différents est celle de l’enthalpie libre :
GHTS (1.1) Où H correspond à l’enthalpie et S correspond à l’entropie [163].
L’expression théorique de l’énergie libre G est le point de départ pour prédire le comportement des phases à l’équilibre [164]. Pour qu’il y ait une miscibilité, il faut que G0. Or, plus les chaines sont longues, plus ΔS sera petit et donc plus ΔG sera élevée. Ceci explique thermodynamiquement le problème d’immiscibilité de nombreux polymères [165]. Or, cette condition est nécessaire mais pas suffisante [163,165], une deuxième condition doit être satisfaite :
26
Avec ϕi la fraction volumique d’un composé i [163]. Une valeur négative de l’équation
(1.2) même si G0 indique que le mélange peut se séparer en deux phases, chacune riche en l’un des composés [163].
La théorie la plus pertinente pour calculer l’énergie libre du mélange est celle de Flory-Huggins qui a été développée de façon indépendante par Flory [160] et Flory-Huggins [161]. Étant donné que la miscibilité dépend des interactions entre les polymères, on peut la caractériser grâce à cette théorie. Même si les interactions sont compliquées et que les paramètres utilisés sont complexes et constitués de plusieurs composantes [166], cette approche est la plus simple d’un point de vue pratique et est largement utilisée pour l’estimation de la miscibilité [155, 167, 168,169].
Cette théorie se base sur certaines hypothèses simplificatrices, à partir desquelles on pourrait obtenir l’expression suivante de l’énergie libre du mélange [165].
ΔG = kT ( Ln
+ Ln
+ Ӽ
)
(1.3)Avec
K : la constante de Boltzmann
NA et NB le degré de polymérisation de A et B χ: le paramètre d’interaction de Flory
T : la température en degré kelvin. Φ : la fraction volumique.
1.3) Évaluation de la miscibilité
La miscibilité pourrait être évaluée à l’aide de plusieurs méthodes. L’analyse par spectroscopie infrarouge à transformée de Fourier (IR-TF) et par spectroscopie différentielle à balayage figurent parmi les plus utilisées.
27 Avec l’analyse DSC, la Tg du mélange est déterminée [153,154] et la miscibilité est alors déduite du fait qu’il y ait une seule Tg du le mélange qui est située entre les Tg des composants purs [153,170].
On trouve souvent deux températures de transition vitreuse qui se déplacent chacune vers l’autre en changeant la composition du mélange [152]. Le résultat est évalué de manière qualitative tandis qu’on peut l’analyser de manière quantitative grâce à l’approche de Kim et Burns [171].
Autre que la température de transition vitreuse, la température de fusion peut donner une indication sur les interactions dans le mélange selon la méthode de Nishi et Wang [172]. La base de cette approche est la théorie de Flory-Huggins.
La spectroscopie IR-TF est aussi largement utilisée pour étudier les interactions [148, 173,174], lesquelles sont reflétées par les changements dans les pics caractéristiques des composés [175,176].
La microscopie électronique à balayage peut aussi renseigner sur la miscibilité ou non des différentes phases d’un mélange. Il y a généralement recours à une attaque chimique d’une phase ou simplement à l’extraction à l’eau chaude des composés solubles [177] lorsqu’il n’y a pas assez de contraste permettant de distinguer les phases.
2) Compatibilisation
Les compatibilisants présentent généralement une activité interfaciale dans les mélanges de polymères hétérogènes [159], tandis que l’effet de la compatibilisation est généralement attribué à une augmentation de l’adhésion interfaciale et à des particules dispersées plus petites résultant en de meilleures propriétés mécaniques. On peut distinguer différentes stratégies de compatibilisation. Dans le cas des méthodes non réactives, les composées amphiphiles préfabriqués, tels les blocs de copolymères, sont rajoutés au mélange. Une des extrémités ou un des blocs étant miscible avec un des composés du mélange, tandis que l’autre est miscible avec le deuxième composé du mélange [162].
28
La représentation la plus significative de la compatibilisation non réactive des mélanges de biopolymères est l’ajout de blocs de copolymères [178,179]. Le développement d’autres méthodes telles que l’incorporation de composés amphiphiles de faibles poids moléculaires [180], les ionomères [143] ou un troisième polymère au moins partiellement miscible avec les deux polymères composant le mélange [138] est dans une phase initiale. Une des raisons principales du faible succès de la compatibilisation non réactive est que les procédés réactifs sont plus efficaces [159]. Dans ce cas, la structure en bloc agissant comme un compatibilisant se forme in-situ durant le malaxage. Ceci peut impliquer l’ajout de polymères avec les groupes réactifs [181,182], ou des réactifs de faible poids moléculaire [183-186] pour former le compatibilisant. Une autre possibilité est la modification chimique de l’un des composés pour qu’il y ait des groupes réactifs [145, 156,157]. Le fait que les biopolymères ont souvent divers groupements réactifs rend l’application de ces méthodes plausible et pratique [162].
Un des compatibilisants les plus utilisés est le polycaprolactone, PCL, qui est un polymère biodégradable issu de la pétrochimie. Il a un faible point de fusion (60°C), une faible viscosité et est facile à traiter à cause de la flexibilité de ses chaines moléculaires [187]. Le PCL possède une élongation à la rupture élevée entre 450% et 1100% pour une résistance à la traction de 25 et 33 MPa respectivement [188,189]. Ces propriétés sont meilleures que celles du LDPE qui possède une élongation à la rupture de 500 à 725 % et une résistance à la traction de 9.7 à 17.2 MPa [189].
3) Plastification
Les plastifiants sont des composés organiques de faibles poids moléculaires utilisés pour assouplir les polymères rigides [190]. Ils agissent en réduisant la Tg des polymères, réduisant leurs cristallinité ou leur température de fusion [191].
Les plastifiants se dissolvent dans les polymères en séparant les chaînes les unes des autres, facilitant ainsi le mouvement moléculaire. Ils sont employés pour augmenter la maniabilité, la flexibilité et l’extensibilité des polymères [192]. Ils agissent comme des lubrifiants internes en réduisant les forces de friction entre les chaines de polymère [193]. Leur action peut causer des changements dramatiques dans les propriétés mécaniques des
29 polymères [194,195]. Les plastifiants peuvent être de différentes natures chimiques comme les esters, les hydrocarbones, l’eau, les alcools, les glycols, les phénols, les cétones et les éthers [193,194]. Les plastifiants idéaux sont miscibles et compatibles pour toutes les proportions avec les composées plastiques. Par contre, la compatibilité et la migration hors du polymère suivent deux chemins différents : plus le plastifiant est compatible et efficace, plus il peut diffuser rapidement hors du polymère [194].
Les plastifiants peuvent être ajoutés aux polymères en solution (technique de dispersion) ou après que le solvant ait été enlevé (technique d’absorption) [196]. D’une manière générale, le pouvoir plastifiant d’une molécule dépend de sa masse molaire et du nombre de groupes hydroxyles présents sur la molécule. En effet la masse molaire va directement influencer la diffusion dans le mélange. Plus la masse moléculaire est faible, meilleure est la diffusion. Concernant le nombre de groupes hydroxyles, plus le nombre de fonction alcool est important, meilleur est le pouvoir plastifiant de la molécule [165].
Plusieurs théories ont été proposées pour expliquer le mécanisme d’action du plastifiant, résultant dans la diminution de la température de traitement [197]. Dans la ‘théorie de lubrification’, le plastifiant agit comme un lubrifiant en facilitant le mouvement des macromolécules, tandis que la ‘théorie du gel’ considère la perturbation des interactions polymère-polymère (les bandes hydrogène et les forces ioniques de van des Waals). La ‘théorie du volume libre’ indique que la plastification mène à l’augmentation du volume libre et a été utile pour clarifier la diminution de la Tg grâce au plastifiant.
Peu importe la théorie, l’action du plastifiant est de s’interposer entre les chaînes de polymères et d’atténuer les forces qui les maintiennent ensemble [198]. Entwistle et Rowe [198] ont observé que l’efficacité du plastifiant dans la diminution de la Tg augmente quand le degré d’interactions plastifiant-polymère diminue. Les groupes de recherche de Kalichevsky et de Cuq [199,200] ont attribué l’effet de plastification élevé des protéines avec de petites molécules, telles le glycérol, à la facilité d’insertion et de positionnement du plastifiant dans le réseau protéique tridimensionnel.
30
4) Méthodes d`élaboration des mélanges
Deux des procédés les plus utilisés sont le ‘casting’ et le mélange par voie fondue.
4.1) Mélange en solution (casting)
Cette méthode repose sur le caractère filmogène du chitosane, sans lequel on ne pourrait obtenir des films à partir du mélange. Elle consiste à dissoudre chacun des polymères dans un solvant adéquat et à mélanger les différentes solutions par la suite. La solution obtenue est étalée sur une surface plane pour que les solvants s’évaporent et que le film se forme [6,201,202,203,204,205]. Toutefois, le séchage peut avoir lieu de différentes manières. Il peut être effectué à la température ambiante ou avec un chauffage, sous vide ou non et il peut durer jusqu’à 48 h.
Plusieurs études ont déjà porté sur la synthèse des films de chitosane par la technique du ‘casting’ et se sont intéressées à l’effet de la concentration du plastifiant [204], du temps de stockage [120], du type d’acide utilisé et de sa concentration [206], du poids moléculaire du chitosane [207] et de son degré de déacétylation [121] sur les propriétés mécaniques et barrières des films.
Le mélange en solution de PLA et de chitosane prend souvent un compatibilisant tout autant qu’un plastifiant, vu que ces deux polymères sont incompatibles et cassants. Le polyéthylène glycol (PEG) est l’un des plastifiants les plus utilisés pour ce mélange [6,87]. Parmi les compatibilisants essayés pour les mélanges PLA/Chitosane, il y a le 4,4'-méthylène bis (phénylisocyanate) MDI [54] et l’alcool polyvinylique [203].
Pour procéder sans compatibilisant, certains chercheurs [12] ont essayé de modifier le chitosane en le faisant réagir avec le chlorure d’hexanoyle afin le rendre plus hydrophobe et donc plus compatible avec le PLA.
4.2) Mélange par voie fondue
Dans l’industrie, pour mélanger des polymères par voie fondue, on utilise généralement un mélangeur interne (batch) ou un mélangeur continu, tel que l’extrudeuse bi-vis [208].
![Figure 1.1 : Les monomères optiques de l’acide lactique [17]](https://thumb-eu.123doks.com/thumbv2/123doknet/6660333.182269/22.918.310.574.669.827/figure-les-monomères-optiques-l-acide-lactique.webp)
![Figure 1.2 : Étapes de la synthèse du PLA [18]](https://thumb-eu.123doks.com/thumbv2/123doknet/6660333.182269/23.918.226.736.671.1000/figure-étapes-synthèse-pla.webp)
![Figure 1.3 : Structure chimique de la chitine (a) et du chitosane (b) [54]](https://thumb-eu.123doks.com/thumbv2/123doknet/6660333.182269/29.918.237.713.749.1033/figure-structure-chimique-chitine-chitosane.webp)