UNIVERSITE MOHAMMED V - AGDAL
FACULTÉ DES SCIENCES
Rabat
THESE DE DOCTORAT
Présentée parEL MORHIT Mohammed
Discipline : Sciences de l’Environnement Spécialité : Toxicologie
Soutenue le 05 décembre 2009 Devant le jury :
Président :
H. JAZIRI, Professeur à la Faculté des Sciences de Rabat Examinateurs :
M. FEKHAOUI, Professeur à l’Institut Scientifique de Rabat
A. YAHYAOUI, Professeur à la Faculté des Sciences de Rabat
L. MOUHIR, Professeur à la Faculté des Sciences et Technique de Mohammedia
M. JBILOU, Docteur, responsable du Laboratoire de Toxico-Pharmacologie de la Gendarmerie Royale à Rabat
A. EL ABIDI, Docteur, responsable du Laboratoire d’Hydrologie et Toxicologie à l’Institut National d’Hygiène de Rabat
Faculté des sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat - Maroc Tel+212(05) 37 77 18 34/35/38, Fax : + 212 (05) 37 77 42 61 http://www.fsr.ac.ma
Les travaux présentés dans ce mémoire ont été effectués au sein de l’UFR: Biodiversité et Aquaculture, à la Faculté des Sciences de Rabat avec la collaboration du Laboratoire d’Hydrologie et Toxicologie de l’Institut National d’Hygiène et le Laboratoire d’Hydrologie et Ecotoxicologie de l’Institut Scientifique de Rabat.
Une grande partie de ce travail a été réalisée dans le cadre du Programme Thématique d’Appui à la Recherche Scientifique PROTARS III D14/52.
Les travaux de cette thèse ont été menés sous la direction conjointe de Messieurs les Professeurs YAHYAOUI A. de la Faculté des Sciences de Rabat et FEKHAOUI M. de l’Institut Scientifique de Rabat, avec la collaboration et le co-encadrement du Docteur
EL ABIDI A., responsable du Laboratoire d’Hydrologie et Toxicologie de l’Institut National d’Hygiène de Rabat. Au moment de présenter ce travail, nous mesurons tout le prix des soutiens et concours dont nous avons bénéficié dans l’accomplissement de notre tâche et sans lesquels plusieurs obstacles auraient été insurmontables. Nous assurons de notre profonde reconnaissance les responsables de ces institutions qui ont contribué à la réalisation de ce travail et tous ceux qui nous ont apporté leur aide.
Ma gratitude et mes respects à Monsieur le Professeur YAHYAOUI A., directeur de l’UFR : « Biodiversité et Aquaculture » pour son encadrement exemplaire, son assurance, ses amples conseils, ses aides précieuses, sa bienveillante attention et sa disponibilité permanente.
Mes sincères remerciements vont également à Monsieur le Professeur M. FEKHAOUI, directeur du Laboratoire d’Hydrologie et Ecotoxicologie de l’Institut Scientifique de Rabat. Qu’il me soit permis ici d’exprimer ma profonde gratitude pour la confiance qu’il m’a témoigné en m’intégrant dans son équipe pluridisciplinaire sur la problématique de complexe zones humides de la ville de Larache. Vous m’avez toujours soutenu normalement dans les circonstances difficiles et vous avez parrainé et guidé ce travail avec bienveillance.
Mes remerciements s’adressent également à Monsieur JAZIRI H., Professeur à la Faculté des Sciences de Rabat, qui a bien voulu présider l’honorable jury de ce travail.
Il m'est agréable d'exprimer mes sincères remerciements, ma gratitude et mon profond respect à mes co-encadrants Monsieur le Dr. JBILOU M., responsable du département de Toxico-Pharmacologie au Laboratoire Médical de la Gendarmerie Royale à Rabat et Monsieur le Dr. EL ABIDI A., responsable du Laboratoire d’Hydrologie et Toxicologie à l’Institut National d’Hygiène de Rabat, qui ont dirigé et suivi de très près ce travail de recherche et qui ont bien voulu juger ce mémoire. C'est grâce à leurs suggestions, leurs remarques et critiques que ce travail a pu être réalisé.
Mes remerciements s’adressent également à Madame le Professeur MOUHIR L. membres du jury, qui a bien accepté de siéger au jury de cette thèse. Qu’elle trouve ici l’expression de ma reconnaissance !
Mes remerciements s’adressent également à Mesdames les Professeur A. SERGHINI et S. EL BLIDI, Professeurs à l’Institut Scientifique de Rabat, qui m’ont chaleureusement accueilli dans leur laboratoire pour la réalisation de l’étude géochimique des sédiments. Malgré leurs multiples responsabilités et leur temps précieux, elles n’ont pas hésité à m’aider tant sur le plan technique que moral. Mon séjour parmi elles s’est déroulé dans une ambiance amicale et les discussions que j’ai eues avec elles ont été très fructueuses.
Je réserve une attention redevable à mes amis et collègues, Dr. ZINDIN A., Dr. BENBAKHTA C., Inj. BENAAKAM R., INJ. BENAAMI F., Inj BARAKAT N., Adams. REDOU N. Inj. LABRINI F., de Institut National d’Hygiène de Rabat, pour les aides intellectuelles et morales. Ils m’ont soutenu, encouragé et épaulé tout au long de ces années de recherche. Je leur témoigne mon affection la plus sincère.
Il est bon et juste d’évoquer l’appui moral ainsi que la sollicitude trouvée auprès de toute ma famille. Je tiens à exprimer mes sentiments les plus respectueux et ma profonde reconnaissance à mes très chers parents, à mes frères et sœurs, pour les encouragements constants qu’ils ont déployé tout au long de ces années de recherche.
Enfin, je remercie toutes les personnes qui, de près ou de loin, ont apporté leur contribution à ce travail. Je leur exprime ici toute ma reconnaissance et ma sympathie.
"
Nous nous sommes trop aisément accommodes
d'un peu plus de disparités sociales, d'un peu
plus de violence sociales, d'une atmosphère un
peu plus polluée, d'un environnement un peu
plus en danger. Cette indifférence ou cette
accoutumance, si elles devraient perdurer et donc
s'aggraver, conduiraient à un suicide collectif.
La est le vrai danger, la est le véritable enjeu".
Extrait du discours du feu S.M le roi Hassan II à l'occasion de la journée mondiale contre la pauvreté, le 17 octobre 1997.
« Nous avons tenu à présider l'ouverture des travaux du Conseil
Supérieur de l'Eau et du Climat, tant nous mesurons
l'importance primordiale de l'eau qui constitue, à nos yeux, l'un
des éléments de la souveraineté nationale, et tant nous sommes
convaincus de la vertu du dialogue constructif qui s'engage
dans les instances compétentes sur toutes les questions
nationales majeures. Si notre pays recèle, par la grâce de Dieu,
des ressources naturelles abondantes, c'est aussi la volonté
divine qui tient à nous mettre à l'épreuve de la sécheresse.
Les effets pervers de ce phénomène auraient pu être plus graves
pour notre économie et pour l'équilibre de notre écosystème, sans
la politique éclairée de l'eau conduite par notre vénéré père- que
Dieu l'ait en sa Sainte miséricorde-, politique qui a amené le
Conseil Mondial de l'Eau à attribuer le nom de Hassan II au
prix international le plus prestigieux qui consacre la meilleure
œuvre mondiale dans le domaine de l'hydraulique. »
Extrait de l'allocution prononcée par SA MAJESTE LE ROI MOHAMMED VI 9ème session du CSEC, Agadir le 21 juin 2001.
i
PRINCIPALES PUBLICATIONS ET COMMUNICATIONS REALISEES DANS LE CADRE DE CE TRAVAIL
1. EL MORHIT M., FEKHAOUI M., SERGHINI A., EL BLIDI S., EL ABIDI A.,
BENNAAKAM R., YAHYAOUI A. & M. JBILOU, 2008. - Impact de l’aménagement hydraulique sur la qualité des eaux et des sédiments de l’estuaire du Loukkos (côte atlantique, Maroc). Bulletin de l’Institut Scientifique, 30 : 39–47.
2. EL MORHIT M., FEKHAOUI M., ELIE P., GIRARD P., YAHYAOUI A., EL ABIDI
A. & M. JBILOU, 2009. - Heavy metals in sediment, water and the European glass eel, Anguilla anguilla (Osteichthyes : Anguillidae) from Loukkos river estuary (Morocco, eastern Atlantic). Cybium (sous presse).
3. EL MORHIT M., FEKHAOUI M.,EL ABIDI A.,YAHYAOUI A.& M. JBILOU. -
Metallic contamination in muscle of five fish species from Loukkos estuary (Atlantic coast Morocco) (sous presse).
COMMUNICATIONS ORALES
1. EL MORHIT M., EL ABIDI A., SERGHINI A., YAHYAOUIA. et JBILOU M. & M.
FEKHAOUI, 2008. - Contamination métallique de Sardina pilchardus de la côte atlantique marocaine et des sédiments de l’estuaire du bas Loukkos.Biodiversité et Ecosystèmes.Vèmes Journées Nationales de BiodiversitéSurBiodiversité au service du développement durable. 18 au 20 décembre 2008, Fès- Maroc (soumis).
2. EL MORHIT M. 2009. Impact des activités hydro-agricoles sur la qualité des
sédiments de l’estuaire du bas Loukkos (Maroc). Problématiques des Déchets Solides. Société Marocaine de Toxicologie Faculté de Médecine et de Pharmacie, 28 avril 2009, Rabat. Maroc (soumis).
3. EL MORHIT M., EL ABIDI A., SERGHINI A., EL BLIDI S., YAHYAOUI A.,
JBILOU M. & M. FEKHAOUI, 2009. - Contamination métallique de Sardina pilchardus de la côte atlantique marocaine et des sédiments de l’estuaire du bas Loukkos. 5ème Journées Internationales des Géosciences de l’Environnement. Gestion des déchets : « Pollution et dépollution : eau, air et sol ». Faculté des Sciences Dhar El Mahraz B.P. 1796. 13-14 mai 2009, Fès – Maroc (soumis).
4. EL MORHIT M., FEKHAOUI M., EL ABIDI A., YAHYAOUI A. & M. JBILOU,
2009. - Impact des activités hydro-agricoles sur la qualité des eaux et des sédiments de l’estuaire du bas Loukkos (Côte atlantique, Maroc). Conférence Internationale sur la Gestion Durable des Déchets Solides (MWM-09). Décharges - Impacts environnementaux. Université Chouaib Doukkali, 19-20 juin 2009– El Jadida – Maroc (soumis).
ii
5. EL MORHIT M., FEKHAOUI M., EL ABIDI A., YAHYAOUI A. & M. JBILOU,
2009. - Étude de la variation spatio-temporelle des paramètres hydrologiques caractérisant la
qualité des eaux de l’estuaire du bas Loukkos (Maroc). La 2ème édition du Congrès
International. « Eaux, Déchets et Environnement ». Union des pays de la méditerranée. 26-27 novembre 2009, El Jadida, Maroc (soumis).
6. EL MORHIT M., EL ABIDI A., SERGHINI A., YAHYAOUI A., JBILOU M.,
FEKHAOUI M., GIRARD P. & P. ELIE, - Contamination métallique des muscles de cinq espèces de poissons de la côte atlantique Marocaine et de l’estuaire adjacente du Loukkos. La 2ème édition du congrès international. « Eaux, déchets et environnement ». Union des pays de la méditerranée. 26-27 novembre 2009, El Jadida, Maroc (soumis).
7. EL MORHIT M. 2005. - Evaluation de la pollution métallique des poissons de la côte
atlantique marocaine. Eaux Usées : Risques Sanitaires, Traitement et Réutilisation. Première séminaire de la formation continue. 30 juin 2005, Kenitra, Maroc (soumis).
COMMUNICATIONS PAR AFFICHES
1. EL MORHIT M., FEKHAOUI M., SERGHINI A., EL ABIDI A., YAHYAOI A. &
JBILOU M.,2007. - Contamination métallique d’Anguilla anguilla au niveau de l’estuaire de
Loukkos (Maroc). VIIème Congrès Maghrébin des Sciences de la Mer et Premier Congrès
Franco - Maghrébin de Zoologie et d’Ichtyologie – 4-7 novembre 2007, El Jadida, Maroc.
2. EL MORHIT M., FEKHAOUI M., JBILOU M., EL ABIDI A., EL BLIDI S. & A.
SERGHINI, 2007. - Evaluation de la pollution métallique de l’estuaire des sédiments du bas Loukkos (ville de Larache). Equipe de Recherche "Valorisation des Ressources Naturelles et Biodiversité". Quatrième Journées Internationales. Oiseaux d'Eau et Zones Humides au Maroc. Faculté des Sciences (Univ. Chouaib Doukkali), 16-17 février 2007, d'El Jadida Maroc.
3. EL MORHIT M., FEKHAOUI M., SERGHINI A., EL ABIDI A., YAHYAOUI A. &
M. JBILOU, 2008. - Contamination métallique des muscles de cinq espèces de poissons de l’estuaire du bas Loukkos (côte atlantique Marocaine). 2ème Congrès des Sciences Analytiques (CSA), 29 octobre 2008, Casa, Maroc (soumis).
4. EL MORHIT M. 2009. - L’impact de la pollution sur l’environnement et la santé :
Approche de Remédiation. Association Marocaine pour l’Environnement et le Développement Durable, à l’Institut Agronomique et Vétérinaire Hassan II, 4 juin 2009, Rabat, Maroc (soumis).
iii
INTRODUCTION GENERALE ... 1
I.1. Cadre général et présentation du bassin de Loukkos ... 6
I.1.1. Le Bassin Versant ... 6
I.1.2. La plaine alluviale ... 7
I.1.3. Aménagement hydraulique ... 7
I.1.4. Source de pollution dans le bassin de Loukkos ... 8
I.1.4.1. La pollution domestique ... 8
I.1.4.2. Les mines et industries ... 8
I.1.4.3. La pollution industrielle ... 8
I.1.4.4. L’agriculture ... 9
I.1.4.5. Etat de la qualité des eaux du bas Loukkos ... 10
I.1.4.6. Alimentation en eau potable et industrielle ... 10
I.1.4.7. Les industries isolées ... 10
I.2.1. L’estuaire du bas Loukkos ... 12
I.2.2. Délimitation de la zone d’étude ... 13
I.2.3. Morphologie de l’estuaire. ... 14
I.2.4. Hydrographie ... 14
I.2.5. Cadre géologique ... 15
I.2.6. L’hydrologie de l’estuaire ... 15
I.2.6.1. L’hydrologie fluviale ... 15
I.2.6.2. L’hydrologie marine ... 15
I.3. Climatologie ... 18
I.3.1. Régime climatique ... 18
I.3.2. Pluviosité ... 19
I.3.3. Température ... 20
I.3.4. Insolation ... 21
I.3.5. Vent ... 21
I.3.6. Aperçu pédologique ... 21
I.4. Population urbaine et rurale ... 21
I.5. Situation géographique de nos stations de prélèvement et sources de pollution locale de l’estuaire du bas Loukkos ... 22
I.5.1. Sources de pollution en amont de l’estuaire du bas Loukkos ... 23
I.5.2. Sources de pollution en aval de l’estuaire du bas Loukkos ... 23
I.5.3. Lutte contre la pollution ... 24
II.1. Présentation de la zone d’étude ... 25
II.2. Echantillonnage ... 26
II.3. Préparation des échantillons et leur conservation ... 27
II.3.1. Mesure des paramètres physico-chimiques de l’eau ... 27
II.3.1.1. Relevés effectués sur le terrain ... 27
II.3.1.2. Analyses effectuées au laboratoire ... 28
II.3.2. Prélèvement des sédiments, des eaux et poissons pour l’analyse des ETM ... 28
II.3.2.1. Sédiments ... 28
II.3.2.2. Eau ... 29
iv
II.3.2.4. Dosage des métaux lourds des différents prélèvements ... 30
II.3.2.5. Contrôle de qualité ... 30
II.3.2.6. Analyse statistique ... 31
I.1. Introduction ... 33
I.2. Evaluation spatio-temporelle des paramètres physico-chimiques de la qualité de l’eau ... 33
I.2.1. Température de l’air (Ta) ... 34
I.2.2. Température de l’eau (Te) ... 35
I.2.3. Salinité (Sa) ... 37
I.2.4. Conductivité (Ce) ... 39
I.2.5. Oxygène dissous (OD) ... 40
I.2.6. Potentiel hydrogène (pH) ... 41
I.2.7. Matière en suspension (MES) ... 43
I.2.8. Carbone Organique Total (COT) ... 44
I.2.9. Nitrates (NO3) ... 45
I.2.10. Demande chimique en oxygène (DCO) ... 46
I.2.11. Demande biologique en oxygène (DBO5) ... 47
I.3. Bilan de la qualité des paramètres physicochimiques des eaux ... 48
I.3.1. Approche spatiale ... 48
I.3.2. Autoépuration et évolution globale des paramètres étudiés. ... 51
I.3.3. Paramètres globaux de la pollution des eaux de l’estuaire du bas Loukkos. ... 53
I.3.4. Normes relatives à la qualité des eaux d’alimentation humaine ... 53
I.4. Structure Typologique de l’estuaire du bas Loukkos ... 54
I.4.1. But de l’analyse ... 54
I.4.2. Définition et principe ... 55
I.4.3. Nature des données ... 55
I.4.4. Résultats et interprétation ... 56
I.4.5. Dynamique marégraphique des paramètres physicochimiques de l’eau de l’estuaire du bas Loukkos ... 58
I.4.6. Dynamique de l’hydrosystème des paramètres physicochimiques de l’eau de l’estuaire du bas Loukkos ... 61
I.5. Grands traits du fonctionnement hydrologique de l’estuaire du bas Loukkos ... 63
I.6. Bilan ... 65
II.1. Introduction ... 66
II.2. Détermination de la teneur métallique naturelle des sédiments ... 66
II.3. Évaluation de la variation spatio-temporelle de la contamination métallique des sédiments ... 68
II.3.1. Le fer (Fe) ... 69
II.3.2. Le zinc (Zn) ... 70
II.3.3. Le cuivre (Cu) ... 70
II.3.4. Le chrome (Cr) ... 71
II.3.5. Le plomb (Pb) ... 72
II.3.6. Le cadmium (Cd) ... 73
II.4. Bilan de la contamination métallique des sédiments ... 76
II.5. Evaluation du degré de contamination métallique des sédiments ... 79
II.5.1. Définition ... 79
II.5.2. Evaluation du degré de contamination à partir des données brutes. ... 80
II.6. Interprétation de la contamination métallique des sédiments ... 85
v
II.8. Analyse de variance (ANOVA) de la contamination métallique des sédiments ... 89
II.9. Effet de la marée sur la contamination métallique des sédiments ... 90
II.9.1. Dynamique marégraphique des sédiments ... 90
II.9.2. Dynamique de l’hydrosystème des sédiments ... 92
II.10. Conclusion sur la contamination métallique des sédiments ... 94
III.1. Introduction ... 95
III.2. Évaluation de la variation spatio-temporelle des ETM des eaux ... 95
III.2.1. Le fer (Fe) ... 96
III.2.2. Le zinc (Zn) ... 96
III.2.3. Le cuivre (Cu) ... 97
III.2.4. Le chrome (Cr) ... 98
III.2.5. Le plomb (Pb) ... 98
III.2.6. Le cadmium (Cd) ... 99
III.3. Bilan de la contamination métallique des eaux ... 101
III.4. Évaluation du degré de contamination des eaux ... 102
III.4.1. Définition ... 102
III.4.2. Evaluation du degré de contamination à partir des valeurs brutes ... 103
III.5. Interprétation de la contamination métallique des eaux ... 105
III.6. ACP des ETM dans l’eau ... 107
III.7. ANOVA des ETM dans l’eau ... 111
III.8. Effet de la marée sur la contamination métallique des eaux ... 111
III.8.1. Dynamique marégraphique des ETM dans l’eau ... 111
III.8.2. Dynamique de l’hydrosystème des ETM dans l’eau ... 113
III.9. Qualité de la contamination métallique des eaux ... 116
III.10. Conclusion sur la contamination métallique des eaux ... 116
IV.1. Introduction ... 117
IV.2. Espèces de poissons ... 119
IV.2.1. Pagellus acarne (Risso, 1826) Rome, 1998 ... 119
VI.2.2. Sardina pilchardus (Walbaum, 1792) Rome, 1998 ... 119
IV.2.3. Diplodus vulgaris (Geoffroy St. -1817) Rome, 1998 ... 120
IV.2.4. Liza ramada (Thomson, 1986) ... 120
IV.2.5. Barbus callensis (Risso, 1810) ... 121
IV.2.6. Anguilla anguilla (civelles) Linnaeus, 1758 ... 121
IV.3. Variation intra-spécifique des teneurs métalliques chez les poissons étudiés ... 122
IV.3.1. Variation des teneurs métalliques dans les différents organes étudiés chez Pagellus acarne ... 122
IV.3.1.1. Le fer (Fe) ... 122
IV.3.1.2. Le zinc (Zn) ... 123
IV.3.1.3. Le cuivre (Cu) ... 123
IV.3.1.4. Le chrome (Cr) ... 123
IV.3.1.5. Le plomb (Pb) ... 124
IV.3.1.6. Le cadmium (Cd) ... 124
IV.3.1.7. Analyse et structure typologique de la contamination métallique chez Pagellus acarne ... 125
IV.3.1.8. L’analyse de variance (ANOVA) des ETM chez Pagellus acarne ... 128
IV.3.2. Variation des teneurs métalliques dans les différents organes étudiés chez Sardina pilchardus ... 129
vi
IV.3.2.2. Le zinc (Zn) ... 130
IV.3.2.3. Le cuivre (Cu) ... 130
IV.3.2.4. Le chrome (Cr) ... 130
IV.3.2.5. Le plomb (Pb) ... 131
IV.3.2.6. Le cadmium (Cd) ... 131
IV.3.2.7. Analyse et structure typologique de la contamination métallique chez Sardina pilchardus ... 132
IV.3.2.8. L’ANOVA des ETM chez Sardina pilchardus ... 135
IV.3.3. Variation des teneurs métalliques dans les différents organes étudiés chez Diplodus vulgaris ... 135
IV.3.3.1. Le fer (Fe) ... 136
IV.3.3.2. Le zinc (Zn) ... 136
IV.3.3.3. Le cuivre (Cu) ... 137
IV.3.3.4. Le chrome (Cr) ... 137
IV.3.3.5. Le plomb (Pb) ... 137
IV.3.3.6. Le cadmium (Cd) ... 137
IV.3.3.7. Analyse et structure typologique de la contamination métallique chez Diplodus vulgaris ... 138
IV.3.3.8. ANOVA des ETM chez Diplodus vulgaris ... 141
IV.3.4. Variation des teneurs métalliques dans les différents organes étudiés chez Liza ramada ... 141
IV.3.4.1. Le fer (Fe) ... 142
IV.3.4.2. Le zinc (Zn) ... 143
IV.3.4.3. Le cuivre (Cu) ... 143
IV.3.4.4. Le chrome (Cr) ... 143
IV.3.4.5. Le plomb (Pb) ... 143
IV.3.4.6. Le cadmium (Cd) ... 144
IV.3.4.7. Analyse et structure typologique de la contamination métallique chez Liza ramada ... 145
IV.3.4.8. ANOVA des ETM chez Liza ramada ... 147
IV.3.5. Variation des teneurs métalliques dans les différents organes étudiés chez Barbus callensis ... 148
IV.3.5.1. Le fer (Fe) ... 148
IV.3.5.2. Le zinc (Zn) ... 149
IV.3.5.3. Le cuivre (Cu) ... 149
IV.3.5.4. Le chrome (Cr) ... 149
IV.3.5.5. Le plomb (Pb) ... 149
IV.3.5.6. Le cadmium (Cd) ... 150
IV.3.5.7. Analyse et structure typologique de la contamination métallique chez Barbus callensis ... 151
IV.3.5.8. ANOVA ETM chez Barbus callensis ... 154
IV.4. Variation interspécifique des teneurs métalliques chez les espèces étudiées ... 155
IV.4.1. Variation spatiale des ETM dans les branchies ... 156
IV.4.2. Variation spatiale des ETM dans le foie ... 157
IV.4.3. Variation spatiale des ETM dans les muscles ... 158
IV.4.4. Variation spatiale des ETM dans tous les organes des poissons étudiés ... 158
IV.5. Facteur d’enrichissement des ETM dans les différents organes chez les espèces étudiées ... 160
IV.5.1. Facteur d’enrichissement (Branchies/Muscles) ... 160
IV.5.2. Facteur d’enrichissement (Foie/Muscles) ... 162
IV.6. Métaux lourds dans les tissus des civelles ... 163
IV.6.1. Variation des teneurs métalliques dans les tissus des civelles ... 164
IV.6.1.1. Le fer (Fe) ... 166
IV.6.1.2. Le zinc (Zn) ... 166
IV.6.1.3. Le cuivre (Cu) ... 166
IV.6.1.4. Le chrome (Cr) ... 166
IV.6.1.5. Le plomb (Pb) ... 166
IV.6.1.6. Le cadmium (Cd) ... 166
IV.6.1.7. ACP de la contamination métallique chez les civelles ... 168
IV.6.1.8. ANOVA de la contamination métallique chez les civelles ... 170
IV.7. Comparaison de nos résultats avec ceux de la littérature ... 171
IV.8. Normes des teneurs de certains métaux toxiques ... 172
vii
IV.9.1. Les branchies ... 174
IV.9.2. Le foie et les muscles ... 175
IV.9.3. Les muscles ... 177
IV.9.4. Les civelles ... 178
IV.10. Corrélation des ETM entre les eaux, sédiments et poissons (AA) ... 182
CONCLUSION GENERALE ... 185
REFERENCES BIBLIOGRAPHIQUES ... 190
vi
LISTE DES TABLEAUX PAR PARTIE PREMIERE PARTIE
CHAPITRE I
Tableau I.1 : Estimation de la pollution domestique des villes de plus de 10000 habitants (DRPE, 1991). ... 7
Tableau I.2 : Estimation de la pollution domestique des principaux centres urbains (DRPE, 1991). ... 8
Tableau I.3 : Inventaire des unités industrielles (DRPE, 1991). ... 9
Tableau I.4 : Industries non raccordées aux réseaux de distribution d’eau (CSE, 1991). ... 10
Tableau I.5 : Précipitation mensuelle moyenne durant les années 2004-2007 (ORMVAL, 2005). ... 19
Tableau I.6 : Température mensuelle moyenne durant les années 2004−2007 (ORMVAL, 2005). ... 20
Tableau I.7 : Données démographiques de la municipalité et la province de Larache (RGPH, 2004). ... 22
Tableau I.8 : Données démographiques de la municipalité de Larache (RGPH, 2004). ... 22
CHAPITRE II Tableau II.1 : Coordonnées géographiques des stations de l’estuaire du bas Loukkos. ... 25
Tableau II.2 : Campagnes de prélèvements... 27
Tableau II.3 : Date des campagnes de prélèvement des échantillons d’eau à (MH et MB). ... 27
Tableau II.4 : Caractéristiques biométriques des poissons étudiées. ... 30
Tableau II.5 : Valeurs trouvées et certifiées provenant de l’Agence International de l’Energie Atomique (IAEA. 433) au niveau du sédiment, eaux marines et estuariennes adjacentes et par DORM2 au niveau des poissons. .. 31
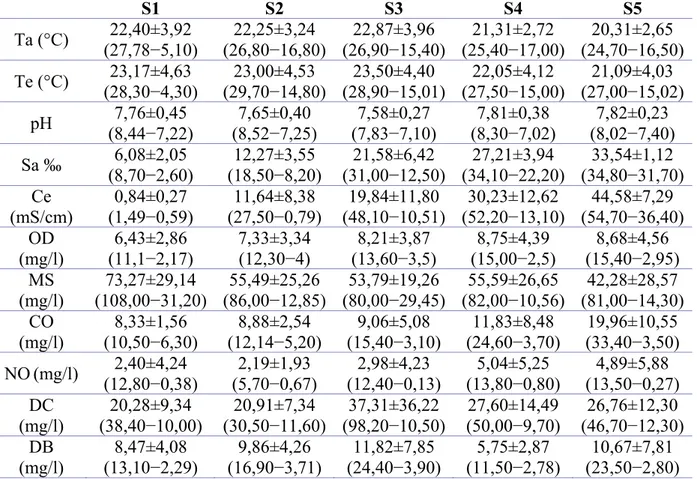
DEUXIEME PARTIE CHAPITRE I Tableau I.1 : Caractéristiques hydrologiques de l’estuaire du bas Loukkos durant l’année 06/07 (moyenne±écart-type, valeurs limites). ... 34
Tableau I.2 : Le pH des différents métaux (Duchauffour, 1995). ... 42
vii
Tableau I.3 : Normes relatives à la qualité des eaux d’alimentation humaine. ... 54
Tableau I.4 : Répartition de l’inertie entre les deux axes (F1XF2) à MH et MB. ... 56
Tableau I.5 : Matrice de corrélation (Pearson (n)) entre les variables étudiés. ... 56
Tableau I.6 : Codes de l’ACP et corrélations des variables avec les axes pour les deux cycles. ... 58
Tableau I.7 : Répartition de l’inertie entre les deux axes (F1XF2) pendant les deux cycles (MH et MB). ... 59
Tableau I.8 : Pourcentages des différents types de variabilité obtenue par l’analyse factorielle discriminante (AFD). ... 64
Tableau I.9 : Résultats de l’analyse de variance (ANOVA) des paramètres hydrologiques. ... 64
CHAPITRE II Tableau II.1 : Teneurs naturelles en ETM dans les sédiments exprimées (µg/g du poids sec). ... 67
Tableau II.2 : Niveau de référence des concentrations en métaux dans les sédiments fins de différentes origines (µg/g du poids sec ; RNO, 1998). ... 67
Tableau II.3 : Teneurs en métaux des différents échantillons de sédiments des différentes stations exprimées en µg/g du poids sec sauf Fe en mg/g de l’estuaire du bas Loukkos durant l’année 06/07 (moyenne±écart-type, valeurs limites). ... 68
Tableau II.4 : Ordre d'enrichissement des sédiments de stations. ... 74
Tableau II.5 : Ordre d'enrichissement des éléments métalliques ... 74
Tableau II.6 : Valeurs guides des teneurs métalliques dans les sédiments (µg/g) proposées par USEPA, d’après Hamdy et Post (1985). ... 76
Tableau II.7 : Teneurs métalliques en Cu et Cd (µg/g) au niveau de sédiment de large dans la zone de Jorf Lasfar (INRH, 1996). ... 77
Tableau II.8 : Indices de contamination (IC) et Indices de Contamination Moyen (ICM) calculés par rapport à la station de référence (SR=S3) dans les sédiments de l’estuaire du bas Loukkos. ... 81
Tableau II.9 : Ordre d'enrichissement des stations pour chaque métal dans les sédiments. ... 82
Tableau II.10 : Indices de contamination (Fe, Zn et Cu) calculés par rapport à la station de référence (SR=S3). 83 Tableau II.11 : Indices de contamination (Cr, Pb et Cd) calculés par rapport à la station de référence (SR=S3). 84 Tableau II.12 : Code de l’ACP et corrélations des variables des ETM dans les sédiments avec les axes. ... 86
viii
Tableau II.14 : Résultats de l’ANOVA des ETM étudiés dans les sédiments. ... 89
Tableau II.15 : Ordre de contamination décroissante des ETM des sédiments dans les stations et les campagnes. ... 89
CHAPITRE III Tableau III.1 : Teneurs en métaux des différents échantillons d’eaux des différentes stations exprimées en µg/l de l’estuaire du bas Loukkos durant les deux années 2006 et 2007 (moyenne±écart-type, valeurs limites). ... 95
Tableau III.2 : Ordre d'enrichissement des stations d’étude pour chaque métal dans l’eau. ... 100
Tableau III.3 : Ordre d'enrichissement des ETM de l’eau dans les stations d’étude. ... 100
Tableau III.4 : Concentrations moyennes exprimées en (µg/l) des ETM dans l’eau... 103
Tableau III.5 : Concentrations des métaux dans les eaux des estuaires marocains et autres estuaires européens exprimées en µg/l. ... 107
Tableau III.6 : Répartition de l’inertie entre les deux axes F1XF2 des ETM dans l’eau. ... 108
Tableau III.7 : Matrice de corrélation des ETM étudiés dans l’eau. ... 108
Tableau III.8 : Code de l’ACP et corrélations des variables des ETM dans l’eau avec les axes. ... 109
Tableau III.9 : Résultats de l’analyse de variance des ETM étudiés dans les eaux. ... 111
Tableau III.10 : Comparaison des normes internationales de métaux lourds pour les eaux de consommations (USA, 1992 ; OMS, 1993 ; CEE, 1980 ; France, 1991) exprimées en µg/l. ... 116
CHAPITRE IV Tableau IV.1 : Systématique des différents types de poissons étudiés selon (information sur l'environnement des pêches dans la république Algérienne démocratique et populaire, novembre 2003 ; Yahyaoui et Jaziri, 2002 ; Yahyaoui et al., 2004). ... 119
Tableau IV.2 : Teneurs en métaux (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans les différents organes chez Pagellus acarne issus de la côte atlantique méditerranéenne. ... 122
Tableau IV.3 : Ordre d'accumulation des organes de l’espèce Pagellus acarne pour les ETM. ... 124
Tableau VI.4 : Ordre d'accumulation en ETM dans les différents organes de poissons chez l’espèce Pagellus acarne. ... 124
Tableau IV.5 : Répartition de l’inertie des ETM entre les deux axes F1XF2 chez Pagellus acarne. ... 125
ix
Tableau IV.7 : Corrélation des variables avec les composantes principales chez Pagellus acarne. ... 127
Tableau IV.8 : Résultats de L’ANOVA des paramètres étudiés chez Pagellus acarne. ... 128
Tableau IV.9 : Teneurs en métaux (Fe, Cu, Cr, Pb, Zn et Cd) exprimées en µg/g du poids frais dans les différents organes chez Sardina pilchardus issus de la côte atlantique méditerranéenne ... 129
Tableau IV.10 : Ordre d'accumulation des organes de l’espèce Sardina pilchardus pour les ETM. ... 131
Tableau IV.11 : Ordre d'accumulation des différents ETM dans les différents organes chez les Sardina pilchardus. ... 131
Tableau IV.12 : Répartition de l’inertie des ETM entre les deux axes (F1XF2) chez Sardina pilchardus. ... 132
Tableau IV.13 : Matrice de corrélation (Pearson (n)) entre les variables chez Sardina pilchardus. ... 134
Tableau IV.14 : Corrélation des variables avec les composantes principales chez Sardina pilchardus. ... 134
Tableau IV.15 : Résultats de L’ANOVA des paramètres étudiés chez Sardina pilchardus. ... 135
Tableau IV.16 : Teneurs moyennes en métaux (Fe, Cu, Cr, Pb, Zn et Cd) exprimées en µg/g du poids frais dans les différents organes chez Diplodus vulgaris (côte atlantique marocaine). ... 135
Tableau IV.17 : Ordre d'accumulation des organes de l’espèce Diplodus vulgaris pour les ETM. ... 138
Tableau IV.18 : Ordre d'accumulation des métaux étudiés dans des différents organes chez les Diplodus vulgaris. ... 138
Tableau IV.19 : Répartition de l’inertie des ETM entre les deux axes chez Diplodus vulgaris. ... 139
Tableau IV.20 : Matrice de corrélation (Pearson (n)) entre les variables chez Diplodus vulgaris. ... 140
Tableau IV.21 : Corrélation des variables avec les composantes principales chez Diplodus vulgaris. ... 140
Tableau IV.22 : Résultats de L’ANOVA des paramètres étudiés chez Diplodus vulgaris. ... 141
Tableau IV.23 : Teneurs moyennes en métaux (Fe, Zn, Cu, Cr, Pb et Cd) exprimés en µg/g du poids frais dans les différents organes chez Liza ramada issus de l’estuaire du bas Loukkos. ... 142
Tableau IV.24 : Ordre d'accumulation des organes de l’espèce Liza ramada pour les ETM... 144
Tableau IV.25 : Ordre d'accumulation des ETM dans des différents organes chez les Liza ramada... 144
Tableau IV.26 : Répartition de l’inertie entre les deux axes chez Liza ramada. ... 145
Tableau IV.27 : Matrice de corrélation (Pearson (n)) entre les variables chez Liza ramada. ... 146
x
Tableau VI.29 : Résultats de L’ANOVA des paramètres étudiés chez Liza ramada. ... 147
Tableau IV.30 : Teneurs moyennes en métaux (Fe, Zn, Cu, Cr, Pb et Cd) exprimés µg/g du poids frais dans les différents organes chez Barbus callensis issus de l’estuaire du bas Loukkos. ... 148
Tableau IV.31 : Ordre d'accumulation des organes de l’espèce Barbus callensis pour les ETM. ... 150
Tableau IV.32 : Ordre d'accumulation des métaux étudiés dans des différents organes chez les Barbus callensis. ... 150
Tableau IV.33 : Répartition de l’inertie entre les deux axes chez Barbus callensis. ... 151
Tableau IV.34 : Matrice de corrélation (Pearson (n)) entre les variables chez Barbus callensis. ... 153
Tableau IV.35 : Corrélation des variables avec les composantes principales chez Barbus callensis. ... 153
Tableau IV.36 : Résultats de L’ANOVA des paramètres étudiés chez Barbus callensis... 154
Tableau IV.37 : Ordre d'accumulation des différentes espèces étudiées (PA, SP, DV, LR et BC). ... 155
Tableau IV.38 : Ordre d'accumulation des différents ETM étudiés dans les différentes espèces de poissons (PA, SP, DV, LR et BC). ... 156
Tableau IV.39 : Teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans les branchies chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 156
Tableau IV.40 : Teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans le foie chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 157
Tableau IV.41 : Teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans les muscles chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 158
Tableau IV.42 : Teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans tous les organes (B, F et M) chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 159
Tableau IV.43 : Ordre d'accumulation des ETM dans les différents organes des poissons étudiés. ... 159
Tableau IV.44 : Facteur d’enrichissement (concentration du métal dans les branchies/concentration du métal dans les muscles) dans l’estuaire et la côte atlantique marocaine étudiés. ... 160
Tableau IV.45 : Facteur d’enrichissement (concentration du métal dans le foie/concentration du métal dans les muscles) dans l’estuaire et la côte atlantique marocaine étudiés. ... 162
Tableau IV.46 : Teneurs en métaux (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids sec dans l’espèce AA (moyennes, écart-types, valeurs limites). ... 164
Tableau IV.47 : Ordre d'enrichissement de stations d’étude pour chaque métal. ... 167
xi
Tableau IV.49 : Résultats de L’ANOVA des ETM étudiés chez AA. ... 170
Tableau IV.50 : Teneurs métalliques dans les branchies, le foie et les muscles chez certaines espèces de poisson. ... 171
Tableau IV.51 : Normes des teneurs de certains métaux toxiques exprimées en µg/g du poids frais. ... 173
Liste des figures Figure 1 : Schéma synoptique du bassin versant de l’oued Loukkos. ... 6
Figure 2 : Principaux foyers de pollution industrielle. ... 9
Figure 3 : Situation géographique du périmètre du Loukkos. ... 12
Figure 4 : Localisation des stations d’étude dans l’estuaire du bas Loukkos (Maroc). ... 13
Figure 5 : Précipitation mensuelle moyenne durant les années 2004−2007. ... 19
Figure 6 : Température mensuelle moyenne durant les années 2004−2007. ... 20
Figure 7 : Localisation des stations d’études sur l’estuaire du bas Loukkos. ... 26
Figure 8 : Evolution spatio-temporelle de la température de l’air et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 35
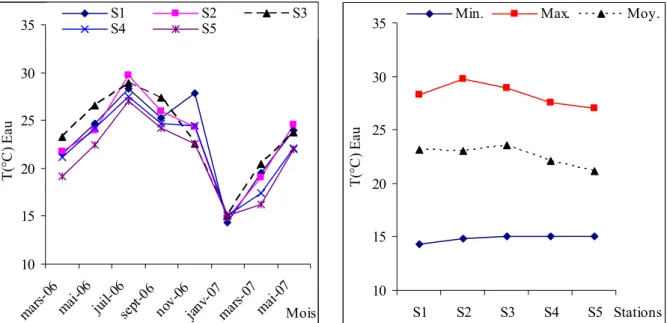
Figure 9 : Evolution spatiotemporelle de la température de l’eau et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 36
Figure 10 : Evolution spatiotemporelle de la salinité et celle des teneurs minimales, moyennes et maximales de ce paramètre. ... 38
Figure 11 : Evolution spatiotemporelle de la conductivité et celle des teneurs minimales, moyennes et maximales de ces paramètres. ... 40
Figure 12 : Evolution spatiotemporelle de l’oxygène dissous et celle des teneurs minimales, moyennes et maximales de ce paramètre. ... 40
Figure 13: Evolution spatiotemporelle du pH et celle des teneurs minimales, moyennes et maximales de ce paramètre... 43
Figure 14 : Evolution spatiotemporelle de la matière en suspension et celle des teneurs minimales, moyennes et maximales de ce paramètre. ... 44
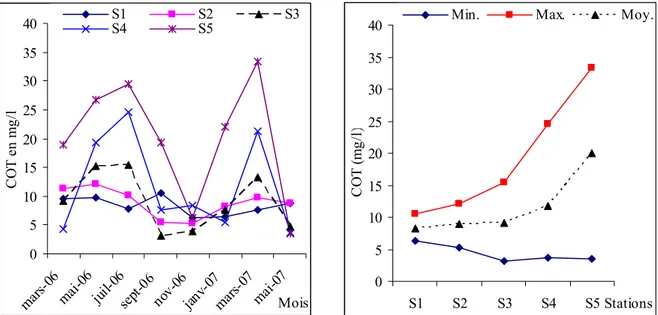
Figure 15 : Evolution spatiotemporelle du carbone organique total et celle des teneurs minimales, moyennes et maximales de ce paramètre. ... 45
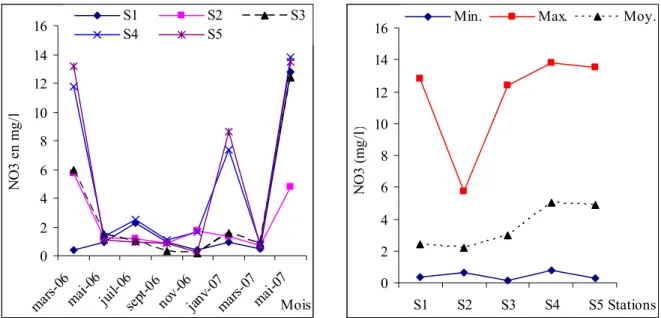
Figure 16 : Evolution spatiotemporelle du nitrate et celle des teneurs minimales, moyennes et maximales de ce paramètre... 46
xii
Figure 17 : Evolution spatiotemporelle de la DCO et celle des teneurs minimales, moyennes et maximales de ce paramètre... 47 Figure 18 : Evolution spatiotemporelle de la DBO5 et celle des teneurs minimales, moyennes et maximales de ce
paramètre... 48 Figure 19 : Approche graphique de l’analyse en ACP des paramètres hydrologiques. A : répartition de l’inertie entre les axes ; B : Cercle de corrélation des variables ; C : Carte factorielle des stations. ... 57 Figure 20 : Approche graphique de l’analyse en ACP de la dynamique marégraphique : répartition de l’inertie entre les axes, cercle de corrélation des variables et carte factorielle des stations (MH et MB). ... 60 Figure 21 : Représentation graphique dans le plan F1XF2 de l’évolution spatiale de la qualité des eaux de l’estuaire du bas Loukkos pour chaque campagne. ... 62 Figure 22: Variation spatiotemporelle des teneurs métalliques du Fe dans les sédiments dans les différentes stations d'étude et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 69 Figure 23 : Variation spatiotemporelle des teneurs métalliques du Zn dans les sédiments dans les différentes stations d'étude et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 70 Figure 24 : Variation spatiotemporelle des teneurs métalliques du Cu dans les sédiments dans les différentes stations d'étude et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 71 Figure 25 : Variation spatiotemporelle des teneurs métalliques du Cr dans les sédiments dans les différentes stations d'étude et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 72 Figure 26 : Variation spatiotemporelle des teneurs métalliques du Pb dans les sédiments dans les différentes stations d'étude et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 73 Figure 27 : Variation spatiotemporelle des teneurs métalliques du Cd dans les sédiments dans les différentes stations d'étude et celles des teneurs minimales, moyennes et maximales de ce paramètre. ... 74 Figure 28 : Graphiques sémantiques différentiels des éléments métalliques dans les sédiments. ... 75 Figure 29 : Variation spatiale de l’indice de contamination des sédiments dans les différentes stations d’étude en rapport avec celles trouvées dans la station 3 de l’estuaire du bas Loukkos. ... 81 Figure 30 : Variation spatiale de l’indice de contamination polymétallique moyen (Fe, Zn, Cu, Cr, Pb et Cd) des sédiments dans les différentes stations d’étude. ... 82 Figure 31 : Variation spatiale des indices de contamination (Fe, Zn et Cu) calculée par rapport à la station de référence (SR=S3). ... 83 Figure 32 : Les indices de contamination (Cr, Pb et Cd) calculés par rapport à la station de référence (SR=S3). 84 Figure 33 : Approche graphique de l’ACP des métaux dans les sédiments. A : Répartition de l’inertie entre les axes, B : Cercles de corrélation des variables, C et D : Carte factorielle des stations et des campagnes. ... 87
xiii
Figure 34 : Représentation graphique de l’analyse en ACP de la dynamique marégraphique des ETM dans les sédiments à MH et à MB. A-D : Valeurs propres de l’inertie, B-E : Cercle de corrélation des variables, C-F : Carte factorielle des stations. ... 91 Figure 35 : Représentation graphique dans le plan F1XF2 de l’évolution spatiale de la dynamique de
l’hydrosystème des ETM dans les sédiments de l’estuaire du bas Loukkos pour chaque campagne... 93 Figure 36 : Evolution spatiotemporelle des teneurs métalliques du Fe de l’eau exprimées µg/l en dans les différentes stations d'étude et celles des moyennes de ce paramètre. ... 96 Figure 37 : Variation spatiotemporelle des teneurs métalliques du Zn de l’eau exprimées µg/l dans les différentes stations d'étude et celles des moyennes de ce paramètre. ... 97 Figure 38 : Variation spatiotemporelle des teneurs métalliques du Cu de l’eau exprimées µg/l dans les différentes stations d'étude et celles des moyennes de ce paramètre. ... 97 Figure 39 : Variation spatiotemporelle des teneurs métalliques du Cr de l’eau exprimées µg/l dans les différentes stations d'étude et celles des moyennes de ce paramètre. ... 98 Figure 40 : Variation spatiotemporelle des teneurs métalliques du Pb de l’eau exprimées µg/l dans les différentes stations d'étude et celles des moyennes de ce paramètre. ... 99 Figure 41 : Variation spatiotemporelle des teneurs métalliques du Cd de l’eau exprimées µg/l dans les différentes stations d'étude et celles des moyennes de ce paramètre. ... 99 Figure 42 : Graphiques sémantiques différentiels des métaux lourds dans l’eau. ... 101 Figure 43 : Variation spatiale de l’indice de contamination dans les différentes stations d’étude en rapport avec celle trouvée dans la station 3 dans l’eau de l’estuaire du bas Loukkos. ... 104 Figure 44 : Variation spatiale de l’indice de contamination polymétallique moyen dans les différentes stations d’étude dans l’eau de l’estuaire du bas Loukkos. ... 104 Figure 45 : Approche graphique de l’analyse en ACP des ETM dans les eaux. A : Répartition de l’inertie des ETM dans l’eau entre les deux axes F1XF2. B : Représentation graphique de l’analyse en ACP des ETM dans l’eau. Carte factorielle des variables. C : Représentation graphique de l’analyse en ACP des ETM dans l’eau. Variation spatiale. D : Représentation graphique de l’analyse en ACP des ETM dans l’eau. Variation saisonnière. ... 109 Figure 46 : Représentation graphique de l’analyse en ACP de la dynamique marégraphique des ETM dans l’eau à MH et à MB (A-B : axes d’inertie, C-D: cercles de corrélation des variables, E-F : cartes factorielles des stations). ... 112 Figure 47 : Représentation graphique de l’évolution spatiale de la dynamique de l’hydrosystème de la qualité des ETM dans l’eau de l’estuaire du bas Loukkos pour chaque campagne pendant les deux cycles (MH et MB). .. 114 Figure 48 : Teneurs métalliques moyennes en Fe, Zn, Cu, Cr, Pb et Cd dans les différents organes de Pagellus acarne exprimées en µg/g du poids frais (n=30). ... 122
Figure 49 : Organotropisme de métaux étudiés (Fe, Zn, Cu, Cr, Pb et Cd) exprimés en µg/g du poids frais dans les organes de poissons Pagellus acarne. ... 125
xiv
Figure 50 : Représentation graphique de l’analyse en ACP des ETM dans les organes des Pagellus acarne. -A : Répartition de l’inertie entre les deux axes (F1XF2). -B : Cycle de corrélation des variables. -C : Carte factorielle des organes [B : branchies, F : foie et M : muscles]. -D : Carte factorielle des saisons [O : novembre, N : janvier, R : mars et A : mai]. ... 126 Figure 51 : Teneurs métalliques moyennes en Fe, Zn, Cu, Cr, Pb et Cd dans les différents organes de Sardina pilchardus exprimées en µg/g du poids frais (n=30). ... 129
Figure 52 : Organotropisme de métaux étudiés (Fe, Zn, Cu, Cr, Pb et Cd) exprimés en µg/g du poids frais dans les organes de poissons Sardina pilchardus. ... 132 Figure 53 : Représentation graphique de l’analyse en ACP des ETM dans les organes des Sardina pilchardus. -A : Répartition de l’inertie entre les deux axes. -B : Cycle de corrélation. -C : Carte factorielle des organes. -D : Carte factorielle des saisons. ... 133 Figure 54 : Teneurs métalliques moyennes en Fe, Zn, Cu, Cr, Pb et Cd dans les différents organes de Diplodus vulgaris exprimées en µg/g du poids frais (n=30). ... 136
Figure 55 : Organotropisme des métaux étudiés (Fe, Zn, Cu, Cr, Pb et Cd) exprimés en µg/g du poids frais dans les différents organes chez Diplodus vulgaris. ... 138 Figure 56 : Représentation graphique de l’analyse en ACP des ETM dans les organes des Diplodus vulgaris. -A : Répartition de l’inertie entre les deux axes. -B : Cycle de corrélation. -C : Carte factorielle des organes. -D : Carte factorielle des saisons. ... 139 Figure 57 : Teneurs métalliques moyennes des éléments étudiés (Fe, Zn, Cu, Cr, Pb et Cd) dans les différents organes de Liza ramada exprimées en µg/g du poids frais (n=60). ... 142 Figure 58 : Organotropisme des métaux étudiés exprimés en µg/g du poids frais dans les différents organes chez Liza ramada. ... 144
Figure 59 : Représentation graphique de l’analyse en ACP des ETM dans les organes des Liza ramada. -A : Répartition de l’inertie entre les deux axes. -B : Cycle de corrélation. -C : Carte factorielle des organes. -D : Carte factorielle des saisons. ... 145 Figure 60 : Teneurs métalliques moyennes en (Fe, Zn, Cu, Cr, Pb et Cd) dans les différents organes de Barbus callensis exprimées en µg/g du poids frais (n= 40). ... 148
Figure 61 : Organotropisme des métaux étudiés exprimés en µg/g du poids frais dans les différents organes chez Barbus callensis. ... 151
Figure 62 : Représentation graphique de l’analyse en ACP des ETM dans les organes des Barbus callensis. -A : Répartition de l’inertie entre les deux axes. -B : Cycle de corrélation. -C : Carte factorielle des organes. -D : Carte factorielle des saisons. ... 152 Figure 63 : Organotropisme des teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans les branchies chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 157 Figure 64 : Organotropisme des teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans le foie chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 157
xv
Figure 65 : Organotropisme des teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans les muscles chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 158 Figure 66 : Teneurs métalliques moyennes (Fe, Zn, Cu, Cr, Pb et Cd) exprimées en µg/g du poids frais dans tous les organes (B, F et M) chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 159 Figure 67 : Facteur d’enrichissement (concentration du métal dans les branchies/concentration du métal dans les muscles) chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 161 Figure 68 : Facteur d’enrichissement (concentration du métal dans le foie/concentration du métal dans les muscles) chez les cinq espèces de poissons étudiées (PA, SP, DV, LR et BC). ... 162 Figure : 69 : Teneurs métalliques moyennes en Fe, Zn, Cu, Cr, Pb et Cd dans l’espèce AA exprimées en µg/g du poids sec (n=225). ... 165 Figure 70 : Organotropisme de métaux étudiés dans l’espèce AA. ... 167 Figure 71. Approche graphique de l’ACP des ETM dans les AA. -A : Répartition de l’inertie entre les axes. -B : Cercles de corrélation des variables. -C et D : Carte factorielle des stations et des campagnes. ... 169
Liste des photos
Photo 1 : Barrage de garde sur l’Oued Loukkos ... 23 Photo 2 : Rejets des rizicultures. ... 23 Photo 3 : Pagellus acarne de la côte atlantique marocaine. ... 119 Photo 4 : Sardina pilchardus de la côte atlantique marocaine. ... 120 Photo 5 : Diplodus vulgaris de la côte atlantique marocaine. ... 120 Photo 6 : Liza ramada de l’estuaire du bas Loukkos. ... 120 Photo 7 : Barbus callensis de l’estuaire du bas Loukkos. ... 121 Photo 8 : Civelles l’estuaire du bas Loukkos. ... 121
Liste des annexes
1- Paramètres physicochimiques de l’eau ... 212
Annexe tab. 1 : Evolution spatiotemporelle des paramètres physicochimiques de l’eau. ... 212 Annexe tab. 2 : Evolution globale des paramètres physico-chimiques de l’eau étudiée. ... 214
xvi
Annexe tab. 3 : Ratios de paramètres globaux de la pollution des eaux des l’estuaire du bas Loukkos. ... 215 Annexe tab. 4 : Evolution spatio-temporelle des paramètres physico-chimiques de l’eau de l’estuaire du bas Loukkos (MH et MB). ... 215 Annexe tab. 5 : Caractéristiques hydrologiques lors de la MH et MB. ... 217 Annexe tab. 6: Date des campagnes de prélèvement des échantillons d’eau à MH. ... 217 Annexe tab. 7 : Valeurs brutes des paramètres physicochimiques de l’eau étudiés lors de la MH. ... 217 Annexe tab. 8 : Date des campagnes de prélèvement des échantillons d’eau à MB. ... 217 Annexe tab. 9 : Valeurs brutes des paramètres physicochimiques de l’eau étudiés lors de la MB. ... 217 Annexe tab. 10 : Les relevés hydrologiques pendant les deux cycles. ... 218 Annexe tab. 11 : Valeurs brutes des paramètres hydrologiques de l’estuaire du bas Loukkos pour chaque campagne. ... 218
2- Contamination métallique des sédiments ... 220
Annexe tab. 12 : Teneurs en métaux des différents échantillons de sédiments de différentes stations exprimées en µg/g du poids sec sauf Fe en mg/g de l’estuaire du bas Loukkos durant l’année 06/07 (n=30, moyenne±écart-type, valeurs limites). ... 220 Annexe tab. 13 : Date des campagnes de prélèvement des échantillons des sédiments (MH). ... 220 Annexe tab. 14 : Teneurs des ETM dans les sédiments à MH. ... 221 Annexe tab. 15 : Date des campagnes de prélèvement des échantillons des sédiments à MB. ... 221 Annexe tab. 16 : Teneurs des ETM dans les sédiments à MB. ... 221 Annexe tab. 17 : Valeurs brutes des ETM mesurées dans les sédiments de l’estuaire du bas Loukkos pour chaque campagne exprimés en µg/g du poids sec sauf Fe en mg/g durant les deux cycles de marées (MH/MB). ... 222
3- Contamination métallique des eaux ... 222
Annexe tab. 18 : Date des campagnes de prélèvement des échantillons d’eau à MH. ... 222 Annexe tab. 19 : Teneurs des ETM dans les eaux à MH. ... 223 Annexe tab. 20 : Date des campagnes de prélèvement des échantillons d’eau à MB. ... 223 Annexe tab. 21 : Teneurs des ETM dans les eaux à MB. ... 223 Annexe tab. 22 : Les valeurs brutes des ETM mesurées dans l’eau de l’estuaire du bas Loukkos pour chaque campagne (n=30) exprimée en (µg/l) durant les deux cycles de marées (MH/MB). ... 224
xvii
4- Contamination métallique des poissons ... 224
Annexe tab. 23 : Teneurs brutes des ETM chez Pagellus acarne (n=30) exprimés en µg/g du poids frais. ... 224 Annexe tab. 23 : L’ACP chez Pagellus acarne (suite). ... 225 Annexe tab. 24 : Teneurs brutes des ETM chez Sardina pilchardus (n=30) exprimés en µg/g du poids frais. .. 225 Annexe tab. 24 : L’ACP chez Sardina pilchardus (suite). ... 226 Annexe tab. 25 : Teneurs brutes des ETM chez Diplodus vulgaris (n=30) exprimés en µg/g du poids frais. .... 226 Annexe tab. 25 : L’ACP chez Diplodus vulgaris (suite). ... 227 Annexe tab. 26 : Teneurs brutes des ETM chez Liza ramada (n=60) exprimés en µg/g du poids frais. ... 227 Annexe tab. 26 : L’ACP chez Liza ramada (suite). ... 229 Annexe tab. 27 : Teneurs brutes des ETM chez Barbus callensis (n=40) exprimés en µg/g du poids frais. ... 229 Annexe tab. 27 : L’ACP chez Barbus callensis (suite). ... 231 Annexe tab. 28 : Teneurs brutes des ETM chez Anguilla anguilla (n=225) exprimés en µg/g du poids sec. ... 231
Liste des abréviations AA : Espèce de poisson migrateur AA.
ACP: Analyse en Composantes Principales, Principal Components Analysis. AFD: Analyse Factorielle Discriminante, Discriminant Factor Analysis.
BCR: Bureau des Communautés de Références, Office of the Communities of References. COSIMA : Construction spéciale pour l’irrigation au Maroc,
CRM: Matériaux de Référence Certifiés, Certified Reference Material. ETM: Elément Trace Métallique, Traces Metal Element.
FBC : Facteur de bioconcentration=teneur du métal dans l’organisme/celle dans l’eau. MES: Matières En Suspension, Suspended Matter.
MO: Matière Organique, Organic Matter. NO: Nord-Ouest, North-West.
NE: Nord-Est, North-East.
OMS : Organisation mondiale de la santé.
PC: Composante Principale, Principale Component. P.E : présente étude, present study.
xviii
SAA: Spectrométrie d‘Absorption Atomique, Atomic Absorption Spectrometry.
SAAF: Spectrométrie d‘Absorption Atomique en Flamme, Atomic Absorption Spectrometry. with
Flames.
UNEP: Programme des Nations Unies pour l‘Environnement, United Nations Environment
Programme.
PPCE : Paramètres physico-chimiques de l’eau, physical and chemical parameters in the water. SUCRAL : Sucrerie raffinerie de canne du Loukkos.
SUNABEL : Sucrerie nationale de betterave du Loukkos. SURLOUK : Surgélation du Loukkos.
Pt : Phosphore : élément chimique présent dans les engrais chimiques et dans certains composés
organiques.
CF : Micro-organisme en bâtonnets, capable de vivre en aérobiose en milieu liquide. Ce sont des
bons indicateurs de la contamination fécale d’une eau.
GLOSSAIRE
Accumulation : C’est la capacité qu’à une substance tels les métaux lourds, de se fixer dans un
compartiment donné (sédiment) à des concentrations supérieures aux valeurs naturelles.
Bio-accumulateur : Organisme (animal ou végétal) capable de retenir des traces infimes de
polluants présents dans l'air, le sol ou l'eau et de les accumuler à des doses bien supérieures à celles auxquelles elles se rencontrent dans les milieux.
Biomarqueur : Un changement observable et : ou mesurable au niveau moléculaire, biochimique,
cellulaire, physiologique ou comportemental, qui révèle l’exposition présente ou passée d’un individu à au moins une substance chimique à caractère polluant.
Carburateur : Pièce du moteur procédant au mélange de l'air et du carburant avant explosion. Catalyseur : Corps qui rend possible ou accélère une réaction chimique, sans subir de
modification.
Charge critique : Valeur d'exposition à un ou plusieurs polluants en dessous de laquelle des effets
significatifs sur l'environnement n'apparaissent pas en l'état actuel de nos connaissances.
Composés organiques volatils : Composés organiques gazeux que l'on rencontre dans l'atmosphère,
dont les principaux sont des hydrocarbures.
Cd : Cadmium, élément métallique
Contamination : On parle de contamination lorsque les concentrations en une substance donnée
(physique, chimique et biologique) avoisinent ou dépassent les normes admises.
xix
Cu : Cuivre, élément métallique
DCO (demande chimique en oxygène) : La mesure du taux d’oxygène nécessaire à l’oxydation de
tous les composés (organiques et inorganiques), dans l’eau.
Écosystème : Association, stable dans le temps, entre un environnement physico-chimique
spécifique (le biotope) et un ensemble d'espèces animales et végétales (la biocoenose).
Effets biologiques : Le terme d’effets biologiques désigne toute perturbation, aussi bien au niveau
cellulaire (biomarqueurs), au niveau de l’individu qu’au niveau de la population, permettant à la fois le suivi dans l’espace et dans le temps de la réponse des organismes à la pression toxique du milieu et à la mise en relation des sources polluantes et des effets enregistrés.
Effluent : terme général désignant les eaux (généralement altérées par une pollution organique,
chimique, thermique…) sortant de chez un usager.
Granulométrie : Dimension des grains, se dit aussi de la méthode de classement des matières selon
la proportion de grains de différentes tailles qui les composent.
Histogramme : Représentation graphique par rectangles dont la hauteur est proportionnelle à chaque
valeur de la fonction étudiée.
HAP : Hydrocarbures aromatiques polycycliques Hg : Mercure, élément métallique
IdC : Indice de différenciation du comportement.
Indicateur d'exposition : Donnée significative du niveau d'exposition à un polluant.
Microgramme par mètre cube (µg/m3) : Concentration d'un millionième de gramme par mètre
cube.
MES (matières en suspension) : Ensemble des particules solides de petite taille transportées au sein
de la masse d’eau.
Métaux lourds : Éléments métalliques dont le nombre atomique est généralement supérieur à 20
(mercure, plomb, cadmium...). Ils peuvent induire des dommages à de faibles concentrations, et tendent à s’accumuler dans la chaîne alimentaire.
Nitrates : NO3- : Stade final de l’oxydation de l’azote.
Oxydation : Réaction chimique de combinaison d'un corps avec l'oxygène.
Oxydes d'azote (NOx) : Mélange, en proportions variables, de monoxyde d'azote (NO) et de
dioxyde d'azote (NO2). Seul le dioxyde d'azote est un polluant réglementé, du fait de ses effets sur la santé.
Polluant secondaire : Polluant produit par l'interaction chimique de polluants primaires dans
l'atmosphère, par exemple l'ozone.
xx
Ppm (parties par million) : Concentration d'un pour un million. Pb : Plomb, élément métallique
Pesticides : Produits chimiques utilisés en agriculture pour lutter contre les insectes, moisissures,
mauvaises herbes, acariens, vers...
Polluants chimiques : Le terme de polluants chimiques désigne l’ensemble des composés toxiques
(métalliques et organiques) libérés dans le milieu; mais aussi les substances qui, sans être vraiment dangereuses pour les organismes, exercent une influence perturbatrice sur l’environnement.
Ressources en eau : Disponibilité en eau souterraine ou superficielle, renouvelée par le cycle naturel
de l’eau.
Sédimentation : Processus de dépôt de particules sur une surface.
Substrat : Support stable d'un phénomène, d'une réaction chimique par exemple.
Toxicité : Capacité propre d’une substance ou d’un milieu complexe de provoquer des effets nocifs
chez les organismes vivants.
Toxicité sublétale : Ensembles des premiers effets (physiologiques, biochimiques,
histopathologiques et comportementaux) d’une substance ou d’un effluent sur différentes fonctions d’un organisme, ou d’un ensemble d’organismes (population), se situant en dessous des effets létaux (mortels).
Valeur limite : voir tableau des valeurs de référence, avec définitions, au début du chapitre : "2.
1
INTRODUCTION GENERALE
Depuis plus de cinquante ans, la pollution est l'un des plus graves problèmes auxquels
est confronté notre monde moderne. On entend par pollution, la présence dans l'environnement des grandes quantités de produits chimiques dangereux, généralement crées par l'homme, dont les effets nuisibles peuvent se faire durant de longues périodes sur toute la planète. Cette pollution peut affecter l'eau, l'air et la terre. Elle peut être évidente (nappes d'hydrocarbures flottante sur la mer). Comme elle peut être beaucoup moins visible (pesticides répandus sur les champs ou métaux lourds dissous dans les systèmes aquatiques).
Le 20ème siècle voit de plus apparaître des quantités de substances nouvelles totalement étrangères au milieu naturel dont la dégradation et l’assimilation par la faune et la flore sont inefficace. C’est ainsi que, les pollutions apparaissent actuellement d’origine et de nature de forme et d’actions multiples et se révèlent comme un problème majeur de notre temps. Les différentes dégradations résultant de la pollution de l’écosphère compromettent l’équilibre des écosystèmes concernés, le renouvellement des ressources naturelles ainsi que le bien être et la santé de la population humaine.
Les déversements dans les cours d'eau atteignent, de nos jours, des proportions
catastrophiques. Par mesure d'économie, usines et villes rejettent directement leurs eaux résiduaires, sans les avoir traitées au préalable. Il y a aussi des produits toxiques qui aboutissent dans les rivières, tuant de nombreuses formes de vie. Parmi ces polluants, citons le chrome, en provenance des tanneries, des margines et des huileries; le mercure, en provenance des usines de pâte à papier. La flore et la faune aquatique peuvent dans ce cas s'appauvrir de façon considérable, non seulement quantitativement mais aussi qualitativement.
L’écosystème aquatique est de plus en plus menacé par différentes sources de
pollution qui risquent de diminuer ses potentialités économiques et d’avoir des répercussions néfastes sur la santé humaine. Plus que jamais, en cette fin de millénaire, la lutte contre la pollution des eaux est au centre des discussions et des débats à l’échelle mondiale. Des centaines de titres consacrés à ce sujet ont pu être relevés dans la presse, des centaines de colloques, rencontres, congrès se sont déroulés pour en débattre, sans oublier les campagnes de sensibilisation sur les graves problèmes de pollution subis par les différents écosystèmes. Parmi les substances chimiques susceptibles de constituer un danger pour la vie aquatique en général, nous signalons les métaux lourds dont certains comme le chrome, le plomb et le cadmium. Ces éléments sont très toxiques et de plus en plus utilisés dans les secteurs industriels. Certains métaux non toxiques le deviennent vu leur pouvoir bio-accumulateur et
2
leur rémanence dans le milieu aquatique et notamment dans les sédiments compte tenu de leur non dégradation biologique.
Le Maroc compte parmi les pays d’Afrique les plus menacés par la déficience des
ressources en eau suite à la sécheresse qui frappe de plus en plus durement de nombreuses Régions. Les réserves hydriques s’avèrent insuffisantes tant en milieu urbain qu’en milieu rural. Devant cette situation s’imposent donc la préservation et l’optimisation du potentiel hydrique de notre pays, avec le développement de l’insuffisance d’une législation et son application stricte qui régisse le contrôle de la pollution rejetée dans le milieu naturel sans aucun traitement préalable.
Au Maroc, l’approche environnementale est devenue un enjeu autant écologique
qu’économique surtout avec ses ressources naturelles fragiles et limitées. La situation est d’autant plus grave car le Maroc est en déficit hydrique depuis plusieurs décennies. En effet selon le rapport mondial de mise en valeur des ressources en eau des nations unies, de nombreux pays dont le nôtre, sont déjà en situation de crise. Avec 971 m3 /hab. /an, le Maroc est classé au rang 155 par rapport à 180 pays.
Le Maroc est confronté à des problèmes environnementaux, parfois assez sérieux.
Cette situation est due à une forte croissance démographique, une urbanisation galopante et une gestion insuffisamment prévoyante des ressources pour satisfaire les besoins générés par le développement économique.
Aussi les ressources en eau au Maroc sont confrontées à des problèmes de quantités et
de qualités. Ces ressources sont limitées en raison du climat semi-aride et aride et subissent une détérioration de leur qualité par les différents rejets polluants, telles que les eaux usées (Serghini, 2003 ; El Morhit, 2005).
Au Maroc, quelques travaux ont été menés sur la détermination des niveaux
métalliques chez les moules et les poissons prélevés de la côte atlantique (Mahyaoui et al., 1989 ; Alaoui Hassani, 1991 et Chafai Alaoui, 1994 ; Cheggour et al., 2005) et de la côte méditerranéenne (Sabhi, 1990 ; El Hraiki et al., 1992 ; El Morhit, 2005 ). Ces travaux ont montré que les connaissances acquises sur le Maroc sont fragmentaires d’où la nécessité d’étudier de manière régulière, précise et plus concrète la présence des métaux lourds dans les divers compartiments du milieu aquatique.
Dans le cadre de la recherche sur l’environnement littoral et marin de la côte atlantique
marocaine, une contribution intéressante nous a paru envisageable, par l’étude de l’origine et du devenir des polluants dans l’estuaire du bas Loukkos où sont déversés de nombreux rejets
3
(industriels, urbains, agricoles…). Ce qui n’est pas sans conséquence, à plus au moins long terme, sur la qualité du milieu estuarien de la région.
L’oued Loukkos, l’une des principales rivières du Maroc traversant plusieurs villes en
particulier la ville de Larache et débouchant sur l’océan, connaît depuis plusieurs années, une dégradation notable de la qualité de ses eaux engendrées par différents rejets de polluant émis sans traitement dans la rivière. Ces rejets résultent de différentes activités urbaines, industrielles et agricoles que connaît ce bassin. Parmi les formes de pollution que connaissent les eaux de ce fleuve, apparaissent les métaux lourds qui résultent des rejets émis par différentes industries et unités artisanales le long de l’oued. Vu la diversification des produits chimiques utilisés dans les agricoles, les effluents de ces unités sont caractérisés par une pollution chimique.
La caractérisation mésologique hydro-chimique permet donc d’évaluer la qualité des
eaux superficielles. Elle constitue l’une des composantes principales dans toute étude du fonctionnement des écosystèmes aquatiques, plus particulièrement celle qui intéresse les milieux paraliques soumis à la double influence océanique et continentale. En effet, l’hydro-chimique de l’estuaire du bas Loukkos est la résultante des flux marégraphiques océaniques et des apports d’eaux douces de l’oued Loukkos.
C’est dans ce contexte que nous avons entrepris l’étude de l’écosystème aquatique de
l’estuaire du bas Loukkos; la présente étude vient compléter et apporter des éléments nouveaux aux travaux antérieurs réalisés par Snoussi (1984) ; Cheggour et al. (2004) ; Bazairi et al. (2005) ; Fekhaoui (2005) ; El Morhit et al. (2008). Le chois a été motivé par l’importance socioéconomique que représente cet écosystème pour la région de la ville de Larache et par la forte pression que subit celui-ci en matière de pollution. En effet ce secteur continue à recevoir beaucoup de rejets polluants à cause de nombreuses agglomérations et unités industrielles installées sur ses rives et ses affluents. Par ailleurs, l’emploi non raisonnées des fertilisants et d’engrais dans cette région très agricole ne fait qu’accentuer la pollution et augmenter le risque de contamination des eaux superficielles et profondes de cet écosystème.
L’essor démographique important qu’a connu la ville de Larache et l’accroissement des activités industrielles donnent aux eaux d’origine domestique ou industrielle une importance particulière. Leurs rejets dans la zone estuarienne peuvent modifier la qualité du milieu et empêcher et freiner le développement de certaines activités. Dans ce contexte, nous nous sommes intéressés à évaluer l’état de salubrité de l’estuaire du bas Loukkos.
4
Le contrôle des métaux lourds dans l’environnement a acquis une importance croissante durant les dernières années. Dans ce contexte, la présente étude consiste à :
Etudier la qualité des eaux superficielles de l’estuaire du bas Loukkos par le suivi spatio-temporel d’un certain nombre de traceurs physicochimiques. Les résultats préliminaires seront synthétisés par une analyse multivariée (ACP) afin de comprendre le fonctionnement de cet hydro-système et le conditionnement de la charge polluante en fonction de la dynamique marégraphique.
évaluer la contribution à l’étude de la pollution métallique de l’estuaire du bas Loukkos de la Région de Larache (nord du Maroc) à travers le suivi spatio-temporel de la contamination de l’eau, des sédiments et de poissons par six ETM. L’utilisation d’indices de contamination s’avère d’un emploi judicieux.
réaliser une étude marégraphique dans les stations de l’estuaire étudié.
La présente étude est constituée de la première partie comprend deux chapitres: Chapitre I : Milieu d’étude, sa situation géographique et ses principales sources de pollution et Chapitre II : Matériels et méthodes: consacrée à la présentation des stations de prélèvement, échantillonnages, prélèvement et les analyses physico-chimiques et la deuxième partie (Résultats et Discussions) comprend quatre chapitres: Chapitre I : Qualité des paramètres physicochimiques de l’eau, Chapitre II : Etude de la contamination métallique des sédiments et Chapitre III : Etude de la contamination métallique des eaux et Chapitre IV : Etude de la contamination métallique des poissons.