Faisabilité du traitement des eaux d’un oued chargé en éléments traces métalliques (ETM )par filtres plantés de macrophytes (phragmites australis) : cas de l’oued Meboudja – Annaba – Algerie
230
0
0
Texte intégral
Figure
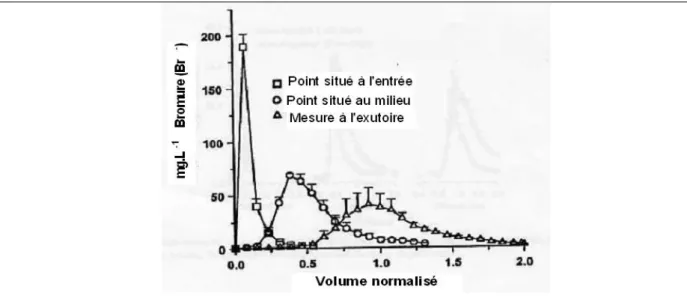
+7
Outline
Documents relatifs