Université de Montréal
Luminogènes-AIE à base de ligands hydroxyamidines : Synthèse,
caractérisation et application comme pigments pour dispositifs
OLED
par Jessica Julieth Castro
Département de Chimie Faculté des Arts et des Sciences
Mémoire présenté
en vue de l’obtention du grade de Maître ès Sciences M.Sc. en chimie
Août 2018
Résumé
Les dispositifs OLED (organic light-emitting diode) sont capables de la transduction efficace de l’énergie électrique en lumière; par leur flexibilité, leur légèreté et leur très haute qualité de couleurs elles sont aussi d’intérêt pour l’affichage sophistiqué sur écran plat. Cependant, l'emploi de cette technologie se voit ralenti par le cout élevé des matériaux et des méthodes de fabrication utilisés. Le but de cette recherche est de trouver des pigments pour OLED moins dispendieux tout aussi efficaces qui pourraient en même temps faciliter les méthodes de fabrication des dispositifs. Dans ce projet, on a développé une nouvelle série des ligands benzamidine-N-oxyde (AMOX) bidentés de type N,O capables d’émission induite par agrégation moléculaire (AIE) lorsque complexés à un centre cationique. L’AIE permet aux molécules non-émissives en solution de devenir intensément luminescentes à l’état solide. Les matériaux luminogènes AIE représentent une catégorie de pigments d’intérêt pour les dispositifs
OLED puisque ces derniers fonctionnent selon le principe d’émission à l’état solide. Les
propriétés AIE sont déclenchées par la rigidité accrue du cœur O-N-C=N du ligand avec la formation des complexes. La chimie de coordination nous permet d’utiliser les ligands et les centres métalliques comme des blocs de construction pour obtenir des complexes AIE avec des caractéristiques structurelles et photo-physiques très intéressantes. On additionne à cela la facile modulation des facteurs électroniques et stériques des complexes à base des ligands AMOX par la modification structurelle des ligands avec l’ajout des substituants. Exploiter cette propriété permettrait de varier la couleur d’émission des pigments. Finalement, en utilisant des centres cationiques à partir d’éléments abondants et peu toxiques les coûts de production et l’impact environnementale peuvent être réduits ouvrant ainsi la porte à la commercialisation d’une technologie durable et rentable.
Mots-clés : chimie de coordination, zinc, aluminium, bore, ligands N,O-donneurs, amidine N-oxyde, hydroxyamidine, benzamidine N-N-oxyde, substituants, isomérie, interactions électrostatiques, émission à l’état solide, morphologie, émission induite par agrégation moléculaire, AIE, AIEE, CIEE, mécanochromisme, vapochromisme, thermochromisme, OLED,
iii
Abstract
OLEDs (organic light-emitting diode) are able to transduce electrical energy efficiently into light and because of their flexibility, lightness and high-quality colors, they can also be used in flat-screen display applications. However, the commercialization of this technology is slowed-down by the high cost of the materials and the complex methods that are used for the device fabrication. The purpose of this research is to find low-cost affordable dyes for OLEDs with good energy efficiency characteristics that can be integrated in the device by less complex fabrication methods. In this project, we developed a new series of N,O bidentate benzamidine N-oxide ligands for aggregation-induced emission characteristics (AIE) through complexation. AIE is the non-emissive molecules in solution that luminesce in the solid state. AIE luminigens are a new category of dyes for solid state emission in optoelectronic devices. AIE characteristics can be triggered by the coordination of cationic center, which rigidify the O-N-C=N backbone of the ligand. Coordination chemistry allows the use of ligands and metallic centers as element-blocks for the construction of AIE complexes that have interesting structural and photophysical properties. In addition to this, the tunability of electronic properties and sterics of the complexes with AMOX ligands can be easily obtained by modifying the ligand with the addition of substituents. This would allow to vary the emission color of the dyes. Finally, by using cationic centers from less toxic earth-abundant elements, the production-cost and the environmental impact of this technology can be reduced, thus, opening a door to the commercialization of a sustainable and cost-effective lighting technology.
Keywords : coordination chemistry, zinc, aluminum, boron, N,O ligands, amidine N-oxide, hydroxyamidine, benzamidine N-oxide, substituents, isomerism, electrostatic interactions, solid state emission, morphology, aggregation-induced emission, AIE, AIEE, CIEE, mechanochromism, vapochromism, thermochromism, OLED, WOLED.
Table des matières
Résumé ... ii
Abstract ... iii
Table des matières ... iv
Liste des tableaux ... viii
Liste des sigles et abréviations ... xii
Remerciements ... xvi
Chapitre 1 : Introduction ... 2
Partie 1. Efficacité énergétique et développement des technologies écologiques. ... 2
1.1 Contexte général : L’énergie ... 2
1.1.1 Demande énergétique globale. ... 2
1.1.2 L’éclairage ... 6
1.1.3 Principe de fonctionnement des dispositifs OLED ... 12
1.1.4 Utilisation des complexes organométalliques dans les dispositifs OLED ... 16
1.1.5 Les défis ... 18
1.1.6 Bibliographie ... 20
Partie 2. Phénomène d’émission induite par agrégation moléculaire (AIE) des complexes à base de ligands AMOX ... 25
1.2 L’AIE ... 25
1.2.1 Introduction et mécanisme ... 25
1.2.2 Design moléculaire ... 27
1.2.3 Applications ... 28
1.3 Contexte spécifique : Développement de nouveaux pigments AIE pour dispositifs OLED à base de complexes de coordination des ligands Amidine-N-Oxides. ... 30
v
1.3.1 Cadre théorique ... 30
1.3.2 Méthodologie ... 35
1.3.3 Bibliographie ... 37
Chapitre 2 : Complexes de zinc(II) avec de ligands N,N’-diphénylbenzamidines-N-oxides - Synthèse, caractérisation et application WOLED. ... 39
2.1 Introduction ... 39 2.2 Résultats et discussion ... 40 2.2.1 Synthèse ... 40 2.2.2 Caractérisation. ... 43 2.3 Application OLED ... 56 2.3.1 Fabrication du dispositif ... 56 2.3.2 Propriétés d’électroluminescence ... 57 2.4 Conclusion ... 58 2.5 Bibliographie ... 60
Chapitre 3 : Complexes d’aluminium (III) à base de ligands N,N’-diphénylbenzamidines-N-oxides - Synthèse, caractérisation et application WOLED. ... 63
3.1 Introduction ... 63 3.2 Résultats et discussion ... 64 3.2.1 Synthèse ... 64 3.2.2 Caractérisation ... 66 3.3 Application OLED ... 81 3.3.1 Fabrication du dispositif ... 81 3.3.2 Propriétés d’électroluminescence ... 81 3.4 Conclusion ... 83
3.5 Bibliographie ... 85
Chapitre 4 : Composés de bore tétracoordonés à base de ligands N,N’-diphénylbenzamidines-N-oxides - Synthèse, caractérisation et application OLED. ... 88
4.1 Introduction ... 88 4.2 Résultats et discussion ... 89 4.2.1 Synthèse ... 89 4.2.2 Caractérisation ... 90 4.3 Application OLED ... 105 4.3.1 Fabrication du dispositif ... 105 4.3.2 Propriétés d’électroluminescence ... 106 4.4 Conclusion ... 109 4.5 Bibliographie ... 111
Chapitre 5 : Conclusion générale ... 114
5.1 Dernières remarques ... 114
5.2 Perspectives ... 115
5.3 Bibliographie ... 119
Chapitre 6 : Annexes ... 121
6.1 Procédures expérimentales générales ... 121
6.2 Feuilles de synthèse et caractérisation ... 124
6.3 Spectres RMN ... 170
6.4 Spectres FT-IR ... 222
6.5 Spectres d’absorbance UV-Vis ... 243
6.6 Spectres d’émission à l’état solide ... 264
vii
6.8 Diffraction de rayons X sur monocristal ... 306
6.9 Diffraction de rayons X sur poudre ... 343
6.10 Résultats de calculs DFT/TDDFT ... 351
Liste des tableaux
Tableau I. Rendement isolé de la synthèse des complexes de Zn(II) avec des ligands N,N’-diphenylbenzamidines-N-oxides. ... 42 Tableau II. Morphologie des cristaux formés par les complexes de Zn(II) avec des ligands
N,N’-diphenylbenzamidines-N-oxides selon la méthode de synthèse utilisée. ... 43
Tableau III. Données spectroscopiques[a], électrochimiques[b] et théoriques [c] des complexes de Zn(II) à l’étude. ... 52 Tableau IV. Rendement isolés de la synthèse des complexes d’Al(III) avec des ligands
N,N’-diphenylbenzamidines-N-oxides. ... 65
Tableau V. Données spectroscopiques[a], électrochimiques[b] et théoriques [c] des complexes Al(AMOX)3 à l’étude. ... 74 Tableau VI. Rendements isolés de la synthèse des complexes B(AMOX)Ph2. ... 90 Tableau VII. Données spectroscopiques[a], électrochimiques[b] et théoriques[c] des complexes B(AMOX)Ph2 à l’étude. ... 95
ix Liste des figures
Figure 1. Contribution selon le type de carburant au total des ressources en énergie
primaire mondiales (TPES). ... 4
Figure 2. Contribution anthropique mondiale des gaz à effet de serre selon secteur en 2014. ... 5
Figure 3. Carte composite du monde réalisée à partir des données acquises par le satellite de la centrale de Suomi en avril et octobre 2012. ... 6
Figure 4. Consommation d’énergie par ménage et consommation d’énergie totale pour l’éclairage pour la période de 1990-2013. ... 7
Figure 5. Représentation de l’émission dans un dispositif LED. ... 9
Figure 6. Structure chimique des isomères méridional et facial du complexe Alq3 tris(8-hydroxyquinoléine) aluminium(III). ... 10
Figure 7. Structure générale d’un dispositif OLED.. ... 13
Figure 8. Mobilité de charges dans le dispositif OLED. ... 13
Figure 9. Représentation des mécanismes de transfert d’énergie Förster et Dexter. ... 15
Figure 10. Probabilités de radiation d’un exciton selon sa multiplicité. ... 16
Figure 11. Représentation des excimères et électromères. ... 19
Figure 12. Différence entre ACQ et AIE... 26
Figure 13. Comportement ACQ du complexe Alq3. ... 27
Figure 14. Exemples de molécules ACQ et AIE. ... 28
Figure 15. Synthèse générale des ligands AMOX. ... 30
Figure 16. Famille de ligands AMOX à l’étude. ... 31
Figure 17. Synthèse des complexes Zn(AMOX)2 et Zn2(AMOX)2. ... 40
Figure 18. Exemple de complexes Zn(AMOX)2 avec des ligands AMOX N,N’-disubstitutées. ... 41
Figure 19. Synthèse des complexes de Zn(II) avec des ligands N,N’-diphenylbenzamidines-N-oxides. ... 41
Figure 20. Structure de rayons X du complexe dimérique Zn-D3. ... 44
Figure 21. Structure de rayons X du complexe monomérique Zn-1. ... 45
Figure 22. Structure de rayons X du complexe monomérique Zn-5. ... 45
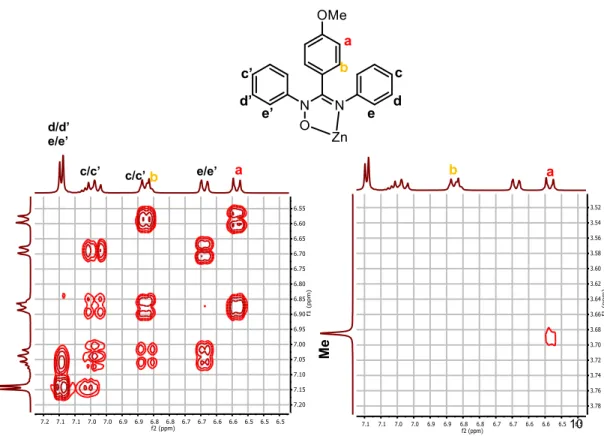
Figure 24. Spectre RMN COSY du complexe Zn-1. ... 47
Figure 25. Spectre RMN 1H des complexes Zn-1, Zn-2, Zn-D3, Zn-4 et Zn-5. ... 48
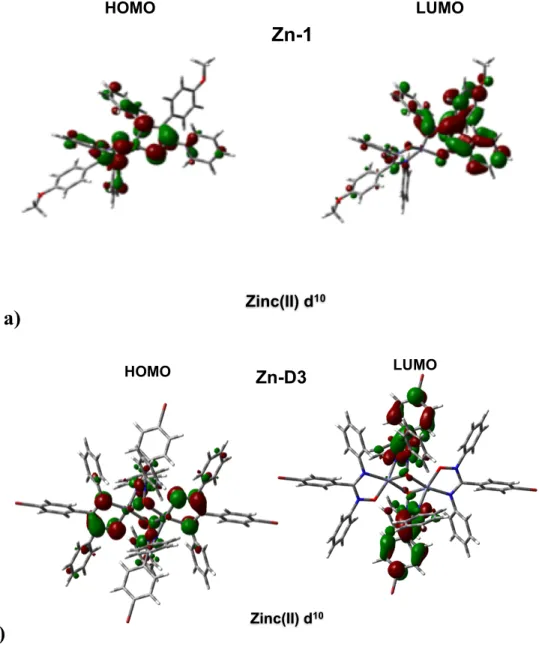
Figure 26. Positionnement des orbitales moléculaires frontière par DFT pour a) Complexe Zn-1 et b) Complexe Zn-D3. ... 50
Figure 27. Spectres d’émission AIE du complexe Zn-2. ... 54
Figure 28. Spectres d’émission AIE du complexe Zn-D3. ... 54
Figure 29. Spectres normalisés d’émission à l’état solide des poudres de complexes Zn-1, Zn-2, Zn-D3, Zn-4, Zn-5. ... 55
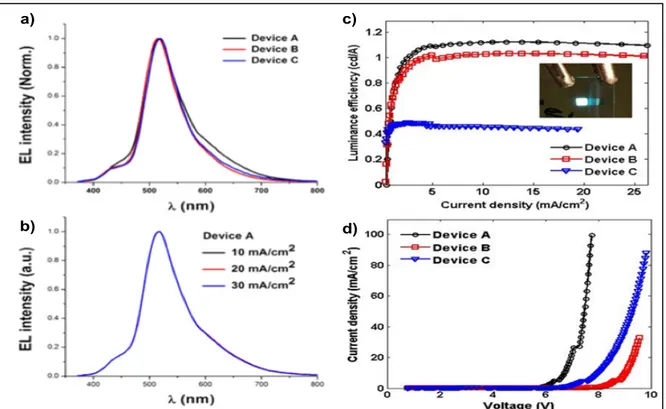
Figure 30. Propriétés d’électroluminescence des dispositifs contenant pigment Zn-D3. . 57
Figure 31. Synthèse des complexes Al(III) avec des ligands N,N’-diphenylbenzamidines-N-oxides. ... 64
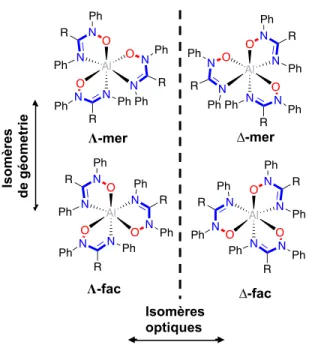
Figure 32. Stéréoisomérie des complexes Al(AMOX)3 ... 66
Figure 33. Structure de rayons X des complexes Al-3 et Al-5. ... 67
Figure 34. Structures de rayons X du complexe Al-2. ... 67
Figure 35. Spectres RMN 1H des complexes Al(AMOX) 3 comparés aux ligands. ... 68
Figure 36. Positionnement des ligands AMOX-1 selon isomérie du complexe Al-1. ... 69
Figure 37. Spectres RMN 1H et 13C du complexe Al-1, complexe Al-1 avec ajout de D 2O et du ligand AMOX-1. ... 70
Figure 38. Possibles produits de l’hydrolyse du complexe Al-1. ... 71
Figure 39. Positionnement des orbitales moléculaires frontière par DFT pour le complexe Al-2. ... 72
Figure 40. Spectres d’émission AIE du complexe Al-3. ... 75
Figure 41. Émission à l’état solide des complexes Al(AMOX)3 sous lampe UV. ... 76
Figure 42. Spectres normalisés d’émission à l’état solide des poudres de complexes Al(AMOX)3 contenant des molécules d’éthanol. ... 77
Figure 43. Spectres normalisés d’émission à l’état solide des poudres de complexes Al(AMOX)3 secs. ... 78
Figure 44. Spectres d’émission normalisés à l’état solide des poudres séchées ou avec des molécules d’éthanol du complexe Al-1. ... 79 Figure 45. Spectres d’émission non-normalisés à l’état solide des poudres séchées ou avec
xi
Figure 46. Propriétés d’électroluminescence du complexe Al-2... 82
Figure 47. Synthèse des complexes B(AMOX)Ph2. ... 89
Figure 48. Structure de rayons X du complexe B-1. ... 91
Figure 49. Motif de diffraction de poudre par rayons X du complexe B-1. ... 92
Figure 50. Spectre RMN 1H des complexes B(AMOX)Ph2. ... 93
Figure 51. Orbitales moléculaires frontière par DFT pour le complexe B-2. ... 94
Figure 52. Comparaison de l’énergie des orbitales moléculaires frontière théoriques et expérimentales des complexes B(AMOX)Ph2. ... 97
Figure 53. Spectres d’émission AIE du complexe B-2. ... 98
Figure 54. Émission à l’état solide des complexes B(AMOX)Ph2 sous lampe UV. ... 99
Figure 55. Spectres normalisés d’émission à l’état solide des poudres cristallines des complexes B(AMOX)Ph2. ... 100
Figure 56. Spectres normalisés d’émission à l’état solide des films amorphes de complexes B(AMOX)Ph2. ... 100
Figure 57. Spectres normalisés d’émission à l’état solide d’une poudre amorphe de complexe B-1. ... 102
Figure 58. Réponse du complexe B-1 aux stimuli physiques externes ... 103
Figure 59. Spectres d’électroluminescence des films bruts du complexe B-1. ... 106
Figure 60. Spectres d’électroluminescence des films dopés du complexe B-1. ... 108
Liste des sigles et abréviations
Å δ D L ФPL A AcOEt ACQ AFM AIE AIEE AMOX ATR B3LPYP BODIPY Cd CDCl3 CIEE COSY D2O DCM DFT DMSO DSC EA E-chem Eq. EQE EtOH Angström Déplacement chimique (ppm) Delta LamdaRendement quantique de photoluminescence Ampères
Acétate d’éthyle
Aggregation-caused quenching Atomic force microscopy Aggregation-induced emission
Aggregation-induced emission enhancement
Hydroxyamidine
Attenuated total refractance
Becke, three-parameter, Lee-Yang-Parr exchange-correlation functional Boron-dipyrromethene
Candela
Chloroforme deuteré
Crystallization-induced emission enhancement Correlation spectroscopy
Deuterium oxide
Dichlorométhane
Density functional theory
Diméthylsulfoxyde
Differential scanning calorimetry
Elemental analysis
Electrochemistry Équation
External quantum efficiency Éthanol
xiii fac FT-IR H Hex HOMO ILCT IQE ISC J LED LMCT LUMO mCP m-CPBA Me MeOH Mer Min MLCT Mtoe NOESY Nm NMR NTO OLED ORTEP Ph ppm PPSE PVK q RISC Facial
Fourier transform infrared
Heure(s) Hexane
Highest occupied molecular orbital Intra-ligand charge transfer
Internal quantum efficiency Intersystem crossing
Constante de couplage
Light-emitting diode
Ligand-to-metal charge transfer Lowest unoccupied molecular orbital
1,3-Bis(N-carbazolyl)benzene Meta-chloroperoxibenzoic acid Méthyle Méthanol Méridional Minute(s)
Metal-to-ligand charge transfer Million tonnes of oil equivalent
Nuclear overhauser effect spectroscopy
Nanomètres
Nuclear magnetic resonance Natural transition orbital Organic light-emitting diode
Oak Ridge Thermal Ellipsoid Program
Phényle
Partie par million
Polyphosphoric acid triméthyle ester
Poly(9-vinylcarbazole) 8-Hydroxyquinoléine
RMN 1S SCE SWV 3T TADF TD-DFT TGA UV V VC Vis WOLED
Résonnance magnétique nucléaire
Singlet excited state
Saturated calomel electrode Square-wave voltammetry Triplet excited state
Thermally activated delayed fluorescence Time-dependent density functional theory Thermogravimetric analysis
Ultraviolet Volts
Voltampérométrie cyclique
Visible
xv
À mon père, un bon père.
« Un bon père. Un homme possédant une tête, un cœur et une âme. Un homme capable d'écouter, de guider et de respecter un enfant, et non de l'étouffer sous ses propres défauts. Quelqu'un que l'enfant n'aimerait pas seulement parce que c'est son père, mais qu'il admirerait pour ce qu'il est réellement. Quelqu'un à qui son enfant voudrait ressembler. » Carlos Ruiz Zafón « L’ombre du vent »
Remerciements
Tout d’abord, je remercie ma famille et amis pour leur confiance, leur support ainsi que leur présence lors de la rédaction de ce mémoire. Je remercie aussi mes collègues au laboratoire qui m’ont soutenue et conseillée et ont partagés leurs connaissances et expériences ces dernières années. Aussi, un grand remerciement à mon directeur de recherche, Professeur Garry S. Hanan, qui m’a fait confiance et qui me permet de développer mes connaissances et mes aptitudes en tant que chercheuse.
Je souhaite aussi remercier les personnes qui ont collaboré et qui se sont impliquées avec moi dans la présente recherche. Je remercie spécialement ma collègue et amie, Mihaela Cibian, sans qui le présent projet n’aurait pu voir le jour, pour sa disponibilité, sa participation et pour sa passion de la chimie qui m’inspire et me permet d’aller plus loin dans mes recherches.
Enfin, un grand remerciement à mes enseignants du département de Chimie ainsi qu’au personnel au services de caractérisation (Diffraction de rayons X, TGA, EA, RMN, AFM…) offerts par l’Université de Montréal.
Chapitre 1 : Introduction
Partie 1. Efficacité énergétique et développement des technologies
écologiques.
1.1 Contexte général : L’énergie
L’énergie est un concept vaste et complexe à définir. L’énergie peut prendre plusieurs formes et l’on observe constamment sa manifestation dans notre univers. On l’étudie et on l’utilise même si une définition absolue nous échappe. En physique, l’énergie est surtout vue comme la
capacité à effectuer un travail.1 On est capable de percevoir l’énergie par les formes qu’elle
peut prendre tel que le mouvement, le rayonnement électromagnétique ou la chaleur. Et voilà un point extrêmement important, car c’est par les façons dont l’énergie se manifeste que l’être humain est devenu conscient de cette capacité et a été en mesure de l’utiliser pour assurer et renforcer la survie et l’avancement de l’espèce. De nombreuses avancées technologiques et médicales n’auraient jamais vu le jour sans cette énergie qui permet de convertir nos idées en actions. L’utilisation de l’énergie a permis la formation de sociétés complexes tout en l’augmentant l’espérance et la qualité de vie des personnes. Trouver et utiliser de l’énergie est pour l’être humain une nécessité.2
1.1.1 Demande énergétique globale.
Avant la révolution industrielle, la plupart des sociétés vivaient principalement de l’agriculture. Les fermiers travaillaient la terre à l’aide des machines qui utilisaient le vent et l’eau (énergies cinétiques) comme source d’énergie. Le bois sec de son côté a permis pendant de nombreuses années de générer de la chaleur et de la lumière. L’énergie provenant de la combustion du charbon était aussi utilisée, mais limitée par la difficulté du processus d’extraction et de transport. À cela, on ajoute l’utilisation de technologies de combustion inefficaces.3 Avec le
temps, les technologies ont évolué à un point tel que la capacité de production s’est vue exceptionnellement maximisée le tout en exigeant moins d’effort humain. Ceci a provoqué une
3
demande d’énergie augmenter en conséquence. Le bois ne suffisait plus à répondre à la demande énergétique. Pour trouver du bois il fallait s’aventurer de plus en plus profond dans la forêt ce qui rendait son transport laborieux. En plus, le bois doit passer par un processus de séchage qui peut prendre plusieurs mois avant qu’il puisse être utilisé. Cette étape est absolument nécessaire, car le bois humide ne peut pas être allumé. La demande grandissante, le transport difficile et la longue période de séchage du bois sont les inconvénients qui ont inévitablement contribué à la transition vers les combustibles fossiles.3 Même si la densité d’énergie des combustibles fossiles
est plus élevée que celle du bois sec, ce n’est qu’à la fin du 18e siècle, que les quantités
d’extraction du charbon des mines ont augmenté considérablement.3 Ceci est dû au fait que
pour extraire du charbon en grande quantité il faut creuser des fosses profondes. Le défi est que pour y parvenir il faut pomper de l’eau, ce qui était très difficile et couteux en énergie. Il était donc pressant de trouver les technologies appropriées. Le début de la révolution industrielle est donc associé à des inventions comme la machine à vapeur de James Watt (1769)4 qui ont changé
complètement la façon d’utiliser l’énergie. La machine à vapeur pouvait produire du travail mécanique grâce à la pression de la vapeur d’eau produite par la chaleur dégagée lors d’un processus de combustion (énergie chimique ® énergie thermique ® énergie mécanique). Ce type de machine a rendu non seulement les procédés industriels plus simples et efficaces, mais aussi les milieux du transport terrestre et maritime se sont vus complètement métamorphosés. Peu de temps après, il y a aussi eu de grandes avancées dans la compréhension des phénomènes électriques. L’électricité pouvait être maitrisée et générée à partir de plusieurs types de sources. Elle était par sa polyvalence, la forme d’énergie la plus adaptée aux sociétés modernes. La commercialisation de l’électricité et l’électrification des villes ont changé complètement le rapport que l’humain avait avec l’environnement et marquent le début de la deuxième étape de la révolution industrielle.2-3, 5
En résumé, ce qui caractérise cette révolution n’est pas l’utilisation du charbon et d’autres combustibles fossiles comme sources d’énergie, mais plutôt le développement de technologies capables d’extraire, de raffiner et de convertir ces énergies efficacement. Ceci a finalement permis aux villes de trouver les ressources nécessaires à leur épanouissement socio-économique.6 Cette période de l’histoire a déclenché toute une sorte d’évènements qui ont
prolongement de l’espérance de vie, l’agriculture industrielle, l’accès à l’eau potable, la globalisation, l’urbanisation, l’accès aux soins de santé et d’éducation tout cela grâce aux découvertes scientifiques et avancées technologiques.7 L’être humain moderne avait le pouvoir
de choisir et de construire son avenir.
Pourtant, l’humanité comprend aujourd’hui que l’avenir n’est plus une certitude. On parle de réchauffement climatique, de déforestation, d’espèces en danger d’extinction, de pollution, de famine et de manifestations météorologiques extrêmes.8 Qu’est-ce qui a bien pu se produire
pour que l’humanité se retrouve dans une telle situation? Qu’elles sont les conséquences de la révolution industrielle sur notre planète?
a)
b)
Figure 1. Contribution selon le type de carburant au total des ressources en énergie primaire mondiales (TPES). a) Valeurs en Mtoe de 1971 à 2015. Reproduit à partir de la référence 9 b) Valeurs en % pour l’année 2015.Reproduit à partir de la référence 10. On compte maintenant plus de 7 billons d’habitants sur terre et la population ne cesse pas d’augmenter. La croissance démographique a entrainé une augmentation de la demande énergétique. Le total des ressources en énergie primaire mondiales estimé en 2015 était 13 647
5
Mtoe (Million tonnes of oil equivalent) (Figure 1).11 Pour permettre de satisfaire cette demande,
on a mis en place un modèle économique qui ne pouvait fonctionner qu’à court terme. La croissance économique de chaque pays dépend de la quantité des ressources d’énergie qui peuvent être trouvées et exploitées. En suivant ce modèle, les ressources d’hydrocarbures ont été utilisées de façon excessive sans penser aux conséquences. Les carburants fossiles sont des hydrocarbures qui peuvent prendre des millions d’années à se former sous haute pression et chaleur à partir de la matière organique des plantes et animaux morts. Les hydrocarbures, comme leur nom l’indique, comportent des atomes de carbone et hydrogène qui peuvent former des chaines ou des cycles (alcanes, cycloalcanes ou arènes) avec des liaisons chimiques très riches en énergie. Lorsqu’on les oxyde complètement par combustion en CO2 et H2O on dégage
une quantité formidable d’énergie.12 Ceci est un aspect important, car utiliser des carburants
fossiles augmente la concentration moyenne de CO2 dans l’atmosphère (403 ppm en 2016,
augmentation de 40% par rapport à 1850).13. Actuellement, 82 % de l’énergie utilisée provient
de ce type de ressource et en conséquence le réchauffement climatique s’accélère.14
Figure 2. Contribution anthropique mondiale des gaz à effet de serre selon secteur en 2014. Reproduit à partir de la référence 13.
La Figure 2 montre que les émissions de dioxyde de carbone et d’autres gaz à effet de serre proviennent du secteur de l’énergie qui en 2014 contribuait pour 68% du total mondial selon l’Agence Internationale de l’Énergie. On comprend aujourd’hui que les ressources de carburants fossiles sont très précieuses et elles qu’elles renferment beaucoup d’énergie, mais on comprend aussi qu’elles ne sont pas illimitées ni renouvelables, et contribuent au réchauffement climatique.
1.1.2 L’éclairage
Crédits : NASA Earth Observatory / NOAA NGDC.
Figure 3. Carte composite du monde réalisée à partir des données acquises par le satellite de la centrale de Suomi en avril et octobre 2012.Reproduit à partir de la référence 15. Les animaux diurnes ajustent leurs activités pour profiter le plus possible de la lumière du grand astre. Biologiquement, l’être humain continue d’être un animal diurne, mais l’éclairage artificiel lui a permis de s’adapter aussi à un rythme de vie nocturne. L’apparition de l’éclairage artificiel contribue à augmenter le niveau de vie des personnes. Les rues sont plus sécuritaires depuis que l’électrification des villes a permis l’éclairage de l’espace public. L’épanouissement social et économique devrait arrêter en absence d’éclairage nocturne. Pour continuer à maitriser son environnement pendant la nuit l’humain a dû créer toute sorte de technologies d’éclairage. Il va sans dire que pour atteindre ce but il faut une énorme quantité d’énergie.
En 2015, on a consommé 1 737 Mtoe en électricité globale. Elle a été produite principalement par des sources d’énergie thermique fossile comme la combustion du charbon, pétrole et gaz naturel. L’électricité est utilisée au milieu industriel (42.0%), résidentiel (27.1%) et commercial et services publics (22.2%).9 En moyenne, 20% de cette électricité est utilisée pour l’éclairage
ce qui représente 6% des émissions de CO2 globales soit l’équivalent à 1,9 milliard de tonnes.16
L’être humain a bâti un système socio-économique qui requiert une consommation extraordinaire d’énergie et changer ceci de façon précipitée mettrait en péril sa survie.
7
les changements environnementaux sont dévastateurs. Les prévisions à long terme ne présagent rien de bon si aucune action n’est prise. Heureusement, les dirigeants des pays industrialisés deviennent de plus en plus conscients de la nécessité à adopter de politiques environnementales pour la protection de la planète. Un modèle promouvant une économie verte permettrait de diminuer les pertes monétaires associées aux conséquences du réchauffement climatique et la pollution. Ces pertes sont estimées à 4,6 trillions de dollars américain.17 L’organisation pour
les Nations Unies pour l’environnement propose dans ses objectifs de développement durable une transition économique qui mise sur trois aspects principaux :
1. Diminution de l’utilisation des carburants fossiles (transition vers des énergies renouvelables).
2. Efficacité énergétique (technologies vertes). 3. Économie sociale.
Figure 4. Consommation d’énergie par ménage et consommation d’énergie totale pour l’éclairage pour la période de 1990-2013. Reproduit à partir de référence 18 Pour ce qui est de l’éclairage, plusieurs pays ont adopté de politiques d’efficacité énergétique permettant d’accélérer la transition vers des technologies vertes. Ceci a eu comme impact de diminuer la consommation d’électricité reliée à l’éclairage. Par exemple, au Canada, selon le ministère des Ressources naturelles il y a eu une diminution de la consommation d’énergie d’éclairage par ménage dans le secteur résidentiel depuis l’année 2007 (Figure 4).18 Cette
diminution est attribuable à l’utilisation de technologies d’éclairage plus efficaces comme les lampes fluorescentes compactes et les diodes électroluminescentes. En même temps, on observe
que la demande d’énergie totale pour l’éclairage continue à augmenter, raison pour laquelle il est primordial de continuer à miser sur des technologies qui ont une bonne efficacité énergétique.
On peut suivre l’histoire de l’éclairage artificiel électrique et se rendre compte que dans ce cas-ci miser sur l’efficacas-cité énergétique a vraiment permis de réaliser des économies d’énergie. En 1880, Thomas Edison commercialisait les ampoules à incandescence. Ce type d’ampoule fait partie de la première génération de l’éclairage artificiel électrique. À cette époque, cette technologie était innovatrice et permettait l’éclairage des rues et des résidences de façon plus efficace. Cette technologie était aussi plus facile d’utilisation comparativement aux lampes à paraffine qu’on utilisait antérieurement.16 Pour produire de la lumière, les ampoules à
incandescence utilisent le passage du courant électrique par un fil de tungstène. Ce dernier devient très chaud et en conséquence il émet de la lumière (rayonnement du corps noir).19 Même
si le cout de fabrication des ampoules incandescentes est économique, le désavantage de ce type de système est qu’une très grande quantité d’énergie est transformée en chaleur. En général, cette technologie n’utilise que 5% de l’énergie fournie pour produire de la lumière et le 95% restant se perd sous forme de chaleur.20 Cela engendre d’énormes quantités d’électricité
gaspillées. Un autre inconvénient de type d’ampoule est sa très courte durée de vie de seulement 1000 h.21 Les couts de fonctionnement et de remplacement de ce type de technologie n’étant pas
négligeables à long terme d’autres technologies ont été proposés pour remplacer ce type de système.22
Ce ainsi que dans les années 1970, les ampoules incandescentes ont été délaissées à profit des ampoules compactes fluorescentes (CFL). Les CFL comme son nom l’indique sont une version plus petite des lampes à tube fluorescent de la Westinghouse Electric Corporation commercialisées en 1938. Ces dernières sont reconnues comme la deuxième génération de technologies d’éclairage artificiel électrique.23 Les CFL incorporent des atomes de mercure qui
émettent un rayonnement UV, lorsqu’excités électriquement. Ce rayonnement excite à son tour un composé fluorescent dans le revêtement interne de la lampe capable d’émettre de la lumière dans le domaine du visible.19 Ce type de technologie était très intéressante, car elle est capable
9
aux CFL tels que leur sensibilité aux températures froides. Le plus grand désavantage est que l’ampoule contient du mercure; un élément chimique extrêmement toxique.22, 2423, 25
Les diodes électroluminescentes
Dans les années 1960, les LED (Light-emitting diode) commençaient à faire leur apparition. Elles permettent un rayonnement presque monochromatique en utilisant des matériaux semi-conducteurs inorganiques. Les premières couleurs découvertes pour les LED ont été le rouge, le jaune et le vert. Elles ont été fabriquées à partir de phospho-arséniure de gallium en différentes fractions (GaAs1-xPx) pour obtenir les couleurs d’émission rouge et jaune et à partir du
phosphure de gallium dopé à l’azote (GaP:N) pour l’obtention de l’émission verte. Ce n’est qu’en 1994 que les LED à lumière bleue (GaN) ont été développées par Shuji Nakamura chez Nichia Corporation au Japon. Cette découverte a été essentielle pour permettre subséquemment d’obtenir des LED à lumière blanche (WLED).19, 23 De ce fait, les lampes WLED sont
considérées comme la troisième génération de technologies d’éclairage artificiel électrique. De nos jours, les LED sont souvent employées pour l’éclairage général, pour de l’affiche lumineux et pour la signalisation du trafic grâce à la variété de couleurs offertes. Leur mode de luminescence à l’état solide est l’un des plus efficaces, soit 2 fois de plus que les CFL et 10 fois de plus que les lampes à incandescence. Ceci représente 85% d’économie d’énergie. En plus, leur durabilité aux différentes conditions de température avec une durée de vie qui peut se prolonger jusqu’à 60,000 heures diminue les couts associés au remplacement des lampes.21, 23
Figure 5. Représentation de l’émission dans un dispositif LED. Modifié de la référence 23.
Én e rg ie EC EV Eg Bande de conduction Bande de valence Vecteur d’onde (k) k=0 -k +k Photon 2 = hv2 Photon 1 = hv1 Recombination
Le principe de fonctionnement de ce type de lampe repose sur l’émission à l’état solide créée par l’excitation électrique des matériaux semi-conducteurs qui la composent. Le mécanisme d’émission peut alors être expliqué par la théorie des bandes. Une lampe LED comprend des matériaux semi-conducteurs dopés positivement (trous) ou négativement (électrons) pour former une jonction p-n. Quand le courant électrique passe à travers le dispositif de l’anode (côté p) vers la cathode (côté n), il y a une recombinaison des trous dans la bande de valence avec les électrons de la bande de conduction engendrant l’émission d’un photon (Figure 5).
Ephoton= Eg = Ec-Ev (équation 1)
La longueur d’onde d’émission de ce dernier est équivalente à l’écart d’énergie qui sépare la bande conduction (Ec), en son point le plus bas, de la bande de valence (Ev) en son point le plus
haut (Ev) (Équation 1). Cet écart énergétique (Eg) est connu comme bande interdite, car on ne
retrouve aucune densité d’états électroniques. Le rayonnement final obtenu est dit presque monochromatique à cause de la structure des bandes des semi-conducteurs à l’état solide qui permet l’émission de photons avec une fréquence légèrement plus élevée, car l’écart énergétique pour la recombinaison devient plus grand (Figure 5). Dans le cas de matériaux semi-conducteurs inorganiques l’énergie du photon émis peut donner une luminescence dans le proche UV, dans le visible, ainsi que dans le proche IR. Ce phénomène est connu comme l’électroluminescence. Une LED est de ce fait une diode capable d’émettre de la lumière lors de l’application d’un voltage. 23, 25-26
Figure 6. Structure chimique des isomères méridional et facial du complexe Alq3
tris(8-hydroxyquinoléine) aluminium(III). O O Al N N O N O O Al N N O N mer-Alq3 fac-Alq3
11
Les premières observations d’électroluminescence remontent à 1950. Une décennie après, un groupe de recherche de la New York University (NYU) a observé pour la première fois l’électroluminescence d’un composé organique. Ce composé était de l’anthracène sous sa forme cristalline soumis à un voltage de plus de 300 V. Malheureusement, à l’époque l’électroluminescence de ce matériel organique ne s’avérait pas intéressante, car elle utilisait un voltage trop élevé. Ce n’est que dans les années 1980 qu’un premier film amorphe contenant de l’anthracène a été étudié dans la même université. En raison de sa morphologie, ce dernier n’a pas eu besoin d’un fort voltage pour donner une luminescence appréciable. Ces études ont aussi démontré l’importance des conditions d’énergie requises pour l’injection efficace de trous et d’électrons dans la couche organique. Quelques années après Tang et Van Slyke ont fabriqué le premier dispositif OLED (Organic light-emitting diode) en utilisant du tris(8-hydroxyquinoléine)aluminium(III) (Figure 6) comme couche émissive chez Kodak.27 Ces
évènements sont à l’origine de la technologie des diodes électroluminescentes organiques (OLED). 23, 28
Des avancées majeures ont été réalisées dans ce domaine permettant aujourd’hui d’obtenir des dispositifs efficaces qui peuvent être actionnés à bas voltage.29 On peut dire que les OLED sont
une catégorie de LED qui utilise des molécules organiques plutôt que des matériaux semi-conducteurs. Elles donnent alors des dispositifs plus légers (films minces) et flexibles (substrat en polymère) avec un design moléculaire plus varié et une meilleure efficacité que les LED conventionnelles pour l’éclairage général.22, 30 Toutes ses caractéristiques offrent aussi la
possibilité aux OLED d’être utilisées dans des applications d’affichage lumineux sophistiqué.31
Elles se veulent donc une alternative aux technologies actuelles d’affichage sur écran plat comme le plasma ou les cristaux liquides LCD.25, 28, 32 À ce jour, il existe deux principales
catégories de dispositifs OLED, soit ceux faits à partir de matériaux polymères et ceux fabriqués à partir de petites molécules. Cette dernière catégorie regroupe les molécules purement organiques et les complexes organométalliques. Les OLEDs faites à partir de petites molécules ont l’avantage de permettre un meilleur contrôle sur les propriétés optiques ainsi qu’une meilleure flexibilité quant à la méthode de fabrication utilisée. Les petites molécules peuvent facilement former des films par solution (déposition par spin coating) grâce à leur bonne solubilité, mais elles peuvent aussi former des films par sublimation ou évaporation sous vide.
Cette dernière méthode donne des films homogènes et reproductibles. Ceci est possible vu la petite taille de ces molécules comparativement à celle des polymères.23. Le choix du matériel
dépendra cependant du type d’application que l’on envisage, car chaque type de pigment a ses avantages et ses désavantages.23
L’évolution continuelle vers des méthodes de fabrication plus versatiles et économiques ainsi que la découverte d’une grande variété de matériaux font en sorte que les dispositifs d’émission à l’état solide LED et OLED deviennent plus rentables; permettant ainsi une transition plus rapide des systèmes d’éclairage traditionnels vers des technologies plus efficaces.33
1.1.3 Principe de fonctionnement des dispositifs OLED
L’électroluminescence
De la même façon que les LED, les OLED utilisent le phénomène d’électroluminescence pour permettre l’affichage lumineux. L’électroluminescence est la conversion d’une énergie électrique en énergie radiative. Contrairement à la photoluminescence qui se produit après l’absorption d’un photon, l’électroluminescence est le résultat de l’application d’un potentiel. L’électroluminescence des OLED se produit par le passage de courant électrique à travers les couches minces des molécules organiques conductrices à l’état solide sur un substrat transparent. Des trous de charge positive sont injectés par l’anode et des électrons par la cathode dans le dispositif. Leur recombinaison par attraction coulombienne permet la formation d’un exciton (électron-trou) dans la couche émettrice qui libère son surplus d’énergie sous forme de lumière visible équivalent à l’énergie de l’écart Eg du pigment emetteur.34
Même si l’électroluminescence et la photoluminescence se réfèrent à deux phénomènes différents, on se sert de la dernière pour approximer la longueur d’onde d’émission d’un composé avant de l’intégrer dans un dispositif.35
13
L’importance de la structure du dispositif
Figure 7. Structure générale d’un dispositif OLED. Modifié de référence 23.
Pour rendre la recombinaison efficace, on doit empêcher les charges de se recombiner ailleurs que dans la couche d’émission. On doit aussi garder une bonne mobilité électronique pour avoir un dispositif capable de fonctionner à un potentiel relativement faible. À la Figure 7, on peut voir une représentation de la structure d’un dispositif OLED. Une structure en films minces apporte un meilleur contrôle et une meilleure efficacité de la recombinaison électrons-trous dans le dispositif. Pour que tout électron injecté se recombine avec un trou et forme un exciton, chaque couche du film à un rôle spécifique à jouer. La composition chimique, la morphologie et l’épaisseur des couches ont une incidence sur l’efficacité du dispositif et sur les propriétés optiques observées. Ainsi, les couches imposent des conditions d’énergie pour diriger les charges vers l’endroit idéal à la recombinaison. Ces conditions d’énergie sont déterminées par les niveaux d’énergie des orbitales HOMO et LUMO des molécules qui composent chaque couche du dispositif (Figure 8).23
Figure 8. Mobilité de charges dans le dispositif OLED. Modifié de référence 23.
CIE Cathode CTE CEM CTT CIT Anode Substrat Couche d’injection d’électrons
Couche de transport d’électrons Couche d’émission Couche de transport de trous
Couche d’injection de trous
Lumière ∆V Anode Cathode CIT CTT CEM CTE CIE Recombination Én e rg ie HOMO LUMO
L’orbitale moléculaire occupée la plus haute en énergie est appelée HOMO. De son côté, la LUMO est l’orbitale moléculaire inoccupée la plus basse en énergie. Dans le dispositif, les trous sont injectés dans les orbitales HOMO et les électrons dans les orbitales LUMO. En utilisant la stratégie d’une structure en couches minces, on peut affiner la mobilité des trous et électrons à l’intérieur du dispositif. Comme résultat on voit une augmentation de l’accumulation des charges sur la couche d’émission, ceci donne une efficacité fortement améliorée.34, 36
L’OLED est composée d’une anode, d’une couche d’injection de trous (CIT), d’une couche de transport de trous (CTT), d’une couche d’émission (CEM), d’une couche de transport d’électrons (CTE), d’une couche d’injection d’électrons (CIE) et d’une cathode métallique. L’anode est incorporée directement sur le substrat et elle est souvent composée d’oxyde d'indium dopé à l'étain ou ITO (indium tin oxide). Celui-ci est le composé de choix pour les
OLED, car en plus de posséder une bonne conductivité électrique, ce matériel forme une couche
transparente sur le substrat permettant le passage de la lumière émisse.34-35 Le rôle de l’anode
est d’extraire des électrons, en laissant des places vacantes de charge positive sur la CIT. Un trou est donc un espacement de charge positive formé par l’extraction d’un électron par l’anode. Les charges positives formées par l’anode se déplacent par les orbitales HOMO du CTT, car des électrons de cette dernière quittent pour occuper les trous sur la CIT en laissant à leur tour une nouvelle place inoccupée positive. De cette façon, les trous continueront à se déplacer jusqu’à la couche d’émission. Ce mécanisme est appelé saut de trous (hole hopping). De ce fait, l’énergie de l’orbitale HOMO du composé qui constitue la CIT doit se situer entre l’énergie du travail de sortie de l’anode et l’énergie de l’orbitale HOMO de la CTT. Un autre rôle important de la CTT est d’imposer des contraintes énergétiques, soit un écart HOMO-LUMO plus grand que celui de la CEM. Ceci a comme effet d’empêcher le transfert de l’énergie de la CEM vers la CTT.34
D’un autre côté, la cathode métallique est responsable de l’injection d’électrons dans l’orbitale LUMO de la CIE. Les électrons se retrouvent par la suite dans l’orbitale LUMO de la CTE qui est légèrement plus haute en énergie. Ces dernières couches sont composées d’un matériel ayant une énergie d’orbitale HOMO très stable pouvant bloquer le passage des trous vers la cathode.37
15
Les électrons et les trous sont guidés vers la CEM par les conditions d’énergie de chaque couche, mais aussi par l’attraction coulombienne de l’anode et de la cathode. Sur cette couche se retrouve un composé émissif à l’état solide qu’on appelle pigment. Le but est de recombiner les charges pour provoquer la formation d’un exciton qui excite le pigment dans la CEM produisant de la lumière lors de la relaxation vers l’état fondamental. Toutefois, la majorité d’excitons est formée à l’interface entre la CTT et la CEM. On doit alors s’assurer d’avoir un bon transfert d’énergie entre les deux pour être capable d’obtenir un photon qui émettra à la couleur déterminée par l’écart HOMO-LUMO du pigment. Ces transferts d’énergie peuvent être de type Forster ou Dexter (Figure 9). Le type de transfert dépend de la nature de l’exciton formé (singlet ou triplet). Ce dernier est déterminé par la nature des molécules qui composent la couche d’émission.38 Ces
transferts sont également importants lorsque la couche d’émission est composée d’un pigment dopé dans une matrice (ou co-hôte). Dans ce dernier cas, la matrice doit être en mesure de transférer l’énergie de l’exciton vers le pigment efficacement pour obtenir la luminescence attendue. C’est pour ce motif que le choix de la matrice doit être adapté selon la couleur d’émission du pigment choisi.39
Figure 9. Représentation des mécanismes de transfert d’énergie Förster et Dexter. Reproduit de référence 38b.
1.1.4 Utilisation des complexes organométalliques dans les dispositifs OLED
Figure 10. Probabilités de radiation d’un exciton selon sa multiplicité. Reproduit à partir de référence 40.
À présent, on compte avec trois générations de dispositifs OLED, qui se caractérisent par le type d’émission formée lors de l’électroluminescence (Voir Figure 10).
• 1re génération : OLEDs fluorescentes
• 2e génération : OLEDs phosphorescentes
• 3e génération : OLEDs TADF
L’électroluminescence, de la même façon que la photoluminescence, peut se faire par fluorescence ou par phosphorescence. Lorsque la relaxation vers l’état fondamental S0 se fait à
partir de l’état singulet S1 on l’appelle fluorescence et si cette relaxation se fait à partir d’un état
triplet T1 on l’appelle phosphorescence. Il existe une seule combinaison possible pour obtenir
un exciton S1 (spin =0) et trois pour un exciton T1 (spin =1). Dans le cas des molécules
fluorescentes ceci représente donc statistiquement une efficacité quantique interne (IQE) maximale de 25% pour un dispositif contenant un pigment fluorescent.
La relaxation à partir de l’état triplet possède un temps de vie plus long que la fluorescence, car c’est une transition interdite par la règle du spin (conservation du moment angulaire). La loi du spin peut être transgressée lorsque les molécules possèdent des atomes suffisamment lourds pour permettre un couplage spin orbite efficace. Le système passe d’un état singulet à un état triplet (plus bas en énergie) car leurs courbes d’énergie potentielle S1 et T1 se touchent. Ce
Petit TADF (3egénération) Phosphorescence (2egénération) Fluorescence (1regénération)
17
Les OLEDs phosphorescentes sont donc capables d’atteindre une efficacité quantique interne de 100% grâce à la formation des exciton triplet.41 Cependant, pour obtenir des matériaux
capables de phosphorescence il faut dans une grande majorité des cas utiliser des métaux lourds pour être en mesure d’avoir un bon couplage spin-orbite. Ces métaux sont peu abondants, dispendieux et quelquefois toxiques ce qui limite leur utilisation.
Les OLEDs TADF (3e génération) sont aussi capables d’une efficacité interne de 100%, mais à
travers un mécanisme de fluorescence retardée activée thermiquement (TADF) plutôt que par phosphorescence.40 La TADF est un processus de récupération des excitons triplet vers l’état
singlet en passant par une conversion intersystèmes inverse (RICS) de T1 vers S1. La relaxation
à partir de T1 devient très difficile en absence d’atome lourd et les processus qui ne respectent
pas la loi du spin devient plus lents.40 Grace à la RICS les molécules TADF sont capables de
déjouer ce chemin non radiatif communément observé chez les molécules fluorescentes. Cependant, pour être en mesure de permettre l’échange et d’avoir un bon taux de RISC il faut que la différence d’énergie entre S1 et T1 (DEST)soit très petite (DEST > 0.1 eV).42
Dans tous cas, une stratégie de design moléculaire s’impose pour tirer profit de toutes ces possibilités et être capable de créer un pigment adapté à chaque besoin. Sur ce point les complexes métalliques ont un très grand avantage comparativement aux molécules purement organiques et polymères. Chez les complexes métalliques, le fait d’avoir la possibilité de coordonner des ligands à un ion métallique permet une grande variété de géométries. Le centre métallique offre la possibilité d’avoir un certain contrôle sur les propriétés non seulement structurales, mais aussi mécaniques, thermodynamiques et optiques du matériel.38b
L’ion métallique peut être choisi entre une grande variété de possibilités soit les métaux alcalino-terreux, les métaux de transition, les métalloïdes et les lanthanides. Les complexes métalliques permettent d’améliorer les propriétés de transport d’électrons, car comparativement aux molécules organiques ils acceptent plusieurs états d’oxydation et possèdent un nuage électronique plus diffus. Ils ont aussi une grande stabilité thermique grâce à une plus grande rigidité structurale. Les chélates organométalliques utilisés dans les OLED sont capables de résister à des températures aussi élevées que 350 °C sans se décomposer.43 D’un autre côté, le
les facteurs stériques et/ou électroniques . On peut donc moduler la couleur d’émission en ajustant l’écart HOMO-LUMO du complexe.44
1.1.5 Les défis
Un des obstacles à la commercialisation en masse de la technologie OLED est le manque d’émetteurs bleus stables. Les complexes d’iridium (III) sont le plus utilisés pour obtenir des
OLEDs bleues, malheureusement le cout de ce métal ainsi qu’une stabilité moindre
comparativement aux autres phosphores limite le temps de vie du dispositif OLED et des alternatives doivent être envisagées. Les émetteurs bleus sont indispensables pour les applications d’affiche sur écran plat, mais ils sont aussi nécessaires à la fabrication d’OLEDs à lumière blanche WOLED (White organic light-emitting diode). Ces dernières sont typiquement fabriquées à partir d’un mélange de molécules émettrices de couleurs ou à partir d’une seule molécule émettrice dans tout le domaine du visible. Dans le premier cas, la lumière blanche est obtenue par l’émission de molécules émettrices dans le rouge, vert et bleu (couleurs primaires) ou par un mélange d’émission d’émetteurs aux couleurs complémentaires.29, 38a, 45 Ce type de
WOLED a le désavantage d’être compliqué à fabriquer et ne permet pas un bon contrôle des
transferts d’énergie parmi les couches, ce qui cause des petites inconsistances de couleur d’un dispositif à un autre. Aussi, comme mentionné avant, il est très difficile de trouver un matériel stable qui émet très fortement dans le bleu ce qui diminue l’efficacité du dispositif, car on a plusieurs composés, ayant tous un temps d’usure différent.31
Il est aussi possible d’utiliser une seule molécule émettrice, soit un matériel capable d’émettre à plusieurs longueurs d’onde. L’utilisation de ce type de molécule réduit considérablement le cout et la complexité de fabrication du dispositif.45a De plus, l’emploi d’une seule molécule
permet d’éviter l’instabilité de couleur. Il est possible d’obtenir la lumière blanche par l’émission simultanée d’une molécule qui émet bleu dans son état excité et qui a une émission rouge-orange lorsqu’elle forme des excimères ou électromères (Figure 11). Les excimères sont des agrégats de la molécule dans l’état excité avec la même molécule à l’état fondamental. Les électromères sont des agrégats de la molécule ayant un électron en excès avec la même molécule avec un trou (charge positive, car électron de moins).29, 38a, 45a, 46 Néanmoins, trouver une telle
19
molécule et contrôler efficacement la formation des excimères ou électromères représente tout un défi.
Figure 11. Représentation des excimères et électromères. Reproduit de référence 45a.
Une autre limitation à la commercialisation en masse des OLEDs est la complexité de fabrication et le cout dispendieux de dispositifs à grande surface (panneaux d’affichage lumineux).47 Ceci
est dû au fait qu’une majorité des émetteurs doivent être dopés (dilués) dans une matrice pour empêcher l’auto désactivation de l’émission causée par la formation d’agrégats moléculaires lorsque la molécule se retrouve à haute concentration. Cependant, depuis quelques années on a pris connaissance d’un phénomène qui pourrait aider à régler ce problème et simplifier le processus de fabrication des dispositifs. Ce phénomène et ses implications sont discutés en détail dans la partie 2 du chapitre 1 de ce mémoire.
1.1.6 Bibliographie
1. Atkins, P. W., Physical Chemistry. 7th ed.; New York : W.H. Freeman: New York, 2002. 2. Clark Ii, W. W.; Cooke, G., Chapter 2 - Industrial Development. In The Green Industrial
Revolution, Butterworth-Heinemann: Boston, 2015; pp 13-35.
3. Smil, V., Energy and Civilization: A History. MIT Press: 2017.
4. https://www.britannica.com/biography/James-Watt (accessed 17-05-2018).
5. Devine, W. D., From Shafts to Wires: Historical Perspective on Electrification. J Econ
Hist 1983, 43 (2), 347-372.
6. Levin, M. R., Urban Modernity : Cultural Innovation in the Second Industrial
Revolution. MIT Press: Cambridge, 2010.
7. (a) Juniper, T.; Wales, H., What's Really Happening to Our Planet? DK Publishing: 2016; (b) Stearns, P. N., The Industrial Revolution in World History. Westview Press: 1998.
8. Clark Ii, W. W.; Cooke, G., Chapter 5 - Climate Change, Science and Technology, and Economics Are the Forces Behind the Gir. In The Green Industrial Revolution, Butterworth-Heinemann: Boston, 2015; pp 95-121.
9. Key World Energy Statistics 2017. International Energy Agency: 2017.
10. Renewables Information: Overview 2017. International Energy Agency: 2017. 11. World Energy Balances: Overview 2017. International Energy Agency: 2017. 12. Solomons, T. W. G., Chimie Organique. Modulo: Québec, 2000; p 137-139.
13. CO2 Emissions from Fuel Combustion 2017: Overview 2017 ed.; International Energy Agency: 2017.
14. Schobert, H. H., Fuels and the Global Carbon Cycle. In Chemistry of Fossil Fuels and
Biofuels, Schobert, H., Ed. Cambridge University Press: Cambridge, 2013; pp 1-9.
15. https://www.nasa.gov/mission_pages/NPP/news/earth-at-night.html (accessed
17-05-2018).
16. Light’s Labour’s Lost Policies for Energy-Efficient Lighting. International Energy
Agency: 2006.
17. Altenburg, T.; Assmann, C., Green Industrial Policy - Concept, Policies, Country Experiences. UN Environment; German Development Institute: Geneva, 2017.
21
18. https://www.rncan.gc.ca/sites/www.nrcan.gc.ca/files/energy/pdf/evolution2013.pdf
(accessed 14-12-2016).
19. Feng, Z. C., Handbook of Solid-State Lighting and Leds. 1st ed.; Boca Raton: 2017.
20.
http://www.hydroquebec.com/residentiel/mieux-consommer/comment/produits-ecoenergetiques/eclairage/ampoules-del-cfl.html (accessed 13-12-2016).
21. Accelerating the Global Adoption of Energy-Efficient Lighting. United Nations Environment Programme 2017. (accessed May 29 2018).
22. Lighting Energy Efficiency Reference Guide. CEATI International: 2014. (accessed 29-05-2018).
23. Khanna, V. K., Fundamentals of Solid-State Lighting : LEDs, OLEDs, and Their
Applications in Illumination and Displays. Boca Raton : CRC Press: 2014.
24. Makoto, B.; Keiichi, S., Latest Trends in LED Lighting. Electron Commun Jpn 2012, 95 (1), 1-7.
25. Held, G., Introduction to Light Emitting Diode Technology and Applications. Boca Raton : CRC Press: 2009.
26. Cees, R., Emission and Excitation Mechanisms of Phosphors. In Luminescence from
Theory to Applications, WILEY-VCH Verlag GmbH & Co. KGaA: Weinheim, 2008.
27. Tang, C. W.; VanSlyke, S. A., Organic Electroluminescent Diodes. Appl Phys Lett 1987,
51, 913.
28. Cees, R., Organic Electroluminescence. In Luminescence from Theory to Applications, WILEY-VCH Verlag GmbH & Co. KGaA: Weinheim, 2008.
29. Shahroosvand, H.; Zakavi, S.; Sousaraei, A.; Mohajerani, E.; Mahmoudi, M., Unusual Near-White Electroluminescence of Light Emitting Diodes Based on Saddle-Shaped Porphyrins. Dalton Trans 2015, 44 (18), 8364-8368.
30. Yam, V. W. W., Woleds and Organic Photovoltaics : Recent Advances and Applications. Springer: Berlin, 2010.
31. http://www.oled-info.com/oled-technology?page=0%2C1. (accessed 14-12-2016).
32. (a) Jou, J.-H.; Kumar, S.; Agrawal, A.; Li, T.-H.; Sahoo, S., Approaches for Fabricating High Efficiency Organic Light Emitting Diodes. J Mater Chem C 2015, 3 (13), 2974-3002; (b) Yersin, H., Electroluminescence from Metal-Containing Polymers and Metal
Complexes with Functional Ligands. In Highly Efficient OLED with Phosphorescent
Materials, Wiley-VCH Verlag GmbH & Co. KGaA: 2009; pp 329-358.
33. (a) Haitz, R.; Tsao, J. Y., Solid-State Lighting. Opt Photonik 2011, 6 (2), 26-30; (b) Tsao, J. Y.; Crawford, M. H.; Coltrin, M. E.; Fischer, A. J.; Koleske, D. D.; Subramania, G. S.; Wang, G. T.; Wierer, J. J.; Karlicek, R. F., Toward Smart and Ultra-Efficient Solid-State Lighting. Adv Opt Mater 2014, 2 (9), 809-836; (c) Tonzani, S., Lighting Technology: Time to Change the Bulb. Nature 2009, 459 (7245), 312-314.
34. Tsujimura, T., OLED Display Structure. In OLED Displays, John Wiley & Sons, Inc.: 2012; pp 5-35.
35. Yersin, H.; Finkenzeller, W. J., Triplet Emitters for Organic Light-Emitting Diodes: Basic Properties. In Highly Efficient Oleds with Phosphorescent Materials, Wiley-VCH Verlag GmbH & Co. KGaA: 2008; pp 1-97.
36. Mitschke, U.; Bauerle, P., The Electroluminescence of Organic Materials. J Mater Chem 2000, 10 (7), 1471-1507.
37. Adamovich, V. I.; Cordero, S. R.; Djurovich, P. I.; Tamayo, A.; Thompson, M. E.; D’Andrade, B. W.; Forrest, S. R., New Charge-Carrier Blocking Materials for High Efficiency OLEDs. Org Electron 2003, 4 (2), 77-87.
38. (a) Kamtekar, K. T.; Monkman, A. P.; Bryce, M. R., Recent Advances in White Organic Light-Emitting Materials and Devices (WOLEDs). Adv Mater 2010, 22 (5), 572-582; (b) Xu, H.; Chen, R.; Sun, Q.; Lai, W.; Su, Q.; Huang, W.; Liu, X., Recent Progress in Metal-Organic Complexes for Optoelectronic Applications. Chem Soc Rev 2014, 43 (10), 3259-3302; (c) Kepler, R. G.; Beeson, P. M.; Jacobs, S. J.; Anderson, R. A.; Sinclair, M. B.; Valencia, V. S.; Cahill, P. A., Electron and Hole Mobility in Tris(8-Hydroxyquinolinolato-N1,O8) Aluminum. Appl Phys Lett 1995, 66 (26), 3618-3620; (d) Movla, H., Influence of the Charge Carrier Mobility on the Dynamic Behavior and Performance of the Single-Layer Oled. Optik 2015, 126 (24), 5237-5240.
39. (a) Fukagawa, H.; Shimizu, T.; Iwasaki, Y.; Yamamoto, T., Operational Lifetimes of Organic Light-Emitting Diodes Dominated by Förster Resonance Energy Transfer. Sci
Rep 2017, 7 (1), 1735; (b) Ingram, G. L.; Lu, Z.-H. In Design Principles for Highly Efficient Organic Light-Emitting Diodes, SPIE: 2014; p 18.
23
40. Wong, M. Y.; Zysman-Colman, E., Purely Organic Thermally Activated Delayed Fluorescence Materials for Organic Light-Emitting Diodes. Adv Mater 2017, 29 (22), 1605444.
41. (a) Dumur, F., Zinc Complexes in Oleds: An Overview. Synth Met 2014, 195, 241-251; (b) Xu, X.; Liao, Y.; Yu, G.; You, H.; Di, C. a.; Su, Z.; Ma, D.; Wang, Q.; Li, S.; Wang, S.; Ye, J.; Liu, Y., Charge Carrier Transporting, Photoluminescent, and Electroluminescent Properties of Zinc(II)-2-(2-Hydroxyphenyl)Benzothiazolate Complex. Chem Mater 2007, 19 (7), 1740-1748.
42. (a) Xian-Kai, C.; Youichi, T.; Yuma, I.; Cheng, Z.; Chihaya, A.; Jean-Luc, B., A New Design Strategy for Efficient Thermally Activated Delayed Fluorescence Organic Emitters: From Twisted to Planar Structures. Adv Mater 2017, 29 (46), 1702767; (b) Ball, P., A New Twist for OLEDs. Nat Mater 2016, 15, 822.
43. Chen, C. H.; Shi, J., Metal Chelates as Emitting Materials for Organic Electroluminescence. Coord Chem Rev 1998, 171, 161-174.
44. Huixia, X.; Bingshe, X.; Xiaohong, F.; Liuqing, C.; Hua, W.; Yuying, H., Correlation between Molecular Structure and Optical Properties for the Bis(2-(2-Hydroxyphenyl)Benzothiazolate) Complexes. J Photochem Photobiol, A 2011, 217 (1), 108-116.
45. (a) Farinola, G. M.; Ragni, R., Electroluminescent Materials for White Organic Light Emitting Diodes. Chem Soc Rev 2011, 40 (7), 3467-3482; (b) Huo, Y.; Pan, C.; Wang, S.; Ji, S.; Kong, T.; Gao, L.; Cai, N.; Zeng, H., Color-Tunable Solid-State Emissions of Zn(II) and Cd(II) Complexes Derived from Cyano-Modified 2-Substituted 8-Hydroxyquinolines. Polyhedron 2016, 119, 175-183.
46. Huo, Y.; Lu, J.; Lu, T.; Fang, X.; Ouyang, X.; Zhang, L.; Yuan, G., Comparative Studies on OLED Performances of Chloro and Fluoro Substituted Zn(II) 8-Hydroxyquinolinates.
New J Chem 2015, 39 (1), 333-341.
47. (a) Park, J. W.; Shin, D. C.; Park, S. H., Large-Area Oled Lightings and Their Applications. Semicond Sci Technol 2011, 26 (3), 034002; (b) Matsuoka, K.; Albrecht, K.; Yamamoto, K.; Fujita, K., Mulifunctional Dendritic Emitter: Aggregation-Induced Emission Enhanced, Thermally Activated Delayed Fluorescent Material for Solution-Processed Multilayered Organic Light-Emitting Diodes. Sci Rep 2017, 7, 41780; (c)
Chen, Y.; Wang, J.; Zhong, Z.; Jiang, Z.; Song, C.; Hu, Z.; Peng, J.; Wang, J.; Cao, Y., Fabricating Large-Area White OLED Lighting Panels Via Dip-Coating. Org Electron 2016, 37, 458-464.