Activité physique et structure artérielle carotidienne chez de jeunes
adultes apparemment en santé
Mémoire
Béatrice Deschênes St-Pierre
Maîtrise en médecine expérimentale
Maître ès sciences (M.Sc.)
Québec, Canada
Résumé
L‟activité physique est un facteur protecteur contre les évènements cardiovasculaires; les preuves ont été établies par des études épidémiologiques de grande envergure il y a plus de 30 ans. Cependant, puisque l‟activité physique modifie de façon bénéfique plusieurs facteurs de risque cardiovasculaire (hypertension artérielle, dyslipidémie, diabète, obésité), des données probantes manquent encore pour établir si cette association, entre l‟activité physique et le risque cardiovasculaire, est indépendante des modifications induites dans les paramètres métaboliques. Notre étude a permis d‟évaluer, chez de jeunes adultes ne présentant pas de facteurs de risque cardiovasculaire traditionnels, les différences entre les personnes sédentaires et actives au niveau de la structure de la paroi artérielle carotidienne (marqueur de substitution du risque cardiovasculaire). Nos résultats portent à croire que les jeunes adultes apparemment en santé actifs auraient un fardeau d‟athérosclérose comparable à celui des jeunes individus sédentaires.
Abstract
Physical activity is a protective factor against cardiovascular (CV) events; this evidence has been established by the data of large epidemiological cohort studies over 30 years ago. However, since physical activity modifies favourably several cardiovascular risk factors (hypertension, dyslipidemia, diabetes, obesity), evidence is still missing to determine if this association, between physical activity and cardiovascular risk, is independent from the exercise-induced modifications in metabolic parameters. Our study evaluated, in young adults devoid of cardiovascular risk factors, the differences between sedentary and active individuals in arterial wall structure (a surrogate marker of cardiovascular risk). Our results suggest that apparently healthy young adults have a similar atherosclerosis burden whether active or sedentary.
Table des matières
Résumé ... iii
Abstract ... v
Table des matières ... vii
Liste des figures ... ix
Abréviations ... xi Remerciements ... xv Avant-propos ... xvii Chapitre 1 : Introduction ... 1 1.1 Athérosclérose ... 3 1.1.2 Marqueur de substitution ... 8 1.2 L‟activité physique ... 14 1.2.1 Concepts et définitions ... 14 1.2.2 Recommandations actuelles ... 15
1.2.3 Mesure de l‟activité physique ... 15
1.3 Activité physique et athérosclérose : structure et fonction de la paroi artérielle ... 17
1.3.1 Hémodynamie, tension artérielle et oxydation ... 19
1.3.2 Inflammation ... 19
1.3.3 Vasoconstriction et vasodilatation ... 20
1.3.4 Intensité ... 22
1.4 Recension des écrits sur l‟association entre l‟activité physique et la structure artérielle carotidienne ... 22
1.5 Limites des études actuelles et perspectives ... 26
Problématique ... 29
Hypothèses ... 29
Objectifs ... 29
Chapitre 2: Physical activity and carotid wall structure in apparently healthy young adults ... 31
Chapitre 3 : Conclusion et perspectives ... 67
Liste des figures
Figure 1: Aspect pathologique des lésions athérosclérotiques de bas grade ... 5
Figure 2: Progression de l'athérosclérose telle que décrite par Glagov ... 6
Figure 3: Classification des lésions athérosclérotiques. ... 7
Figure 4: Mesure de l'épaisseur intima-média par échographie. ... 11
Figure 5: Coupe transversale en imagerie par résonance magnétique de la paroi artérielle carotidienne. ... 12
Figure 6: Construction d'un modèle tridimensionnel de paroi carotidienne par IRM ... 13
Figure 7: Facteurs médiant l'effet de l'activité physique sur le risque cardiovasculaire. ... 18
Abréviations
AVC Accident vasculaire cérébral
CALV Volume de la lumière artérielle carotidienne (Carotid artery lumen volume) CAWV Volume de la paroi artérielle carotidienne (Carotid artery wall volume) CIMT Épaisseur de l‟intima-média carotidienne (Carotid intima-media thickness) EAT Tissu adipeux épicardique (Epicardial adipose tissue)
ECG Électrocardiogramme
eNOS Synthétase d‟oxyde nitrique endothélial (endothelial nitric oxide synthase)
ET-1 Endothéline 1
FSE Séquence d‟écho de spins rapides (Fast-spin echo) HDL Lipoprotéine de haute densité (High-density lipoprotein)
ICAM-1 Molécule d‟adhésion intercellulaire 1 (Intercellular adhesion molecule 1)
IL-6 Interleukine 6
IMT Épaisseur intima-media (Intima-media thickness) IRM Imagerie par résonance magnétique
LDL Lipoprotéine de faible densité (Low-density lipoprotein) MCAS Maladie coronarienne athérosclérotique
MCP-1 Protéine de chimioattraction des monocytes 1 (Monocytes chemioattractant protein 1)
NADPH Nicotinamide adénine dinucléotide phosphate
NO Oxyde nitrique (Nitric oxide)
OMS Organisation Mondiale de la Santé
PAS Score d‟activité physique (Physical activity score) PAT Tissu adipeux péricardique (Pericardial adipose tissue)
PCAM-1 Molécule d‟adhésion cellulaire plaquettaire (Platelet cell adhesion molecule 1)
SAAT Tissu adipeux abdominal sous-cutané (Subcutaneous abdominal adipose tissue)
SMC Cellule musculaire lisse (Smooth muscle cell)
TDM Tomodensitométrie
TEP Tomographie par émission de positons
TNF- Facteur nécrosant des tumeurs alpha (Tumor necrosis factor alpha) TOF Temps de parcours (Time-of-flight)
VCAM-1 Molécule d‟adhésion cellulaire vasculaire 1 (Vascular cell adhesion molecule 1)
VAAT Tissu adipeux abdominal viscéral (Visceral abdominal adipose tissue)
VEGF Facteur de croissance vasculaire endothélial (Vascular endothelial growth factor)
VO2max Capacité maximale de consommation d‟oxygène
VTAT Tissu adipeux viscéral thoracique (Visceral thoracic adipose tissue) VTPC Volume total de plaque carotidienne
WHR Ratio taille-hanches (Waist-to-hip ratio)
« La phrase la plus excitante à entendre en science, celle qui annonce de nouvelles découvertes, n‟est pas „Euréka!‟, c‟est „C‟est drôle…‟ »
Remerciements
D‟abord, je désire exprimer ma gratitude envers mon directeur de recherche, Dr Éric Larose, qui m‟a offert une place sur son équipe et m‟a permis de réaliser une maitrise en recherche dans le laps de temps relativement court dont je disposais. J‟ai profité de chaque minute qu‟il avait à m‟accorder; considérant ces échanges comme une ressource précieuse et limitée d‟expertise et d‟expérience. Ensuite, je voudrais remercier mon co-directeur, Jean-Pierre Després PhD, qui est un modèle d‟équilibre dans le milieu de performance de la recherche. Énergique et passionné, il transmet la passion de la recherche et du sport à ceux qu‟il rencontre.
Un énorme et sincère merci à Karine Bibeau PhD pour le support, la disponibilité et les conseils qu‟elle m‟a offerts. Avec sa vivacité d‟esprit, sa compétence scientifique et sa rigueur, elle est un pilier dans l‟équipe de Dr Larose et a été mon pilier tout au long de ma maitrise.
Je tiens aussi à remercier Dr Florent LeVen pour ses précieux conseils, ses connaissances et sa présence, il a été un mentor superbe. Une ancienne étudiante de Dr Larose et camarade de classe en médecine, Élianne De Larochellière, m‟a été d‟une grande aide, en partageant avec générosité son expérience et le fruit de son travail. Merci à mes autres collègues étudiants, Dre Maria de la Paz Ricapito et Dr Andreas Kumar; aux professionnels de recherche de l‟équipe, Marianne Desroches, Michèle Cyr, Julie Carange MSc; aux technologues en résonance magnétique, Justine Couture et Isabelle Chouinard; aux étudiants et professionnels de recherche qui m‟ont précédée dans l‟équipe grâce à qui j‟ai eu accès à une quantité de données bien plus grande que celle que j‟ai moi-même recueillie. Merci à tous les participants à l‟étude qui nous ont volontairement accordé de leur temps.
Merci à la Faculté de Médecine de l‟Université Laval. Merci à l‟Institut universitaire de cardiologie et de pneumologie de Québec, au Fonds de la recherche du Québec-Santé (FRQ-S), aux Instituts de recherche en santé du Canada (IRSC) et à la Fondation des maladies du cœur pour leur soutien financier essentiel.
Avant-propos
L‟article contenu dans ce mémoire de maitrise n‟a pas été soumis pour publication jusqu‟à maintenant. Les résultats préliminaires ont été diffusés à la Journée de la recherche de l‟Université Laval, mais n‟ont pas fait l‟objet de présentation dans un congrès.
Béatrice Deschênes St-Pierre, auteure du présent mémoire, a contribué à la collecte des données, a effectué la revue de littérature, les analyses statistiques ainsi que leur interprétation et a rédigé l‟article scientifique.
Éric Larose, DVM, MD, FRCPC, FAHA, cardiologue hémodynamicien et chercheur à l‟Institut de cardiologie et de pneumologie de Québec, l‟investigateur principal est le chef d‟orchestre d‟un grand projet de recherche sur le risque cardiovasculaire d‟une cohorte de jeunes adultes en santé. En lui se fonde une expertise sur l‟athérosclérose et plus spécifiquement sur l‟imagerie de l‟athérosclérose par résonance magnétique. Les idées originales qui sous-tendent l‟étude qui est l‟objet de l‟article, la conception et l‟établissement du protocole de recherche, la supervision du recrutement de participants et de la collecte de données, de même que de la rédaction d‟article sont les fruits de son travail.
Karine Bibeau, PhD, professionnelle de recherche à l‟Institut universitaire de cardiologie de pneumologie de Québec, est le bras droit du chef d‟orchestre. Elle s‟est impliquée dans la collecte de données, supervise le recrutement des participants et chapeaute l‟analyse des données et la rédaction d‟article.
Jean-Pierre Després, PhD, FAHA, représente l‟expertise en activité physique; il a contribué à la conception des idées originales, participé à l‟élaboration du protocole de recherche.
L‟athérosclérose est une maladie inflammatoire chronique de la paroi artérielle qui sous-tend la moitié des décès actuellement dans les sociétés occidentales1 et représente la première cause de mortalité à l‟échelle planétaire2. Elle se manifeste généralement à un âge avancé, entre autres, par un infarctus du myocarde ou un accident vasculaire-cérébral (AVC). Cependant, l‟évolution de la maladie est lente et occulte. Avant l‟âge de 19 ans, 60% des enfants auront déjà des lésions athérosclérotiques de bas grade tandis qu‟au début de la trentaine, 75% des jeunes adultes sont touchés3. Alors que la maladie au stade symptomatique a largement été étudiée dans une population adulte âgée, on s‟est moins souvent penché sur ce qui détermine son développement dans une population de jeunes adultes, surtout chez ceux qui ne présentent aucun facteur de risque cardiovasculaire. Au stade symptomatique de la maladie athérosclérotique, les lésions sont irréversibles tandis que dans les premiers stades pathologiques, les lésions ont encore un potentiel de régression4.
Des études épidémiologiques de grande envergure ont démontré que l‟activité physique est inversement et indépendamment associée au risque cardiovasculaire puisque les individus plus actifs connaissent une incidence plus faible d‟évènements cardiovasculaires et une plus faible mortalité cardiovasculaire5-9. En réponse à l‟activité physique régulière, le système cardiovasculaire, de même que pulmonaire, endocrinien, immunitaire et musculaire, s‟adapte tant fonctionnellement que structurellement; il a été postulé que cet effet d‟entrainement sur le système cardiovasculaire prévient le développement et la progression de la maladie athérosclérotique10. Par ailleurs, il a été démontré que l‟activité physique modifie plusieurs facteurs de risque cardiovasculaire tels que l‟adiposité11 et l‟obésité viscérale12-15, la résistance à l‟insuline16 et le diabète17, les dyslipidémies18-20, l‟hypertension artérielle21-23; ce qui en fait un outil thérapeutique intéressant pour le traitement du risque cardiovasculaire global24. Dans l‟ensemble des études sur lesquelles se fondent les évidences de l‟association entre l‟activité physique et le risque cardiovasculaire, des individus souffrant déjà d‟une maladie cardiovasculaire ont été inclus et/ou des sujets présentant des facteurs de risque (obèses, diabétiques, hypertendus, dyslipidémiques) forment une grande partie de l‟échantillon. Aussi, on note des différences significatives au niveau des facteurs de risque cardiovasculaire entre les individus sédentaires et les
individus actifs. Plusieurs de ces études ont démontré statistiquement que les relations étaient significatives malgré un ajustement correctif pour l‟effet potentiel des différences au niveau des facteurs de risque des individus. Pour déterminer le rôle de l‟activité physique dans la prévention primordiale cardiovasculaire (i.e. prévention de l‟apparition de facteurs de risque cardiovasculaire chez des individus), il faut se tourner vers cette population spécifique, les adultes jeunes et sains (sans facteur de risque).
1.1 Athérosclérose
Même si les percées de la médecine ont réussi à diminuer la mortalité et la morbidité qui sont attribuées à l‟athérosclérose, le bilan annuel de ses conséquences au Canada est lourd: 72 000 morts, 190 000 hospitalisations et 22.2 milliards de dollars en frais de santé25. Le risque d‟avoir un évènement cardiovasculaire augmente avec la présence d‟un ou plusieurs de facteurs de risque reconnus : obésité26, dyslipidémie, intolérance au glucose, hypertension artérielle et tabagisme27-30.
Les plaques athérosclérotiques peuvent se former dans toutes les artères, mais ont tendance à se loger à des sites où le flot sanguin n‟est pas laminaire31. Les premières manifestations pathologiques apparaissent dans l‟aorte dans la première décennie de vie sous forme de stries lipidiques, i.e. une accumulation sous-endothéliale de cellules spumeuses qui sont des macrophages remplis de cholestérol. Ces stries lipidiques se développent par la suite dans les artères coronaires à la 2e décennie et dans les artères cérébrales aux 3e et 4e décennies de vie1. Même si le processus débute en enfance et touche tous les individus à un moment ou un autre de leur vie, il ne doit pas être considéré normal puisqu‟il témoigne d‟une réaction inflammatoire de la paroi artérielle. En effet, l‟inflammation est un mécanisme universel de guérison révélant une agression et, potentiellement, un dommage. L‟endothélium, mince couche monocellulaire en contact avec la lumière artérielle, joue un rôle de barrière physique qui permet ou empêche les échanges entre la paroi artérielle et le sang et contrôle l‟environnement de la paroi en libérant plusieurs molécules actives32; la dysfonction endothéliale serait le marqueur le plus précoce du processus athérosclérotique33. En réponse à un agresseur, l‟endothélium produit des substances qui attirent des cellules
immunitaires34 : la libération de molécules d‟adhésion cellulaire (molécule d‟adhésion intercellulaire-1 (ICAM-1), molécule d‟adhésion cellulaire plaquettaire (PCAM-1), molécule d‟adhésion cellulaire vasculaire (VCAM-1), P-sélectine, E-sélectine) favorise l‟adhérence des lymphocytes et des monocytes qui adhèrent à la paroi et la production de la protéine de chimioattraction des monocytes-1 (MCP-1) entraine leur diapédèse34. Après avoir pénétré l‟intima, les monocytes deviennent des macrophages; ils modulent l‟expression des récepteurs de lipoprotéines, ce qui leur permet d‟absorber les particules de cholestérol oxydées en circulation et de se transformer en cellules spumeuses. Parallèlement, le processus inflammatoire est entretenu par les lymphocytes T qui produisent des cytokines, molécules induisant la réplication des cellules musculaires lisses contribuant à l‟épaississement de l‟intima34. L‟épaississement de l‟intima par des cellules musculaires lisses uniquement (Figure 1A), en absence de macrophages chargés de lipides, est aussi appelé épaississement adaptatif de l‟intima puisqu‟il dépend du débit sanguin et de la tension exercée sur la paroi35. Lorsque ce phénomène se produit par l‟entremise d‟une matrice riche en protéoglycans avec une accumulation de lipides extracellulaires 4 et une
perte de cellules musculaires lisses35, on parle d‟épaississement pathologique de l‟intima (Figure 1B/C). On parle ensuite d‟athérome (ou plaque) lorsqu‟il se produit une nécrose dans un amas de lipides. Le noyau nécrotique peut se recouvrir d‟une chape fibreuse plus ou moins épaisse, calcifiée ou non4 (Figure 1D). Plus cette chape fibreuse est mince et plus il y a de cellules inflammatoires, plus la lésion est vulnérable, c‟est-à-dire plus elle est à risque causer une thrombose en s‟érodant ou en se rupturant. Lorsque qu‟une lésion s‟érode ou se rupture, il y a exposition du facteur tissulaire (produit par les cellules inflammatoires), ce qui déclenche la cascade de coagulation1. Lorsqu‟il y a thrombose dans une artère, celle-ci peut devenir soudainement obstruée et le territoire normalement perfusé par cette artère devient ischémique. Le thrombus peut aussi s‟emboliser, c‟est-à-dire quitter le site où il s‟est formé et migré dans la circulation sanguine pour éventuellement se loger à un autre endroit et potentiellement y obstruer le flot sanguin. L‟ischémie d‟un tissu, si elle est maintenue pendant un certain laps de temps, mène à la nécrose (mort cellulaire); c‟est ce phénomène qui se produit lors d‟un infarctus du myocarde.
Figure 1: Aspect pathologique des lésions athérosclérotiques de bas grade. Adapté de
Virmani et al. Arterioscler Thromb Vasc Biol (2000) 4
Couleurs : en vert, les cellules musculaires lisses; en jaune, les lipides extracellulaires; en rouge, le sang ou la paroi; en blanc, fentes de cholestérol; en bleu, macrophages (cellules spumeuses); en orangé, noyau nécrotique; en violet, plaque calcifiée.
Glagov et al.36 ont démontré que la lésion athérosclérotique croît d‟abord excentriquement sans compromettre la lumière du vaisseau. Puis, il y a remodelage de la paroi artérielle qui accommode ce changement et qui rend la maladie silencieuse pendant la majeure partie de son évolution. À un certain point de l‟expansion, la lésion débute sa progression vers la lumière et c‟est à ce moment que la sténose se manifeste et qu‟on peut déceler la pointe de l‟iceberg à l‟angiographie (Figure 2).
(C) (D)
(A) (B)
Épaississement de
l’intima Xanthome intimal
Épaississement pathologique de l’intima
Athérome à chape fibreuse
Figure 2: Progression de l'athérosclérose telle que décrite par Glagov
.
Tiré de Berman DS, 200637La lésion athérosclérotique peut prendre de l‟expansion progressivement jusqu‟à obstruer partiellement ou « sténoser » la lumière d‟un vaisseau, responsable de symptômes chroniques tels l‟angine de poitrine ou l‟ischémie cérébrale transitoire lorsque cette sténose occupe plus de 50-70% de la lumière. Cependant, une plaque encore non-obstructive et non-visualisable par angiographie peut tout de même se rompre ou s‟éroder et causer un évènement cardiovasculaire majeur38. D‟ailleurs, les évènements cardiovasculaires majeurs, tels l‟infarctus du myocarde ou l‟AVC sont le plus souvent produits par des lésions initialement peu obstructives (sténose de <50%), lorsqu‟il y a une thrombose subite par rupture de la chape fibreuse de la plaque ou simplement par érosion de la chape4. L‟évolution pathologique de la maladie athérosclérotique vers un évènement cardiovasculaire majeur ne peut être réduite à un continuum de lésions précoces à des lésions plus avancées (Figure 3).
Artère normale Pas de plaque Pas de sténose
Expansion compensatoire.
Lumière inchangée, pas de sténose Limite de
l‟expansion. Début de sténose.
Phénomène de Glagov
Modéré Sévère
Figure 3: Classification des lésions athérosclérotiques. Tiré de Virmani et al. Arterioscler
Thromb Vasc Biol (2000)4.
Ce schéma illustre les multiples relations entre les différents types pathologiques de lésions et le lien entre chacune d’elles et les évènements cardio-vasculaires.
L‟athérosclérose se distribue asymétriquement et envahit la paroi artérielle de façon hétérogène39,40, se logeant préférentiellement dans des régions où les forces de cisaillement sont faibles41-43.
Les forces de cisaillement représentent la force tangentielle appliquée sur une aire de la paroi vasculaire par la résultant frottement du flot sanguin à la surface endothéliale du vaisseau44. On croit qu‟elles ont un effet sur la structure et la fonction de cette aire de paroi45. Lorsque les artères suivent un trajet linéaire, les forces de cisaillement sont antérograde : le flux sanguin est laminaire et unidirectionnelle (de la circulation proximale à la circulation distale)45. Ce stimulus mécanique enclenche un cascade biochimique : diminution de l‟activité des récepteurs de l‟angiotensine-II de type I qui entraine une réduction de la production de NADPH oxydase et des espèces réactives de l‟oxygène, préservant ainsi la biodisponibilité du monoxyde d‟azote (NO)46, car les espèces réactives de l‟oxygène accélèreraient la dégradation du NO47. À l‟inverse, lorsque les forces de
Mort subite Mort subite
Mort subite Sténose > 75% Plaque fibro-calcifiée Thrombose Épaississement de l’intima Rupture de la chape fibreuse (rare )
Inflammation, mort cellulaire, consolidation du noyau lipidique, protéolyse, angiogenèse, hémorragie intra-plaque, calcification Rupture (noyau nécrotique) Guérison Guérison Thrombose Formation d‟une chape fibreuse Xanthome
initial Formation d‟un noyau nécrotique
avec la masse intimale Nodule calcifié Athérome à chape fibreuse mince Athérome à chape fibreuse Épaississement pathologique de l’intima Érosion
cisaillement sont faibles ou oscillatoires auraient un effet opposé, i.e. pro-athérogène. Il y a une composante rétrograde au vecteur de force de cisaillement qui engendre de nombreuses perturbations biochimiques : la production de NO est diminuée, la production d‟espèces réactives de l‟oxygène est augmentée, les monocytes s‟accumulent dans l‟intima, des molécules d‟adhésion cellulaire (VCAM-1, ICAM-1) et de l‟endothéline-1 (ET-1) sont sécrétées48, de même que des facteurs inflammatoires (TNF-α), il se produit une régulation à la hausse de la captation de LDL par l‟endothélium45. Des forces de cisaillement augmentées transitoirement et de façon antérograde, comme c‟est le cas lors d‟une activité physique, améliorent la fonction endothéliale48. Ainsi, les forces de cisaillement détiennent un rôle déterminant dans la fonction endothéliale, dans l‟oxydation des lipoprotéines et dans le processus athérosclérotique49.
1.1.2 Marqueur de substitution
Comme l‟athérosclérose peut évoluer insidieusement sur plusieurs dizaines d‟années, l‟utilisation de la mortalité et des évènements cardiovasculaires majeurs comme critères d‟évaluation peut suffire pour des études épidémiologiques ou encore des études de prévention dans des populations avec un risque cardiovasculaire intermédiaire ou élevé. Cependant, pour des études de prévention chez des individus à faible risque cardiovasculaire, ces critères d‟évaluation demandent de nombreuses années, voire des décennies, de suivi rendant les résultats représentatifs des derniers stades de la maladie plutôt que des facteurs de risque présents à son apparition et sa progression initiale50. L‟angiographie de la lumière artérielle fait partie de la pratique clinique courante permettant de visualiser la lumière artérielle et le degré d‟obstruction de celle-ci. Les découvertes de Glagov sur la progression des lésions athérosclérotiques illustrent cependant que lorsqu‟on veut observer la maladie athérosclérotique à des stades précoces, on doit se tourner vers l‟imagerie de la paroi artérielle. En tomodensitométrie, un score calcique peut être calculé au niveau des artères coronaires en tant qu‟indice de présence d‟athérosclérose, mais ce score s‟adresse à des patients à risque intermédiaire puisque les lésions doivent être calcifiées pour être visualisées. C‟est dans le but de décrire et étudier des lésions athérosclérotiques plus jeunes que des marqueurs de substitution ont été étudiés. Il existe
des marqueurs fonctionnels qui témoignent de la fonction endothéliale en faisant état de la distensibilité et de la rigidité des artères. La vélocité de l‟onde de pouls, la dilatation médiée par le débit et l‟hyperémie réactive constituent trois paramètres de distensibilité/rigidité. La vélocité de l‟onde de pouls (pulse wave velocity, PWV) est un paramètre indicateur de la rigidité artérielle qui est calculé par le délai entre l‟arrivée de l‟onde de pouls d‟une artère plus distale en comparaison avec une artère plus proximale, ce délai étant mis en relation avec la longueur des segments51. La dilatation médiée par le débit (flow-mediated dilatation, FMD) est mesurée par échographie en comparant le diamètre de repos d‟une artère et son diamètre maximal obtenu après le retrait d‟une compression mécanique externe. En d‟autres mots, le FMD de l‟artère brachiale est obtenu en imageant par échographie l‟artère brachiale au repos et par la suite, après avoir comprimé le bras avec une pression de 200 millimètres de mercure pendant quelques minutes, en imageant le diamètre de l‟artère brachiale dans la minute suivant le relâchement de la compression du bras52. Selon les résultats d‟une méta-analyse regroupant un total de près de 15 000 sujets, le FMD est inversement associé au risque d‟évènements cardiovasculaires53. L‟hyperémie réactive est aussi mesurée avec un protocole de compression et décompression : on compare l‟amplitude de l‟onde de pouls (mesurée par échographie-Doppler) au repos à celle obtenue dans la minute suivant la décompression du membre52.
On se sert aussi de marqueurs structurels, qui sont plus fiables et plus représentatif du processus athérosclérotique à long terme, tels que l‟épaisseur de l‟intima-média de l‟artère carotidienne (CIMT)54,55, paramètre le plus utilisé jusqu‟à présent en tant que marqueur de substitution du fardeau d‟athérosclérose, ou encore l‟aire ou le volume de la paroi artérielle et l‟aire ou le volume de la plaque athérosclérotique, qui sont des paramètres qui ont fait leur entrée plus récemment en tant que marqueurs du risque cardiovasculaire. Pour mesurer l‟épaisseur de l‟intima-média, on peut utiliser les artères fémorales, brachiales et coronaires, mais la majorité des laboratoires ont utilisé les artères carotidiennes comme référence puisqu‟elles sont larges, superficielles et relativement éloignées des mouvements du cœur et de la respiration permettant une imagerie de meilleure qualité56. Dans les études de prévention cardiovasculaire, la technique la plus couramment utilisée pour évaluer la
paroi artérielle est la mesure du CIMT par échographie. L‟évaluation de la paroi artérielle carotidienne en tant que marqueur du risque cardiovasculaire a été validée : une méta-analyse a conclu qu‟une déviation de 0.1mm par rapport à la moyenne est associé à une augmentation du risque d‟infarctus du myocarde de 15% et du risque d‟AVC de 18% et qu‟une déviation d‟un écart-type par rapport à la moyenne entraine une élévation de 26% du risque relatif d‟infarctus du myocarde et de 32% du risque relatif d‟AVC57. Le CIMT est relié à la maladie vasculaire périphérique58. Même chez les sujets asymptomatiques, le CIMT aurait une valeur prédictive d‟évènements cardiovasculaires majeurs aussi puissante que le score de Framingham59, score utilisé pour prédire le risque cardiovasculaire en prenant en compte l‟âge, le sexe, la tension artérielle, le cholestérol total, le cholestérol High-Density Lipoproteins (HDL), le diabète et le tabagisme. Aussi, une mesure d‟épaisseur de l‟intima-média prise au niveau de l‟artère carotidienne (CIMT) serait représentative du fardeau d‟athérosclérose systémique puisqu‟elle corrèle avec les valeurs d‟IMT mesurées au niveau des artères brachiales et fémorales60.
Lorsqu‟il y a présence d‟un ou plusieurs facteurs de risque, le CIMT croît plus rapidement, de même que la probabilité d‟avoir des lésions athérosclérotiques plus avancées61. Le CIMT est associé aux facteurs de risque cardiovasculaires traditionnels : âge avancé62, sexe masculin63, race noire63, faible taux de cholestérol HDL62, taux élevé de cholestérol Low-Density Lipoprotein (LDL)64, glycémie à jeun élevée65, tension artérielle élevée63, obésité63 et circonférence de taille élevée62. L‟ensemble de ces associations, auparavant robustement démontrées avec d‟autres méthodes, suggère que l‟imagerie de la paroi artérielle carotidienne constitue un marqueur adéquat pour évaluer la relation entre un facteur et le risque cardiovasculaire.
Cependant, malgré l‟abondance d‟études ayant utilisé le CIMT déterminé par échographie, plusieurs limitations méthodologiques minent sa fiabilité et sa validité en tant que modalité d‟imagerie de l‟athérosclérose carotidienne. D‟abord, selon l‟artère utilisée (carotide externe, carotide interne, carotide commune, bifurcation carotidienne), chez un même individu, on observe des différences importantes. Le segment le plus souvent impliqué dans la mesure du CIMT est la carotide commune puisque cette section est plus près de la
surface de la peau et permet d‟obtenir des résultats qui ont une reproductibilité satisfaisante66. Cependant, les sites les plus propices à la formation de plaques athérosclérotiques sont la bifurcation carotidienne et la carotide interne puisque le flot sanguin y est plus turbulent67, deux sections plus difficilement visualisables par échographie. De plus, le positionnement de la sonde échographique et les variations anatomiques interindividuelles dans le trajet de la carotide par rapport à la surface de la peau font varier l‟angle d‟interrogation de la paroi et par le fait-même, l‟épaisseur mesurée68. Ensuite, le CIMT jauge la paroi carotidienne de façon discrète au niveau de l‟arc de circonférence couvert sur la coupe, souvent par deux mesures : environ 5 degrés à 6h, near wall, et environ 5 degrés à 12h, far wall69 (Figure 4).
Figure 4: Mesure de l’épaisseur intima-média par échographie. Adapté de Stein et al. J Am
Soc Echocardiogr (2008)69. On y observe la
coupe longitudinale d’une artère carotidienne avec la lumière hypoéchogène (en noir) et, entre les deux points rouges, la paroi artérielle carotidienne.
Dans cette perspective, un épaississement de la paroi entre 1h et 5h ne sera pas visualisé. Puisque l‟athérosclérose est une pathologie qui se distribue asymétriquement,
l‟extrapolation à partir de mesures d‟épaisseur en deux points sur l‟arc de circonférence pourrait fournir un portrait inexact de l‟état de la paroi artérielle (Figure 5).
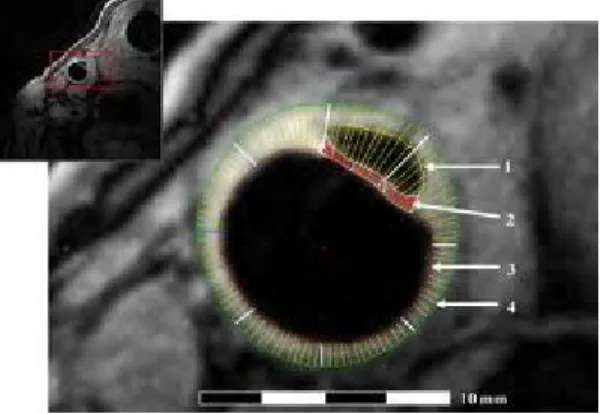
Figure 5: Coupe transversale en imagerie par résonance magnétique de la paroi artérielle carotidienne. Tiré de Duivenvoorden et al. Atherosclerosis (2009)70.
On y repère aisément la lumière artérielle au centre (en noir), la paroi artérielle mesurée en plusieurs rayons (en jaune et en blanc). Une plaque est visualisée à 13h sur cette coupe.
L‟imagerie tridimensionnelle pourrait pallier aux faiblesses de la mesure échographique de l‟épaisseur de la paroi (CIMT) en éliminant les variations dues à l‟angle d‟interrogation de la paroi, en englobant à la fois la carotide commune, interne et externe, en l‟imageant de façon continue (Figure 6) et en rendant compte de tout l‟arc de circonférence. Effectivement, il a été démontré que l‟imagerie par résonance magnétique (IRM) fournit des mesures plus exactes71 et plus reproductibles que le CIMT72,73. Dans un contexte de recherche plus appliqué, les travaux de Migrino et son équipe74 illustrent la sensibilité supérieure de l‟imagerie tridimensionnelle par IRM comparativement à la mesure bidimensionnelle de CIMT par échographie pour détecter un changement. Dans le cadre de cette étude, les artères carotidiennes de 26 individus (âgés de 65 à 69 ans, souffrant de maladie athérosclérotique cardiovasculaire ou cérébrovasculaire, avec une plaque d‟athérosclérose connue de diamètre supérieur à 1.1mm), ont été imagés avant et après un traitement de six mois (médicament utilisé pour traiter la dyslipidémie). On recherchait à détecter une changement évaluant la paroi artérielle à la fois en mesurant le CIMT par échographie et le volume de plaque carotidienne par IRM (entre zéro et six mois). La
2.0% du VTPC alors que la mesure de CIMT n‟a pas mis en évidence de différence significative entre le début et la fin de l‟intervention.
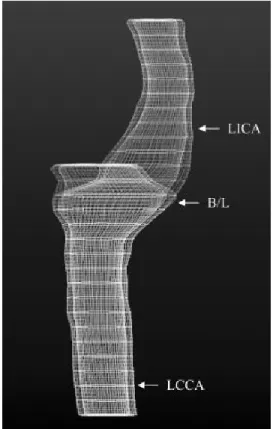
Figure 6: Construction d'un modèle tridimensionnel de paroi carotidienne par IRM. Tiré
de Varghese et al. J Magn Reson Imaging (2006)75
LCCA: artère carotidienne commune gauche; B/L : bifurcation; LICA : artère carotidienne interne gauche. On peut déceler les limites de la paroi artérielle.
La mesure du volume de paroi carotidienne peut aussi s‟effectuer par échographie tridimensionnelle. Cependant, elle présente une faible précision dans l‟épaisseur et la superposition des coupes comparativement à d‟autres appareils conçus pour l‟imagerie tridimensionnelle, comme la tomodensitométrie (TDM) et la résonance magnétique (IRM)
76. L‟échographie intravasculaire (IVUS) est une technique qui a le potentiel d‟améliorer la
précision de l‟échographie77. Cependant, son effractivité limite l‟utilisation de l‟IVUS en recherche en prévention primordiale. Dans le même ordre d‟idée, bien que non-effractive, la TDM comporte une forte dose de radiations ionisantes et des produits de contraste qui
justifiée en vue d‟un traitement, elle ne l‟est pas chez un sujet en santé en vue d‟une étude, surtout si un suivi avec de multiples séances d‟imagerie est prévu. La tomographie par émission de positrons (TEP), autre modalité d‟imagerie de la paroi artérielle, comporte aussi des radiations ionisantes, de par les traceurs qui sont utilisés. En IRM, des protocoles standardisés ont été décrits afin d‟optimiser la résolution, le ratio signal-bruit et la suppression du sang tout en rendant la durée cliniquement acceptable78. Aussi, l‟automatisation des techniques augmente la reproductibilité des mesures, diminue le temps d‟analyse et atténue la variabilité entre les observateurs et entre les centres78. Ainsi, la résonance magnétique est applicable dans le monitoring de la taille de lésion carotidienne, de sa progression ou de sa régression79.
1.2 L’activité physique
1.2.1 Concepts et définitions
L‟activité physique est définie comme « un mouvement du corps produit par les muscles squelettiques résultant en une dépense calorique »80 d‟un individu pour un temps donné. Il existe un nombre important de méthodes pour mesurer l‟activité physique. Contrairement à d‟autres concepts dont la définition est très restreinte, par exemple la glycémie, le concept d‟activité physique est très large.
La condition physique est un concept différent de l‟activité physique qui peut effectivement servir à estimer l‟activité physique, mais dépend aussi de facteurs ponctuels (exemples : état de fatigue, présence d‟une infection mineure), de facteurs constitutionnels et/ou génétiques (adiposité, la masse maigre, taux d‟hémoglobine) et de facteurs découlant du mode de vie (tabagisme, diète)81. Par ailleurs, la relation entre la condition physique et la santé est bidirectionnelle, c‟est-à-dire qu‟il a été démontré que l‟aptitude physique est un déterminant important de la mortalité82, mais l‟état de santé influence aussi la condition physique83. Pour des fins de recherche en prévention, il y a lieu de se demander si les facteurs génétiques et environnementaux qui jouent un rôle dans la variabilité interindividuelle du niveau de condition physique « de base » peuvent être des déterminants
indépendants du risque de mortalité, devenant ainsi des facteurs confondants.
1.2.2 Recommandations actuelles
Les lignes directrices de la Société Canadienne de Physiologie de l‟Exercice en matière d‟activité physique chez les adultes de 18 à 64 ans84, similaires à celles de l‟Organisation Mondiale de la Santé85, comprennent :
- 150 minutes d‟activité physique modérée à vigoureuse par semaine (réparties en périodes de 10 min et plus)
- Un entrainement musculaire deux jours par semaine ou plus
Une activité physique modérée se définit par une intensité entre trois et six équivalents métaboliques (METs), soit de trois à six fois la dépense énergétique basale (au repos assis, 1 METs ou 1 kcal/kg/h) tandis qu‟une activité vigoureuse se définit par une intensité supérieure à six METs85.
1.2.3 Mesure de l‟activité physique
L‟activité physique habituelle d‟une personne comporte plusieurs dimensions, soit la fréquence, l‟intensité, le temps (durée) et le type d‟activité80. Idéalement, ces quatre dimensions devraient être examinées. Lorsqu‟il est question de l‟activité physique en tant que paramètre de santé, la mesure obtenue devrait être représentative des variations quotidiennes86, de même que saisonnières et tenir compte des divers domaines où une dépense énergétique peut être effectuée87 (travail, activités domestiques, loisirs et transports). Créer un protocole qui permet de rendre compte le plus exactement possible de l‟activité physique quotidienne ou hebdomadaire habituelle d‟un sujet constitue un défi important en recherche.
Par calorimétrie, c‟est-à-dire en mesurant la quantité de chaleur dégagée, on peut évaluer le coût énergétique d‟une activité effectuée par un individu pendant un laps de temps donné dans un environnement contrôlé88. Cette méthode permet de quantifier avec précision le
coût calorique d‟une activité spécifique, mais est peu appropriée pour mesurer l‟activité physique spontanée d‟un individu puisqu‟elle restreint le comportement naturel, l‟individu étant confiné dans un laboratoire88. La méthode à l‟eau doublement marquée repose sur la mesure de la production de CO2 en tant que marqueur de la dépense énergétique. Le sujet
ingère de l‟eau où l‟hydrogène et l‟oxygène sont tous deux marqués et la différence entre l‟élimination de l‟oxygène et l‟élimination de l‟hydrogène est déterminée par l‟excrétion de CO2. On objective ainsi la dépense énergétique totale d‟un organisme pendant une période
prédéterminée (dépassant rarement une ou deux semaines), qu‟on peut comparer à la dépense énergétique basale83. Puisque les mesures déterminant l‟énergie dépensée nécessitent l‟utilisation d‟isotopes, ce type de protocole est très coûteux, ce qui le rend applicable surtout pour des études avec un nombre restreint de particpants. Ces méthodes ont contribué à documenter la dépense énergétique associée à des activités spécifiques, données qui peuvent été utilisées pour dans d‟autres modalités d‟évaluation de l‟activité physique en tant que comportement de santé.
On peut mesurer l‟activité physique par enquêtes (questionnaire, journal d‟activité) ou par détecteurs de mouvements (podomètre, accéléromètre), par monitoring de fréquence cardiaque. Les enquêtes permettent de tenir compte des dimensions de l‟activité physique et des divers domaines où elles peuvent être effectuées, mais sont sujettes aux biais de rappel et de désirabilité sociale86 alors que les journaux d‟activité comportent une charge de travail importante pour le participant. Les appareils électroniques détecteurs de mouvement fournissent des données objectives et requièrent un investissement minime du participant, mais évaluent inégalement les divers types d‟activité (exemple : vélo, natation) et comportent une variabilité inter-instrument dans la sensibilité au mouvement88. Le monitoring de fréquence cardiaque est plus représentatif de toutes les activités, mais ne peut différencier l‟augmentation de la fréquence cardiaque due à un facteur psychologique de celle due à un facteur physique86. Aussi, la variabilité individuelle dans la fréquence cardiaque basale et à l‟effort rend un test de condition cardiorespiratoire nécessaire pour associer les fréquences cardiaques de chaque individu à la dépense énergétique, ce qui rend cette méthode plus difficilement applicable à large échelle qu‟elle ne le parait. Le monitoring de l‟apport alimentaire permet d‟évaluer la dépense énergétique en dehors d‟un
environnement contrôlé et sur une plus longue période, mais impose une grande charge de travail au participant88 et comporte aussi un grand risque de modification du comportement pendant l‟étude, en plus d‟être affecté par la variabilité dans les mesures du monitoring du poids et du taux de tissu adipeux qui doivent être effectuées concomitamment.
L‟activité physique peut aussi être inférée par la mesure de la condition physique d‟un individu (force, endurance, flexibilité, capacité aérobique, capacité anaérobique, composition corporelle)83. Ces divers éléments ne sont pas nécessairement tous évalués lorsqu‟on parle de condition physique (fitness). En recherche, lorsqu‟on réfère au „‟fitness‟‟ ou à la condition physique, le plus souvent, c‟est seulement la condition cardio-respiratoire (ou capacité aérobique) qui a été évaluée. La condition cardio-respiratoire peut être mesurée en laboratoire par un test de consommation maximale d‟oxygène (VO2max) sur
tapis roulant ou ergocycle ou peut-être estimée sur le terrain par des épreuves aérobiques (tests Léger-Boucher89, Cooper90, Margaria91 et autres).
1.3 Activité physique et athérosclérose : structure et fonction de la paroi artérielle
Les effets de l‟activité physique sur les facteurs de risque cardiovasculaires ne semblent expliquer que 59% de la réduction du risque cardiovasculaire qu‟elle apporte92,93 (Figure 7). Mora et al. ont étudié 27 055 femmes âgées de 55 ans en moyenne apparemment en santé (sans maladie cardiovasculaire). Ils ont consigné la présence de diabète, d‟hypertension, de tabagisme, d‟histoire parentale d‟infarctus du myocarde avant 60 ans, la consommation d‟alcool, le statut pré ou post-ménopause, l‟utilisation d‟hormonothérapie de substitution, la consommation de gras saturés, l‟apport de fruits et légumes, l‟apport de fibres alimentaires. Ils ont évalué leur IMC, leur hémoglobine glyquée, leur bilan lipidique traditionnel (cholestérol total, HDL et LDL), leurs niveaux sanguins de lipoprotéine (a), d‟apolipoprotéine-A1 et B-100, leur créatininémie, leur homocystéinémie, leur niveau sanguin de protéine C-réactive (haute sensibilité), de fibrinogène et d‟ICAM-1. Ces participants étaient divisées en quatre groupes d‟activité physique (évaluée par questionnaire) : dépense énergétique de moins de 200, entre 200 et 599, entre 600 et 1499 et plus de 1500 kilocalories par semaine. Les participantes ont été suivies pendant une
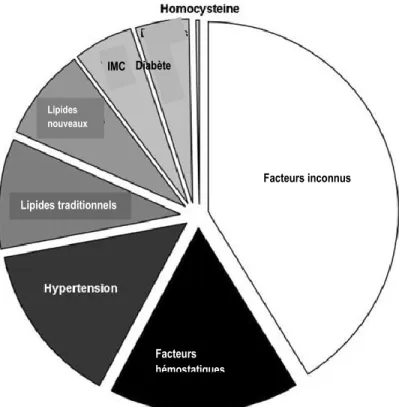
enregistrés (AVC, infarctus du myocarde, pontages aorto-coronariens, interventions coronaires percutanées). En comparaison au groupe le plus sédentaire (moins de 200 kilocalories par semaine), les groupes plus actifs démontraient une incidence d‟évènements cardiovasculaires et cérébrovasculaires réduite de 27% (200 à 599 kilocalories/semaines), 32% (600 à 1499 kilocalories/semaine) et 41% (plus de 1500 kilocalories/semaine). Les contributions respectives des divers paramètres cardiométaboliques à la diminution du risque cardiovasculaire selon le niveau d‟activité physique sont illustrées dans la figure 7. On y remarque que 41% de cette réduction du risque d‟évènements cardiovasculaires demeurent inexpliquée par les facteurs de risque connus. Dans un article de synthèse, Green et al. ont proposé que ce 41% restant pourrait s‟expliquer en partie par des effets directs sur les vaisseaux 94.
Figure 7: Facteurs médiant l'effet de l'activité physique sur le risque cardiovasculaire. Tiré de Mora et al. Circulation (2007)93
D‟un point de vue chronologique, les premiers changements mesurables induits par l‟activité physique sont des changements fonctionnels, suivis par les changements
Facteurs inconnus Diabète Lipides nouveaux Lipides traditionnels Facteurs hémostatiques IMC
et la structure artérielle implique plusieurs mécanismes physiopathologiques différents. Il a été postulé que l‟activité physique induirait d‟abord une amélioration de la fonction vasculaire (capacité de vasodilatation), puis qu‟à l‟obtention d‟un effet d‟entrainement, la structure vasculaire se modifiait (augmentation du calibre artériel) avec un retour de la capacité de vasodilatation à l‟état de base48,96.
1.3.1 Hémodynamie, tension artérielle et oxydation
Il a été démontré in vitro qu‟une augmentation chronique de la tension artérielle (en hypertension artérielle) a un effet pro-athérogénique sur l‟endothélium en diminuant l‟expression d‟eNOS et en augmentant la libération de VCAM-1, d‟ICAM-1, d‟ET-1 et d‟espèces réactives de l‟oxygène.97 Il a été postulé que l‟exercice, produisant des augmentations transitoires de la tension artérielle, aurait un effet différent sur les facteurs d‟adhésion cellulaire, d‟inflammation et d‟oxydation48. Cet effet est encore controversé et a été peu exploré.
L‟exercice, surtout vigoureux (et particulièrement l‟effort vigoureux pratiqué de façon sporadique), occasionne un stress oxydatif; à l‟effort, le muscle qui se contracte produit des espèces réactives de l‟oxygène98. Cependant, la production d‟espèces réactives de l‟oxygène à l‟effort aurait pour effet une activation des enzymes anti-oxydantes endogènes : augmentation de la superoxide dismutase99 et de la glutathione peroxidase100 via l‟activation du facteur de transcription du facteur nucléaire κB101. Ainsi, l‟adaptation à l‟exercice produirait une augmentation des défenses anti-oxydantes du corps102 et aurait un effet anti-athérogène103.
1.3.2 Inflammation
Puisque l‟athérosclérose est une réaction inflammatoire complexe à différents stimuli, les médiateurs de l‟inflammation jouent un rôle déterminant dans le développement de la pathologie. L‟équilibre dans l‟activation et la polarisation des macrophages agit sur le métabolisme des lipides, la réponse inflammatoire, l‟apoptose endothéliale, le stress oxydatif, biodisponibilité du NO, le remodelage vasculaire et l‟athérogénèse104,105. Alors
que les macrophages M1 produisent des cytokines inflammatoires, les macrophages potentiellement M2 produiraient des cytokines ayant un effet opposé105. L‟activité physique favoriserait l‟activité des macrophages M2 (antiathérogènes) par rapport aux M1 (pro-athérogènes)106.
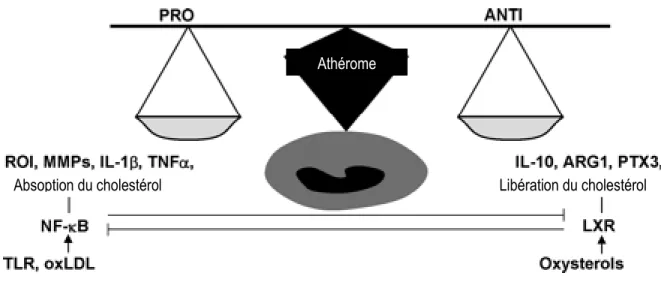
Figure 8. L’équilibre de l’activation et la polarisation des macrophages. Tiré de Mantovani, Arterioscl Thromb Vasc Biol (2009)105
À gauche le phénotype M1 et à droite le phénotype M2. oxLDL: LDL oxydés; ROI: intermédiaires oxygénés réactifs; MMPs: métalloprotéases; ARG1: arginase 1; PTX3: pentraxine 3; LXR: Récepteur X du foie; TLR: Récepteur de type Toll.
1.3.3 Vasoconstriction et vasodilatation
Maiorana et al. ont démontré que, chez des individus atteints de maladie cardiovasculaire, l‟activité physique améliore la fonction de vasodilatation107. Cette équipe a étudié la capacité de vasodilatation artérielle en mesurant les débits sanguins à travers au niveau de l‟avant-bras suite à une compression mécanique et suite à une perfusion d‟acétylcholine chez 12 hommes insuffisants cardiaques qui ont été soumis à un programme d‟exercice de huit semaines incluant trois séances de 1h d‟exercice aérobique et de résistance excluant spécifiquement tout exercice impliquant une contraction de l‟avant-bras. Ils ont observé une
Libération du cholestérol Absoption du cholestérol
amélioration de la fonction de vasodilatation suite au programme d‟exercice. Par ailleurs, il semble plus difficile d‟améliorer une fonction vasculaire (capacité de vasodilatation) normale chez une population en santé, puisque le même programme d‟activité physique n‟a pas modifié la capacité de vasodilatation chez 19 sujets en santé107. Analogiquement, Meyer et al108 ont démontré qu‟un programme d‟exercice de six mois, à raison de trois séances de 1h par semaine, peut améliorer la capacité de vasodilatation (évaluée par la dilatation médiée par le débit (FMD)) chez des enfants obèses ayant une capacité de vasodilatation altérée. Similairement, Watts et al109 ont prouvé qu‟un programme d‟exercice de huit semaines pouvait augmenter le FMD chez de jeunes obèses ayant un FMD diminué. Il est possible qu‟une intensité plus importante soit nécessaire pour qu‟un bénéfice soit ressenti dans une population en santé. Kozakova et al. 112 ont évalué l‟activité physique par accéléromètre et ont mesuré la rigité artérielle carotidienne (établie par la distension de l‟artère carotidienne au cours du cycle cardiaque, ajustée selon la variation de tension artérielle) chez 432 individus ne présentant pas de facteur de risque cardiovasculaire. Ils ont observé une association négative entre le niveau d‟activité physique total et la rigidité artérielle. Par ailleurs, Ferreira et al. ont établi des associations négatives entre le VO2max et la rigidité artérielle, de même qu‟entre le VO2max et la
compliance artérielle chez 351 sujets en santé de 36 ans110.
Les évidences des modifications de la vasoconstriction sont moins solides. Quelques études se sont intéressées aux facteurs humoraux endothéliaux, notamment l‟ET-1 et l‟angiotensine II; ces dernières suggèrent un effet bénéfique de l‟exercice sur la fonction vasoconstrictrice chez des sujets âgés via l‟ET-1 et des sujets avec maladie cardiovasculaire via l‟angiotensine II111.
D‟un point de vue plus technique, le tonus vasculaire peut modifier les mesures structurelles de la paroi artérielle. Les résultats d‟une étude effectuée sur des sujets chez qui le diamètre artériel et l‟épaisseur de la paroi artérielle ont été mesurés avant et après l‟administration de nitroglycérine (vasodilatateur) suggère que l‟élargissement du calibre artériel résulterait en une mesure de CIMT plus faible112. Il faut tenir compte de ce facteur confondant potentiel en standardisant les protocoles pour que la paroi artérielle soit
examinée dans la même phase du cycle cardiaque, mais surtout le considérer lorsque des données provenant d‟études différentes sont comparées.
1.3.4 Intensité
Il existe peu d‟évidence scientifique démontrant une association entre une intensité d‟activité physique particulière et la structure artérielle. Goto et al96,113 ont tenté de répondre à cette problématique en évaluant l‟effet de trois programmes d‟entrainement sur ergocycle: léger (25% du VO2max), modéré (50% du VO2max) et élevé (75% du VO2max)
sur la fonction artérielle. Les 26 participants ont été soumis à trois mois d‟un programme d‟activité physique à raison de cinq à sept séances de 30 minutes par semaine. Selon leurs résultats, l‟activité physique légère ne serait pas suffisante pour induire des changements dans la fonction de vasodilatation endothélium-dépendante, l‟activité modérée améliorerait cette fonction alors que l‟activité physique intense n‟entrainerait pas d‟amélioration, possiblement en raison d‟un stress oxydatif augmenté. Tel qu‟expliqué dans la section 1.3.1, le muscle squelettique produit des radicaux libres. Lorsque l‟intensité de l‟exercice est modérée, l‟organisme a la capacité de « métaboliser » ces déchets, résultant en l‟absence de stress oxydatif. Lorsque l‟exercice est pratiqué à une intensité plus élevée, la production de radicaux libres peut dépasser la capacité des défenses anti-oxydantes corporelles et induire un stress oxydatif de façon aigüe. Cependant, lorsque l‟activité physique d‟intensité vigoureuse est pratiquée régulièrement, un effet d‟entrainement est obtenu : les défenses anti-oxydantes de l‟organisme sont donc accrues102. Cette hypothèse est supportée par les résultats de l‟étude de Kozakova et al. 111 : en mesurant l‟intensité de l‟activité physique par accélérométrie chez des sujets en santé, ils ont illustré que la pratique d‟activité physique d‟intensité élevée (supérieure à 5724 comptes/minute, ce qui correspond à 8 METs114) dans les loisirs prédisait une diminution de l‟IMT sur 3 ans alors que le niveau d‟activité physique quotidien total (nombre de comptes total dans la journée) n‟avait pas cette capacité prédictive115,116.
1.4 Recension des écrits sur l’association entre l’activité physique et la structure artérielle carotidienne
La pertinence de l‟activité physique dans la prise en charge en prévention secondaire cardiovasculaire (c‟est-à-dire dans le but de ralentir la progression de la maladie et limiter les complications) n‟est plus à débattre117. Jusqu‟à présent, en prévention primaire (i.e. chez des individus ayant des facteurs de risque de maladie cardiovasculaire), plusieurs études ont été conduites pour vérifier la relation entre l‟activité physique et la structure artérielle carotidienne : la majorité converge vers une association inverse entre l‟activité physique et l‟épaisseur de la paroi artérielle118. Cependant, les résultats des études portant sur des populations sans facteur de risque sont plus rares et elles divergent de façon notable. Voici une revue non-systématique de la littérature actuelle en matière de prévention primordiale de la maladie athérosclérotique, c‟est-à-dire les études menées sur des populations ne présentant aucun facteur de risque ou présentant comme seul facteur de risque l‟âge avancé.
Chez des adultes âgés (45 à 64 ans), Folsom et al. ont rapporté une relation inverse entre le CIMT et l‟activité rapportée au travail, mais aucune association avec l‟activité physique rapportée dans les loisirs chez 14 430 adultes119. Cependant, Nordstrom et al. ont révélé une
association inverse entre l‟activité physique rapportée dans les loisirs et le CIMT chez 500 adultes d‟âge similaire (40 à 60 ans)120. Dans The Tromso Study, effectuée chez 3000 sujets de 45 à 60 ans suivis pendant 15 ans, l‟activité physique rapportée dans les loisirs est associée au CIMT chez les hommes seulement121. Dans une cohorte de 101 hommes de 60 ans (en moyenne) suivis pendant 25 ans, il a été observé que les hommes très actifs avaient des valeurs de CIMT, de score de calcification des artères coronaires (CACS) et d‟index d‟hyperhémie réactive plus faibles que les hommes légèrement à moyennement actifs122.. Considérées dans leur ensemble, les études concernant les sujets adultes âgés en santé tendent vers une association négative entre l‟activité physique et le fardeau d‟athérosclérose.
Chez des adultes d‟âge moyen, l‟association entre l‟activité physique aérobique chronique (c‟est-à-dire, de façon régulière pendant plusieurs années) et le CIMT a été étudiée chez des marathoniens (en moyenne 46 ans) qualifiés pour le marathon de Boston qui ont été comparés à leur conjoint(e) : aucune différence n‟a été notée au niveau de la rigidité artérielle de même qu‟au niveau du CIMT123. De façon similaire, chez des populations
d‟adultes sains (16 à 78 ans), aucun lien n‟a été établi entre l‟activité de loisirs et le CIMT124. Aussi, aucune différence n‟a été détectée entre des coureurs d‟endurance et des personnes sédentaires au niveau du CIMT125. Cependant, chez des hommes en santé d‟âges variés, une étude observationnelle et interventionnelle suggère que l‟activité physique induirait un remodelage expansif de la paroi artérielle126: mesure de CIMT plus faible, diamètre artériel plus élevés et rapport lumière/paroi plus faibles chez les sujets plus entrainés comparativement aux sujets sédentaires et leurs observations suivent la même tendance après un programme d‟intervention en activité physique126. Chez 432 adultes de 43 ans (en moyenne), l‟activité physique quotidienne mesurée par accélérométrie n‟était pas associée à la valeur du CIMT116. En bref, chez les adultes d‟âge moyen, on ne peut tirer de conclusions sur la littérature actuelle, les résultats révélant parfois une association négative entre l‟activité physique et le CIMT, parfois une absence d‟association.
Chez des jeunes adultes en santé, Juonala et al. ont démontré que le niveau d‟activité physique en enfance influence la progression sur six ans du CIMT au début de l‟âge adulte127. Dans une cohorte de 600 jeunes indiens (dont certains présentaient des facteurs de risque cardiovasculaire notamment tabagisme, obésité, diabète, syndrome métabolique), une association entre un niveau d‟activité faible et un CIMT élevé62 (significative après ajustement pour les facteurs de risque) a été remarquée. En 2013, un groupe danois a publié trois articles sur les relations entre l‟activité physique modérée à vigoureuse et le CIMT dans une cohorte suivie en enfance, en adolescence et à l‟âge adulte. Dans un premier temps, aucune association n‟a été établie entre l‟activité en enfance et le CIMT en enfance (transversalement)128. Similairement, le suivi de l‟activité physique en enfance en lien avec le CIMT à l‟adolescence n‟a pas révélé d‟association129. Finalement, une relation positive significative a été démontrée entre le niveau d‟activité physique à l‟adolescence et le CIMT à l‟âge adulte (environ 27 ans) : un niveau d‟activité plus élevé à l‟adolescence prédisait un CIMT plus élevé à 27 ans130. Dans cette même année, une étude d‟intervention en activité physique a publié des données dans une direction opposée131: en comparant les changements observés au niveau de l‟IMT des artères carotidiennes et fémorales suite à un programme d‟entrainement de vélo de huit semaines (à raison de trois séances de 30 minutes à 80% de la fréquence cardiaque maximale) chez neuf sujets en santé d‟en
moyenne 23 ans et de huit semaines de poursuite des activités habituelles chez cinq sujets contrôles, une diminution du CIMT ainsi qu‟une diminution du rapport paroi⁄lumière a été notée chez le groupe d‟intervention (aucun changement pour le groupe contrôle). Malgré la taille très petite de l‟échantillon, les résultats demeurent surprenants puisqu‟on a tendance à concevoir la paroi artérielle comme une structure se modifiant très lentement. Cependant, l‟étude a été critiquée132,133 du fait qu‟on ne mentionne pas si les participants ont été attribués au groupe intervention ou contrôle au hasard et on donne peu de détails sur les valeurs de base et au terme de l‟intervention des facteurs de risque (bilan lipidique, glycémie à jeûn, marqueurs d‟inflammation, circonférence de taille). Néanmoins, l‟indice de masse corporelle (IMC) moyen du groupe intervention représente un surpoids comparativement au groupe contrôle qui se situe dans un poids santé (différences non significatives sur le plan statistique).
La littérature sur les études menées dans des populations d‟athlètes comporte le même caractère mitigé: alors que certaines études ont conclu que la paroi artérielle des athlètes était plus mince que celle des contrôles134,135, d‟autres études n‟ont pas détecté de différence ou au contraire, ont mis en évidence, une paroi artérielle plus épaisse chez les athlètes136-138. Popovic et al. n‟ont pas détecté de différence au niveau du CIMT entre des athlètes et non-athlètes (de 20 à 40 ans)139. L‟étude de Rowley et al. a révélé que le CIMT de joueurs de squash d‟élite était plus faible que celui de sportifs récréatifs; des résultats qui suggèrent que, chez de jeunes adultes en santé, une plus grande dose d‟activité physique serait nécessaire pour qu‟une différence soit observée au niveau de la paroi artérielle carotidienne138.
Par ailleurs, il peut être intéressant de s‟attarder à certaines études sur l‟association entre la condition physique et la structure artérielle, une littérature connexe à celle qui fait l‟objet de cette revue. Même si un test de VO2max ne mesure pas directement l‟activité physique,
mais bien l‟aptitude physique (qui dépend de facteurs génétiques non-modifiables), l‟association entre la forme cardiorespiratoire et le CIMT est une mesure qui présente l‟avantage d‟être plus objective. Hägg et al. ont observé une corrélation inverse entre la forme cardio-respiratoire et le CIMT chez 29 sujets de 20-40 ans140. Ferreira et al. ont
rapporté une relation inverse significative entre le VO2max à 15 ans et le CIMT à 36 ans de
même qu‟entre le VO2max à 36 ans et le CIMT à 36 ans chez les hommes alors que ces
deux relations étaient positives et non-significatives chez les femmes110. Dans ce même échantillon, les changements longitudinaux de VO2max (entre l‟adolescence et l‟âge adulte)
n‟étaient pas corrélés avec le CIMT141.
Finalement, alors que les résultats des études actuelles chez les adultes âgés en santé convergent vers une association inverse entre l‟activité physique et le fardeau d‟athérosclérose, chez les adultes jeunes et d‟âge moyen, les données divergent de façon notable. Ainsi, la question, à savoir si l‟activité physique est associée au fardeau d‟athérosclérose indépendamment des facteurs de risque cardiovasculaire (incluant l‟âge avancé) demeure entière.
1.5 Limites des études actuelles et perspectives
Malgré les critiques qui ont été adressées à la mesure de la paroi artérielle par CIMT142,143, cette technique sous-tend la quasi-totalité de la littérature sur la relation entre l‟activité physique et le fardeau d‟athérosclérose chez une population dépourvue de facteurs de risque cardiovasculaire. Sa validité a été remise en question, notamment à cause des limites techniques pour imager les segments pertinents de l‟artère et du type de mesure prise en compte. De plus, sa sensibilité est remise en question, étant donné que la plus petite différence détectable est de 0.30mm alors que le changement annuel moyen est de 0.15mm143, particulièrement lorsqu‟on désire étudier des sujets à risque cardiovasculaire minimal qui ont des parois artérielles plus minces et pour qui une différence plus faible peut-être cliniquement significative. Les techniques d‟échographie (CIMT) éprouvées chez une population âgée ayant des lésions athérosclérotiques avancées50 pourraient se révéler inadaptées pour étudier les artères de jeunes individus sans facteurs de risque. La divergence des résultats pourrait s‟expliquer par les faiblesses de l‟instrument et de la procédure, c‟est pourquoi une nouvelle méthodologie est requise.
niveau de la carotide. La sensibilité de l‟imagerie tridimensionnelle de la paroi artérielle carotidienne par IRM pour détecter des lésions sous-millimétriques s‟avère excellente, ce qui en fait un outil ayant le potentiel d‟évaluer et suivre le développement de lésions athérosclérotiques à des stades précoces145. Elle a été désignée comme une solution à exploiter pour détecter les lésions de bas grade de façon adéquate50,56. Une modalité d‟imagerie tridimensionnelle apporte aussi la possibilité d‟investiguer la structure artérielle dans une autre perspective; l‟étude d‟un segment de paroi artérielle permet de mettre en lumière les variations d‟épaisseur de la paroi dans une même région, chez un même individu. L‟excentricité de la paroi carotidienne, a été définie par l‟écart-type entre les mesures d‟épaisseur de paroi sur un segment146 ou encore par le rapport de l‟épaisseur maximal et l‟épaisseur minimale de la paroi sur un même segment147. Ces mesures font état de l‟asymétrie et l‟hétérogénéité de la paroi artérielle, signant la présence d‟athérosclérose et prédisant un risque cardiovasculaire plus élevé147, 146. Jusqu‟à maintenant, au meilleur de mes connaissances, ces paramètres n‟ont pas été étudiés en relation avec le niveau d‟activité physique.
Dans la littérature actuelle sur l‟association entre l‟activité physique et l‟athérosclérose, beaucoup d‟études ont considéré comme « population en santé » des cohortes issues de la population générale. Cependant, ces groupes non-dépistés comprennent souvent des individus ayant des facteurs de risque cardiovasculaire ou des maladies cardiovasculaires. À titre d‟exemple, Rauramaa et al.148 ont recruté et suivi pendant six ans 140 hommes âgés entre 50-60 ans pour évaluer l‟effet d‟un programme d‟exercice progressif sur la
progression de leur CIMT. Le programme d‟entrainement débutait avec trois entrainements de 30-45 minutes par semaine pour les trois premiers mois pour atteindre cinq
entrainements par semaine par la suite, à une intensité de 40 à 60% de leur VO2max
(déterminé par leur fréquence cardiaque à l‟effort et selon un test de condition cardiorespiratoire effectué chaque année). Ils ont observé un ralentissement de la
progression du CIMT (en excluant les patients prenant des statines)148. Parmi ces hommes, 13 souffraient d‟une maladie cardiovasculaire, 3 étaient diabétiques et 24 étaient
hypertendus. Les études où les individus inclus selon l‟absence de maladie cardiovasculaire ou de facteurs de risque cardiovasculaire connus sont moins nombreuses et encore moins