Année 2018
Thèse N° 193
Les comorbidités au cours
de la polyarthrite rhumatoïde
THÈSE
PRÉSENTÉE ET SOUTENUE PUBLIQUEMENT LE 13/06/2018
PAR
Mlle.
Nezha EL BOUHI
Née Le 14 Juillet 1990 à Agadir
POUR L’OBTENTION DU DOCTORAT EN MÉDECINE
MOTS-CLÉS
Polyarthrite rhumatoide – Comorbidités - Maladies cardiovasculaires -
Infections- Ostéoporose
JURY
Mr.
Mr.
M
PmeP.
M
PmeP.
A. KHATOURI
Professeur de Cardiologie
R. NIAMANE
Professeur de Rhumatologie
N.TASSI
Professeur de Maladies Infectieuses
A. BELKHOU
Professeur agrégée de Rhumatologie
PRESIDENT
RAPPORTEUR
"
َﻚَﺘَﻤْﻌِﻧَﺮُﻜْﺷَﺃ ْﻥَﺃ ﻲِﻨْﻋ ِﺯ ْﻭَﺃ ِّﺏَﺭ
ْﻥَﺃ َﻭ ﱠﻱَﺪِﻟﺍ َﻭ ﻰَﻠَﻋ َﻮﱠﻴَﻠَﻋ َﺖْﻤَﻌْﻧَﺃ ﻲِﺘﱠﻟﺍ
ﻲِﻨْﻠ ِﺧْﺩَﺃ َﻮُﻫﺎَﺿ ْﺮَﺗ ًﺎﺤِﻟﺎَﺼَﻠَﻤْﻋَﺃ
َﻦﻴ ِﺤِﻟﺎﱠﺼﻟﺍ َﻙِﺩﺎَﺒِﻋ ﻲِﻓ َﻚِﺘَﻤْﺣَﺮِﺑ
."
ﻢﻴﻈﻌﻟﺍ ﷲ ﻕﺪﺻ
ﺔﻳﻵﺍ ﻞﻤﻨﻟﺍ ﺓﺭﻮﺳ
19
Au moment d’être admis à devenir membre de la profession médicale, je
m’engage solennellement à consacrer ma vie au service de l’humanité.
Je traiterai mes maîtres avec le respect et la reconnaissance qui leur
sont dus.
Je pratiquerai ma profession avec conscience et dignité. La santé de
mes malades sera mon premier but.
Je ne trahirai pas les secrets qui me seront confiés.
Je maintiendrai par tous les moyens en mon pouvoir l’honneur et les
nobles traditions de la profession médicale.
Les médecins seront mes frères.
Aucune considération de religion, de nationalité, de race, aucune
considération politique et sociale, ne s’interposera entre mon devoir et
mon patient.
Je maintiendrai strictement le respect de la vie humaine dés sa
conception.
Même sous la menace, je n’userai pas mes connaissances médicales
d’une façon contraire aux lois de l’humanité.
Je m’y engage librement et sur mon honneur.
LISTE DES
PROFESSEURS
UNIVERSITE CADI AYYAD
FACULTE DE MEDECINE ET DE PHARMACIE
MARRAKECH
Doyens Honoraires
: Pr. Badie Azzaman MEHADJI
: Pr. Abdelhaq ALAOUI YAZIDI
ADMINISTRATION
Doyen
: Pr. Mohammed BOUSKRAOUI
Vice doyen à la Recherche et la Coopération
: Pr. Mohamed AMINE
Vice doyen aux Affaires Pédagogiques
: Pr. Redouane EL FEZZAZI
Secrétaire Générale
: Mr. Azzeddine EL HOUDAIGUI
Professeurs de l’enseignement supérieur
Nom et Prénom Spécialité Nom et Prénom Spécialité ABOULFALAH Abderrahim Gynécologie-
obstétrique
FINECH Benasser Chirurgie – générale ADERDOUR Lahcen Oto- rhino-
laryngologie
FOURAIJI Karima Chirurgie pédiatrique B
ADMOU Brahim Immunologie GHANNANE Houssine
Neurochirurgie AIT BENALI Said Neurochirurgie KHALLOUKI
Mohammed
Anesthésie- réanimation AIT-SAB Imane Pédiatrie KHATOURI Ali Cardiologie AKHDARI Nadia Dermatologie KISSANI Najib Neurologie AMAL Said Dermatologie KOULALI IDRISSI
Khalid
Traumato- orthopédie AMINE Mohamed Epidémiologie-
clinique
KRATI Khadija Gastro- entérologie AMMAR Haddou
Oto-rhino-laryngologie
LAOUAD Inass Néphrologie ARSALANE Lamiae Microbiologie –
Virologie
LMEJJATI Mohamed Neurochirurgie ASMOUKI Hamid Gynécologie-
obstétrique B
LOUZI Abdelouahed Chirurgie – générale ASRI Fatima Psychiatrie MAHMAL Lahoucine Hématologie -
clinique BENELKHAIAT BENOMAR Chirurgie - générale MANOUDI Fatiha Psychiatrie
BOUAITY Brahim Oto-rhino- laryngologie
MANSOURI Nadia Stomatologie et chiru maxillo faciale
BOUGHALEM Mohamed Anesthésie – reanimation
MOUDOUNI Said Mohammed
Urologie BOUKHIRA Abderrahman Biochimie – chimie MOUTAJ Redouane Parasitologie BOUMZEBRA Drissi Chirurgie
Cardio-Vasculaire
MOUTAOUAKIL Abdeljalil
Ophtalmologie BOURROUS Monir Pédiatrie A NAJEB Youssef Traumato-
orthopédie BOUSKRAOUI Mohammed Pédiatrie A NEJMI Hicham Anesthésie-
réanimation CHAKOUR Mohamed Hématologie NIAMANE Radouane Rhumatologie CHELLAK Saliha Biochimie- chimie OULAD SAIAD
Mohamed
Chirurgie pédiatrique CHERIF IDRISSI EL
GANOUNI Najat
Radiologie RAJI Abdelaziz Oto-rhino-laryngologie CHOULLI Mohamed
Khaled
Neuro pharmacologie SAIDI Halim Traumato- orthopédie DAHAMI Zakaria Urologie SAMKAOUI
Mohamed Abdenasser
Anesthésie- réanimation EL ADIB Ahmed Rhassane Anesthésie-
réanimation
SARF Ismail Urologie EL FEZZAZI Redouane Chirurgie pédiatrique SBIHI Mohamed Pédiatrie B EL HATTAOUI Mustapha Cardiologie SOUMMANI
Abderraouf
Gynécologie- obstétrique A/B EL HOUDZI Jamila Pédiatrie B TASSI Noura Maladies infectieuses ELFIKRI Abdelghani Radiologie YOUNOUS Said Anesthésie-
réanimation ESSAADOUNI Lamiaa Médecine interne ZOUHAIR Said Microbiologie ETTALBI Saloua Chirurgie réparatrice
et plastique
Professeurs Agrégés
Nom et Prénom Spécialité Nom et Prénom Spécialité ABKARI Imad Traumato-
orthopédie B
FADILI Wafaa Néphrologie ABOU EL HASSAN Taoufik Anésthésie-
reanimation
FAKHIR Bouchra Gynécologie- obstétrique A
ABOUCHADI Abdeljalil Stomatologie et chir maxillo faciale
FAKHRI Anass Histologie- embyologie cytogénétique ABOUSSAIR Nisrine Génétique GHOUNDALE Omar Urologie ADALI Imane Psychiatrie HACHIMI
Abdelhamid
Réanimation médicale ADALI Nawal Neurologie HAJJI Ibtissam Ophtalmologie
AGHOUTANE El Mouhtadi Chirurgie pédiatrique A
HAOUACH Khalil Hématologie biologique AISSAOUI Younes Anesthésie –
réanimation
HAROU Karam Gynécologie- obstétrique B AIT AMEUR Mustapha Hématologie
Biologique
HOCAR Ouafa Dermatologie AIT BENKADDOUR Yassir Gynécologie-
obstétrique A
JALAL Hicham Radiologie ALAOUI Mustapha Chirurgie-
vasculaire péripherique KAMILI El Ouafi El Aouni Chirurgie pédiatrique B
ALJ Soumaya Radiologie KHOUCHANI Mouna Radiothérapie AMRO Lamyae Pneumo-
phtisiologie
KRIET Mohamed Ophtalmologie ANIBA Khalid Neurochirurgie LAGHMARI Mehdi Neurochirurgie ATMANE El Mehdi Radiologie LAKMICHI Mohamed
Amine
Urologie BAIZRI Hicham Endocrinologie et
maladies métaboliques LAKOUICHMI Mohammed Stomatologie et Chirurgie maxillo faciale
BASRAOUI Dounia Radiologie LOUHAB Nisrine Neurologie BASSIR Ahlam Gynécologie-
obstétrique A
MADHAR Si Mohamed
Traumato- orthopédie A
BELBARAKA Rhizlane Oncologie médicale
MAOULAININE Fadl mrabih rabou
Pédiatrie (Neonatologie) BELKHOU Ahlam Rhumatologie MATRANE Aboubakr Médecine nucléaire BEN DRISS Laila Cardiologie MEJDANE Abdelhadi Chirurgie Générale BENCHAMKHA Yassine Chirurgie
réparatrice et plastique
MOUAFFAK Youssef Anesthésie - réanimation BENHIMA Mohamed Amine Traumatologie -
orthopédie B
MOUFID Kamal Urologie BENJELLOUN HARZIMI
Amine
Pneumo- phtisiologie
BENLAI Abdeslam Psychiatrie NOURI Hassan Oto rhino laryngologie BENZAROUEL Dounia Cardiologie OUALI IDRISSI
Mariem
Radiologie BOUCHENTOUF Rachid Pneumo-
phtisiologie
OUBAHA Sofia Physiologie BOUKHANNI Lahcen Gynécologie-
obstétrique B
QACIF Hassan Médecine interne BOURRAHOUAT Aicha Pédiatrie B QAMOUSS Youssef Anésthésie-
réanimation
BSISS Mohamed Aziz Biophysique RABBANI Khalid Chirurgie générale CHAFIK Rachid Traumato-
orthopédie A
RADA Noureddine Pédiatrie A DAROUASSI Youssef Oto-Rhino –
Laryngologie
RAFIK Redda Neurologie DRAISS Ghizlane Pédiatrie RAIS Hanane Anatomie
pathologique EL AMRANI Moulay Driss Anatomie RBAIBI Aziz Cardiologie EL ANSARI Nawal Endocrinologie et
maladies métaboliques
ROCHDI Youssef Oto-rhino- laryngologie EL BARNI Rachid Chirurgie-
générale
SAJIAI Hafsa Pneumo- phtisiologie EL BOUCHTI Imane Rhumatologie SAMLANI Zouhour Gastro- entérologie EL BOUIHI Mohamed Stomatologie et
chir maxillo faciale
SEDDIKI Rachid Anesthésie - Réanimation EL HAOUATI Rachid Chiru Cardio
vasculaire
SORAA Nabila Microbiologie - virologie EL HAOURY Hanane Traumato-
orthopédie A
TAZI Mohamed Illias Hématologie- clinique EL IDRISSI SLITINE Nadia Pédiatrie ZAHLANE Kawtar Microbiologie -
virologie
EL KARIMI Saloua Cardiologie ZAHLANE Mouna Médecine interne EL KHADER Ahmed Chirurgie générale ZAOUI Sanaa Pharmacologie EL KHAYARI Mina Réanimation
médicale
ZEMRAOUI Nadir Néphrologie EL MGHARI TABIB Ghizlane Endocrinologie et
maladies métaboliques
ZIADI Amra Anesthésie - réanimation EL OMRANI Abdelhamid Radiothérapie ZYANI Mohammed Médecine interne
Professeurs Assistants
Nom et Prénom Spécialité Nom et Prénom Spécialité ABDELFETTAH Youness Rééducation et
Réhabilitation Fonctionnelle
Hammoune Nabil Radiologie ABDOU Abdessamad Chiru Cardio
vasculaire HAZMIRI Fatima Ezzahra Histologie – Embryologie - Cytogénéque ABIR Badreddine Stomatologie et
Chirurgie maxillo faciale
IHBIBANE fatima Maladies Infectieuses ADARMOUCH Latifa Médecine
Communautaire (médecine préventive, santé publique et hygiène)
JALLAL Hamid Cardiologie
AIT BATAHAR Salma Pneumo- phtisiologie
JANAH Hicham Pneumo- phtisiologie AKKA Rachid Gastro –
entérologie
KADDOURI Said Médecine interne ALAOUI Hassan Anesthésie –
Réanimation
LAFFINTI Mahmoud Amine
Psychiatrie
AMINE Abdellah Cardiologie LAHKIM Mohammed Chirurgie générale ARABI Hafid Médecine physique
et réadaptation fonctionnelle
LALYA Issam Radiothérapie ARSALANE Adil Chirurgie
Thoracique
LOQMAN Souad Microbiologie et toxicologie environnementale ASSERRAJI Mohammed Néphrologie MAHFOUD Tarik Oncologie médicale BAALLAL Hassan Neurochirurgie MARGAD Omar Traumatologie
-orthopédie BABA Hicham Chirurgie générale MILOUDI Mohcine Microbiologie -
Virologie BELARBI Marouane Néphrologie MLIHA TOUATI
Mohammed
Oto-Rhino - Laryngologie BELBACHIR Anass Anatomie-
pathologique
MOUHSINE Abdelilah Radiologie BELFQUIH Hatim Neurochirurgie MOUNACH Aziza Rhumatologie
BELHADJ Ayoub Anesthésie – Réanimation
MOUZARI Yassine Ophtalmologie BENNAOUI Fatiha Pédiatrie
(Neonatologie)
NADER Youssef Traumatologie - orthopédie BOUCHAMA Rachid Chirurgie générale NADOUR Karim Oto-Rhino -
Laryngologie BOUCHENTOUF Sidi
Mohammed
Chirurgie générale NAOUI Hafida Parasitologie Mycologie BOUKHRIS Jalal Traumatologie –
orthopédie
NASSIM SABAH Taoufik Chirurgie Réparatrice et Plastique
BOUZERDA Abdelmajid Cardiologie NYA Fouad Chirurgie Cardio - Vasculaire
CHETOUI Abdelkhalek Cardiologie OUERIAGLI NABIH Fadoua
Psychiatrie CHRAA Mohamed Physiologie REBAHI Houssam Anesthésie -
Réanimation EL HARRECH Youness Urologie RHARRASSI Isam
Anatomie-patologique EL KAMOUNI Youssef Microbiologie
Virologie
SALAMA Tarik Chirurgie pédiatrique EL MEZOUARI El Moustafa Parasitologie
Mycologie
SAOUAB Rachida Radiologie ELBAZ Meriem Pédiatrie SEBBANI Majda Médecine
Communautaire (médecine préventive, santé publique et hygiène)
ELQATNI Mohamed Médecine interne SERGHINI Issam Anesthésie - Réanimation
ESSADI Ismail Oncologie Médicale TAMZAOURTE Mouna Gastro - entérologie FDIL Naima Chimie de
Coordination Bio-organique
TOURABI Khalid Chirurgie réparatrice et plastique
FENNANE Hicham Chirurgie Thoracique
YASSIR Zakaria Pneumo- phtisiologie GHAZI Mirieme Rhumatologie ZARROUKI Youssef Anesthésie -
Réanimation GHOZLANI Imad Rhumatologie ZIDANE Moulay
Abdelfettah
Chirurgie Thoracique HAMMI Salah Eddine Médecine interne ZOUIZRA Zahira Chirurgie
Je dédie cette thèse à …
TOUT D’ABORD à ALLAH
Le tout puissant et miséricordieux, qui m’a donné la force et la patience
d’accomplir ce modeste travail.
Qui m’a inspiré et guidé dans le bon chemin,
Je lui dois ce que je suis devenue.
Louange et remerciement pour sa clémence et sa miséricorde.
Dédicace à la plus belle des mères : la Mienne
- Madame KELTOUMA AMDKIK-
Autant de phrases aussi expressives soient-elles ne sauraient montrer le
degré d’amour et d’affection que j’éprouve pour toi car rien au monde ne
vaut les efforts que tu as fournis jour et nuit pour mon éducation et mon
bien être. Tu as fait plus qu’une mère puisse faire pour son enfant .Tu es
ma mère, mon amie et mon modèle. Ce travail est le fruit des sacrifices
que tu as consentis pour mon éducation et ma formation. En ce jour
mémorable pour moi ainsi que pour toi, reçoit ce travail en signe de ma
grande reconnaissance et mon profond amour. Puisse Dieu, le tout
puissant, te préserver et t’accorder santé, longue vie et bonheur.
A mon très cher père Mr. JAMAA EL BOUHI-
Autant de phrases et d’expressions aussi éloquentes soit-elles ne sauraient
exprimer ma gratitude et ma reconnaissance. Tu as su m’inculquer le
sens de la responsabilité, de l’optimisme et de la confiance en soi face aux
difficultés de la vie. Tes conseils ont toujours guidé mes pas vers la
réussite. Ta patience sans fin, ta compréhension et ton encouragement
sont pour moi le soutien indispensable que tu as toujours su m’apporter.
Je te dois ce que je suis aujourd’hui et ce que je serai demain et je ferai
toujours de mon mieux pour rester ta fierté et ne jamais te décevoir. Que
Dieu le tout puissant te préserve, t’accorde santé, bonheur, quiétude de
l’esprit et te protège de tout mal.
A mon cher petit frère ISMAIL-
Pour toute l’ambiance dont tu m’as entouré, pour toute la spontanéité et
ton élan chaleureux, Je te dédie ce travail. Puisse Dieu le tout puissant
exhausser tous tes vœux
A mes chères sœurs HAFSA et RADIA et leurs petites familles -
Aucune dédicace ne saurait exprimer tout l’amour que j’ai pour vous, Votre
joie et votre gaieté me comblent de bonheur. Puisse Dieu vous garder,
éclairer votre route et vous aider à réaliser vos vœux les plus chers.
A mon cher grand frère CHIHAB-
Merci pour ton amitié pour ton soutien et tendresse.
En témoignage de mon affection fraternelle, de ma profonde
reconnaissance, je vous souhaite une vie pleine de bonheur et de succès et
que Dieu, le tout puissant, vous protège et vous garde.
A mes chers cousins OMAR et FAISAL-
Veuillez trouver dans ce travail l’expression de mon respect le plus
profond etmon affection la plus sincère.
A la famille AJEDIG-
En témoignage de l’attachement, de l’amour et de l’affection que je porte
pour vous. Je vous dédie ce travail avec tous mes vœux de bonheur, de
santé et de réussite.
A mon cher professeur HICHAM AJANA-
Merci pour vos encouragements, pour votre soutien, pour avoir rendu les
maths faciles et amusants. Veuillez trouver dans ce travail l’expression
de mon respect le plus profond
À mes Chères amies ET collègues : SOUMIA, MALIKA, KELTOUM,
NAJWA, GHITA, IMANE, NADIA, SAKINA, SAADIA, KAOUTAR
En souvenir de notre sincère et profonde amitié et des moments agréables
que nous avons passés ensemble. Veuillez trouver dans ce travail
l’expression de mon respect le plus profond et mon affection la plus
sincère.
A LA MEMOIRE DE NOS DEFUNTS COLLEGUES
Que Dieu, le miséricordieux, vous accueille dans son éternel paradis.
À TOUTES LES PERSONNES QUI ONT PARTICIPÉ A L’ÉLABORATION
A notre maître et rapporteur de thèse,
Monsieur RADOUANE NIAMANE,
Chef du service de Rhumatologie (HMA)
J’ai eu le privilège de travailler avec vous et d'apprécier vos qualités et
vos valeurs.
Votre sérieux, votre compétence et votre sens du devoir m’ont
énormément marqué.
Veuillez trouver ici l'expression de ma respectueuse considération et ma
profonde admiration pour toutes vos qualités scientifiques et humaines.
Veuillez accepter, cher Maître, l'assurance de mon estime et mon profond
respect.
A notre maître et président du jury,
Monsieur. ALI KATOURI,
Chef du service de Cardiologie (HMA),
Vous nous faîtes l’honneur d’avoir accepté avec tant de spontanéité la
présidence de cette thèse.
Vos connaissances et votre rigueur sont un modèle pour tous les
étudiants.
Veuillez trouver dans ce travail un modeste témoignage de notre profond
respect et l’expression de nos sentiments les plus distingués.
A notre maître et juge de thèse,
Madame NOURA TASSI,
Chef du service de Maladies infectieuses (CHU MED VI)
Vous avez accepté de juger ce travail avec une spontanéité et une
simplicité émouvante.
C’est pour nous un grand honneur de vous voir siéger parmi le jury de
cette thèse.
Nous tenons à vous exprimer nos sincères remerciements et profond respect
A notre Maître et juge de thèse,
Madame AHLAM BELKHOU,
Professeur agrégée de Rhumatologie (CHU MED VI)
Vous nous faites l’honneur d’accepter de juger ce travail. La qualité de
votre enseignement et votre sens intellectuel font de vous un maître
exemplaire. Je vous remercie et vous prie d’accepter l’assurance de mon
profond respect.
A tout le personnel médical et paramédical du service de Rhumatologie
HMA.
Liste desabreviations :
AAP : Antiagrégant plaquettaire ATCD : Antécédents
ACPA : Anticorps anti-peptides citrullinés ACR : American College of Rheumatology
AFSSAPS : Agence Française de sécurité sanitaire et des produits de santé AINS : Anti-inflammatoires non stéroïdiens
AOMI : Artériopathies des membres inférieurs APS : Antipaludéens de synthèse
DMARDs : Disease-Modifying Antirheumatic Drugs bDMARDs : biological DMARDs
bsDMARDs : biosimilar DMARDs
csDMARDs : conventional synthetic DMARDs CRP : c - reactive protein.
DAS28 : Disease Activity Score DDB : Dilatation des branches DM : Dérouillage matinale
EULAR : European League Against Rheaumatism EVA : Echelle Visuelle Analogique
FR : Facteur rhumatoïde
FRAX : Fracture risque assessement tool
GC : Glucocorticoides
HAQ : Health Assessment Questionnaire HbA1c : Hémoglobine glyquée
HP : Hélicobacter Pylori HTA : Hypertension artérielle.
HTP : Hypertension portale HVB : Virus de l’hépatite B HVC : Virus de l’hépatite C HZV : Herpes Zona Virus IAo : Insuffisance aortique IL : Interleukine
IM : Insuffisance mitrale IR : Insulinorésistance IT : Insuffisance tricuspide LAA : Luxation atloïdo-axoïdienne LEF : Leflunomide
MCV : Maladies cardiovasculaires
MCP : Articulations métacarpophalangiennes MTP : Articulations métatarsophalangiennes MTX : Méthotrexate
NAD : Nombre d’articulations douloureuses NAG : Nombre d’articulations gonflées ODM : Ostéodensitométrie
OP : Ostéoporose
ORALE : Outcome of Rheumatoid Arthritis Longitudinal Evaluation PR : Polyarthrite rhumatoïde.
RN : Réveil nocturne RTX : Rituximab
SAHS : San Antonio Heart Study SLZ : Salazopyrine
UGD : Ulcère gastroduodénal TNF : Tumor Necrosis Factor VS : Vitesse de sédimentation
INTRODUCTION 1
PATIENTS ET MÉTHODES 3
I. Type et lieu d’étude 4
II. Période de l’étude 4
III. Population étudiée 4
IV. Considérations éthiques 4
V. Méthodes 4
1. Les données démographiques 4
2. Les caractéristiques cliniques de la polyarthrite rhumatoïde (PR) 5 3. Les caractéristiques paracliniques de la PR 6 4. Les caractéristiques thérapeutiques 6
5. Les comorbidités 6
6. La prise en charge des comorbidités 7
7. Analyse des données 7
RÉSULTATS 8
I. Etude descriptive 9
1. Données démographiques 9
2. Les caractéristiques de la polyarthrite rhumatoïde (PR) 10 3. Evaluation globale de la polyarthrite rhumatoïde (PR) 14
4. Les thérapeutiques 18
5. Evaluation des comorbidités 21 6. Evaluation de la prise en charge de ces comorbidités 26
DISCUSSION 28 I. GENERALITES SUR LA PR 29 1. Epidémiologie 29 2. Clinique et diagnostic 30 3. Examens complémentaires 35 4. Evaluation de l’activité de la PR 37 5. Facteurs pronostiques 38
6. Traitement et stratégie thérapeutique 39
7. Mortalité 43 II. COMORBIDITES 43 1. PR et risque cardiovasculaire 44 2. PR et risque infectieux 50 3. PR et ostéoporose (OP) 65 4. PR et autres comorbidités 69 CONCLUSION 71
ANNEXES 75
RÉSUMÉS 86
La polyarthrite rhumatoïde (PR) est le plus fréquent des rhumatismes inflammatoires chroniques, avec une prévalence moyenne de 0,5 à 1 % dans les pays développés [1], et de 0,3 à 0,5 % dans les pays en voie de développement [2]. Elle est caractérisée par une évolution destructrice des articulations entraînant des répercussions fonctionnelles, psychologiques, sociales et professionnelles.
Les comorbidités sont des affections associées à la PR. Les mécanismes de ces associations peuvent être liés à la PR elle même, aux effets des traitements utilisés pour l’améliorer, ou bien l’apanage d’une coïncidence [1,8].
Les données provenant de plusieurs études menées en Amérique du Nord, en Europe et en Australie avaient montré une forte prévalence des comorbidités chez les patients présentant une PR [1,5-11]. Cependant, l’information sur les comorbidités chez les patients atteints de PR a été moins explorée dans les pays en voie de développement.
Les comorbidités les plus fréquentes observées dans la PR comportent les maladies cardiovasculaires, les cancers, les infections bactériennes, l’anémie chronique, l’ulcère gastroduodénal, la cataracte, l’ostéoporose et la dépression [1,3–10].
Les comorbidités entraînent non seulement une aggravation de la maladie, mais aussi une augmentation de la mortalité et des coûts [8,11].
La prise en charge des comorbidités associées à la PR sont maintenant reconnus comme un problème majeur comme dans toute maladie chronique.
La recherche et la prise en charge de ces comorbidités vise à préserver voire améliorer la qualité de vie du patient et son espérance de vie ainsi pouvoir limiter les conséquences psychosociales.
Notre étude a pour objectif d’étudier la prévalence et le type des comorbidités ainsi que leur prise en charge chez des patients Marocains atteints de PR suivis au service de rhumatologie de l’hôpital militaire Avicenne de Marrakech.
PATIENTS
&
I.
Type et lieu d’étude
Il s’agit d’une étude rétrospective, descriptive de type transversale, réalisée au service de rhumatologie de l’hôpital militaire Avicenne de Marrakech.
II.
Période de l’étude
Etude menée sur une période de 10 ans allant du 1er janvier 2006 au mars 2016.
III.
Population étudiée
Sont inclus dans l’étude les cas de polyarthrites rhumatoïdes diagnostiqués selon les critères de l’ACR 1987 pour les PR établies et anciennes et les critères de l’ACR/EULAR 2010 (Annexe 1) pour les PR débutantes.
IV.
Considérations éthiques :
Le recueil des données a été effectué avec respect de l’anonymat des patients et de la confidentialité de leurs informations.
V.
Méthodes
L’ensemble des données recueillies ont été rapportées sur une fiche d’exploitation, comportant les chapitres suivants :
1.
Les données démographiques
2.
Les caractéristiques cliniques de la polyarthrite rhumatoïde (PR) :
• •
Le délai de diagnostique •
Le délai de prise en charge •
La durée d’évolution •
L’atteinte articulaire L’activité
L’indice composite Disease Activity Score (DAS 28) (Annexe 2) a été calculé chez nos patients. Selon la valeur de ce score, les PR ont été définies en « rémission » si le score DAS 28 était < 2.6, et en « faible activité » si ce score était ≤ 3 .2 et > 2.6. Une PR « active » était définie par un score de DAS 28 > 3.2, une PR « modérément active » par un score de DAS 28 > 3.2 et ≤ 5.1, et une PR « très active » était définie par un score > 5.1.
•
Le retentissement fonctionnel de la PR chez nos patients a été apprécié par le HAQ (Annexe 3) (Health Assessment Questionnaire) qui varie entre 0 (pas de retentissement fonctionnel) et 3 (retentissement fonctionnel majeur). Un HAQ ≥ 0.5 signifie l'existence d'un retentissement fonctionnel de la maladie.
L’handicap fonctionnel
•
Une PR sévère se définit par l’existence d’un handicap fonctionnel mesuré par le HAQ ≥0,5 (Health Assessment Questionnaire), ou par l’existence ou la progression de lésions structurales en imagerie, ou par l’existence de manifestations systémiques. La présence d’un syndrome inflammatoire important et/ou forte positivité du FR/ACPA représentait également un signe de sévérité de la PR.
3. Les caractéristiques paracliniques de la PR
3.1. Bilan biologique
Les examens biologiques réalisés ont inclus :
- le bilan inflammatoire (VS et C-Réactive protéine : CRP),
- le bilan immunologique : Facteur rhumatoïde (FR), et anticorps anti-peptides citrullinés (anti-CCP ou ACPA).
3.2. Bilan radiologique
Les radiographies standards des mains et des pieds ont été réalisées chez nos patients pour mettre en évidence les signes radiologiques de la PR.
La radiographie du rachis cervical face et profil en hyper-flexion ont été demandées pour mettre en évidence une luxation atloïdo-axoïdienne. La radiographie du thorax et du bassin ont été réalisées à la recherche d’atteinte pulmonaire et de coxite qui constituent des signes de sévérité de la maladie.
4. Les caractéristiques thérapeutiques
Les traitements reçus ont été précisés pour nos patients atteints de PR. On a définis 3 chapitres :
a- Chapitre des traitements symptomatiques (AINS et corticothérapie) b- Chapitres des traitements de fond classiques
c- Chapitre des biothérapies 1- Indications
2- Types de biothérapies
5. Les comorbidités
On a recueillis les données en rapport avec les tares préexistantes chez nos patients ainsi que les comorbidités survenues au cours de la polyarthrite rhumatoïde.
Huit comorbidités ont été étudiées :
- Pathologies cardiovasculaires et pathologies constituant des facteurs de risque pour une cardiopathie ischémique (hypertension artérielle, diabète et dyslipidémie) - Cancers - Infections - Maladies gastro-intestinales - Ostéoporose - Dépression - Pneumopathies - Et maladies ophtalmiques
Concernant le diabète, l’hypertension artérielle et la dépression, seuls les patients diagnostiqués et mis sous traitement sont inclus dans cette étude.
Pour la dyslipidémie sont inclus tous les patients mis sous hypolipémiants ou présentant un trouble du bilan lipidique.
Seuls les patients dont l’ostéoporose a été diagnostiquée en évaluant la densité minérale osseuse sont inclus dans cette étude.
6. La prise en charge des comorbidités
On a défini trois chapitres : - Risque Cardiovasculaire - Ostéoporose
- Infection et vaccination
7. Analyse des données :
I. Etude descriptive
Nous avons recruté 135 patients atteints de polyarthrite rhumatoïde.
1. Données démographiques :
1.1. Age :
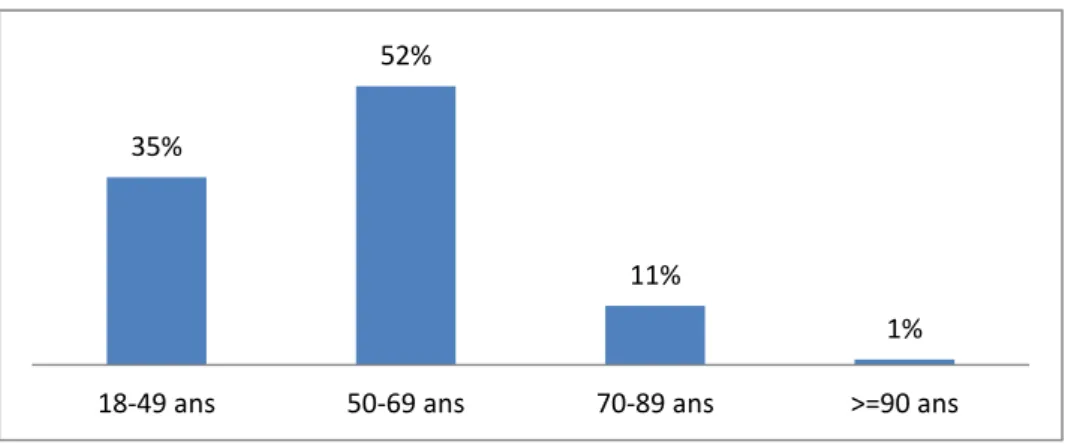
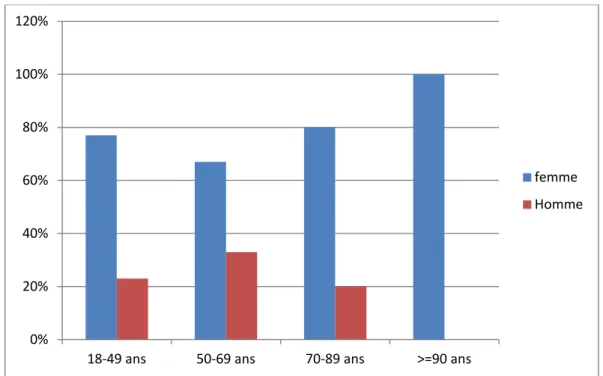
L’âge moyen des patients était de 53,54 ± 12,25 ans avec des extrêmes allant de 18 ans à 97 ans, dont 52% des patients avaient un âge entre 50 et 69 ans (Figure 1).
Figure 1: Répartition des patients étudiés selon les tranches d’âge
1.2. Sexe :
Dans la population étudiée, 77% des malades étaient de sexe féminin (Figure 2).
Figure 2: Répartition des patients selon le sexe 77% 23% Femmes hommes 35% 52% 11% 1% 18-49 ans 50-69 ans 70-89 ans >=90 ans
1.3. Répartition selon l’âge et le sexe :
Les femmes représentaient 77%, 67%, 80% et 100% respectivement chez les tranches d’âge « 18 à 49 ans », « 50 à 69 ans », « 70 à 89 ans » et « ≥90 ans » (Figure 3).
Figure 3 : Répartition des patients étudiés selon l'âge et le sexe.
2. Les caractéristiques de la polyarthrite rhumatoïde (PR) :
2.1. Diagnostic de la PR
Tous les malades répondaient aux critères de l’ACR 1987 pour les PR établies et anciennes et les critères de l’ACR/EULAR 2010 (Annexe 1) pour les PR débutantes.
2.2. Durée d’évolution de la PR :
La durée moyenne d’évolution de la PR était de 14±7.13 ans avec des extrêmes allant de 4 ans à 37 ans. Dans notre étude, 74% des patients avaient une PR ancienne de plus de 10 ans. (Figure 4) 0% 20% 40% 60% 80% 100% 120%
18-49 ans 50-69 ans 70-89 ans >=90 ans
femme Homme
Figure 4: Répartition des malades selon l'ancienneté de la PR
2.3. Délai diagnostique :
Le délai diagnostique moyen était de 3 ± 4.19 ans avec des extrêmes allant de 8 mois jusqu’ à 20 ans. Les diagnostics ont été portés dans un délai inferieur à une année dans 36% des cas (Figure 5).
Figure 5: Répartition des malades selon le délai diagnostique de la maladie
2.4. Délai de prise en charge :
Le délai de prise en charge moyen était de 1.8 mois avec des extrêmes allant de 0 mois à 3 ans. 26% 74% <=10 ans >10 ans 36% 30% 23% 11% <1 an 1 an-2 an 3 ans-6 ans >= 7 ans
2.5. Atteinte articulaire:
a. Topographie de l’atteinte articulaire:
De façon globale, l’atteinte était poly-articulaire bilatérale et symétrique dans plus de la moitié des cas (83%). Dans l’étude présente, 94.3% des patients avaient une arthrite des petites et moyennes articulations (poignets et MCP) de la main.
b. Etude des déformations articulaires:
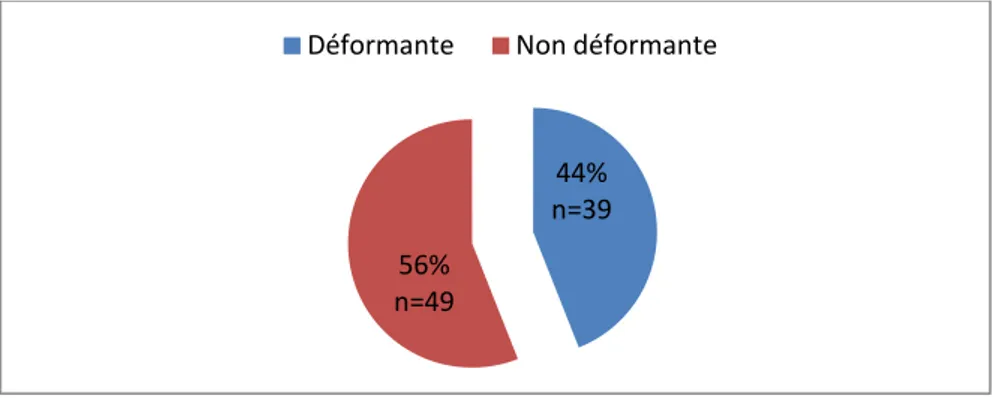
Dans notre étude, 44.3% (n=89) des patients recrutés avaient une PR déformante (Figure 6).
Figure 6: Répartition des malades selon les déformations (N=88).
Les différentes déformations constatées chez nos patients figurent sur le tableau suivant (TableauI): Tableau I : Etude des déformations articulaires.
Types de déformations (n=88) Nombre de cas % de patients
luxation atloïdo-axoïdienne (LAA) 1 1.1%
Mains
Coup de vent cubital 33 37.5%
Doigt en Boutonnière 26 30%
Pouce en Z 20 23%
Dos de chameau 18 20.4%
Doigt en Maillet 15 17%
Touche de piano 12 13.6%
Doigt en Col de cygne 10 11.36%
Pieds
Affaissement de la voute plantaire 6 7%
Hallux-valgus 22 25%
Quintus varus 11 12.5%
Valgus de l’arrière pied 4 4.5%
Subluxation des MTP 4 4.5%
44% n=39 56%
n=49
Un seul patient avait une luxation atloïdo-axoïdienne (LAA) de 4 mm de diastasis sur la radiographie du rachis cervicale.
2.6. Atteintes extra –articulaires:
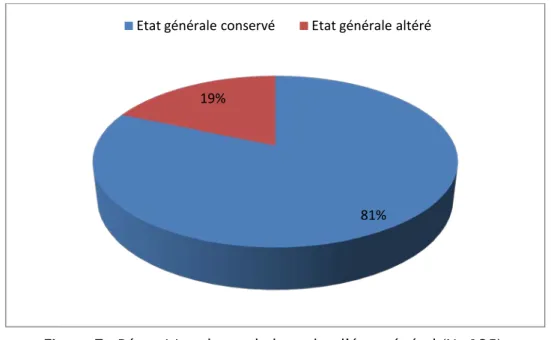
Dans notre étude, 81.4% de nos patients soit 110 malades avaient un état général conservé et seulement 18,5% soit 25 malades avaient un état général altéré (Figure 7).
Figure 7 : Répartition des malades selon l’état général (N=135).
Les manifestations extra-articulaires étaient présentes chez 74 malades soit 55 %. Elles sont détaillées dans le tableau II.
Tableau II: Etude des manifestations extra articulaires (n=135)
Nombre de patients % de patients
Atteinte extra-articulaire 74 55%
Syndrome de Gougerot Sjögren 54 40% Nodules rhumatoïdes cutanés 20 14.8%
Atteinte rénale (protéinurie) 1 1%
Vascularite rhumatoïde 0 0%
81% 19%
3. Evaluation globale de la polyarthrite rhumatoïde (PR) :
3.1. Evaluation des paramètres cliniques d’activité de la PR:
a. Dérouillage matinal et réveils nocturnes:
Au moment du diagnostic, le dérouillage matinal (DM) était supérieur à 30 minutes chez 62.5% des cas, et 44% des malades avaient des réveils nocturnes multiples (RN).
b. Indice articulaire et indice synovial
Le nombre élevé d’articulations gonflées (NAG>3) était présent chez 62 malades soit 90% (n=69) et le nombre élevé d’articulations douloureuses (NAD>3) chez 52 patients soit 71% (n=73)
Nombre moyen d’articulations douloureuses (NAD) était de 21,16± 8,11 Nombre moyen d’articulations gonflées (NAG) était de 8,86 ± 4,9
c. Etude de la douleur:
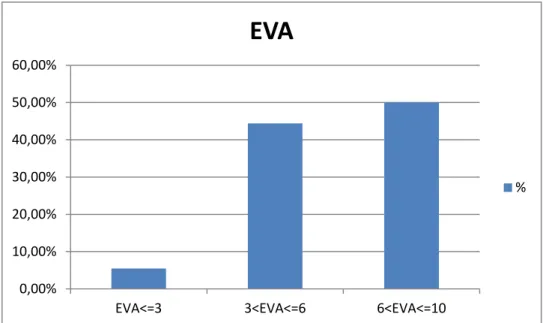
La moyenne de l’EVA douleur (Annexe 4) était de 6.3± 2.22 sur une échelle de 0 à 10 cm. Dans la population étudiée, 50% des malades qualifiaient leur douleur comme étant intense et 44.4% des malades qualifiaient leur douleur comme étant modérée (Figure 8).
Figure 8: La perception de la douleur chez les patients par l'échelle visuelle analogique (EVA) 0,00% 10,00% 20,00% 30,00% 40,00% 50,00% 60,00%
EVA<=3 3<EVA<=6 6<EVA<=10
EVA
d. Score DAS 28:
Au moment du diagnostic, le DAS 28 moyen était de 4,03 ± 1,5 allant de 1,36 à 8,11. En effet, parmi 71 patients chez qui le DAS28 a été calculé, 14 malades (19,7%) avaient un score DAS 28>5,1 alors que 30 malades (42,3%) avaient une PR modérément active (3,2< DAS 28 ≤ 5,1) et 22 patients avaient une PR de faible niveau d’activité (31%) et seulement 5 patients (1,4%) étaient en rémission (Figure 9).
Figure 9: Répartition des patients selon l'activité de la PR évaluée par le DAS 28.
3.2. Evaluation des paramètres biologiques d’activité de la maladie:
a. Syndrome inflammatoire biologique
Dans notre étude, 50 cas soit 60% (n=83) présentaient une élévation de la vitesse de sédimentation (VS)>30mm et 65 cas soit 83% (n=78) présentaient une CRP> 20mg/l (Tableau III).
La valeur moyenne de la vitesse de sédimentation (VS) chez nos patients était de 52,6 ±20,62 mm
La valeur moyenne de la CRP chez nos patients était de 30 ± 13,85 mg/l
Tableau III : Etude de la vitesse de sédimentation et de la protéine C réactive. La valeur moyenne Les extrêmes VS >30mm (N=83) 52,6± 20,62 [26-95] CRP>20mg/l (N=78) 30± 13,85 [21-67] 0 10 20 30 40 50
activité élevée activité modérée faible niveau
d'activité rémission
b. Sérologie rhumatoïde et ACPA :
Dans notre étude, 59 soit 67% malades (n=86) étaient positifs pour le facteur rhumatoïde (FR) (Figure 10), alors que 53 malades soit 65% (n=82) étaient positifs pour les ACPA (Figure 11).
Figure 10: Répartition des patients selon la sérologie rhumatoïde (N=86)
. Figure 11: Répartition des patients selon la présence d’ACPA (n=82)
3.3. Evaluation de l’atteinte structurale:
Parmi 76 malades, on avait 58 cas (76%) qui étaient des PR érosives et 12 cas de PR (24%) étaient non érosives (Figure 12).
67% 24%
9%
positif Négatif dissociés
65% 35%
Figure 12: Répartition des malades selon le caractère érosif de la PR (N=76)
Pour le Sharp pincement et Sharp érosion (Annexe 5) nous disposions de données de deux patients seulement chez qui ces deux indices ont été précisés. Les deux présentaient un Sharp pincement à 65 et un Sharp érosion à 37.
3.4. Evaluation du retentissement socioprofessionnel par l’indice HAQ:
Vu la nature rétrospective de l’étude, nous disposions de données de seulement 17 patients chez qui l’indice HAQ a été calculé. Il était supérieur à 0,5 chez tous ces patients, sa valeur moyenne était de 1,82 ± 0,47 avec des extrêmes [1→2,9]
3.5. Facteurs pronostiques:
L’évaluation globale des paramètres de sévérité symptomatique, structurale et fonctionnelle a permis de réunir les différents facteurs de mauvais pronostic de la PR.
Dans notre série, nos malades avaient en moyenne 5 facteurs de mauvais pronostic. Ces facteurs sont :(Figure 13)
- L’activité élevée de la maladie (DAS 28>3.2) chez 44 patients soit 62 % (n=71).
- Le nombre élevé d’articulations gonflées (NAG>3) chez 62 soit 90% (n=69) et d’articulations douloureuses (NAD>3) chez 52 patients soit 71% (n=73).
76% 24%
- L’importance du syndrome inflammatoire biologique : 50 malades soit 60% (n=83) avec une VS>30mm la 1ère
- La présence d’ACPA chez 53 malades soit 65% (n=82)
heure et 65 malades soit 83% (n=78) avec une CRP>20 mg/l. - PR érosive chez 58 malades soit 76% (n=76)
- Les nodules rhumatoïdes cutanés chez 20 cas soit 14.8% malades (n=74)
Figure 13: Répartition des malades selon les facteurs de mauvais pronostic de la PR.
4. Les thérapeutiques :
4.1. Traitements symptomatiques :
a. Les anti-inflammatoires non stéroïdiens (AINS) et les antalgiques :
Dans notre étude, 55,6% des patients avaient reçu des AINS comme traitement symptomatique de la douleur.
b. La corticothérapie :
Dans l’étude présente, 87% des patients étaient sous corticothérapie. 90% 71% 60% 83% 65% 67% 100% 76% 15% 62% 10% (n=69) 29% (n=73) 40% (n=83) 17% (n=78) 35% (n=82) 33% (n=86) (n=17) 24% (n=76) 85% (n=74) 38% (n=71) NAG>3 NAD>3 VS>30mm CRP>20 mg/l. ACPA+ FR+ HAQ>0.5 PR érosive Nodules rhumatoïdes DAS 28>3,2 OUI NON
b.1. Dose de la corticothérapie :
La dose moyenne de la corticothérapie était de 8,4 ± 2.58 mg/j de prédnisone avec des extrêmes de 5 à 15 mg/j.
4.2. Traitements de fond classiques:
Dans notre série, 121 patients soit 90% des cas étaient sous traitement de fond, à savoir le méthotrexate, la salazopyrine, les antipaludéens de synthèse, les sels d’or et Leflunomide (Tableau IV).
Le méthotrexate constituait le traitement de fond classique le plus utilisé et ce dans 81% des cas.
Pour les deux patients qui ont été mis sous traitement de fond « sels d’or », il s’agissait de deux cas de PR séropositive, érosive et déformante, diagnostiquées en 1980 et 1994. Les deux patients ont été mis sous d’autres traitements de fond suite à l’inefficacité des « sels d’or ».
Tableau IV : Répartition des patients selon le type du traitement de fond classique administré. Type de traitement de fond administré Nombre de patients % des patients
Méthotrexate (MTX) 98 81%
Salazopyrine (SLZ) 45 37%
Anti paludéens de synthèse (APS) 13 11%
Sels d’or 2 2%
Leflunomide (LEF) 1 1%
Figure 14: Répartition des malades selon le traitement de fond classique administré 0 10 20 30 40 50 60 70 80 90
MTX SLZ APS Sels d’or LEF
4.3. Biothérapie
a. Indications de la biothérapie:
La biothérapie a été indiquée chez 49 malades. Les indications majeures de la biothérapie dans notre série étaient :
• L’échec du traitement de fond chez 45 patients soit 91.8%.
• L’activité sévère de la maladie chez 38 malades soit (77.5%) et le caractère déformant ou érosif chez 36 malades (73.5%).
• Il y’avait 9 cas d’intolérance au traitement de fond, 2 cas de contre-indication (le premier présentait une cirrhose hépatique + HTP et le deuxième présentait une fibrose pulmonaire) et un cas de cortico-dépendance (Tableau V).
L’étude de ces indications est détaillée dans le tableau V :
Tableau V : Etude des indications de la biothérapie.
Indication % des patients Nombre de patients Echec du traitement de fond 91,8% 45/49
Activité sévère 77,5% 38/49
PR érosive et ou déformante 73,5% 36/49 Intolérance au traitement de fond 18,4% 9/49 Contre indication au traitement de fond 4,1% 2/49
Cortico-dépendance 2,1% 1/49
Tableau VI : Répartition des 9 cas d’intolérance au traitement de fond classique.
Nombre de cas Traitement de fond
Intolérance digestive 3 MTX
Hépatite cytolytique 2 MTX
Hépatite choléstatique 1 MTX
Pneumopathie interstitielle hypoxémiante 1 MTX Thrombose veineuse étendue de la veine iliaque
droite arrivant à la veine cave inférieure en rapport avec une hyperhomocystéinémie associée à une anémie mégaloblastique.
1 MTX
b. Types de biothérapie :
La population bénéficiant de la biothérapie était majoritairement sous Rituximab (32/49 patients soit 65.3%) (Tableau VII).
Tableau VII : Répartition des patients selon le type de biothérapie utilisée
Type de biothérapie Nombre de patients % des patients
Rituximab 32 65
Adalimumab 11 22
Etanercept 8 16
Figure 15: Répartition des patients selon le type de biothérapie utilisée
5. Evaluation des comorbidités :
On a relevé les comorbidités chez 88 patients dont on avait suffisamment de données sur le dossier médical. La prévalence des comorbidités dans ce groupe de patients était de 71.5%.
Les différentes comorbidités sont détaillées dans les tableaux (VIII et IX) suivants : Tableau VIII : Répartition des patients selon les catégories de comorbidités
Catégorie de comorbidités Nombre de patients % des patients
Pathologies cardiovasculaires 25 27% Maladies métaboliques 43 49% Infections 26 28.4% Ostéoporose 22 25% Maladies gastroduodénales 12 14% Maladies psychiatriques 3 3% Maladies ophtalmiques 10 11% Pneumopathies 6 7% Cancers 0 0% 0 10 20 30 40 50 60 70
Rituximab Adalimumab Etanercept
Nombre de patients % de patients
Tableau IX : Répartition des patients selon les différents types de comorbidités.
Catégorie de comorbidités Comorbidité Nombre de patients Pourcentage %
Pathologies cardiovasculaires
HTA
Artériopathie oblitérante des membres inférieurs Phlébite surale
Hypertension artérielle pulmonaire Angine de poitrine
Valvulopathies
Trouble du rythme cardiaque
14 1 1 1 2 3 3 16 1 1 1 2.3 3.4 3,4 Maladies métaboliques Diabète Dyslipidémie 21 22 24 25
Infections
Infections virales :
5 cas d’infections par le virus de l’hépatite B 1 cas d’infection par le virus de l’hépatite C 2 cas de zona
Infections bactériennes : 2 cas d’arthrites septiques 5 cas d’infections urinaires 2 cas de syphilis
2 cas de salpingite
2 cas de tuberculeuse pulmonaires Infections parasitaires et fongiques : 1 cas de leishmaniose cutanée 1 cas de Giardiose intestinale 2 cas de candidoses oesophagiennes
8 13 4 9 15 4.5 Maladies gastroduodénales Ulcère gastroduodénal gastrite 3 9 3.4 10.2 Maladies psychiatriques Dépression 3 3.4
Maladies ophtalmiques Cataracte Glaucome Uvéite Episclérite Kératite Maculopathie 4 2 1 1 2 1 4.5 2.3 1 1 2.3 1 Pneumopathies Asthme Fibrose pulmonaire avec dilatation des branches 5 1 5.7 1
ostéoporose Ostéoporose 22 25 Cancer Sein Col utérin Prostate Colorectal Lymphome Cutané Poumon 0 0 0 0 0 0 0 0 0 0 0 0 0 0
Figure 16: Répartition des patients selon le type de comorbidité relevée
Dans notre population les comorbidités les plus fréquentes étaient les maladies métaboliques avec une prévalence à 49%, les infections à 28,5%, les maladies cardiovasculaires à 27% et l’ostéoporose à 25%.
Les comorbidités cardiovasculaires relevées dans notre série étaient : - L’hypertension artérielle chez16% des cas
- L’angor chez 2% des cas
- Trois cas de valvulopathies soit 3,4% des cas, deux patients avaient l’association d’une insuffisance mitrale (IM) et une insuffisance tricuspide (IT) minime, et un patient avait une IM et une insuffisance aortique (IAo) minime.
- Les troubles du rythme cardiaque chez 3,4% des cas - Un cas d’hypertension artérielle pulmonaire (HTAP) (1%)
- Un cas d’artériopathie oblitérante des membres inférieurs (AOMI) (1%) - Un cas d’une phlébite surale (1%)
Les maladies métaboliques objectivées dans notre étude étaient comme suivant : - Le diabète chez 24% des cas
Les infections étaient de quatre types, les infections bactériennes, virales, parasitaires et fongiques. Les infections bactériennes étaient les plus fréquentes dans notre étude ; il s’agissait de treize cas répartis comme suivant :
- Cinq cas d’infections urinaires dont deux cas sont survenus sous Rituximab, - Deux cas d’arthrites septiques qui sont survenus également sous rituximab
- Deux cas de tuberculose pulmonaire déclarés chez deux patients sous Anti-TNFα (Adalimumab)
- Deux cas de syphilis - Et deux cas de salpingites.
Figure 17: Répartition des malades selon le type de l’infection bactérienne
Les infections virales étaient prédominées par l’hépatite B. Le profil sérologique d’une hépatite B guérie (Ac anti HBc présents, Ag HBs absents, Ac anti HBs présents) a été retrouvé chez quatre patients et le portage chronique asymptomatique d’hépatite virale B chez un seul cas.
L’infection par le virus de l’hépatite C a été retrouvée chez un seul cas qui présentait une cirrhose post-hépatitique C.
Les infections par l’herpès zona virus ont été notées chez deux patients, il s’agissait de : - Un cas de zona ophtalmique
- Un cas de zona intercostal survenu sous anti-TNF α (Etanercept). Arthrite septique Infection urinaire Syphilis
Salpingite
Figure 18: Répartition des malades selon le type de l’infection virale Les infections parasitaires et fongiques étaient notées chez quatre patients :
- Deux cas de candidose oesophagienne révélée lors d’un examen par fibroscopie œsogastroduodénale, dont un cas est survenu sous Rituximab
- Un cas de leishmaniose cutanée - un cas de giardiose intestinale.
La maladie gastroduodénale représentait une prévalence de 14% de l’ensemble des comorbidités. L’ulcère gastroduodénal a été noté chez trois patients alors que neuf patients avaient une gastrite, dont cinq cas de gastrite à Hélicobacter Pylori (Hp) et quatre cas de gastrite sans Hp.
La prévalence de la maladie oculaire était de 11%, la cataracte était la plus fréquente. Il s’agissait de deux cas de cataracte intéressant l’œil droit et un cas de cataracte bilatérale, deux cas de glaucome cortisonique dont un était associé à une cataracte de l’œil droit, deux patients avaient une kératite et un patient avait une épisclérite bilatérale. Les autres anomalies notées étaient : un cas d’uvéite et un cas de maculopathie.
La prévalence des pneumopathies était de 7%. L’asthme était la maladie pulmonaire la plus fréquente notée chez cinq de nos patients. La fibrose pulmonaire avec dilatation des branches (DDB) a été notée chez un seul cas.
La prévalence de la dépression était de 3%.
Dans l’étude présente, on n’a pas relevé de cas de cancer.
Infection virale par HVB Infection virale par HVC Infection virale par HZV
6. Evaluation de la prise en charge des comorbidités :
6.1. Le risque cardiovasculaire :
L'évaluation du risque cardiovasculaire, y compris la mesure de la pression artérielle, du cholestérol total, de la glycémie et de la créatininémie, a été réalisée respectivement chez 56%, 52%, 62%, 63% des patients.
Trois-quarts des patients (75%) ont eu un test d’HbA1c au cours des 6 derniers mois. En termes de mesures des résultats, il y avait une proportion plus élevée de patients atteints de PR avec un bon contrôle glycémique avec une HbA1c récente ≤7,0%, et 24% des patients avec une hyperglycémie (HbA1c ≥8%).
Les antiagrégants plaquettaires ont été prescrits dans un cadre prophylactique chez 4 patients soit 4.5% des cas. Les hypolipémiants à type de statine ont été prescrits chez 10/22 malades (45%) diagnostiqués avec une dyslipidémie.
Concernant les mesures hygiéno-diététiques, 2 patients étaient en sevrage tabagique, 37% faisaient une activité physique de façon régulière et 10% suivaient un régime diététique.
La prise en charge de ces cas était assurée principalement par les médecins rhumatologues.
6.2. Ostéoporose :
Dans la population étudiée, quatorze malades (15.9%) recevaient de la vitamine D, treize malades (14.8%) recevaient les biphosphonates et six cas (6.8%) recevaient du calcium.
Parmi les patients atteints d’ostéoporose, on avait seulement 2 cas qui recevaient la vitamine D, 7 cas recevaient les biphosphonate et un seul cas recevait le calcium.
6.3. Infections :
- Aucun de nos patients n’a reçu le vaccin antigrippal et le vaccin antipneumococcique.
- 36% des cas (n=135) ont bénéficiés d’un test à l’intradermoréaction (IDR) à la tuberculine et le quantiféron. C’était tous des patients candidats aux biothérapies
- 3 patients ont été mis sous prophylaxie antibacillaire - 1cas a été vacciné contre l’hépatite B
Figure 19: Répartition des patients en fonction des mesures instaurés dans la prise en charge des comorbidités de la PR 0 10 20 30 40 50 60 70 80
I. GENERALITES SUR LA PR
1. Epidémiologie
Les études épidémiologiques de la PR sont difficiles et donnent des résultats variables pour de nombreuses raisons : la PR est une affection hétérogène, il n’y a pas de test biologique ou radiographique suffisamment sensible et spécifique pour affirmer le diagnostic de PR à sa phase de début.
Les critères de classification ont varié dans le temps (critères de l’ARA en 1958, critères de Rome, critères de New York puis critères de l’American College of Rheumatology (ACR) révisés en 1987). Les critères de l’ACR 1987 étaient assez satisfaisants puisque dans leur description initiale, Arnett et coll [12] rapportaient une sensibilité de 93,5 % et une spécificité de 89,3 %. Cependant ces données ont été contredites par d’autres études et semblent varier en fonction de la durée d’évolution de la polyarthrite. Ces critères sont peu adaptés à la PR débutante et sont donc peu performants pour le diagnostic précoce de la PR [13]. De nouveaux critères de classification mais développés également dans un but diagnostique ont été élaborés en 2010 par l’ACR et l’EULAR [14]. Ces critères ont été établis à la fois à partir de cohortes de patients atteints d’arthrites débutantes et par une méthodologie complexe à partir de scénarios de cas-patients atteints d’arthrites débutantes (Annexe1).
La polyarthrite rhumatoïde est présente dans le monde entier. Il y a de grandes variations de la fréquence de cette maladie en fonction des pays et des éthnies. Ainsi, en Europe du Nord et en Amérique du Nord, la prévalence rapportée est de l’ordre de 0,8 % de la population adulte alors qu’elle est, en Asie, de 0,3 à 0,8 %. En Afrique, dans certaines éthnies sud-africaines, la PR est particulièrement fréquente (3,3 %) mais ceci uniquement en milieu urbain, alors qu’elle est exceptionnelle en zone rurale. Sa prévalence est particulièrement élevée dans certaines populations où le taux de consanguinité est important comme les Indiens Chipewa (5,3 %), Yakima (6 %) et Pima (5,3 %). Elle est rare en Chine, à la fois en milieu rural et urbain. En France, une étude la situe à 0,4% [15]. On peut estimer que la prévalence générale de la PR varie selon les pays, entre 0,3 et 0,8 % de la population adulte tous sexes confondus.
La PR peut survenir à tout âge mais on observe son début surtout entre 40 et 60 ans. Elle est, à cet âge, quatre fois plus fréquente chez la femme que chez l’homme. Cette différence de sexe ratio s’atténue progressivement avec l’âge au-delà de 70 ans. La PR est 2 à 3 fois plus fréquente chez les parents de sujets atteints ; sa concordance chez les jumeaux monozygotes est de 15 à 30 % et, chez les jumeaux dizygotes de 5 à 10 %.
L’incidence de la PR a fait l’objet de diverses études qui donnent, pour des raisons méthodologiques, des résultats extrêmement variables allant de 20 à 140/100.000 [16]. L’incidence habituellement retenue est de 20 à 40 pour 100.000 aux USA. En France, dans deux études réalisées dans l’ouest et le nord-est, l’incidence est respectivement de 7,6/100.000 (critères de New York) et de 8,8/100.000 (critères ACR 1987). On estime qu’il y aurait en France environ 300.000 patients atteints que ce soit par des formes bénignes, modérées ou sévères.
2. Clinique et diagnostic
2.1. Les modes de début de la PR
Il s’agit, dans la majorité des cas (70 %), d’une oligo ou polyarthrite distale d’apparition progressive intéressant les poignets, une ou plusieurs articulations métacarpophalangiennes (surtout la 2ème ou la 3ème) ou inter phalangiennes proximales, parfois les avant-pieds. Les articulations concernées sont douloureuses, partiellement enraidies. Le rythme des douleurs est caractéristique d’un rhumatisme inflammatoire.
L’atteinte articulaire est fixe et relativement symétrique. Les articulations concernées sont parfois légèrement enflées, les doigts prennent un aspect “ en fuseau ” très évocateur. Il n’y a habituellement jamais d’atteintes des interphalangiennes distales. Des signes généraux avec discrète altération de l’état général, fébricule à 38°, amaigrissement et surtout asthénie, sont fréquents.
Dans 20 % des cas environ, la PR commence comme une polyarthrite aiguë fébrile avec importante altération de l’état général, évoquant volontiers un état infectieux.
D’autres modes de début sont possibles mais plus rares :
L’atteinte rhizomélique touchant les hanches et les épaules (5% des cas), après la soixantaine, pouvant poser un problème diagnostique difficile avec la pseudo-polyarthrite rhizomélique.
Une monoarthrite (poignets ou genoux surtout) peut précéder l’apparition d’une PR de plusieurs mois ou même de plusieurs années. Au début il faudra dans ce cas éliminer une atteinte infectieuse.
Des manifestations articulaires inflammatoires intermittentes mono ou oligoarticulaires. Le rhumatisme palindromique peut en effet, dans 25 % des cas environ, correspondre au mode de début d’une PR. Il s’agit d’accès généralement mono articulaires, très inflammatoires, d’évolution spontanément régressive en 24 ou 48 heures sans séquelles mais récidivants.
Des polyarthralgies sans signes objectifs persistant pendant plusieurs mois.
Un début après un traumatisme : exceptionnellement la PR peut apparaître au décours d’un traumatisme.
La PR peut exceptionnellement commencer par des manifestations extra-articulaires isolées : vascularite, atteinte pleuro-pulmonaire, nodules rhumatoïdes.
Manifestations tendineuses : En effet les ténosynovites, fréquentes au début de la PR, ont une grande valeur diagnostique. Elles peuvent intéresser les tendons extenseurs des doigts, constituant alors une tuméfaction mobile avec les tendons sur le dos du poignet, les fléchisseurs des doigts, déterminant volontiers un syndrome du canal carpien, ou le tendon de l’extenseur ulnaire du carpe, cette dernière localisation étant particulièrement évocatrice ou, encore les longs fibulaires.
2.2. Les manifestations articulaires de la PR à la phase d’état
Les articulations touchées sont le siège d'une inflammation permanente. Cela se traduit par une tuméfaction articulaire avec hydarthrose et parfois un épaississement considérable de la synoviale et secondairement des lésions ligamentaires et ostéo-cartilagineuses et des déformations irréversibles.
Les déformations articulaires de la PR sont prévisibles. Toutes ces lésions, initialement réversibles, se fixent secondairement entrainant un handicap fonctionnel parfois majeur et des déformations inesthétiques. Seuls le rachis dorsal, lombaire et les sacro-iliaques ne sont jamais touchés
L'atteinte des mains est la plus fréquente et souvent inaugurale (90% des cas). La corrélation entre les déformations et la fonction de la main n’est pas bonne, certains malades ayant des mains très déformées conservant une fonction satisfaisante. Les déformations classiques les plus caractéristiques à la main sont la déviation ulnaire des doigts “en coup de vent”, la déformation en “col de cygne” qui touche plus particulièrement l'index et le médius, la déformation en “boutonnière” qui est fréquente, la déformation du doigt en “maillet” ou en “marteau” plus rarement. Enfin l'atteinte du pouce est particulièrement fréquente prenant soit l’aspect du pouce en “Z” liée à l’arthrite métacarpo-phalangienne, soit l’aspect en pouce adductus secondaire à une arthrite trapézo-métacarpienne.
Les poignets sont le siège d'une arthrite dans plus de 70% des cas, avec une atteinte précoce de l’articulation ulnaire inférieure, luxation de la styloïde ulnaire et arthrite radio-carpienne favorisant la limitation articulaire et l’instabilité douloureuse du carpe.
L’atteinte des pieds est presque constante. Les arthrites métatarsophalangiennes sont souvent inaugurales, entraînant progressivement un avant-pied plat puis rond avec subluxation ou luxation plantaire des métatarsiens. Des arthrites talo-naviculaires et sous-taliennes sont également fréquentes, souvent plus tardives et très douloureuses, gênant la marche et contribuant à l’affaissement de l’arche plantaire interne. L’atteinte tibio-tarsienne est plus rare mais douloureuse et source d’instabilité.
Les genoux sont fréquemment touchés, avec une arthrite prédominante dans le compartiment fémoro-tibial externe. On observe parfois un kyste du creux poplité qui peut se rompre et donner un tableau “pseudo-phlébitique” mais qui se complique rarement de compression veineuse.
Les épaules sont également fréquemment touchées, avec initialement une synovite scapulo-humérale et souvent une bursite sous-deltoïdienne entraînant non seulement des
lésions cartilagineuses puis osseuses mais également des lésions périarticulaires, notamment de la coiffe des rotateurs.
Les coudes sont touchés dans 40% des cas environ. Leur atteinte s’accompagne d’une attitude antalgique en flexion.
La coxite rhumatoïde est retrouvée dans environ 15% des cas. Il s’agit d’une localisation particulièrement grave du point de vue fonctionnel et souvent peu accessible aux traitements généraux ou locaux.
Le rachis cervical est intéressé surtout dans les polyarthrites sévères, érosives et nodulaires. L'arthrite de la charnière cervico-occipitale est la plus classique. Il peut s’agir d’une arthrite occipito-atloïdienne et surtout atloïdo-axoïdienne qui peut se traduire par des douleurs cervicales hautes ou par une luxation atloïdo-axoïdienne secondaire à la destruction du ligament transverse et souvent asymptomatique. Cette lésion, surtout si elle est instable, peut entraîner une compression médullaire cervicale haute. Le dépistage de l’atteinte cervico-occipitale est nécessaire par une radiographie du rachis cervical de face bouche ouverte et de profil avec cliché dynamique. L’IRM pourra préciser les lésions et leur retentissement neurologique. Plus rarement il existe une atteinte du rachis cervical moyen ou bas.
D’autres atteintes telles que celles des articulations temporo-mandibulaires, des sterno-claviculaires, manubrio-sternales ou crico-arythénoïdiennes sont rares.
Les ténosynovites sont pratiquement constantes à la phase d’état de la PR, essentiellement à la main où elles favorisent les déformations et peuvent se compliquer de ruptures tendineuses, notamment sur les extenseurs et les fléchisseurs des doigts. Les ténosynovites sont également fréquentes au pied, favorisant là aussi douleur et déformation.
2.3. Le diagnostic
La nécessité d’une prise en charge très précoce de la PR justifie un diagnostic dans les trois à six premiers mois après le début des symptômes [17-19].
Le diagnostic d’une PR débutante peut cependant être difficile. Il s’applique autour d’un faisceau d’arguments comportant essentiellement des manifestations cliniques et parfois
biologiques évocatrices [20]. Pour contourner ce problème de subjectivité dans le diagnostic de la PR débutante, le consensus international actuel qui a été repris par la HAS (Haute Autorité de Santé) propose d’effectuer la démarche diagnostique en trois étapes [21] :
1ère étape : reconnaître un rhumatisme inflammatoire débutant
Pouvant correspondre à une PR (PR « possible »). Ceci repose sur des arguments cliniques dont le meilleur est l’existence d'au moins deux articulations gonflées mais également un dérouillage matinal de plus de trente minutes sur les articulations périphériques et une douleur à la pression transverse des avant-pieds et des métacarpophalangiennes (squeeze test).
2ème étape : éliminer un autre rhumatisme inflammatoire défini
3ème étape : rechercher devant cette PR « probable » des éléments permettant de prédire l’évolution vers une polyarthrite chronique et destructrice (recherche des facteurs pronostiques)
a. Les critères de classification 2010 ACR et l’EULAR
Ils ont été élaborés également dans un but diagnostique. Pour lui être appliqués, un patient doit avoir au moins une synovite clinique constatée par un expert rhumatologue et qui ne réponde pas à un autre diagnostic plus probable que la PR. Dans ce cas les critères à tester comportent 4 types d’items pondérés :
- mode d’atteinte articulaire évaluée sur les articulations gonflées ou douloureuses à la pression ou encore sur l’imagerie pour les centres entrainés (IRM, échographie) ; la pondération dépend surtout du nombre et du type d’atteintes (petites ou grosses articulations).
- sérologie : présence de facteur rhumatoïde ou d’ACPA, avec un poids différent en fonction d'un titre faible ou élevé (plus de 3 fois la limite supérieure de la normale)
- inflammation biologique : VS ou CRP normale / anormale
- durée des symptômes (synovite) inférieure ou supérieure à 6 semaines
Si le patient a un score d’au moins 6 sur 10 il répond au diagnostic de PR définie
Si le patient a des érosions radiologiques typiques de PR il répond également aux critères même si le score n’est pas validé. Cette lésion caractéristique sera évaluée sur le nombre
d'articulations sièges d'au moins une érosion parmi celles évaluées par le score de Sharp van der Heijde (métacarpophalangiennes et inter phalangiennes aux mains, partie proximale du poignet, métacarpophalangiennes des orteils et inter phalangienne de l'hallux). On considérera l'atteinte "typique" si au moins 3 de ces articulations présentent une érosion [22; 23].
3. Examens complémentaires
3.1. Biologiques
a. Syndrome biologique inflammatoire
Il existe dans 90 % des cas un syndrome inflammatoire non spécifique, avec augmentation de la vitesse de sédimentation globulaire (VS), et/ou de la C Réactive protéine (CRP). La normalité de ces examens n’élimine toutefois pas le diagnostic.
L’électrophorèse des protéines sériques objective une augmentation des alpha-2 et, parfois, des gammaglobulines.
Il existe parfois une anémie modérée d’origine inflammatoire.
On peut également noter une hyperleucocytose avec polynucléose, une thrombocytose et parfois une hyperéosinophilie.
b. Facteur rhumatoïde (FR)
Le facteur rhumatoïde (FR) est un anticorps anti-gammaglobulinique qui appartient le plus souvent à la classe des IgM. Il peut être aussi de type IgA, IgG, IgD ou IgE.
Au début de la PR, la recherche du FR est classiquement souvent négative et se positiverait secondairement. La présence d’un taux significatif de FR à ce stade est un élément de mauvais pronostic [24]. Chez certains patients le FR peut être présent dans le sérum sans aucune manifestation clinique et ceci plusieurs années avant le début de la PR.
Le FR est présent dans 80 à 85 % des cas, ce qui correspondait aux PR dites “séropositives” par opposition aux PR “séronégatives” chez lesquelles il n’y avait pas de FR décelable.

![Tableau III : Etude de la vitesse de sédimentation et de la protéine C réactive. La valeur moyenne Les extrêmes VS >30mm (N=83) 52,6± 20,62 [26-95] CRP>20mg/l (N=78) 30± 13,85 [21-67] 0 10 20 30 40 50](https://thumb-eu.123doks.com/thumbv2/123doknet/1999215.2058/38.892.124.828.960.1040/tableau-etude-vitesse-sedimentation-proteine-reactive-moyenne-extremes.webp)