Mobilisation des dépôts ectopiques de tissu adipeux : ses implications dans
la résolution des comorbidités associées à l’obésité sévère suivant une
chirurgie bariatrique
Thèse
Audrey Auclair
Doctorat en sciences pharmaceutiques
Philosophiae doctor (Ph.D.)
Québec, Canada
Mobilisation des dépôts ectopiques de tissu adipeux : ses implications dans
la résolution des comorbidités associées à l’obésité sévère suivant une
chirurgie bariatrique
Thèse
Audrey Auclair
Sous la direction de :
Résumé
La prévalence de l’obésité sévère ne cesse d’augmenter. La problématique associée à l’obésité sévère est la présence possible de nombreuses comorbidités qui peuvent coexister et altérer le système cardiovasculaire, pulmonaire, endocrinien, articulaire et même favoriser le développement de certains cancers. L’excès de poids, plus particulièrement l’excès de tissu adipeux, sont tous deux liés au développement de ces comorbidités. Aucune donnée n’est disponible quant au rôle de la déposition ectopique du tissu adipeux. Considérant le caractère morbide de l’obésité sévère, la mortalité de toute cause augmentée et l’espérance de vie réduite, à ce jour le seul traitement dit efficace à long terme pour le traitement de l’obésité sévère est la chirurgie bariatrique. L’efficacité est définie par la perte de poids, le maintien à long terme de cette perte de poids ainsi que par l’amélioration ou la résolution des comorbidités. L’intérêt clinique et scientifique pour la chirurgie bariatrique est grandissant. Un nombre important d’études s’intéresse aux mécanismes sous-jacents de la résolution des comorbidités. Le diabète de type 2 est la comorbidité la plus étudiée et peu d’études se sont intéressées aux déterm meil.inants de la résolution de l’hypertension artérielle et de l’apnée obstructive du som
Comme premier objectif, cette thèse visait à caractériser les différences de la composition corporelle et de la distribution du tissu adipeux de patients obèses sévères avec ou sans diagnostic de diabète de type 2, d’hypertension artérielle et d’apnée obstructive du sommeil. Le deuxième objectif de cette thèse visait à comparer l’évolution postopératoire suite à une chirurgie bariatrique sur les changements de la composition corporelle et de la distribution du tissu adipeux selon le statut de résolution du diabète de type 2, de l’hypertension artérielle et de l’apnée obstructive du sommeil. De plus, considérant le peu d’évidences dans la littérature au sujet des déterminants de la résolution de l’hypertension artérielle et de l’apnée obstructive du sommeil, l’évaluation du profil inflammatoire, des adipokines et de l’activité du système nerveux autonome ont aussi été caractérisés.
Premièrement, nous avons documenté qu’en présence d’obésité sévère, la déposition ectopique du tissu adipeux était plus importante chez les patients avec un diabète de type 2, une hypertension artérielle et une apnée obstructive du sommeil comparativement à ceux n’ayant pas ces comorbidités. Nous avons par la suite montré que la résolution du diabète de type 2 et de l’hypertension artérielle était caractérisée par une réduction plus
importante du tissu adipeux viscéral. Au contraire, la résolution de l’apnée obstructive du sommeil était plutôt caractérisée par une réduction plus importante du tissu adipeux sous-cutané à la mi-cuisse et par une tendance à une perte de poids plus élevée. De plus, nous avons observé que chez les patients qui n’avaient pas résolu leur diabète de type 2, leur hypertension artérielle et leur apnée obstructive du sommeil, la quantité de tissu adipeux viscéral, à 12 mois suivant la chirurgie bariatrique, était plus importante comparativement à celle mesurée chez les patients n’ayant pas résolu ces comorbidités. Spécifiquement à l’évaluation du profil inflammatoire et des adipokines, nous avons observé que chez les patients obèses sévères, la présence de l’hypertension artérielle et de l’apnée obstructive du sommeil n’était pas caractérisée par un profil altéré au niveau des marqueurs inflammatoires et des adipokines. Également, nous n’avons pas observé de changements majeurs qui pouvaient expliquer, en partie, la résolution de l’hypertension artérielle et de l’apnée obstructive du sommeil. Quant à l’activité du système nerveux autonome, nous avons observé une faible activité du système nerveux parasympathique chez les patients obèses sévères avec hypertension artérielle et apnée obstructive du sommeil. Nous avons également documenté que la résolution de l’hypertension artérielle et de l’apnée obstructive du sommeil était associée à une tendance à une augmentation plus importante de l’activité parasympathique du système nerveux autonome.
Les résultats obtenus au cours de ce doctorat supportent l’importance de la déposition ectopique du tissu adipeux en situation d’obésité sévère, particulièrement le rôle du tissu adipeux viscéral, dans le développement du diabète de type 2, de l’hypertension artérielle et de l’apnée obstructive du sommeil ainsi que dans la résolution de ces comorbidités suivant une chirurgie bariatrique. D’autres recherches devront davantage s’intéresser à la mobilisation des dépôts ectopiques de tissu adipeux comme un déterminant important dans la résolution à plus long terme de ces comorbidités.
Abstract
Prevalence of severe obesity has risen considerably. Severe obesity is associated with many deleterious health effects that can impact on the cardiovascular, pulmonary and endocrine systems, and to promote the development of cancers. Excess weight, especially excess fat, are both related to the development of comorbidities. However, no data is available on the role of ectopic fat deposition in promoting the development of associated comorbidities. Considering the morbidity of severe obesity and also the increased mortality and the decreased life expectancy, the only treatment that allows significant weight loss, long-term maintenance of weight loss and improvement or cure of comorbidities is bariatric surgery. The interest for bariatric surgery is growing and a significant number of studies focus on mechanisms underlying resolution of comorbidities. Type 2 diabetes is the comorbidity the most commonly studied whereas few studies have examined the determinants of hypertension and obstructive sleep apnea resolution.
The first objective of this thesis aimed to characterize the difference in body composition and body fat distribution of severely obese patients with or without type 2 diabetes, hypertension and obstructive sleep apnea. The second objective of this thesis was to compare the postoperative changes in body composition and body fat distribution according to the resolution of type 2 diabetes, hypertension and obstructive sleep apnea. Moreover, considering the lack of evidence in the literature regarding the determinants of the resolution of hypertension and obstructive sleep apnea: the inflammatory profile, adipokines and autonomic nervous activity have also been characterized.
We have documented that in the presence of severe obesity, ectopic fat deposition was higher in patients with type 2 diabetes, hypertension and obstructive sleep apnea compared to those without these comorbidities. Also, we have shown that resolution of type 2 diabetes and hypertension was characterized by a greater reduction in visceral adipose tissue. This is in contrast with obstructive sleep apnea, where the resolution was characterized by a greater reduction of mid-thigh subcutaneous adipose tissue and a trend toward higher weight loss. In addition, we have observed that patients who had not resolved their type 2 diabetes, hypertension and obstructive sleep apnea had higher amounts of visceral adipose tissue than those who have experienced their resolution. Specifically, regarding the changes in the inflammatory profile and adipokines, we showed that in severely obese patients, hypertension and obstructive sleep apnea were not
characterized by altered inflammatory markers and adipokines concentrations, compared to severely obese patients without these comorbidities. Also, we did not observe any major changes in these variables that could explain the hypertension and obstructive sleep apnea resolution. As for the autonomic nervous system activity, we showed low parasympathetic nervous system activity in severely obese patients with hypertension and obstructive sleep apnea and documented that hypertension and obstructive sleep apnea resolution were characterized by a trend toward greater increases in parasympathetic nervous system activity.
The results obtained support the importance of the concept of ectopic fat deposition in severe obesity, especially the role of visceral adiposity in type 2 diabetes, hypertension and obstructive sleep apnea and in their resolution following bariatric surgery. More researches is needed and should focus on the mobilization of ectopic fat depots as an important mechanism implicated in the longer-term resolution of these comorbidities.
Table des matières
Résumé ... III
Abstract ... V
Table des matières ... VII
Liste des tableaux ... XII
Liste des figures ... XIV
Liste des abréviations ... XVII
Dédicaces... XIX
Remerciements ... XX
Avant-propos ... XXIII
Chapitre 1. Introduction : Obésité et obésité sévère ... 1
1.1 Définition et classification de l’obésité ... 1
1.2 Prévalence de l’obésité ... 3
1.3 Causes de l’obésité ... 3
1.3.1 Facteurs génétiques ... 4
1.3.2 Facteurs environnementaux ... 5
1.3.2.1 Inactivité physique et sédentarité ... 5
1.3.2.2 Mauvaises habitudes alimentaires ... 6
1.3.3 Adaptations physiologiques aux variations de poids ... 7
1.3.3.1 Hormones régulatrices de l’appétit ... 9
1.3.3.2 Balance énergétique ... 9
1.3.3.3 Appétit subjectif ... 10
1.4 Conséquences de l’obésité ... 11
1.4.1 Espérance de vie ... 11
1.4.2 Mortalité ... 12
Chapitre 2. Comorbidités associées à l’obésité et à l’obésité sévère ... 13
2.1 Système endocrinien ... 13
2.1.1 Pathophysiologie du diabète de type 2 ... 14
2.1.2 Causes du diabète de type 2 ... 15
2.1.3 Conséquences du diabète de type 2 ... 17
2.1.4 Facteurs de risque du diabète de type 2 ... 17
2.1.5 Prévalence du diabète de type 2 ... 18
2.1.6 Critères diagnostiques du diabète de type 2 ... 18
2.1.7 Traitements du diabète de type 2 ... 19
2.1.7.2 Approche médicale ... 21
2.1.7.3 Approche chirurgicale ... 22
2.2 Système cardiovasculaire ... 23
2.2.1 Pathophysiologie de l’hypertension artérielle ... 23
2.2.2 Causes de l’hypertension artérielle ... 24
2.2.3 Conséquences de l’hypertension artérielle ... 26
2.2.4 Facteurs de risque de l’hypertension artérielle ... 26
2.2.5 Prévalence de l’hypertension artérielle ... 27
2.2.6 Critères diagnostiques de l’hypertension artérielle ... 27
2.2.7 Traitements de l’hypertension artérielle ... 29
2.2.7.1 Modification des habitudes de vie ... 29
2.2.7.2 Approche médicale pharmacologique ... 31
2.3 Système pulmonaire ... 32
2.3.1 Pathophysiologie de l’apnée obstructive du sommeil ... 32
2.3.2 Causes de l’apnée obstructive du sommeil ... 33
2.3.3 Conséquences de l’apnée obstructive du sommeil ... 34
2.3.4 Facteurs de risque de l’apnée obstructive du sommeil ... 35
2.3.5 Prévalence de l’apnée obstructive du sommeil ... 35
2.3.6 Critères diagnostiques de l’apnée obstructive du sommeil ... 36
2.3.6.1 Polysomnographie en laboratoire ... 36
2.3.6.2 Polysomnographie ambulatoire à domicile ... 36
2.3.7 Traitements de l’apnée obstructive du sommeil ... 38
2.3.7.1 Modification des habitudes de vie ... 38
2.3.7.2 Approche médicale ... 39
2.3.7.3 Approche chirurgicale ... 40
Chapitre 3. Métabolisme des lipoprotéines, du glucose et des lipides ... 41
3.1 Métabolisme des lipoprotéines ... 41
3.1.1 Voie exogène ... 41
3.1.2 Voie endogène ... 42
3.1.3 Transport inverse ... 43
3.2 Métabolisme du glucose et des lipides ... 44
3.2.1 Foie ... 44
3.2.2 Tissu adipeux ... 46
3.2.3 Muscle squelettique ... 47
3.2.4 Régulation hormonale du métabolisme des glucides et des lipides ... 49
3.2.4.1 Insuline ... 49
3.2.4.2 Glucagon ... 50
3.3 Régulation anormale du métabolisme des glucides et des lipides dans la résistance à l’insuline, le diabète de type 2 et l’obésité. ... 50
3.3.1 Tissu adipeux ... 51
3.3.2 Muscle squelettique ... 51
Chapitre 4. Excès de tissu adipeux et dépôts ectopiques du tissu adipeux .. 54
4.1 Processus d’accumulation du tissu adipeux ... 54
4.2 Perspective historique des dépôts ectopiques du tissu adipeux à la région abdominale et glutéo-fémorale ... 55
4.2.1 Région abdominale ... 55
4.2.2 Région glutéo-fémorale ... 56
4.3 Anatomie et morphologie du tissu adipeux ... 56
4.3.1 Région abdominale ... 56
4.3.2 Région glutéo-fémorale ... 58
4.4 Hyperplasie et hypertrophie des adipocytes à la région abdominale et glutéo-fémorale ... 58
4.4.1 Région abdominale ... 59
4.4.2 Région glutéo-fémorale ... 59
4.5 Activité métabolique des adipocytes ... 60
4.5.1 Différence régionale de l’activité métabolique ... 60
4.5.2 Activité de la lipoprotéine lipase ... 62
4.5.3 Mise en réserve postprandiale des lipides ... 62
4.5.4 Débit sanguin régional du tissu adipeux ... 63
4.5.5 Synthèse de cytokines ... 63
Chapitre 5. Évaluation de la composition corporelle et de la distribution du
tissu adipeux ... 68
5.1 Indice de masse corporelle ... 68
5.2 Circonférence de taille ... 70
5.2.1 Ratios associés à la circonférence de taille ... 72
5.2.1.1 Circonférence de taille sur la taille ... 72
5.2.1.2 Circonférence de taille sur la circonférence de hanche ... 73
5.3 Balance à impédance ... 73
5.3.1 Caractéristiques distinctives des balances à impédance ... 74
5.3.1.1 Type d’appareils : monofréquence ou multifréquence ... 74
5.3.3.2 Système d’électrodes : 4 électrodes ou 8 électrodes ... 75
5.4 Absorption biphotonique à rayon X ... 77
5.5 Tomodensitométrie ... 80
5.6 Résonance magnétique ... 84
Chapitre 6. Prise en charge de l’obésité et de l’obésité sévère ... 87
6.1 Approche non-pharmacologique ... 88
6.1.1 Lignes directrices canadiennes ... 88
6.1.2 Lignes directrices américaines ... 88
6.1.3 Lignes directrices spécifiques pour les patients obèses sévères en attente d’une chirurgie bariatrique ... 89
6.1.5 Étude DPP ... 90
6.2 Approche pharmacologique ... 94
6.2.1 Orlistat (XENICAL®) ... 94
6.2.2 Lorcasérine (Belviq®) ... 95
6.2.3 Combinaison Phentermine / Topiramate à libération prolongée (Qsymia®) ... 96
6.2.4 Combinaison Naltrexone / Bupropion (Contrave®) ... 97
6.2.5 Liraglutide (Saxenda®) ... 98
6.3 Approche pharmacologique hors indication pour le traitement de l’obésité ... 99
6.3.1 Inhibiteur du cotransporteur sodium-glucose de type 2 ... 99
6.3 Approche chirurgicale ... 105
Chapitre 7. Chirurgie bariatrique ... 106
7.1 Digestion des aliments ... 106
7.2 Critères d’inclusion et d’exclusion pour la chirurgie bariatrique ... 107
7.3 Chirurgies bariatriques ... 108
7.3.1 Chirurgies bariatriques restrictives ... 108
7.3.1.1 Anneau gastrique ajustable ... 109
7.3.1.2 Gastrectomie pariétale ... 111
7.3.2 Chirurgies bariatriques mixtes ... 112
7.3.2.1 Dérivation gastrique Roux-en-Y ... 112
7.3.2.2 Dérivation biliopancréatique avec commutation duodénale ... 114
7.4 Résultats de la chirurgie bariatrique ... 116
7.4.1 Taux de complications et de mortalité postopératoire ... 116
7.4.2 Perte de poids ... 117
7.4.3 Résolution des comorbidités ... 117
7.4.3.1 Diabète de type 2 ... 118
7.4.3.2 Hypertension artérielle ... 119
7.4.3.3 Apnée obstructive du sommeil ... 120
7.5 Nouvelles technologies en chirurgie bariatrique ... 120
7.5.1 Électrostimulation gastrique ... 121
7.5.2 Ballon intragastrique ... 122
7.5.3 Plicature gastrique ... 123
7.5.4 Dispositif « EndoBarrier » ... 124
7.5.5 Dispositif « ValenTx » de dérivation gastrique ... 125
7.5.6 Dispositif « AspireAssist » ... 126
Chapitre 8. Objectifs et hypothèses de recherche ... 128
Chapitre 10. Article “Role of bariatric surgery in diabetes” ... 170
Chapitre 11. Article “Is there a role for visceral adiposity in inducing type 2
diabetes remission in severely obese patients following biliopancreatic
diversion with duodenal switch surgery?” ... 189
Chapitre 12. Article “Bariatric Surgery-Induced Resolution of Systemic
Hypertension and Obstructive Sleep Apnea: Analysis of Ectopic Fat
Mobilization, Autonomic Nervous Modulation, Inflammatory and Adipokines
Profiles” ... 215
Chapitre 13. Discussion et conclusion ... 246
13.1 Résumé des principaux résultats et discussion ... 246
13.2 Perspective ... 252
13.3 Conclusion ... 256
Annexe 1. Table de la classification du poids de la Metropolitan Life
Insurance Compagny pour les femmes adultes âgées entre 25 et 59 ans. .. 306
Annexe 2. Table de la classification du poids de la Metropolitan Life
Insurance Compagny pour les hommes adultes âgés entre 25 et 59 ans. ... 309
Annexe 3. Table de classification du gabarit, selon la largeur entre les
épicondyles de l’humérus, chez
les femmes et les hommes adultes âgés
entre 25 et 64 ans.
... 312
Annexe 4. Illustration de la première représentation des différentes
catégories d’indice de masse corporelle arbitrairement déterminées à 25, 30
et 40 kg/m
2. ... 314
Annexe 5. Article « If not dieting, how to lose weight? Tips and tricks for a
better global and cardiovascular health » ... 316
Annexe 6. Article « Omentin changes following bariatric surgery and
predictive links with biomarkers for risk of cardiovascular disease » ... 353
Liste des tableaux
Chapitre 1
Tableau 1
Classification du poids selon l’indice de masse corporelle. ... 2
Tableau 2
Principales hormones peptidiques impliquées dans la régulation de la prise alimentaire. ... 8
Chapitre 2
Tableau 3
Critères diagnostiques pour le prédiabète et le diabète de type 2. ... 19
Tableau 4
Hypoglycémiants pour le traitement du diabète de type 2. ... 21
Tableau 5
Classification de la pression artérielle chez l’adulte. ... 27
Tableau 6
Critères canadiens pour le diagnostic de l’hypertension artérielle selon la méthode de mesure ... 28
Tableau 7
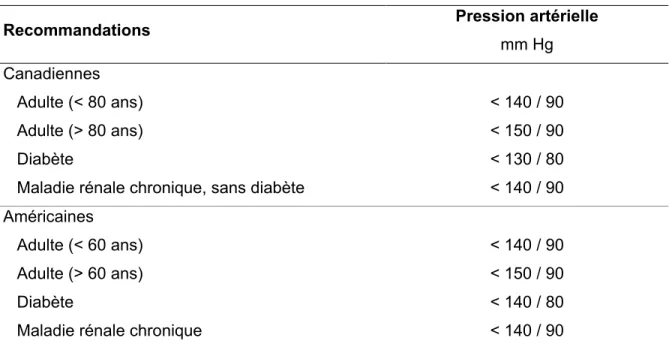
Valeurs cibles à atteindre pour le traitement de l’hypertension artérielle. ... 29
Tableau 8
Réduction approximative attendue de la pression artérielle systolique suivant la
modification des habitudes de vie. ... 31
Tableau 9
Principaux antihypertenseurs pour le traitement de l’hypertension artérielle. ... 31
Chapitre 4
Tableau 10
Chapitre 5
Tableau 11
Évolution de la classification du poids selon l’indice de masse corporelle. ... 69
Tableau 12
Seuils à risque de la circonférence de taille selon le genre et l’ethnicité. ... 72
Tableau 13
Coefficient de densité utilisé pour la segmentation des images de l’abdomen et de la cuisse de la tomodensitométrie. ... 82
Chapitre 6
Tableau 14
Effets d’une intervention de modification des habitudes de vie, incluant l’activité physique, chez des patients avec une obésité de classe 2 et de classe 3, sur le poids, l’indice de masse corporelle, la masse grasse et les paramètres en lien avec le profil
cardiométabolique. ... 92
Tableau 15
Résultats de perte de poids à 1 an dans les essais cliniques randomisés. ... 101
Tableau 16
Changements du profil cardiométabolique à 1 an dans les essais cliniques randomisés. ... 103
Chapitre 7
Tableau 17
Critères d’inclusion et d’exclusion à la chirurgie bariatrique. ... 108
Tableau 18
Critères de définition pour la résolution du diabète de type 2, de l’hypertension artérielle et de l’apnée obstructive du sommeil suivant une chirurgie bariatrique. ... 118
Liste des figures
Chapitre 2
Figure 1
Principales comorbidités associées à l’obésité et à l’obésité sévère. ... 13
Figure 2
Métabolisme normal du glucose. ... 14
Figure 3
Évolution de la glycémie à jeun et de la capacité sécrétoire du pancréas en insuline. ... 15
Figure 4
Principales conséquences macrovasculaires, microvasculaires et neuropathiques
associées au diabète de type 2. ... 17
Figure 5
Boucle de régulation rénine-angiotensine-aldostérone de la pression artérielle. ... 24
Figure 6
Principales conséquences de l’hypertension artérielle. ... 26
Figure 7
Pathophysiologie de l’apnée obstructive du sommeil. ... 33
Chapitre 3
Figure 8
Voie exogène et endogène du métabolisme des lipides. ... 42
Figure 9
Transport inverse du cholestérol. ... 44
Figure 10
Métabolisme au niveau hépatique des glucides et des lipides. ... 45
Figure 11
Métabolisme au niveau du tissu adipeux des glucides et des lipides. ... 47
Figure 12
Chapitre 4
Figure 13
Processus normal et dysfonctionnel d’accumulation du tissu adipeux. ... 55
Figure 14
Division anatomique du tissu adipeux à la région abdominale et glutéo-fémorale. ... 57
Chapitre 5
Figure 15
Mesure de la circonférence de taille chez l’homme et la femme selon les protocoles de l’Organisation mondiale de la santé et du National Institute of Health. ... 71
Figure 16
Degrés de pénétration du courant à haute et basse fréquence à travers le milieu
cellulaire. ... 75
Figure 17
Transport du courant électrique selon le modèle de balance à impédance. ... 76
Figure 18
Illustration d’un appareil d’absorption biphotonique à rayon X. ... 78
Figure 19
Dose efficace moyenne reçue lors d’examens médicaux. ... 80
Figure 20
Illustration de la tomodensitométrie. ... 81
Figure 21
Illustration de la résonance magnétique. ... 85
Chapitre 6
Figure 22
Prise en charge de l’obésité. ... 87
Chapitre 7
Figure 23
Chapitre 7 (suite)
Figure 24
Chirurgie restrictive, l’anneau gastrique ajustable. ... 110
Figure 25
Chirurgie restrictive, la gastrectomie pariétale. ... 111
Figure 26
Chirurgie mixte, la dérivation gastrique Roux-en-Y. ... 113
Figure 27
Liste des abréviations
Abréviations
ASMBS : American society for metabolic and bariatric surgery : Bêta
BID : Deux fois par jour CCK : Cholécystokinine cm : Centimètre
CRP : Protéine C réactive
DASH : Dietary approaches to stop hypertension DEXA : Absorption biphotonique à rayon X DPP-4 : Dipeptidyl peptidase-4
Dr : Docteur g : Gramme
GIP : Peptide insulinotrope glucodépendant GLP-1 : Glucagon-like peptide
GLUT 2 : Transporteur de glucose 2 GLUT 4 : Transporteur de glucose 4 HbA1c : Hémoglobine glyquée HDL : lipoprotéine de haute densité HU : Hounsfield units
IAH : Index d’apnée-hypopnée IC : Intervalle de confiance ID : Une fois par jour
IDL : Lipoprotéine de densité intermédiaire IL-6 : Interleukine 6
IMC : Indice de masse corporelle IOTF : International obesity task force kg : Kilogramme
kg/m2 : Kilogramme par mètre élevé au carré kHz : Kilohertz
kcal/jour : Kilocalorie par jour LDL : lipoprotéine de faible densité n : Nombre
NIH : National institutes of health
OMS : Organisation mondiale de la santé mSv : Millisievert
PaO2 : Pression partielle en oxygène
PaCO2 : Pression partielle en dioxyde de carbone PAD : Pression artérielle diastolique
PAS : Pression artérielle systolique PC1 : Prohormone convertase 1 PHN/TPM : Phentermine/topiramate POMC : Proopiomélanocortine
PP : Peptide P
PPAR : Peroxisome proliferator-activated receptor gamma PYY : Peptide YY
LEP : Gène codant de la leptine
LEPR : Gène codant le récepteur de la leptine m2 : Mètre élevé au carré
MC4R : Récepteur de la mélanocortine-4 METs : Équivalent métabolique
mg : Milligramme ml : Millilitre
mm Hg : Millimètre de mercure mmol/L : Millimole par litre n/a : Non admissible
SGLT2 : Inhibiteur du cotransporteur sodium-glucose de type 2 T : Tesla
TID : Trois fois par jour
TNF- : Facteur de nécrose tumoral alpha VLDL : Very low-density lipoprotein
5-HT2 : 5-Hydroxytryptamine2
Noms d’études
ACCORD : Action to control cardiovascular risk in diabetes
ADVANCE : Action in diabetes and vascular disease: Preterax and Diamicron MR controlled evaluation
BLOOM : Behavioral modification and Lorcaserin for overweight and obesity management BLOOM-DM : Behavioral modification and Lorcaserin for overweight and obesity
management in diabetes mellitus
BLOSSOM : Behavioral modification and Lorcaserin second study for obesity
management
COR-I : Contrave obesity research I COR-II : Contrave obesity research II
COR-BMOD : Contrave obesity research - behavior modification COR-D : Contrave obesity research - diabetes
DPP : Diabetes prevention program
Look AHEAD : Look action for health in diabetes
SCALE maintain : Satiety and clinical adiposity – Liraglutide evidence in non-diabetic and diabetic individuals - maintain
SCALE obesity : Satiety and clinical adiposity - Liraglutide evidence in non-diabetic and diabetic individuals - obesity
Dédicaces
À mon directeur de recherche, Dr Paul Poirier. Un énorme merci pour ces belles années aux études graduées. Je te remercie de ton dévouement, de ta disponibilité, de tes conseils et merci pour ces nombreuses séances de discussion qui ont été, tout simplement, une source d’inspiration et de dépassement pendant toutes ses années. À mon équipe de recherche. Infirmières, secrétaires et étudiantes, c’est pour moi un réel plaisir de vous avoir côtoyé pendant toutes ces années. C’est à vous tous que je dois le plaisir quotidien de mes études. Vous êtes la meilleure équipe de recherche en ville ! À ma formidable sœur Karen. Mon infirmière, ma professionnelle en gâteau, ma coéquipière de « cupcakes » et ma compagne en vélo de montagne, je te remercie pour tes nombreux encouragements et pour tous tes petits plats que tu m’as amenés à l’hôpital ! Je suis choyée d’avoir une sœur comme toi. Je t’aime ma sœur.
À mes parents Valérie et Clément que j’aime plus que tout. Mes fidèles à l’entrainement, je suis fière de vous ! Vous rayonnez de bonheur à la retraite. Je vous dois entièrement cette thèse, pour vos encouragements, votre présence, votre confiance et votre support. Je ne le vous dirai jamais assez, merci. Je vous aime.
Finalement, et non le moindre, à celui qui partage ma vie, Laurence. Mon designer graphiste, mon partenaire d’entraînement à la course à pied et à vélo, mon amoureux depuis plus de 11 ans, je ne te remercierai jamais autant pour ton support à travers toutes ces années. Merci de faire partie de mon quotidien, merci de ta patience des derniers mois et merci d’être la personne que tu es. Les prochaines années nous réserveront de belles surprises. Je t’aime fort.
Remerciements
Déjà plusieurs années se sont écoulées depuis le début de mes études graduées. C’est avec beaucoup d’émotions que je tiens à remercier les nombreuses personnes avec qui j’ai vécu cette belle aventure.
Merci à Dr Paul Poirier de m’avoir accueilli comme étudiante, lors de mes débuts à la maitrise. À ce moment-là, j’avais mon idée de carrière et au grand jamais j’aurais pensé faire des études doctorales. Je suis fière d’avoir foncé dans cette aventure qu’est le doctorat. Merci pour tous ces congrès, je n’en serai jamais autant reconnaissante. Je suis choyée et privilégiée d’avoir accompli cette importante étape de ma carrière à tes côtés. Paul, tu es inspirant, ton énergie est contagieuse, tu débordes d’idées (parfois farfelues !) et ta personnalité colorée, a fait de toi le mentor idéal à mes yeux. Merci pour ta présence, merci pour tes encouragements et merci de m’accueillir à nouveau (!) dans ton équipe de recherche.
Je tiens aussi à remercier la merveilleuse équipe de recherche du projet PURE. Dr Gilles R Dagenais, Murielle Cayer, Anne Leblanc De Bluts, Anne-Sophie Bourlaud et Ginette Turbide, j’ai apprécié énormément travailler à vos côtés dans cette grande aventure. Nos 5 à 7, nos soupers, nos périples sur la route et nos soirées chez les sœurs avec nos sacs de croustilles (!), sont tous des souvenirs inoubliables qui me feront toujours sourire. Un merci spécial à Ginette pour ton écoute, ta disponibilité et pour tous ces moments divertissants où l’on a discuté de nos petites bêtes poilues ! Aussi, merci Ginette et Michel pour les personnes inspirantes que vous êtes et pour votre accueil lors de nos sorties de vélo, à Laurence et moi, sur la 138.
Pendant mon doctorat, j’ai eu la chance de créer, coordonner et participer à l’évaluation des patients dans le cadre d’un projet de recherche en activité physique en postopératoire de chirurgie bariatrique, le projet ACTIVE. N’étant pas inclus dans ma thèse, le projet ACTIVE a, tout de même, fait partie de mon quotidien pendant mes études doctorales. Il est donc très important pour moi de remercier les personnes impliquées dans cette étude. Tout d’abord, merci à tous les patients qui ont investi cœur et âme à ce projet. Vous êtes tous des personnes inspirantes pour moi, dont je garderai de merveilleux souvenirs. Je tiens à remercier les infirmières Pascale Léger, Marie-Mai Larivière et Louise Dugas pour
votre disponibilité pour les prises de sang qui étaient parfois un défi de taille ! J’aimerais aussi remercier Diane Landry pour toute ton aide au fil du temps et pour ton support administratif. J’aimerais également remercier Éric Nadreau, Didier Saey et Fernanda Ribeiro qui m’ont offert leur support et leur expertise dans l’élaboration du projet ACTIVE. De plus, merci à Jenny Carier, Élyse Morissette et à Dre Kim O’Connor pour leur collaboration essentielle dans la réalisation des échocardiographies. Merci au personnel de radiologie pour la réalisation des tomodensitométries et merci à Véronic Tremblay pour son support dans l’analyse des images de la tomodensitométrie. Je remercie également Michel Jourdain pour l’analyse des Holters. Merci au pavillon de prévention des maladies cardiaques de votre accueil pour l’entraînement en salle des patients. Je veux aussi remercier sincèrement tout le personnel de la clinique de chirurgie bariatrique. Infirmières, nutritionnistes et chirurgiens, merci d’avoir cru au projet ACTIVE et pour votre support clinique et scientifique. Un énorme merci à ma précieuse collègue Jany Harvey de m’avoir donné un gros coup de main dans la réalisation de ce projet qui n’a pas été de tout repos ! Merci à toi Paul de m’avoir fait confiance et de m’avoir permis de vivre cette belle aventure qu’est le projet ACTIVE. C’est une fierté d’avoir réalisé, avec succès, cette belle étude.
Au-delà de mes collègues de travail, je tiens également à remercier ma famille. Tout d’abord, j’aimerais remercier mes parents Valérie et Clément pour tout le support, les encouragements et l’amour reçus. La personne que je suis aujourd’hui est en grande partie grâce à vous et je vous suis extrêmement reconnaissante de tout ce que vous aviez fait pour moi.
J’aimerais remercier ma sœur Karen pour ta présence, ton aide et pour tous les petits réconforts sucrés que tu m’as amenée à l’hôpital. Merci pour tous les beaux moments que nous avons passé ensemble en voyage, sur le bord de la piscine, en vélo sur la route ou en montagne. C’est toujours mémorable et surtout rempli de rires et de péripéties. J’ai déjà hâte à l’été 2016 !
J’aimerais aussi remercier ma belle-famille : Céline, Jean, Louise, Judith, Benoit et André. Déjà 12 ans se sont écoulés depuis cette première soirée de football à Trois-Rivières. Qui aurait dit que je complèterais un doctorat, surtout qu’à cette période je désirais devenir comptable ! Vous êtes bien importants à mes yeux. C’est toujours un réel plaisir et
agréable de vous rendre visite à Trois-Rivières et au Mont St-Anne. Merci pour les bons moments autour de la table et de m’avoir encouragée tout au long de ces années.
Je tiens aussi à remercier ma précieuse collègue de travail et amie Jacinthe. Jacinthe, tu es une amie, une femme de carrière et une maman, de trois enfants (!), inspirante. Je suis énormément contente de t’avoir rencontrée pendant mes études graduées. Tu es une amie précieuse, une confidente et une personne très importante pour moi. Merci pour cette belle amitié. Merci de nous avoir donné le privilège à Laurence et moi d’être parrain et marraine du beau Jérémy ! Jacinthe, Guillaume, Julien, Gabrielle et Jérémy vous êtes une famille rayonnante de bonheur, je vous adore.
Je tiens à remercier mon amoureux, celui avec qui je partage ma vie, Laurence. Merci d’avoir été près de moi, de m’avoir encouragée et d’avoir participé, à ta manière, à mes études doctorales. Je ne te remercierai jamais assez, mais merci d’avoir été mon graphiste « perso (!) » pour toutes les figures et fonds de PowerPoint que j’ai pu te demander tout au long de mes études graduées. Merci également de ta patience des derniers temps. En presque douze ans de vie de couple, nous avons déjà de magnifiques souvenirs en banque : nos voyages « dans le sud », notre voyage de ski, nos voyages de vélo et tous nos défis personnels que nous avons accomplis. Maintenant, j’ai hâte de tourner la page du doctorat et de commencer une nouvelle histoire, notre histoire. Merci de faire partie de mon quotidien, merci de faire partie de ma vie. Je t’aime.
Avant-propos
Cette thèse a comme thèmes généraux 1) l’obésité sévère, 2) la déposition ectopique du tissu adipeux, 3) la chirurgie bariatrique et 4) la résolution des comorbidités suivant une chirurgie bariatrique. À travers un continuum, ces thèmes sont abordés dans les chapitres 1 à 7.
Dans le chapitre 1, à titre d’introduction générale, l’obésité et l’obésité sévère sont les premiers sujets abordés dans cette thèse. Ensuite, dans le chapitre 2, une introduction spécifique traitant des comorbidités associées à l’obésité sévère, plus particulièrement le diabète de type 2, l’hypertension artérielle et l’apnée obstructive du sommeil, est présentée. Les chapitres 3 et 4 traitent principalement de métabolisme et de déposition ectopique du tissu adipeux. Plus spécifiquement, le chapitre 3 présente un survol des différentes voies métaboliques impliquées dans le métabolisme des lipides et du glucose. Quant au chapitre 4, il discute de la distinction anatomique du tissu adipeux, des processus d’accumulation du tissu adipeux, des processus d’hyperplasie et d’hypertrophie des adipocytes et de l’activité métabolique du tissu adipeux. Le chapitre 5 présente les différents indices et mesures pour l’évaluation de la composition corporelle et de la distribution du tissu adipeux. Ensuite, le chapitre 6 aborde les options de traitement pour la prise en charge de l’obésité et de l’obésité sévère. Pour terminer l’introduction, le chapitre 7 présente les principaux types de chirurgie bariatrique, les effets escomptés de la chirurgie sur la perte de poids et la résolution des comorbidités ainsi que les nouvelles technologies de chirurgie pour le traitement de l’obésité.
Le premier article présenté dans cette thèse (chapitre 9) intitulé « How to choose and use bariatric surgery in 2015 » est une revue de la littérature traitant principalement des effets de la chirurgie bariatrique sur les complications, sur la perte de poids et sur la résolution des comorbidités associées à l’obésité sévère. J’ai écrit cette revue en collaboration avec Dre Marie-Ève Piché, madame Jany Harvey, Dr Simon Marceau et Dr Paul Poirier. Cette revue de la littérature a été publiée dans le journal « Canadian Journal of Cardiology ».
Le deuxième article présenté dans cette thèse (chapitre 10) intitulé « Role of bariatric surgery in diabetes » est une autre revue de la littérature discutant plus particulièrement de l’importance de la chirurgie bariatrique spécifiquement dans le diabète de type 2. Cette
revue de la littérature a été écrite avec la collaboration de Dr Paul Poirier. Elle a été publiée dans le journal « Current Cardiology Reports ».
Le troisième article présenté dans le chapitre 11 intitulé « Is there a role for visceral adiposity in inducing type 2 diabetes remission in severely obese patients following biliopancreatic diversion with duodenal switch surgery? » est le premier article de résultats provenant de mes travaux au doctorat. Dans un premier temps, nous nous sommes intéressés à caractériser la composition corporelle et la distribution du tissu adipeux chez des patients obèses sévères avec ou sans diabète de type 2. Dans un deuxième temps, nous avons comparé l’évolution postopératoire de la composition corporelle et de la distribution du tissu adipeux selon le statut de résolution du diabète de type 2, à 6 et 12 mois suivant une chirurgie bariatrique mixte, la dérivation biliopancréatique avec commutation duodénale. Bien que le diabète de type 2 est la comorbidité la plus étudiée dans le domaine de la chirurgie bariatrique, il n’y avait aucune étude évaluant précisément le rôle de la mobilisation du tissu adipeux ectopique dans la résolution du diabète de type 2 suivant une chirurgie bariatrique. Les données utilisées pour l’écriture de cet article proviennent d’un projet de recherche dont l’évaluation de tous les patients a été effectuée par Dre Julie Martin et Mme Marjorie Bastien. Tous les chirurgiens bariatriques, soit les Drs Laurent Biertho, Simon Marceau, Frédéric-Simon Hould, Simon Biron, Stéfane Lebel et Odette Lescelleur, ont participé au recrutement des patients. Tous les auteurs ont pris part à la révision de l’article. Pour ma part, j’ai analysé les images de la tomodensitométrie de l’abdomen et de la mi-cuisse et j’ai effectué l’écriture de l’article. Cet article est publié en ligne dans le journal « Obesity Surgery ».
Le dernier article présenté dans le chapitre 12 intitulé « Bariatric surgery induced resolution of systemic hypertension and obstructive sleep apnea: analysis of ectopic fat mobilization, autonomic nervous modulation, inflammatory and adipokines profiles » est le deuxième article de résultats de mes travaux au doctorat. Nous nous sommes intéressés à caractériser la composition corporelle, la distribution du tissu adipeux, le profil inflammatoire, les concentrations d’adipokines et l’activité du système nerveux autonome chez des patients obèses sévères avec ou sans hypertension artérielle et apnée obstructive du sommeil. Dans un deuxième temps, nous avons comparé l’évolution de tous ces paramètres, à 12 mois suivant une dérivation biliopancréatique avec commutation duodénale, selon le statut de résolution de l’hypertension artérielle et de
l’apnée obstructive du sommeil. Au contraire du diabète de type 2, ces deux comorbidités sont très peu étudiées dans le domaine de la chirurgie bariatrique et peu d’évidences sur les mécanismes associés à la résolution de ces comorbidités sont connues. Les données utilisées pour l’écriture de cet article proviennent d’un projet de recherche dont l’évaluation de tous les patients a été effectuée par Dre Julie Martin et Mme Marjorie Bastien. Tous les chirurgiens bariatriques, soit les Drs Laurent Biertho, Simon Marceau, Frédéric-Simon Hould, Simon Biron, Stéfane Lebel et Odette Lescelleur, ont participé au recrutement des patients. Les Drs Katherine Cianflone, David St-Pierre, Sebastian Demian Parlee et Kerry Goralski ont été impliqués dans le dosage des adipokines incluses dans cet article. Le Dr Yves Lacasse, pneumologue, a participé à l’interprétation des résultats et l’écriture de l’article. Tous les auteurs ont pris part à la première révision de l’article. Pour ma part, j’ai analysé les images de la tomodensitométrie de l’abdomen et de la mi-cuisse et j’ai effectué l’écriture de l’article. Cet article est présentement en deuxième révision auprès des coauteurs et sera soumis prochainement.
Finalement, dans le chapitre 13, une discussion générale soulignant les principaux résultats, les perspectives de mes travaux de doctorat ainsi qu’une conclusion évoquant les futures pistes de recherche clorent la présente thèse.
L’annexe 5 et 6, sont deux articles publiés pour lesquels je suis coauteure. L’annexe 5 intitulée « If not dieting, how to lose weight? Tips and tricks for a better global and cardiovascular health » est une revue de la littérature dont j’ai collaboré à l’écriture de la section sur les mesures d’adiposité et à la révision de l’article. Quant à l’annexe 6 ayant pour titre « Omentin changes following bariatric surgery and predictive links with biomarkers for risk of cardiovascular disease », mon implication a été principalement dans la création de la base de données et dans la révision de l’article.
Chapitre 1.
Introduction : Obésité et obésité sévère
Depuis des siècles, l’obésité a évolué : ses origines remontent à 30 000 ans1. Pendant des milliers d’années, le surpoids et l’obésité étaient une condition exceptionnelle, rarement vue et très peu étudiée jusqu’à tout récemment1. L’obésité était plutôt prisée et considérée comme un signe de richesse et de prospérité : seuls les plus riches avaient la possibilité de devenir obèses1. Le degré d’obésité caractérisait même le niveau de richesse à défaut des vêtements et des bijoux voyants. Les Grecs ont été les pionniers à réaliser les dangers de l’obésité et son association avec les maladies1. À ce sujet, Hippocrate a été le premier à identifier le concept de l’équation de la balance énergétique soulignant que pour conserver son corps dans un état stable, tout aliment ingéré devait être compensé par un exercice quelconque pour éliminer l’excès d’énergie1. Des dizaines de milliers d’années se sont écoulées depuis la survenue de l’obésité. La situation n’est guère plus réjouissante ayant atteint un niveau d’épidémie mondiale2. Dans ce chapitre, un survol de la définition, de la prévalence, des causes et des conséquences liées à l’obésité est présenté.
1.1 Définition et classification de l’obésité
L’Organisation mondiale de la santé (OMS) définit le surpoids et l’obésité comme « une accumulation anormale ou excessive de graisse qui présente un risque pour la santé »3. Historiquement, l’obésité était définie à partir du concept de poids idéal et celui-ci a été largement utilisé pour la classification du poids. Établi à partir de données fournies par les compagnies d’assurance, les valeurs de référence de poids idéal étaient spécifiques selon la grandeur, l’âge et le genre de la personne et étaient utilisées pour tenter de déterminer des valeurs de poids associées à une plus grande longévité4, 5. La table de référence de poids idéal la plus populaire est celle de la Metropolitan Life Insurance Compagny, dont la dernière mise à jour, à partir de données incluant tout près de 4,2 millions d’assurés Canadiens et Américains, remonte à 19836 (Annexe 1 et 2). Ainsi, à partir du gabarit de la personne, déterminé par la largeur entre les deux épicondyles de l’humérus7 (Annexe 3), était proposée une valeur de poids idéal, qui était associée à un faible taux de mortalité6, 8, 9. L’obésité se définissait à un poids au-delà de 20% de la valeur du poids idéal et l’obésité sévère par le double du poids idéal ou par un surplus de poids de 45 kg (100 lb) et plus, du poids idéal10. Quelques années plus tard, l’utilisation de cette table a été abandonnée
en raison de ces limitations : 1) applicable seulement chez les personnes âgées entre 25 et 59 ans, 2) non-standardisation de la mesure en ce qui concerne le port des souliers et des vêtements, et 3) valeurs de référence basées sur des valeurs de poids provenant de personnes avec des maladies chroniques et de personnes fumeuses11-13. À ce jour, cette table n’est plus d’intérêt pour la classification du poids, son utilisation a plutôt été remplacée par l’indice de masse corporelle (IMC).
L’IMC est la mesure la plus couramment utilisée pour la classification du poids chez l’adulte et se calcule à partir du poids et de la taille de la personne, selon la formule ci-dessous.
Indice de masse corporelle =
L’IMC est uniquement un rapport de proportionnalité entre le poids et la taille d’une personne ne donnant aucune information sur la distribution du poids et ne faisant aucune discrimination par rapport au genre. Cette mesure permet une classification complète du poids, allant de la catégorie poids insuffisant à obésité de classe 5 (Tableau 1). L’obésité est définie par un IMC supérieur ou égal à 30,0 kg/m2 et l’obésité sévère par un IMC supérieur ou égal à 40,0 kg/m2.
Tableau 1 : Classification du poids selon l’indice de masse corporelle.
Catégories Indice de masse corporelle
(kg/m2) Poids insuffisant 18,5 Poids normal 18,5 - 24,9 Surpoids 25,0 - 29,9 Obésité classe 1 30,0 - 34,9 Obésité classe 2 35,0 - 39,9
Obésité classe 3 ou extrême 40,0
Obésité classe 4 50,0
Obésité classe 5 60,0
Source : traduite de 14 Poirier P et al. 2009.
Les limites de l’utilisation et de l’interprétation de l’IMC sont discutées dans le chapitre 5. Poids (kg)
1.2 Prévalence de l’obésité
Auparavant, l’obésité était considérée comme un problème de santé spécifique aux pays à revenus élevés15, 16. Maintenant, elle est présente autant dans les pays à faible revenu et les pays à revenu moyen, avec une augmentation spectaculaire depuis les dernières années17-20. Ce changement a débuté avec la survenue de l’urbanisation, de l’industrialisation, de la mondialisation et du développement économique21-24. Mondialement, la prévalence combinée du surplus de poids et de l’obésité (IMC ≥ 25,0 kg/m2) a augmenté de 27,5% entre 1980 et 2013 représentant 2,1 billions d’individus25. Spécifiquement à la prévalence de l’obésité, définie par un IMC supérieur ou égal à 30 kg/m2, elle a pratiquement doublé; en 2008, 10% des hommes et 14% des femmes étaient considérés comme obèse comparativement à 5% des hommes et 8% des femmes en 198026. Au Canada, la situation n’est pas plus réjouissante; la prévalence de l’obésité a triplé entre 1985 et 2011 passant de 6,1% à 18,3%27. Depuis 1985, la prévalence de l’obésité de la classe 1 (30,0 - 34,9 kg/m2) a augmenté de 5,1% à 13,1%, de classe 2 (35,0 - 39,9 kg/m2) de 0,8% à 3,6% et de classe 3 (≥ 40,0 kg/m2) de 0,3% à 1,6%, correspondant à une augmentation respective de 257%, 450% et 533%27. Aux Etats-Unis, la situation n’est guère mieux. Entre 1986 et 2000, la prévalence respective d’un IMC supérieur à 30,0 kg/m2, à 40,0 kg/m2 et à 50,0 kg/m2 a doublé, quadruplé et quintuplé28. En contrepartie, depuis les années 2000, malgré une augmentation de la prévalence pour toutes les catégories confondues, le taux d’augmentation de la prévalence de l’obésité est beaucoup moins marqué. Malgré tout, la prévalence de l’obésité (IMC ≥ 30,0 kg/m2) reste élevée à 34,9%29 ainsi que celle pour un IMC supérieur à 40,0 kg/m2 et supérieur 50,0 kg/m2 qui sont respectivement de 6,5% et 0,5%30. Très récemment, une étude regroupant près de 19,2 millions d’individus a montré que, mondialement, 2,3% des hommes et 5,0% des femmes ont une obésité sévère définie par un IMC ≥ 35,0 kg/m2 31.
1.3 Causes de l’obésité
Vu simplement, l’obésité découle d’un bilan énergétique positif entre l’apport énergétique et la dépense énergétique32. La dépense énergétique est la somme de l’énergie dépensée
par le métabolisme de base, l’effet thermique des aliments et l’activité physique33. Le
métabolisme de base représente environ 60% de la dépense énergétique totale et l’effet thermique des aliments, qui correspond à l’énergie dépensée pour la digestion, la transformation et le stockage des aliments, compte pour environ 8 à 10% de la dépense énergétique33. Quant à la dépense énergétique associée à l’activité physique, elle est la
composante la plus variable et modulable. Une balance énergétique neutre est atteinte lorsque l’apport est équivalent à la dépense énergétique. Lorsque l’apport excède la dépense énergétique, une balance positive résulte et conséquemment, une augmentation du poids, pour laquelle 60 à 80% est de la masse grasse, s’en suit34.
Avec l’âge, l’énergie dépensée par le métabolisme de base est réduite représentant une baisse moyenne de 1 à 2% par décennie35, ce qui correspond à une diminution de la
dépense énergétique journalière d’environ 95 kilocalories, entre 20 et 70 ans. Malgré qu’il soit clairement démontré que, comparativement aux jeunes adultes, les personnes plus âgées aient un métabolisme de base plus faible, dans son ensemble, il est certes peu probable que ce phénomène explique l’augmentation de la prévalence de l’obésité avec l’âge, indépendamment des autres facteurs associés36. En réalité, l’obésité n’est tout
simplement pas le problème unique d’un déséquilibre de la balance énergétique. Elle implique un amalgame de facteurs génétiques, environnementaux et d’adaptations physiologiques aux variations de poids, principalement dans le développement de l’obésité sévère.
1.3.1 Facteurs génétiques
Le rôle des facteurs génétiques dans le développement de l’obésité est connu. Une prédisposition génétique pour l’obésité a déjà, il y a plusieurs années, été documentée chez des enfants adoptés et des jumeaux37, 38. Les défauts génétiques identifiés sont soit une atteinte de gènes uniques et rares induisant de l’obésité sévère et ce, dès l’enfance, ou une atteinte des gènes communs entre les individus qui induisent une prédisposition à développer de l’obésité dans un environnement favorable dit « obésogène »39, 40. L’héritabilité de l’obésité, définie par le degré d’influence des facteurs génétiques dans la probabilité d’apparition d’un trait phénotypique donné, n’est pas considérée comme une entité fixe37, 39, 41. Elle varie étroitement avec l’exposition à un environnement « obésogène » et semble expliquer de 30 à 70%, donc en moyenne 50%, des variations interindividuelles de poids et d’IMC40, 42, 43. En d’autres mots, cela signifie que les changements de poids d’un individu sont expliqués à 50% par le bagage génétique de celui-ci.
Il existe quelques formes monogéniques d’obésité. Elles sont rares, vont apparaître dès l’enfance, vont engendrer un gain de poids fort important et représentent moins de 5% des
cas d’obésité sévère40. Les mutations des gènes les plus fréquemment rencontrés dans les formes monogéniques d’obésité44 sont celles codant pour les gènes de la leptine (LEP)45, 46 et de son récepteur (LEPR)47, de la proopiomélanocortine (POMC)48, 49, de la prohormone convertase 1 (PC1)50, 51 et du récepteur de la mélanocortine-4 (MC4R)52. Cliniquement, l’hyperphagie est la caractéristique la plus commune de l’obésité monogénique et la stratégie préventive la plus efficace est la restriction stricte de l’accès à la nourriture39.
1.3.2 Facteurs environnementaux
Aux facteurs génétiques précédemment discutés, s’ajoutent les facteurs environnementaux qui peuvent, à différents niveaux d’importance, favoriser le développement de l’obésité chez des personnes non prédisposées génétiquement. L’inverse est aussi vrai : des conditions environnementales favorables peuvent prévenir l’obésité chez une personne prédisposée génétiquement. Les facteurs environnementaux comportent une multitude de déterminants étroitement liés à l’obésité: le statut socioéconomique faible, le milieu rural53, 54, la cessation tabagique55, 56, la surconsommation d’alcool57 et le manque de sommeil58. Quant à l’inactivité physique, la sédentarité et les mauvaises habitudes alimentaires, elles sont discutées en détail dans la présente section.
1.3.2.1 Inactivité physique et sédentarité
L’inactivité physique, c’est-à-dire ne pas faire suffisamment d’activité physique d’intensité modérée à vigoureuse59, et la sédentarité, définie par la pratique d’activités qui exigent une faible dépense énergétique (< 1,5 équivalent métabolique [METs]) pendant la période d’éveil59, ont tous deux une action indépendante60 et sont étroitement liées à la diminution de l’espérance de vie, à l’augmentation de la mortalité et impliquées dans le développement de l’obésité et de plusieurs autres maladies chroniques61-64. La modernisation et l’expansion technologique à travers le quotidien jumelées à un niveau d’occupation élevé se sont traduits, depuis les dernières décennies, par un déclin généralisé de la pratique de l’activité physique65, 66. Au Canada, le dernier rapport de l’Enquête Canadienne sur les mesures de la santé a révélé que les adultes de 18 à 79 ans effectuaient en moyenne 12 minutes d’activité physique modérée à vigoureuse par jour, ce qui correspondait à un total de 84 minutes par semaine67. Environ un
adulte sur cinq, soit 20%, respectait la recommandation Canadienne de cumuler au moins 150 minutes d’activité physique, par période minimale de 10 minutes consécutives, à une intensité de modérée à vigoureuse, par semaine67. Aux États-Unis, c’est également 20% des adultes qui respectent les recommandations d’activité physique68. L’inactivité physique est d’autant plus importante lorsque l’obésité est présente. L’enquête Canadienne de 2007 à 2011 sur l’activité physique a montré que les hommes et les femmes avec un poids normal avaient consacré quotidiennement, respectivement 34 et 23 minutes d’activité physique d’intensité modérée à vigoureuse, comparativement à 19 et 13 minutes chez les hommes et les femmes obèses69. En plus du manque d’activité physique, une proportion importante du temps de la journée est attribuée à des activités sédentaires qu’elles soient pour les loisirs ou pour le travail. En moyenne, au Canada et aux États-Unis, 70% et 55% respectivement, du temps d’une journée est consacré à des activités sédentaires67, 70 tels que le travail de bureau, les déplacements en voiture et les courts déplacements à pied dans la maison.
1.3.2.2 Mauvaises habitudes alimentaires
L’offre alimentaire a radicalement changé depuis les dernières décennies71. Au Canada, plus de 60% des produits consommés représentent des produits transformés par l’industrie agroalimentaire72. De plus, près de 30% des dépenses alimentaires hebdomadaires des ménages sont expliquées par les repas achetés dans les restaurants73. En contrepartie, le niveau socioéconomique est l’un des facteurs fortement associés à la qualité de l’alimentation et à l’obésité74-77. Le coût monétaire est un déterminant majeur des choix alimentaires, où les aliments sains sont généralement plus dispendieux que ceux riches en calories, en matières grasses, en sucre et/ou en sodium74-76. En 2014, seulement 40% des Canadiens soit 32% des hommes et 47% des femmes âgés de 12 ans et plus, rapportaient manger au moins cinq portions de fruits et légumes quotidiennement78; une proportion inférieure à celle de 2009, où 46% des Canadiens respectaient la recommandation78. Même si l’urbanisation, la modernisation, la sédentarité et l’inactivité physique sont des facteurs tous étroitement liés à l’obésité, il reste que la facilité d’accès aux aliments à densité calorique élevée, aux larges portions et aux boissons sucrées sont des facteurs pouvant facilement expliquer la surconsommation de calories. Au Canada, entre 1971 et 2008, l’offre alimentaire a
augmenté de 559 calories par personne par jour, et aux États-Unis, pour une période de temps similaire, l’augmentation a été de 768 calories79. Cet accroissement est en partie expliqué par les aliments ultra transformés qui sont appétissants, accessibles, bon marché et largement publicisés et donc qui favorisent la surconsommation de calories et le développement de l’obésité79.
1.3.3 Adaptations physiologiques aux variations de poids
À la base, le poids est régulé par un système neurohormonal très complexe. Essentiellement, les signaux impliqués dans la régulation homéostatique de la prise alimentaire et dans la balance énergétique sont intégrés au niveau du noyau arqué de l’hypothalamus80, de la partie caudale du tronc cérébral ainsi qu’au niveau du cortex et du
système limbique81. Un nombre important de neuropeptides et d’hormones sont impliqués
dans la régulation de l’appétit et agissent dans la région centrale de l’hypothalamus. Leur action est soit orexigène, c’est-à-dire qui stimule l’appétit, ou soit anorexigène, donc qui inhibe l’appétit. Quelques-uns sont présentés dans le Tableau 282. L’hypothalamus traite
les signaux en provenance de la périphérie sur la disponibilité des nutriments et sur les réserves énergétiques83, 84. Au final, des boucles de rétroaction sont créées entre le
cerveau et les organes cibles en périphérie incluant le tractus gastro-intestinal, le pancréas, le foie, le muscle squelettique et le tissu adipeux81, 84. La régulation à court,
moyen et long terme de la prise alimentaire comprend des mécanismes complexes incluant un nombre important d’hormones peptidiques soit orexigènes ou anorexigènes (Tableau 2). L’hypothalamus intègre, au niveau du cortex et du système limbique, tous les signaux hédoniques associés au principe de récompense et de palatabilité de la prise alimentaire81. En dépit de l’homéostasie dans les mécanismes régulant la faim et la
satiété, les signaux hédoniques peuvent surpasser cet équilibre et accentuer le désir de manger des aliments avec une densité énergétique élevée et donc favoriser la surconsommation d’aliments et le gain de poids81, 85, 86. Plusieurs neurotransmetteurs,
incluant ceux impliqués dans les systèmes dopaminergique, opioïdergique et cannabinoïde ont aussi un rôle important dans les mécanismes hédoniques associés à la prise alimentaire82.
Tableau 2 : Principales hormones peptidiques impliquées dans la régulation de la prise alimentaire.
Nom Sécrétée par Action
anorexigène orexigène Leptine Adipocyte x Ghréline Estomac Duodénum x Cholécystokinine (CKK) Duodénum Jéjunum x Peptide YY (PYY) Iléon Colon x Neuropeptide Y (NPY) Cerveau x Peptide P (PP) Pancréas Duodénum Jéjunum Iléon Colon x Insuline Pancréas x Polypeptide insulinotrope glucodépendant (GIP) Duodénum Jéjunum Iléon Colon proximal x ou neutre Glucagon-like peptide (GLP-1) Iléon x
Abréviations. CKK : cholécystokinine, PYY : peptide YY, NPY : neuropeptide Y, PP : peptide P, GIP : polypeptide insulinotrope glucodépendant, GLP-1 : glucagon-like peptide.
Sources : traduites et adaptées 81Lenard NR et al. 2008. et 83Sumithran P et al. 2011.
Plusieurs évidences ont montré qu’après une perte de poids, des mécanismes compensatoires au niveau des voies de signalisation, impliquées dans la régulation de l’appétit, de l’utilisation et de la mise en réserve de l’énergie, encouragent le regain de poids à moyen et long terme82. Ces mécanismes compensatoires affectent le système
perturbations au niveau des hormones régulatrices de l’appétit et de la balance énergétique.
1.3.3.1 Hormones régulatrices de l’appétit
Dans un contexte de perte de poids, les hormones régulatrices de l’appétit ont un rôle clé dans la reprise de celui-ci. À l’exception de l’augmentation du peptide P (PP), les changements hormonaux favorisent la reprise du poids en augmentant la sensation de faim et en favorisant la mise en réserve de l’énergie83, 87. En effet, ils se traduisent par une augmentation de la ghréline88 et du peptide insulinotrope glucodépendant (GIP)83 ainsi que par une diminution de la leptine83, 89, du peptide YY (PYY)90, de la cholécystokinine (CKK)91, de l’insuline83, 87 et du glugagon-like peptide-1 (GLP-1)92, 93, chez des patients en surpoids ou obèses pour lesquels une perte de poids était induite par une diète entre 6 semaines à 6 mois. Selon les évidences actuelles, ces changements hormonaux semblent même persister jusqu’à un an suivant la diète83, 87, 94. Ainsi, les changements compensatoires des hormones régulatrices de l’appétit ne semblent pas être une réponse transitoire à la perte de poids82. Elles favorisent plutôt un regain de poids à long terme.
Fait intéressant rapporté dans une étude de Crujeiras et collaborateurs, les patients obèses ou en surpoids, qui avaient repris plus de 10% de leur perte de poids initiale, avaient des concentrations beaucoup plus élevées de leptine et plus basses de ghréline, comparativement aux patients ayant maintenu leur poids95. Ces résultats contre-intuitifs suggèrent donc que la reprise de poids est possiblement associée à une réduction de la sensibilité à l’action de ces hormones et donc, par le fait même favorise, voire engendre, le regain de poids.
1.3.3.2 Balance énergétique
La balance énergétique est un concept quantitatif simple qui informe sur l’équilibre entre l’apport et la dépense énergétique et selon le déséquilibre, une perte ou un gain de poids en résulte86, 96. Suivant une perte de poids, des modifications compensatoires de la dépense énergétique tendent à favoriser le regain de poids97 et s’expliquent par une diminution de la dépense énergétique totale selon trois mécanismes84, 97, 98. Premièrement, la perte de masse maigre contribue à réduire la dépense énergétique associée au métabolisme de base84. Deuxièmement,