© Bocar Allaye Diallo, 2019
Fractions chimiques du plomb dans le sol et
phyto-extraction du plomb par le saule (Salix miyabeana)
cultivé dans un sol calcaire riche en éléments traces
métalliques traité avec des amendements acides
Thèse
Bocar Allaye Diallo
Doctorat en sols et environnement
Philosophiæ doctor (Ph. D.)
Fractions chimiques du plomb dans le sol et
phyto-extraction du plomb par le saule (Salix
miyabeana) cultivé dans un sol calcaire riche en
éléments traces métalliques traité avec des
amendements acides
Thèse de doctorat
BOCAR ALLAYE DIALLO
Sous la direction de :
ii
RÉSUMÉ LONG
Les sols pollués aux métaux lourds ou éléments traces métalliques (ÉTM) toxiques constituent un problème environnemental et économique dû de la nécessité de les gérer. Les sites complètement ou partiellement dénudés de végétation durable, abritant des sols pollués dans des environnements venteux et humides comme le Québec, sont particulièrement sujets à l’érosion éolienne et hydrique, d’où le risque accru de l’exposition humaine à des métaux toxiques.
Dans un contexte de développement durable, l'utilisation de plantes accumulatrices de métaux comme le saule (Salix miyabeana) à des fins de réhabilitation de sols riches en ÉTM peut s’avérer un bon choix technologique. D’une façon particulière, par cette présente étude, nous voulons déterminer le prélèvement et la distribution du Pb dans les organes du saule cultivé dans des échantillons de sol calcaire provenant d’un site industriel ainsi que sur le fractionnement du Pb dans les sols cultivés. Ceci, afin de disposer des éléments nécessaires soit à l’abaissement du niveau du Pb du sol notamment par phyto-extraction induite utilisant des amendements à base de soufre élémentaire (S0)
et d’acide sulfurique (H2SO4), soit à la stabilisation durable du Pb dans le sol, notamment
en utilisant le S. miyabeana comme plante accumulatrice de Pb dans ses parties racinaires, pour son éventuelle mise en valeur.
Un essai cultural a été mené en serre pour examiner les effets de l’apport de doses croissantes de S0 combiné à une dose de fumure minérale suivi de l’apport de fortes concentrations de H2SO4 sur les fractions chimiques du Pb dans les sols cultivés ainsi que
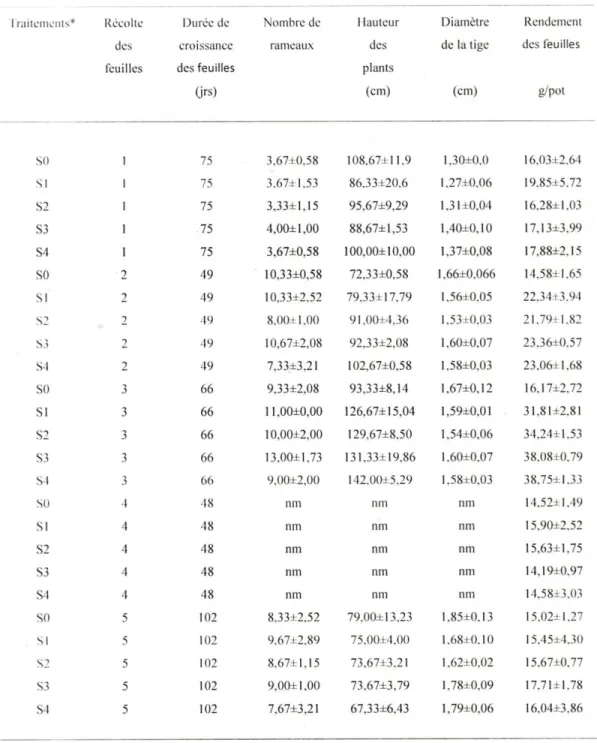
sur les paramètres de croissance de la plante et les prélèvements du Pb et d’autres métaux lourds tels que le cuivre (Cu), le fer (Fe), le manganèse (Mn) et le zinc (Zn) dans les parties du saule (Salix miyabeana) cultivé dans des échantillons de sol (pH 7,55) riche en calcaires actifs et en ÉTM. À cet effet, plusieurs portions (1 kg) d’échantillons de sol ont été mélangées avec cinq doses de S0 puis ont été laissées incuber pendant un mois à l’air libre. Chaque traitement a été répété trois fois. Une bouture (tige) de saule a été plantée dans chaque pot. Les paramètres de croissance et les rendements en matière sèche des
iii
feuilles (Rfeuilles) du saule ont été mesurés après 75 jrs (récolte 1), 124 jrs (récolte 2), 190
jrs (récolte 3), 238 jrs (récolte 4), 340 jrs (récolte 5), 396 jrs (récolte 6) et 472 jours (récolte 7) du début de plantation de la bouture du saule dans les sols. Les tiges et les racines du saule ont été récoltées à la fin de l’essai cultural (472e jour). Ainsi, au total, sept récoltes des parties aériennes vertes (feuilles + brindilles) et une récolte des tiges et des racines (fin de l’essai cultural) ont été réalisées sur une période de 472 jours. Après la 5e et la 6e récolte des feuilles, les sols cultivés ont reçu de fortes doses de solutions de H2SO4. Tous les plants ont reçu une fertilisation minérale complète (N, P, K) avant et
après chaque récolte des feuilles.
D’une manière générale, l’essai cultural comprend deux périodes successives de croissance du saule, la première qualifiée de phyto-stabilisation a duré 340 jours (total de 5 récoltes successives des feuilles) où les sols ont reçu des doses croissantes de S0 commercial [0 (S0); 6,25 g (S1); 12,5 g (S2); 25,0 g (S3); 50,0 g (S4)] avant la plantation des boutures dans les sols, suivie d’une deuxième période qualifiée de phyto-extraction induite, qui a duré 132 jours (total de 2 récoltes) où les sols des traitements S0, S1, S2, S3 et S4 ont reçu respectivement des apports de H2SO4 comme suit: i) ) 0 mM; 16,2 mM;
32,4 mM; 64,8 mM; 129,6 mM avant la 6e récolte des feuilles et ii) 0; 64,2 mM; 128,4 mM; 256,8 mM; 513,6 mM avant la récolte des organes du saule (fin de l’essai). Les doses totales de H2SO4 sont représentées par H0 (total de 0 mM), H1 (total de 80,4 mM),
H2 (total de 160,8 mM), H3 (total de 321,6 mM) et H4 (total de 643,2 mM).
Les résultats obtenus durant la première phase de croissance du saule (premiers 340 jours) ont mis en évidence l’effet hautement bénéfique de l’apport de S0 combiné à la fumure minérale (N, P et K) sur le rendement en matière sèche des feuilles (Rfeuilles) du
saule. D’une manière générale, les valeurs de Rfeuilles ont augmenté graduellement avec
les doses de S0 jusqu’à la 3e récolte des feuilles (g de matière sèche/pot) comme suit: 16,2 (S0) < 31,8 (S1) < 34,2 (S2) < 38,1 (S3), 38,7 (S4). Il existe une très bonne relation linéaire (P<0,001) entre les valeurs de Rfeuilles et les teneurs en S total des feuilles de la 2e
(r= 0,803) et de la 3e récolte (r= 0,874). Durant cette période, les doses de S0 utilisées n’ont pas créé des conditions acides dans le sol, i.e. des valeurs du pH < 6,5. Le saule a
iv
accumulé des concentrations traces de Pb (<1 mg/kg m.s., en deçà de la limite de détection) dans les feuilles pendant plus de 340 jours de croissance.
Les résultats obtenus durant la deuxième phase de croissance du saule (derniers 132 jours) mettent en évidence les effets de l’acidification prononcée (pH 6,5 – 4,5) des échantillons de sols sur l’augmentation significative de la disponibilité du Pb pour la plante ainsi que sur l’inhibition de la croissance des feuilles (7e récolte). Les résultats de l’analyse de variance (à un seul facteur) laissent indiquer un effet adverse de l’ajout de fortes quantités de H2SO4 sur la croissance et le développement des feuilles de la plante.
La plus forte quantité de H2SO4 (513,6 mM) ajoutée au sol ayant reçu le traitement S4 a
causé un effet toxique chez la plante. Les valeurs de Rfeuilles de la 7e récolte des feuilles
(fin de l’essai) ont varié, en moyenne, de 16,1-16,4 g/pot pour les traitements H0, H1 et H2 à : i) 12,1 g/pot pour H3 et ii) à 3,7 g/pot pour H4, démontrant ainsi l’effet délétère de l’acidification prononcée du sol sur la croissance des parties aériennes vertes de la plante. Par ailleurs, les doses cumulatives de H2SO4 (étalées sur 132 jours) a significativement
acidifié les sols (P<0,001) et a considérablement augmenté la concentration du Pb dans les organes de la plante. À la fin de l’essai cultural, les valeurs du pH des sols cultivés ont suivi l’ordre suivant : 6,99 (H0) > 6,56 (H1) > 6,45 (H2) > 5,70 (H3) > 4,1(H4). Les concentrations moyennes du Pb (fin de l’essai) dans les organes de la plante ont varié : i) de < 1 mg/kg (S0 +H0) à 34,3 mg/kg (S4+H4) pour les feuilles, ii) de 7,0 mg/kg (S0 +H0) à 22,4 mg/kg (S4+H4) pour les tiges, et iii) de 64,5 mg/kg (S0+H0) à 383,6 mg/kg (S4+H4) pour les racines, démontrant l’effet de l’acidification prononcé du sol sur l’augmentation des teneurs du Pb dans les feuilles, les tiges et les racines du saule, tout en confirmant le fait que le Pb s’accumule en grande quantité dans les racines de la plante. En outre, les valeurs du pH des sols étaient négativement corrélées (P<0,001) avec les concentrations du Pb dans les feuilles (r= 0,945), les tiges (r= 0,793) et les racines (r= -0,985) du saule.
Les résultats de l’analyse de variance (valeurs de F du modèle d’ANOVA à un seul facteur) ont révélé un effet significatif des doses de H2SO4 ajoutées après la 6e récolte des
v
du Pb ([Pb]ECH) dans les sols cultivés, la dose 513,6 mM ayant généré la quantité de
[Pb]ECH (très facilement labile ou mobile) significativement la plus élevée.
La labilité (extractibilité) du Pb dans les sols cultivés a été évaluée au moyen d’une extraction séquentielle avec trois solutions d’acides inorganiques diluées (0,01N) (HCl, HNO3, H2SO4), deux solutions d’acides organiques diluées (0,01 N) (acide citrique
(C6H8O7) et acide acétique (C2H4O2)) et cinq solutions salines (0,01 N) (BaCl2, CaCl2,
MgCl2, KCl et NaCl). Les quantités totales de Pb extraites (total de huit extractions
successives) ont suivi l’ordre suivant : acides inorganiques (103 – 105 mg/kg) ≥ acides organiques (95 – 102 mg/kg) ˃ sels cationiques (4 – 34 mg/kg), confirmant l’effet marquant des solutions acides sur la mise en solution du Pb. Il existe une relation non linéaire de type polynomial, très hautement significative (P≤0,001), entre les quantités de Pb extraites par les solutions acides et les valeurs du pH des suspensions de sol (sol/solution extractive) de la première extraction (r = -0,827) et de la huitième extraction (r = -0,778). Également, les quantités de Pb extraites par les sels cationiques sont négativement corrélées (P≤0,001) avec les valeurs du pH des suspensions de sol (sol/solution extractive) de la première extraction (r = -0,774) et de la huitième extraction (r = -0,668). L’importance du pH du milieu est mise en évidence dans la désorption du Pb.
Globalement, les résultats de l’essai cultural indiquent qu’une quantité relativement importante d’ÉTM et de Pb présents dans le sol calcaire peut être mobilisée sous des conditions acides. Le pH du sol joue un rôle important dans le prélèvement et l’accumulation du Pb dans les parties du saule. Toutefois, un pH inférieur à 5,5 provoque un effet toxique chez la plante et une baisse considérable des rendements des parties aériennes récoltables. Ceci est à prendre en considération lorsque l’on tente d’abaisser la valeur du pH du sol calcaire riche en ÉTM à une valeur < 6,5, en vue de favoriser le transfert sol-plante du Pb.
vi
RÉSUMÉ COURT
La présence du plomb (Pb) sous forme mobile ou en quantité importante dans les sols est indésirable car le Pb est biologiquement toxique dans l’environnement. La stabilisation ou la réduction de la quantité du Pb total dans les sols calcaires riches en éléments traces métalliques (ÉTM) peuvent être réalisées par les procédés de phyto-stabilisation ou de phyto-extraction induite, respectivement. Un essai cultural a été mené en serre pour examiner l’effet de l’ajout de soufre élémentaire (S0) combiné à la fumure minérale
(N-P-K) suivi de l’ajout de fortes doses d’acide sulfurique (H2SO4) sur les paramètres de
croissance de la plante ainsi que sur les fractions chimiques du Pb dans le sol et l’accumulation du Pb dans les organes du saule (Salix miyabeana) cultivé dans des échantillons d’un sol (pH moyen 7,55) riche en ÉTM, développé sur roche-mère calcaire. Les résultats indiquent qu’en conditions non acides (neutres à alcalins), le saule accumule des concentrations traces de Pb (<1 mg/kg m.s., en deçà de la limite de détection) dans les feuilles. Néanmoins, une proportion du Pb présent dans le sol calcaire peut être mobilisée par les racines de la plante, particulièrement sous des conditions acides. Le Pb s’accumule en plus grande quantité dans les racines que dans les autres parties de la plante et ce, peu importe la nature des traitements du sol. Le pH du sol joue un rôle important dans le prélèvement et l’accumulation du Pb dans les parties du saule. Toutefois, une valeur du pH inférieure à 5,5 a tendance à produire un excès de prélèvement de Pb et provoque une inhibition de la croissance des feuilles ou une baisse considérable des rendements en feuilles. Ceci est à prendre en considération lorsque l’on tente d’abaisser la valeur du pH du sol calcaire riche en ÉTM en dessous de 6,5, en vue de favoriser le transfert sol-plante du Pb.
vii
ABSTRACT
The presence of large amounts or mobile fraction of lead (Pb) in soils is undesirable because Pb is highly toxic even in minor quantity in the environment. The remediation of Pb in calcareous soils with high amount of metallic trace metals (MTE) can be achieved by phytostabilization or induced phytoextraction processes.
For this purpose, a greenhouse study was carried out to determine the effects of elemental sulfur (S0) and mineral fertilizers (N-P-K) followed by the addition of high amounts of sulfuric acid (H2SO4) to cultivated soils on the soil chemical fractions of Pb, growth
parameters and uptake and accumulation of Pb in willow (Salix miyabeana) grown in a calcareous soil (mean pH 7.55) rich in MTE.
The results indicate that in near neutral and weak alkaline conditions, willow accumulates very small amount of Pb (<1 mg / kg d.w, below the detection limit) in the leaves. Nevertheless, some proportion of soil Pb can be mobilized by plant roots, particularly under acidic conditions. Willow accumulates more Pb in the roots than in other plant parts, regardless of the nature of soil treatments. Soil pH plays an important role in the uptake and accumulation of Pb in willow parts.
However, a pH value less than 5.5 tends to produce an excess of Pb removal and causes inhibition of leaf growth or a considerable reduction in leaf yield. This is to be considered when attempting to reduce the pH value of a calcareous soil rich in MTE to less than 6.5, in order to enhance the soil-plant transfer of Pb.
viii
TABLE DES MATIÈRES
RÉSUMÉ LONG ... ii
RÉSUMÉ COURT ... vi
ABSTRACT ... vii
Table des matières ... viii
Liste des tableaux ... xi
Liste des figures ... xii
Liste des abréviations ... xiv
REMERCIÉMENTS ... xvii
INTRODUCTION ... 1
CHAPITRE 1 : REVUE DE LITTÉRATURE ... 5
1.1. Problèmes liés au plomb ... 5
1.1.1. Santé humaine ... 5
1.1.2. Croissance des plantes ... 6
1.2. Le plomb dans les sols ... 7
1.2.1. Formes et espèces de Pb dans les sols ... 8
1.2.2. Contamination des sols au plomb ... 8
1.3. Facteurs affectant la mobilité et la phytodisponibilité du plomb dans les sols ... 11
1.3.1. pH du sol ... 11
1.3.2. Carbonates... 12
1.3.3. Phosphates... 13
1.3.4. Matières organiques ... 15
1.3.5. Oxydes et hydroxydes de fer, de manganèse et d'aluminium ... 15
1.3.6. Minéraux argileux (phyllosilicates) ... 15
1.4. Adsorption ou immobilisation du plomb par les amendements de sols ... 16
1.5. Fractionnement du plomb dans le sol ... 17
1.6. Phytoremédiation des sols pollués aux métaux lourds ... 19
1.6.1. Généralités ... 19
1.6.2. Plantes utilisées en phytostabilisation et phytoextraction des métaux ... 20
1.6.2.1. Généralités ... 20
1.6.2.2. Les saules (Salix spp.) ... 23
1.6.3. Agents chélateurs utilisés en phytoextraction des métaux ... 24
1.6.4. Soufre élémentaire et acide sulfurique pour acidifier les sols calcaires ... 25
1.6.5. Phytoextraction du plomb ... 27
CHAPITRE 2 : HYPOTHÈSES ET OBJECTIFS DE L’ÉTUDE ... 28
2.1. Introduction ... 28
2.2. Hypothèses ... 28
ix
2.3.1. Généralités ... 29
2.3.2. Objectif général ... 30
2.3.3. Objectifs spécifiques ... 30
2.3.4. Utilisation des données de la recherche ... 30
2.3.5. Motivation de la recherche... 31
CHAPITRE 3 : MATÉRIELS ET MÉTHODES ... 32
3.1. Matériels ... 32
3.1.1. Sols ... 32
3.1.2.Engrais minéraux ... 33
3.1.3. Agents acidifiants... 34
3.1.4. Solutions acides et salines d’extraction séquentielle du plomb ... 34
3.1.5. Plante accumulatrice de métaux... 34
3.2. Méthodes d’analyses chimiques des sols ... 35
3.2.1. Caractérisation des échantillons de sols ... 35
3.2.2. Fractions chimiques du Pb dans les échantillons de sols ... 36
3.2.3. Extraction séquentielle du plomb par des solutions acides et salines dans les sols cultivés ... 37
3.3. Essai cultural en serre ... 38
3.3.1. Traitements ... 38
3.3.2. Première période de croissance du saule : Effets des doses de soufre élémentaire sur les valeurs du pH des sols ainsi que sur les paramètres de croissance, le rendement et la concentration de quelques éléments dans les feuilles du saule ... 40
3.3.3. Deuxième période de croissance du saule : Effets des doses d’acide sulfurique sur les valeurs du pH des sols ainsi que sur les paramètres de croissance, le rendement et les concentrations de quelques éléments dans les organes du saule ... 40
3.3.4. Paramètres mesurés ... 41
3.3.4.1. Paramètres de croissance et tissus végétaux ... 41
3.3.4.2. Sols ... 42
CHAPITRE 4 : RÉSULTATS ET DISCUSSION ... 44
4.1. Première période de croissance du saule : Effets des doses de soufre élémentaire sur les valeurs du pH des sols ainsi que sur les paramètres de croissance, le rendement et la concentration de quelques éléments dans les feuilles du saule ... 44
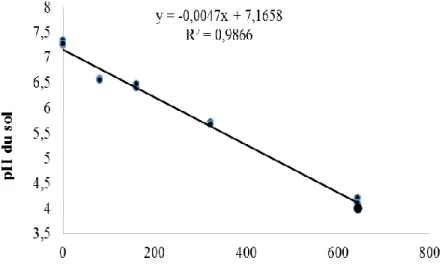
4.1.1. Variation du pH des échantillons de sol ... 44
4.1.2. Paramètres de croissance du saule ... 49
4.1.3. Teneurs en soufre et croissance des feuilles du saule ... 54 4.1.4. Concentrations de six éléments majeurs (carbone, azote, phosphore, potassium, calcium, magnésium) dans les feuilles du saule (5 récoltes successives)63
x
4.1.5. Concentrations de quatre oligo-éléments (cuivre, fer, manganèse, zinc) dans
les feuilles du saule (5 récoltes successives)... 68
4.1.6. Concentrations du plomb dans les feuilles du saule (5 récoltes successives) . 71 4.1.7 Conclusion de section ... 72
4.2. Deuxième période de croissance du saule : Effets des doses d’acide sulfurique sur les valeurs du pH des sols ainsi que sur les paramètres de croissance, le rendement et les concentrations de quelques éléments dans les organes du saule ... 73
4.2.1. Variation du pH des échantillons de sol ... 74
4.2.2. Paramètres de croissance du saule ... 75
4.2.3. Concentrations du soufre dans les organes de la plante (6e et 7e récoltes) ... 80
4.2.4. Concentrations de six éléments majeurs (carbone, azote, phosphore, potassium, calcium, magnésium) dans les organes de la plante (6e et 7e récoltes) ... 84
4.2.5 Concentrations de quatre éléments traces métalliques (Fe, Cu, Mn, Zn) dans les parties de la plante (6e et 7e récolte) ... 87
4.2.5.1. Cuivre ... 87
4.2.5.2. Fer ... 88
4.2.5.3. Manganèse ... 89
4.2.5.4. Zinc ... 90
4.2.5.5. Considérations générales ... 91
4.2.6. Concentrations du plomb dans les organes du saule (6e et 7e récolte) ... 93
4.2.6.1. Concentrations et prélèvements du Pb par les organes du saule ... 93
4.2.6.2. Prélèvements du plomb par les organes du saule ... 100
4.2.6.3. Fractions chimiques du plomb dans les sols cultivés... 103
4.2.6.3.1. Méthode de Sidhu et al. (1977) ... 103
4.2.6.3.2. Méthode de Tessier et al. (1979) ... 106
4.2.6.4. Labilité (extractibilité) du plomb des sols cultivés ... 109
4.3. Discussion générale ... 113
CONCLUSION GÉNÉRALE ... 118
RÉFÉRENCES ... 121
xi
LISTE DES TABLEAUX
Tableau 1.1 : Grille des critères génériques pour les sols (mg/kg de matière sèche)
(MDDELCC-Québec, 2001). ... 10
Tableau 3.1: Identification des traitements relatifs à l’utilisation de doses de soufre élémentaire suivi de doses d’acide sulfurique et des récoltes des feuilles de saule. ... 39
Tableau 4.1: Paramètres de croissance du saule cultivé en serre dans un sol calcaire riche en certains ÉTM ayant reçu des doses de S0 et une dose d’engrais minéraux (N-P-K). .. 51
Tableau 4.2: Concentrations du soufre (S) (% m.s.) dans les feuilles du saule. ... 55
Tableau 4.3: Résultats de l’analyse de variance des effets des doses croissantes de S0 et du nombre de récoltes sur les teneurs en carbone (C), azote (N), phosphore (P), potassium (K), calcium (Ca) et magnésium (Mg) des feuilles du saule. ... 67
Tableau 4.4: Concentrations (mg/kg) de quatre éléments traces métalliques dans les parties aériennes vertes du saule (cinq récoltes successives). ... 68
Tableau 4.5: Paramètres de croissance du saule cultivé en serre dans un sol calcaire riche en ÉTM ayant reçu des doses de H2SO4 (H1 à H4) après la 5e récolte des feuilles. ... 76
Tableau 4.6: Concentrations du soufre (S) dans les organes du saule à la 7e récolte des feuilles. ... 81
Tableau 4.7 : Concentrations du plomb dans les organes du saule. ... 93
LISTE DES TABLEAUX DES ANNEXES Tableau 1A. Concentration du C dans les organes du saule. ... 153
Tableau 2A. Concentration du N dans les organes du saule. ... 153
Tableau 3A. Concentration du P dans les organes du saule. ... 154
Tableau 4A. Concentration du Ca dans les organes du saule. ... 154
Tableau 5A. Concentration du K dans les organes du saule. ... 155
Tableau 6A. Concentration du Mg dans les organes du saule. ... 155
Tableau 7A. Concentration du Cu dans les organes du saule. ... 156
Tableau 8A. Concentration du Fe dans les organes du saule... 156
Tableau 9A. Concentration du Mn dans les organes du saule. ... 157
Tableau 10A. Concentration du Zn dans les organes du saule. ... 157
xii
LISTE DES FIGURES
Figure 1.1 : Pollution anthropique de l’environnement au plomb. ... 10 Figure 3.1: Tamisage du sol contaminé renfermant de roches et de cailloux. ... 32 Figure 3.2 : Fractions granulométriques des sols prélevés sur le terrain du site contaminé.
... 33
Figure 3.3: Réaction de l’acide acétique (1 N) avec les carbonates actifs du sol. ... 33 Figure 3.4: Boutures de saule avant leur plantation dans les sols. ... 34 Figure 4.1: Valeurs du pH des sols cultivés à deux temps de croissance du saule (1ère et
5e récolte des feuilles), en fonction de doses de S0 (pH1 et pH5). ... 44
Figure 4.2: Évolution de la croissance du saule cultivé en fonction des doses de S0 seules (S0 à S4) entre le 20 juin 2017 et le 16 avril 2018. ... 50
Figure 4.3: Valeurs moyennes du rapport N/S (5 coupes) des feuilles du saule, en
fonction de 5 doses de S0 (g/kg) ajoutées aux sols : S0 (0); S2 (6,15); S3 (12,5); S4 (50,0). ... 65
Figure 4.4: Concentrations moyennes (5 coupes) de quatre éléments traces métalliques
dans les feuilles du saule, en fonction de 5 doses de S0 (g/kg) ajoutées aux sols : S0 (0); S2 (6,15); S3 (12,5); S4 (50,0). ... 70
Figure 4.5: Valeurs moyennes du pH (à la 7e récolte) des sols ayant reçu un total de 0 mM; 80,4 mM; 160,8 mM; 321,6 mM; et 643,2 mM de H2SO4, respectivement, durant
132 jours de croissance du saule. ... 74
Figure 4.6: Valeurs moyennes du rendement en matière sèche des parties aériennes à la
6e récolte, en fonction de doses croissantes de H
2SO4 (H0 à H4) ajoutées aux sols cultivés
(S0 à S4) avant la 6e récolte des feuilles. H0, H1, H2, H3, H4 = 0 mM; 16,2 mM; 32,4 mM; 64,8 mM; 129,6 mM H2SO4, respectivement. ... 77
Figure 4.7 : Valeurs moyennes des paramètres de croissance du saule à la 7e récolte, en
fonction de doses croissantes de H2SO4 (H0 à H4) ajoutées aux sols cultivés (S0 à S4)
avant la 7e récolte des feuilles. H0, H1, H2, H3, H4 =0 mM; 64,2 mM; 128,4 mM; 256,8 mM; 513,6 mM H2SO4, respectivement. ... 77
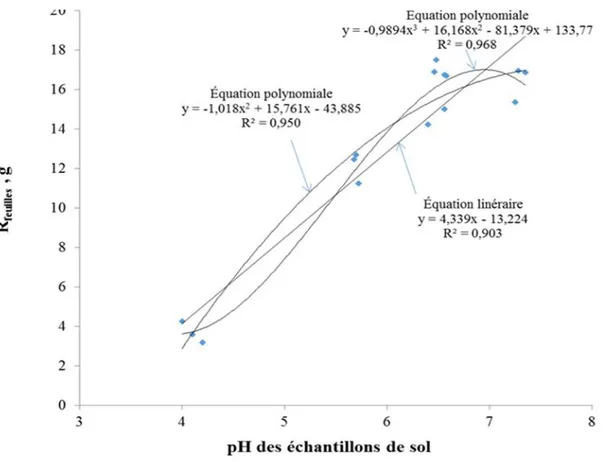
Figure 4.8: Effet du pH des sols cultivés ayant reçu des doses de H2SO4 sur le rendement
en matière sèche des parties aériennes vertes (Rfeuilles) de la 7e récolte des feuilles. ... 79
Figure 4.9: Effet des doses de H2SO4 sur les teneurs en S des feuilles et des racines du
saule (fin de l’essai cultural). ... 83
Figure 4.10: Teneurs moyennes du Cu dans les parties du saule (7e récolte), en fonction de doses de H2SO4 (H0 à H4) ajoutées aux sols initialement fertilisés avec du S0 (S0 à
S4) après la 6e récolte des feuilles. H0, H1, H2, H3, H4 =0 mM; 64,2 mM; 128,4 mM;
256,8 mM; 513,6 mM H2SO4, respectivement. ... 88
Figure 4.11: Teneurs moyennes du Fe dans les parties du saule (7e récolte), en fonction de doses de H2SO4 (H0 à H4) ajoutées aux sols initialement fertilisés avec du S0 (S0 à
S4) après la 6e récolte des feuilles. H0, H1, H2, H3, H4 =0 mM; 64,2 mM; 128,4 mM;
256,8 mM; 513,6 mM H2SO4, respectivement. ... 89
Figure 4.12: Teneurs moyennes du Mn dans les parties du saule (7e récolte), en fonction de doses croissantes de H2SO4 (H0 à H4) ajoutées aux sols initialement fertilisés avec du
S0 (S0 à S4) après la 6e récolte des feuilles. H0, H1, H2, H3, H4 =0 mM; 64,2 mM; 128,4 mM; 256,8 mM; 513,6 mM H2SO4, respectivement. ... 90
xiii
Figure 4.13: Teneurs moyennes du Zn dans les parties du saule (7e récolte), en fonction
de doses de H2SO4 (H0 à H4) ajoutées aux sols initialement fertilisés avec du S0 (S0 à
S4) après la 6e récolte. H0, H1, H2, H3, H4 =0 mM; 64,2 mM; 128,4 mM; 256,8 mM; 513,6 mM H2SO4, respectivement ... 91
Figure 4.14: Teneurs moyennes du Pb dans les feuilles de la plante (6e récolte), en fonction de doses de H2SO4 (H0 à H4) ajoutées aux sols initialement fertilisés avec du S0
(S0 à S4) après la 6e récolte. H0, H1, H2, H3, H4 =0 mM; 16,2 mM; 32,4 mM; 64,8 mM; 129,6 mM H2SO4, respectivement. ... 94
Figure 4.15: Teneurs moyennes du Pb dans les organes du saule (7e récolte), en fonction de doses de H2SO4 (H0 à H4) ajoutées aux sols initialement fertilisés avec du S0 (S0 à
S4) après la 6e récolte. H0, H1, H2, H3, H4 =0 mM; 16,2 mM; 32,4 mM; 64,8 mM; 129,6
mM H2SO4, respectivement ... 95
Figure 4.16 : : Proportion du Pb dans les organes du saule à la 7e récolte des feuilles. Les sols ont reçu les doses les plus élevées en S0 (50 g avant la culture du saule) et en H2SO4
(ajout de 129,6 mM avant la 6e coupe et de 513,6 mM avant la 7e coupe).. ... 96
Figure 4.17: Concentrations moyennes du Pb dans les parties du saule à la 7e récolte, en fonction de doses de H2SO4 (total de 0 mM; 80,4 mM; 160,8 mM; 321,6 mM; et 643,2
mM) ajoutées aux sols pendant 132 jours. ... 98
Figure 4.18: Teneurs moyennes du Pb dans les parties du saule, en fonction du pH des
sols ayant reçus des doses de H2SO4 (total de 0 mM; 80,4 mM; 160,8 mM; 321,6 mM; et
643,2 mM) ajoutées aux sols pendant 132 jours. ... 99
Figure 4.19: Teneurs moyennes des formes labiles et peu labiles du Pb (méthode de
Sidhu et al. 1977) dans les sols cultivés après la 7e récolte du saule. S0= 0; 6,25 g; 12,50 g; 25,00 g; 50,00 g S0, respectivement. H0, H1, H2, H3, H4 =0 mM; 64,2 mM; 128,4 mM; 256,8 mM; 513,6 mM H2SO4, respectivement. ... 104
Figure 4.20: Teneurs moyennes du Pb sous formes soluble+échangeable (ECH) et
associés aux phases carbonates (CAR), oxydes (OX) et organiques (MO) (méthode de Tessier et al., 1979) dans les sols cultivés après la 7e récolte du saule. S0, S1, S2, S3 et S4
= 0; 6,25 g; 12,50 g; 25,00 g; 50,00 g S0, respectivement. H0, H1, H2, H3, H4 = 0 mM; 64,2 mM; 128,4 mM; 256,8 mM; 513,6 mM H2SO4, respectivement... 107
Figure 4.21: Quantités totales de Pb extraites des sols cultivés (7e récolte du saule) par dix solutions (0,01N) d’acides inorganiques et organiques et des sels cationiques. ... 110
Figure 4.22: Relation entre les quantités de Pb extraites par les cinq solutions d’acides
inorganiques et les valeurs du pH des suspensions de sol (sol/solution extractive) après la 1ère extraction (A) et la 8e extraction (B). ... 111
Figure 4.23: Relation entre les quantités de Pb extraites par les solutions salines et les
valeurs du pH des suspensions de sol (sol/solution extractive) après la 1ère extraction (A) et la 8e extraction (B). ... 112
xiv
LISTE DES ABRÉVIATIONS
ATP : Adénosine triphosphate Ba : Baryum
BPCs : biphényles polychlorés C : Carbone
Ca : Calcium
CaCO3 : Carbonate de calcium
CAR : Phase des carbonates dans le sol
CCME : Conseil canadien des ministres de l’environnement Cd : Cadmium
CEC : Capacité d’échange cationique Co : Cobalt
Cs : Césium Cu : Cuivre
DTPA : Acide éthylène-triamine-penta-acétique ECC : Équivalant en carbonate de calcium ECH : Fraction échangeable du Pb dans le sol EDTA : Acide éthylène-diamine-tétra-acétique ÉTM : Éléments traces métalliques
F : Test de F de l’analyse de variance (ANOVA)
FBA : Facteur de bioaccumulation Fe : Fer
H0 à H4 : traitements des sols cultivés après la 5e récolte des feuilles du saule, avec de H 2SO4
ha : Hectare
HA : Hydroxyapatite
HEDTA : Acide N-hydroxyéthyl éthylène-diamine-triacétique HOAc : Acide acétique
HCl : Acide chlorhydrique HNO3 : acide nitrique
H2SO4 : Acide sulfurique
jrs : jours K : Potassium kg : kilogramme
ksp : constante du produit de solubilité M : Molaire
m : Mètre
m.s. : Matière sèche
MDDELCC : Ministère du développement durable, de l'environnement et de la lutte contre les changements climatiques mé : Milliéquivalent Mg : Magnésium mg : milligramme min : Minute mL : Millilitre mm : Millimètre mM : Millimolaire Mn : Manganèse
MO : Matière organique du sol MTE : Metallic trace element
xv
N : Azote Na : Sodium
NH4OAc : Acétate d’ammonium
Ni : Nickel
Ox : Phase des oxydes dans le sol P : Phosphore
Pb : Plomb
ppm : Partie par million
R : Rendement en matière sèche de la plante Rs : ([Pb]DTPA+ HCl) / ([Pb]CaNO3+MgNO3)
S : Soufre
S0 :Soufre élémentaire
S0 à S4 : traitements des échantillons de sols avec du S0
sem : Semaine t : Temps t° : Température TEA : Triétanolamine
trm : Nombre de tours par minute V : Volume
Zn : Zinc
xvi
xvii
REMERCIEMENTS
Nous rendons tout d’abord grâce à ALLAH, le Tout Puissant pour tous ses bienfaits innombrables dont Il nous a comblés.
Au terme de ce travail d’étude, de recherche et d’encadrement tant exigeant en temps, en pensée et en disponibilité j’adresse mes remerciements infinis et profonds à mon directeur de thèse Pr Antoine Karam. Sans cesse et sans lasse, Pr Karam m’a conduit à l’étape finale de ma thèse.
Je remercie toute l’équipe de recherche du Pr Karam (Équipe de Recherche en Sols Agricoles et Miniers) en les personnes de : Claver Nguema Ondo, Papa Malik Sall, Fatou Youssouf Koné, Korotoumou Dissa et Anta Barry, sans oublier Cedrick, Monique Goulet, Nadine Lemay et Daniel Marcotte du département des sols et de génie agroalimentaire.
Je remercie le projet Formation Agricole pour la Sécurité Alimentaire au Mali (FASAM), organe de financement de mes études et de mon séjour au Canada. Mes remerciements au directeur du projet FASAM en la personne de M. Daniel Campeau et tout le personnel de FASAM.
Mes remerciements s’adressent à tout le corps professoral du département des sols et de génie agroalimentaire, aux employés et aux étudiants inscrits aux cycles supérieurs particulièrement ceux ou celles qui sont passé(e)s par le local 2224 et le local 2227. Je remercie la direction et tout le personnel de mon établissement d’origine IPR/IFRA de Katibougou particulièrement son Excellence Monsieur le Ministre Mahamadou Famanta, le DG Pr Soumano, les professeurs Issa Dembélé, Feu Drissa Diallo, Sidiki Gabriel Dembélé et Amoro Coulibaly.
Mes remerciements sincères à l’adresse de ma famille : mes épouses, mes enfants, mes petits-enfants, mes belles familles, mes frères et sœurs et tous mes amis. Que tous et toutes sachent que leurs patience, endurance, soutien et conseil ont porté fruit et je leurs en suis reconnaissant.
A toutes les personnes physiques ou morales qui se sont évertuées à me porter un soutien moral, matériel, financier ou technique pendant ma formation, je tiens à exprimer mes sincères remerciements.
1
INTRODUCTION
Le sol est une ressource non renouvelable, il relie de nombreuses activités anthropiques avec ceux de l'environnement en agissant comme une plate-forme.
La contamination de l'environnement par les métaux toxiques et les polluants organiques (Vassil et al., 1998) suscite une inquiétude primordiale dans le monde entier, car elle a conduit le sixième (1/6) des terres arables du monde à être impropres à l'agriculture (Hakeem et al., 2014). Représentant 37,3% de l’ensemble des polluants, les métaux lourds posent les plus grands risques de dommages à la vie (Morel, 2012).
Les sols pollués aux métaux lourds ou éléments traces métalliques (ÉTM) toxiques constituent un problème environnemental et économique dû à la nécessité de les gérer. Ces sols peuvent nécessiter différentes procédures de réhabilitation, afin de ramener le sol à un état relativement proche de son état naturel ou à un niveau de contamination acceptable conformément à la législation ou aux lois gouvernementales sur la protection des sols et la réhabilitation des terrains contaminés. Les sites abandonnés complètement ou partiellement dénudées de végétation, abritant les sols pollués dans des environnements venteux et humides comme le Québec, sont particulièrement sujets à l’érosion éolienne et hydrique d’où le risque accru de l’exposition humaine à des métaux toxiques. « En vivant dans un environnement fortement pollué, les gens sont continuellement exposés à de nombreux agents dont la plupart sont cancérigènes et/ou perturbent les hormones et, dans tous les cas, peuvent gêner le fonctionnement correct des cellules et des organes » Schill et al., 2008). Dans ce contexte, la phyto-stabilisation, i.e. l'utilisation de plantes pour la stabilisation in
situ de métaux lourds toxiques tels le plomb (Pb) dans le sol, est une solution écologique
envisageable.
Dans un contexte de développement durable, la valorisation des sols contaminés par les ÉTM à des fins de production de biomasse verte connaît actuellement un net intérêt résultant du renforcement de la législation environnementale qui se traduit par une
2
augmentation considérable des contraintes et des frais de mise en décharge des sols contaminés. Par ailleurs, la communauté internationale soucieuse de la préservation de la qualité de la planète Terre propose « des lois contraignantes pour limiter le réchauffement planétaire à 1,5 degrés » (Le Journal de Québec, 28 septembre 2019). C’est pourquoi la valorisation des sols contaminés par les ÉTM à des fins de production de biomasse verte et d’arbres susceptibles de restreindre la production de gaz à effet de serre, notamment en absorbant le CO2 atmosphérique, représente une solution particulièrement intéressante. En
effet, d’un point de vue technique et économique, la transplantation de ligneux comme le saule dans les sols contaminés par ÉTM ne présente qu’un faible surcoût et offre en outre un intérêt environnemental. Cependant, l’implantation des saules ne doit en aucun cas déprécier le capital foncier, ni constituer une source de pollution génératrice de risques pour l’homme et son environnement.
Dans la présente étude, le sol, qui provient d’un vaste terrain en zone industrielle, affiche une contamination pluri-métallique légère à modérée pour le zinc (Zn) et le cuivre (Cu) et et une contamination élevée en plomb (Pb) et en manganèse (Mn). La présence du Pb en forte quantité dans ce sol pourrait poser un problème s’il est libéré dans l’environnement, car le Pb est classé parmi les métaux potentiellement toxiques pour la santé humaine (Amaya et al., 2010). Bien que le Pb soit moins mobile dans les sols riches en matériaux adsorbants (e.g. argiles, carbonates), sa présence pourrait constituer un problème à long terme si les conditions édaphiques et climatiques permettent la dissolution des carbonates et la libération du Pb.
Compte tenu d’une part, que les plantes peuvent séquestrer les ÉTM du sol dans leurs parties aériennes et d’autre part, que les carbonates actifs (calcaires) peuvent stabiliser les métaux (sous formes non échangeables) dans les sols, il s’ensuit que les techniques de phyto-extraction et de phyto-stabilisation peuvent se révéler utiles soit dans la diminution des teneurs ÉTM dans les sols (phyto-extraction) soit dans la stabilisation des ÉTM dans les sols calcaires (phyto-stabilisation), tout en préservant l’environnement (Hakeem et al., 2014; Karam et al., 2015; Kirpichtchikova, 2009). Toutefois, l’efficacité de la phyto-extraction est fonction entre autres de la phyto-disponibilité du métal dans le sol, i.e., sa
3
mise en solution sous forme soluble pour son absorption par la plante (Lasat, 2002). Ainsi, les processus ou facteurs qui influent sur la disponibilité ou "labilité" des métaux à des fins d’absorption et de translocation doivent être priorisés (Waoo et al., 2011; Arunakumara et al., 2015). En règle générale, la phyto-disponibilité des métaux lourds ainsi que leur mobilité augmente à mesure que le pH du sol diminue (Kabata-Pendias, 2011).
Or, le sol industriel mis à l’étude est alcalin et contient des carbonates actifs car il a été développé sur roche-mère calcaire. Il est connu que la présence de carbonates dans les sols contribue à augmenter leur pH et à adsorber ou à précipiter les métaux lourds (Kabata-Pendias, 2011) et par conséquent à les stabiliser dans le sol (Karam et al., 2015). Dans ce contexte, la phyto-extraction assistée par de l’acide sulfurique (H2SO4) dissolvant les
composés de Pb solides présents dans le sol calcaire durant la croissance végétale peut s’avérer une bonne option pour favoriser la libération d’une quantité importante de Pb et de son absorption par la plante. Dans le cadre d’essais préliminaires menés sur ce sol, Karam et al. (2016b, 2017a,b) ont trouvé que le H2SO4 résultant de l'oxydation du soufre
élémentaire (S0) ajouté au sol avant le semis ainsi que celui ajouté fraîchement au sol avant la récolte des plantes tendaient à acidifier légèrement le sol calcaire, et par conséquent à favoriser la dissolution/désorption/extraction d’une partie du Pb total du sol sous forme assimilable pour la plante (Diallo et al., 2016).
À notre connaissance, relativement peu de travaux spécifiques ont été consacrés à l’étude de la fertilisation soufrée en combinaison avec des engrais à base d’azote (N), de phosphore (P) et de potassium (K) sur la croissance du saule (Salix miyabeana) et de la capacité de celle-ci à stabiliser ou à accumuler dans ses parties aériennes le Pb présent dans les sols développés sur roche-mère calcaire. En outre, on connaît peu l’efficacité de la phyto-extraction induite utilisant de fortes quantités de H2SO4 à abaisser le niveau de
contamination de Pb ainsi que le fractionnement du Pb dans les sols calcaires pollués après leur mise en végétation.
Le principal avantage de la culture de saules concerne le caractère durable de leur exploitation du point de vue de l’environnement. Grâce à leur fort enracinement, ils
4
conviennent bien pour stabiliser les sites dégradés contre l’érosion éolienne (Guittonny-Larchevêque et Lortie, 2017). Le saule a déjà été utilisé dans des essais de mise en végétation de sols perturbés dans certains lieux nordiques du Canada (http://www.rpic-ibic.ca/documents/2012_fcs_presentations/Zeeb_F.pdf), de phytoremédiation de sédiments (Vervaeke et al., 2003, 2004) et de sols contaminés (Licinio, 2017), ainsi que dans des études d’évaluation de l'influence des facteurs pédoclimatiques et nutritifs régissant la production de biomasse épigée de Salix miyabeana SX67 dans des sites dispersés au sein du Québec méridional (Fontana, 2016).
Finalement, par cette présente étude, nous voulons déterminer le fractionnement du Pb dans un sol calcaire pollué aux ÉTM provenant d’un site industriel situé à Sainte-Croix dans le comté de Lotbinière (Québec, Canada). Ceci, afin de disposer des éléments nécessaires à : i) l’abaissement du niveau de contamination du sol notamment par phyto-extraction induite utilisant des amendements à base de S0 et de H2SO4, ou ii) à la
phyto-stabilisation durable du Pb dans le sol, en utilisant le S. miyabeana comme plante accumulatrice des ÉTM dans ses racines, pour son éventuelle mise en valeur.
5
CHAPITRE 1 : REVUE DE LITTÉRATURE
1.1. Problèmes liés au plomb
Le Pb constitue un problème environnemental préoccupant car il est dangereux pour l'homme et les animaux qui l’ingèrent à partir de trois sources : la chaîne alimentaire, l’inhalation de poussières et la géophagie (Kabata-Pendias, 2011). Dans le passé, l’utilisation intensive et non contrôlée du Pb ont provoqué son accumulation dans tous les compartiments des écosystèmes (Belatik, 2014).
Le Pb est un métal non essentiel, par conséquent, même la plus petite concentration peut avoir des effets létaux. Les effets toxiques du Pb sont liés à sa capacité à réagir avec d'autres groupes fonctionnels tels que des groupes carboxyle, amine et sulfhydrile, ce qui entraîne une perte des activités cellulaires (Hakeem et al., 2014).
1.1.1. Santé humaine
Le Pb est un métal non essentiel, par conséquent, même la plus petite concentration peut avoir des effets létaux (Hakeem et al., 2014). Le saturnisme est la maladie liée à une intoxication au Pb à la suite d’une exposition intense ou prolongée.
Le Pb, qui est non biodégradable, a une demi vie de 20 ans, ce qui lui permet de s’accumuler jusqu’à 73-95% dans les os (Robidas, 2011). Cause d’anémie, le Pb a une toxicité hématologique (Mench et Baize, 2004). Dans un récent reportage portant sur la présence du Pb dans les eaux des écoles du Québec paru dans le média écrit Le Soleil (7 octobre 2019), Ricard-Châtelain écrit «Le plomb, est jugé particulièrement néfaste pour les plus jeunes, du fœtus à l’école primaire, vers 6 à 8 ans». «Le plomb est reconnu comme un neurotoxique capable d’affecter le développement de l’enfant, tout ce qui est capacité d’apprentissage, etc.».
6 1.1.2. Croissance des plantes
Si certains éléments métalliques présents à l’état de traces (Mn, Zn, Cu, Ni, Co) dans la majorité des sols agricoles sont essentiels pour la plante, d’autres tels le Pb et le Cd n’ont pas d’activités physiologiques reconnues (Lasat, 2002) et peuvent devenir toxiques. L’exsudation des racines permet de mobiliser les métaux lourds adsorbés à la surface des particules d’argile ou de la matière organique (Gagné, 2000). L'absorption du Pb par les racines varie de façon significative selon sa concentration et sa forme dans le sol. Seulement environ 0,005 à 0,13% de Pb dans la solution du sol est disponible pour les plantes (Kabata-Pendias, 2011).
La toxicité du Pb à l’égard des plantes a rarement été observée dans les conditions de terrain (Kabata-Pendias, 2011). Une forte concentration en plomb peut aboutir à une ankylose qui est une diminution de la mobilité conduisant à des plantes naines (Pelikan et Lescourret, 2008).
Lorsque le Pb est présent sous formes solubles, les racines des plantes sont en mesure de prélever une quantité importante. Le transfert du Pb des racines vers les parties aériennes est fortement limité pour la plupart des cultures car seulement 3% du Pb dans les racines est transporté aux parties aériennes (Kabata-Pendias, 2011). L'antagonisme Zn-Pb affecte négativement la translocation de chaque élément des racines aux sommets. L'interférence du Pb avec Ca est d'une importance métabolique car le Pb peut imiter le comportement physiologique du Ca, inhibant ainsi certains enzymes mais le chaulage agit favorablement à la réduction de l'absorption du Pb par les racines (Kabata-Pendias, 2011).
Une accumulation excessive de Pb dans les cellules végétales altère de nombreuses fonctions morphologiques, physiologiques et biochimiques des plantes, soit directement soit indirectement, induisant ainsi des effets délétères (Pourrut et al., 2011). Entre autres, un excès de Pb dans les tissus végétaux induit le ralentissement de la division des cellules et de la photosynthèse; la diminution de la teneur en chlorophylle; l’inhibition de la production d’ATP et l’altération du statut hormonal provoque un déséquilibre entre les
7
éléments nutritifs ; et finalement affecte la structure et la perméabilité de la membrane cellulaire (Eun, Youn et Lee, 2000; Sharma et Dubey, 2005; Pourrut et al., 2011)
Le Pb peut affecter négativement la croissance de la plante notamment en induisant un stress hydrique entrainant la fermeture des stomates (Cecchi, 2008). Parmi les symptômes visibles, le Pb induit une inhibition de la croissance des différentes parties de la plante, ce qui diminue le rendement et la production de biomasse aérienne et une chlorose, et un noircissement du système racinaire (Pourrut et al., 2011). Une étude rapportée par Kabata-Pendias (2011) sur l’absorption du Pb par le riz cultivé sur un sol contenant 1000 mg Pb/kg indique une réduction du rendement de riz de 11,5%.
Des études ont montré que les feuilles de laitue peuvent emmagasiner sept fois plus de plomb que les racines des carottes (Phaneuf et al., 2012).
L’effet le plus habituel d’une toxicité au Pb consiste en une réduction de la croissance des différentes parties de la plante. Selon l’importance du stress, les feuilles peuvent présenter une chlorose due à la fois à une perte de chlorophylle, à une relative augmentation des caroténoïdes et à une déficience en fer (Romanowska et al., 2002). Dans les cas les plus sévères, une apparition de tâches nécrotiques est observée (Fodor, 2002).
Ces effets apparents résultent en fait d’une altération de processus vitaux tels que le transport et le métabolisme. Ainsi, une diminution de la conductivité hydraulique racinaire associée à la fermeture des stomates entraîne une baisse du CO2 foliaire et une réduction de
la transpiration (Poschenrieder et al., 1989; Barceló et Poschenrieder, 1990; Haag-Kerwer et al., 1999), il en résulte une réduction de l’apport ou l’approvisionnement en éléments nutritifs majeurs dont les nitrates et, de ce fait, une perturbation du métabolisme azoté des feuilles (Gouia et al., 2000; Klobus et al., 2002).
8 1.2.1. Formes et espèces de Pb dans les sols
La teneur moyenne en Pb de la croûte terrestre est estimée à environ 15 mg/kg, avec des différences importantes selon l’origine des sols (Kabata-Pendias, 2011). Dans la nature, on distingue deux types de Pb : le Pb primaire et le Pb secondaire. Le Pb primaire est d'origine géogénique et a été incorporé dans les minéraux au moment de leur formation (Pauget, 2015) tandis que le Pb secondaire est issu de la désintégration de l'uranium et du thorium (Consoglobe, 2016).
Le Pb est présent dans l'environnement à des degrés d'oxydation (0) métal, (+II) et (+IV) mais sa forme plus dominante dans la nature est le Pb2+ (Belatik, 2014).
Les formes minérales de Pb (e.g. PbS, PbO, PbSO4, PbO•PbSO4) constituent les principaux
polluants du sol et le Pb d’auparavant échappé des automobiles est principalement sous la forme de sels halogénures (PbBr, PbBrCl, Pb(OH)Br et (PbO)2PbBr) (Kabata-Pendias,
2011). En solution, le Pb peut se présenter sous différentes formes cationiques selon le pH et la nature et la concentration des ions présents dans la solution du sol : Pb2+, PbCl+, PbOH+ et espèces anioniques : PbCl3- et Pb(CO3)22- (Beausoleil et Price, 2010).
1.2.2. Contamination des sols au plomb
Bien que le Pb dans l'essence soient interdits dans la plupart des pays, l'augmentation des niveaux de Pb dans le sol le long de la route à fort trafic peut atteindre jusqu'à 7000 mg/kg (Kabata-Pendias, 2011). Il y a environ 20 ans, 30 % de l’apport alimentaire humaine en plomb provenait de la consommation de céréales, de fruits et de légumes, alors que plus de 60 % de cet apport provenait de boissons et de jus de fruits entreposés dans des boîtes de conserve soudées au plomb (Phaneuf et al., 2012).
La pollution anthropique des sols au Pb a reçu beaucoup d'attention (Figure 1.1). La contamination des milieux terrestre et aquatique par le Pb peut se produire de nombreuses manières (Santé Canada, 2013):
9
i) Érosion des roches et des sols contenant du Pb et dispersion du Pb dans le profil de sol (Smith et al., 2009). Dépôt du Pb issu de l'atmosphère (Stafilov et al., 2010). Dans l'atmosphère, le plomb se trouve à l'état de particules sous forme de composés de type oxydes, sulfures, sulfates, ces particules vont évoluer chimiquement (oxydation, dissolution) une fois déposées sur le sol, elles vont se dissoudre à l'état de cation métallique Pb2+ ou bien réagir avec les composés du sol sous forme solide (Sobanska, 1999).
ii) Élimination de produits à base de plomb comme les cartouches et la grenaille de plomb (Chrastný, Komárek et Hájek, 2010). Traditionnellement 90% des balles de tirs sont constitués de plomb (Sorvari, 2011). Les projectiles militaires ont jusqu’à présent un noyau en plomb et une chemise en cuivre (Santé Canada, 2013).
iii) Utilisation, élimination ou incinération de produits contenant du plomb comme les batteries, les accumulateurs au plomb, les appareils électroniques, les plombs de pêche et turluttes en plomb, les masses d'équilibrage en plomb et les revêtements de plomb dans l'industrie du bâtiment (Santé Canada, 2013).
iv) Utilisation de munitions au plomb dans les champs de tir à des fins de formation militaire (Santé Canada, 2013).
v) Utilisation de l’essence, de pesticides, de peintures ou de boues de station d’épuration contenant du Pb (CCME, 1999; Pereira et Sonnet, 2007; Santé Canada, 2013). Les peintures constituent une source importante de contamination des sols urbains au voisinage des maisons.
vi) Utilisation d’engrais chimiques pouvant contenir du Pb comme impuretés (Pereira et Sonnet, 2007).
vii) Déversement d’effluents industriels dans l'eau et les sédiments (Besser et al., 2009) ou les dépôts de Pb issus des fonderies (Brugger et Tassé, 2010).
10
Figure 1.1 : Pollution anthropique de l’environnement au plomb.
Le Ministère du développement durable de l'environnement et de la lutte contre les changements climatiques (MDDELCC-Québec, 2001), dans sa politique de protection des sols et de réhabilitation des terrains contaminés prévoie trois critères pour les contaminants comme l’indique le Tableau 1.1.
Tableau 1.1 : Grille des critères génériques pour les sols (mg/kg de matière sèche)
(MDDELCC-Québec, 2001).
N.B: A : Teneurs de fond pour les paramètres inorganiques et limite de quantification pour les paramètres organiques; B : Limite maximale acceptable pour des terrains à vocation résidentielle, récréative et institutionnelle; C : Limite maximale acceptable pour des terrains à vocation commerciale, non situés dans un secteur résidentiel, et pour des terrains à usage industriel.
11
1.3. Facteurs affectant la mobilité et la phytodisponibilité du plomb dans
les sols
Baize (1997) définit la biodisponibilité comme étant « l’aptitude d’un élément à être transféré d’un compartiment du sol vers un organisme vivant (bactérie, végétal, animal, homme) ». Si l’organisme vivant est une plante on parle alors de phytodisponibilité (Cecchi, 2008).
De nombreux facteurs de sols tels que le pH, la teneur en phyllosilicates et matières organiques ayant une forte affinité pour le métal lourd et la présence d’autres éléments minéraux carbonates, phosphates, oxydes et hydroxydes influencent la disponibilité des métaux lourds tel le Pb, pour les plantes (Kabata-Pendias, 2011). Seule une fraction du contenu total en métal lourd du sol est disponible.
La phytodisponibilité peut être évaluée au laboratoire par des solutions contenant des agents chélateurs (EDTA, DTPA); des acides minéraux à diverses concentrations (HCl, H2SO4 ou HNO3); des sels neutres tels que CaCl2, MgCl2 (Kabata-Pendias, 2011; Pauget,
2015) ou des sels à base d’ammonium tels que NH4OAc ou NH4NO3 (Cecchi, 2008).
Toutes ces méthodes d’extraction tentent de prédire la phytodisponibilité des métaux et leur éventuel mouvement (Pauget, 2015). Bien que la quantité d’éléments traces prélevées par les plantes varie selon l’espèce considérée, la variété, l’organe considéré, une des meilleures façons d’évaluer la phytodisponibilité des métaux est la culture d’une plante sur le sol pollué (Baize, 1997).
1.3.1. pH du sol
Le pH du sol influence la mobilité des métaux lourds et leur biodisponibilité (Beausoleil et Price, 2010; Hedhli, 2010; Manouchehri et al., 2014). Ces études ont montré que le pH est le paramètre le plus important pour prédire la solubilité et l’extractibilité des éléments traces métalliques.
12
La diminution du pH est le facteur qui favorise la mobilité de la plupart des métaux suite à la mise en solution des sels métalliques et/ou la destruction de leur phase de rétention (Braud, 2007). La mobilisation de Pb est généralement lente, mais certains paramètres du sol, comme l'augmentation de l'acidité peut augmenter sa solubilité et par conséquent constituer une importante source de pollution des sols au Pb (Douay et Sterckeman, 2002; Magali, 2008; Kabata-Pendias, 2011).
L'alcalinité du sol réduit la mobilité des métaux lourds tels que Zn, Cu, Pb et Ni puisque ces derniers ont tendance à précipiter avec les carbonates présents dans les sols calcaires. L’adsorption du Pb par la matière organique du sol augmente avec l'augmentation du pH (Karam et al., 1983; Kabata-Pendias, 2011) ont trouvé que les quantités de Zn sorbées étaient très fortement corrélées avec le pH des solutions d'équilibre. La teneur en argile et le pH du sol étaient les propriétés du sol dominantes influençant la sorption spécifique Zn.
1.3.2. Carbonates
Parmi les roches sédimentaires carbonatées, la calcite (CaCO3) et la dolomite
(CaMg(CO3)2) sont les composés les plus abondants dans le sol (Sobanska, 1999). La
concentration du Pb dans les carbonates de calcium ou les particules de phosphate peuvent atteindre 20000 mg/kg comme dans les nodules Fe-Mn (Kabata-Pendias, 2011).
En milieu oxydé, ce sont les carbonates et les phosphates qui sont majoritairement responsables de la rétention du Pb alors qu’en milieu réducteur, sa mobilité est limitée surtout par la galène (PbS) (Philippe et al., 2012). La calcite (CaCO3), les chaux calciques,
les géomatériaux riches en carbonates de calcium et les sous-produits industriels ou agroalimentaires riches en calcium, en carbonates ou en produits calcaires calcite, dolomite, chaux calcique, ciment Portland, …) ont été utilisés comme adsorbant ou agent de précipitation de métaux pour décontaminer des eaux riches en métaux ou pour immobiliser des métaux solubles dans les sols, les résidus miniers ou les eaux usées (McBride, 1979, 1980; Papadopoulos et Rowell, 1988, 1989; Zachara et al., 1991; Evanko
13
et Dzombak, 1997; Green-Pedersen et al., 1997; Hoffmann et Stipp, 2001; Ashaki et al., 2002; Matlock et al., 2002; Rouff et al., 2005; Al-Degs et al., 2006; Karam et De Coninck, 2007; Lakshtanov et Stipp, 2007; Karam et al., 2009a,b; Karam et Jaouich, 2009; Song et al., 2011; You et al., 2011; Merrikhpour et Jalali, 2012; Karam et al., 2015).
1.3.3. Phosphates
Les composés phosphatés sont très efficaces pour réduire la biodisponibilité du Pb et cet aspect est plus accentué avec les roches phosphatées que les engrais phosphatés et contribue à alimenter les fractions organiques en particulier les fractions résiduelles (Kabata-Pendias, 2011). Dans les sols fortement pollués au Pb contenant suffisamment de P (Cotter-Howells, 1996), on observe la formation de phosphate de plomb de type pyromorphite, Pb5Cl(PO4)3 (Cao et al., 2003). La concentration de ce minéral dans le sol
est élevée près des racines de graminées (Agrostis capillaris), ce qui laisse indiquer que la rhizosphère influence les processus de sa formation dans le sol (Kabata-Pendias, 2011).
Outre l’adsorption du Pb par les oxydes métalliques du sol, la formation de composés de Pb insolubles est un autre processus potentiellement important contrôlant la disponibilité du Pb dans les sols (Hettiarachchi et al., 2000; Kabata-Pendias, 2011). Hettiarachchi et al. (2000) ont examiné l’effet de l’application du cryptomélane, un oxyde de manganèse ainsi que deux engrais phosphatés, le superphosphate triple et le phosphate naturel, sur la disponibilité du Pb dans cinq sols contaminés par des métaux ou dans des résidus miniers du Kansas et du Missouri. Les résultats ont montré que l’apport de P plus minéral de manganèse s’est avéré plus efficace pour réduire la forme disponible du Pb que l’ajout de l’un ou de l’autre amendement seul dans les sols. Ces résultats montrent que ces amendements sont des agents de précipitation (cas des engrais phosphatés) et d’adsorption (cas du cryptomélane) du Pb dans les sols.
Dans une étude portant sur la décontamination in situ d’un sol contaminé par des ÉTM provenant d’un ancien site de fonderie de zinc en Belgique, Boisson et al. (1999) ont
14
évalué l’effet de l’ajout de l’hydroxyapatite (HA) sur la disponibilité des métaux dans le sol et sur la croissance et les teneurs des métaux dans le maïs (Zea mays) et les haricots (Phaseolus vulgaris). L’hydroxyapatite ayant diminué la disponibilité des métaux dans le sol, les concentrations des métaux toxiques dans les feuilles des deux plantes cultivées dans le sol traité étaient inférieur au sol témoin.
Jalali et Moharami (2010) ont mené une expérience en colonnes de lixiviation pour examiner l’effet de l’application de deux sources de P, le phosphate monopotassique (KH2PO4)(PMP) et le phosphate diammonium (NH4)2PO4)(PDA), sur la répartition de cinq
métaux lourds (Cd, Cu, Pb, Ni, Zn) parmi les fractions chimiques d’un sol calcaire contaminé. Le sol a été lixivié avec des solutions 0,01 M (NH4)2HPO4 ou 0,01 M KH2PO4.
Les résultats ont montré que le PDA a significativement augmenté les concentrations de Cd, Cu, Ni et Zn dans la fraction échangeable, tandis que la concentration du Pb dans la fraction échangeable a diminué avec l’application du PDA et du PMP. Cette baisse est attribuée à la précipitation/fixation du Pb par les engrais phosphatés, ce qui a amené les auteurs à conclure que les engrais phosphatés contribuent à immobiliser le Pb dans le sol.
Cao et al. (2003) ont mené une expérience in situ à l’échelle pilote sur un site contaminé par des métaux lourds dans le centre de la Floride pour évaluer l’efficacité de trois sources de P (H3PO4, Ca(H2PO4)2 et phosphate naturel) à immobiliser trois métaux lourds (Cu, Pb
et Zn) dans le sol cultivé avec l’herbe de St-Augustin (Stenotaphrum secundatum). Les sources de P ont été appliquées à un rapport molaire P/Pb de 4,0 avec trois traitements comme suit : i) 100% de P provenant du H3PO4, ii) 50% de P provenant du H3PO4 + 50%
de P provenant du Ca(H2PO4)2, et iii) 50% de P provenant du H3PO4 + 50% de P provenant
du phosphate naturel. Les auteurs ont observé la formation d’un minéral non soluble de type pyromorphite dans le sol. Bien que les sources de P aient amélioré l’absorption du Pb par les racines de la plante, elles ont réduit le transfert du Pb vers les parties aériennes notamment en précipitant le Pb au niveau des membranes racinaires sous forme de pyromorphite.
15 1.3.4. Matières organiques
La matière organique du sol constitue un facteur clé dans les échanges ioniques et les cycles géochimiques des éléments métalliques. Certains auteurs ont fait remarquer que la fixation du Pb par la MO est plus importante que la fixation par les oxydes hydratés (Kabata-Pendias, 2011) et que généralement le Pb est accumulé près de la surface du sol, principalement en raison de sa sorption par la MO. Celle-ci présente une forte affinité à l’égard du Pb (Kabata-Pendias, 2011).
1.3.5. Oxydes et hydroxydes de fer, de manganèse et d'aluminium
Le Pb a une grande affinité pour les oxydes de Fe. Les oxydes de Fe enrichis en P se combinent plus facilement avec le Pb que les oxydes de Fe sans P (Sobanska, 1999). La distribution du Pb dans les profils de sol n’est pas uniforme et révèle une grande association avec des hydroxydes, en particulier de Fe et de Mn. Baize (1997) a trouvé que le Pb est plus corrélé au fer libre qu’au Fe total. Les concentrations de Pb dans les nodules Fe-Mn peuvent être très élevés et atteindre 20000 mg/kg (Kabata-Pendias, 2011). Le prélèvement de Pb du sol par les plantes est réduit en présence de phosphates et d’oxydes de Mn hydratés (Mench et Baize, 2004).
1.3.6. Minéraux argileux (phyllosilicates)
Selon Kabata-Pendias (2011), la distribution du Pb dans les sols minéraux montre une corrélation positive avec la fraction fine granulométrique, ce qui indique des niveaux croissants avec l'augmentation de la teneur en argile riche en phyllosilicates.
Différents types d’aluminosilicates (attapulgite, illites, montmorillonite, kaolinite, sépiolite, bentonite, zéolites) ont été utilisés comme adsorbant de métaux (Cd, Co, Cr, Cs, Fe, Pb, Mn, Ni, Zn) pour décontaminer des eaux usées ou naturelles riches en métaux ou pour immobiliser des métaux solubles dans les sols ou les résidus miniers (Sanchez et al.,
16
1999; Al-Degs, Shahwan et Erten, 2002; Alvarez-Ayuso et García-Sánchez, 2003; Tutunji et Baker, 2003; Yavuz et al., 2003; Ayari et al., 2005; Al-Degs et al., 2006; Fonseca et al., 2006; Bhattacharyya et Gupta, 2008; Ijagbemi et al., 2009; Karam, et al., 2009a,b; Vieira et al., 2009; Ghorbel-Abid, et al., 2010; Ding et al., 2011; Karam et al., 2011; Sdiri et al., 2011; El-Eswed et al., 2012; Guerra et al., 2013; Zhao et al., 2013; Anthony et Godfrey, 2014; Lim et Aris, 2014; Akpomie et Dawodu, 2015; Ghorbel-Abid et Trabelsi-Ayadi, 2015).
Parmi les phyllosilicates, la bentonite a souvent été utilisée comme adsorbant de métaux, dans les sols, les résidus miniers et les eaux usées ou enrichies en (Chegrouche et al., 1997; Mellah et Chegrouche, 1997; Sheta, et al., 2003; Ayari et al., 2005; Vega et al., 2005; Bhattacharyya et Gupta, 2006; Xu et al., 2008; Karam et al., 2009a,b; Meneguin et al., 2011; Galindo, et al., 2013; Aljlil et Alsewailem, 2014). La bentonite est le nom commercial d’une argile naturelle (phyllosilicate) contenant une forte quantité de montmorillonite (Maujean, 1993). La montmorillonite est une argile de type 2 :1 dioctaédrique possédant une capacité d’échange cationique et une surface spécifique élevées (Kabata-Pendias, 2011; Dutta et Mishra, 2016). La présence de groupements silanol et aluminol sur la surface des bentonites est responsable de la sorption des ions métalliques (Akpomie et Dawodu, 2015).
Les cations échangeables prédominant dans les bentonites sont le Na+ (bentonite sodique) ou le Ca2+ (bentonite calcique). Les bentonites que l’on retrouve dans plusieurs gisements à
travers le monde peuvent contenir une combinaison de plusieurs autres minéraux comme minéraux accessoires ou impuretés, quelques-uns en concentration trace.
1.4. Adsorption ou immobilisation du plomb par les amendements de sols
Plusieurs études ont démontré que l’ajout d’amendements inorganiques ou agents d’adsorption/séquestration ou de précipitation de métaux tels que zéolite, bentonite, sépiolite, calcite ou carbonate de calcium, chaux agricole, sous-produits calcaires, ciment, sous-produits riches en gypse, sous-produits marins (résidus de crevettes, poissons),
17
composts, tourbe, engrais à base de phosphate, apatite, hydroxyapatite, oxyde de fer ou grenaille de fer peut immobiliser les métaux dans les sols (Gworek, 1992; Sappin-Didier et al., 1994; Knox et al., 2003; Illera et al., 2004; Karam et al., 2011), les sédiments ou résidus miniers (Casséus et Karam, 2006; Karam et De Coninck, 2007; Karam, et al., 2009a,b; Nduwayezu et al., 2013; Sdiri et Higashi, 2013) ou pour réduire les quantités de métaux toxiques prélevés par la plante (Chlopecka et Adriano, 1997; Keller et al., 2005).
1.5. Fractionnement du plomb dans le sol
Bien que le plomb soit peu mobile, son accumulation dans le sol constitue un problème à long terme. Afin d’estimer le risque d'une dégradation de la qualité des sols, il est utile de comprendre le processus de transfert des métaux d'une forme à une autre dans les sols (Bataillard, 2002). Les essais d’extractibilité des métaux au moyen de solutions chimiques permettent de prédire le transfert sol-plante du métal donc une estimation des quantités potentiellement disponibles (Manouchehri et al., 2014). Le fractionnement du métal est un paramètre important à prendre en compte pour connaître la mobilité des métaux dans le milieu naturel (Sobanska, 1999). Ce qui permet de prédire les risques d’une contamination métallique de la chaine alimentaire (plantes-animaux-humains) (Sénat, 2016).
La spéciation des éléments chimiques dans les phases solide et liquide du sol représente un critère déterminant de leur mise en disponibilité pour les plantes (Remon, 2006; Philippe et al., 2012). La biodisponibilité fait référence au potentiel d’un élément à être absorbé par un organisme et pouvant réagir à l’intérieur de son métabolisme (Gagné, 2000). Le fractionnement de l’élément ou la spéciation de la phase solide du sol se rapporte à des procédés d'identification et de quantification des différentes espèces, formes et phases physicochimiques dans lesquelles un élément est présent dans les matériaux étudiés (Magali, 2008; Kabata-Pendias, 2011). On peut alors dire que l’objectif de la spéciation est de localiser les métaux dans les différents compartiments du sol susceptible de les fixer (Douay et Sterckeman, 2002).