Lixiviation du potassium sous culture de pomme de
terre irriguée en sol sableux :
Impact des engrais azotés
Mémoire
Ameni Chaouechi
Maîtrise en sols et environnement
Maître ès sciences (M. Sc.)
Québec, Canada
III
Résumé
Au Québec, la pomme de terre est cultivée sur des sols sableux favorisant les pertes par lixiviation de l’azote et du potassium. Selon le principe de réactions d’échanges cationiques, on a supposé que les doses et les sources d'azote puissent avoir un impact sur la lixiviation du potassium. Ainsi, une expérience a été menée, pendant trois années, dans un champ de pomme. Le dispositif expérimental est un bloc complet aléatoire de quatre répétitions constitué de 10 traitements qui sont un factoriel de trois sources d'azote (nitrate d’ammonium, sulfate d’ammonium et un engrais à libération lente) et trois doses (120, 200 et 280 kg N ha-1) avec un traitement témoin. Des lysimètres ont été installés pour récupérer la solution du sol et doser sa concentration en potassium aux deux semaines.
Les résultats ont révélé un effet non significatif de la source et de la dose de l'azote sur la lixiviation du potassium. Un modèle d’évolution de la lixiviation de potassium est obtenu pour aider les producteurs à mieux fractionner leurs engrais potassiques. Le bilan partiel de K montre une lixiviation nette pour les parcelles qui ont reçu une fertilisation azotée mais pas pour le témoin.
V
Table des matières
Résumé... ... III Table des matières ... V Liste des tableaux ...VII Liste des figures ... IX Liste des abréviations et des sigles ... XI Dédicace ... XIII Remerciements ... XV
Chapitre 1. Introduction générale ... 1
Chapitre 2. Revue de littérature ... 3
2.1. Pomme de terre et régie potassique ... 3
2.1.1. Différents stades de développement ... 3
2.1.2. Exigences en potassium et effet de la carence en cet élément ... 4
2.1.3. Effet de la teneur en eau disponible sur le rendement ... 8
2.1.4. Calibration des besoins en engrais potassiques de la pomme de terre au Québec ... 9
2.1.5. Engrais minéraux potassiques utilisés ... 10
2.2. Dynamique et gestion du potassium du sol ... 12
2.2.1. Fractionnement du potassium en lien avec la minéralogie des sols ... 12
2.2.2. Facteurs influençant la disponibilité de potassium du sol ... 14
Minéraux argileux et CEC ... 14
Potassium échangeable ... 15
pH du sol ... 15
Humidité et aération du sol ... 16
Interaction du K avec les autres éléments N, Ca et Mg ... 17
Chapitre 3. Hypothèse et objectifs de recherche ... 21
3.1. Hypothèse de recherche ... 21
3.2. Objectifs de recherche ... 21
Chapitre 4. Matériels et méthodes ... 23
4.1. Présentation du site ... 23
4.1.2. Climat ... 24
4.1.3. Caractérisation pédologique et physico-chimique des sols des sites expérimentaux ... 24
4.2. Dispositif expérimental... 26
4.3. Extraction et dosage de la solution du sol ... 27
4.4. Échantillonnage et analyse du potassium du sol ... 29
4.5. Bilan partiel du potassium dans le sol ... 30
4.6. Méthodes statistiques ... 30
Chapitre 5. Résultats et discussion ... 31
5.1. Conditions pluviométriques et irrigation ... 31
5.2. Mesure du potassium dans la solution du sol ... 32
5.3. Mesure du potassium dans le sol ... 41
5.4. Prélèvement de K par les plantes ... 44
5.5. Bilan partiel du potassium ... 45
Conclusion générale ... 49
Références bibliographiques ... 51
VII
Liste des tableaux
Tableau 1. Caractéristiques principales recherchées au niveau des tubercules de PDT de transformation (Gravoueille, 1996) ... 5 Tableau 2. Grille de référence pour la fertilisation en potassium pour la pomme de terre ... 10 Tableau 3. Dates de plantation et de récolte ... 24 Tableau 4. Textures des sites expérimentaux dans les deux champs A et B ... 25 Tableau 5. Caractéristiques physico-chimiques des 20 premiers centimètres des sols des sites expérimentaux ... 25 Tableau 6. Traitements de fertilisation potassique et azotée ... 26 Tableau 7. Calendrier de collecte de l'eau des lysimètres ... 28 Tableau 8. Résultats d’ANOVA des différentes interactions pour les 3 années
2010-2012 ... 32 Tableau 9. Statistiques descriptives pour le potassium lixivié par sources, par doses d’azote et pour l’interaction de sources X doses mesuré lors des saisons 2010-2011-2012 ... 35 Tableau 10. Bilan de K entre le printemps-récolte et lessivage hivernal-récolte ... 46
IX
Liste des figures
Figure 1. Cycle de croissance et de développement de la pomme de terre (Kotchi,
2004) ... 3
Figure 2. Évolution de l'absorption des éléments nutritifs majeurs par la pomme de terre ... 4
Figure 3. Évolution des rendements de la PDT en fonction de la dose de K ... 6
Figure 4. Tubercule de pomme de terre atteint par le mildiou (Gérard, 2013) ... 7
Figure 5. Tubercules de pomme de terre atteints par la fusariose (Gérard, 2013) ... 7
Figure 6. Rendement de la pomme de terre en fonction de la source de potassium (Panique et al., 1997) ... 11
Figure 7. Le cycle biogéochimique du potassium et biodisponibilité du potassium minéral du sol (Schvartz et al., 2005) ... 14
Figure 8. Disponibilité relative d’éléments courants dans les sols minéraux selon le pH (Truog, 1948) ... 16
Figure 9. Localisation géographique du site expérimental (46°50’30’’ N, 71°38’20’’ O) (Google maps) ... 23
Figure 10. Installation des lysimètres ... 28
Figure 11. Échantillonnage des cylindres pour la détermination masse volumique apparente ... 29
Figure 12. Comparaison entre la quantité mensuelle de précipitation mesurée sur le site expérimental en 2010, 2011 et 2012 et la normale de 30 ans et quantité d’eau apportée sous forme d’irrigation ... 31
Figure 13. Relation entre la moyenne des concentrations de K (mg L-1) dans les lysimètres et la dose totale d’azote (kg ha-1) appliquée en fonction de la source d'azote (NA : nitrate d'ammonium, SA : Sulfate d'ammonium, ESN : engrais à libération lente) lors de la saison 2011 ... 33
Figure 14. Concentrations moyennes annuelles du K (mg L-1) mesurées dans la solution du sol via les lysimètres en fonction des différentes sources d’azote (Nitrate d'ammonium (NA), Sulfate d'ammonium (SA) et engrais à libération lente (ESN)), lors des saisons 2010, 2011 et 2012 ... 36
Figure 15. Concentrations moyennes annuelles du potassium (K) (mg L-1) mesurées dans la solution du sol via les lysimètres en fonction des différentes doses d’azote lors des saisons 2010, 2011 et 2012 ... 37 Figure 16.Concentrations moyennes du potassium (K) (mg L-1) mesurées dans les lysimètres en fonction des différentes sources d'azote (Nitrate d'ammonium (NA), Sulfate d'ammonium (SA) et engrais à libération lente (ESN) et le témoin) et de la période de récolte (JAP) lors des saisons 2010, 2011 et 2012 ... 38 Figure 17. Concentrations moyennes du potassium (K) (mg L-1) mesurées dans les lysimètres en fonction des différentes sources (Nitrate d'ammonium (NA), Sulfate d'ammonium (SA) et engrais à libération lente (ESN)) et doses d’azote lors des saisons 2010, 2011 et 2012 ... 40 Figure 18. Teneur en K (kg ha-1) du sol en fonction de la profondeur et de la période d'échantillonnage en 2010 ((a) témoin (sans azote), (b) 200 kg N ha-1) ... 42 Figure 19. Teneur en K (kg ha-1) du sol en fonction de la profondeur et de la période d'échantillonnage en 2011 ((a) témoin (sans azote), (b) 200 kg N ha-1) ... 43
Figure 20. Teneur en de K (kg ha-1) du sol en fonction de la profondeur et de la période d'échantillonnage en 2012 ((a) témoin (sans azote), (b) 200 kg N ha-1) . 44 Figure 21. Relation entre le potassium prélevé par les plants et le K lixivié (mesuré dans les lysimètres) durant le cycle végétatif de la culture de pomme de terre exprimé en nombre de jours après la plantation (JAP) ... 45
XI
Liste des abréviations et des sigles
Al : Aluminium Ca : Calcium
CAH : Complexe argilo-humique CEC : Capacité d’Echange Cationique ESN : Engrais à libération lente
HATS : Système de transport de haute affinité JAE : Jours après l'émergence
JAP : Jours après la plantation K : Potassium
KM-3 : Potassium extrait selon la méthode Mehlich 3
LATS : Système de transport de faible affinité Mg : Magnésium Mn : Manganèse MO : Matière Organique MS : Matière sèche NA : Nitrate d'ammonium Na : Sodium N : Azote P : Phosphore PDT : Pomme de terre SA : Sulfate d'ammonium SR : Sucres réducteurs
XIII
Dédicace
À mes très chers parents
À ma mère, source de tendresse et d’amour, pour son soutien tout le long de ma vie scolaire.
À mon père, qui m’a toujours soutenu et qui a fait tout son possible pour m’aider.
Les mots me manquent pour exprimer toute la reconnaissance, la fierté et le profond amour que je vous porte pour les sacrifices que vous avez consentis pour ma réussite, que vous trouvez ici le témoignage de mon attachement, gratitude et respect, que Dieu vous préserve bonne santé et longue vie.
À mon mari
À l’homme de ma vie, mon exemple éternel, mon soutien moral et source de joie et de bonheur, celui qui s’est toujours sacrifié pour me voir réussir.
À mes sœurs
À mes chères sœurs, j’espère atteindre le seuil de vos espérances. Que ce travail soit l’expression de ma profonde affection. Je vous remercie pour le soutien moral et l’encouragement que vous m’avez accordés.
À tous ceux qui sont chers pour moi et que je le suis pour
eux.
XV
Remerciements
« Dieu soit loué, car sans sa bénédiction ce présent travail n’aurait pas pu voir le jour ».
des sols et de génie agroalimentaire, pour le temps qu'il m'a accordé et Je tiens à remercier mon directeur de recherche, Mr Lotfi Khiari, professeur au département les précieuses recommandations et suggestions pertinentes.
Mes remerciements les plus sincères s’adressent également à ma co-directrice de recherche Dr Athyna Cambouris qui m’a accueillie avec bienveillance dans son bureau et qui a mis à ma disposition tout le matériel nécessaire pour la réalisation de ce projet. Son expérience, son talent professionnel et ses qualités humaines m’ont été d’une grande utilité.
Je témoigne aussi une particulière gratitude à Mme Noura Ziadi, pour le soutien moral, d'avoir cru en mes capacités, de m'avoir fourni de l'aide et de m'avoir accueillie dans son laboratoire. Qu’elle soit assurée de ma gratitude et ma reconnaissance les plus respectueuses.
J'aime aussi souligner la contribution des membres du laboratoire de pédologie et d'agriculture de précision : M. Mario Deschênes, M. Claude Lévesque, M. André Martin, Mme Isabelle Perron, Mme Sarah Maude Parent et M. Charles Fournier Marcotte qui m'ont accordé toute l'aide et les facilités pour mener à bien les analyses au laboratoire et pour l'ambiance de travail. J'adresse aussi mes vifs remerciements à Mme Sylvie Michaud qui m'a consacré de son temps pour mes analyses au sein du laboratoire du Centre de recherche et de développement sur les sols et les grandes cultures.
Je remercie énormément les évaluateurs de ce mémoire. Il s’agit de M. Silvio José Gumière et M. Michel Caillier du département des sols et de génie agroalimentaire.
À tous ceux que j’ai cité et à tous ceux qui ne sont pas cités et qui m’ont apporté à un moment ou un autre une aide à la conduite de ce travail : un grand merci du fond de mon cœur.
1
Chapitre 1. Introduction générale
La consommation de la pomme de terre (PDT) est très répandue à l’échelle mondiale. Cette culture vivrière occupe le quatrième rang en importance après le maïs, le blé et le riz. Le Canada avec 4,1 millions de tonnes occupe le 14ème rang en termes de production (FAOSTAT, 2011). En termes de rendement, le Canada se classe au 18ème rang mondial avec 31,3 t ha-1 (Drouin, 2008).
La PDT est la culture légumière la plus importante du Canada. En 2007, elle représentait 33% des recettes monétaires tirées de la culture des légumes, soit 846 millions de dollars canadiens (Drouin, 2008). Elle est cultivée à l’échelle commerciale dans toutes les provinces canadiennes. La production est toutefois concentrée en bonne partie à l’Île-du-Prince-Édouard, au Manitoba, en Alberta, au Nouveau-Brunswick et au Québec. Au Québec, environ 17000 hectares sont utilisés pour la production de la PDT (Institut de la statistique du Québec, 2012).
Dans le contexte du Québec, la PDT est produite sur des sols sableux, très fortement podzoliques, acides, et très propices à la lixiviation des éléments fertilisants et notamment le potassium qui est essentiel à de bons rendements et une bonne qualité. Non toxique, le potassium ne forme pas de gaz qui peut s’échapper dans l’atmosphère, mais étant donné que c'est un ion mobile dans le sol, des quantités importantes peuvent être perdues par lixiviation. Cependant, jusqu’à aujourd’hui, peu d'attention a été accordée à cet élément car il ne provoque pas directement l’eutrophisation des systèmes aquatiques (Alfaro et
al., 2004).
Dans le sol, les éléments nutritifs sont soit en synergie soit en concurrence. Le potassium du sol sous forme de K+ est en compétition avec l’ion ammonium NH4+, chargés tous les
deux positivement, sur les sites d’échanges du complexe argilo-humique. De ce fait, les engrais azotés apportant l’ion NH4+ peuvent avoir un impact sur la lixiviation du
potassium. Cet impact est d’autant plus important si la forme d’engrais azoté utilisée est formée à 100 % par les ions NH4+.
Au Québec, l’irrigation de cette culture ne cesse de croître et la superficie irriguée représente 27% de la superficie totale cultivée (Bergeron, 2012). L’irrigation de cette
2
culture a favorisé de plus en plus le risque de lixiviation, posant aux agriculteurs une contrainte de coût élevé pour les fertilisants potassiques. Par conséquent une utilisation raisonnée et efficace des fertilisants potassiques doit être mise de l’avant, d'une part pour éviter les pertes économiques et diminuer le coût de production et d’autre part pour répondre aux besoins de la culture de la PDT.
Dans ce contexte s’inscrit notre travail de recherche dans lequel on a orienté notre intérêt à l’effet des doses et des sources des engrais azotés sur la lixiviation du potassium dans le sol. Le corps de ce projet est subdivisé essentiellement en quatre parties :
Une synthèse bibliographique portant sur le potassium, son importance dans la culture de la PDT et sa dynamique dans le sol.
Une partie consacrée à la présentation de la zone d’étude et la méthodologie adoptée.
Une partie réservée aux résultats du projet, leurs interprétations et discussion. Une dernière partie pour emmètre les conclusions et les recommandations de
3
Chapitre 2. Revue de littérature
2.1. Pomme de terre et régie potassique
2.1.1. Différents stades de développement
La PDT peut être reproduite par multiplication végétative ou par graine (reproduction sexuée). Cette dernière est très peu pratiquée dans le milieu agricole. Le cycle de croissance ou de développement de la pomme de terre est très court (trois à quatre mois), mais il peut être subdivisé en plusieurs stades qui dépendent des facteurs génétiques de la plante elle-même et des facteurs édapho-climatiques.
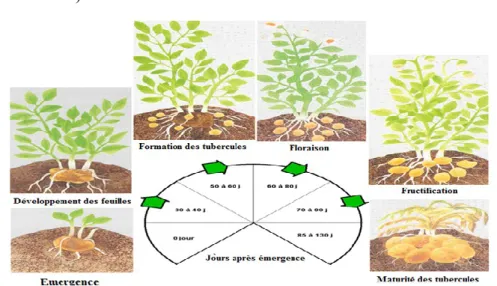
Le cycle de développement de la culture de la pomme de terre comporte six stades (Kotchi, 2004) (figure 1) soit :
La germination et l’émergence de la plantule ;
Le développement des feuilles (30 à 40 jours après l’émergence (JAE)) ; La formation des tubercules et l’émergence de l’inflorescence (50 à 60 JAE) ; La floraison et le développement des tubercules (60 à 80 JAE) ;
Le développement des fruits et la poursuite du développement des tubercules (70 à 90 JAE) ;
La sénescence des feuilles et l’arrêt de développement des tubercules (85 à 130 JAE).
4
2.1.2. Exigences en potassium et effet de la carence en cet
élément
Les critères de qualité de la PDT dépendent principalement des exigences du marché (Gravoueille, 1996) (taille des tubercules, teneur en matière sèche (MS), teneur en amidon, susceptibilité aux taches noires, noircissement après cuisson, teneur en sucres réducteurs). Ces différents aspects sont en étroite relation avec la composition chimique du tubercule, régit elle-même par plusieurs facteurs dont la fertilisation potassique.
Le potassium favorise la circulation et le stockage des hydrates de carbone, notamment l’amidon dans les tubercules. Il active la maturation de ces derniers en synthétisant des sucres et des acides organiques. Il en résulte une teneur en MS à la récolte plus élevée, qui expliquera la diminution des pertes en eau lors du stockage et augmente en même temps le rendement utile pour la transformation industrielle (Panique et al., 1997).
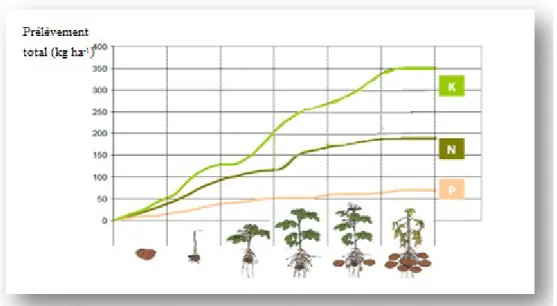
La pomme de terre a une exigence élevée pour le potassium (Dahnke et Nelson, 1993) qui varie entre 350-450 kg de K ha-1 et les recommandations sont fonction du cultivar, du type du sol et de sa richesse en K. L’absorption du potassium varie selon le stade de développement de la culture (figure 2). Elle est plus importante au stade de maturation des tubercules et d’accumulation de l'amidon.
Figure 2. Évolution de l'absorption des éléments nutritifs majeurs par la pomme de terre (Harris, 1978)
5
L'accumulation des sucres réducteurs et la diminution de la teneur en amidon sont les principaux facteurs responsables d'une couleur sombre indésirable lors de la cuisson des croustilles (Martin-Prevel, 1989 et Usherwood, 1985). Il est souhaitable d'avoir un taux de MS élevé, cela permet d'obtenir des frites et des croustilles plus croquantes. La teneur en sucres réducteurs est également importante pour les produits destinés à être cuits à forte température (frites, croustilles). En effet, plus la teneur en sucres est forte, plus la réaction de Maillard (brunissement à la cuisson) est marquée. Pour les croustilles les exigences sont les plus strictes en ce qui concerne la teneur en sucres réducteurs (tableau 1).
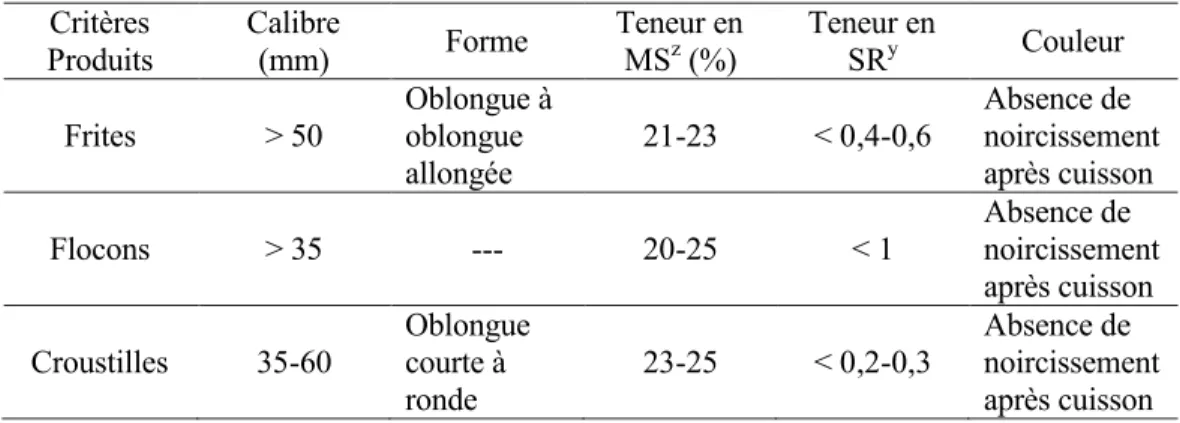
Tableau 1. Caractéristiques principales recherchées au niveau des tubercules de PDT de transformation (Gravoueille, 1996)
zMS : matière sèche ySR : sucres réducteurs
Une carence en potassium affecte plusieurs processus métaboliques tels que l’efficacité de la photosynthèse, de la translocation et de la respiration, ainsi que divers systèmes enzymatiques (Marschner, 1995 et Mengel, 1997). La conséquence générale consiste en une réduction de la croissance de la plante et par la suite une diminution de la qualité des tubercules. Elle peut entraîner une baisse des rendements et de la taille des tubercules (McDole et al., 1978 et Panique et al., 1997). Dans les sols faibles en K, divers chercheurs ont trouvé une réponse significative du rendement en tubercules à la fertilisation potassique (McDole et al., 1978 ; Sharma et Arora, 1987 ; Chapman et al., 1992 et Tindall et Westermann, 1994). D’autres chercheurs, au contraire, n'ont trouvé aucune réponse du rendement à la fertilisation potassique (Ridgman et Jones, 1986 ;
Critères
Produits Calibre (mm) Forme Teneur en MSz (%) Teneur en SRy Couleur
Frites > 50 Oblongue à oblongue allongée 21-23 < 0,4-0,6 Absence de noircissement après cuisson Flocons > 35 --- 20-25 < 1 Absence de noircissement après cuisson Croustilles 35-60 Oblongue courte à
ronde
23-25 < 0,2-0,3 Absence de noircissement après cuisson
6
Roberts et Beaton, 1988 et Curwen, 1992), généralement sur des sols bien pourvus en K disponible pour les plantes.
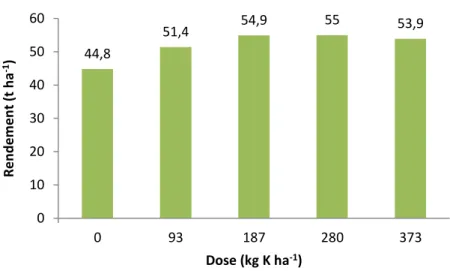
Une autre expérience faite par Panique et al. (2007) a montré les mêmes résultats (figure 3). Le rendement augmente de 45 t ha-1 à 55 t ha-1 pour des doses respectives de 0 et 280 kg K ha-1, en augmentant la dose encore plus (373 kg K ha-1), on remarque que le rendement diminue de 1 t ha-1.
Figure 3. Évolution des rendements de la PDT en fonction de la dose de K (Panique et al., 1997 ; modifié)
D’autres chercheurs ont lié cette observation à la forme de l'engrais potassique utilisé qui peut contenir d’autres éléments essentiels à la plante notamment du soufre (S) ou du chlore (C1). Certains auteurs ont rapporté une plus grande augmentation du rendement en utilisant le chlorure de potassium (KC1) (Tindall et Westermann, 1994) et d'autres en utilisant le sulfate de potassium utilisant K2SO4 (Wilcox, 1961).
La carence en potassium peut diminuer la résistance de la PDT à certaines maladies. Il a été démontré qu’une carence en fertilisation potassique dans la culture de la PDT entraine une augmentation de l'incidence des maladies sévères comme le mildiou (Phytophtora
infestans), l’ennemi numéro 1 de la PDT (figure 4), la fusariose (Fusarium ssp.) (figure
5), la gale poudreuse (Spongospora subterranea) et l'alternariose (Alternaria solani) (Marschner, 1995). 44,8 51,4 54,9 55 53,9 0 10 20 30 40 50 60 0 93 187 280 373 R e n d e m e n t (t h a -1) Dose (kg K ha-1)
7
Figure 4. Tubercule de pomme de terre atteint par le mildiou (Gérard, 2013)
Figure 5. Tubercules de pomme de terre atteints par la fusariose (Gérard, 2013)
Roberts et McDole (1985) ont mis en évidence qu’une nutrition adéquate de la plante en potassium réduit la susceptibilité du tubercule au noircissement interne. Le coeur creux consiste en des cavités dans les tubercules avec des tissus bruns nécrotiques (Bergmann, 1992). Plusieurs auteurs ont démontré que l'application des engrais potassiques peut réduire l'incidence du coeur creux. Nelson (1970), a montré que les effets additifs du semis précoce, de l’espacement serré entre les plants et de la fertilisation potassique réduit le cœur creux de 45,9 à 5,7 %, mais cet effet peut être particulier aux sols riches en potassium puisque l’ajout de K à des sols pauvres a entraîné une augmentation de l'incidence du coeur creux (Moore, 1927 et Nelson, 1970).
8
2.1.3. Effet de la teneur en eau disponible sur le rendement
La PDT, comme toutes les plantes, assure sa croissance et son développement d’une part par les produits élaborés par la photosynthèse et, d’autre part, par l’eau et les éléments minéraux puisés dans le sol. Plusieurs auteurs s’accordent pour dire que l’irrigation dans la culture de la pomme de terre est quasi nécessaire (Kashyap et Panda, 2003 et Thibault, 2003). Au Québec, les travaux de Giroux (1987) ont démontré une relation entre le rendement de la pomme de terre et la réserve en eau disponible d'un sol.
Cette culture est très vulnérable au stress hydrique car elle possède un système radiculaire peu développé et localisé près de la surface (Bergeron, 2006) et, selon la même source, le déficit hydrique a des effets négatifs sur le rendement en tubercules et la qualité de la PDT. Tout dépend du stade de croissance, il peut causer :
- Peu ou pas d’effets sur la qualité des tubercules, mais les tubercules produits par tige sont moins nombreux (avant l’initiation des tubercules) ;
- La formation de tubercules difformes (à l’initiation des tubercules) ;
- L'obtention de tubercules de forme irrégulière, des fissures de croissance, d'excroissance « téton », de réduction du calibre et de la densité, ainsi qu'une augmentation des sucres réducteurs (au grossissement des tubercules).
Un stress hydrique se manifestant au moment de l’initiation des tubercules peut entraîner une réduction du nombre d’ébauches formées par plante (Bernhards, 1998) et aussi engendrer des tubercules de moins bonne qualité (Stark et Wright, 1985). Selon Tsé Bi (1999), les besoins en eau de la pomme de terre sont plus importants aux phases d’émergence et de croissance des tubercules. Un stress hydrique survenant lors de la maturation cause moins de pertes de rendement qu’un stress survenant plutôt dans le développement ou au stade de la formation des tubercules.
L’importance de l’irrigation dans la culture de la pomme de terre au Québec est étudiée par Gallichand et Broughton (1993) qui ont remarqué que le déficit hydrique dû à une mauvaise répartition des précipitations dans le Sud-Ouest du Québec a influencé les productions. Cette condition défavorable pour la culture peut faire chuter les rendements en tubercules.
9
Cependant, l’irrigation de la pomme de terre engendre des coûts élevés et requiert des quantités d’eau importantes. Les besoins en eau varient tout au long du cycle végétatif et dépendent de facteurs comme la date de maturité du cultivar, la densité des plants, la dose d'engrais, la capacité de rétention en eau des sols, les conditions climatiques, les pratiques culturales, le système racinaire et le type de marché visé (semence, table, transformation) (Thibault, 2003). Un excès d’eau, survenant en début de la formation du système racinaire, limite, quant à lui, le développement des racines et retarde la maturité. Il peut causer le pourrissement des plants ou des tubercules-fils (Kotchi, 2004). Pour une saison de croissance complète, les besoins totaux en eau atteignent environ 455 mm. La production de PDT sous irrigation est en forte expansion dans l'Ouest canadien. Les producteurs appliquent des engrais et des pesticides afin d'obtenir des rendements élevés. Toutefois, la lixiviation de ces produits dans l'eau souterraine est souvent considérée comme le plus grand risque de la culture sous irrigation, particulièrement lorsque la conduite des cultures n’est pas effectuée adéquatement (Kotchi, 2004).
2.1.4. Calibration des besoins en engrais potassiques de la
pomme de terre au Québec
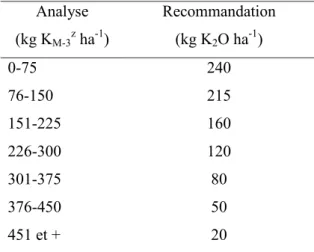
Le raisonnement de la fertilisation repose sur quatre critères : les exigences de la culture, la teneur du sol en K, le passé de fertilisation et le devenir des résidus de la récolte précédente. Les recommandations en potassium pour la culture de la pomme de terre au Québec sont mentionnées dans le guide du CRAAQ (2010) (tableau 2). Ces recommandations en K2O dépendent du résultat de l’analyse du sol en K extrait au
Mehlich (KM-3), mais un excès de K peut nuire à l’absorption du calcium et du
10
Tableau 2. Grille de référence pour la fertilisation en potassium pour la pomme de terre
z K
M-3: Potassium du sol extrait au Mehlich-3 Source : (CRAAQ, 2010)
2.1.5. Engrais minéraux potassiques utilisés
La PDT est une culture exigeante en fertilisants potassiques, de ce fait l'apport du potassium sous formes d'engrais est un garant pour l’obtention de bons rendements (quantité et qualité des tubercules). Les deux principales sources de potassium utilisées sont : le chlorure de potassium appelé aussi muriate de potasse et le sulfate de potassium. 1) Chlorure de potassium (KCl) : est le produit le moins onéreux et le plus courant de tous les engrais potassiques (Khiari, 2012). Il est soit :
- Rouge : de formule 0-0-60 et d’appellation courante muriate rouge de potassium, issu d’un procédé simple d’extraction mécanique laissant des résidus de fer (responsable de la couleur rougeâtre à rosâtre de l’engrais).
- Blanc : de formule 0-0-62 appelé muriate blanc de potassium, issu d’un procédé de solubilisation à la vapeur suivie d’une recristallisation. Ce lavage contribue à l’élimination du fer.
Les muriates rouge et blanc de potassium ont des masses volumiques respectives de 1,1 et 1,2 kg l-1. Vu son indice global de sel élevé 109,4, il faut éviter son application sous des conditions salines et pour les cultures sensibles au sel et au chlore.
2) Sulfate de potassium (K2SO4) de formule (0-0-50) : est un engrais solide blanc de
masse volumique 1,2 kg l-1 contenant 17 % de soufre sous forme hydrosoluble. Il est plus
Analyse (kg KM-3z ha-1) Recommandation (kg K2O ha-1) 0-75 240 76-150 215 151-225 160 226-300 120 301-375 80 376-450 50 451 et + 20
11
coûteux que le muriate de potassium et utilisé surtout pour les plantes sensibles pour le chlorure comme la pomme de terre et le tabac (Khiari, 2012). Son indice de sel est de 40. Les chercheurs ont émis des opinions très différentes et parfois divergentes sur l'évaluation des engrais potassiques et leur influence sur les pommes de terre. Selon les uns, il n'y a pas lieu de préférer les sulfates aux chlorures puisque les rendements de tubercules obtenus par les deux formes d'engrais sont semblables (Cooke, 1960 et Harrap, 1960), d’autres ont aussi démontré que les rendements sont supérieurs avec le sulfate du potassium.
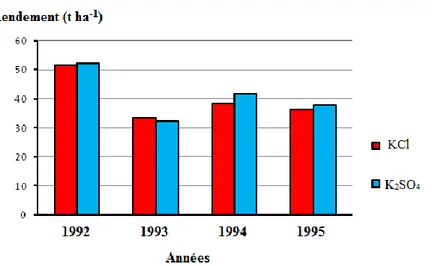
Panique et al. (1997) ont conduit une expérience sur différentes variétés de PDT parmi lesquelles on trouve la Russet Burbank cultivée en sol sableux caractérisé par une faible teneur en K (80 mg kg-1). Les résultats trouvés montrent qu’ils n’existent pas de différence significative entre le muriate de potassium et le sulfate de potassium pour les quatre années d’essai en termes de rendement (figure 6).
Dickins et al. (1962) ont comparé l'effet de différents taux de KCl et K2SO4 sur le
rendement en tubercules et la concentration en MS. L’utilisation de KCl a réduit la concentration en MS des tubercules dans 11 des 16 expériences comparativement à seulement trois réductions lorsque K2SO4 a été utilisé. Allison et al. (2001) ont prouvé
aussi que l’utilisation d’une dose de KCl supérieure à la dose optimale cause des réductions de la concentration en MS. Davenport et Bentley (2001) ont montré que l’application de KCl diminue le rendement total en tubercules.
Figure 6. Rendement de la pomme de terre en fonction de la source de potassium (Panique et al., 1997)
12
2.2. Dynamique et gestion du potassium du sol
Troisième élément essentiel à la croissance des plantes, le potassium est un élément abondant dans la nature car toutes les roches en contiennent. Il se retrouve surtout sous forme non échangeable et dans les minéraux primaires (micas, feldspaths), mais aussi sous forme échangeable et dans la solution du sol. Les roches cristallines en sont plus riches que les roches sédimentaires (0,4 à 6 % contre 0,2 à 2,5 %). Mhiri (2002) souligne que les minéraux argileux (muscovite, biotite, illite, vermiculite et smectite) constituent à la fois, le principal réservoir et le piège à potassium dans les sols. Ils représentent la principale source de potassium pour les plantes. Selon la FAO (2003), le potassium représente entre 1 à 4 % de la MS de la plante.
2.2.1. Fractionnement du potassium en lien avec la minéralogie
des sols
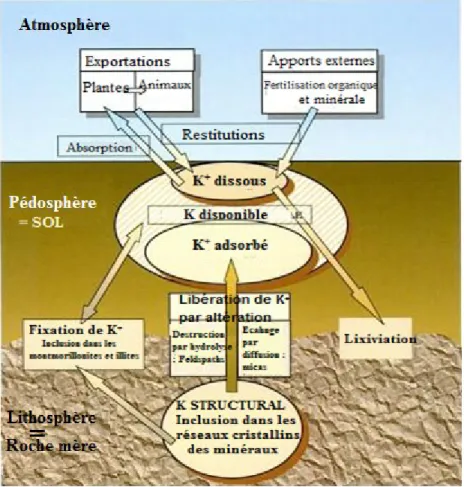
Pour raisonner une fertilisation potassique il est nécessaire de connaître la dynamique du potassium dans le sol. Diverses tentatives ont été faites pour classer les différentes formes de potassium du sol dans un cadre conceptuel simple. Il s'agit de essentiellement de quatre formes "pools" de potassium dans le sol (Sparks et Huang, 1985 ; Barber, 1994 et Syers, 2003) (figure 7). La disponibilité de K pour les plantes diffère d’une forme à une autre.
K dans la solution du sol (Ksol) est sous forme d’ions K+ et constitue la forme la plus
disponible pour les plantes.
K échangeable (Kex) est représenté par le potassium adsorbé sur les sites d’échange
(colloïdes argilo-humiques). Sa valeur dépend beaucoup de la capacité d’échange cationique (CEC) du sol. Les sols à texture fine sont mieux pourvus que les sols sableux. Il contribue au réapprovisionnement de la solution du sol en K et peut être absorbé par les plantes.
Tout apport d’engrais potassique entraîne une augmentation des deux formes précédentes. Il a été rapporté aussi qu'une partie va se fixer entre les feuillets d’argiles pour devenir moins disponible pour les plantes.
13
K fixé entre les feuillets des argiles : lorsque les ions K+ passent de la surface externe
des argiles pour s’insinuer à l’intérieur, entre les feuillets, on dit que le potassium est fixé. Cette forme représente 1 à 10 % du potassium total du sol. Il n'est pas facilement accessible pour l'échange avec d'autres cations dans la solution du sol et, par conséquent, est lentement disponible pour les plantes.
K minéral ou de constitution représente plus de 95 % du potassium total des minéraux silicatés (Mhiri, 2002). Cette forme n’est disponible qu’au terme d’une activité biologique plus ou moins longue aboutissant à l’altération des minéraux silicatés.
Le potassium fixé peut sous certaines conditions être échangé avec les précédentes formes. L’excès de K est à éviter car il est sujet au phénomène de lixiviation surtout en sol sableux. De même, il existe dans le sol une concurrence pour le K entre la plante et le complexe argilo-humique. Pour maintenir un niveau adéquat de la concentration du sol en potassium échangeable, il est opportun d’apporter plus de potassium dans un sol argileux qu’un sol sableux où il est préférable de fractionner les apports et de les synchroniser en fonction des besoins de la plante.
14
Figure 7. Le cycle biogéochimique du potassium et biodisponibilité du potassium minéral du sol (Schvartz et al., 2005)
2.2.2. Facteurs influençant la disponibilité de potassium du sol
La disponibilité du potassium pour les plantes est affectée par plusieurs facteurs, elle est fonction des caractéristiques intrinsèques du sol, ainsi que des pratiques culturales telles que la fertilisation (forme d’engrais et doses ; mode et temps d’application) et les conditions climatiques. Ces facteurs sont la CEC, le pH du sol, la teneur en potassium échangeable, l’humidité, la température et l’aération, de même que l’interaction de K avec les autres éléments minéraux.
Minéraux argileux et CEC
La CEC correspond au nombre de sites négatifs sur le complexe d’échange, c’est la quantité de cations que le sol peut retenir, elle est plus élevée dans les sols à texture fine que dans les sols à texture grossière, ce qui facilite la lixiviation des éléments nutritifs dans ces derniers (Calvet, 2003). Plus la proportion de minéraux argileux contenant du
15
potassium est élevée, plus la disponibilité potentielle du potassium dans le sol est élevée. Les sols contenant de la vermiculite, montmorillonite ou du mica sont plus riches en K que les sols contenant principalement de la kaolinite, qui sont plus altérés et ont une faible teneur en K. Les sols contenant la montmorillonite et intensivement cultivés peuvent être pauvres en K et pour une production agricole optimale, ils doivent être fertilisés (Havlin et al., 2004). Askegaard et al. (2004) ont montré qu’il y a un risque potentiellement élevé de perte de K par lixiviation en raison d'une faible capacité d'échange cationique sur les sols sableux de texture grossière, risque qui a été estimé entre 20 et 46 kg ha-1 an-1.
Une teneur en argile de plus en plus élevée du sol se traduit non seulement par une plus grande CEC, mais aussi par une plus grande capacité de rétention en eau, ce qui peut retarder le mouvement de K. Dans de tels sols, Askegaard et al. (2004) ont prouvé aussi que les pertes par lixiviation peuvent être aussi basses que 1 kg de K ha-1an-1 pour un sol avec 24 % d'argile, alors qu'elles sont de 46 kg ha-1an-1 pour un sol avec seulement 5 % d'argile.
Potassium échangeable
La détermination de K échangeable est une mesure indirecte de la disponibilité de K. Plusieurs recherches ont montré la relation entre l’analyse du potassium dans le sol et la réponse à la fertilisation potassique. L’application des engrais potassiques peut être ajustée à la baisse avec des niveaux croissants de K disponible dans le sol. En général, la quantité de K nécessaire pour augmenter le K échangeable de 1 ppm peut varier de 1 à 23 kg K ha-1 en fonction du type du sol (Havlin et al., 2004). La différence est liée à la variation du pouvoir fixateur de K entre les sols.
pH du sol
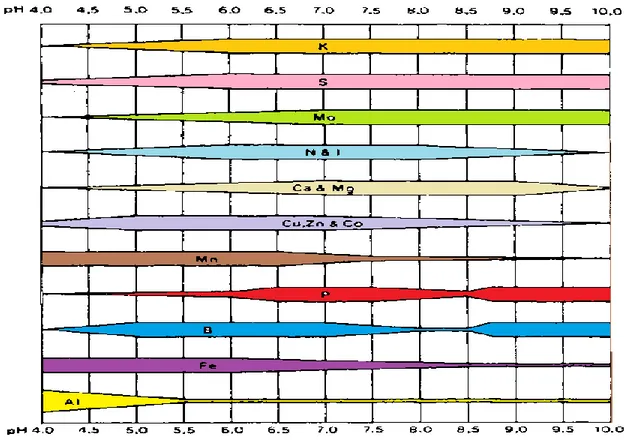
Le pH affecte la disponibilité de tous les éléments chimiques du sol pour les plantes. Le K est plus disponible à des pH proches de la neutralité (figure 8), il est de moins en moins disponible dans les sols acides car il entre en concurrence avec l’Al 3+ pour les sites d’échanges sur le complexe argilo-humique.
16
Figure 8. Disponibilité relative d’éléments courants dans les sols minéraux selon le pH (Truog, 1948)
Dans les sols à pH faible, des quantités toxiques de Mn2+ et Al3+ échangeables créent un environnement racinaire défavorable pour l'absorption des nutriments. Lorsque les sols acides sont chaulés, Al3+ échangeable est converti en Al(OH)3 insoluble. La réduction
d'Al3+ échangeable diminue la concurrence avec K+, permettant à ce dernier de rivaliser avec Ca2+ pour les sites d’échange vacants, par conséquence, une plus grande quantité de K+ peut être adsorbée aux colloïdes. Les pertes par lixiviation de K seront aussi vraisemblablement réduites (Havlin et al., 2004).
Humidité et aération du sol
Un taux d’humidité du sol trop faible ralentit le mouvement du K vers les racines et favorise des formes de K non assimilable (Duval, 2012), car les films d'eau autour des particules du sol sont plus minces et discontinus. L’augmentation des niveaux de K dans le sol ou sa teneur en humidité peut augmenter cette diffusion. L'humidité du sol peut avoir des répercussions importantes sur le transport de K dans le sol. L’augmentation de l'humidité du sol de 10 à 28 % augmente le transport total de 175 % (Havlin et al., 2004).
17
Par contre, un sol saturé en eau aura un mauvais niveau d’oxygénation et causera un développement racinaire limité (Duval, 2012), car l'alimentation en O2 est diminuée.
L’action inhibitrice de la mauvaise aération sur l'absorption des nutriments est la plus prononcée avec le potassium (Havlin et al., 2004).
Interaction du K avec les autres éléments N, Ca et Mg
Comme tout élément chimique le potassium peut avoir un effet antagoniste avec certains autres éléments, à savoir NH4+, Ca2+ et Mg2+ chargés tous positivement, ce qui les met en
compétition sur les sites d’échange du complexe argilo-humique chargé négativement en surface. Les sites d’échange présentent une certaine affinité vis-à-vis la fixation des éléments nutritifs, de ce fait certains sont retenus plus fortement sur le complexe, ce qui augmente de plus cette compétitivité entre les cations. La force de fixation des cations croit dans l'ordre suivant : Na+ < NH4+ < K+ < H+ < Mg2+ < Ca2+ < Al3+ ...., elle dépend
du rayon atomique, de la valence (à rayon atomique semblable, les monovalents sont moins retenus que les bivalents), du degré d'hydratation des ions et du pH du sol (Gobat
et al., 2010).
Jarvis (1987) et Guo et al. (2007) ont montré que la concurrence entre K+ et NH4+ est due
à leur similarité chimique et leur statut ionique identique. Stehouwer et Johnson (1991) ont trouvé que la baisse de la fixation de K+ a été attribuée à la fixation de NH4+
préférentielle qui a bloqué la fixation de K+.
Zhang et al. (2010) ont montré qu’il y a une interaction positive entre N et K pour plusieurs cultures, l’absorption de K a été améliorée en utilisant des engrais N mais ils ont attribué cet effet à une relation de vecteur de transport entre NO3- et K+. Deux
systèmes de transport membranaires distincts pour l'absorption de K par les plantes ont été décrits : un système de transport de haute affinité (HATS) et un système de transport de faible affinité (LATS) (Kochian et Lucas, 1982 et Hirsch et al., 1998). Le HATS fonctionne principalement à des concentrations extérieures basses (<1 mM) de K+ par l'intermédiaire de transporteurs, par contre le LATS domine à des concentrations externes plus élevées (> 1 mM), principalement par l'intermédiaire de canaux (Maathuis et Sanders, 1997 ; Hirsch et al., 1998 ; Véry et Sentenac, 2002 et Szczerba et al., 2006). Un grand nombre de gènes codant pour des systèmes de transport K+ ont été identifiés, révélant un haut niveau de complexité (Véry et Sentenac, 2002 et Szczerba et al., 2006).
18
Différentes formes d'azote influencent l'activité des deux systèmes de transport de K distincts. NH4+ inhibe le HATS (Scherer et al., 1984 ; Vale et al., 1988 ; Hirsch et al.,
1998 ; Spalding et al., 1999 ; Santa-Maria et al., 2000 ; Ashley et al., 2006 ; Nieves-Cordones et al., 2007 et Szczerba et al., 2008), tandis que le LATS est relativement insensible aux ions NH4+ (Santa-Maria et al., 2000 ; Britto et Kronzucker, 2002 et
Kronzucker et al., 2003).
Allison et al. (2001) ont montré qu’une forte teneur en K+ dans le sol fait diminuer la concentration en Mg des feuilles de la PDT, ils ont supposé que cette diminution est due à une diminution de cet élément dans la solution du sol et par la suite à une mauvaise absorption de Mg par la plante. Dans le guide du CRAAQ (2010) la fertilisation potassique de la PDT a été ajustée en fonction de l’analyse du sol en Mg Mehlich 3, si elle dépasse 101 kg Mg ha-1, une carence peut survenir en raison d’un antagonisme du potassium envers le magnésium.
Lorsque l’application de K augmente, la concentration de Mg dans les pétioles diminue (Hossner et Doll 1970 et Giroux, 1987). Walsh et O’Donohoe (1945) prouvent qu’en absence de fertilisant Mg, l’augmentation des doses de K de 105 à 264 Kg K ha-1 diminue le rendement en tubercules de 25 à 22 t ha-1 mais ils n’ont pas prouvé si l’application du fertilisant Mg peut alléger cet effet. Hossner et Doll (1970) ont montré que l’augmentation de la quantité appliquée de K de 200 à 665 kg K ha-1 augmente les besoins en Mg de 56 kg Mg ha-1.
Johnston et Goulding (1992) ont montré qu’une quantité de 1 kg K+ ha-1 est perdue pour chaque 100 mm de précipitations filtrées à travers le sol, mais cette valeur serait plus importante si K+ a été déplacé en utilisant une solution riche en ions Ca2+. Jalali et Rowell (2003) ont prouvé aussi qu’une faible quantité de K+ est lixiviée à travers le sol avec une solution à faible concentration en CaCl2, mais l’augmentation de la concentration de Ca2+
dans la solution lixiviante augmente la concentration de K+ dans le lixiviat, ce qui montre encore cet effet d’antagonisme entre ces deux éléments.
Ces antagonismes entre les différents éléments nutritifs du sol sont à l’origine de la perturbation de l’équilibre de l’absorption de ces éléments et par la suite de l’équilibre de ces éléments dans la plante. Fontes et al. (1996) ont trouvé qu’une concentration élevée de K dans le sol engendre une diminution du poids des tubercules et des pousses. Ils ont
19
montré aussi que dans le cas où la concentration du K est déficiente, la faible croissance est due à une absorption réduite de K à cause de l’interaction avec de forte concentration en Ca et Mg. Panique et al. (1997) ont montré que l’augmentation de l’application de K diminue le poids spécifique de la pomme de terre bien que des diminutions ne sont généralement pas aussi marquées en utilisant K2SO4.
Les interactions entre les éléments nutritifs ont été considérées comme des sujets de recherches très importants. Madramootoo et al. (1992) ont attribué l’augmentation de la concentration de K dans les eaux de drainage à une possibilité d’interaction avec NH4+ vu
21
Chapitre 3. Hypothèse et objectifs de recherche
3.1. Hypothèse de recherche
La fertilisation azotée (doses et sources de N) de la PDT au Québec a une influence sur la lixiviation du potassium dans les sols minéraux.
3.2. Objectifs de recherche
Les objectifs de ce travail sont : i) l'étude de l'effet de différentes sources et doses d'azote sur la lixiviation du potassium dans des sols sableux sous culture de pomme de terre irriguée et ii) l'élaboration des patrons de lixiviation de potassium durant le cycle végétatif de la pomme de terre, comme outil d’aide au fractionnement des engrais potassique et iii) l’établissement d’un bilan potassique par parcelle expérimentale pour une meilleure estimation des pertes par lixiviation du potassium.
23
Chapitre 4.
Matériels et méthodes
4.1. Présentation du site
4.1.1. Localisation et description
Le site expérimental se situe dans la ville de Sainte-Catherine de la Jacques-Cartier traversée du nord au sud par la rivière Jacques-Cartier (figure9). Connue par ses sols sableux et la bonne qualité d’eau (Hébert, 2006), cette région est propice pour la culture de pomme de terre. Le site est conduit sous irrigation et la variété utilisée est le cultivar Russet Burbank destiné au marché de la transformation.
Figure 9. Localisation géographique du site expérimental (46°50’30’’ N, 71°38’20’’ O) (Google maps)
En 2010 et 2012 notre site expérimental est localisé dans le champ A, il s’agit d’un sol de la série Morin, en 2011 notre site est localisé dans le champ B. Le changement de site est essentiel pour le respect des rotations appliquées à la ferme et le déplacement du système d’irrigation qui est de type pivot. Le sol du champ B est un sol de la série Pont Rouge caractérisée par une présence plus importante de gravier et un drainage plus rapide que la série Morin du champ A. Selon la classification canadienne ce sont tous deux des podzols humo-ferriques caractérisés par une texture qui varie de loam sableux en surface à sable en profondeur. Le cycle végétatif de la pomme de terre est très court, il dure seulement trois à quatre mois. Les dates de la plantation et de la récolte (tableau 3) varient selon les conditions climatiques et édaphiques du site, pour les années 2010, 2011 et 2012.
Champ B
24
Tableau 3. Dates de plantation et de récolte
Année 2010 2011 2012
Date de plantation 10 mai 25 mai 14 mai Date de récolte 20 septembre 26 septembre 24 septembre
La récolte de la pomme de terre est faite sur 6 m de long prélevé sur le deuxième rang de la parcelle, elle est réalisée mécaniquement à l’aide d’une récolteuse à pomme de terre.
4.1.2. Climat
Cette région est caractérisée par un climat continental humide avec un été tempéré. Le suivi des données climatiques telles la température et la pluviométrie est essentiel à l’étude de la lixiviation du potassium. C’est pourquoi, il a eu installation d’une station météo de type HOBO au site expérimental. Cette dernière est composée d’un capteur de vitesse du vent, d’un écran de mesure des radiations solaires, d’un pluviomètre, d’un thermomètre. Les mesures sont enregistrées à chaque 10 minutes et sont ensuite sauvegardées dans des fichiers de données.
4.1.3. Caractérisation pédologique et physico-chimique des sols
des sites expérimentaux
À l'automne précédent le semis, une prospection pédologique du site expérimental (un pédon par bloc) a été faite pour déterminer la série de sol présente sur le site et dans chaque pédon, un échantillonnage de sol est fait pour déterminer la texture du sol pour les horizons Ap, Bf ou Bhf et C (tableau 4). La texture du sol varie du sable loameux au sable, le drainage est généralement bon à modérément bon et la perméabilité est bonne. À la même période, un échantillonnage composite de 12-15 carottes de sol de surface (0-20 cm) prélevé avec une tarière hollandaise de 5 cm est aussi effectué pour chaque bloc du dispositif expérimental. Cet échantillonnage a servi à établir les caractéristiques physico-chimiques (tableau 5).
25
Tableau 4. Textures des sites expérimentaux dans les deux champs A et B
G : texture grossière regroupant les loam sableux, sable loameux et sable (CRAAQ, 2010)
Tableau 5. Caractéristiques physico-chimiques des 20 premiers centimètres des sols des sites expérimentaux
Les éléments P, K, Mg et Ca sont dosés par spectrométrie d’émission au plasma (ICP) après extraction au Mehlich 3 (Ziadi et Sen Tran, 2007). Pour déterminer le pourcentage de la matière organique on a utilisé la méthode Walkley Black (Walkley et Black, 1934). Un ratio de 1:1 est utilisé pour mesurer le pH eau et la méthode SMP a permis de mesurer le pH tampon (Shoemaker et al., 1961). La capacité d’échange cationique est estimée à partir des bases échangeables mesurées.
Site Série du sol
Classification
canadienne Horizon
Argile Limon Sable Groupe textural %
Champ A
(2010-2012)
Morin Podzol humo-ferrique Ap Bf C 5,9 3,8 2,8 16,3 7,3 5,7 77,9 88,8 91,5 G3 Champ B (2011) Pont Rouge Podzol humo-ferrique Ap Bhf C 5,5 3,9 2,0 15,8 10,9 2,5 78,7 85,2 95,5 G3 2010 (Champ A) Bloc
pH eau SMP pH CEC MO Ca Mg K P Al P/Al
Meq/100g % ---kg ha-1--- mg kg-1 % Moyenne 5,40 5,90 9,93 4,85 1800 43 232 533 2018 11,9 Ecart type 0,14 0,08 0,75 0,51 424 17 37 100 111 2,8 CV (%) 2,62 1,38 7,56 10,45 24 41 16 19 5,5 23,5 2011 (Champ B) Bloc pH eau pH SMP CEC MO Ca Mg K P Al P/Al Meq/100g % ---kg ha-1--- mg kg-1 % Moyenne 5,3 5,9 9,1 5,5 1375 34 190 510 2125 10,7 Ecart type 0,06 0,05 0,5 0,3 96 24 12 50 47 1,2 CV (%) 1,1 0,9 5,6 5,9 7,0 69,5 6,1 9,9 2,2 11,1 2012 (Champ A) Bloc pH eau pH SMP CEC MO Ca Mg K P Al P/Al Meq/100g % ---kg ha-1--- mg kg-1 % Moyenne 5,3 5,8 11,1 4,8 1625 31 324 521 1925 12,2 Ecart type 0,21 0,18 0,5 0,7 222 16 66 78 86 2,2 CV (%) 4,0 3,1 4,8 14,8 13,6 52,4 20,5 14,9 4,5 17,9
26
4.2. Dispositif expérimental
Le dispositif expérimental du site est un bloc complet aléatoire de quatre répétitions constitué de 10 traitements. Les traitements sont un factoriel de trois sources d’engrais azotés (nitrate d’ammonium, sulfate d’ammonium et un engrais à libération lente) et de trois doses de N (120, 200 et 280 kg de N ha-1) et d’un témoin sans engrais N (tableau 6). Les engrais potassiques sont appliqués d’une manière uniforme à raison de 230 kg K2O
ha-1. Les parcelles sont réparties sur 0,5 ha, chacune ayant 8 m de long et 5,5 m de large (6 rangs espacés de 0,91 m).
Tableau 6. Traitements de fertilisation potassique et azotée
Nitrate d’ammonium NH4NO3 (34-0-0) : il contient habituellement 98,5 % de
NH4NO3, 1 % d’enrobant et 0,5 % d’humidité (Khiari, 2012). C’est un engrais à action
rapide grâce à sa solubilité et à sa composition, l'azote est assimilé par les racines sous forme de nitrates (NO3-) ou, parfois, d'ions ammonium (NH4+). Ces derniers sont retenus
par le complexe d’échange des sols et sont peu susceptibles à la lixiviation par contre les ions nitrates sont très mobiles et sont facilement lixiviés.
Sulfate d’ammonium (NH4)2 SO4 (21-0-0) : il est la source la plus ancienne d’azote
ammoniacal ; il a une concentration en soufre de 24 %. Son principal désavantage est que
Fertilisation azotée
Fertilisation potassique Dose de K2O
(kg ha-1) Id Source (kg haDose N -1)
Fractionnement % Pré-semis Plantation
Plantation Buttage KCl KCl Kmag
T 1 Témoin - - - 170 30 30 T 2 T 3 T 4 NAz 120 200 280 40 40 40 60 60 60 170 30 30 T 5 T 6 T 7 SAy 120 200 280 40 40 40 60 60 60 170 30 30 T 8 T 9 T 10 ESNx 120 200 280 100 100 100 0 0 0 170 30 30 zNA : Nitrate d'ammonium; ySA: Sulfate d'ammonium; xESN : Engrais à libération lente.
27
c’est l’engrais azoté le plus acidifiant (Fortin, 2011). L’azote est à 100 % sous forme ammoniacale.
Le NA et le SA sont des engrais ammoniacaux. "Ils sont acidifiants à long terme parce qu'ils produisent, en présence d'eau, des ions NH4+ qui, par nitrification, se transforment
en NO3- en libérant des ions H+" (Fortin, 2011).
Engrais à libération lente ESN (46-0-0) : est un engrais commercial composé de granules d'azote recouverts d'une mince pellicule de polymère. Cette pellicule est conçue pour retarder la libération de l'azote jusqu'à ce que le sol soit à une température assez élevée et atteigne un certain niveau d'humidité. Ainsi, l'azote ne sera libéré que lorsque les cultures seront susceptibles de bien l’absorber (Agrium Inc, 2014).
Les engrais azotés sont tous fractionnés de la même manière, soit 40% lors de la plantation et 60 % lors du buttage, à l’exception des engrais à libération lente qui sont apportés en une seule fois lors de la plantation car il faut prévoir plus de temps avant leur disponibilité pour la plante.
L’engrais potassique est le muriate blanc de potassium KCl (0-0-62). Il a été fractionné de la manière suivante, 170 kg ha-1 avant la plantation, à la volée. Ensuite à la plantation, on ajoute 60 kg ha-1, 50 % sous forme K-mag (0-0-22, 11 % Mg et 22 % S) et 50 % sous forme KCl.
Les engrais phosphorés sont appliqués en bande lors de la plantation et les doses sont ajustées en fonction des recommandations en vigueur au Québec (CRAAQ 2010).
4.3. Extraction et dosage de la solution du sol
La solution du sol est extraite à l’aide de bougies poreuses installées au centre de butte ensuite analysée pour doser les différents éléments chimiques. Le principe de cette méthode repose sur l’utilisation d’une coupelle en céramique poreuse installée au bout d’un tuyau de polychlorure de vinyle de 90 cm de long et de 4,8 cm de diamètre (modèle 1900, Soilmoisture equipment corp, 2007). Ils sont placés dans le sol à la profondeur désirée à 90 cm. L’installation se fait par le creusage d’un trou à l’aide d’une tarière hollandaise de 5 cm de diamètre, puis on replace le sol retiré du trou en le tassant pour s’assurer qu’il ait un bon contact entre le tube et le sol et éviter l’infiltration préférentielle de l’eau.
28
Les bougies poreuses ont été installées sur le deuxième rang de chaque parcelle, ce qui fait un total de 40. On maintien les lysimètres sous tension de la plantation à la récolte des pommes de terre. Chaque deux semaines, on récupère l’eau des lysimètres et on les remet sous une tension de 70 cbar. Le tuyau à col rouge permet de vider le lysimètre de son eau, l’autre permet de le vider de son air et ce à l’aide d’une pompe (figure 10). La solution du sol est mise dans des flacons en plastique pour être ensuite analysée au laboratoire. Les échantillons de la solution du sol sont immédiatement congelés et décongelés au moment de leur analyse au laboratoire. À chaque année, neuf collectes de la solution de l’eau du sol ont été effectuées (tableau 7).
Figure 10. Installation des lysimètres
Tableau 7. Calendrier de collecte de l'eau des lysimètres
Le potassium dans la solution du sol est dosé par spectrophotométrie d'absorption atomique (Ziadi et Sen Tran, 2007) (SpectrAA modèle 220FS). Le spectrophotomètre permet de quantifier le niveau d’absorption par une solution d’une lumière à une longueur d'onde prédéterminée (766 nm pour le K). L’appareil est ajusté pour isoler cette
29
longueur d'onde et la diriger vers un détecteur qui mesure l’intensité lumineuse qu'il reçoit, ainsi à cette longueur d’onde précise il y a autant d’intensité lumineuse émise et détectée qu’il y a de K dans la solution analysée.
4.4. Échantillonnage et analyse du potassium du sol
Au niveau du sol les analyses ont été faites sur les parcelles ayant reçu soit 0 et 200 kg ha-1 d'azote qui est la dose jugée optimale pour la nutrition azotée de la pomme de terre. L’échantillonnage du sol est fait trois fois par cycle agricole (avant le semis, juste après la récolte et le printemps suivant). En pré-semis, il a été fait avant l'application du potassium. Il consiste à creuser trois trous par parcelle en utilisant une tarière hollandaise de 5 cm de diamètre. Le composite des trois trous correspondant à chaque profondeur est mélangé dans un seau en plastique puis conservé dans des sacs en plastique et gardé à un endroit frais et sec après le séchage à l'air.
Les prélèvements ont été faits pour 4 profondeurs différentes (0-15, 15-30, 30-60 et 60-90 cm). L'extraction des éléments nutritifs est réalisée en utilisant la solution extractive Mehlich 3 (Ziadi et Sen Tran, 2007) et pour les doser on a utilisé la méthode de spectrométrie d’absorption atomique. L’extractif Mehlich 3 dose la somme des formes solubles et rapidement échangeables (facilement disponibles à la plante) et non le K de réserve (Simard et al., 2001). Pour calculer la quantité de K dans le profil du sol en kg ha-1, on a mesuré la masse volumique apparente selon la méthode des cylindres (Hao et
al., 2007) pour 4 profondeurs différentes (0-15, 15-30, 30-60 et 60-90 cm) (figure 11).
Figure 11. Échantillonnage des cylindres pour la détermination masse volumique apparente
30
4.5. Bilan partiel du potassium dans le sol
La détermination du bilan de K dans le sol permet de prévoir les doses à apporter par culture et type de sol et même le fractionnement de ces apports. Elle nécessite une connaissance quantitative des processus gérant cet élément nutritif.
Stock final du sol = stock initial du sol + entrées – sorties (1)
Les entrées sont présentées par les dépôts atmosphériques, les apports sous forme d’engrais et les résidus de la culture précédente. Les sorties sont sous forme de prélèvement par la plante, fixation par le sol et pertes par lixiviation. Pour faciliter le calcul on peut négliger les dépôts atmosphériques et les apports par les résidus de culture ainsi que la partie fixée.
Les prélèvements de la plante sont évalués en dosant le potassium dans la plante (biomasse aérienne et tubercules) à la récolte. Nous avons récolté le deuxième rang de PDT (tubercules et biomasse aérienne) par parcelle. Un échantillon représentatif de six tubercules de chaque parcelle a été sélectionné, coupé en lanières de 1 cm, pesé, séché dans un séchoir à air forcé à 558 C et repesé pour déterminer la teneur en matière sèche (Cambouris et al., 2007). Les échantillons de tubercules séchés sont ensuite broyés. L'extraction et le dosage du K dans les plantes sont effectués selon la méthode de digestion (Isaac et Johnson, 1980).
4.6. Méthodes statistiques
Les analyses de variance ont été effectuées avec la procédure MIXED sur le logiciel SAS, qui permet d'analyser des mesures répétées et toute une suite de contrastes déterminés à priori (SAS Institute, 2004). Les effets fixes sont les sources, les doses et les périodes d’échantillonnage, les effets aléatoires sont les blocs. Cette procédure est conçue pour analyser des effets mixtes et non seulement les modèles linéaires standards, elle est également plus robuste pour tenir compte des données manquantes sans éliminer les sujets concernés. Les données ont été compilées sur le logiciel EXCEL (Microsoft Excel, 2007).
31
Chapitre 5.
Résultats et discussion
5.1. Conditions pluviométriques et irrigation
L’année 2010 est caractérisée par une faible pluviométrie pour les mois de mai, juin, juillet et août, nettement inférieure à la normale de 30 ans (figure 12). De ce fait, pendant le mois de juillet, il a eu quatre irrigations de 22 mm chacune, suivies de deux irrigations en août. Ce n’est qu’au mois de septembre que la pluviométrie était même plus élevée que la normale de 30 ans. La saison de culture 2011 était plus pluvieuse, surtout au mois d’août (figure 12). Donc il y a eu recours à une seule irrigation d’appoint de 22 mm au début du mois d’août. L’année 2012 était chaude et sèche surtout dans les mois de stress hydrique les plus critiques (juillet et août) (figure 12). On a eu recours à trois irrigations d’appoints de 22 mm chacune en juillet et trois autres au mois d’août 2012.
Figure 12. Comparaison entre la quantité mensuelle de précipitation mesurée sur le site expérimental en 2010, 2011 et 2012 et la normale de 30 ans et quantité d’eau apportée sous forme d’irrigation
0 50 100 150 200 250 300 350
mai juin juillet août septembre
2010 2011 2012 Normale de 30 ans P luv iom étrie ( mm ) X 4 X 2 X 1 X 3 X 3 0 50 100
Mai Juin Juillet Août Septembre
Do se d 'irr igat ion (mm ) Mois 2010 2011 2012
32
5.2. Mesure du potassium dans la solution du sol
La solution du sol a été récupérée chaque deux semaines à l'aide des lysimètres installés dans chaque parcelle. Le tableau des contrastes pour les années 2010, 2011, et 2012 (tableau 8) nous a permis de constater un premier effet significatif de la période en jours après la plantation (JAP), ce qui veut dire que la quantité de K lixivié en fonction du cycle de la PDT est variable pour les trois années. En ce qui concerne l'année 2010, on remarque qu'il y a une tendance significative pour l'interaction source X JAP avec une valeur de p de 0,04, ce qui veut probablement dire que l’ordre du plus grand au plus petit est variable d’une date de mesure à l’autre. Par exemple, pour la première date d'échantillonnage, on a eu une quantité de K lixivié plus importante avec la source NA (82 mg l-1) comparé à SA (69 mg l-1) et ESN (51 mg l-1). À la deuxième date c'est le ESN qui l'emporte et par après c'est le SA qui donne toujours des fortes doses de K lixivié (annexe 1). En 2011, le tableau des contrastes montre qu'il y a un effet significatif de l’interaction dose X source, puis il y a une tendance significative pour l'interaction triple dose X source X JAP. Le graphique (figure 13) montre bien un effet linéaire de la dose avec le ESN et un effet quadratique pour les deux autres sources de N. En 2012, on n’observe aucun effet significatif pour les différentes interactions.
Tableau 8. Résultats d’ANOVA des différentes interactions pour les 3 années 2010-2012
zDDL : Degré de liberté
y : Dose de N (120, 200 et 280 kg de N ha-1) X : Source de fertilisants azotés NA, SA et ESN wJAP : jours après la plantation
v*, **, *** : significatif à 0,05, 0,01 et 0,001
Libellé DDLz 2010 2011 2012
Valeur F Pr > F Valeur F Pr > F Valeur F Pr > F
Dosey 2 1.01 0.375 2.39 0.108 0.10 0.901 Sourcex 2 0.28 0.754 0.22 0.803 0.08 0.925 JAPw 8 40.41 <.0001***v 8.45 <.0001*** 18.21 <.0001*** Dose* source 4 0.07 0.990 4.12 0.008** 0.31 0.866 Dose*JAP 16 1.22 0.253 0.47 0.957 0.82 0.663 Source*JAP 16 1.74 0.041* 0.92 0.546 1.07 0.383 Dose*source*JAP 32 1.13 0.301 1.51 0.046* 1.08 0.360
33
Figure 13. Relation entre la moyenne des concentrations de K (mg L-1) dans les lysimètres et la dose totale d’azote (kg ha-1) appliquée en fonction de la source d'azote (NA : nitrate d'ammonium, SA : sulfate d'ammonium, ESN : engrais à libération lente) lors de la saison 2011
Les teneurs moyennes de K, dans la solution du sol, lixivié par différentes sources de N varient en fonction du cycle végétatif de la plante. En 2010, la moyenne de la concentration de K dans les lysimètres durant tout le cycle de développement de la plante est plus importante avec le sulfate d'ammonium (31 mg L-1) (tableau 9) par rapport aux autres sources, de même elle est plus importante pour la dose 280 kg ha-1 (36 mg L-1), ce qui est en accord avec notre hypothèse. Les valeurs enregistrées pour le traitement témoin (1) sont plus importantes que les différentes sources de N (33 mg L-1).
Pour les différentes sources de N, on remarque très bien que la dose 280 kg ha-1 donne plus de K lixivié que les doses plus faibles. Par exemple pour le nitrate d'ammonium, on obtient une moyenne de 23 mg l-1 de K lixivié avec la dose 120 et 40 mg l-1 avec la dose 280 kg N ha-1 (tableau 9).
En 2011, les concentrations moyennes de potassium lixivié en fonction de la source de N varient de 10 à 22 mg l-1 pour toutes les sources et on ne remarque pas une très grande variation entre les différentes sources, avec une moyenne aux alentours de 17 mg l-1. La seule remarque qu’on peut faire est que les valeurs maximales sont 2 à 3 fois plus petites que celles de 2010 et 2012. Cette fois on remarque, qu'au départ et jusqu'à 58 JAP, le
10 15 20 25 120 200 280 K ( m g L -1) Dose N (kg ha-1) NA SA ESN