HAL Id: dumas-01685856
https://dumas.ccsd.cnrs.fr/dumas-01685856
Submitted on 16 Jan 2018HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Intérêt de la pression expiratoire positive variable dans
la stabilisation des voies aériennes supérieures au cours
de la ventilation non invasive nocturne
Loïc Leray
To cite this version:
Loïc Leray. Intérêt de la pression expiratoire positive variable dans la stabilisation des voies aériennes supérieures au cours de la ventilation non invasive nocturne. Médecine humaine et pathologie. 2017. �dumas-01685856�
UNIVERSITE DE NICE SOPHIA-ANTIPOLIS
FACULTE DE MEDECINE DE NICE
THESE
Pour l’obtention du Diplôme d’Etat de
Docteur en Médecine
Présentée et soutenue publiquement à la Faculté de Médecine de Nice
Le Lundi 16 octobre 2017
Par
Loïc LERAY
Né le 27 mars 1989 à Cannes (06) Interne de D.E.S. de Pneumologie
INTERET DE LA PRESSION EXPIRATOIRE POSITIVE VARIABLE DANS LA
STABILISATION DES VOIES AERIENNES SUPERIEURES AU COURS DE LA
VENTILATION NON INVASIVE NOCTURNE
Devant le jury composé de :
Monsieur le Professeur Charles-Hugo MARQUETTE, Président du jury
Monsieur le Professeur Georges LEFTHERIOTIS, Assesseur
Madame le Professeur Sabrina SACCONI, Assesseure
Remerciements,
« A cœur vaillant, rien d’impossible »
Jacques Cœur
« C’est un sport d’équipe, t’es pas seul en scène. » Remember the Titans
A notre Maître et Président du Jury,
Monsieur le Professeur Charles-Hugo MARQUETTE,
Vous me faites l’immense honneur de présider ce jury de thèse.
C’est un privilège d’apprendre à travailler à vos côtés.
Vos compétences professionnelles font de vous un exemple.
Je vous remercie de l’écoute et des conseils que vous m’avez prodigués tout au long de ces quatre années.
A notre Maître et Juge,
Monsieur le Professeur Georges LEFTHERIOTIS,
Vous me faites l’honneur de juger ce travail de thèse,
Je sollicite votre expertise dans le domaine de la physiologie,
A notre Maître et Juge,
Madame le Professeur Sabrina SACCONI,
Vous me faites l’honneur de juger ce travail de thèse,
Je regrette de ne pas avoir eu le plaisir de travailler avec vous.
Votre expertise scientifique et vos compétences sont unanimement reconnues.
A mon Directeur de Thèse,
Monsieur le Docteur Christophe PERRIN,
Vous m’avez fait l’honneur de diriger cette thèse, et je vous remercie de m’avoir confié ce travail qui nous tenait tant à cœur.
Je vous remercie de la bienveillance dont vous avez fait preuve à mon égard dès le premier jour.
Mon intérêt pour le sommeil a débuté à vos côtés, durant de longues heures devant nos écrans d’ordinateurs.
Malgré un choix professionnel vous engageant à un dur labeur dans un autre pays, vous ne m’avez pas mis de côté et avez été présent pour ce projet.
A mes maîtres d’internat,
Docteur Fernand MACONE, le chef, l’âme du H. Tout d’abord merci pour votre présence, votre soutien (notamment pendant les premières gardes), votre enseignement et votre gentillesse. Votre Harley, votre côté bad-boy et votre mauvaise humeur matinale sont reconnus dans tout le CHU. Nous avons eu notre part de désaccord. Mais malgré tout, vous êtes le médecin de terrain, celui qui est dans le service de 7h à 22h, toujours présent au moindre problème que ce soit pour les internes ou les IDE. Je n’imagine pas mon internat sans vous. Sachez que je vous apprécie en tant qu’homme et en tant que médecin. Recevez par ces quelques mots mon plus grand respect.
Docteur Sylvie LEROY, Merci pour toutes ces connaissances que vous m’avez apprises. Vous êtes pour moi l’une des personnes les plus intelligentes que j’ai été amené à rencontrer. Vous avez même réussi à me faire apprécier l’allergologie et c’était loin d’être gagné. Je vous souhaite tout le courage et la réussite pour vos futurs projets. Recevez ma sincère reconnaissance.
Docteur Céline SANFIORENZO, merci de ton soutien et de ton enseignement durant ces quatre années.
Docteur Sylvia KORZENIEWSKI, tu m’as connu au tout début, et déjà externe tu me recadrais. J’ai beaucoup apprécié travailler avec toi, je te remercie pour ton enseignement, ta patience. Je te souhaite plein de réussite pour ce nouveau départ.
Docteur Johanna PRADELLI, il y a tellement de choses à dire. Travailler avec toi est un immense plaisir, toujours prête à rendre service, toujours une réponse à un problème et bien entendu dans la bonne humeur (je ne le dirai pas sur du Maitre Gimms mais pas loin). Tu es le 4x4 du H comme on aime te le rappeler, tu sais tout faire. En mettant de côté tes compétences qui ne sont pas discutées, tu es avant tout quelqu’un que j’apprécie, avec ta moue boudeuse et nos éclats de rire. Merci pour tout, et félicitation pour ton futur Zidane !
A la merveilleuse équipe de pneumologie de Nice, vous m’avez beaucoup appris surtout dans mes débuts. Merci à vous pour votre soutien, votre patience, votre bonne humeur et rigolade ! Vous avez égaillé mon internat, et rendu ces longues journées moins difficiles !
Au CH de Cannes,
Docteur Yannick DUVAL, merci « DUDU » ou monsieur Force Calme. J’ai eu la chance d’apprendre à
tes cotés. Ton empathie, tes connaissances et ton sérieux font de toi un modèle. Malgré tes compétences footballistiques plus qu’hasardeuses, je serai heureux de pouvoir travailler avec toi dans le futur (si c’est toujours bon après ces remerciements !).
Docteur Fabien ROLLAND, merci pour tout ce que tu m’as appris. Tu as une vision de la pneumologie
très universitaire que j’admire. Ta connaissance s’étend même aux noms propres et signes cliniques inconnus (par le grand public). Je te remercie aussi pour ton aide et ton soutien dans ce travail mais aussi pour la rédaction du mémoire de DES. Je suis très heureux d’avoir eu l’opportunité de travailler avec toi. J’espère que ce n’est que le commencement (si tu ne deviens pas millionnaire entre temps).
Docteur Florence LEMEUNIER, ta bonne humeur, ta rigueur facilitent le travail avec toi. Tu as
grandement aidé mon intégration au sein du CH de Cannes. Tes connaissances en infectiologie et endoscopies m’ont été précieuses. C’est une chance de te connaître.
Docteur Alexia SETIEN, merci de ta gentillesse et de ton soutien au cours de ce dernier stage. J’espère
que tu arriveras à surmonter ta faim incessante (de 8h30 à environ 18h quotidienne).
A l’équipe de Cannes, c’est un plaisir de travailler avec vous ! A tel point que vous me reverrez bientôt !
Aux co-internes,
A Linda, pour nos misères partagées ! Merci de m’avoir laissé diffuser mon stress durant cette dernière ligne droite.
A Jérémy, Juliette, merci pendant ces 6 mois de m’avoir facilité la vie pour ce travail. A Jérémy bonne chance pour ton projet (on sera surement amener à travailler ensemble) et princesse Juliette, courage l’internat c’est pas si long !
Aux plus anciens,
Martin (AKA Mémé), il en a des choses à dire, cela fait 15 ans qu’on se connait et je t’ai apprécié dès
le 1er jour. Nous nous sommes construit et avons évolué ensemble. On s’est même envoyé en l’air. Je
te remercie surtout pour avoir toujours été là pour moi que ce soit dans les bons ou les mauvais moments. Tu fais partie de ces amis que l’on compte sur les doigts d’une main. Merci d’être toi, de m’avoir supporté et accompagné jusque-là.
A Tigrou, Petit Xav, je me rappelle encore de la 5ème, le bras droit de Robert avec ta banane Quicksilver.
Le petit teigneux avec toujours le mot pince sans rire. Un basketteur de petite taille mais de haut niveau. On s’est suivi tout au long de nos études et malgré ton départ sur Paris, on est toujours aussi proche. C’est un honneur de participer à ton futur mariage. Je te souhaite tout le bonheur possible avec ta Caro, et sache que l’EVG va être inoubliable !
A Corbo, un ami depuis plus de 10ans. On se voit moins mais lorsque c’est le cas rien ne change. Je te remercie pour toute ces années de délires.
A Emilie, bécassine, une logorrhée à toute épreuve ! Tu fais partie de la famille, vous vous êtes avec Jessica mutuellement aidées dans les moments difficiles. Je te remercie pour ça mais aussi pour ta gentillesse et ton humour. Je te souhaite sincèrement d’être heureuse.
Aux collocs,
A Xav, la machine, le surhomme, grand cake, on en a vécu des choses ensemble, de l’Afrique du Sud, en passant par NY et le Canada. De ma sous colle privée personnelle de la P1 aux sous colles acharnées de la D4. Avec même une finale de basket de l’université et à la collocation… En tout cas je te remercie de m’avoir accompagné tout au long de ce parcours. Tu as rencontré ton âme sœur avec la petite sportive gwendo, je vous souhaite plein de bonheur.
A Alexis, colloc, capable du meilleur comme du pire, un temps boudeur et un temps euphorique. Malgré tes colères au ping pong, tu es quelqu’un d’attachant, toujours à l’écoute et de bon conseil. Tu fais partie des 2 personnes avec lesquelles « je me suis envoyé en l’air » (self control). Tu as rencontré
Alice qui te comble de bonheur (7 wonders). Je vous souhaite le meilleur.
A Clément, mon coco (co-interne/colloque), on a fait nos 10 ans d’études ensemble, on a tout partagé, nos déboires nos coups de gueules et surtout plein de bons moments. La pneumologie sans toi aurait été moins intéressante. Je te félicite encore pour ton parcours et je suis sûr que tu feras de grandes choses. Je te souhaite plein de réussite pour ton séjour aux Antilles. En un mot tu es, incroyable.
Peskett, Qui aurait cru que cet homme venu de la profonde campagne, aux chemises à carreaux serait
l’icône emblématique de la Peskett Team. Ta répartie et ta facilité d’élocution en sont pour quelque chose (le comble pour un chirurgien…) Tu es simple, généreux et toujours prêt à rendre service. Je suis heureux d’avoir partagé ces études avec toi. Tu nous abandonnes pour Manue, l’athlète, avec son petit caractère mais aussi sa gentillesse et sa douceur. Vous allez tellement bien ensemble, je ne vous souhaite que du bonheur.
A Polo, la révélation de l’internat. Tu es une personne à part, ton soutien et nos délires ont été très importants pour moi. Merci d’avoir été mon martyre au squash, mon coéquipier au foot, et mon compagnon de soirée. Je te souhaite plein de bonheur ! Océane, le petit rondoudou de Polo, une infirmière hors pair. Tu apportes beaucoup aux patients par ta bonne humeur et ton sérieux. Je suis triste que tu nous quittes pour la réanimation, j’espère qu’ils t’apprendront mieux que moi à apporter le café.
A l’ancienne colloc, pour Kevin qui m’a charrié avec son PSG, Cyril le geek de MPG, et Luigi le prodige (« bizarre ? »). J’espère que l’on continuera à se voir, ces 6 mois ont été courts, et m’ont permis de rencontrer des personnes formidables.
A la Peskett TEAM,
A Luluzub, la personne la plus déjantée que je connaisse, un rythme dans la peau unique. Je me rappelle encore de ce buffle au Kruger qui ne demandait rien à personne... A côté de ça, tu as réalisé le 1er mariage de la peskett et ce n’est pas rien. Tu as déjà l’ambition d’être père et c’est tout ce que je
te souhaite. J’espère qu’on se retrouvera dans la région (pour un ptit call of !) avec tes futurs petits ninoutes.
A Réda, l’escroc, l’homme qui savait tout faire (mais vraiment tout). Sans conteste l’une des personnes les plus douées que je connaisse et surtout un ami de route formidable.
A La Viv, le sportif, le combattant. Pour ton sens des valeurs, ton amitié et ton écoute. Je te souhaite plein de bonheur avec ta petite Chloé et … ?
A Maxime, picoloLucho, l’enfant du groupe. Toujours le 1er à faire n’importe quoi (on s’en souviendra
de cette soirée PT…). Tu as grandement contribué à la bonne ambiance du groupe, j’espère te revoir dans les parages le plus tôt possible.
A Trompette, Gicien, tu as toujours eu la potion magique pour me remonter le moral. Tu as été présent dans les moments difficiles. Je ne te remercierai jamais assez pour ça. Bref un mec en or !
A Pedro, j’ai beaucoup apprécié nos longs débats philosophiques de fin de soirées, la fameuse création de l’agence tout risque, mais surtout ta protection contre les consanguins de la Marne. Je te souhaite la vie d’aventurier que tu désires tant.
Philou, le Corse, un style de danse à part lors de ces nombreux Critchinis, un record absolu au 1er…
Merci pour ta gentillesse et ton amitié. Tu nous abandonnes pour Bastia, mais je suis certain que tu as fait le bon choix et que tu y seras heureux.
Aux filles de la Peskett, Lilou la maman, Margaux la princesse, Mathilde la clubbeuse et jojo, on a tant partagé ensemble. Merci d’avoir un peu amené de féminité à notre groupe.
Aux amis,
A Remy, j’ai appris à te connaître au tout début de mon internat, tu es quelqu’un d’exceptionnel par
ta gentillesse, ton humour et ta simplicité. Tu supportes peut-être la mauvaise équipe (Dague Munegu), mais sache que je n’aurai de cesse de te remettre dans le droit chemin.
A Lucille, tu es quelqu’un sur qui l’on peut vraiment compter. La maman qui nous a canalisés durant cette année au BDE. Je suis très heureux de t’avoir parmi mes amis. Tu es maintenant responsable de BB chat et ce boulot te va à merveille. Votre couple est un modèle pour tous.
A Doudou, mousse, un mec à part, souriant, sociable, attachant. Tu t’es intégré à notre groupe en un instant, et j’en suis très heureux. Je te souhaite 6 bons mois chez les helvètes, et si tu recherches vraiment le bonheur avec Lorène, commence par changer d’équipe à supporter.
A Ceka et Caro, le couple parfait par excellence. Je vous souhaite du courage à Nancy !
A Julie et Faf, bravo encore pour la petite Louise, je suis sûr que vous ferez des parents formidables. Je suis impatient de vous revoir dans la région.
A ma famille,
A maman, (chérie d’amour ?) une mère « presque » parfaite, toujours présente, toujours prête à résoudre n’importe quel problème quel que soit l’heure. Sans parler des relectures en urgence pour les fautes d’orthographes ! Si j’en suis là ce soir c’est en grande partie grâce à toi, avec ton soutien sans faille. Tu sais que je ne suis pas très doué pour exprimer mes sentiments, mais tu sais aussi que je t’aime.
A papa, jean, merci pour ton soutien considérable. Ta faculté à prendre plaisir à rendre service m’impressionnera toujours. Tu m’as épaulé tout au long de ces études et en dehors. Je te remercie pour tout ça, mais aussi pour les valeurs que tu m’as transmises notamment ta force calme et le fait de voir toujours le bon côté des choses.
A Jessica, ma petite sœur chérie. Tu m’en a fait voir de toute les couleurs depuis que je suis tout petit. Mais tu as toujours été d’un grand soutien dans les moments difficiles. Je sais que ce n’a pas été facile ces derniers temps, mais j’admire ta manière d’avancer. Te voilà maintenant mère de 2 adorables petites filles. Alyssia, la petite reine des neiges déjà grande et intelligente, Cléa la filleule parfaite (la petite boule qui n’en ai plus une). Je t’ai vu te reconstruire et je te vois épanouie aujourd’hui. Merci d’être là et sache que je suis très fier de toi.
A mamé, ma grand-mère adorée. Tu as toujours eu les mots pour tous nous émouvoir. Tu as été présente pour nous 3 et je pense parler au nom de tous pour te remercier. On a la chance de t’avoir, ton amour, ta gentillesse ont été précieuses. Je te vois toujours autant en forme, malgré toutes les misères que l’on t’a fait endurer ! Reçois par ces mots tout mon amour.
A tonton, le biker, pour lequel le sport national est la vanne. Je suis grâce à toi le « poupe » de la famille. Tu m’as aidé à me construire, à ne pas me laisser faire, à avoir de la répartie. Tu fais partie de ces patients médecins difficiles à prendre en charge. J’espère que l’on poursuivra nos balades à motos, et surtout que tu arriveras un jour à me suivre… (ce n’est pas gagné). Merci à Grazy pour ta gentillesse et ton soutien.
A Cédric, le pic, un cousin mais surtout un frère, on a fait les 400 coups ensemble. Petit tu as été mon modèle, tu as grandement participé à faire de moi ce que je suis. J’ai enfin réussi récemment à te battre au sport (sisi au squash), mais j’attends toujours ma revanche au tennis. Je te souhaite tout le bonheur que tu mérites. J’espère qu’on maintiendra ce lien qui est pour moi si important.
A Sabou, l’élue de mon cœur. Cela fait 4 ans que l’on est ensemble et chaque moment passé avec toi est un bonheur. Tu es la perle rare que l’on recherche toute sa vie, un mélange de douceur, de gentillesse et de naïveté qui font tout ton charme. Ton intelligence, ta passion et ton empathie feront de toi, je suis sûr un très bon médecin. Avec toi la vie n’est que plus belle et je vais m’assurer de te garder le plus longtemps possible à mes côtés.
Table des matières
LISTE DES ABREVATIONS ... 2
INTRODUCTION ... 3 MATERIELS ET METHODES : ... 13
Profil de l’étude ... 13 Matériels ... 14 Méthode : ... 15 Calcul du nombre de sujets nécessaires à la vérification de l’hypothèse testée : ... 16
RESULTATS :... 17 DISCUSSION : ... 26 CONCLUSION ... 32 BIBLIOGRAPHIE ... 33 ANNEXES : ... 40 Serment d’Hippocrate ... 45
2
LISTE DES ABREVATIONS
AI : aide inspiratoire
BPCO : broncho-pneumopathie chronique obstructive EEG : électro-encéphalogramme
EMG : électro-myogramme EOG : électro-oculogramme GDS : gaz du sang
HCO3- : bicarbonates
IAH : index d’apnées hypopnées ICD : index de chute de débit IMC : index de masse corporel
IRC : insuffisance respiratoire chronique
PaO2 : pression partielle en oxygène dans le sang artériel
PaCO2 : pression partielle en dioxyde de carbone dans le sang artériel
PEP : pression expiratoire positive PG : polygraphie ventilatoire PIP : pression inspiratoire positive PPC : pression positive continue PSG : polysomnographie REM : sommeil paradoxal
SLA : sclérose latérale amyotrophique
SpO2 : saturation en oxygène à l’oxymètre de pouls
VAS : voies aériennes supérieures VD : volume de l’espace mort VT : volume courant
3
INTRODUCTION
La ventilation non invasive (VNI) nocturne est reconnue comme un traitement efficace au cours de l’insuffisance respiratoire chronique (IRC) hypercapnique.
L’insuffisance respiratoire chronique est définie par l’incapacité de l’appareil respiratoire à assurer l’hématose. Le seuil d’hypoxémie retenu pour parler d’insuffisance respiratoire chronique est de 70 mmHg de PaO2 (en air ambiant, au repos et à l’état stable).
Les IRC peuvent résulter de trois mécanismes :
¾ Un trouble de la distribution de l’air par atteinte des voies aériennes distales : inadéquation ventilation/perfusion.
¾ Une atteinte de la surface d’échange alvéolo-capillaire : atteinte de la diffusion des gaz à travers la membrane.
¾ Une atteinte de la pompe respiratoire ou de la commande centrale : hypoventilation alvéolaire.
A cette hypoxémie peuvent s’associer une hypocapnie, une normocapnie ou une hypercapnie. L’hypercapnie est plus fréquemment liée à une hypoventilation alvéolaire. En effet, l’incapacité du système respiratoire à assurer les échanges gazeux (diminution du renouvellement de l’air) entraine une modification de l’élimination du gaz carbonique. La PaC02 est dépendante et proportionnelle à la
ventilation alvéolaire.
L’hypoventilation chronique est secondaire à une diminution du volume minute. Celui-ci est dépendant du volume courant et de la fréquence respiratoire.
L’hypoventilation alvéolaire peut être due à deux principaux mécanismes :
¾ Le premier est l’atteinte de la pompe ventilatoire ou de la commande centrale pouvant toucher tous les niveaux du système respiratoire [1] :
o Commande ventilatoire centrale (comas toxiques, métaboliques...) o Transmission nerveuse :
- Atteinte du motoneurone : sclérose latérale amyotrophique (SLA), syndrome post poliomyélite, amyotrophies spinales.
- Atteinte des nerfs périphériques : Charcot-Marie-Tooth, polyneuropathie démyélinisante inflammatoire chronique.
o Morphologie ou fonction anormale des muscles de la cage thoracique : myopathie de Duchenne, dystrophie Fascio-scapulo-huméral., broncho-pneumopathie obstructive chronique (BPCO) avec distension pulmonaire majeure
4
o Morphologie anormale de la cage thoracique : cyphoscoliose, séquelles tuberculeuses, obésité
¾ Le second est l’hétérogénéité des rapports ventilation/perfusion (V/Q) utile pour les échanges gazeux :
o Augmentation de l’espace mort
o Augmentation de la fréquence respiratoire chez un patient dont la charge ventilatoire est excessive.
On peut citer comme exemple la BPCO, les dilatations de bronches disséminées (dont la mucoviscidose).
Par ailleurs, l’hypercapnie apparait précocement lors de pathologies de la pompe ventilatoire.
Néanmoins, lors de pathologies de l’échangeur, l’hypercapnie apparait à un stade avancé, lorsque le travail ventilatoire dépasse les capacités maximales du patient (signe de gravité).
On a montré que la VNI au long cours, chez les insuffisants respiratoires chroniques hypercapniques améliore la qualité du sommeil, la qualité de vie et la survie, en particulier au cours de l’IRC restrictive [2,3].
Au cours de la BPCO [4], les résultats sont plus controversés. Cependant plusieurs études récentes mettent en évidence une augmentation de la survie [5,6].
Du fait du retentissement défavorable du sommeil sur la ventilation [7], la VNI à domicile est principalement proposée au cours du sommeil [8].
Le cycle de sommeil normal est composé de trois stades de sommeil lent et d’un stade dit paradoxal (REM). Chaque cycle à une périodicité de 90 minutes, le sujet normal effectue environ 4 à 5 cycles de sommeil par nuit [9].
La progression dans le sommeil à partir de l’éveil se caractérise par une diminution de la fréquence et une augmentation de l’amplitude des ondes électro-encéphalographiques (EEG).
Le sommeil normal se compose de 4 stades de sommeil :
¾ Le stade 1 et 2 sont le sommeil dit léger (50% de la nuit). Ils se caractérisent par des ondes de bas voltage avec des fréquences multiples. Les complexes K et les fuseaux de sommeil à l’EEG signent le stade 2.
¾ Le stade 3 est le sommeil lent profond (25%), présentant des ondes lentes (1 à 2Hz) et de haut voltage (>75uV).
¾ Le REM (25%), pour lequel on retrouve un bas voltage avec une fréquence mixte, accompagné de mouvements oculaires rapides et d’une atonie musculaire des muscles striés (à l’exception du diaphragme et des muscles oculaires).
5
Le sommeil lent permet un repos mental et corporel, une économie d’énergie, la croissance et la restauration des protéines ainsi que du système immunitaire.
Le sommeil paradoxal met au repos le système responsable du tonus musculaire (atonie musculaire), permet une maturation du système nerveux et consolide la mémoire implicite.
Durant le sommeil normal, la réponse des centres respiratoires aux récepteurs à l’hypoxie et à l’hypercapnie est diminuée [10,11].
Au cours du sommeil lent, la ventilation minute s’abaisse et s’associe à une polypnée superficielle et régulière responsable d’une augmentation de la PaCO2.
A l’inverse, la résistance des voies aériennes supérieures (VAS) augmente suite à la diminution de l’activité des muscles dilatateurs du pharynx.
En REM, ces modifications physiologiques sont plus marquées. Il existe, de plus, une réduction du tonus de l’ensemble des muscles striés et notamment des muscles dilatateurs du pharynx et des muscles inspiratoires : les scalènes, le sterno-cléïdo-occipito-mastoïdien, le trapèze, et les intercostaux externes.
Le diaphragme travaille donc seul pour maintenir une ventilation alvéolaire correcte.
Chez les sujets normaux, cette baisse de la ventilation minute ne cause que des altérations mineures de l’hématose. Mais chez les insuffisants respiratoires chroniques, elle contribue à une profonde hypoventilation et hypoxémie [12].
Les gaz du sang diurne montrent donc une élévation de la PaCO2 avec un pH conservé et une élévation
des bicarbonates. En effet, le rein augmente la rétention de bicarbonate la nuit pour compenser partiellement l’acidose respiratoire résultant de l’élévation de la capnie durant le sommeil (majoritairement en REM) [13,14].
Or les changements de PaCO2 se produisent rapidement en quelques minutes alors que la modification
des bicarbonates peut prendre plusieurs heures. Au cours de la journée, le patient reprend une ventilation normale. On observe alors, une alcalose métabolique reflet de l’hypoventilation nocturne. L’hypoventilation pathologique nocturne contribue à des éveils fréquents durant le sommeil (secondaire à l’hypercapnie), ce qui induit une diminution du temps de sommeil total et de son efficacité, responsables de symptômes diurnes et de privation de sommeil.
Les éveils nocturnes diminuent la désaturation et l’hypercapnie en changeant le stade de sommeil (diminution du temps passé en REM), en augmentant le tonus des muscles posturaux, et en recrutant les muscles respiratoires et des VAS afin de restaurer la ventilation. Ces éveils sont un mécanisme de protection pour minimiser l’altération de l’hématose.
Cependant, ces éveils nocturnes sont responsables d’une pauvre qualité du sommeil et de symptômes diurnes tels que la fatigue et l’hyper somnolence.
6
Au cours du temps, du fait de la privation de sommeil, la commande ventilatoire centrale (par le biais des chémorécepteurs) s’habitue aux modifications des échanges gazeux, ce qui entraine non seulement des périodes de REM plus longues, mais aussi des périodes d’hypoxies plus marquées. L’hypoventilation devient plus prolongée, ce qui augmente la rétention de bicarbonate et majore la dépression respiratoire.
C’est un cercle vicieux, qui par la perte des mécanismes d’éveils, entraine une sévère hypoventilation non seulement en REM mais aussi durant la journée.
L’objectif de la VNI est la correction de l’hypoventilation [15]. On comprend alors l’intérêt de son utilisation au cours du sommeil dans le traitement des patients insuffisants respiratoires chroniques hypercapniques.
Figure 1 : Poumons d'aciers durant la pandémie de poliomyélite
C’est au cours de la première partie du 20ème siècle que les précurseurs de la VNI sont apparus.
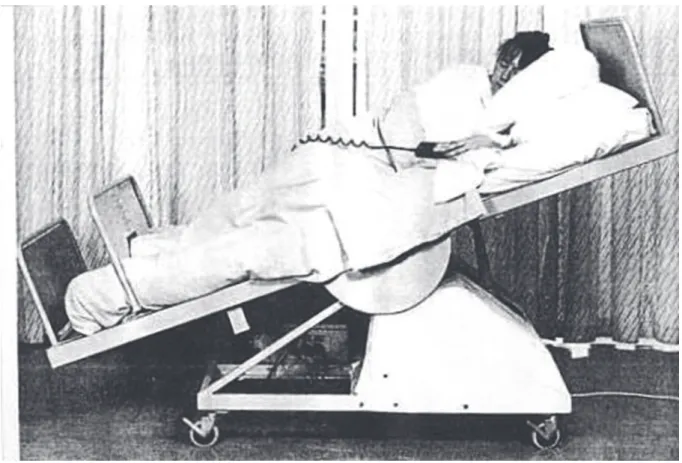
En effet, la ventilation par pression négative (poumon d’acier : figure 1) a sauvé des milliers de patients atteints de paralysie des muscles respiratoires [16] secondaire à la pandémie de poliomyélite. Ensuite des ventilateurs plus commodes ont été utilisés tels que le « jacket ventilator » ou le « rocking bed » (figure 2). Avec l’augmentation de la popularité de la ventilation en pression positive dans les années 1960, les patients neuromusculaires ont pu être pris en charge par trachéotomie s’ils souhaitaient un support ventilatoire. Cependant, les sondes en caoutchouc utilisées étaient source d’infection et les ballonnets trop gonflés entrainaient fréquemment des lésions trachéo-laryngées. Ces arguments ont incité à utiliser des interfaces « non invasives » : pièces buccales, masques d’anesthésies voire masques d’aviateurs. Néanmoins, l’interface a posé des problèmes de tolérance pour certains patients et a limité le succès de la VNI.
7
La VNI utilisée la nuit et si besoin la journée a permis de traiter avec succès certains patients neuromusculaires mais seulement dans quelques centres spécialisés. (1960) [17]
C’est l’introduction du masque nasal dans la pression positive continue (PPC) pour le traitement du syndrome d’apnée obstructive du sommeil (SAOS) qui a permis dans les années 1980, l’utilisation généralisée de la VNI.
En 1984, Rideau et al [18]ont montré qu’en utilisant ces masques nasaux sous VNI chez des patients porteurs d’une myopathie de Duchenne, on réduisait la progression de la pathologie.
Figure 2 : Rocking bed.
Depuis lors, l’utilisation de la ventilation nasale a montré une amélioration des échanges gazeux et des symptômes diurnes et nocturnes chez de nombreux patients neuromusculaires [19,20].
La VNI est préférée à la ventilation invasive pour la ventilation au long cours des patients neuromusculaires du fait de sa facilité d’utilisation, de sa portabilité et des moindres coûts et morbidités [17].
8
Figure 3 : Exemple de VNI avec masque facial (Stellar)
De nos jours, la ventilation non invasive regroupe toutes les techniques d’assistance ventilatoire délivrant une aide ventilatoire sous la forme de pression positive, sans intubation trachéale ou trachéotomie. Elle délivre un volume courant via un masque facial ou nasal au patient par la fixation de pression ou de volume prédéfini. On utilise le plus fréquemment une ventilation en pression, permettant les réglages de la pression expiratoire positive (PEP), la pression inspiratoire positive (PIP) et la fréquence respiratoire de sécurité.
La VNI a pour objectif de traiter l'hypoventilation alvéolaire, dont le marqueur biologique principal est l'hypercapnie, en assurant une prise en charge partielle ou complète de la ventilation.
Elle peut être utilisée lors de défaillances respiratoires aigües hypercapniques (en urgence) ou au cours de l’insuffisance respiratoire chronique hypercapnique à domicile.
9
On retient comme principales indications à l’utilisation de la VNI au cours de l’hypoventilation alvéolaire :
x Ceux qui ne peuvent pas ventiler :
o Pathologies neuromusculaires : SLA [21], traumatismes médullaires, myopathie de Duchenne, poliomyélite…
o Paralysie diaphragmatique o Myopathie, myasthénie
o Cyphoscoliose, séquelles de tuberculose… o BPCO
x Ceux qui ne veulent pas ventiler :
o Hypoventilation alvéolaire primitive (Syndrome d’Ondine) o AVC, poliomyélite bulbaire
o Malformation d’Arnold-Chiari
x Ceux qui ne veulent et ne peuvent pas ventiler : o Syndrome d’obésité hypoventilation
L’objectif de la PIP est d’apporter une aide à la pompe respiratoire (muscle respiratoire, diaphragme) synchronisée à l’effort du patient.
Si la synchronisation est harmonieuse, le patient va diminuer son travail respiratoire, augmenter son volume courant et cela aura comme conséquence une diminution de la fréquence respiratoire et une amélioration des échanges gazeux.
L’adjonction d’une PEP peut, grâce au recrutement alvéolaire, diminuer les efforts inspiratoires et améliorer l’oxygénation artérielle.
La PEP permet dans le SAOS de maintenir les voies aériennes supérieures ouvertes durant le sommeil si elle est supérieure ou égale à la pression critique (Pcritique) de fermeture des VAS. Cependant aucune donnée dans la littérature ne nous permet d’extrapoler ces résultats à la VNI.
La VNI est le seul traitement efficace pour traiter l’hypercapnie [22]. Mais il existe plusieurs problèmes inhérents à son utilisation dont essentiellement les fuites non intentionnelles (principalement au niveau du masque), l’instabilité des VAS et les asynchronismes patient/machine.
Afin de traiter le patient de manière optimale [23], il est important de détecter [24] et de corriger les évènements respiratoires sous VNI responsables de mauvaise tolérance et de mauvaise efficacité de la ventilation [25].
10
Bien que l’histoire de la VNI à domicile ait débuté avec un simple contrôle clinique et gazométrique, le niveau de monitorage a considérablement évolué (annexe 1), intégrant systématiquement des contrôles nocturnes d’ordre oxymétrique, capnométrique et parfois polygraphique voire polysomnographique (PSG) [26,27]. En effet la PSG est, à ce jour, le gold standard dans l’investigation du sommeil et de la respiration. C’est la seule technique qui permet de différencier le sommeil de l’éveil, et de voir les micro-éveils induits par des évènements respiratoires [28].
Notamment le groupe SomnoVNI de la Société de Pneumologie de la Langue Française (SPLF) a mis en évidence bon nombre de causes d’évènements respiratoires anormaux survenant sous VNI [29]. Parmi ceux-ci, l’obstruction des voies aériennes supérieures est un problème fréquent et de causes multiples [30,31].
L’analyse des tracés de polygraphie (PG) sous VNI, requiert de connaître le type et le mode de fonctionnement du ventilateur. La ventilation peut être administrée en volume constant (volumétrique), en pression constante (barométrique) ou en volume cible.
- Si la ventilation est en pression, le signal de pression est supposé constant, les variations du signal de débit permettront alors de comprendre la cause de l’évènement respiratoire. - A l’inverse, si la ventilation est en volume, le signal de débit est constant. Dans ce cas, la
variation de la pression permet de comprendre le mécanisme de l’évènement respiratoire. - Le volume cible [32] se caractérise par une variabilité des signaux de pression et de débit. Un
volume est paramétré sur le respirateur. Celui-ci va adapter sa pression afin d’obtenir le volume cible à délivrer au patient.
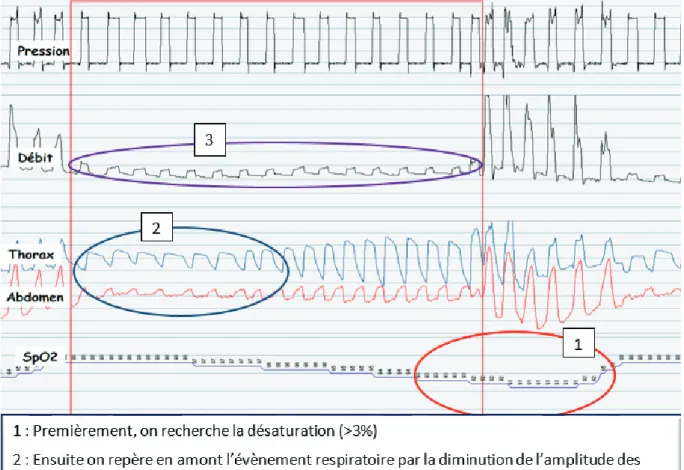
Les modalités de lecture de ventilation en barométrique (plus fréquentes) sont simples. Le praticien repère sur les tracés une désaturation ou un micro-éveil. Ensuite, il recherche en amont une diminution de l’amplitude des sangles thoraco-abdominales. Puis, il identifie l’évènement avec les variations de débit.
- Si la pression est constante, que le débit et l’amplitude des sangles thoraco-abdominales sont réduites, on considère qu’il y a une obstruction des VAS (ou chute de débit).
- En revanche, si le débit augmente et que les pressions diminuent, nous nous orientons vers des fuites non intentionnelles majeures.
11
On distingue :
x Les obstructions des VAS sans diminution de la commande ventilatoire : (figure 4)
Les efforts inspiratoires augmentent, traduisant la persistance de la commande ventilatoire contre l’obstruction. Ces efforts persistent jusqu’à ce que se produise un micro-éveil, rétablissant le tonus musculaire des VAS, leur perméabilité, et donc mettre fin à l’évènement. Une opposition de phase des mouvements thoraco-abdominaux sont caractéristiques de ces efforts persistants contre le collapsus des VAS [33].
Les deux mécanismes en cause sont :
x La pression critique de fermeture des VAS supérieure à la PEP administrée.
x L’interface : le masque facial peut induire une obstruction des VAS [19] par plusieurs mécanismes. On peut citer le recul postérieur de la mandibule par l’appui du masque sur le menton [34].
Une autre cause possible est l’arrivée du flux d’air délivré par la bouche qui entraine une mobilisation de la langue et du palais en arrière et induit une obstruction du pharynx [35,36].
12
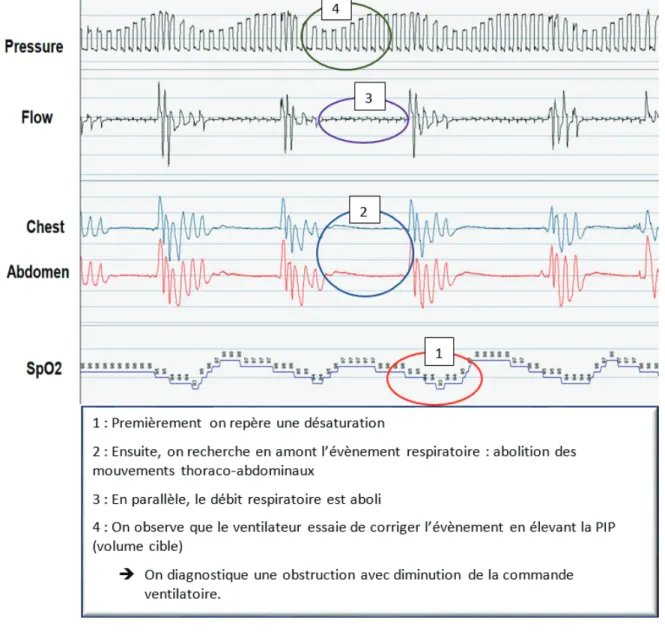
x Les obstructions des VAS avec diminution de la commande ventilatoire : (figure 5)
Les efforts inspiratoires décroissent, on observe une diminution voire une abolition des mouvements thoraco-abdominaux sans déphasage.
Les principaux mécanismes en causes sous VNI sont :
x Hyperventilation induite par la VNI responsable d’une fermeture glottique. La fermeture glottique est proportionnelle à la ventilation totale et inversement proportionnelle au CO2 de fin de cycle [30,37,38]
x Diminution de la commande ventilatoire. Si la VNI entraîne une hyperventilation, des salves d’apnées ou d’hypopnées centrales peuvent survenir. Dans l’étude de Guo[39], 40% des obèses avaient un index de respiration périodique élevé, principalement en sommeil léger.
x Obstruction induite par la fermeture des VAS [40,41]l’hypopnée centrale est corrigée par l’ouverture des VAS.
La conduite à tenir vis-à-vis de ce problème n’est pas claire dans la littérature. Modifier l’aide inspiratoire ou la PEP sont différentes options possibles.
Nous émettons l’hypothèse qu’une stabilisation des VAS par une PEP adaptée permet d’améliorer la ventilation alvéolaire.
Le but de cette étude est d’évaluer l’apport de la VNI « avec PEP variable » versus « PEP standard » dans la stabilisation des VAS au cours du sommeil et de démontrer que la PEP variable est supérieure à la PEP standard dans le traitement des obstructions des VAS sous VNI
L’objectif principal de ce projet est de mettre en évidence une réduction d’au moins 50% de l’index de chute de débit par l’utilisation de la PEP variable versus PEP standard.
Dans un second temps, on s’intéressera à l’impact de la PEP variable sur la qualité du sommeil, l’hématose et la tolérance de la ventilation.
13
MATERIELS ET METHODES :
Profil de l’étude
Nous avons réalisé un essai clinique randomisé, contrôlé, croisé, en simple aveugle, monocentrique dans le service de pneumologie du Centre Hospitalier (CH) de Cannes.
Le critère d’évaluation principal est la modification de l’index de la chute de débit sous VNI avec PEP variable versus VNI avec réglages standards.
Les critères d’évaluation secondaires associent : x La modification de l’architecture du sommeil ;
x La modification de l’index de fuite non intentionnelle et de l’asynchronisme patient/machine ; x La modification de l’hématose sur :
o L’oxymétrie (SpO2 moyenne, SpO2 minimale, durée avec une SpO2 inférieure à 90%, le
nombre de désaturation et l’index de désaturation)
o La capnométrie transcutanée (PtcCO2moyenne, PtcCO2 médiane)
o Les GDS au réveil
x La modification de la qualité du sommeil et du confort de la ventilation (questionnaire de St MARY et tolérance de la VNI).
Tous les patients qui sont suivis au CH de Cannes pour une insuffisance respiratoire chronique hypercapnique traitée par VNI au domicile sont éligibles.
Les critères d’inclusion sont :
x Patient âgé de 18 ans ou plus.
x Capacité du patient à donner son consentement.
x Insuffisance respiratoire chronique hypercapnique traitée par VNI nocturne au domicile. x Stabilité respiratoire (absence d’hospitalisation pour exacerbation respiratoire dans les 6
derniers mois).
x Index de chute de débit sous VNI supérieur à cinq par heure monitoré par PSG. Les critères de non inclusion sont :
x Absence d’instabilité des VAS sous VNI (Index de chute de débit inférieur à 5/h) x Présence d’une insuffisance cardiaque avec une FEVG inférieure à 45%
x Présence d’un syndrome d’apnée obstructive du sommeil préexistant. x Incapacité ou refus du patient à donner son consentement
14
Matériels
a) Dispositif médical utilisé
Pour raison de méthodologie, Le ventilateur Prisma VENT 40 (Löwenstein, Hamburg, Allemagne), permettant les 2 réglages est utilisé. Ce ventilateur est commercialisé et possède un marquage CE. Les réglages en PEP variable ou PEP standard sont accessibles à tout praticien utilisant la VNI.
b) Conditions de réalisation des examens
Tous les examens réalisés au cours de l’étude sont des examens pratiqués en routine dans le cadre de l’évaluation de la ventilation nocturne de patients sous VNI.
Conditions de réalisation de la polysomnographie : EEG standard (7 électrodes : Cx, F3/4, O1/2, C3/4), électro-oculogramme (EOG) gauche et droit, électro-myogramme (EMG)mentonnier, utilisation d’un pneumotachographe pour la mesure du débit d’insufflation expiratoire, pression au masque, bandes thoracique et abdominale, position corporelle. Le logiciel utilisé pour l’analyse est Noxturnal, le polygraphe est le Nox T3 / Nox A1 (Resmed).
Le sommeil est scoré sur des épisodes de 30 secondes selon les critères classiques [42].
Les paramètres suivants sont quantifiés : le temps de sommeil total, les micro-éveils respiratoires (définis par un retour en onde alfa de l’EEG ou une fréquence élevée différente des périodes précédentes, durant entre 3 et 15s), la latence d’endormissement sur l’EEG. Au niveau respiratoire, nous recueillons le nombre et l’index des asynchronismes patient/machine, des fuites non intentionnelles et des obstructions des VAS ainsi que leurs mécanismes.
Utilisation d’un oxymètre de pouls (OxiMax N560, Nellcor, Pleasaton, CA, Etats Unis), la saturation est mesurée en continue sur le doigt du patient.
La capnie est estimée par capnométrie transcutanée au niveau du lobe de l’oreille (TOSCA 500 TM, radiometer, Austrasse en Suisse.
Réalisation d’un gaz du sang le matin au réveil sous VNI.
15
Méthode :
Le patient est sélectionné lors de son hospitalisation dans le service de pneumologie de l’hôpital de Cannes dans le cadre du suivi de son insuffisance respiratoire chronique hypercapnique sous VNI.
Lors de cette première nuit, le monitorage de la VNI nocturne par PSG est pratiqué avec le ventilateur du domicile.
Le patient est randomisé dans le bras VNI avec PEP variable ou VNI avec PEP standard à l’issue de cette journée (après information par l’Investigateur Principal et signature du consentement éclairé).
Après la randomisation, le patient est ventilé par le respirateur prismaVENT40 et il ne connait pas ni le bras ni les réglages paramétrés sur la VNI.
La deuxième nuit, le patient change de bras de randomisation.
Chaque nuit, une polysomnographie, une oxymétrie, une capnométrie transcutanée et un GDS artériel au réveil sont pratiqués.
2eme nuit 3eme nuit Signature consentement
Inclusion Groupe A Groupe B
1ère nuit Groupe B Groupe A VNI avec PEP variable VNI avec PEP variable PSG de contrôle Randomisation VNI avec PEP faible VNI avec PEP faible
16 Calcul du nombre de sujets nécessaires à la vérification de l’hypothèse testée :
Le modèle expérimental proposé est celui d’une étude clinique en cross-over dans laquelle le patient est son propre témoin.
Les patients sont randomisés après visite d’éligibilité (analyse de la PSG aux conditions actuelles), information et consentement écrit, dans un bras avec VNI et PEP variable d’emblée ou bien poursuite de la VNI avec les paramètres standards.
Le calcul du nombre de sujets nécessaires (paires) montre qu’avec 10 patients différents (5 paires), une fréquence d’exposition à la VNI avec PEP variable égale à 0.50, une fréquence de réussite en VNI avec réglages standards égale à 0.05, un risque alpha unilatéral de 0.05 et une puissance de l’étude à 0.90, une fréquence de réussite d’au minimum 0.836 avec VNI et PEP variable peut être attendu de façon statistiquement significative.
17 RESULTATS :
Avec l’aide du CH de Cannes qui s’est porté promoteur de l’étude, nous avons réalisé le protocole de recherche. Celui-ci a été soumis au comité de protection des personnes (CPP) le 24 avril 2017.
L’étude a été enregistrée (n°ID-RCB), et nous avons souscrit à une assurance.
Le dossier a été examiné le 12 mai 2017, un avis défavorable nous a été adressé (annexe 2).
Jusqu’à novembre 2016, les études portant sur les soins courants nécessitaient uniquement une autorisation du CPP. Cependant, un nouveau texte de loi, la loi Jardé (n° 2016-1537 du 16 novembre 2016), a remplacé les soins courants par la catégorie 2 dénommée : recherche impliquant la personne humaine à risques et contraintes minimes.
Cette modification implique :
x Un avis favorable du CPP après soumission d’un protocole de recherche (désigné par tirage au sort dans toute la France)
x Information de l’ANSM, enregistrement n°ID-RCB x Information et consentement écrit du patient x Autorisation à la CNIL et conformité MR001 x Un promoteur et la souscription à une assurance.
Le CPP a émis un avis négatif et a remis en question plusieurs points du protocole sur le plan méthodologique.
Nous avons essayé de répondre et de corriger aux interrogations du CPP, afin de soumettre à nouveau ce protocole.
Tout d’abord, nous avons défini certaines notions importantes du sujet afin de faciliter la compréhension de personnes non formées à l’utilisation de la VNI.
PEP variable : la VNI reconnait les évènements respiratoires (via un algorithme) et adapte la PEP en fonction (augmentation si le patient présente une apnée, diminution si la VNI ne détecte aucun évènement).
PEP faible/standard : la valeur doit être comprise entre 3 et 5cm H2O, afin d’éliminer le CO2 contenu
dans le circuit ventilatoire. (Le patient inspire et expire dans le même tuyau, la PEP permet le rinçage du CO2 par les fuites au masque lors de l’expiration).
18
Puis, nous avons répondu à chaque interrogation du CPP.
1) Le critère d’évaluation principal est mal précisé : nous avons redéfini l’objectif et le critère
d’évaluation principal avec l’aide du professeur Marquette.
L’objectif principal est de montrer que la PEP variable est supérieure à la PEP faible dans le traitement des obstructions des VAS sous VNI.
Le critère d’évaluation principal : diminution de l’index de chute de débit d’au moins 50% sous PEP variable par rapport à PEP standard.
2) Le choix du design cross over n’est pas argumenté
3) L’absence de période de wash-out entre les 2 phases de traitement n’est pas argumenté.
Pour ces deux points, nous avons argumenté et expliqué qu’il n’y a pas de nécessité de wash-out entre chaque nuit.
La perméabilité des voies aériennes supérieures est le résultat de forces opposées qui s'exercent sur les parois pharyngées (d’origines multiples). Au cours de la nuit lorsque la pression atteint la Pression critique (Pcritique), les VAS se ferment complètement. La PEP réalise une contre pression afin de maintenir celles-ci ouvertes.
C’est un phénomène mécanique, si la PEP n’est pas assez élevée (ou retirée) pour contre balancer la Pcritique, les VAS se collabent et entrainent une apnée ou hypopnée.
De ce fait, la PEP est administrée ponctuellement, son effet disparait au moment où la VNI est retirée. Il n’est donc pas nécessaire de réaliser un wash-out entre les deux nuits.
Pour chaque individu, la variabilité de l’index d’apnée/hypopnée d’une nuit à l’autre est faible (44,45). Il est donc possible de réaliser une étude en cross over.
4) La randomisation n’est pas décrite
5) Sur le plan statistique, le calcul du nombre de sujets nécessaires, le choix du risque alfa unilatéral, et de façon générale, l’ensemble de l’analyse ne sont pas acceptables.
Sur ce point nous avons sollicité l’aide du Professeur Staccini.
Suite aux modifications apportées, nous avons envoyé par l’intermédiaire du promoteur (CH Cannes) une lettre de demande auprès du ministère de la santé, afin de solliciter une nouvelle présentation auprès du CPP. Celle-ci a été adressée fin juin. Nous sommes toujours en attente de leur réponse. L’utilisation de la Prisma vent 40 avec la PEP variable est autorisée (CE), et est déjà largement utilisée dans la pratique courante.
19
Nous avons décidé de commencer à inclure les patients dans cette étude dans l’attente du CPP.
De juin 2017 à ce jour, sept patients ont été enregistrés dont quatre ont pu être inclus dans le protocole. Sur les trois patients non inclus, deux présentent un SAOS sévère (index de chute de débit supérieur à 30/h sans diminution de la commande ventilatoire) et le dernier ne dort qu’une heure au cours de la nuit.
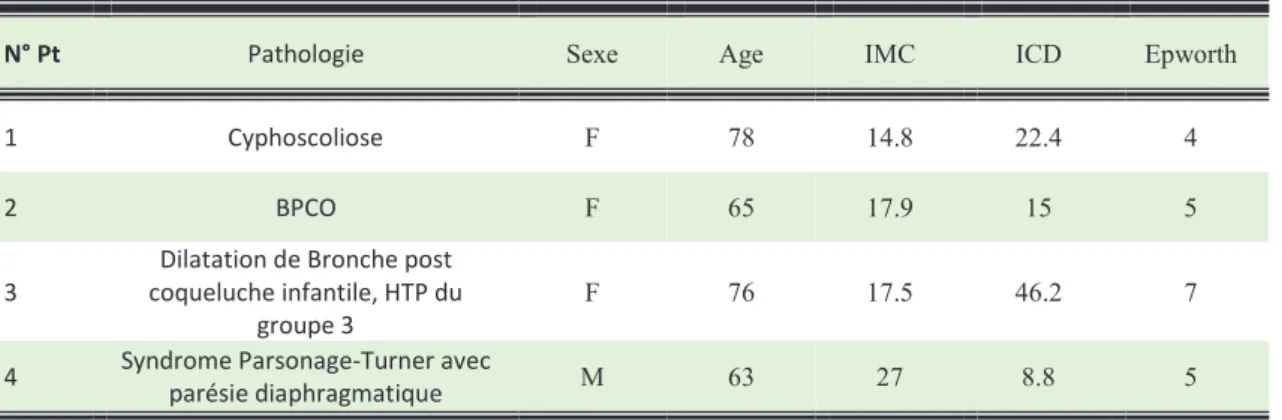
Les tableaux 1,2,3 et 4 montrent les différentes caractéristiques des patients inclus.
Dans le premier tableau, on s’aperçoit que chaque patient présente une pathologie différente. Le premier patient a une insuffisance respiratoire restrictive par cyphoscoliose avec une CPT à 53%. Le patient 2 présente une BPCO sévère avec un VEMS 0.47L et un tiffeneau à 38%.
Les patients 2 et 3 ont un trouble ventilatoire mixte, le patient 3 est atteint de dilatation de bronches post coqueluche et le patient 4 d’un syndrome de Parsonage-Turner avec une paralysie d’une coupole diaphragmatique.
Tableau 1. – Caractéristiques des patients
N° Pt Pathologie Sexe Age IMC ICD Epworth
1 Cyphoscoliose F 78 14.8 22.4 4
2 BPCO F 65 17.9 15 5
3
Dilatation de Bronche post coqueluche infantile, HTP du
groupe 3
F 76 17.5 46.2 7
4 Syndrome Parsonage-Turner avec
parésie diaphragmatique M 63 27 8.8 5
IMC : Index de Masse Corporel ; ICD : Index de chute de débit ; BPCO : Broncho-Pneumopathie Chronique Obstructive, HTP : Hypertension artérielle Pulmonaire.
20
Tableau 2.- Epreuve Fonctionnelle Respiratoire
N°PT VEMS CVF VEMS /CVF CPT
L % L % % L %
1 0.54 27 0.75 31 70 2.48 53
2 0.47 20 1.03 37.8 33 Assis Couché Assis Couché
3 1.12 56 0.73 0.64 45 34 59 3.58 80
4 1.54 54 3.22 2.52 81 63 50
VEMS : Volume Expiratoire Maximum Seconde, CVF : Capacité Vitale Forcée, CPT Capacité pulmonaire totale
Ils sont tous traités par VNI au long cours, ils présentent un index de chute de débit supérieur à 5/h. Concernant les ventilateurs, ce sont des machines de Resmed, les réglages sont similaires, avec une ventilation en pression, en mode ST. Il faut noter que le patient 3 est le seul à avoir une PEP aussi élevée à 12cmH2O. Un autre point important est que les 3 premiers patients ont un litre d’oxygène en plus sur leur ventilation.
L’interface majoritaire est le masque facial, sauf pour le dernier patient qui est ventilé avec un masque nasal.
Concernant les GDS diurne, on remarque que le patient 1 et 3 ont une capnie très élevée (1 : pCO2 65
3 : 75) reflet de la gravité de leur insuffisance respiratoire.
TABLEAU 3.- Paramètres de la VNI N°
Pt VNI Interface Mode PIP PEP FR Ti
Pente
inspiratoire Trigger Cyclage O2
1 Lumis Airfit F20 Facial ST 14 5 18 1-1,6 150 Très haut Très faible 1L
2 Stellar Quatro air
Facial ST 21 5 15
1-1 ,7 150 Moyen Moyen 1L
3 Lumis Amara View
Facial ST 24 12 14 1-1,6 150 Haut Moyen 1L 4 Stellar Mirage Fx Nasal ST 14,6 3 11 0,8-1,7 150 Moyen Moyen 0L ST : Spontaneous/Triggered, PIP : Pression Inspiratoire Positive, PEP : Pression Expiratoire
21
Concernant le critère d’évaluation principal (tableau 5), l’utilisation de la PEP variable permet de diminuer, quel que soit le mécanisme, l’ICD de plus de 50% : pour le 1er patient : de 22.5/h à 6.9/h, le
2ème de 15.5/h à 6.9/h, le 3ème 57/h à 18.1/h, et le dernier de 10.3/h à 0.6/h.
Si on regarde l’ICD avec ou sans diminution de la commande ventilatoire, on s’aperçoit que l’utilisation d’une PEP plus élevée permet de corriger chacun des mécanismes.
Concernant l’obstruction des VAS sans diminution de la commande ventilatoire, le patient 1 diminue son ICD de : 21.9/h à 5.3/h, le patient 4 de 5/h à 0.4/h.
Pour l’obstruction des VAS avec diminution de la commande ventilatoire : le patient 2 diminue de 15.5/h à 6.9/h, le patient 3 de 57/h à 18.1/h, et le patient 4 de 5.3/h à 0.2/h.
Tableau 4.- Gaz du sang diurne
Patient 1 Patient 2 Patient 3 Patient 4
Sous 1L Sous 1L Sous 1L En Air ambiant
pH 7.42 7.43 7.36 7.43
PCO2 65 47.7 75.5 39
PO2 66 75 61.5 82
HCO3- 40.2 31.9 42.8 27
Tableau 5. – Index d’obstruction des VAS sous VNI.
Patient 1 Patient 2 Patient 3 Patient 4
PEP faible PEP Variable PEP faible PEP Variable PEP faible PEP Variable PEP faible PEP Variable
Index de chute de débit
des VAS 22.9 6.9 15.5 6.9 57 18.1 10.3 0.6 Avec diminution de la commande ventilatoire 0.2 1.6 15.5 6..9 57 18.1 5.3 0.2 Sans diminution de la commande ventilatoire 22.7 5.3 0 0 0 0 5 0.4
22
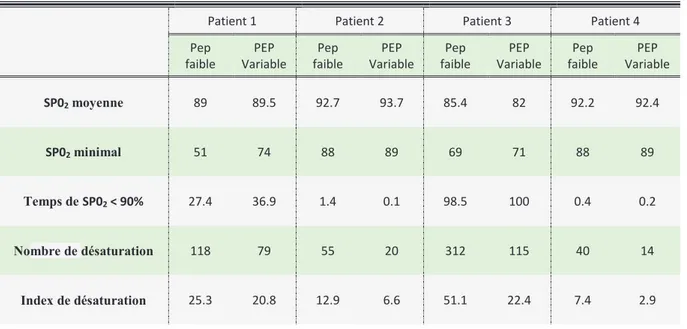
Le tableau 6, 7 et 8 nous fournissent les différents résultats concernant l’hématose.
Sur l’oxymétrie, on s’aperçoit que l’index et le nombre de désaturation diminuent sous PEP variable (respectivementpatient 1 : de 25.3/h à 20.8/h et de 118 à 7, le 2 de 12.9/h à 6.6/h et de 55 à 20, le 3 de 51.1/h à 22.4/h et de 312 à 115 et le 4 de 7.4/h à 2.9/h et de 40 à 14). La saturation minimale est plus élevée sous PEP variable, de même pour la saturation moyenne. Il faut noter une perte de 3% de la SpO2 moyenne chez le patient 3.
Cependant, on observe pour le patient 1 et 3 une augmentation du temps passé au-dessous de 90%, réciproquement de 27 à 37% et de 98.5 à 100%.
Concernant la capnométrie transcutanée, il n’y a pas de différence évidente sur la capnie entre la PEP standard et la PEP variable avec même une tendance à une discrète augmentation de celle-ci sous PEP variable. Par contre, pour le 3ème patient, il y a une baisse de 7 point de la capnie avec la PEP variable.
Tableau 6. – Oxymétrie
Patient 1 Patient 2 Patient 3 Patient 4
Pep faible PEP Variable Pep faible PEP Variable Pep faible PEP Variable Pep faible PEP Variable SP02 moyenne 89 89.5 92.7 93.7 85.4 82 92.2 92.4 SP02 minimal 51 74 88 89 69 71 88 89 Temps de SP02 < 90% 27.4 36.9 1.4 0.1 98.5 100 0.4 0.2 Nombre de désaturation 118 79 55 20 312 115 40 14 Index de désaturation 25.3 20.8 12.9 6.6 51.1 22.4 7.4 2.9
23
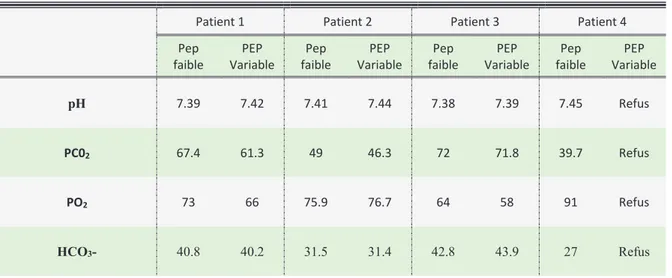
Enfin sur les GDS de réveil, il existe une diminution de la capnie pour les 2 premiers patients seulement (1 : de 67.4 à 61.3 et 2 : 2 49 à 46.3), et une diminution de la pO2 pour le 1er et 3ème patient (patient 1 :
73 à 66, patient 3 : 64 à 58).
Au niveau de l’architecture du sommeil (tableau 9), l’utilisation de la PEP variable entraine chez tous les patients une diminution du temps de sommeil total (1 : 280 à 227min – 2 : 255 à 183min – 3 : 366 à 308 min – 4 : 325 à 293 min), une diminution ou une stabilisation du sommeil paradoxal, une augmentation du sommeil lent léger et lent profond.
Cependant, on remarque une nette diminution du nombre de micro-éveils respiratoires sous PEP variable (pour le patient 1 : de 7.7 à 2.9/h – 2 : 7.5 à 2.6/h – 3 : 28 à 10.1/h – 4 : 6.3 à 2.3/h).
En ce qui concerne les asynchronismes patient/machine, on remarque que l’utilisation de la PEP variable augmente le nombre de fuites non intentionnelles, majoritairement sur le patient 1 : de 5 à 7% et le 4 : de 0 à 8.7%.
Tableau 7. – Capnométrie transcutanée
Patient 1 Patient 2 Patient 3 Patient 4
PEP faible PEP Variable PEP faible PEP Variable PEP faible PEP Variable PEP faible PEP Variable TC PCO2 moyenne 69.1 69.4 43.3 47.7 82.7 74.8 44.9 45.7 Médiane 69 70 48 48 82 75 47 46
Tableau 8. – Gaz du sang au réveil
Patient 1 Patient 2 Patient 3 Patient 4
Pep faible PEP Variable Pep faible PEP Variable Pep faible PEP Variable Pep faible PEP Variable pH 7.39 7.42 7.41 7.44 7.38 7.39 7.45 Refus PC02 67.4 61.3 49 46.3 72 71.8 39.7 Refus PO2 73 66 75.9 76.7 64 58 91 Refus HCO3- 40.8 40.2 31.5 31.4 42.8 43.9 27 Refus
24
Les résultats sur la qualité du sommeil et du confort de la ventilation sont décrits dans le tableau 10. On ne retrouve pas de modification majeure entre la PEP variable et la PEP faible.
A noter que pour le 1er patient, son sommeil a été perturbé par des fuites, d’où un plus mauvais confort
et une mauvaise qualité du sommeil.
Tableau 9. – Architecture du sommeil
Patient 1 Patient 2 Patient 3 Patient 4
PEP faible PEP Variable PEP faible PEP Variable PEP faible PEP Variable PEP faible PEP Variable TST 280 227 255 183 366.6 308 325.5 293 % SLL 36.2 36.9 41.3 47 45.5 41.8 46 51 % SLP 34.5 40.9 30.7 32.6 35.7 38.7 31 32 % REM 29.1 22.2 28 20 18.8 19.4 23 15.7 Micro-réveils respiratoires 10.7 2.9 7.5 2.6 28 10.1 6.3 2.3 Fuites % 5 7 1.4 1.2 0 0.1 0 8.7 Minutes 11.4 19 3.7 3.7 0 0.3 0 25.5
25
Tableau 10. – Questionnaire du sommeil de St Mary’s
Patient 1 Patient 2 Patient 3 Patient 4
Pep faible PEP Variable Pep faible PEP Variable Pep faible PEP Variable Pep faible PEP Variable Profondeur du sommeil (1-6) 5 5 8 8 6 6 8 8 Nb de réveil nocturne 3 0 0 0 1 1 0 1 Durée du sommeil 7h 5h 6h 5h 7h 7h 8h 5h Qualité du sommeil (1-5) 3 4 4 4 3 3 5 5 Fatigue matinale (1-6) 1 1 1 1 2 2 1 1 Satisfaction de la qualité du sommeil (1-5) 5 3 5 5 2 3 5 5
Réveil précoce (oui/non) Non Non Oui Non Non Non Non Oui
Difficulté à
l’endormissement (1-4) 2 3 2 2 2 1 1 1
Temps à s’endormir (min) 15 30 60 20 10 60 10 10
Confort de la ventilation : noter les items suivants de 0 à 10 :
Confort de la ventilation 8 5 8 8 5 8 10 10
Désynchronisation perçue
par le patient 2 0 0 1 0 2 2 0
Trop d’air délivré 0 5 0 0 0 0 0 0
Pas assez d’air délivré 0 0 0 0 0 0 0 0
Céphalées matinales 0 0 0 0 0 0 0 0
Fuites perçus 1 5 4 2 0 0 2 3
Bruit du ventilateur 1 0 0 0 4 2 2 0
26
DISCUSSION :
Nous avons réalisé une étude clinique prospective, randomisée, croisée, monocentrique dans le service de pneumologie du Centre Hospitalier de Cannes sur quatre patients.
Nous avons montré la faisabilité de ce projet de recherche. Les résultats obtenus sont en faveur d’une amélioration de la stabilité des VAS sous PEP variable. Nous montrons effectivement une diminution de l’index de chute de débit (ICD) et de l’index de désaturation. Enfin la PEP variable montre une augmentation du temps passé en sommeil lent profond.
En effet, nous observons une diminution de l’index de chute de débit de plus de 50% avec l’utilisation d’une PEP variable par rapport à une PEP standard : pour le 1er patient : de 22.5/h à 6.9/h, le 2ème de
15.5/h à 6.9/h, le 3ème 57/h à 18.1/h, et le dernier de 10.3/h à 0.6/h. Ces résultats sont reproductibles
lorsque l’obstruction est associée à une diminution de la commande ventilatoire (le patient 2 diminue de 15.5/h à 6.9/h, le patient 3 de 57/h à 18.1/h, et le patient 4 de 5.3/h à 0.2/h) ou lorsqu’au contraire, la commande ventilatoire n’est pas abaissée (le patient 1 diminue son ICD de : 21.9/h à 5.3/h, le patient 4 de 5/h à 0.4/h).
La PEP variable n’a pas montré de différence sur la moyenne de SpO2 et PtcCO2, chez des patients déjà
ventilés avec une aide inspiratoire significative. Cependant, sous VNI avec PEP variable nous constatons une diminution de l’index de désaturation (> 3%) en rapport avec une optimisation de la stabilité des VAS sous VNI (respectivement, patient 1 : de 25.3/h à 20.8/h, le 2 de 12.9/h à 6.6/h, le 3 de 51.1/h à 22.4/h et le 4 de 7.4 à 2.9).
Nous remarquons une aggravation du temps passé avec une SpO2 inférieure à 90% chez les patients 1
et 3 (respectivement pour le 1er : 27.4% à 36.9% et le second : 98.5% à 100%) ainsi qu’une diminution
de la SpO2 moyenne chez le 3ème sujet (85.4% à 82%).
L’aggravation pour le 1er patient est imputable à l’augmentation des fuites non intentionnelles.
Pour le 3ème patient, l’hypothèse d’une compression du lit vasculaire pulmonaire liée à l’augmentation
de la PIP pour expliquer cette désaturation est à évoquer.
Concernant l’architecture du sommeil, il existe une diminution du temps de sommeil total, du temps passé en REM, et une augmentation du sommeil lent léger et profond sous PEP variable.
Le nombre de micro-éveils respiratoires diminue (pour le patient 1 : de 7.7/h à 2.9/h – 2 : 7.5/h à 2.6/h – 3 : 28/h à 10.1/h – 4 : 6.3/h à 2.3/h), en lien avec la correction des évènements respiratoires. En revanche, l’utilisation de la PEP variable augmente le nombre de fuites non intentionnelles, majoritairement sur le patient 1 : de 5 à 7% et le patient 4 : de 0 à 8.7%.Le ventilateur a pu générer une PEP excessive responsable d’une élévation de la PIP. Cette élévation de pression a porté atteinte à l’étanchéité du masque sur la peau. Celui-ci s’est soulevé, et est responsable de fuites non intentionnelles.
27
La VNI nocturne est un traitement efficace de l’IRC hypercapnique. Elle améliore l’hématose [17], la qualité du sommeil, la qualité de vie et la survie, au cours de l’IRC restrictive mais aussi chez les patients BPCO [6].
Cependant, des évènements respiratoires (fuites non intentionnelles, obstructions des VAS et asynchronismes) peuvent affecter la tolérance du patient et l’efficacité de la ventilation [46]. Le groupe SomnoVNI de la SPLF a répertorié et proposé une méthode d’analyse polygraphique des évènements respiratoires anormaux au cours de la VNI nocturne [29].
Bien que manquant d’épidémiologie, l’obstruction des VAS lors de la VNI nocturne paraît fréquente et de causes multiples.
Au cours de la VNI, les VAS peuvent changer leur résistance au flux aérien compromettant la délivrance d’un volume courant efficace aux poumons [47].
Ainsi, on distingue les obstructions des VAS sans ou avec diminution de la commande ventilatoire. ¾ Les obstructions des VAS sans diminution de la commande respiratoire correspondent aux
évènements obstructifs au niveau pharyngé en raison d’un collapsus résultant d’une PEP réglée en dessous de la Pcritique de fermeture des VAS. L’exemple le plus parlant est le syndrome d’obésité/hypoventilation pour lequel il existe dans plus de 90% des cas un syndrome d’apnée du sommeil associé [48].
L’interface à type de masque naso-buccal [19] peut, lui aussi, en être une cause par rétropulsion de la mandibule.
Il peut également s’agir d’un simple reflux de la langue vers l’arrière sous l’effet de la pression positive.
¾ Les obstructions des VAS avec diminution de la commande respiratoire, peuvent être secondaires à la moindre ouverture physiologique des VAS au cours du sommeil (phénomène exacerbé au cours des phases de sommeil paradoxal ou REM) [30,38] ou à une respiration périodique (par capture du seuil d’apnée) au cours de la VNI [39].
La physiopathologie de l’obstruction des VAS [49] durant le sommeil implique des interactions entre l’instabilité de la commande ventilatoire et l’anatomie défavorable du pharynx [50–56].
Il a été montré que le pharynx se ferme lors d’apnées/hypopnées d’origine centrale soit physiologiquement au cours du sommeil ou induites par la VNI par sollicitation du seuil d’apnée [40,41,57]
En 1986, ISSA et Sullivan [58], avaient traité des patients présentant un syndrome d’apnée centrale du sommeil par PPC nasale. Ils avaient ainsi maintenu la perméabilité pharyngée et stabilisé leur respiration.
28
De leurs côtés, Guilleminault et al [59] avaient enregistré 5 patients qui se plaignaient de troubles respiratoires du sommeil et 2 patients qui présentaient des lésions cérébrales irréversibles (infarctus vertébro- basilaire, atteinte du tronc cérébral).
Chez les 5 premiers, lors des évènements centraux, ils observaient une réduction du calibre des VAS. Ils avaient donc instauré un traitement par PPC qui avait corrigé les hypopnées et les désaturations chez tous ces patients. Cependant, celle-ci avait été inefficace chez les sujets lésés cérébraux.
Les mécanismes responsables des apnées centrales sont divers :
9 L’instabilité du système des centres respiratoires (liée à la plupart des apnées centrales). 9 Les lésions du tronc cérébral responsables d’apnées centrales répétées (destruction du signal
respiratoire).
9 L’occlusion partielle due à une anatomie défavorable des VAS. Dans ce dernier cas, la PPC permet de corriger ces évènements.
L’obstruction complète des VAS durant les apnées centrales [57] et l’efficacité de la PPC nasale dans certains SAS centraux [58] sont en faveur d’un overlap dans la physiopathologie du syndrome d’apnée centrale et obstructive du sommeil [60].
En pratique, au cours de la VNI, la PEP est principalement utilisée pour améliorer le recrutement alvéolaire ou pour diminuer les efforts inspiratoires. Il est important de rapporter que la correction de l’hypoventilation, quel que soit son mécanisme, dépend habituellement du réglage de l’aide inspiratoire.
Par ailleurs, l’intérêt de la PEP (via la PPC) dans la stabilisation des VAS au cours du SAOS est clairement démontré. Elle permet de diminuer l’obstruction des VAS en s’opposant à la Pcritique de fermeture. Aussi, Douglas et al. [61] ont même proposé l’utilisation de la PPC dans le traitement du syndrome d’apnée du sommeil central. En effet, au cours d’une hypopnée d’origine centrale, la réduction d’une moindre ouverture des VAS sous l’action de la PPC optimise la ventilation du sujet et diminue la variation péjorative des échanges gazeux.
Ainsi, l’ensemble de ces éléments fondent le rationnel de l’utilisation de la PEP afin de stabiliser les VAS au cours de la VNI nocturne.
Au-delà de la faisabilité que nous montrons dans ce projet de recherche, les résultats que nous rapportons démontrent la correction des obstructions des VAS quel que soit le mécanisme par l’utilisation de la PEP variable.
En effet, chez l’ensemble de nos patients, l’index de chute de débit baisse de plus de 50% avec la PEP variable (1er patient : de 22.5/h à 6.9/h, le 2ème de 15.5/h à 6.9/h, 3ème de 57/h à 18.1/h, et 4ème de