L'utilisation des autotests officinaux dans l'automédication responsable
Texte intégral
Figure

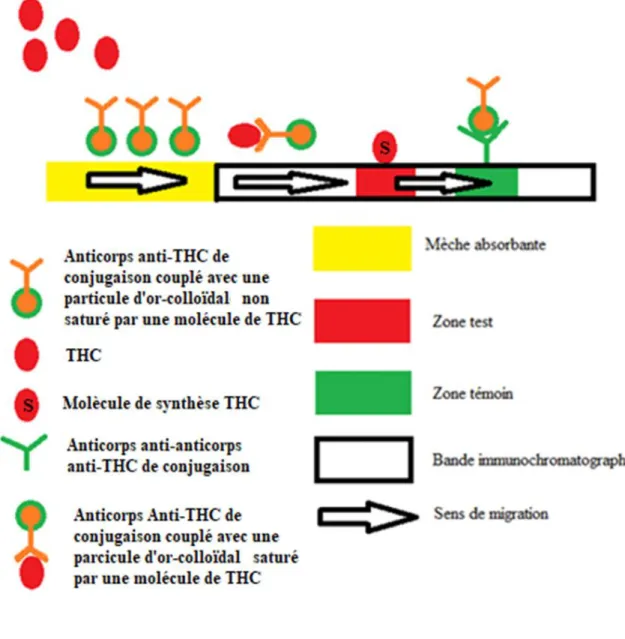


Outline
Documents relatifs
[r]
Donner la mesure de l’angle marqué en justifiant
Considère que les 35 organisations énumérées au paragraphe 4 du présent document répondent aux critères énoncés dans les Directives opérationnelles et recommande à
Pour ce faire, il faut utiliser la fonction réciproque Z (F). Bien sûr, on peut envisager d'effectuer des inter- polations pour des fonctions tabulées mais nous avons préféré par
La fonction de répartition
Regardez attentivement la perspective des colonnes, des cintres et du grand escalier : cette prison est vraiment imaginaire, mais il faut y regarder de près avant de s'en
L’objectif de cet exercice est de calculer le nombre moyen de tablettes qu’il faut acheter pour obtenir chacune des n images.. Un joueur lance cette pièce jusqu’à obtenir le
En pratique, soit parce que les lois ne sont pas continues, soit parce qu’on a des mesures arrondies, on peut avoir des ex-aequos.. Dans ce cas, la solution la plus couramment