HAL Id: tel-00598644
https://tel.archives-ouvertes.fr/tel-00598644
Submitted on 7 Jun 2011HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Caractérisation de revêtements de silicate de lanthane
de structure apatite dopé au magnésium réalisés par
projection plasma en vue d’application comme
électrolyte de pile à combustible de type IT-SOFC
Fu Sun
To cite this version:
Fu Sun. Caractérisation de revêtements de silicate de lanthane de structure apatite dopé au magné-sium réalisés par projection plasma en vue d’application comme électrolyte de pile à combustible de type IT-SOFC. Mécanique [physics.med-ph]. Université de Technologie de Belfort-Montbeliard, 2010. Français. �NNT : 2010BELF0141�. �tel-00598644�
N° d’ordre : 141 Année:2010 Ecole Doctorale “Sciences pour l’ingénieur et Microtechnique”
Université de Franche-Comté
Université de Technologie de Belfort-Montbéliard
THESE
Présentée pour obtenir le grade de
Docteur de l’Université de Technologie de Belfort-Montbéliard en
Sciences pour l’Ingénieur
Par
Fu SUN
Présentée et soutenue publiquement le 10 décembre 2010 Membres du jury
Rapporteurs
Daniel Morvan Professeur, École nationale supérieure de chimie de Paris Fabrice Mauvy Professeur, Université Bordeaux 1
Examinateurs
Thierry Grosdidier Professeur, École Nationale d’Ingénieurs de Metz
Christian Coddet Professeur, Université de Technologie de Belfort-Montbéliard Hanlin Liao Professeur, Université de Technologie de Belfort-Montbéliard
Directeur de thèse
Caractérisation de revêtements de silicate de lanthane de
structure apatite dopé au magnésium réalisés par projection
plasma en vue d’application comme électrolyte de pile à
combustible de type IT-SOFC
Remerciements
Les travaux présentés dans ce mémoire ont été réalisés au Laboratoire d’Etudes et de Recherches sur les Matériaux et les Propriétés de Surface (LERMPS) de l’Université de Technologie de Belfort-Montbéliard(UTBM) sous la direction de Monsieur le professeur Hanlin LIAO.
Je tiens à remercier Monsieur le professeur Christian Coddet, directeur du LERMPS, de m’avoir accueillie au sein de son équipe.
Cette thèse a été réalisée sous la direction de Monsieur le Professeur Hanlin Liao qui m’a soutenu et conseillé beaucoup tout au long de cette étude. En travaillant avec lui, j’ai appris beaucoup de connaissances scientifiques et morales qui sont très importantes pour mes futures projets. Je lui suis très reconnaissant des aides que il m’a apporté, non seulement techniques mais aussi des aides gentils dans la vie quotidienne.
Je remercie vivement Monsieur le professeur Thierry Grosdidier de m’avoir fait l’honneur de présider le jury, ainsi que Messieurs les professeurs Fabrice Mauvy et Daniel Morvan pour avoir accepté de rapporter ma thèse.
Je remercie Monsieur le professeur Fabrice Mauvy et Mademoiselle Cécile Lalanne pour leurs aides de mesure des propriétés électriques de la pile à l’ICMCB.
Je tiens à adresser un remerciement spécial à Marie-Pierre Planche, Pierre-Laurent Coddet, Yoann Danlos, Pascale Hoog et Olivier Marchand pour leurs aides concernant les corrections de ma thèse.
Je remercie le CSC (Chine Scholarship Council) qui m’a soutenu financièrement pendant cette thèse.
Enfin, je voudrais adresser des remerciements particuliers à mes parents qui ont su être compréhensifs et patients.
Table des matières
U
Introduction
U... 1
U
Chapitre I
U: UEtude
bibliographique
U... 3
UI.1. Piles à combustible à oxydes solidesU... 4
UI.1.1. HistoriqueU... 4
UI.1.2. Structure et fonctionnement d’une pile SOFCU... 4
UI.1.2.1. Principe de fonctionnement d’une pileU... 4
UI.1.2.2. Géométries de piles existantesU... 5
UI.1.3. Matériaux utilisés pour les piles SOFCU... 7
UI.1.3.1. CathodeU... 7
UI.1.3.2. ElectrolyteU... 8
UI.1.3.3. AnodeU... 10
UI.1.3.4. InterconnexionU... 11
UI.1.4. Pile IT-SOFCU... 12
UI.2. ApatitesU... 12
UI.2.1. StructureU... 13
UI.2.2. Propriétés électriques des apatitesU... 15
UI.2.3. Mécanismes de conductionU... 17
UI.3. Projection thermiqueU... 21
UI.3.1. Historique et principe de la projection thermiqueU... 21
UI.3.2. Projection plasmaU... 23
UI.3.2.1. Principe de la projection plasmaU... 23
UI.3.2.2. Développement de la projection plasmaU... 26
UI.3.3. Utilisation de la projection thermique pour l’élaboration de la pile de type SOFCU28 UI.3.3.1. Fabrication de l’anodeU... 28
UI.3.3.2. Fabrication de la cathodeU... 28
UI.3.3.3. Fabrication de l’électrolyteU... 29
UI.4. Objectif de la rechercheU... 30
UI.5. Références bibliographiquesU... 31
U
Chapitre II
U: UPréparation du silicate de lanthane d’apatite dopé par
magnésium
U... 37
UII.1. Méthode de synthèse des oxydes d’apatiteU... 38
UII.2. Procédé de synthèseU... 39
UII.2.1. MatériauxU... 39
UII.2.2. Procédés de frittageU... 42
UII.3. Caractérisation de la poudre frittéeU... 46
UII.3.1. DensitéU... 46
UII.3.2. PhaseU... 47
UII.3.2.1. Diffraction des rayons XU... 47
UII.3.2.2. Diagramme de phases du système La2O3-SiO2U... 47
UII.3.2.3. Analyse de phasesU... 48
UII.3.3. MicrostructureU... 52
UII.3.4. Conductivité électriqueU... 53
UII.3.4.1. Principe et dispositif de mesureU... 53
UII.3.4.2. Conductivité électriqueU... 56
UII.4. ConclusionsU... 58
UII.5. Références bibliographiquesU... 59
U
Chapitre
III
U:
UElaboration de l’électrolyte par projection plasma
U... 61
UIII.1. Elaboration de l’électrolyte par projection APSU... 62
UIII.1.1. Protocole expérimentalU... 62
UIII.1.1.1. Les poudresU... 62
UIII.1.1.2. Projection plasma sous air sur un substrat non préchaufféU... 63
UIII.1.1.3. Projection plasma sous air sur un substrat préchaufféU... 64
UIII.1.2. Résultats de DRXU... 67
UIII.1.2.1. Dépôts réalisés sur le substrat non préchaufféU... 67
UIII.1.2.2. Dépôts réalisés sur substrat préchaufféU... 69
UIII.1.2.3. BilanU... 70
UIII.1.3. Microstructure des dépôtsU... 71
UIII.1.3.1. Dépôt sur le substrat non préchaufféU... 71
UIII.1.3.2. Dépôt sur substrat préchaufféU... 75
UIII.1.3.3. BilanU... 77
UIII.1.4. Propriétés électriquesU... 78
UIII.1.4.1. Dépôts réalisés sur substrat non préchaufféU... 78
UIII.1.4.2. Dépôts réalisés sur substrat préchaufféU... 80
UIII.1.4.3. BilanU... 83
UIII.1.6. Cinétique de transition de phaseU... 85
UIII.2. Elaboration de l’électrolyte par procédés LPPS et VLPPSU... 90
UIII.2.1. Montage expérimentalU... 90
UIII.2.2. Structures des dépôtsU... 92
UIII.2.3. Analyses de phases des dépôtsU... 94
UIII.2.4. Perméabilités des dépôts élaborés par VLPPSU... 96
UIII.2.5. BilanU... 98
UIII.3. ConclusionsU... 99
UIII.4. Références bibliographiquesU... 101
U
Chapitre IV
U:
UFabrication de la pile de type SOFC et mesure des propriétés
électriques
U... 103
UIV.1. Présentation de la cellule complète SOFCU... 104
UIV.2. Elaboration de la cellule complète par projection thermiqueU... 105
UIV.2.1. Préparation de la plaque supportU... 105
UIV.2.2. Elaboration de l’anodeU... 106
UIV.2.3. Elaboration de l’électrolyteU... 110
UIV.2.4. Elaboration de la cathodeU... 110
UIV.2.5. Traitement thermiqueU... 114
UIV.2.6. Structure de la cellule complèteU... 115
UIV.2.7. BilanU... 116
UIV.3. Propriétés électriques de la pileU... 116
UIV.3.1. Principe de la mesureU... 116
UIV.3.2. Caractéristiques I-E et I-P des cellulesU... 119
UIV.3.3. Résistance électrique de la celluleU... 122
UIV.3.4. Vieillissement de la celluleU... 125
UIV.4. ConclusionsU... 125
UIV.5. Références bibliographiquesU... 127
Introduction
La pile à combustible à oxyde solide est un générateur d’énergie qui permet de transformer directement l’énergie chimique en énergie électrique via des réactions d’oxydo-réductions. Cette pile est considérée comme l’une des solutions pour combattre la crise énergétique grâce à son rendement global élevé (de l’ordre de 70%) et surtout grâce à son faible rejet de gaz carbonique.
Une pile à combustible à oxyde solide est constituée d’une anode, d’une cathode et d’un électrolyte fabriqué souvent par zircone yttriée (YSZ). Ce type de pile fonctionne uniquement à très haute température; supérieure à 1000°C qui correspond en fait à la température de conduction de la zircone. Une haute température de fonctionnement provoque quelques inconvénients, par exemple, des problèmes de contraintes thermiques, de réaction « frontière chimique » entre l’électrolyte et les électrodes, de coût de fabrication, et de durée d'usage de la pile trop courte, etc. Pour éviter ces inconvénients, la pile à combustible à oxyde solide à température intermédiaire (IT-SOFC), qui fonctionne à température entre 600 °C et 800°C, est étudiée. Il devient donc nécessaire de développer de nouveaux matériaux d’électrolyte ayant de bonnes propriétés électriques à une température intermédiaire.
Ces dernières années, des oxyapatites dont la formule est La9,33+x(SiO4)6O2+3x /2 ont été
développées en tant qu’électrolyte pour la pile de type IT-SOFC. Il est possible d’améliorer les propriétés de conductivité électrique par le dopage en site de Si4+. Parmi ces matériaux, le
silicate de lanthane dopé par magnésium de formule La10Si5,8Mg0,2O26,8 montre de bonnes
potentialités en matière de conductivité électrique.
Puisqu’une pile se compose de différentes couches, les procédés de revêtement sont couramment utilisés pour la fabriquer. Parmi les techniques de dépôt, la projection thermique est moins coûteuse et efficace, et permet en plus d’élaborer des piles de type SOFC de différentes formes.
Cependant en tant que nouveau matériau de l’électrolyte, la mise en forme du dépôt de silicate de lanthane dopé par magnésium (La10Si5,8Mg0,2O26,8 ) par projection plasma pose des
difficultés. L’objectif de ce travail est d’étudier les processus de préparation du dépôt de l’électrolyte La10Si5,8Mg0,2O26,8 par projection plasmaet d’aboutir à la réalisation de pile de
Cette thèse est organisée suivant quatre chapitres : une étude bibliographique, la préparation de matériau La10Si5,8Mg0,2O26,8, la préparation de l’électrolyte La10Si5,8Mg0,2O26,8 par
projection plasma, et la préparation de la cellule complète avec l’électrolyte La10Si5,8Mg0,2O26,8 par projection thermique.
Le chapitre I, essentiellement bibliographique, est composé de trois parties: un bref rappel du principe de fonctionnement des piles de type SOFC, la structure et le principe de la conductivité électrique des oxyapatites et le principe de la projection thermique et son utilisation pour la préparation de la pile de type SOFC.
Le chapitre II décrit l’élaboration du matériaux La10Si5,8Mg0,2O26,8. Dans un premier temps, le
procédé d’élaboration par voie solide est présenté. Ensuite les paramètres du frittage sont optimisés et un protocole est proposé pour élaborer ce matériau. Finalement, les propriétés du matériau La10Si5,8Mg0,2O26,8 synthétisé (densité, phase, et propriétés électriques) sont
présentées.
Le chapitre III concerne essentiellement la mise en forme du dépôt La10Si5,8Mg0,2O26,8 en tant
qu’électrolyte par projection plasma. D’abord, le dépôt La10Si5,8Mg0,2O26,8 est réalisé sur le
substrat non préchauffé par APS (projection plasma sous air). Le traitement thermique est étudié afin de réaliser la recristallisation et la densification des dépôts. La cinétique de cristallisation des dépôts à condition isotherme a été étudiée par la mesure de la conductivité électrique. La perméabilité et la conductivité électrique des dépôts avant et après traitement thermique sont également mesurées. Ensuite, la projection est réalisée sur substrat préchauffé aux températures 545°C et 700°C afin d’éviter la présence de la phase amorphe. Finalement, le dépôt est réalisé sur substrat préchauffé par procédé LPPS (projection plasma sous faible pression) et VLPPS (projection plasma sous très faible pression). Les microstructures, phases, et perméabilités des dépôts sont caractérisées.
Le chapitre IV montre l’élaboration par projection thermique de la cellule complète de la pile SOFC de structure planaire avec l’électrolyte La10Si5,8Mg0,2O26,8. Les paramètres de
préparation de la cathode et de l’anode sont optimisés afin d’obtenir une structure poreuse. Deux types de cellule avec l’électrolyte réalisé par technique APS sur substrat non préchauffé et par technique VLPPS sont élaborés. Les propriétés électriques des cellules ont été caractérisées à l’ICMCB (Institut de Chimie de la matière condensée de Bordeaux).
Un dernier chapitre résume les principaux résultats de cette étude. Les perspectives afin d’améliorer ces travaux sont représentés finalement.
U
Chapitre I
I.1. Piles à combustible à oxydes solides
I.1.1. Historique
Une pile à combustible à oxyde solide est un système qui peut transformer directement de l’énergie chimique en l’énergie électrique. Elle est une des solutions technologiques les plus prometteuses pour combattre la pollution résultant de la dépendance du monde aux énergies fossiles, parce qu’elle ne pollue pas l’atmosphère, ne fait pas de bruit et libère uniquement de l’eau et de la chaleur. Elle correspond à un type de piles à combustible.
En 1838, le principe de fonctionnement des piles à combustible fut découvert par Christian Friedrich Schoenbein. En 1839, le premier modèle de laboratoire de pile à combustible fut réalisé par William R.Grove. Ce système utilisait l’acide sulfurique comme l’électrolyte et le platine comme matériau des électrodes.
La première tentative de réalisation d’une pile à combustible haute température mettant en œuvre un électrolyte solide est due à Baur et Press [14], au début des années 30.
Depuis les années 1960 et l’exploitation des propriétés conductrices de la zircone stabilisée, les piles de type SOFC font l’objet d’études approfondies. Ces travaux participent d’un effort de recherche général sur les différents types des piles à combustible, effort motivé par des besoins nouveaux en matière de production et de stockage d’énergie liés aux développements de l’exploration spatiale ou sous-marine ainsi qu’à des applications militaires.
En 1990, parmi les laboratoires industriels qui consacrent un effort important aux PCHT on peut citer : Westinghouse (USA), Dornier (RFA), Asea Brown Boveri Co (Heidelberg RFA), ou encore Electrotechnical (Japon).
I.1.2. Structure et fonctionnement d’une pile SOFC
I.1.2.1. Principe de fonctionnement d’une pile
Le schéma de principe d’une cellule élémentaire d’une pile à combustible de type SOFC est représenté sur la figure I.1. Elle est constituée par trois couches :
-un électrolyte solide
Il doit correspondre à une couche mince et étanche afin de séparer le combustible du côté anode du comburant du côté cathode pendant le fonctionnement de la pile. Il doit être isolant électrique et capable de conduire les ions oxygène de la cathode vers l'anode.
-une électrode à oxygène (cathode)
Elle doit correspondre à une couche poreuse afin de permettre au combustible d’atteindre l’interface cathode-électrolyte. C’est un conducteur électrique et ionique.
-une électrode à combustible (anode)
Elle doit correspondre à une couche poreuse afin de permettre à l’air d’atteindre l’électrolyte. C’est le côté positif de la pile qui doit conduire l’électricité.
La force motrice totale est définie par l’énergie de réaction chimique entre l’oxygène et le combustible (par exemple: H2). La combustion chimique directe est empêchée par
l’électrolyte dense et imperméable aux gaz. Mais l’électrolyte solide est un conducteur ionique. Du côté de la cathode qui est exposée à l’air, l’oxygène est réduit en ions oxygène (O2-) (réaction notée I.1). Du côté de l’anode, la réaction chimique entre l’hydrogène et les
ions oxygène qui traversent l’électrolyte solide a lieu, ce qui produit de l’eau (réaction notée I.2). La réaction chimique globale est donnée dans l’équation I.3.
Cathode:
+
2
−1
→
2− 2e
O
O
2
1
EQN I.1 Anode: 1 2 2 2 O H O 2e H + − → + − EQN I.2 Global: O H H O 2 1 2 2 2 + → EQN I.3Le flux de charges ioniques qui traverse l'électrolyte, doit être équilibré par un circuit extérieur. L'énergie électrique est donc produite par cet équilibre.
I.1.2.2. Géométries de piles existantes
Plusieurs cellules élémentaires sont connectées entre elles par un matériau d’interconnexion
él ec tr o ly te an o d e ca th o d e e -e -Combustible ou Hydrogène Comburant ou Oxygène H2+O H2O+2e - 1 /2O2+2e - O 2-Sous-produit Sous-produit O 2-Dispositif
conducteur électronique afin de constituer la batterie. Plusieurs architectures ont été étudiées pour confectionner ces cellules afin d’optimiser le fonctionnement de la batterie, par exemple les géométries tubulaires et planaires. Mais d’autres technologies ont également été imaginées par différentes sociétés.
Configuration tubulaire
Cette technologie a été développée par la Cie Westinghouse et Brown Boveri Corporation. La cellule élémentaire est constituée d’un tube support (anode poreuse) sur lequel on dépose l’électrolyte dense et la cathode poreuse. Le système tubulaire Westinghouse est représenté en figure I.2.
Configuration bipolaire
Cette technologie permet d’obtenir directement une batterie avec empilement de cellules élémentaires. Le schéma de principe correspondant est représenté en figure I.3(a), et une structure à empilement comportant des plaque métalliques bipolaires est représenté en figure I.3(b).
a b
Figure I.2. Configuration tubulaire [4]: (a) cellule (b) empilement des éléments.
a b
Configuration monolithique
La batterie monolithique à empilement de plaques a été développée par Argonne National Laboratory, représentée en figure I.4.
I.1.3. Matériaux utilisés pour les piles SOFC
Comme mentionné ci-dessus, une pile à combustible de type SOFC est constituée par une anode, un électrolyte, une cathode et une interconnexion. Ces matériaux doivent posséder une stabilité chimique en température de fonctionnement afin d’éviter les réactions chimiques entre eux. Leurs coefficients de dilatation thermique doivent être proches afin de diminuer la contrainte thermique et permettre une bonne tenue mécanique des interfaces lors des cyclages en température de la pile. L’électrolyte doit présenter une bonne conductivité ionique, et les électrodes doivent posséder de bonnes propriétés catalytiques.
I.1.3.1. Cathode
La cathode est le siège des réactions de réduction de l’oxygène. Outre les contraintes de stabilité chimique et thermique vis-à-vis de l’électrolyte et de l’oxygène, elle doit avoir une conductivité électrique élevée, et une activité électro-catalytique aussi élevée de manière à réduire l’oxygène. Elle doit avoir une porosité suffisante pour permettre le transport de l’oxygène gazeux vers les sites actifs.
Les oxydes à base de LaMO3 (M=Co, Mn, Cu, Fe) de structure pérovskite présentent les
meilleures caractéristiques [18] pour cette application. Toutefois et afin d’augmenter leurs propriétés, un dopage généralement au strontium est effectué sur le site de lanthane. Le manganite de lanthane dopé au strontium La1-xSrxMnO3 (x=0,2, 0,3, ou 0,4) est utilisé
généralement dans la pile de type SOFC avec l’électrolyte YSZ. Sa conductivité électrique est de l’ordre de 130 S·cm-1 à 700°C.
Les cobaltites possèdent généralement les meilleures conductivités électriques et une bonne propriété de conduction ionique. Outre les cobaltites, les ferrites ont été largement étudiées. La performance des cathodes peut être augmentée par un mélange d’une certaine quantité de matériau d’électrolyte avec le matériau de la cathode afin de multiplier les zones de point triple [19, 20].
I.1.3.2. Electrolyte
Les qualités requises pour cet élément sont:
-Une structure cristalline stable entre l’ambiante et la température de fonctionnement, -Une conductivité ionique élevée à la température de fonctionnement,
-Une inertie chimique vis-à-vis des gaz présents aux électrodes et vis-à-vis des matériaux électrodes.
L’électrolyte à base de Zircone
La zircone à l’oxyde d’yttrium, notée YSZ, est généralement le matériau électrolyte de la pile de type SOFC. La zircone dopée à l’yttrium (YSZ) avec 8 à 10% molaire de Y2O3 présente
une conductivité purement ionique à température supérieure à 800°C.
Généralement encore, la zircone se présente sous forme cubique à haute température. La stabilisation de la zircone cubique, à température ambiante, peut être réalisée par création de solutions solides de substitution où l’ion Zr4+ est remplacé par des cations de valence
inférieure (Ca2+, Mg2+, Y3+). Dans le même temps, les lacunes d’oxygène sont créées, ce qui
peut permettre le passage des ions O2- au travers de l’électrolyte. Le mécanisme de création
des ions O2- peut être expliqué par l’équation suivante:
• • + + → O X O Zr ZrO 3 2O 2M' 3O V M 2 EQN.I.4
L’électrolyte à base de Cérine
Contrairement au matériau ZrO2, la cérine de formule CeO2 a une structure de type fluorine
qui n’a pas besoin d’être stabilisée. Afin d’augmenter sa conductivité électrique, il est nécessaire d’introduire des ions qui remplacent les ions Ce4+. Ce dopage peut créer des
lacunes d’oxygène qui conduisent à sa conductivité. La structure fluorite dopée par les ions M2+ ou M3+ est représentée en figure I.5.
Les cérines (CeO2) dopées Gadolinium (GDC), Yttrium (YDC) ou Calcium(CDC) avec une
structure fluorite, présentent de bonnes conductivités électriques qui sont données en figure I.6
Cependant, elles présentent des conductivités électroniques élevées, spécialement aux faibles pressions partielles d’oxygène P(O2). Pour cette condition, CeO2 devient CeO2-x et la
conductivité « n-type » augmente avec une la pression partielle P(O2)1/4 [10]. Ainsi, Figure I.6. Conductivité électrique des électrolytes à base de Cérine
(○)(CeO2)0,8(Sm1,5O)0,2 (△)(CeO2)0,8(GdO1,5)0,2 (▽)(CeO2)0,8(YO1,5)0,2
(□)(CeO2)0,8(CaO)0,2 (■)CeO2 (●)(ZrO2)0,85(YO1,5)0,15 [11].
Figure I.5. Cellule de base de la moitié de la structure fluorite montrant le poste vacant du dopant cation-oxygène[3].
l’utilisation des cérines comme électrolyte des piles SOFC est limitée à cause de leurs conductivités électroniques.
Les apatites
Les composés de structure apatite ont été développés par Nakeyama et al[21-23] dans les années 90s. Leur formule générale est A10-x(MO4)6O3±y où M représente l’élément de terre
rare ou l’élément alcalin et X représente l’élément de bloc P(P, Si ou Ge).
La conductivité électrique pour les compostions A10(SiO4)6O3 est présentée sur la figure I.7.
L’élément La10(SiO4)6O3 représente la meilleure conductivité électrique des compostions
A10(SiO4)6O3 (A= La, Pr, Nd, Sm, Gd, Dy) pour des températures comprises entre 200°C et
800°C. La conductivité électrique de valeur 1,02×10-2S·cm-1 est obtenue à 700°C [9].
Récemment, les oxydes de type apatite dopés par MO ou M2O3 (M=Mg, Zn, Sr, Ca, Ti, Fe,
etc.) ont été étudiés dans le but toujours d’augmenter la conductivité électrique [24-31, 5].
I.1.3.3. Anode
Pendant le fonctionnement de la pile à combustible de type de SOFC, l’anode se trouve à côté des gaz combustibles. Elle doit avoir les propriétés suivantes:
- Une bonne stabilité chimique, morphologique et dimensionnelle pour des conditions réductrices du combustible.
- Une conductivité électrique suffisante afin de permettre un passage des électrons à la température de fonctionnement.
- Une stabilité vis à vis de tous les composants de la pile, et en particulier avec le support et l’électrolyte.
- Un coefficient de dilatation proche de celui de l’électrolyte afin d’éliminer ou de diminuer les contraintes thermiques.
- Une porosité suffisante pour permettre aux gaz combustibles d’atteindre les sites actifs. - Une activité catalytique suffisamment grande.
Généralement, l’anode est constituée par les deux matériaux : le métal catalytique (Ni, Cu , Pt etc.) et la céramique qui constitue l’électrolyte. Ni-YSZ et Ni-CDG sont les deux types d’anode couramment utilisés.
Cermet Ni-YSZ
Jusqu'à présent, les composites métal-céramique constitués par les matériaux YSZ et Ni, où la phase métallique agit en tant que conducteur électronique et catalyseur, sont les matériaux communs de l’anode de la pile de type SOFC[32-39]. YSZ peut augmenter la densité de puissance par augmentation des zones de point triple,et diminuer la contrainte thermique par ajustement des coefficients de dilatation.
Le ratio volumique entre Ni et YSZ est critique pour la performance de l’anode. Normalement, un pourcentage volumique de Ni supérieur à 30% peut assurer la conductivité électronique du cermet.
Cermet Ni-CDG
Depuis les premières tentatives (dans les années 1960) d’utilisation de la cérine pour les anodes de la pile SOFC [40, 41], les anodes à base de cérine sont considérées comme possédant une bonne conductivité et une bonne activité catalytique pour des gaz combustibles, et spécialement pour les hydrocarbures.
I.1.3.4. Interconnexion
L’interconnecteur peut correspondre à une couche métallique ou céramique qui permet d’assembler des cellules élémentaires en série ou en parallèle et finalement de constituer les batteries. Il doit séparer le gaz combustible de l’oxygène. Outre les critères de sélection requis pour les matériaux d’électrode en termes de compatibilité chimique et de dilatation thermique, les matériaux d’interconnexion doivent être stables en atmosphères réductrices et oxydantes, et doivent posséder une conductivité électrique prédominante.
Les interconnecteurs céramiques (par exemple LaCrO3 dopé par Ca, Mg ou Sr) [42, 43], ont
été largement utilisés pour les piles SOFC à haute température. Cependant, la difficulté de fabrication et le coût élevé, en limitent leurs utilisations [44]. Heureusement, il est possible d’utiliser des interconnecteurs métalliques pour les piles SOFC à température basse ou intermédiaire (500-800°C), par exemple ceux constitués à partir d’alliage à base de Fe, Ni ou
Cr [45, 46].
I.1.4. Pile IT-SOFC
Dans les conditions normales d’utilisation, la pile à combustible à oxyde solide avec l’électrolyte YSZ est capable de fonctionner à 1000°C. Néanmoins, à cette température de fonctionnement, cela provoque quelques désavantages par exemple, de contrainte thermique, d’interactions chimiques entre l’électrolyte et les électrodes, de coût de fabrication, ou de réduction de la durée d’utilisation de la pile [47]. Pour éviter ces désavantages, la pile à combustible à oxyde solide à température intermédiaire, qui fonctionne à température entre 600 °C et 800°C, est étudiée. Malheureusement, la diminution de température entraîne une baisse de la conductivité électrique de l’électrolyte et des propriétés catalythiques. Il est alors nécessaire de développer de nouveaux matériaux d’électrolyte et d’électrodes pour d’améliorer la performance électrique globale de la pile.
I.2. Apatites
La formule chimique générale des apatites est Me10(XO4)6Y2, où Me représente généralement
un cation divalent, XO4 représente un anion trivalent, et Y représente un anion monovalent.
Ces apatites ont une structure cristalline dans le système hexagonal compact de groupe spatial P63/m[48].
Le tableau I.1 montre quelques exemples de substitutions possibles dans la structure de l'apatite. Il y a deux types de substitution dans cette structure [49]:
- Soit par des ions de même valence que ceux de l’apatite (fluorapatite ou hydroxyapatite): les différences de rayons ioniques engendrent dans ce cas des distorsions de maille.
- Soit par des ions de valence différente: on a dans ce cas non seulement des distorsions de mailles, mais aussi création de défauts ponctuels afin de compenser les charges. Il est à noter que ces défauts ponctuels n’apparaissent que sur les sites Me ou Y.
Tableau I.1. Quelques exemples de substitutions possibles dans la structure de l'apatite.
Formulation générale Me10 (XO4)6 Y2
Ca2+ PO43- F-
Sr2+ AsO
43- Cl-
Substitutions stœchiométriques Ba2+ VO43- OH- Pb2+ MnO43- Br-
… … …
Ln3+ SiO
44- O
2-Zr3+ CO42- CO3 2-Substitutions non stœchiométriques Cs3+ PO42- …
Na3+ HPO42- lacunes
… …
I.2.1. Structure
Les apatites à base de silicate ont été recherchées dans les années 1990 en tant qu’électrolyte de la pile de type de SOFC. Afin de mieux comprendre le mécanisme de conductivité ionique, il est nécessaire de rechercher la structure de l’apatite. La Figure I.8 représente la structure cristalline de l’apatite de formule générale (Me-2)
10(XO4-3)6(Y-1)2. La position des atomes et
leur symbolisation, dans le groupe d’espace P63/m sont données dans le tableau I.2.
Tableau I.2. Site de symétrie du groupe d’espace P6/m, d’après les Tables Internationales de Cristallographie
Site Multiplicité et Symbole de
Wyckoff Positions équivalentes
Y 2a (0; 0; 1/4), (0; 0; 3/4) Me(I) 4f (1/3; 2/3; z), (2/3; 1/3; z), (2/3; 1/3; z+1/2) , (1/3; 2/3; 1/2-z) Me(II) X O(I) O(II)
6h (x; y; 1/4), (1-y; x-y; 1/4), (y-x;1-x; 1/4), (1-x;1-y;
3/4), (y; y-x; 3/4), (x-y; x; 3/4)
O(III) 12i
(x; y; z), (1-x; 1-y; 1-z), (1-x; 1-y; 1/2-z), (1-y; x-y; z), (y; y-x; 1-z), (y; y-x; 1/2+z), (1-y; x-y; 1/2-z), (y-x;1-x; z), (x-y; x; 1-z), (x-y; x; 1/2-z), (x-y;1-x;
.
Les cristaux d’apatites appartiennent au groupe d’espace P63/m, constitués par un tétraèdre
XO4, anion Me et cation Y. Les ions X sont au centre du tétraèdre XO4 coloré en bleu dans la
figure I.8, est constitué par l’ion X qui se trouve au centre de tétraèdre et quatre ions O qui sont au sommet. Les cations Me se trouvent sur deux types de site: MeI se trouve aux sites 4f ;
MeII se trouvent aux sites 6h. Les ions Y- sont distribués le long de l’axe sénaire hélicoïdal et
aux sites 2a.
Il y a deux types de tunnels parallèles à l’axe c: -les premiers sont occupés par des cations Me I .
-les seconds tunnels qui ont des diamètres plus grands que les précédents, contiennent les six autres cations Me II.
Dans le cas d’utilisation des apatites en tant qu’électrolyte pour piles à combustible à oxyde solide, l’anion Y- sera l’ion O2- afin d’élever la conductivité électrique, Me sera l’élément de
terre rare ou l’élément alcalin et X représente l’élément de bloc P (P, Si ou Ge).
La structure cristalline de La9,33(SiO4)6O2 est du même type que celle décrite dans le
paragraphe précédent. Dans ce cas, les changements de valence du cation (Me2+ →La3+) et de
l’anion moléculaire (XO43- →SiO44-) impliquent une compensation des charges électriques
par création de 0,67 lacune sur le site Me(notée ϒ). Sa formule totale est La9,33ϒ0,67(SiO4)6O2.
I.2.2. Propriétés électriques des apatites
Les apatites à base d’élément Ge ou Si présentent de bonnes conductivités électriques. Spécialement, les apatites de formule générale La9,33+x (SiO4)6O2+1,5x ont une bonne stabilité
chimique et une bonne propriété électrique [50-53] pour leur utilisation comme électrolyte de pile de type IT-SOFC. Elles ont des conductivités électriques élevées et des énergies d’activation faibles (présentées dans le tableau I.3).
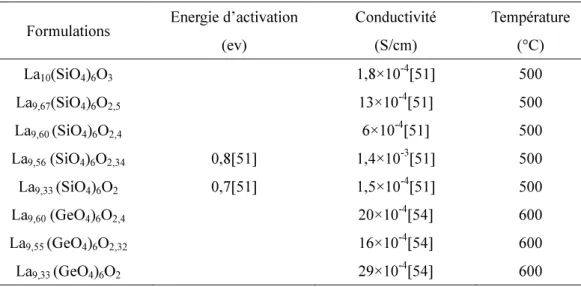
Tableau I.3. Propriétés électriques des apatites de type La9,33+x (Si/GeO4)6O2+1,5x.
Formulations Energie d’activation
(ev) Conductivité (S/cm) Température (°C) La10(SiO4)6O3 1,8×10 -4 [51] 500 La9,67(SiO4)6O2,5 13×10 -4 [51] 500 La9,60 (SiO4)6O2,4 6×10 -4 [51] 500 La9,56 (SiO4)6O2,34 0,8[51] 1,4×10-3[51] 500 La9,33 (SiO4)6O2 0,7[51] 1,5×10-4[51] 500 La9,60 (GeO4)6O2,4 20×10 -4 [54] 600 La9,55 (GeO4)6O2,32 16×10 -4 [54] 600 La9,33 (GeO4)6O2 29×10 -4 [54] 600
H.Yoshioka [55] a montré l’évolution de la conductivité électrique à 800°C de compositions de type La9,33+x (SiO4)6O2+1,5x (pour x<0 et x>0). Ces matériaux ont des conductivités
électriques presque constantes de 1×10-4 S/cm lorsque x ≤ 0,4. Ces conductivités
s’augmentent rapidement lorsque 0,4 <x <0,59. Dans le cas où 0,59 ≤ x ≤ 0,92, cette conductivité électrique peut atteindre 20×10-3 S/cm puis elle diminue à nouveau pour x> 0,92.
Il apparaît alors que la conductivité présente un maximum pour x =0,67.
Influence des substitutions sur les propriétés électriques
Les compositions de type de La9,33+x(Si/GeO4)6O2+3x /2 dopées par MO ou M2O3 (M : Mg, Ca,
Sr, Co, Cu, Al, Zn, Mg, Ti, Ge, Fe…) sont également intéressantes car elles montrent qu’il est possible d’améliorer les propriétés de conductivité électrique. Les dopants peuvent en effet modifier les propriétés électriques en changeant la quantité des porteurs de charges O2- ou
encore la taille des tunnels.
Il y a trois types de substitutions possibles selon les sites de substitution : -Site La substitution par: Mg, Ca, Sr, Ba, Co, Ni, Cu, Mn, Bi.
-Site Si substitution par: B, Al, Ga, Zn, Mg, Ti, Ge, Fe, Co, Ni, Cu, Mn, P. -Sites La et Si substitution par: Mg, Mn, Ni, Cu, Co.
Le tableau I.4 permet de faire la comparaison des propriétés électriques des apatites de type La9,33+x(SiO4)6O2+1,5x dopées par M2+ ou M3+. Les apatites La9,33+x (SiO4)6O2+1,5x dans
lesquelles on substitue une partie des cations Si4+ présentent la plus haute conductivité
ionique et l’énergie d’activation la plus faible.
Tableau I.4. Propriétés électriques des apatites de type La9,33+x (SiO4)6O2+1,5x dopées par MO ou M2O3.
Site de substitution Formules Energie d’activation (eV) Conductivité électrique (S/cm) Température (°C) La La8,67 Ba(SiO4)6O2[56] 0,67 1,1×10 -4 500 La8,67Sr (SiO4)6O2[56] 0,87 8,3×10 -5 500 La8,67Mg (SiO4)6O2[56] 1,13 3,6×10 -6 500 La8,33Mg1,5 (SiO4)6O2[56] 1,23 1,2×10 -6 500 La8,67 Ca(SiO4)6O2[56] 0,86 5,8×10 -5 500 La9Mg0.5Si6O26[57] 0,98 2,1×10 -5 500 Si La8,67Ga0,5Si5,5O26[56] 0,67 4,6×10 -4 500 La10GaSi5O26[56] 0,70 2,4×10 -3 500
La10BSi5O26,5[56] 0,68 1,1×10 -3 500 La9.67Si5.5Mg0.5O26[57] 0,67 3,0×10 -3 500 La et Si La9.33Mg0.5Si5.5Mg0.5O26[57] 0,80 1,0×10 -4 500
I.2.3. Mécanismes de conduction
Afin de comprendre le mécanisme de conduction électrique des apatites, il est nécessaire de s’assurer de la présence des porteurs et des tunnels de conduction. Les conductions des différentes compositions d’apatites ont été mesurées dans différentes gammes de pressions partielles d’oxygène [29, 58, 59]. Ces études montrent que ces conductions sont insensibles à la pression partielle en oxygène, et que le nombre de transporteurs ioniques est suffisamment élevé. Finalement, il revient à dire que la conduction dans les apatites est assurée principalement par le déplacement des ions oxydes. Cette propriété permet d’éviter le court-circuit dans la pile de type de SOFC avec ce genre d’électrolyte à base apatite.
Dans l’électrolyte solide, la conduction s’effectue par le transport des porteurs de charges. Les principaux mécanismes d’échange et de transport sont représentés en figure I.9 :
Figure I.9. Schéma des principaux mécanismes de diffusion (1) échange direct (2) échange par cycle (3) Transport lacunaire (4) Transport Interstitiel direct (5) Transport Interstitiel indirect
- Echange direct : Un ion s’échange avec un autre ion voisin. Ce mécanisme crée des distorsions et des répulsions locales très importantes. Il peut être observé dans les composés ternaires ou plus complexes.
- Echange par cycle : Dans ce cas, il y a un mouvement coopératif de plusieurs espèces. Ce mécanisme ne suppose pas a priori l’existence de défauts ponctuels permanents dans le cristal, même si lors de la transition un désordre local apparaît nécessairement.
- Transport lacunaire : Le déplacement s’effectue par passage d’un atome d’un site normal à un site voisin vide. Cet atome pourra poursuivre son déplacement quand une nouvelle lacune se trouvera à son voisinage. Ces lacunes peuvent être formées, sous l’action de la température, par transfert d’atomes de A et B de sites normaux (pour un solide de composition BmAn) à l’intérieur du cristal sur les sites normaux à la surface du cristal.
- Transport Interstitiel direct : Dans ce cas, un atome passe d’un site interstitiel du réseau à un site interstitiel adjacent vide.
- Transport Interstitiel indirect : L’atome en position interstitielle passe, dans un site interstitiel voisin, en déplaçant un atome de même nature situé sur un site normal. Ce mécanisme met en jeu les sauts simultanés de deux espaces voisins, mais il faut remarquer que ces deux sauts ne sont pas nécessairement colinéaires (déplacement selon une sinusoïde).
- Transport « Crowdion » : Enfin, des mécanismes de sauts coopératifs, par exemple du type crowndion ont été proposés pour expliquer la conductivité dans certains conducteurs ioniques contenant une grande concentration de porteurs mobiles.
Plusieurs moyens sont utilisés afin de rechercher la microstructure cristalline et de trouver le tunnel de conduction dans les oxyapatites [60-62, 30, 49]. On peut citer la diffraction de rayons X, la diffraction de neutrons, la diffusion de Raman, et la simulation atomistique. Comme présenté dans le paragraphe précédent, il y a deux tunnels de circulation des ions O
2-dans les apatites. Les ions semblent circuler principalement 2-dans les tunnels de grande dimensions (notés dans la figure I.8) le long de l’axe c. Ce phénomène a été confirmé en mesurant la conductivité parallèlement et perpendiculairement à l’axe c des oxyapatites du monocristal. La conductivité « parallèle » est environ dix fois plus grande que celle « perpendiculaire » à l’axe c (donnée dans le tableau I.3).
Afin de rechercher le mécanisme de conduction en détail, des modèles atomiques des éléments La9,33(SiO4)6O2 et La8Sr(SiO4)6O2 ont été construits. Le matériau La9,33(SiO4)6O2 a
une bonne conductivité électrique alors que le matériau La8Sr(SiO4)6O2 présente une très
faible conductivité [7]. L’oxygène interstitiel (montré dans la figure I.10), plutôt que d'être situé au centre du canal, se trouve alors situé à la périphérie du canal. Ce résultat a été confirmé par la diffractométrie de neutrons, par la simulation atomistique ainsi que dans
d’autres études [65, 28].
En plus d’identifier la position inertielle du site le plus favorable, il est nécessaire de rechercher les modèles possibles de conduction. La simulation atomique ainsi que la simulation de la dynamique moléculaire ont été utilisées par Julian R. Tolchard et al [7]. Les mécanismes de conduction des matériaux La9,33(SiO4)6O2 et La8Sr(SiO4)6O2 sont différents.
Le mécanisme de conduction dans le matériau La8Sr(SiO4)6O2 se fait par les lacunes
(montrées sur la figure I.11), mais celui du matériau La9,33(SiO4)6O2 se fait grâce au
mécanisme interstitiel. Le chemin de la conduction interstitielle, qui est dit « sinusoïdal », est représenté en figure I.12. Dans ce cas, la migration des ions oxydes se fait le long de sites interstitiels situés au bord des grands canaux de l’oxyapatite.
Figure I.10. Site oxygène interstitiel (sphère orange) à la périphérie du canal, et treillage associé (sphère violette =La, sphère bleue =Si) [5].
Figure I.11. Chemin de migration lacunaire des ions oxyde dans le matériau La8Sr(SiO4)6O2.
L’anisotropie de conduction des oxyapatites du monocristal (donnée dans le tableau I.5) montre que les canaux de l'oxygène sont responsables de la conduction élevée de l’oxyde ionique. L’augmentation de la conduction le long de l’axe c, n’est pas aussi élevée que prévu. En plus, l'énergie d'activation pour la conduction le long de l’axe c et le long de l’axe a ou b sont assez similaires, ce qui suggère que, bien que la voie de conduction principale soit le long des canaux d'ions oxyde, la conduction perpendiculaire de l’axe c est également non négligeable. C’est-à-dire qu’il y a un mécanisme de conduction relatif aux inter-canaux.
Tableau I.5. Evolution de la conductivité électrique dans les deux directions, parallèle et perpendiculaire à l’axe c, de monocristaux de structure apatite [63, 64].
Composition σ(S/cm) at 500°C Ea (eV) (basse Temp./haute temp.) Parallele à l’axe c 1,2×10-2 0,77/0,50 Sm9,33(SiO4)6O2 Perpendiculaire à l’axe c 2,6×10-3 0,69/0,49 Parallele à l’axe c 6,4×10-2 0,68/0,33 Pr9,33(SiO4)6O2 Perpendiculaire à l’axe c 1,3×10-3 0,62/0,48 Parallele à l’axe c 1,3×10-2 0,62/0,31 Nd9,33(SiO4)6O2 Perpendiculaire à l’axe c 1,2×10-3 0,61/0,50
Une explication possible est proposée par la modélisation dans la littérature [5]. Le chemin de conduction inter-canaux est représenté sur la figure I.13. La relaxation locale autour du site
Figure I.12. Chemin de migration interstitiel des ions oxyde dans le matériau La9,33(SiO4)6O2 (a)vu de l’axe a, (b) vu perpendiculaire à l’axe c[5].
interstitiel conduit à la réduction de la distance par rapport à une unité voisine SiO4. Cela
pourrait effectivement créer un chemin, par laquelle un oxyde interstitiel-ion est déplacé entre des canaux adjacents par une série de deux processus de type ''SN2'' (SN2 = substitution
nucléophile bimoléculaire), avec une rotation d'accompagnement des tétraèdres.
I.3. Projection thermique
La projection thermique regroupe les procédés qui permettent de fondre et projeter un matériau sur un support où il se solidifie, afin d’élaborer le dépôt ou le revêtement. Récemment, l’intérêt de la projection thermique pour préparer les piles à combustible de type SOFC [66-73, 8, 74-80] s’est amplifié dû à ses avantages en termes d’efficacité de fabrication élevée, d’un coût de fabrication faible et d’une flexibilité importante entre autres.
I.3.1. Historique et principe de la projection thermique
La première utilisation de la projection thermique remonte au début du 20ème siècle par M.U.Schoop, en Suisse. Il eut l’idée d’utiliser un chalumeau oxyacétylénique pour projeter un métal à bas point de fusion sur un substrat (pièce à revêtir) [81]. Cette technique était utilisée afin de protéger des pièces en acier par des revêtements de zinc et d’aluminium. Depuis
1911: Utilisation de la projection à l’arc électrique par M.U.Schoop
Figure I.13. Chemin de conduction entre des canaux adjacents via le processus de type ''SN2''avec une rotation d'accompagnement des tétraèdres, obtenus à partir des résultats de
simulation du matériau La9.33(SiO4)6O2. L'intégration d'une périphérie interstitielle oxyde-ion
(jaune) (a) les forces de l 'oxygène de silicate (orange) entre les deux unités SiO4 formant une
unité Si2O9 (b), l'unité supérieure de silicate de rotation pour former une unité Si2O9 avec une
unité voisine de silicate (c), et de l'oxygène sur le silicate de haut unité (vert) est lâché en tant que interstitielle dans un canal différent (d)[5].
1951: Invention de la projection plasma 1955: Naissance du canon à détonation
1975: Création de la projection plasma sous faible pression de gaz inerte 1983: Début de la projection à flamme supersonique (HVOF)
1991: Emergence de la projection plasma sous gaz neutre à pression supérieure à la pression atmosphérique
1995: Développement de la projection froide.
La projection thermique consiste à utiliser une source de chaleur afin de fondre et d’accélérer un matériau en le confinant pour qu’il vienne s’écraser sous forme de lamelles sur le substrat et construire le dépôt par empilement successif de ces lamelles [82, 83]. Le matériau à projeter se présente généralement sous forme de poudre, fils ou baguettes [82].
La source de chaleur doit pouvoir fournir suffisamment de chaleur pour chauffer le matériau et produire un jet gazeux capable de transporter le matériau jusqu'au substrat. Plusieurs procédés de projection thermique peuvent être différenciés par la source d’énergie mise en œuvre :
- Source d’énergie chimique de combustible : La projection à la flamme
Ce procédé utilise la combustion d’un gaz pour porter le matériau à déposer à sa température de fusion et le projeter sur le substrat. Ce procédé permet de déposer des matériaux, par exemple de type Zn, Al, Ni, Al2O3 revêtu de Ni, etc. Il est possible de projeter le matériau
sous forme de poudre ou de fils. Ce procédé est le plus simple et le moins coûteux parmi les techniques de projection thermique. Mais il est limité en température et en vitesse de projection.
La projection à la flamme supersonique
Elle utilise le même principe que la projection à la flamme. Mais dans ce cas, une vitesse de gaz de 1800 à 2200 m·s-1 et une température de 2500 à 2800 °C sont atteintes. Elle permet
donc de réaliser un dépôt plus dense que celui réalisé par la projection à la flamme.
La projection par détonation
Comme la projection à flamme supersonique, cette projection a le même principe que la projection à la flamme. Dans ce cas, la combustion utilisée comme source de chaleur est discontinue. Elle se produit dans un canon à l’aide d’une bougie qui enflamme un mélange acétylène-oxygène par exemple. La poudre est chauffée par cette explosion et entraînée par l’onde de choc (3000 m·s-1).
-Source d’énergie électrique : La projection à l’arc électrique
Elle utilise comme source de chaleur pour fondre le matériau un arc électrique entre deux électrodes qui se présentent sous forme de fils consommables. Ce procédé de projection est simple et économique. La température de zone de fusion peut être de l’ordre de 6000K. Le matériau fondu est accéléré par l’air ou un gaz neutre comprimé. Ce procédé est limité aux matériaux conducteurs.
La projection plasma
Dans ce procédé, le plasma est généré à partir des gaz injectés dans une torche de courant continu ou d’induction. Les propriétés du plasma thermique sont favorables à des transferts thermiques et cinétiques. Le plasma a une température suffisamment élevée (environ 15000°C à cœur) pour fondre tous les matériaux et une vitesse assez élevée (de 200 à 2000 m.s-1) pour accélérer les matériaux [83]. Ce procédé sera décrit plus précisément dans le
chapitre I.2.3.
Projection à froid
Cette technique très récente est encore en développement. Elle consiste à utiliser un jet de gaz sous haute pression pour projeter des particules sous forme solide à grande vitesse ; c’est avec la déformation plastique que les particules s’adhérent au substrat. Ce procédé permet de diminuer l’oxydation des particules et de limiter l’échauffement des matériaux et des contraintes résiduelles.
I.3.2. Projection plasma
La projection plasma est un procédé qui permet de projeter des particules métalliques ou céramiques dans un état fondu ou semi-fondu, sur le substrat. Elle a de très nombreuses applications dans les domaines industriels [84, 85, 72, 8, 1, 86-88] : par exemple pour les revêtements dans le domaine du biomédical, pour les dépôts pour des applications tribologiques, pour les couches de protection contre la corrosion, les barrières thermiques, les revêtements de protection contre les gaz chauds, les couches isolantes électriques à haute température, etc. Aujourd'hui, plus de 90% des systèmes industriels de projection plasma utilisent les torches plasma de courant continu [89]. Dans cette partie, on présentera principalement la projection plasma de courant continu.
Le plasma produit par le passage d’un écoulement gazeux dans un arc électrique, est utilisé en tant que source de chaleur. La poudre injectée dans le plasma, est chauffée et projetée sur le substrat. Ce procédé peut se décomposer en 4 étapes différentes (représentées sur la figure I.14) :
- 1ère étape : génération du plasma : Un arc électrique de forte intensité est généré entre l’anode et la cathode à l’aide d’une alimentation électrique afin d’ioniser les gaz (argon, hydrogène, hélium ou azote). Le plasma créé, est électriquement neutre et constitué d’un mélange de molécules, d’ions, d’atomes et d’électrons.
Les plasmas ont des propriétés de hautes températures, de vitesses élevées, et possèdent de bonnes conductivités thermique et électrique. La nature des gaz jouent un rôle important sur les propriétés du plasma [90]. L’ajout d’hydrogène entraîne par exemple une augmentation de l’enthalpie du plasma. De par sa conductivité thermique, l’hydrogène favorise aussi le transfert de quantité de chaleur aux particules. L’ajout d’hélium dans les gaz, sert à augmenter la viscosité du jet.
- 2ème étape : injection de la poudre à l’aide d’un gaz porteur : Normalement, le matériau sous forme de poudre est injecté dans le plasma jet à l’aide d’un gaz porteur, soit à l’intérieur, soit à l’extérieur de l’anode. Afin d’augmenter le temps de contact entre plasma et particules ou encore permettre d’éviter le colmatage des particules fondues sur l’anode, des angles différents entre l’injecteur de poudre et l’axe de plasma jet, peuvent être ajustés. Le débit de gaz porteur joue alors un rôle important sur la trajectoire des particules.
- 3ème étape : chauffage et accélération des particules dans le jet de plasma : les particules
sont fondues et accélérés par le jet de plasma. L’état de fusion des particules dépend de la température du jet de plasma et du temps de séjour des particules dans le jet. Le principal mécanisme de chauffage des particules est celui de la conducto-convection dans la couche limite thermique [91]. Les autres paramètres jouent aussi un rôle sur le chauffage, par exemple: la morphologie de la poudre ou encore la conductivité thermique du matériau. L’accélération des particules est due à plusieurs forces qui sont la force de traînée, la force d’inertie, la force de gravité, la force due au gradient de pression. En général, la force de traînée est la force principale, elle est exercée par le plasma, et est fonction de la taille des particules, de la viscosité du plasma et de la vitesse relative entre le jet et les particules.
- 4ème étape : construction du dépôt : Le dépôt réalisé par projection plasma se construit par empilements de lamelles issues de particules plus ou moins bien fondues. En effet, lors de la collision des particules avec le substrat, celles-ci prennent une forme écrasée ressemblant à des lamelles. L’énergie cinétique et thermique des particules se transforment alors en déformation visqueuse et en énergie de surface. La formation du dépôt peut être divisée par les étapes suivantes:
La formation d’une lamelle écrasée, la formation d’une couche constituée par empilement de lamelles écrasées, le surchappement des cordons pour former une passe, la dernière étape correspondant au temps entre deux passages successifs de la torche au même endroit. L’étalement de la particule peut être décomposée en trois étapes de l’impact initial (une phase très courte, de quelques nanosecondes, correspondant à l'impact initial avec le plus souvent un phénomène d’éclaboussure), à l’étalement de la particule (une deuxième phase de l'ordre de la microseconde), et enfin au refroidissement et à la solidification de la lamelle (quelques microsecondes pour le refroidissement de la lamelle), comme montrées sur la figure I.15. L’étalement des particules est un phénomène complet qui dépend de nombreux paramètres.
La microstructure du dépôt réalisé par la projection plasma est illustrée en figure I.16. Le revêtement comprend certains défauts: des particules infondues, des porosités, des fissures interlamellaires (macrofissuration), ou encore des fissures intralamellaires (microfissuration).
La microstructure dépend des paramètres de la projection plasma. Quelques paramètres importants influençant la qualité du dépôt [83] sont listés ci après : puissance, pression du gaz principale, pression de gaz auxiliaire, débit de poudre, angled'injection, rugosité de la surface, température du substrat, distance de projection, atmosphère de projection.
I.3.2.2. Développement de la projection plasma
La projection plasma sous air est la plus couramment utilisée, car elle permet de projeter des matériaux insensibles à l’oxygène. Afin d’augmenter le domaine d’application de la projection plasma, plusieurs procédés sont développés :
-La projection en atmosphère inerte
Ce procédé représente une solution pour projeter les matériaux sensibles à l’oxygène. Généralement, cela est réalisé dans une chambre remplie d’argon.
-La projection plasma sous haute pression
Dans une atmosphère à haute pression, l’expansion du plasma est beaucoup plus faible qu’à pression atmosphérique (figure I.17). On peut ainsi confiner la puissance du plasma et améliorer le chauffage de la poudre.
Figure I.16. Représentation schématique de l’empilement de lamelles en projection plasma (a)[1] et microstructure d’un dépôt (b)[13] 1 substrat fondu, 2 défaut d’adhérence, 3 macrofissures parallèles à la surface dues aux contraintes thermiques, 4 microfissures interlamellaires, 5 macrofissures perpendiculaires à la surface, 6 porosité ouverte, 7 microfissures interlamellaires dues aux contraintes de trempe 8 particule infondue.
-La projection plasma sous faible pression
Avec une faible pression, l’expansion du plasma est beaucoup plus grande qu’à la pression atmosphérique (montré aussi sur la figure I.17). Un jet de plasma expansé permet d’accélérer des particules à une vitesse plus grande. Cela contribue à améliorer l’étalement des particules, donc la densité et l’adhérence du dépôt. Mais l’expansion du plasma diminue la densité d’énergie, ce qui s’accompagne alors de la difficulté de projeter les matériaux à haut point de fusion. C’est pourquoi, la conception d’un procédé de type PS-PVD est donc proposé, qui permet d’évaporer les matériaux avec le plasma et de fabriquer les revêtements de structure colonnaire de type PVD. Ce procédé est développé au LERMPS (France) et Sulzer (Suisse). La figure I.18 représente les microstructures de revêtement de YSZ et de Cu de structure colonnaire.
Figure I.17. Evolution du plasma en fonction de la pression dans l’enceinte de projection [8].
Figure I.18. Revêtement de YSZ de structure colonnaire déposé par PS-PVD (a)YSZ [6] (b)Cu.
I.3.3. Utilisation de la projection thermique pour l’élaboration de la pile de
type SOFC
Au cours des dernières années, la projection plasma a été largement appliquée pour élaborer des composants de la pile à combustible de type SOFC [68, 76, 77, 80]. Elle a la capacité d’augmenter l'efficacité de la production et de diminuer le coût de fabrication. Différents types de projection plasma (APS, VPS, et SPS) ont été utilisés pour fabriquer les éléments anode, cathode et électrolyte.
I.3.3.1. Fabrication de l’anode
La couche constitutive de l’anode doit être poreuse afin de permettre au combustible d’atteindre l’électrolyte. Généralement, le dépôt réalisé par projection plasma a une porosité de l’ordre de 5 vol% à 15 vol%, qui est moins importante que celle souhaitée : environ 40% vol. L’augmentation de la porosité de l’anode projetée par plasma, peut être réalisée par la réduction de NiO dans le dépôt [77, 92]. L’utilisation de graphite revêtu de Ni au lieu du Ni favorise l’augmentation de la porosité de l’anode.
L’anode avec un changement graduel des compostions et microstructures peut être élaborée par projection plasma en changeant progressivement les débits des poudres pendant la projection. Par le contrôle des compositions et microstructures, cela permet de diminuer la contrainte thermique et d’augmenter les zones de point triple dans le dépôt.
I.3.3.2. Fabrication de la cathode
La projection plasma est un procédé qui permet d’élaborer aussi la cathode [75, 80, 93]. La réaction chimique entre les matériaux de la cathode et de l’électrolyte, peut être évitée grâce à une forte vitesse de refroidissement des particules. Le principal problème lié au procédé est la décomposition du matériau de la cathode, spécialement pour le manganite de lanthane de structure pérovskite. Pour résoudre ce problème, un traitement thermique, doit être réalisé afin de régénérer la structure cristalline de la pérovskite.
La projection plasma sous air, la projection plasma sous faible pression et la projection à la flamme sont principalement utilisées pour réaliser la cathode. Une interface entre la cathode poreuse et l'électrolyte dense devrait être obtenue avec un grand nombre de points de contact pour améliorer les caractéristiques de la pile de type SOFC. Généralement, il est impossible d’injecter des particules trop petites (inférieure à 5 micromètres), par ces procédés. Cela peut être obtenu grâce à la projection de suspensions, dont le principe esr d’injecter des particules de l’ordre du nanomètre ou micromètre [75].
I.3.3.3. Fabrication de l’électrolyte
La projection thermique sous pression atmosphérique (APS) est souvent utilisée pour fabriquer l’électrolyte de la pile de type SOFC. Un traitement thermique ou chimique du dépôt après projection est parfois nécessaire afin de densifier lélectrolyte. Mais dans certains cas, cela n’est pas permis après projection. Un autre moyen pour augmenter la densité de l’électrolyte est alors de projeter des poudres plus fines. La projection de suspension (SPS) devient alors une méthode susceptible de réaliser cet électrolyte dense. Mais il y a beaucoup de paramètres qui influencent la qualité du dépôt.
Après une recherche d’une dizaine d’années, il semble que la projection LPPS soit capable de fabriquer le dépôt dense. En effet, des électrolytes de YSZ denses et minces ont été réalisés avec la torche de F4VB et la buse supersonique par DLR (Allemagne), ou avec la torche O3CP (Sulzer).
Les microstructures de l’électrolyte de YSZ, réalisés par APS, SPS, LPPS ou VLPPS sont montrés en figure I.19.
Figure I.19. Microstructure de l’électrolyte YSZ réalisé par (a) APS [12] (b)SPS [15] (c)VPS [16](d)VLPPS [17].
(a) (b)
(d) (c)
I.4. Objectif de la recherche
Ce chapitre montre que les oxyapatites à base de silicate substitué au site de Si représentent de bonnes potentialités notamment en matière de conductivités électriques pour une application d’électrolyte de pile à combustible de type SOFC à température intermédiaire. En tant que nouveau matériau pour l’électrolyte, il pose la difficulté de la réalisation d’un dépôt par projection thermique qui reste l’une des techniques les moins coûteuses et les plus efficaces d’un point de vue rendement.
L’objectif de cette thèse est d’étudier le processus de synthèse du matériau La10Si5,8Mg0,2O26,8
et de réaliser le dépôt de ce matériau par projection thermique dans le but de l’utiliser comme électrolyte de pile IT-SOFC.
Ce matériau sera initialement synthétisé par frittage en phase solide à haute température et sera projeté ensuite par projection thermique pour deux conditions environnementales sous air et sous faible pression. Une étude du procédé du traitement thermique du dépôt sera menée afin de réaliser sa recristallisation et sa densification. La cinétique de la cristallisation isotherme du dépôt réalisé par projection plasma sous air, sera déterminée par mesure de la conductivité électrique. Finalement, afin de vérifier la faisabilité de la préparation de la pile constituée de l’électrolyte La10Si5,8Mg0,2O26,8, des piles de structure planaire seront élaborées.
I.5. Références bibliographiques
1. Herman, H., Plasma-sprayed Coatings. Scientific American, 1988. 259: p. 112-117. 2. P.D.Lilley, E.E., F,Gross. EUR Report 12249,. 1988. Luxemberg: Office for Official
Public of the European Communities.
3. J.A. Kilner , B.C.H.S., In: O.T. Sorensen. Nonstoichiometric Oxides. in Academic Press. 1981. New York.
4. J.T.Brown, Solid oxide fuel cell technology. IEEE Transactions on Energy Conversion, 1988. 3(2): p. 193-198.
5. Emma Kendrick, M.S.I., Peter R.slater, Developing apatites for solid oxide fuel cells: insight into structrural, transport and doping properties. Jouranl of Materials chemistry, 2007. 17: p. 3104-3111.
6. von Niessen, K., M. Gindrat, and A. Refke, Vapor Phase Deposition Using Plasma Spray-PVD™. Journal of Thermal Spray Technology, 2010. 19(1): p. 502-509.
7. Julian R. Tolchard, M.S.I.a.P.R.S., Defect Chemistry and Oxygen Ion Migration in the Apatite-Type Materials La9.33Si6O26 and La8Sr2Si6O26. Jouranl of Materials chemistry, 2003. 13: p. 1956-1961.
8. Sodeoka, S., M. Suzuki, and K. Ueno, Effects of high-pressure plasma spraying for yttria-stabilized zirconia coating. Journal of Thermal Spray Technology, 1996. 5(3): p. 277-282.
9. Nakayama, S. and M. Sakamoto, Electrical properties of new type high oxide ionic conductor RE10Si6O27 (RE = La, Pr, Nd, Sm, Gd, Dy). Journal of the European
Ceramic Society, 1998. 18(10): p. 1413-1418.
10. Haile, S.M., Fuel cell materials and components. Acta Materialia, 2003. 51(19): p. 5981-6000.
11. Yahiro, H., et al., Electrical properties and microstructure in the system ceria-alkaline earth oxide. Journal of Materials Science, 1988. 23(3): p. 1036-1041.
12. Zhang, C., et al., Study on gas permeation behaviour through atmospheric plasma-sprayed yttria stabilized zirconia coating. Surface and Coatings Technology, 2008. 202(20): p. 5055-5061.
13. S.Kuroda. Properties and caracterization of thermal sprayed coating-A review of recent research progress. in in Thermal spraying: meeting the challenge of the 21 st century. 1998. USA: ASM International.
14. E.Baur, H.Z.P., ed. Z.elektrochem. Vol. 43. 1937. 727.
15. Waldbillig, D. and O. Kesler, The effect of solids and dispersant loadings on the suspension viscosities and deposition rates of suspension plasma sprayed YSZ coatings. Surface and Coatings Technology, 2009. 203(15): p. 2098-2101.
16. M. Lang, A.D., T. Franco, Z. Ilhan, A. Nestle and G. Schiller et al., Electrochemical characterization of vacuum plasma sprayed planar solid oxide fuel cells and short stacks for mobile application. Ceramic Engineering and Science Proceedings, 2005. 26(4): p. 67-74.
17. C. Verdy, C.Z., D. Sokolov; H. Liao, D. Klein, C. Coddet Gas-Tight Coatings Produced by Very Low Pressure Plasma Spraying. in International Thermal Spray Conference & Exposition 2008. 2008: ASM.
![Figure I.3. Schéma de principe de la batterie à empilement bipolaire de plaques [2].](https://thumb-eu.123doks.com/thumbv2/123doknet/14529759.723380/15.892.193.719.886.1114/figure-schéma-principe-batterie-empilement-bipolaire-plaques.webp)


![Tableau I.5. Evolution de la conductivité électrique dans les deux directions, parallèle et perpendiculaire à l’axe c, de monocristaux de structure apatite [63, 64]](https://thumb-eu.123doks.com/thumbv2/123doknet/14529759.723380/29.892.201.692.125.382/evolution-conductivité-électrique-directions-parallèle-perpendiculaire-monocristaux-structure.webp)
![Figure I.17. Evolution du plasma en fonction de la pression dans l’enceinte de projection [8]](https://thumb-eu.123doks.com/thumbv2/123doknet/14529759.723380/36.892.233.670.112.532/figure-evolution-plasma-fonction-pression-l-enceinte-projection.webp)


![Figure II.13. Mécanismes de formation des phases secondaires dans le cas d'un excès local de l'un et l'autre des réactifs [2]](https://thumb-eu.123doks.com/thumbv2/123doknet/14529759.723380/60.892.168.719.119.871/figure-mécanismes-formation-phases-secondaires-excès-local-réactifs.webp)
