UNIVERSITE MOHAMMED V
FACULTE DE MEDECINE ET DE PHARMACIE -RABAT-
ANNEE: 200 THESE N°: 120
U
U
n
n
n
n
o
o
u
u
v
v
e
e
a
a
u
u
c
c
o
o
n
n
c
c
e
e
p
p
t
t
d
d
e
e
p
p
r
r
i
i
s
s
e
e
e
e
n
n
c
c
h
h
a
a
r
r
g
g
e
e
d
d
u
u
c
c
a
a
n
n
c
c
e
e
r
r
d
d
e
e
L
L
’
’
E
E
n
n
f
f
a
a
n
n
t
t
d
d
a
a
n
n
s
s
l
l
e
e
s
s
p
p
a
a
y
y
s
s
a
a
r
r
e
e
s
s
s
s
o
o
u
u
r
r
c
c
e
e
s
s
l
l
i
i
m
m
i
i
t
t
e
e
e
e
s
s
« « EExxeemmppllee ddee llaa mmaallaaddiiee ddee hhooddggkkiinn aauu MMaarroocc »»THESE
Présentée et soutenue publiquement le :………..
PAR
Mme. Ikram BOUBESS
Née le 15 Février 1983 à Martil
Pour l'Obtention du Doctorat en
Médecine
MOTS CLES Cancer – Enfant – Maladie de hodgkin – Abondon de traitement Pays en voie de développement – Prise en charge globale –.
-
JURY
Mr. B. EL GUEDDARI PRESIDENT
Professeur de Radiothérapie
Mme. L. HESSISSEN RAPPORTEUR
Professeur Agrégé de Pédiatrie
Mr. M. KHATTAB
INTRODUCTION... 1
PATIENTS ET METHODES ...
I- Description du projet MDH-MA04 ...
A-Inclusion des patients...
1-critères d’inclusions ...
2- critères d’exclusion ...
B- Protocole thérapeutique ...
1-bilan initial et d’extension ...
a-bilan clinique ...
b-bilan biologique...
c-bilan radiologique ...
d-histopathologie ...
e-bilan pré-thérapeutique ...
2-Définition des groupes pronostic ...
3- Le traitement ...
a- La chimiothérapie ...
-Chimiothérapie du groupe favorable ...
-Chimiothérapie du groupe défavorable ...
b-La radiothérapie ...
4- Evaluation de la réponse au traitement ...
a-Définitions ...
b- Evaluation au cours et à la fin de traitement ...
c- Evaluation a la fin de traitement ...
C- Les mesures complémentaires ...
1- Formation d’un groupe d’étude de la maladie de Hodgkin ...
4- Discussion des cas et évaluation du projet ...
5- Aide au patient ...
II-Description de la série MDH 1995 à 2000 ...
III-Paramètres d’analyses et méthodes statistiques ...
RESULTATS ...
...
I - Résultats MDH MA 04 ...
A- Données générales ...
B- Les antécédents ...
C- Sur le plan clinique ...
D- Confirmation du diagnostic ...
1-Siège de la biopsie ...
2-Le type histologique ...
3-Immunohistochimie ...
E-Stadification ...
1. Le bilan d’extension et bilan pré-thérapeutique ...
2. Stadification Ann Arbor ...
3. Groupe pronostic MDH-Ma 04 ...
F-Traitement ...
1-La chimiothérapie ...
2-La radiothérapie ...
G -Evaluation de la réponse au traitement ...
1-Réponse après 2 cures de la chimiothérapie ...
DISCUSSION ...
I- Résultats thérapeutiques dans la maladie d’hodgkin ...
II- La problématique de l’oncologie pédiatrique dans les pays en voie de développement ...
III- Stratégies d’amélioration de l’oncologie pédiatrique dans les pays en voie de développement ...
CONCLUSION ...
RESUMES ...
REFERENCES ...
HER : Hôpital d’enfant de Rabat
SJCR : St Jude Children’s research Hospital
GFAOP : Groupe Franco-Africain d’Oncologie Pédiatrique SHOP : service d’hémato-oncologie pédiatrique
MDH : maladie de hodgkin
LH : lymphome hodgkinien
SSR : Survie Sans Récidive
OMS : organisation mondiale de la sante
SSE : survie sans événement
SG : survie globale
RTH : radiothérapie
DDN : date des dernières nouvelles VS : vitesse de sédimentation
LDH : lactate déshydrogénase
EPP : électrophorèse des protéines
HVB : hépatite virale B
HVC : hépatite virale C
HIV : virus d’immunodéficience humaine
TDM : tomodensitométrie
FEV : fraction d’éjection ventriculaire IMT : indice médiastino-thoracique ASAT : Aspartate Amino–transférase
NFS : Numération formule sanguine BOM : Biopsie osteom dullaire
PBF : Ponction biopsie de foie
ADP : Adénopathie
RC : Rémission complète
SN : Scl ro-nodulaire
CM : Cellularit mixte
Liste des tableaux
Tableau I : Le protocole VAMP ... 11
Tableau II : Le protocole OPPA ... 11
Tableau III : Le protocole COPP. ... 12
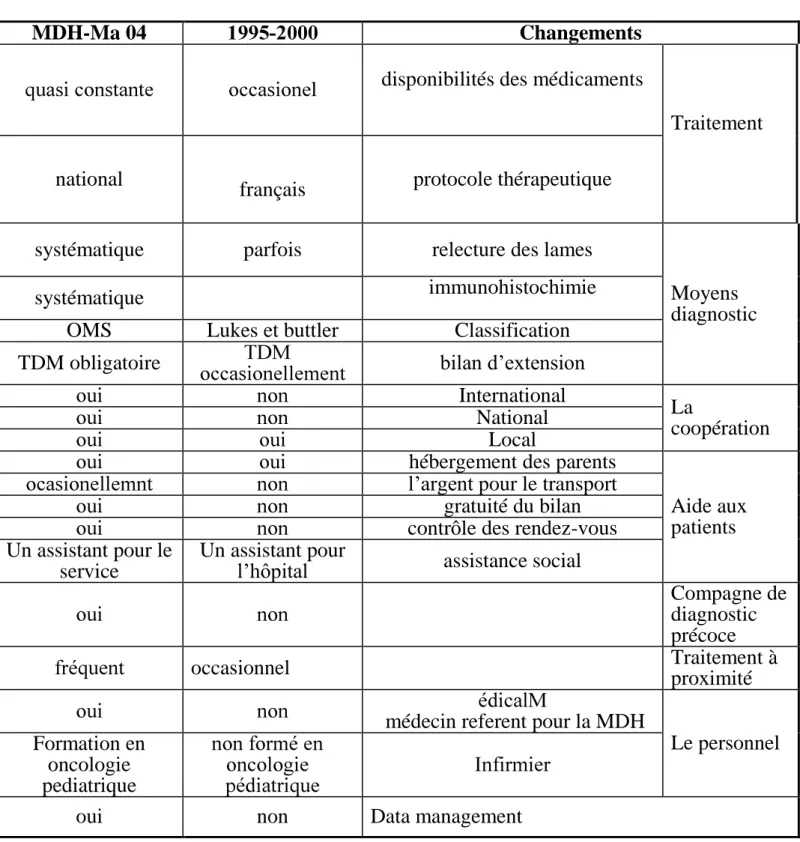
Tableau IV : Les principales différences de prise en charge entre la serie1995-2000 et la série de MDH-Ma 04 ... 18
Tableau V : La répartition géographique des patients ... 23
Tableau VI : Les lésions mise en évidence au terme de ce bilan d’extension ... 30
Tableau VII : Les examens complémentaires disponibles et leurs résultats ... 31
Tableau VIII : La fréquence des stades des malades selon la classification d’Ann Arbor ... 32
Tableau IX : Nombre des patients qui ont reçus des cures non protocolaires ... 34
Tableau X : Type de toxicité et nombre des cas correspondants ... 36
Tableau XI : Type de toxicité et son grade selon OMS ... 37
Tableau XII : Les caractéristiques des patients qui ont abandonné le traitement ... 43
Tableau XIII : Caractéristiques des patients qui ont rechuté au cours de l’étude ... 44
Tableau n° XIV : Caractéristiques des patients qui sont décédés au cours de l’étude ... 45
Tableau n°XV : Etats des patients à la date des dernières nouvelles ... 48
Tableau n°XVI : Comparaison des caractéristiques générales des patients des deux séries ... 49
Tableau n°XVII : comparaison de l’évolution des patients des deux séries ... 50
Liste des figures
Figure 1 : La répartition des patients inclus selon les années d’admission ... 21
Figure2 : La répartition des patients selon les tranches d’âges ... 22
Figure 3 : La répartition géographique des patients ... 23
Figure 4 : Le niveau socio-économique des patients ... 24
Figure 5 : La fréquence des symptômes B ... 27
Figure 6 : Evaluation des malades après administration de 4 cures de chimiothérapie ... 39
Figure 7 : Evaluation des malades après fin de traitement ... 41
Figure 8 : La SSE à 50 mois de recul des 94 patients traités par le protocole MDH –Ma04 en considérant l’abandon comme événement ... .46
Figure 9 : La SSE à 50 mois de recul des 94 patients traités par le protocole MDH –Ma04 en censurant les abandons comme événement... 47
Figure 10 : Les SSE des patients des séries 1 et 2 en censurant les abandons de traitement à la DDN ... 51
Figure11 : Les SSE des patients des séries 1 et 2 en considérant les abandons de traitement comme événement ... 52
Le cancer de l’enfant de moins de 15 ans constitue 1% de tous les cancers. Sur le plan mondial, le nombre annuel de nouveau cas avoisine les 200000 [ ]. Quand ils sont pris en charge correctement, au moins 70% des cancers de l’enfant peuvent être guéris [2] mais malheureusement seuls les 20% de la population pédiatrique mondiale vivant dans les pays développés peuvent bénéficier d’une prise en charge adéquate. Le pourcentage d’enfants atteints de cancer et vivant actuellement dans des pays en voie de développement dépassera bientôt les 90% [3]. Tous ces enfants n’auront pas accès au « state of the art » des traitements et la survie ne dépassera pas les 20%.
Les raisons de cette grande inégalité sont multifactorielles et essentiellement dues au fait que le cancer n’est pas une priorité par rapport aux autres problèmes de santé publique auxquels font face ces pays, au retard diagnostic, aux problèmes nutritionnels, au coût du traitement, à la non disponibilité des drogues, à un manque de soins de support et aux abandons de traitement. Un rapport publié en 2002 par la Société Internationale d’Oncologie Pédiatrique (SIOP) montre que le refus de traitement, la non compliance et les abandons de traitement restent un problème majeur [4].
Il a été démontré que pour améliorer le pronostic du cancer de l’enfant dans les pays en voie de développement il faut suivre une stratégie de prise en charge globale qui inclue la mise en place des structures centralisées d’oncologie pédiatrique, l’élaboration et l’utilisation des protocoles locaux de traitement, la mise en place d’équipes multidisciplinaires dédiés à l’oncologie pédiatrique,
La mise en place des partenariats nord-sud entre des hôpitaux publics dans les pays en voie de développement et des centres de recherche dans les pays développés fait également partie des initiatives qui ont permis d’améliorer la prise en charge du cancer chez l’enfant. Les plus importants de ces partenariats ayant prouvé leur efficacité sont ceux de l’hôpital St Jude Children’s Research Hospital (SJCRH) qui a développé des programmes de coopération avec des pays de centre et sud Amérique [5], et celle des Groupe Franco-africain d’Oncologie Pédiatrique (GFAOP) en coopération avec le nord et l’ouest de l’Afrique [6]. Il existe aussi des partenariats sud sud entre les pays en voie développement comme celle élaboré entre Hong-Kong et la chine [7].
Au Maroc, où on estime à 1000 le nombre des nouveaux cas de cancer de l’enfant par an [8], la prise en change de ces enfants pose les mêmes problèmes que ceux rencontrés au niveau de tous les pays en voie de développement avec surtout des abandons du traitement qui restent un défi à l’oncologie nationale. Pour faire face à ces problèmes, le Maroc a développé des partenariats avec de nombreux centres et groupes d’oncologie pédiatrique en particulier avec le SJCRH et le GFAOP et a aussi élaboré des programmes de prise en charge de certains cancers comme première étape avant de généraliser à tous les types de cancer.
La maladie d’hodgkin qui constitue 9% des cas des cancers suivis au Service d’Hémato-Oncologie Pédiatrique (SHOP) de l’Hôpital d’enfant de Rabat (HER)
[9],est un des cancers qui ont été concerné par l’un des ces programmes lancés à
l’échelle nationale. Il s’agit du projet MDH-Ma 04 qui a démarré à partir de février 2004 et dont le but est d’améliorer la prise en charge de la MDH de
Rabat entre 1995 et 2000 ayant montré que les principaux problèmes étaient l’évaluation initiale incomplète avec un risque de stadification, l’utilisation de protocoles thérapeutiques inadaptés et un nombre très élevé d’abandon de traitement [9].
Les objectifs de ce travail sont :
1. D’analyser les résultats du projet MDH-Ma 04 chez les patients suivis au SHOP en ce qui concerne :
Les données épidémiologiques La présentation clinique
Le respect du protocole thérapeutique Le taux d’abandon de traitement Le taux de survie sans événement
2. De comparer les résultats du projet MDH-Ma 04 en terme d’abandon de traitement et de survie sans événement à celles de la première série de 118 cas de MDH suivis de 1995 à 2000 et dont les données ont été mises à jour en janvier 2009.
I. DESCRIPTION DU PROJET MDH 04
Le projet MDH-Ma 04 qui vise à homogénéiser et à améliorer la prise en charge de la MDH au Maroc, est un projet national qui comporte deux volets essentiels :
1- Un protocole thérapeutique national adapté à notre contexte
2- Des mesures complémentaires permettant de veiller à la bonne application du protocole thérapeutique et d’encourager le patient à adhérer au projet.
Les buts du projet étant :
De rendre homogène sur le plan national la prise en charge de la MDH de l’enfant
De diminuer le taux des abandons de traitement
D’améliorer le taux de Rémission complète et le taux de survie sans évènements passant à 60 à 80% de SSR à 5 ans
D’établir une base de données du lymphome Hodgkinien (LH) de l’enfant au Maroc.
A- Inclusion des patients
1- Critères d’inclusion
Sont éligibles pour ce projet tous les patients présentant les critères suivants : Patients âgés de 20 ans et moins
Non antérieurement traités en dehors de l’administration de corticoïdes ou une irradiation réalisées dans le cadre de l’urgence (compression médiastinale ou de la moelle épinière)
Stade I à IV de Ann Arbor (Annexe n°2)
2- Critères d’exclusion
Sont exclus du projet les cas suivants : LH initialement traité
LH secondaire
Antécédents de déficit immunitaire primitif Les patients HIV positif
Les patients atteints d’une hépatite virale B ou C.
Les cas d’insuffisance cardiaque contre-indiquant les anthracyclines Toute tare viscérale contre-indiquant la chimiothérapie
Infection bactérienne sévère Malnutrition sévère
Femme enceinte ou allaitante. Refus d’adhérer au projet
B- Le protocole thérapeutique
1- Bilan initial et d’extension a- Bilan clinique
Interrogatoire à la recherche des antécédents pathologiques et des signes d’évolutivité clinique
Un examen clinique complet avec précision des aires ganglionnaires atteintes précision du nombre d’adénopathies par aire et mensurations des adénopathies.
Cet examen clinique initial est à réaliser par le radiothérapeute et l’oncologue pédiatre.
b- Bilan biologique
Le bilan biologique initial comprend : Hémogramme
Vitesse de sédimentation à la 1° heure, LDH, Fibrinémie
Créatinémie, Transaminases, Phosphatases alcalines, Bilirubine Sérologies : HVB, HVC, HIV
EPP, CRP
c- Bilan radiologique
Echographie abdominale
En optionnel : Scintigraphie osseuse, TDM cervicale ou échographie cervicale
d- Bilan histopathologique
La relecture des lames par les anatomo-pathologistes de l’HER est systématique si la première lecture de la pièce ayant permis de poser le diagnostique a été faite en dehors du laboratoire de l’HER. La biopsie ostéo-médullaire est indiquée cas de stade III et IV et/ou B.
e- Bilan pré-thérapeutique
Echocardiographie avec mesure de la fraction d’éjection ventriculaire FEV et du taux de raccourcissement
2- Définition des groupes pronostic
Les patients seront stratifiés selon 2 groupes pronostiques
Groupes favorables qui incluent tous les patients répondant aux critères suivants:
- Stades I et IIA et - IMT < 0.33 et
- Volume tumoral ganglionnaire < 6 cm et - Pas d’atteinte contiguë
Groupe défavorable qui comprend tous les patients non inclus dans le groupe favorable :
- Stades IIB, III, IV ou
- Bulky mediastinal avec IMT 0.33 ou - Adénopathies 6 cm ou
- Atteinte viscérale contiguë quelque soit le stade
3- Le traitement
Le traitement comprend une chimiothérapie initiale suivie de la radiothérapie. Le choix du protocole thérapeutique a été fait selon plusieurs critères :
Un protocole dont les résultats thérapeutiques ont été déjà publiés Un coût modéré (annexe n°3)
Des drogues disponibles Peu toxique
Administrable essentiellement en hospitalisation de jour avec possibilité de recevoir des cures à proximité
a- Chimiothérapie
Chimiothérapie du groupe favorable
Les patients du groupe favorables seront traités par une chimiothérapie comportant 4 cures VAMP administrés tous les 28 jours [10].
Tableau I : Protocole VAMP
Drogues Dose Administration Jours
Vinblastine 6 mg/m² IV J1 et J15
Doxorubicine 25 mg/m² IV J1 et J15
Methotrexate 20 mg/m² IV J1 et J15
Prédnisone 40 mg/m² Per os J1 à J15
Chimiothérapie du groupe défavorable
Les patients du groupe défavorable seront traités par une chimiothérapie comportant 2 cures OPPA suivies de 4 cures COPP administrées tous les 28 jours [11].
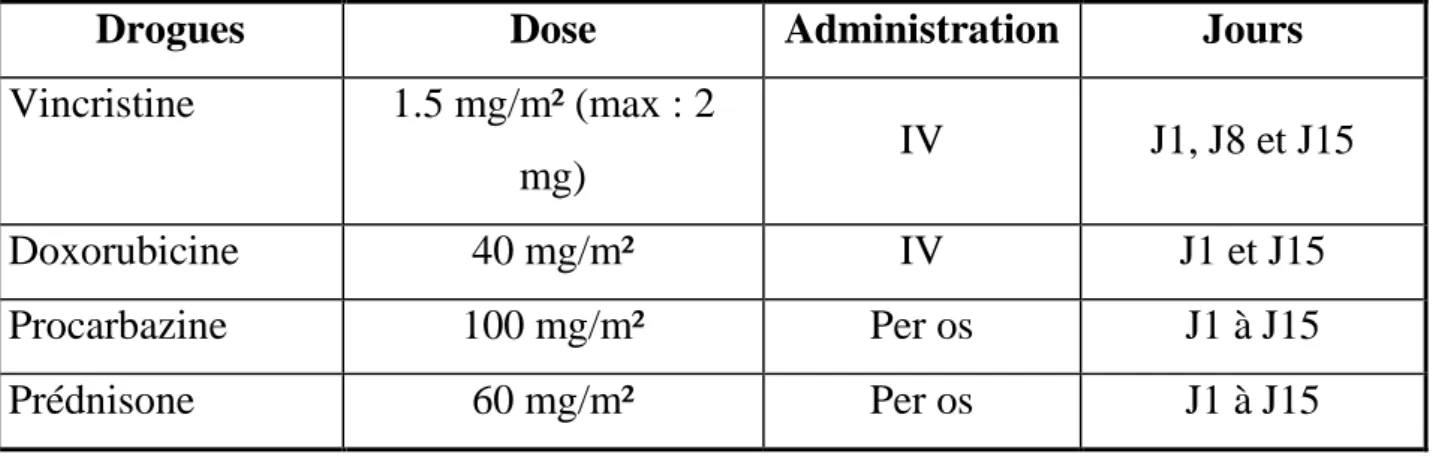
Tableau II: Le protocole OPPA
Drogues Dose Administration Jours
Vincristine 1.5 mg/m² (max : 2
mg) IV J1, J8 et J15
Doxorubicine 40 mg/m² IV J1 et J15
Procarbazine 100 mg/m² Per os J1 à J15
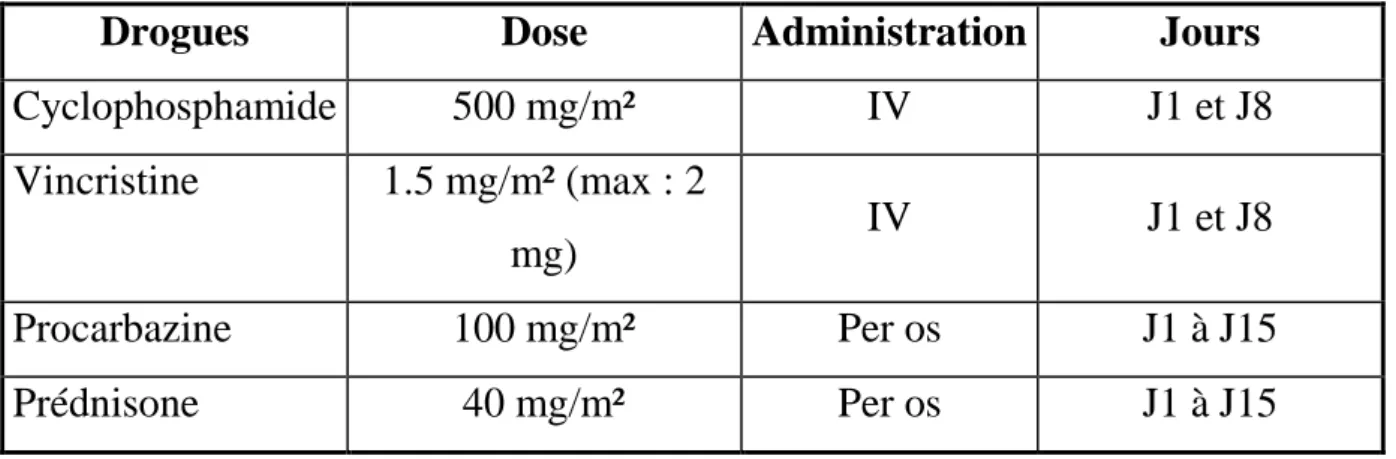
Tableau III: Le protocole COPP
Drogues Dose Administration Jours
Cyclophosphamide 500 mg/m² IV J1 et J8 Vincristine 1.5 mg/m² (max : 2 mg) IV J1 et J8 Procarbazine 100 mg/m² Per os J1 à J15 Prédnisone 40 mg/m² Per os J1 à J15 b- Radiothérapie
La radiothérapie sera administrée à la dose de 25 Gy sur les champs initialement envahis chez les patients dont la réponse à la chimiothérapie a été estimée supérieure à 70%.
La radiothérapie débutera approximativement 2 semaines après la dernière cure de chimiothérapie et après obtention d’un hémogramme normal.
Une transposition des ovaires sera proposée en cas où elles seraient incluses dans le champ d’irradiation. Elle doit être réalisée en fin de chimiothérapie le plus tôt possible afin de ne pas retarder l’irradiation.
4- Evaluation de la réponse au traitement a- Définitions
La rémission complète est définie comme la régression totale de tous les symptômes cliniques, des anomalies biologiques en rapport avec la maladie et la disparition de toute masse tumorale mesurable. La rémission complète est dite « non confirmée » s’il persiste des lésions avec une réduction 70% du volume tumoral initial et régression des signes cliniques initiaux. L’echec du traitement : c’est une réduction < 50% du volume tumoral initial
Evolutivité : Augmentation du volume tumoral initial ou l’apparition de lésions qui n’existaient pas initialement.
b- Evaluation au cours et à la fin de la chimiothérapie
Une évaluation clinique est réalisée après chaque cure afin d’éliminer une éventuelle évolutivité tumorale.
Une évaluation biologique est réalisée avant chaque cure à la recherche d’effets secondaires de la chimiothérapie (Hémogramme, créatinémie, ASAT, ALAT, bilirubine)
Une évaluation radiographique simple (Radiographie du thorax, Echographie abdomino-pelvienne) est réalisée après chaque 2 cures de chimiothérapie
Une évaluation précise radiographique (TDM) et éventuellement histopathologique (BOM) est réalisée à la fin de la chimiothérapie pour décision de la suite du traitement.
Les patients dont la réponse est 70% à la fin de la chimiothérapie sortiront du protocole et seront traités à la convenance de chaque équipe.
c- Evaluation à la fin du traitement
Une évaluation sera réalisée 4 à 8 semaines après la fin du traitement. Elle permet de confirmer la rémission complète. Elle comportera :
Examen clinique
Bilan biologique : VS, LDH
Examens radiologiques initialement pathologiques.
Des évaluations régulières seront réalisées tous les 3 mois pendant la 1° année puis tous les 4 mois durant les 2° et 3° années puis tous les 6 mois pour la 4° année puis de façon annuelle.
La rechute doit être prouvée histologiquement.
C- Les mesures complémentaires
Plusieurs mesures d’accompagnement complètent le protocole thérapeutique et permettent de s’assurer de l’adhésion du patient au projet, la bonne application du protocole thérapeutique, le suivi du patient et le recueil des données. Ces mesures comprennent :
1- Formation d’un groupe d’étude de la maladie de Hodgkin
Organisation d’équipes multidisciplinaires comprenant des oncologues pédiatres, des radiothérapeutes, des radiologues et des anatomo-pathologistes, au niveau de chaque centre .
Désignation d’un médecin référent ou médecin coordinateur pour la MDH au niveau de chaque unité d’oncologie.
2- Le Data management
Un Data manager est en charge de :
Recueil et mise à jour des données à partir des dossiers des patients et enregistrement sur un fichier Excel.
Vérification des informations contenues dans les dossiers et contact permanant avec les médecins de l’unité pour compléter d’éventuelles données manquantes
Vérification des rendez-vous des patients et convocation téléphonique ou par voie postale des patients absents au rendez-vous
3- Collaboration nationale et internationale
Essentiellement entre les services d’oncologie pédiatrique et le St Jude Children Hospital qui a contribué à l’élaboration du protocole thérapeutique et également à développer la télémédecine. Des réunions mensuelles « Horizon Live meeting » avaient lieu pour discuter des cas de MDH avec des évaluations trimestrielles du projet. Des mails circulaient régulièrement entre les membres du groupe chaque fois qu’un avis à propos d’un cas particulier était nécessaire.
4- Elaboration d’une brochure « aide mémoire »
Dans le cadre du projet une brochure aide mémoire a été élaborée à l’attention des médecins ayant en charge les patients atteints de la MDH. Cette brochure est représentée en annexe n°4.
5- Aide au patient
D’autres mesures ont visé directement le patient et sa famille pour assurer une meilleure adhésion au projet et encourager le patient à compléter son traitement :
Accueil et orientation
Recueil des coordonnées des familles (numéro de téléphone, adresse.)
Information concernant la MDH, son traitement, son bon pronostic et des risques liés à la non compliance au traitement.
Gratuité du bilan
II.DESCRIPTION DE LA SERIE MDH 1995 à 2000
La série de MDH 1995 et 2000 est une étude rétrospective de 118 cas d’enfants atteints de maladie d’hodgkin histologiquement prouvée admis à l’unité onco-hematologie de l’hôpital d’enfants de rabat. L’âge médian des patients était de 8 ans avec des extrêmes allant de 2 à 15 ans et un ratio M/F de 4 (94 masculins et 24 féminins). Le délai médian de diagnostic était de 6 mois avec des extrêmes allant de 1 à 72 mois. Selon la classification de Lukes et Buttler, 45% avaient une forme scléro-nodulaire et 41% une forme à cellularité mixte. Les caractéristiques de cette série sont représentées dans le tableau IV.
Ce groupe de malades a été traité selon le protocole de la Société Française d’Oncologie Pédiatrique SFOP: le protocole MDH 90. Les principales différences dans la prise en charge de la maladie de Hodgkin entre la période 1995- 2000 et celle de 2004 - 2007 sont représentées dans le tableau IV.
Les patients de la première série ont été reclassés en deux groupes « favorable » et « défavorable » selon les critères pronostiques du protocole MDH-Ma 04.
Tableau IV : Principales différences de prise en charge entre les deux séries
MDH-Ma 04 - Changements
l disponibilités des médicaments
Traitement
national français protocole thérapeutique
systématique parfois relecture des lames
Moyens diagnostic
systématique immunohistochimie
OMS Lukes et buttler Classification
TDM obligatoire bilan d’extension
International
La
coopération National
Local
hébergement des parents
Aide aux patients l’argent pour le transport
gratuité du bilan contrôle des rendez-vous Un assistant pour le
service
Un assistant pour
l’hôpital assistance social
Compagne de diagnostic précoce
occasionnel Traitement à
proximité médecin referent pour la MDH
Le personnel Formation en
III. PARAMETRES ANALYSES ET METHODES STATISTIQUES
Les variables quantitatives ont été analysées en s’aidant des médianes et des extrêmes. Les variables qualitatives ont été exprimées en effectifs et en pourcentages.
L’évaluation des patients s’est basée sur l’étude de la survie sans évènement (SSE) selon la méthode de Kaplan-Meier. La SSE a été calculée à partir du délai entre le diagnostic et la survenue d’un évènement ou du délai entre le diagnostic et la date des dernières nouvelles si aucun évènement n’a été enregistré. On a considéré comme évènements la survenue d’une rechute, quel que soit son siège et le décès. Deux SSE ont été calculées, une en considérant les abandons comme événement et une autre avec les abandons censurés à la date des dernières nouvelles. On parle d’abandon de traitement si le traitement a été démarré mais non complété [12].
La date fixée pour l’analyse des données a été le 30 mars 2009. Les paramètres comparés ont été
L’âge médian.
Le pourcentage de patients de sexe masculin. Le type histologique.
Le stade de la maladie. Le groupe pronostic le délai diagnostic.
Le taux de survie sans événement.
Le pourcentage d’abandon de traitement
Les variables qualitatives ont été comparées par le test 2 et les survies ont été comparées en utilisant le test du Logrank.
I. RESULTATS MDH MA 04 A. Données générales
Sur la période qui s’est étalée de février 2004 à décembre 2007, 101 cas de MDH ont été admis au service d’Hémato-Oncologie Pédiatrique de l’Hôpital d’Enfant de Rabat soit 8 % des admissions. Quatre vingt quatorze patients ont été inclus dans cette étude et ont été exclus sept patients pour les raisons suivantes :
Suivis dans une autre structure 4 cas
Préalablement traités 2 cas
Refus de traitement 1 cas
En moyenne, 23 nouveaux cas ont été inclus chaque année. L’histogramme de la figure 1 montre le nombre de cas inclus chaque année. Ce nombre a augmenté progressivement jusqu'à se stabiliser autour de 26-27 cas en 2006 et 2007.
La répartition en année 19 22 27 26 0 5 10 15 20 25 30 2004 2005 2006 2007 année
L’âge médian à l’admission des patients inclus était de 9 ans avec des extrêmes
allant de 3 ans à 15 ans. La figure n°2 de la répartition par tranche d’âge des malades montre un pic entre 6 et 10 ans. Quinze patients soit 16% avaient un âge inférieur ou égal à cinq ans.
0 10 20 30 40 50 ]0; 5] ]5; 10] ]10; 15] l'âge
Répartition des patients selon l'âge
Figure 2 : La répartition des patients selon les tranches d’âges
Soixante quatorze patients étaient de sexe masculin et 20 de sexe féminin donnant un ratio M/F de 3.7.
L’origine géographique des patients est représentée dans le tableau I et la
figure 3 qui montrent que 39 patients étaient originaires des régions nord-ouest, 24 du nord-est, 25 des régions du centre et 5 du sud-ouest. Un patient était
Tableau V et figure 3 : Carte du Maroc avec les 16 régions administratives et la répartition
géographique des patients selon la région d’origine.
Régions Administratives Nombre
1 Oued Eddahab-Lagouira 0 2 Laâyoune-Boujdour-Sakia El Hamra 0 3 Guelmim-Es Smara 2 4 Souss-Massa-Draâ 3 5 Gharb-Chrarda-Beni Hssen 10 6 Chaouia-Ourdigha 3 7 Marrakech Tensift El Haouz 3 8 Oriental 11 9 Casablanca 0 10 Rabat-Salé-Zemmour-Zaër 7 11 Doukkala-Abda 0 12 Tadla-Azilal 0 13 Meknès-Tafilalt 6 14 Fès-Boulmane 16 15 Taza-Al Hoceima-Taounate 13 16 Tanger-Tétouan 19 Etranger 1
Concernant les conditions socio-économiques des patients, nous disposons des informations sur la scolarité de 75 patients dont 15 étaient nos scolarisés parmi lesquelles six patients étaient âgés de plus de six ans. Parmi les 60 patients scolarisés, 44 avaient un niveau primaire et 16 secondaires.
Sur le plan couverture médicale, Quatorze pour cent des patients avaient une assurance maladie. Quatre vingt et un patients ne disposaient pas d’une couverture médicale avec 77 cas d’indigents.
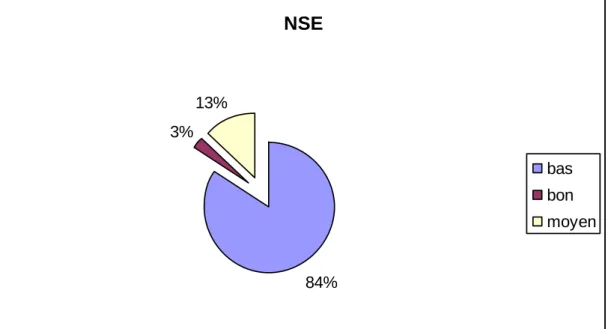
Le niveau socio-économique des patients était bas dans 84% des cas. Douze patients étaient d’un NSE moyen et trois d’un bon NSE.
Figure 4 : Le niveau socio-économique des patients
NSE 84% 3% 13% bas bon moyen
B - Les antécédents
Essentiellement, deux informations ont été recherchées dans les antécédents : la consanguinité des parents et la notion de cancer familial. Le taux de consanguinité parmi nos patients était de 29%.
Concernant les antécédents de cancer dans la famille, l’information était disponible pour 93 patients dont quatre soit 4.3% avaient au moins un parent suivi pour un cancer. Le type de cancer a été précisé dans deux cas : un patient avait un oncle décédé d’un cancer de type non déterminé et une cousine décédée d’un néo du sein et un deuxième patient avait une grand-mère suivie pour un cancer de la lèvre.
C- Sur le plan clinique
La durée d’évolution médiane entre l’apparition des premiers symptômes et la première consultation était de 8 mois avec extrême allant 15 jours à 5 ans. Le motif de consultation était les adénopathies périphériques dans 84 cas soit 89% des cas. Les adénopathies étaient :
Cervicales 77 cas
Inguinales 2 cas
Axillaires 4 cas
Dix patients ont consulté pour d’autres motifs :
Altération de l’état général 2 cas
Syndrome cave supérieur poly arthralgie,
syndrome anémique fièvre au long cours. Dyspnée
Douleur thoracique Ictère
Douleurs abdominales
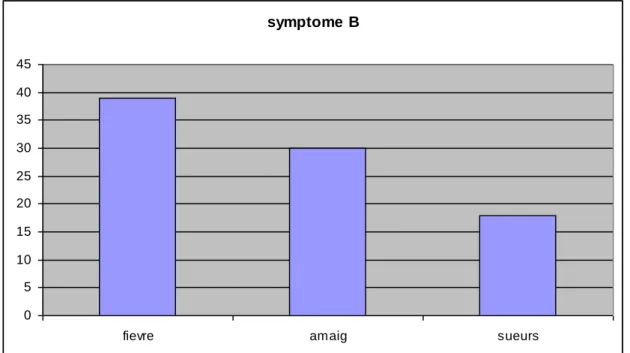
A l’admission, sur les 84 patients qui ont consulté pour des adénopathies, nous disposons des informations sur la taille pour 80 patients dont 39 soit 49% étaient des bulky avec une taille médiane de 8 cm et des extrêmes allant de 6 à 22 cm. Les signes d’évolutivité clinique « symptômes B » étaient présents chez 49 cas soit 52% des cas. Le type exact de symptômes B était précisé dans 48 cas. La fièvre était le signe B le plus fréquent (81%) et était associée le plus souvent à un amaigrissement (61%) :
Fièvre 39 cas (81%)
- Avec amaigrissement 24 cas (61%)
- Avec sueurs 7 cas
Les signes d’évolutivité clinique étaient presque constamment non chiffrés. symptome B 0 5 10 15 20 25 30 35 40 45
fievre amaig sueurs
Figure 5 : Fréquence des symptômes B D. Confirmation du diagnostic
1-Siège de biopsie
Nous disposons d’informations concernant le siège de la biopsie ayant permis de confirmer le diagnostic pour 86 patients. La biopsie était faite au niveau :
Ganglion périphérique 81 cas
Ganglion profond 5 cas
- Médiastinal sous thoracoscopie
2-Type histologique
Le type histologique a été précisé dans 88 cas. Selon la classification OMS et les critères d’inclusion, les 88 patients avaient une MDH classique :
de type scléro-nodulaire dans 63 cas soit 72% à cellularité mixte dans 25 cas.
Aucun cas de MDH à prédominance lymphocytaire ou à déplétion lymphocytaire n’a été décrit dans notre série.
3-Immunohistochimie
Les informations concernant l’immunohistochimie ont été disponibles pour 89 patients et a été réalisée chez 44 d’entre eux soit environ 50% des cas.
Les marqueurs utilisés étaient le CD15, CD20, CD3, CD30, EMA, LMP1 et EBV. Les informations concernant les marqueurs positifs ont été disponibles pour 25 patients : CD15 et CD 30 14 cas CD 15 positif 4 cas - CD15 seul 2 cas - CD15 et CD20 et LMP 1 cas - CD15 et EBV 1 cas CD 30 positif 6 cas - CD30 seul 5 cas - CD30 et CD20 1 cas
E. Stadification
1- Le bilan d’extension et bilan pré-thérapeutique
En plus d’un examen clinique initial, le bilan d’extension a comporté une évaluation le plus souvent biologique, radiologique et échographique. Certains patients ont eu en plus un bilan histo-cytologie et/ou radio isotopique.
Dans le cadre du projet MDH-Ma 04 et pour permettre une bonne stadification de tous les patients un bilan minimal a été obligatoire pour tous les malades. Ce bilan a été gratuit et pris en charge par l’administration de l’HER pour tous les patients indigents : Radiographie pulmonaire Echographie abdominale TDM thoraco-abdomino-pelvienne NFS VS
Fonction rénale et hépatique
La BOM a été, selon le protocole, indiquée dans tous les stades avancés et/ou en présence de signes B. Ainsi elle a été indiquée chez 62 patients et a été réalisée dans 49 cas soit 79% des cas. Elle a montré :
L’absence d’envahissement dans 37 cas avec 36 BOM normales et un cas de dysmyelopoeise
Non contributive dans 6 cas
Pour certains patients d’autres bilans d’extension ont été nécessaires :
La PBF a été réalisée dans deux cas et était normale dans un cas et a montré une hépatite granulomatose dans le deuxième cas.
La scintigraphie indiquée dans le protocole en cas de signes d’appels osseux a été réalisée dans deux cas où elle a montré une hyperfixation. Ponction pleurale dans un cas et n’a pas montré de cellules tumorales.
Tableau n°VI : Le récapitulatif des lésions mises en évidence après un bilan
d’extension
Nombre de patients Description
ADP périphériques
84 39 bulky Taille médiane : cm Médiastin
46 15 Bulky
Nodules pulmonaires 3
Pleurésie
3
1cas cytologie négative 1 cas douteux
1 cas stade IV pleural
ADP latero-trachéale 1 Rate 53 -38 nodulaire -15 SMG homogène Foie 40 -3nodulaire considérés stade IV -37 homogène (2 PBF normales) ADP abdominales 40
Le bilan biologique a comporté :
Une numération formule sanguine Une vitesse de sédimentation Les transaminases
Le fibrinogène La CRP
Les LDH Le TCD
Tableau n° VII: Les examens complémentaires disponibles et leurs résultats
Nombres des patients Résultat
VS 90 32 élevé (>de 70mm) Transaminases 71 - 64 normales -7 élevé CRP 35 30 élevé (>de 10mg/l) Fibrinogène 31 24 élevé (>4g/l) TCD 3 Un cas positif
2 –Stadification Ann Arbor
Selon la classification de Ann Arbor, le stade le plus fréquent était le stade II et 55% avait un stade avancé III-IV
Tableau n° VIII: La fréquence des stades des malades selon la classification
d’Ann Arbor A B TOTAL I 3( 6% ) 0 3(3%) II 28(64% ) 11( 22% ) 39( 42% ) III 11( 25% ) 27(56% ) 38 (41% ) IV 2( 5% ) 11( 22% ) 13( 14% ) Total 44 49 94
3-Groupe pronostic MDH-Ma 04
Parmi les 94 patients de notre série, 89% ont été inclus dans le groupe défavorable :
Stade avancé III/IV 51 cas
Stade IA bulky 1 cas
Stade II
Dix patients étaient inclus dans le groupe favorable :
Stade II A 8 cas
Stade IA 2 cas
F. Traitement
Le traitement s’est basé sur une polychimiothérapie suivie par une radiothérapie des sites initialement atteints.
1-La chimiothérapie
Le délai médian entre l’admission au service et le début de chimiothérapie était de 14 jours avec des extrêmes allant de moins de 24 heures à 56 jours
Tous les patients de notre série ont reçu de la chimiothérapie parmi les quels, 89 patients ont reçu toutes les cures et cinq ont eu une chimiothérapie incomplète (4 abandon et 1 décès)
Le type de cures reçus est représenté dans le tableau IX qui montre que 79 des 89 patients qui ont fini leur chimiothérapie, ont reçu les cures programmés :
2OPPA puis 4 COPP 70 cas
4 VAMP 9 cas
Tableau n°IX: Nombres des patients qui ont reçus des cures non protocolaires
Type de cures Nombres des
patients Commentaires
2 OPPA+4 COPP 70 Selon le schéma programmé
4 VAMP 9 Selon le schéma programmé
4 OPPA+4 COPP
4
2 OPPA supplémentaires car non irradié (3 cas) ou délai d’irradiation prolongé (1cas)
OPPA+4VAMP
1 Initialement défavorable puis
restadifié 2OPPA +5COPP
1 Une cure COPP supplémentaire en
attendant la radiothérapie 4VAMP+2OPPA
1 Adjonction 2 OPPA pour mauvaise
réponse à 4VAMP 3 OPPA+4 COPP
1 Une cure OPPA supplémentaire en
attendant la radiothérapie
VAMP +6 COPP 1 Erreur de stadification initiale
2OPPA +3COPP +ICE
1 Mauvaise évolution changement
de protocole
Tous les patients groupe favorable traités par 4 VAMP ont respecté le protocole de chimiothérapie. Parmi les 70 patients du groupe défavorable traités par 2OPPA/4 COPP, 21 ont présenté une ou plusieurs déviations au protocole:
Omission d’une drogue ou cure incomplète 6 cas
Problème de délai 3 cas
Changement d’une drogue 13 cas
Reçu une drogue supplémentaire 2 cas
Réduction de dose 1 cas
Le changement de drogue a consisté essentiellement en l’utilisation de cyclophosphamide par voie orale au lieu de procarbazine à la même dose et pour la même durée à cause des ruptures de stock.
Le délai médian entre les cures était de 28 jours avec des extrêmes allant de 21 jours dans un cas par erreur sur la date du rendez-vous et de 40 jours dans le cas d’un patient qui a présenté une neutropénie persistante. Le délai inter-cure a été respecté dans 95% des cas.
Nous disposons d’informations concernant la toxicité de la chimiothérapie pour 79 patients parmi lesquels 54 soit 68% ont présenté une ou plusieurs toxicités. Le tableau n°X montre le type de cette toxicité et le nombre des cas correspondants.
Tableau n°X : Type de toxicité et nombre des cas correspondants
Type de toxicité Nombre des cas
Alopécie Isolé 11 et neutropénie 3 et vomissement 15 Associé à neutropénie et vomissement 1 Associé à infection et neutropénie 1 Neutropénie Isolé 6 et infection 2 et vomissement 1 associé à vomissement et diarrhée 1 Associé à vomissement et mucite 1 Mucite Isolé 4 et infection 1 vomissement Isolée 2 Infection Isolée 5
Tableau n°XI : Le type de toxicité et son grade selon OMS
Type de toxicité Grade OMS
I II III Non précisé
Alopécie 2 29
Neutropénie 1 2 13
Vomissement 2 2 9 8
Mucite 2 1 1 2
2- Radiothérapie
Parmi les 94 patients de la série:
la radiothérapie a été faite chez 77 malades soit 82% dont 75 ont été irradiés à l’institut national de l’oncologie (INO) My Abdellah et deux ont été irradiée à titre privé. On dispose des informations sur 56 des patients qui ont été irradiés à l’INO.
non faite chez 17 patients
- Récusée dans 5 cas de MDH stade IV.
- Douze patients sont décédés ou ont abandonné le traitement avant le début de la RTH.
Les patients ont été irradiés par des rayons X de haute énergie (25 MV) ou des rayons γ du cobalt 60 sur les volumes cibles suivants :
Sus diaphragmatiques 33 cas
Sous diaphragmatiques 1 cas
Sus et sous diaphragmatiques 22 cas
Le délai entre fin de la chimiothérapie et début de la radiothérapie était de 59j. La dose médiane était de 25,2Gy en 14 fractions de 1,8Gy à raison d’une fraction par jour et cinq par semaine et l’étalement médian était de 21 j avec des extrêmes allant de 3j à 34 j.
Les types des irradiations sus diaphragmatiques trouvés étaient :
Mantelet 11cas
Mantelet sans axillaire 26cas
Cou+sus claviculaires 15cas
Irradiations des aires ganglionnaires localisées 3cas.
Pour les irradiations sous diaphragmatiques, on trouvait :
Irradiation lombo-aortique et rate 14cas
Irradiation splénique 7cas
G .Evaluation de la réponse au traitement
Pour tous les malades et pour toutes les évaluations intermédiaires, nous avons réalisé une radiographie pulmonaire et une échographie abdominale. La TDM thoraco-abdomino-pelvienne et éventuellement tout autre bilan positif initialement a été réalisé en fin de chimiothérapie.
1- Réponse après deux cures
L’évaluation de La réponse au traitement après l’administration de 2 cures de chimiotheratherapie a été faite chez 68 patients dont 64 avaient répondu de plus de 50% soit 94%, 4 malades avaient une réponse de moins de 50%.
2- Réponse après de 4 cures de chimiothérapie
Parmi les 71 des patients qui ont été évalués après l’administration de 4 cures de chimiothérapie, 63 des malades soit 89% avaient une réponse au traitement de plus de 70 %, 11 % avaient une réponse de moins de 70%.
9%
65% 26%
<70% >=70%
3- Réponse après fin de traitement
Nous possédons des informations de 81 patients sur leur état à la fin de traitement et dont 48 malades avaient une rémission complète soit 59%, 32 patients avaient une rémission complète non confirmée (39,5 %), on note un cas de résistance.
Les localisations trouvées chez les patients qui ont une RC non confirmée étaient :
Masse résiduelle mediastinale 12 cas
Des adénopathies cervicales 12 cas
Des adénopathies abdominales 7 cas
Atteinte de la rate 6 cas
Splénomégalie 4 cas
Nodules spléniques 2 cas Hépatomégalie 2cas Hyperfixation osseuse 2cas Nodule pulmonaire 1cas Rein globuleux bosselé 1cas
76% 7% 1% 16% RC RP Resisrance/Echec non évalué
Figure 7 : Evaluation des malades après fin de traitement
4 – Les événements et calcul de la SSE
Dans notre série, les événements ont été enregistrés chez 19 malades dont : 8 cas d’abandon de traitement
5 cas de rechute 4 cas de décès
Sur les huit cas d’abandon de traitement, cinq ont abandonné en fin de chimiothérapie avant la radiothérapie. Le tableau XII montre les caractéristiques des patients qui ont abandonné le traitement. Tous les patients en abandon de traitement ont été contactés par le data manager. Dans deux cas les parents ont donné un justificatif à l’abandon de traitement et dans tous les autres cas les familles étaient non joignables en utilisant les coordonnées disponibles dans la base de données.
Quatre des cinq cas de rechute ont concerné des patients atteints d’une MDH stade II dont trois étaient classés groupe favorable. Les détails concernant les patients qui ont rechuté sont représentés dans le tableau XIII. Tous les cas de décès ont concerné des patients du groupe défavorable. Le décès est survenu à domicile dans trois cas et à l’hôpital dans un cas. La cause présumée est une varicelle dans deux cas et indéterminée dans les deux autres. Dans tous les cas, le SHOP a été informé du décès après absence du patient a son rendez-vous et convocation par le data manager.
La SSE à 50 mois de recul était 69% 8%. La SSE à 50 mois en censurant les abandons de traitement à la date des dernières nouvelles était de 75% 8% (Figure 8 et figure 9)
Le tableau n° XII : Les caractéristiques des patients qui ont abandonné le traitement
Sexe Age Origine NSE Stade Groupe pronostic Cause Phase
Cas1 M 9 Larache bas III Défavorable Non précisé fin chimio avant RTH
Cas2 M 4 Tanger bas II Défavorable Non précisé fin chimio avant RTH
Cas3 M 9 Hoceima bas IV Défavorable Non précisé fin chimio avant RTH
Cas4 M 7 Taza bas IV Défavorable Non précisé après 2 OPPA
Cas5
M 12 Ouezzane bas III Défavorable Contacté : va bien
sans RTH fin chimio avant RTH
Cas6 M 4 Tanger bas II Défavorable Non précisé COPP3
Cas7
M 5 Kenitra bas III Défavorable Non précisé fin chimio avant RTH
Tableau n° XIII: Les caractéristiques des patients qui ont rechuté au cours de l’étude
sexe âge Origine stade Groupe pronostic Délai de rechute Traitement de la rechute Localisation après rechute Stade après rechute Etat a la DDN
Cas1 M 6 M'diq II Favorable 34 mois
Refus de traitement
Territoire non
irradié III
Vivant en rechute
Cas2 F 13 Rabat II Favorable 40 mois Protocole ICE puis
autogreffe de moelle Territoire irradié + poumon IV poumon Vivant en deuxième RC
Cas3 M 13 Jerada II défavorable 32 mois Cyclophosphamide en
palliatif
Territoire non
irradié + os IV os
Vivant en rechute
Cas4 M 5 Tanger III défavorable 16 mois
BEACOPP
Sus et sous
diaphrag III
Vivant en deuxième RC
Tableau n°XIV: Les caractéristiques des patients qui sont décédés au cours de l’étude
Sexe Age en
année Origine NSE stade
Groupe pronostic Lieu et Cause présumé Durée en mois de participation à l’étude Cas1
M 11 Tata bas III Défavorable A domicile
Inconnu 12
Cas2
M 5 Oujda bas II Défavorable A domicile
Inconnu 6
Cas3
F 8 Fès bas III Défavorable En hospitalier
varicelle? 6
Cas4
M 7 Tétouan bas II Défavorable A domicile
Nous avons enregistré deux cas d`échec ou de résistance. Il s’agit de deux patientes, l’une âgée de 8.5 ans admise pour MDH classée stade IV d’Ann Arbor et traitée dans le groupe défavorable qui est restée évolutive après 2OPPA/COPP avec une réponse partielle après des cycles ICE puis intensification et allogreffe de moelle. La patiente est décédée de maladie évolutive. Le deuxième est âgé de 8 ans classé stade IIIB et traité dans le groupe défavorable. La patiente est en rémission complète après des cures ICE modifié puis radiothérapie à 40 Gy.
Figure 9 : La SSE à 50 mois de recul des 94 patients traités par le protocole MDH –Ma04 en
5- Etat à la date des dernières nouvelles et calcul de la SG
A la date des dernières nouvelles, cinq patients était décédés dont trois en cours de traitement, un en rémission complète et un patient est décédé en maladie évolutive après résistance au traitement. Quatre vingt neuf patients étaient vivants avec 76 RC continue et deux cas de deuxième RC. La survie globale à 50 mois de recul était de 92.8% 3% (figure13) ;
Tableau n° XV: Etats des patients à la date des dernières nouvelles
Nombre des patients Pourcentage
Décès 5 5% Vivants RC Abandon de traitement rechute 89 78 (2 RC2) 8 3 95% 88% 9% 3%
II. COMPARAISON DE LA SERIE 1995 – 2000 AUX RESULTATS DU PROJET MDH-Ma 04
La comparaison des deux séries ne montre pas de différence significative en ce qui concerne l’âge médian au diagnostic, le pourcentage de sujets masculins et les signes d’évolutivité clinique. Les résultats sont représentés dans le tableau XVI qui montre une différence significative en ce qui concerne le type histologique avec significativement plus de type scléro-nodulaire, plus de stade II et moins de stade I dans la série 2. Il existe autant de formes localisés ou avancées et autant de patients du groupe favorable ou défavorable dans les deux groupes.
Tableau n° XVI: Comparaison des caractéristiques générales des patients des
deux séries Série 1 1995-2000 Série 2 2004-2007 P Age médian 8.5 9 NS % masculin 80% 79% NS
Délai diagnostic 6 mois 8 mois NS
Type histologique SN CM 49 41 63 25 < 10-3 Signes B 53 (49%) 49 (52%) NS Stades I II III IV
Stades localisés I-II Stades avancés III-IV
30( 26%) 22( 19 %) 51( 44 %) 12(10 % ) 52 63 (54%) 3(3 %) 40( 47%) 38( 40 %) 13(14%) 43 51(54%) < 10-3 NS Groupe pronostic
La comparaison de l’évolution des patients des deux séries montre significativement plus d’abandon, plus de rechute et de résistance dans la série 1. Le taux de décès est significativement plus élevé dans la série 2. En terme de survie, il n’existe pas de différence significative entre les survies globales des deux groupes. La différence entre les SSE, non significative si on ne tient pas compte des abandons de traitement, devient significative si les abandons sont considérés comme événement. (Voir figure 11 et tableau XVII).
Les résultats de la comparaison de l’évolution des patients sont représentés dans le Tableau n°XVII.
Tableau XVII : La comparaison de l’évolution des patients Série 1 1995-2000 Série 2 2004-2007 P nombre d’événements 71 19 < 10-3 Type d’événement Abandon Décès Rechute Echec ou résistance -37% - 1% -12% -10% -8,5% -4% -5% -2% < 10-3 SSE à 50 mois (abandon
censuré à la DDN) 75% 8 61% 7 NS
SSE à 50 mois avec l’abandon
Figure 10 : Les SSE des patients des séries 1 et 2 en censurant les abandons
Figure 11 : Les SSE des patients des séries 1 et 2 en considérant les abandons de traitement
Courbe de survie globale délai en mois 160 140 120 100 80 60 40 20 0 ta u x d e su rvi e 1.00 .90 .80 .70 .60 .50 .40 .30 .20 .10 0.00
Figure 12 : Les SG des patients des séries 1 et 2.
Globalement les différences entres les deux série sont plus de formes SN dans la série 2, plus de stades I dans la série 2, plus de stades II dans la série 2 et plus d’abandon de traitement dans la série 1. Il existe autant de groupes défavorables dans les deux séries, la différence dans la survie globale est statistiquement non significative et la différence en terme de SSE devient significative si on tient compte des abandons de traitement dans les événements.
Dans les pays en voie de développement et dans un but d’améliorer le pronostic du cancer chez l’enfant un nouveau concept est apparu depuis quelques années, celui de "total care c'est-à-dire le concept de prise en charge globale de la maladie, du malade et de sa famille. Ce concept a été appliqué au Maroc à la MDH dans le cadre du projet MDH-Ma 04. Ce travail donne les résultats du projet MDH-Ma 04 et dans le but d’évaluer l’impact de cette nouvelle stratégie de prise en charge globale, il compare les résultats du projet à ceux d’une série antérieure où le concept n’avait pas encore été appliqué.
Les lymphomes constituent 10-12% des cancers de l’enfant et la troisième affection maligne touchant l’enfant, la maladie d’hodgkin a elle seule une incidence de 7 ,2 par million par an [13]. La MDH a constitué 8 % des cas de cancers chez l’enfant suivis pendant la période de l’étude au Service d’Hémato-Oncologie Pédiatrique de l’HER et le profil clinique des patients suivis dans le cadre de ce projet rejoint celui décrit dans d’autres séries émanant de pays africains avec un âge médian au diagnostic bas et un taux élevé de formes défavorables. Ainsi dans l’étude MDH-Ma 04 les stades avancés ont constitué 55% des cas et ce même taux a été retrouvé dans la série 1 de patients traité dans le même centre entre 1995 et 2000. Le taux plus élevé de stade II avec moins de patients stade I dans la série 2 peut s’expliquer par une meilleur stadification clinique des patients.
Sur le plan histologique, la forme prédominante dans les pays en voie de développement celle à cellularité mixte. Le type histologique prédominant dans la série MDH-04 a été la forme scléro-nodulaire qui a été plus décrite dans les pays développé et chez la population de race blanche dans les pays d’Afrique
[14]. Ce taux de forme SN était significativement plus élevé dans la série 2 par
I – LES RESULTATS THERAPEUTIQUES DANS LA MALADIE DE HODGKIN DE L’ENFANT.
La stratégie thérapeutique actuelle du traitement de la MDH pédiatrique utilise la combinaison entre la chimiothérapie suivie d’une radiothérapie à dose minime (15-25Gy) centrée sur les sites initialement envahis [16]. Ce qui a permis d’obtenir d’excellent taux de survie sans maladie et de survie globale pour la plupart des malades [17]. A titre d’exemple aux USA, le taux de survie globale et de survie sans événement pour les patients de bon pronostic atteint 100% et 96% pour les malades de mauvais pronostic. Les résultats obtenus par les principaux groupes d’oncologie pédiatrique en matière de traitement de la MDH sont représentés dans les tableaux XVIII et XIX.
Tableaux n°XVIII: Résultats de traitement de la maladie de hodgkin groupe
Tableaux n°XIX: Résultats de traitement de la maladie de hodgkin groupe défavorable obtenus par les principaux groupes d’oncologie pédiatriques [18]
C
e résultat a été obtenu grâce à une approche thérapeutique adapté au pronostic de la maladie pour chaque malade. C’est ainsi que plusieurs facteurs cliniques continuent d’influencer le choix et la réussite du traitement mais il n’existe pas de système uniforme de stadification pronostique dans la MDH de l’enfant. Chaque groupe d’étude défini ses propres groupes de risque mais en général les facteurs retenus sont le stade de la maladie, la présence d’une atteinte de type bulky et des symptômes B. [16].Dans un souci de simplicité et de facilité d’application, les patients inclus dans le projet MDH-Ma 04 ont été classés en deux groupes et les facteurs pronostiques utilisés sont ceux décrits précédemment. Ainsi, le groupe de bon pronostic a été défini par l’existence d’une MDH stade I ou II sans atteinte bulky ni signe B ni atteinte contigüe et a été traité par 4 cycles de VAMP suivi de radiothérapie à dose de 15-25 Gy. La même définition du groupe de bon pronostique à été utilisé par le groupe du SJCRH qui initialement a inclus dans ce groupe même les patients présentant des signes B mais les a exclu secondairement de ce groupe après constatation lors des résultats préliminaire de rechutes dans ce groupe de patients [19]. Ces facteurs pronostiques semblaient être les plus adaptés à notre contexte vu le retard diagnostic, le taux élevé de signes B et d’atteintes de type bulky. Le résultat final de ce protocole VAMP a été publié en 2007 et ont montré une SG à 10 ans de 96.1% et une SSE à 10 ans de 89.4% [10]. . Dans notre étude, trois des cinq rechutes ont concerné des patients classés dans le groupe favorable et traités par des cures VAMP mais aucune conclusion ne pourra être tirée avant l’analyse des données à l’échelle nationale.
Tous les patients ne répondant pas aux critères du groupe favorable ont été inclus dans le groupe défavorable et ont été traités par 2OPPA/4COPP utilisés dans le protocole allemand HD95 qui a montré une SSE à 3 ans de 84% [20]. Malheureusement, les résultats rapportés par les structures d’oncologie pédiatrique des pays en voie de développement sont bien inférieurs à ces résultats. Ainsi, le taux de SSE dans la série de MDH traités au SHOP entre 1995 et 2000 ne dépassait pas les 40% [9]. Une étude publiée en 2007 a comparé les résultats du traitement de la MDH de l’enfant dans un centre situé dans un pays en voie de développement (Institut Materno Infantile de Pernambucco à Recife au Brésil) et deux centres d’oncologie pédiatrique aux USA (SJCRH et le Doernbecher Children’s Hospital). Le même protocole thérapeutique a été suivi dans les trois centres. Chez les patients traités dans la première structure, les caractéristiques des patients étaient ceux retrouvés dans d’autres pays en voie de développement avec une prédominance masculine, un âge médian au diagnostique bas et une prédominance de formes à cellularité mixte. Le taux de patients du groupe défavorable était le même dans les trois centres. La survie globale était significativement inférieure chez les patients traités dans la structure du pays en voie de développement avec un taux plus élevé de rechutes et moins de possibilités de rattrapage. La survie dans le groupe favorable traité par des cures VAMP suivis par une radiothérapie des sites initialement envahies était similaire dans les trois groupes [21].
Une étude publiée par l’équipe sud américaine de Stefan et al s’est intéressée à un point important dans la prise en charge du cancer dans un pays en voie du
initiale, la chimiothérapie, la radiothérapie, les évaluations intermédiaires, les soins de support, la radiothérapie et le suivi pendant deux ans, a été estimé à 6647.51 USD. Le coût pour les auteurs reste prohibitif pour un patient vivant dans un pays en voie de développement où le produit intérieur brut PIB dépasse rarement les 2000 USD [22]. Nous nous sommes intéressé également au coût du traitement dans ce projet mais malheureusement il n’a été estimé que pour les cures de chimiothérapie et c’est ainsi que l’un des critères de choix du protocole thérapeutique a était de prendre à efficacité égale, le protocole le moins couteux. Le fait de choisir le protocole le moins toxique et le plus facilement administrable permet une réduction importante du coût.
II. LA PROBLEMATIQUE DE L’ONCOLOGIE PEDIATRIQUE DANS LES PAYS EN VOIE DE DEVELOPPEMENT
Les pays en voie de développement sont définis par un revenue national global annuel inférieur à 735 USD[23]; une réalité économique qui a un grand impact sur la politique sanitaire de ces pays (3% de dépense pour la santé[24] et surtout sur la prise en charge du cancer chez l’enfant qui ne constitue pas une priorité par rapport aux maladies infectieuses (AIDS , malaria, tuberculose...) qui sont considéré comme problèmes majeurs surtout l’immunodéficience acquise qui est à l’origine de 20% de mortalité dans la population de quatre pays subsahariens[25]. D’autres obstacles se dressent devant l’oncologie pédiatrique dans ces pays, tel que la croissance démographique importante. C’est ainsi que plus de 86% des enfants dans le monde vivent dans les pays sous développes et ce chiffre est en augmentation [26] malgré les grands efforts politiques d’encourager la planification familiale et l’Inde donne l’exemple de l’échec de
Les croyances culturelles, l’ignorance qui dépasse 90% dans certains pays[28] ainsi que la situation socioéconomique très limitée des parents ont pour conséquence de limiter l’accès aux centres de traitement adéquat qui sont le plus souvent centrés dans les grands villes et favorisant alors le recours à la médecine traditionnelle et n’oublions pas le coût des voyages et le coût du traitement [3] qui ont le même impact.
Tous ces problèmes sus cités ainsi que plusieurs d’autres constituent la source majeur de refus et d’abondons de traitement et qui constituent à leurs tours les vrais problèmes de l’oncologie pédiatrique dans les pays en voie de développement comme le montre une étude récente de la SIOP [4] et qui défini le refus du traitement par le rejet de toute intervention thérapeutique tandis que l’abandon du traitement si le traitement est démarré mais non achevé [12]. Arora et son équipe a effectué une recherche medline dans la littérature médicale sur l’importance du problème d’abandon au traitement, ses causes et les mesures préventives et ont trouvé un ensemble de cohortes prospectives et rétrospectives publiés dans certains pays sous développés et qui montre l’importance de ce problème. On peut citer l’exemple du centre de Mumbai et son étude sur 46 patients suivis pour tératome et traités entre 1994 et 2004 avec un taux d’abandon à 19%. Au Guatemala, sur un échantillon de 431 patients traités pour cancer durant la période de 1993 à 1997, le taux d’abandon était de 41% [2]. Enfin, au Maroc, on trouve dans la série de 181 enfants traités de 1995 à 2000 pour MDH 50 % de taux d’abandon de traitement. L’importance de ce problème