Ecole d’Infirmier(e)s Anesthésistes Assistance Publique-Hôpitaux de Marseille
BAGNOL Delphine
Promotion 2005-2007
REMERCIEMENTS
Mes remerciements vont tout d’abord aux deux personnes qui m’ont guidé dans la réalisation de ce travail de fin d’études, le Docteur Olivier MAURIN praticien au Bataillon de Marins-Pompiers de Marseille et à Madame Marie-Claude SIMONIN cadre de santé au Service Mobile d’Urgence et de Réanimation de l’hôpital de la Timone.
Je remercie de même les cadres enseignants de l’école d’infirmier(e)s anesthésistes de Marseille qui ont encadré ma formation professionnel, Madame Cathy JUANEDA et Madame Marie-Josée SANCHEZ GUIDA.
Merci à tous les professionnels rencontrés au cours des stages, grâce à qui j’ai pu acquérir un savoir-faire technique, et qui ont participé à mon mémoire en acceptant de répondre aux questions que je leur ai soumis.
Je remercie également mes proches qui, par l’intérêt qu’ils ont porté à mon projet, par leur soutien, et leurs conseils m’ont permis de progresser sereinement.
A chacun d’entre eux et aux autres, Merci !
Sommaire.
• Remerciements Page 1
• Sommaire Page 2
I. Introduction. Page 3
II. Apports théoriques.
A. Historique de la médecine préhospitaliére
L’origine Page 5
Les SMUR Page 7
B. Intubation difficile
• 1.Définitions Page 8
• 2.Pratique Page 11
• 3.Matériels Page 15
C. Intubation difficile en milieu préhospitalier Page 26
• 1.Epidémiologie Page 27
• 2.Morbidité Page 28
• 3.Facteurs associés Page 29
• 4.Matériels Page 34
• 5.Algorithme Page 38
III. Etude rétrospective.
A. Méthodologie Page 41
B. Entretiens Page 43
IV. Conclusion. Page 62
• Bibliographie Page 64
• Références Page 65
• Annexes Page 68
I. INTRODUCTION.
Le sujet de mon travail d’intérêt professionnel de fin d’études est le fruit d’une réflexion personnelle fondée sur mon expérience de terrain en tant qu’infirmière (IDE) et sur les stages de formation d’infirmière anesthésiste (IADE).
Le thème de mon mémoire est l’intubation difficile. Ma motivation s’est portée sur deux points ; celle de la spécialité d’infirmière anesthésiste et celle de maîtriser un acte précis et vital.
De part le Décret de compétence no 2004-802 du 29 juillet 2004 relatif aux parties IV et V du code de la santé publique Article n°R.4311-12 (cf. Annexe 1) les infirmièr(e)s anesthésistes ainsi que les médecins possèdent la qualification nécessaire pour réaliser une intubation.
Cette compétence est davantage liée aux conséquences qu’elle peut entraîner qu’à la réalisation du geste technique. Justifiée par la nécessité du contrôle des voies aériennes ou d’une assistance ventilatoire, l’intubation est un acte fréquent mais pas anodin. Lorsque celui- ci devient difficile à réaliser, le pronostic vital du patient est engagé. L’importance de réussir correctement cet acte a été le second point de ma motivation.
Ce n’est qu’au cours de mon stage au Service Mobile d’Urgence et de Réanimation (SMUR) que j’ai pu définir l’orientation de mon travail de recherche. Par comparaison avec mes stages au sein des différents blocs opératoires, je me suis rendu compte que dans les SMUR le matériel d’intubation difficile était souvent inexistant ou non fonctionnel. Pourtant dans l’urgence, pour un patient qui présente une détresse vitale, l’équipe médicale peut avoir recours au plateau d’intubation difficile.
Suite à ce constat, j’ai relevé plusieurs points importants qui mettent en avant la nécessité de la présence de ce plateau lors d’intervention du SMUR :
• La Fréquence des intubations difficiles en préhospitalier est importante (10 à 20% en France selon différentes études [1,4,5,6])
• La Société Française d’Anesthésie et de Réanimation (SFAR)
recommande la présence d’un plateau d’intubation difficile dans chaque lieux où des
anesthésies sont pratiquées.
• Le caractère urgent auquel est confrontée le SMUR est une des causes de difficultés lors de l’intubation.
• La consultation préanesthesie n’a pas été réalisée et il semble difficile de dépister les intubations difficiles en évaluant les facteurs anatomiques du patient (classe de Mallampati, distance thyromentonniére, ouverture de bouche…) dans les conditions d’urgence.
A ces difficultés peuvent s’ajouter des pathologies ou des terrains anesthésiques fréquemment rencontrés en SMUR : polytraumatisé, incarcération, traumatisme du rachis, traumatisme facial, estomac plein...
De ces constats, on peut se demander si le matériel et la formation du personnel à l’intubation difficile influent sur la prise en charge des patients en préhospitalier.
Nous nous proposons donc d’étudier dans ce travail, les différents axes de cette hypothèse qui sont :
- l’intubation difficile et son matériel spécifique - le milieu préhospitalier
- les connaissances théoriques et pratiques des médecins et des IADE exerçant
en SMUR sur l’intubation difficile.
II. APPORTS THEORIQUES.
A. HISTORIQUE DE LA MEDECINE PREHOSPITALIERE . A l’origine…
La conscience d’une action rapide dans certaines circonstances existe déjà dans l’antiquité ; au VI
émesiècle avant JC, Hippocrate affirme que « les moments favorables pour intervenir passent promptement et la mort survient si on a trop tardé ».
L’origine de l’Aide Médicale d’Urgence (AMU) est liée à la pratique de la guerre. C’est donc sur les champs de bataille, au début de l’ère chrétienne que les premières actions de secours aux victimes ont lieu.
Au XI
émesiècle, les chevaliers de l’Ordre de Saint Jean de Jérusalem, bénéficiant de la meilleure formation de l’époque acquise auprès des médecins grecs et arabes, dispensent les premiers soins aux blessés des deux camps dans des tentes installées à coté des champs de bataille.
Au XII
émesiècle, François 1
erRoi de France, crée le Grand Bureau des Pauvres destiné à secourir les malades trop faibles pour se rendre à l’hôpital.
Le Baron Dominique Larey, chirurgien de la Grande Armée de Napoléon Bonaparte, crée, en 1792, les premières « ambulances volantes ». C’est le début de l’organisation de l’Aide Médicale Urgente.
Le principe est d’aller au devant des blessés, jusque sous le feu ennemi, pour prendre en charge les blessures le plus rapidement possible, prévenant ainsi les complications. Pour la première fois on trouve un médecin dans une ambulance. Larey donne la consigne suivante : « on commencera toujours par les plus dangereusement blessés, sans égard aux rangs et aux distinctions ».
En 1859, lors de la bataille de Solferino, Henri Dunant, bouleversé par le massacre qui se
déroule sous ses yeux, porte secours aux blessés avec 300 volontaires, il fondera ensuite la
Croix-Rouge en 1863.
Lors de la Guerre de Sécession aux Etats-Unis, une véritable organisation moderne du service de santé militaire apparaît, avec des médecins et des infirmiers formés spécialement à cet exercice.
A New York le service des ambulances de l’hôpital Bellevue a été établi en 1869 « Si le blessé ne parait pas transportable au poste de police, l’alerte est donnée directement à l’hôpital par l’appareil télégraphique le plus proche. 43 secondes après…l’ambulance sort de l’hôpital. Ces voitures sont légères et attelées d’un seul cheval. A l’intérieur se trouve un brancard monté sur un rail, dans une caisse sont aménagés des instruments, des médicaments. Le médecin est assis à l’arrière et le cocher actionne au pied une sonnerie afin de demander le passage. »
En 1924, le médecin commandant Charles Cot met sur pied à Paris un service de secours pour les situations urgentes. Il introduit en médecine d’urgence la règle de trois principes sauvetage, secourisme et soins médicaux. Estimant que les soins doivent aller à la victime il s’insurge contre le transport rapide et sans précautions d’une victime évacuée rapidement vers l’hôpital.
En 1956, à la suite d’une épidémie de poliomyélite à forme respiratoire, le Ministère de la Santé charge le laboratoire expérimental de physique de l’Assistance-Publique, d’étudier les possibilités de transport des patients présentant une insuffisance respiratoire.
C’est une ébauche du premier SMUR : véritable unité de réanimation qui se déplace et permet la médicalisation des premiers secours. Le professeur Lareng aménage un fourgon avec un poumon d’acier et une équipe composée d’un médecin et d’une infirmière.
C’est dans les années 60, qu’une poignée de médecins prend conscience de la disproportion entre les moyens impressionnants mis en œuvre dés l’arrivée à l’hôpital d’un blessé et ceux, plus archaïques, utilisés dans la phase préhospitaliére.
Sur ce constat les professeurs Cara, Lareng et Serre mirent en place la médicalisation des secours.
En 1965, la création des services d’urgences et des services de réanimation dans les hôpitaux se distinguent des services mobiles d’urgences et de réanimation (SMUR).
Le premier Service d’Aide Médicale Urgente plus communément appelé SAMU sont des
réseaux fixes, chargés de coordonner les efforts médicaux entre les équipes préhospitaliéres
assurées par le SMUR et les services d’urgences hospitalières. Il fut crée en 1968 à Toulouse par le professeur Louis Lareng.
Il faudra attendre 1976 pour voir leur officialisation, avec la réception et la centralisation des appels téléphoniques du public au « Centre 15 » et la coopération entre structures hospitalières et structures extra-hospitalières.
Les SMUR
De nos jours en France, les SMUR sont une composante de l'urgence médicale à côté des services spécialisés d'accueil et de traitement des urgences (SAU). Une équipe mobile se compose d'un médecin urgentiste, d'un(e) infirmier(e) et d'un ambulancier. Ils se déplacent dans une unité mobile hospitalière (UMH), qui peut être un véhicule terrestre de type ambulance, véhicule léger ou de liaison, un hélicoptère, voir un moyen aéronautique dans lequel on trouve tout le matériel d'une chambre de réanimation (médicaments, matériel de ventilation artificielle, surveillance des paramètres vitaux etc.). Leur rôle est d'apporter sur place au patient les meilleurs soins possibles ; et de définir en accord avec le SAMU le service le plus adapté pour recevoir le patient et d'assurer son transport dans les meilleures conditions.
Les SMUR effectuent également des interventions au sein de l'hôpital, en cas de détresse vitale dans un service : ces interventions sont appelées « pédestres ». Ils peuvent également assurer le transfert de patients vers un autre établissement qui dispose de moyens techniques plus adaptés à l'état de santé du patient. Ces types d'intervention sont appelés :
« Secondaires » .
Les véhicules et vêtements du personnel portent souvent la mention « SAMU », il y a donc de
fait fréquemment une confusion entre SMUR et SAMU. Même s'ils sont intimement liés, les
SAMU sont des réseaux fixes alors que les SMUR sont des unités mobiles. Il y a
habituellement un SAMU par département et des SMUR dans plusieurs hôpitaux afin de
couvrir au mieux le territoire. Le nombre de SMUR en France s’élève à plus de 350 en
France.
B. INTUBATION DIFFICILE.
L’intubation orotrachéale (IOT) constitue un geste courant pour l’anesthésiste- réanimateur. Elle s’effectue le plus souvent, grâce à un matériel simple et dans une position standardisée. L’éventualité d’une intubation difficile (ID), plutôt rare, doit être détectée par un examen préanesthésique. Enfin, si tout membre de l’équipe d’anesthésie ne peut maîtriser l’ensemble des techniques décrites en cas d’intubation difficile, il doit toujours être capable d’assurer une oxygénation efficace.
Par le biais de la Société Française d’Anesthésie et de Réanimation (SFAR), un comité d’experts a défini les bonnes pratiques cliniques pour la détection de l’intubation difficile, à préconisés les techniques et le matériel à utiliser et à donner des recommandations sur l’enseignement des techniques alternatives à l’intubation traditionnelle. Ces bonnes pratiques ont pour objectif de réduire la morbidité de l’intubation difficile.
1. Définitions.
• On considère qu’une intubation est difficile pour un anesthésiste expérimenté, lorsqu’elle nécessite plus de 10 minutes et/ou plus de deux laryngoscopies, dans la position modifiée de Jackson avec ou sans compression laryngée (manœuvre de Sellick).
Position modifiée de Jackson.
• Une laryngoscopie difficile se définit par l’absence de vision de la fente glottique (grades III et IV de Cormack et Lehane).
• La ventilation au masque est considérée comme inefficace lorsqu’on n’obtient pas une SpO
2> 90% en ventilant en oxygène pur les poumons d’un sujet normal.
La fréquence de l’intubation difficile représente 0,5 à 2% en chirurgie générale, celle-ci serait moindre en anesthésie pédiatrique. En revanche, en obstétrique et en chirurgie carcinologique ORL, les fréquences sont plus élevées. Toutefois en médecine préhospitalière la fréquence de l’intubation difficile s’élève entre 4 et 11 %.
L’intubation difficile est responsable, directement ou indirectement, du tiers des accidents entièrement imputables à l’anesthésie et représente ainsi, chez l’adulte, la première cause de morbidité et de mortalité anesthésique. Le pronostic de ces accidents est très péjoratif, puisque dans deux tiers des cas, le patient décède ou présente des séquelles neurologiques graves. Quelle que soit la qualité de l’évaluation préopératoire, il faut souligner que dans 15 à 30% des cas d’intubation difficile ne sont pas détectés avant l’anesthésie.
Structures visibles : I. Toute la glotte II. Partie postérieure de
la glotte
III. Epiglotte seulement
IV. Palais seulement
Stades de Cormack.
Cette détection doit être systématique lors de toute consultation préanethésique, par un interrogatoire et un examen clinique, même si une anesthésie locorégionale est programmée.
Les résultats, précisant les tests utilisés, doivent être colligés par écrit. L’interrogatoire porte sur les conditions de déroulement des anesthésies antérieures. L’examen clinique recherche les lésions dentaires et/ou gingivales. Seront aussi mis en avant les antécédents et les signes d’obésité morbide, d’affection rhumatismale, de traumatismes maxillo-faciaux.
L'examen s'effectue en quatre temps, de face, de profil, bouche fermée et bouche ouverte:
• Temps 1, de face, bouche fermée, pour rechercher une asymétrie mandibulaire, des cicatrices faciales et/ou cervicales, un goitre ou un cou court.
• Temps 2, de face, bouche ouverte, pour préciser l'inclinaison des incisives supérieures, des dents manquantes ou fragilisées et la possibilité de subluxation antéropostérieure de la mandibule. La bouche est ensuite ouverte au maximum, pour évaluer la distance interdentaire et les classes de Mallampati. Ces mesures sont effectuées chez le patient assis, regard à l'horizontale, sans phonation.
• Temps 3, de profil, regard à l'horizontale, pour rechercher une rétrognathie et mesurer la distance mentonos hyoïde.
• Temps 4, de profil, avec la tête en extension maximale, pour mesurer la distance menton-cartilage thyroïde.
Dans cette série de tests, trois éléments tels que la mesure de l’ouverture de bouche, l’évaluation de la classe de Mallampati, la mesure de la distance thyromentonnière déterminent le recours à une intubation difficile. Une intubation difficile sera donc envisagée chez l’adulte si l’ouverture de bouche est inférieure à 35 mm, la classe de Mallampati supérieure à 2 et la distance thyromentonnière inférieure à 65 mm.
De plus, l’ouverture de bouche inférieure à 20 mm, le rachis bloqué en flexion, une dysmorphie faciale sévère de l’enfant ou bien des antécédents d’échec d’intubation par voie orotrachéale doivent être considérées comme des causes d’intubation impossible par voie orotrachéale.
Dans certaines affections, une évaluation plus ciblée est nécessaire : affections cervico-
faciales, obstétrique, pédiatrie, orthopédie et traumatologie, médecine préhospitalière.
2. Intubation difficile en pratique.
Avant l’induction d’un patient à risque d’intubation difficile, il convient de s’assurer de la présence d’aide et de la disponibilité du matériel pour l’intubation difficile.
Plusieurs facteurs influent sur le choix des modalités anesthésiques en cas d’intubation difficile prévue : la vacuité gastrique, la voie d’abord orale ou nasale, la technique d’intubation choisie, l’état cardiorespiratoire, les contraintes chirurgicales et la coopération du patient. Trois niveaux d’anesthésie peuvent être envisagés : une intubation vigile, une intubation sous anesthésie générale en ventilation spontanée, enfin une intubation sous anesthésie générale avec curarisation.
L’administration d’atropine peut être réalisée avant l’induction (10 μ g/kg IV). Une préoxygénation d’au moins 4 minutes est impérative. La méthode de référence est la ventilation spontanée en oxygène pur avec un masque facial étanche, pendant une durée d’au moins 4 minutes. On peut la remplacer par quatre cycles de ventilation à pleine capacité vitale chez les patients anxieux, mais le délai d’apparition d’une hypoxémie en apnée est plus court.
La préoxygénation doit être prolongée chez l’insuffisant respiratoire. Le délai d’apparition de l’hypoxémie en apnée est plus court chez l’enfant, la femme enceinte et l’obèse.
La méthode d’oxygénation pendant l’intubation la mieux adaptée doit être choisie avant l’induction. La ventilation manuelle au masque facial est la méthode la plus fréquemment utilisée, mais elle expose au risque de distension gastrique si la pression d’insufflation dépasse 20 cmH
2O, elle est parfois inefficace et s’interrompt pendant les manœuvres d’intubation. Lorsque la ventilation au masque est/ou devient inefficace, la situation peut rapidement devenir catastrophique si un abord trachéal n’est pas assuré dans les plus brefs délais. Les causes d’échec de la ventilation au masque sont la macroglossie (obésité, grossesse, tumeurs, syndrome d’apnées du sommeil), les fuites au niveau du masque (déformation faciale, barbe, édentation) et des voies aériennes supérieures (plaie, pharyngostome), les corps étrangers et les rétrécissements des voies aériennes (laryngospasme, tumeur, œdème, sténose).
L’administration d’oxygène pendant les tentatives d’intubation est utile chez l’adulte
(10L/min) et indispensable chez l’enfant.
Quelle que soit la méthode choisie (cathéter pharyngolaryngée, laryngoscope conçu à cet usage, jet ventilation…) il faut s’assurer d’une expiration correcte, afin d’éviter les accidents barotraumatiques.
L’anesthésie locale ou locorégionale est recommandée, car elle facilite l’intubation en supprimant les réflexes liés à la stimulation des voies aériennes supérieures. Toutefois, l’anesthésie locale pharyngée comporte un danger accru de laryngospasme.
Le propofol est recommandé comme agent anesthésique en cas d’intubation difficile prévue.
Toutefois, d’autres agents anesthésiques peuvent être employés en cas de contre-indication.
Tel est le cas de la kétamine dans les situations d’urgence. L’halothane et le sévoflurane sont préconisés chez le nourrisson.
L’anesthésie légère est un facteur qui concourt à rendre l’intubation plus difficile.
L’adjonction d’un curare à l’anesthésie ne peut être envisagée que secondairement, lorsqu’un relâchement musculaire est jugée indispensable à la réussite de l’intubation, après s’être assuré que la ventilation au masque est possible. Le suxaméthonium est recommandé dans ce cas.
Lorsque l’intubation est jugée impossible, seule les techniques d’anesthésie vigile sont autorisées chez l’adulte, à l’exception des situations où l’oxygénation peut être maintenue.
En cas d’estomac plein, seule l’intubation sous anesthésie vigile doit être pratiquée, et l’anesthésie locale ne doit pas s’étendre au larynx.
Selon Statistique France et Canada, plus de deux millions de personnes de 15 ans et
plus ont subi une intervention chirurgicale non urgente, en France, en 2001. Tous ces patients
n’ont pas nécessairement reçu une anesthésie générale et on pourrait ajouter à leur nombre
ceux qui ont subi une intervention non réglée ou une anesthésie obstétricale, et les opérés de
moins de 15 ans. Le bi-million de cas étant notre point de départ et l’incidence d’un scénario
d’intubation impossible et de ventilation impossible (IIVI) étant d’environ 0,02 à 0,14%, il y a
de 200 à 1400 incidents annuels à traiter à travers le pays. De même, selon les incidences
souvent citées pour l’intubation difficile (1 à 4%), il y aurait de 10 000 à 40 000 cas, et pour
les échecs à l’intubation (0,09 à 0,6%), il y aurait de 900 à 6 000 incidents. Dans de
nombreuses situations, les difficultés ne peuvent être prévues malgré une évaluation
préopératoire minutieuse. La démarche à adopter devant une intubation difficile imprévue doit
donc être préformulée et maîtrisée. Il est indispensable d'établir un protocole d' intubation
difficile tenant compte des situations rencontrées dans la pratique de chacun.
Toutefois, les algorithmes proposés ont l'intérêt d'être applicables aux situations d’intubation difficile prévue et non prévue. La formation du personnel et la composition du chariot d'intubation difficile sont établies en fonction de ces protocoles.
En dehors de conditions d'urgence, lorsque la technique permettant de surmonter la difficulté n'est pas disponible ou n'est pas maîtrisée par l'anesthésiste, le transfert du patient ou l'appel à une équipe spécialisée est indispensable. Il est le plus souvent inutile de réutiliser la même technique, quand le premier essai a échoué. De plus, au-delà de trois essais, le risque de ne plus pouvoir ventiler au masque devient important. Il faut toujours privilégier les techniques comportant le moins de risques iatrogènes. Comme la priorité est à l'oxygénation, la méthode choisie suppose que celle-ci pourra être maintenue pendant l'ensemble des manœuvres d'intubation. L'éventualité de réveiller le patient doit être envisagée à chaque étape.
Enfin, le choix d'une anesthésie locorégionale ne supprime pas le risque de l’intubation
difficile (échec ou complications de l'anesthésie locorégionale). Cette situation doit être
envisagée avant l'intervention et les moyens pour y faire face doivent être prévus.
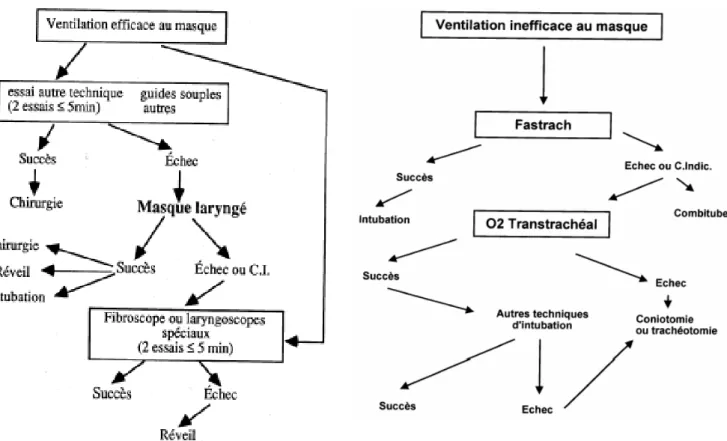
Algorithme décisionnel devant une intubation difficile imprévue.
La priorité absolue est de maintenir une oxygénation suffisante pendant les diverses manœuvres jusqu'au succès de l'intubation ou à la reprise d'une ventilation spontanée. Les algorithmes sont appliqués en fonction de la possibilité ou non de ventiler efficacement au masque (fig. 1 et 2). La règle principale consiste à prévenir les complications de l’intubation difficile que sont l'hypoxie et l'inhalation des sécrétions. Il importe d'accepter à temps l'échec de l'intubation et de demander de l'aide (aide technique, anesthésiste senior). Lorsqu'une oxygénation efficace est obtenue malgré l'échec de l'intubation, le réveil du patient doit toujours être envisagé.
Figure 1: Arbre décisionnel en cas de ventilation efficace au masque facial.
Figure 2: Arbre décisionnel en cas de ventilation
inefficace au masque facial.
3. Matériels d’intubation difficile.
Même en situation d’urgence la priorité est d’abord d’oxygéner le patient et ensuite la possibilité de l’intuber.
Depuis quelques années, de plus en plus de techniques alternatives et de matériels ont été développés pour l’intubation difficile.
a) Moyens simples.
• Position amendée de Jackson ou ‘Sniffing Position”
C’est une surélévation de la tête avec une légère flexion cervicale. Cette position permet une amélioration de la visualisation de la glotte lors de la laryngoscopie.
• Pression laryngée externe
La pression laryngée externe permet d’améliorer l’exposition laryngoscopique en faisant
descendre la glotte et donne la possibilité de corriger une déviation.
• La manœuvre de “BURP”(blackwards, upwards and rightwards pressure)
Cette manœuvre consiste à réaliser une pression sur le cartilage cricoïde, thyroïde et l’os hyoïde vers l’arrière, le haut et la droite. Elle permet de déplacer le cartilage thyroïdien du patient dans un mouvement d’abord postérieur puis céphalique. Elle diminue l’incidence des laryngoscopies difficiles par une meilleure exposition laryngoscopique.
• Les laryngoscopes.
Plusieurs types d’adaptation de matériel pour laryngoscopie directe ont été commercialisés et sont disponibles sur le marché.
o Le laryngoscope à manche court indiqué chez les patients obèses à cou court.
o Le laryngoscope de Bullard : c’est un prototype des laryngoscopes à vision indirecte par oculaire. Equipé d’une lame mince, très recourbée et d’un éclairage par fibre optique. Le champ de vision observé à partir d’un œilleton est d’environ 55°. Il permet ainsi d’exposer la glotte en position neutre rendant inutile toute manipulation de la tête et du cou. Il a une indication chez les patients traumatisés crâniens mais aussi chez les patients dont les difficultés d’intubation viennent du peu d’ouverture de la bouche ou de l’incapacité d’aligner les axes de la bouche, du pharynx et du larynx. Le larynx une fois en vue, on glisse entre les cordes vocales le tube trachéal, déjà monté sur un stylet incorporé à la lame.
Ce laryngoscope trouve ses limites chez les patients avec un long cou car la longueur de la
lame ne permet pas toujours une exposition glottique.
o Le laryngoscope de Mc Coy : il possède un levier situé le long du manche du laryngoscope permettant de relever l’extrémité distale mobile de la lame. Cette angulation permet de soulever l’épiglotte et de mieux visualiser les cordes vocales.
o Le laryngoscope de Piquet, Crinquette et Vilette (PCV) [2] est un laryngoscope tubulaire avec une lame semi-circulaire, incurvée, à lumière froide, pouvant accepter une sonde d'intubation à ballonnet n° 8. Sa section est en forme de C fermé, ce qui permet au laryngoscope de servir de guide à la sonde. Le PCV peut être introduit par voie orale à droite ou à gauche, et en rétro molaire. Ce type de lame permet de récliner les grosses tumeurs friables et bourgeonnantes de la glotte, en chargeant l'épiglotte et en intubant « à travers » la lésion. Elle est particulièrement indiquée en ORL dans les lésions déformant l'orifice glottique. Dans ces indications le PCV remplace le fibroscope souple. La technique est aussi intéressante lorsqu'il existe une limitation de l'ouverture buccale, ou un espace prémandibulaire peu compressible, car la lame déplace la langue sur le côté.
• Les lames de laryngoscopes.
Les lames métalliques réutilisables peuvent faciliter une intubation difficile du fait de la rigidité de la lame et de sa longueur par rapport à une lame jetable a usage unique.
La lame droite ou de Miller permet de charger directement l’épiglotte ou de contourner la
base de la langue quand l’espace prémandibulaire est peu compressible. Cette lame très
utilisée chez l’enfant est également indiquée chez les patients obèses ou a ouverture de
bouche réduite.
La lame angulée à prisme de Belhouse. Cette lame incorpore un prisme permettant d’élargir l’angle de vision. Elle facilite la laryngoscopie en présence d’une limitation de l’extension cervicale.
Lame de Jackson-Wisconsin qui facilite le refoulement et la contention de la langue sur le côté lorsque l'espace prémandibulaire est peu compressible.
Le prisme de Hoffman s’adapte sur l’extrémité proximale d’une lame classique permettant d’augmenter de 30° l’angle de vision.
• Les sondes d’intubations.
Ils en existent de différents types : PVC, avec ou sans ballonnets, préformées, armées.
Les sondes armées permettent de faciliter l’intubation orotrachéale grâce à une flexibilité plus importante.
Le choix d’une sonde d’intubation de diamètre plus petit peu également faciliter l’intubation orotrachéale.
Les sondes trachéales pour microchirurgie laryngée MLT™ possèdent un faible diamètre externe et une longueur correspondant à celle d’une sonde standard n°8. Elles permettent de réaliser l’intubation trachéale dans le cas ou l’espace pharyngée et/ou laryngée sont réduits.
• La pince de Magill.
Elle permet d’améliorer l’orientation de la sonde d’intubation notamment lors d’une intubation nasotrachéale.
• Les mandrins souples.
L’utilisation d’un mandrin souple cathétérisant la sonde d’intubation fait partie des « petits moyens » face à une difficultée d’intubation. Ce type de mandrin est systématiquement utilisé dans les protocoles d’intubation en urgence aux Etats-Unis. Le mandrin souple permet d’imprimer à la sonde d’intubation l’orientation souhaitée.
Le mandrin peut également être utilisé d’une autre manière. Celui ci peut être introduit dans la trachée sous laryngoscopie directe permettant ensuite de faire glisser la sonde d’intubation sur le mandrin.
Le mandrin de Schroeder est un mandrin dont on peut modifier la courbure pendant l’avancement de la sonde d’intubation par pression sur un piston proximal.
On peut également utiliser un guide creux qui permet l’oxygénation concomitante.
• Les mandrins d’Eschmann ou bougies.
Les mandrins longs sont généralement désignés sous le terme de mandrins « d’Eschmann ».
Ce sont des mandrins qui permettent une intubation à l’aveugle sous laryngoscopie directe par la technique de Seldinger en cas de difficulté de visualisation de l’orifice glottique. Ce sont des mandrins longs, flexibles dont l’extrémité distale est recourbée dans les derniers centimètres.
Mandrin d’Eschmann
b) Moyens sophistiqués.
• Stylet lumineux ou Trachlight™.[3]
Le Trachlight™ est un dispositif permettant une intubation à l’aveugle en position neutre et peut être indiqué chez des patients victimes de traumatismes crâniens. Le Trachlight™ diffère des anciens modèles en plusieurs points : l'éclairage est intense, ce qui permet une transillumination efficace même à la lumière ambiante, le stylet rétractile à l'intérieur du mandrin rend le dispositif plus flexible, ce qui facilite l'intubation orale et nasale. Le mandrin flexible permet de visualiser, par transillumination, l'extrémité de la sonde d'intubation dans la trachée. Le repérage de la situation intra trachéale de l’extrémité distale se fait par transillumination sus-sternale, à travers la membrane crico-thyroïdienne.
Le Trachlight™ est composé de trois parties : un manche réutilisable, un guide jetable et un
stylet rigide malléable et rétractable. Il comporte à son extrémité distale une ampoule bulbaire
de grande intensité lumineuse. La forme de l'ampoule permet de projeter le faisceau lumineux
dans l'axe et en avant pour obtenir une transillumination optimale.
Le Trachlight se divise en deux parties. À l'extrémité proximale du guide se trouve le dispositif d'alimentation qui permet le raccordement au rail électrique du manche.
Le stylet métallique amovible, introduit dans le guide, permet de donner la courbure souhaitée en forme de « crosse de Hockey » au système sonde d'intubation-mandrin. Ceci facilite le positionnement de la sonde devant le larynx, mais gêne ensuite le passage dans l'orifice glottique. Le retrait du mandrin permet à la sonde, montée sur le guide souple, de franchir cet orifice et de s'adapter à la courbure des voies aériennes. Le manche du dispositif contient la source lumineuse. Il est muni d'un système de rail sur la face supérieure permettant d'adapter la longueur du mandrin à celle de la sonde et faisant le contact. À sa partie distale, il est muni d'un clip qui solidarise la sonde au manche.
Stylet lumineux ou Trachlight™
• Masque laryngée.
Conçu par Brain en 1981, le masque laryngé est un dispositif oropharyngé avec une partie gonflable distale qui va coiffer le larynx et assurer l’étanchéité de l’orifice laryngé.
Initialement proposé comme alternative au masque facial, son champ d’indication s’est élargi à la prise en charge de patients difficiles à ventiler au masque ou à intuber. Il permet la ventilation et l’oxygénation du patient de maniére peu invasive.
En 1997, Brain crée une évolution du masque laryngé spécifiquement dévolu pour l’intubation difficile : le Fastrach™
• Le Fastrach™.
C’est une technique alternative à l’intubation endotrachéale sous laryngoscopie directe et peut être utilisée comme technique de seconde intention en cas d’intubation difficile. C’est un dispositif supralaryngé permettant une intubation à l’aveugle. Il est dérivé du masque laryngé dont il reprend la forme dans sa partie distale. Néanmoins, il diffère par l’adjonction d’un conduit rigide en acier gradué et incurvé muni d’une poignée permettant une traction aisée.
Le Fastrach™ est conçu pour assurer une intubation endotrachéale à l’aveugle en cas de difficulté a intubé ou devant l’obligation de conserver l’axe du rachis immobile.
Le Fastrach™ peut être introduit si l’ouverture de bouche est supérieure à 2cm.
• Le Combitube™.
Technique alternative à l’intubation endotrachéale en situation d’urgence.
Ce matériel a été développé et inventé en Autriche par Fass et Fenseren en 1987. Il permet une ventilation avec protection des voies aériennes sans positionnement obligatoire de la sonde dans la trachée.
Il s’agit d’une sonde à double lumière en PVC, parcourue par deux canaux de gonflage et deux ballonnets (trachéal et pharyngé). Le cylindre obturé (sonde oesophagienne ) est percé d’orifices dans sa partie moyenne permettant une ventilation pulmonaire lorsque le dispositif est en position oesophagienne. La voie ouverte à l’extrémité distale constitue la sonde trachéale, elle est munie d’un ballonnet. Lorsque la sonde est en position trachéale, son fonctionnement est identique à une sonde endotrachéale classique. Des couleurs permettent de différentier les deux voies.
Combitube en position œsophagienne
Combitube en position
trachéale
• L’intubation rétrograde.
Cette technique a été introduite en 1960 par Butler et al. qui proposent une intubation guidée par un cathéter passé à travers un orifice de trachéotomie et dont l’extrémité distale se situe dans la cavité buccale. La technique s’est modifiée progressivement en proposant une ponction de la membrane cricothyroïdienne à l’aiguille. Le terme d’intubation rétrograde est d’ailleurs incorrect, l’intubation se fait par voie antérograde mais après passage « rétrograde » d’un mandrin du larynx vers la bouche. On récupère ce mandrin dans la bouche et on l’utilise pour faire coulisser une sonde d’intubation de la bouche vers le larynx.
• La Cricothyroïdotomie.
La cricothyroïdotomie constitue l’abord trachéal en urgence de sauvetage. C’est une technique chirurgicale que peuvent utiliser les médecins urgentistes. Elle se distingue de la trachéotomie par le site d’abord, il s’agit d’inciser la membrane cricothyroïdienne et non un anneau trachéal. La lumière trachéale est directement au contact de la face postérieure de ce ligament. Le repère anatomique est facile à déterminer, il s’agit de la première dépression sous la pomme d’Adam. Il existe deux techniques, la technique chirurgicale proprement dite
L’intubation rétrograde.
et la technique d’insertion sur guide d’une sonde sans ballonnet après ponction de la membrane (technique de Seldinger).
Cette voie d’abord est davantage diffusée dans les pays anglo-saxons qu’en France comme alternative à l’intubation en cas d’échec ou de difficulté. Cette approche ne doit s’envisager qu’en cas d’absolue nécessité avec menace vitale immédiate pour le patient.
• La trachéotomie.
La trachéotomie consiste en une ouverture faite dans la trachée. Elle est obtenue par une incision verticale et médiane au niveau des premiers anneaux.
Seule l’impossibilité totale de l’accès à la glotte et donc l’impossibilité absolue de l’intubation, dans un contexte de mort imminente, peut légitimer la décision de prendre le risque de pratiquer une trachéotomie dans les conditions précaires rencontrées en préhospitalier. Ce cas de figure est exceptionnel. Quand la décision est prise et que l’action est entamée, quoiqu’il puisse arriver, elle doit être menée à son terme, c’est à dire à l’introduction d’une canule (ou à défaut d’une sonde d’intubation) dans la trachée.
• L’intubation fibroscopique.
La fibroscopie bronchique est actuellement la technique de référence pour une intubation
prévue difficile ou impossible. On place la sonde d’intubation armée sur le fibroscope, on
intube sous contrôle de la vue avec l’optique puis on fait coulisser la sonde pour l’introduire
dans la trachée. La voie nasale est techniquement plus facile mais plus traumatisante. Les
techniques d’anesthésie vigile facilitent son utilisation.
Justifiée par la nécessité du contrôle des voies aériennes ou d’une assistance ventilatoire, l’intubation est un geste technique fréquent et sûrement pas anodin.
Or l’intubation trachéale se pratique maintenant couramment ailleurs qu’en salle d’opération.
L’intubation en urgence préhospitaliére impose une méthodologie aussi rigoureuse qu’au bloc opératoire, même si ses conditions de réalisation présentent de nombreuses spécificités. En effet il est tout à fait illusoire de comparer une intubation difficile en milieu hospitalier avec une intubation difficile en urgences préhospitaliéres.
Nous nous proposons donc d’étudier maintenant plus spécifiquement les particularités des
intubations en SMUR.
C. INTUBATION DIFFICILE EN MILIEU PREHOSPITALIER.
L’intubation endotrachéale en situation d’urgence est un geste relativement fréquent en médecine préhospitalière. Deux études françaises trouvent une fréquence de mise en oeuvre de cette technique comprise entre 10 % et 26 % des patients pris en charge par les équipes médicales d’un service mobile d’urgence et de réanimation (SMUR) [4] [5].
Ce geste constitue le traitement de dernier recours pour une détresse respiratoire. Il sécurise les voies aériennes contre l’inhalation pulmonaire. De plus, la mise en place d’une sonde d’intubation facilite l’aspiration trachéale [6]. En outre, l’abord invasif trachéal permet d’établir une voie d’administration des drogues d’urgence en attendant la pose d’un abord veineux sûr [6] [7].
L’ensemble des bénéfices que procure une intubation doit être mis en balance avec les risques encourus par le patient. Il existe un certain nombre d’événements indésirables associés à la technique de l’intubation endotrachéale réalisée en urgence. Les conditions de réalisation de ce geste invasif peuvent être difficiles. Le temps nécessaire à l’évaluation des patients est nécessairement réduit, l’environnement préhospitalier peut être hostile ou imposer des contraintes, enfin la présence de personnels qualifiés ou de techniques spécifiques (fibroscopie) peuvent faire défaut.
Le taux de complications immédiates et différées est non négligeable lors d’une intubation en situation d’urgence. Parmi celles-ci, l’incidence des difficultés d’intubation semble être un élément déterminant.
La conférence d’experts de la Société française d’anesthésie et de réanimation (SFAR) sur
l’intubation difficile estime la fréquence de l’intubation difficile (ID) entre 10 % et 20 % en
milieu préhospitalier, nettement supérieure à l’incidence constatée au bloc opératoire [1].
1 2 3 4 5 6 7 8 9 10 IDS
1) Epidémiologie.
Il existe une variabilité de l’incidence de l’intubation difficile en fonction des définitions choisies et du type de population concernée. Si elle est définie comme une intubation réalisée après au moins trois tentatives, elle est retrouvée dans plusieurs études françaises avec une fréquence comprise entre 10 % et 20 % sans sélection préalable de patients [1,4,5,8] . Un travail portant sur des patients en coma toxique et intubés à la phase préhospitalière a mis en évidence une fréquence de 30 % largement supérieure aux autres études [11] . Ce résultat suggère le rôle de la pathologie comme déterminant de l’intubation difficile. En France, pays qui se caractérise par un système préhospitalier médicalisé, on peut globalement estimer que la fréquence de l’échec d’une intubation difficile en milieu préhospitalier est de l’ordre de 0,5 %.
Une étude en groupes parallèles a comparé l’ensemble des degrés de difficulté entre le milieu préhospitalier et la pratique au bloc opératoire. Le spectre des difficultés apparaissait significativement plus important en milieu préhospitalier par rapport à la pratique intrahospitalière.
Comparaison de l’intubation difficile mesurée par l’IDS (intubation difficulty scale) entre la pratique au bloc opératoire et le milieu préhospitalier[12]. Une valeur de l’IDS = 0 représente une intubation sans aucune difficulté et sa valeur augmente parallèlement avec le degré de difficulté.
Comparaison de l'intubation difficile entre le bloc opératoire et le milieu préhospitalier
46
28,2
15,5 16,4
10,5 13,5
9,5 10,9
3,2 7,4
1,9 7,4
0,9 4,5
2,2 3,8
0,3 1,3 0,9 0,9
0 5 10 15 20 25 30 35 40 45 50
Pourcentage d'intubation
Ainsi, l’intubation réalisée en situation préhospitalière médicalisée est associée à une plus grande difficulté et à une incidence d’échecs plus élevée que la pratique intrahospitalière.
Bloc opératoire
Milieu préhospitalier
2) Morbidité.
Le lien entre morbidité et intubation difficile, quoique logique, n’est pas clairement établi en anesthésie réglée. Cependant, la morbidité liée à des accidents lors de l’intubation reste la première cause de plaintes des patients victimes d’accidents d’anesthésie [12,13] .
La situation d’urgence génère deux difficultés supplémentaires :
• l’évaluation des facteurs anatomiques d’intubation difficile (classes de Mallampati, distance thyro-mentonière, ouverture de bouche) est difficilement réalisable dans ce contexte ;
• la procédure doit être rapide chez un patient présentant une détresse.
L’augmentation du temps de réalisation d’une intubation doit être considérée comme un élément morbide (risque de désaturation chez des patients avec une réserve d’oxygène limitée, hypercapnie du traumatisé crânien, risque d’inhalation majoré par la lenteur de la procédure, etc.).
Le caractère urgent à d’ailleurs été évoqué comme une des causes de la difficulté supplémentaire rencontrée lors de l’intubation au bloc opératoire en milieu obstétrical [13] . L’incidence des complications d’une intubation réalisée en urgence varie entre 9 % et 56 %, pourcentage largement supérieur à ce que l’on peut observer au bloc opératoire. Les complications les plus fréquentes sont l’intubation oesophagienne et l’inhalation pulmonaire.
D’autres types de complications sont néanmoins rapportés : désaturation en oxygène ; baisse de pression artérielle. Krisanda et al. ont constaté que l’incidence des complications dépend significativement de la difficulté de celle-ci. En effet, ce taux est de 18 % pour les patients ayant eu un échec d’intubation tandis qu’il n’est que de 7 % pour les patients intubés avec succès [12] . Schwartz et al., dans une étude sur l’intubation en situation urgente, ont trouvé que 40 % des intubations oesophagiennes étaient associées à une difficulté [15]. L’intubation préhospitalière se caractérise donc par un fort taux de complications généré par une incidence de difficultés importantes.
Alors qu’en anesthésie réglée, il existe des facteurs prédictifs d’intubation difficile
spécifiques, l’urgence préhospitalière empêche le plus souvent l’évaluation de ces facteurs. Le
taux élevé de difficultés suppose la présence d’autres facteurs spécifiquement rattachés aux
conditions de l’urgence préhospitalière.
3) Facteurs associés.
Terrains anesthésiques du patient.
L’urgence confère au patient certaine caractéristique, notamment, le plus souvent la méconnaissance des antécédents : interrogatoire impossible ou interprétation difficile.
Dans le cas où le ou les terrains anesthésiques sont identifiés, ils peuvent également être des facteurs associés à l’intubation difficile en milieu préhospitalier.
On retrouve : L’obésité (obstruction pharyngée, cou court et épais, diminution de la mobilité cervicale, diminution de l’ouverture de bouche)
Grossesse au troisième trimestre (prise de poids, muqueuse fragilisée par l’engorgement capillaire)
Diabète (anomalie du collagène entraînant une diminution de la mobilité du rachis)
Affections cervico-faciales (radiothérapie, infiltration tissu sous-cutané, mobilité linguale).
L’estomac plein n’est pas un terrain à risque d’intubation difficile mais plutôt une contrainte pour l’intubation (Sellick, crush induction…)
Pathologie du patient.
Les pathologies associées à l’intubation difficile en milieu prèhospitalier sont :
Les polytraumatismes : les raisons des difficultées de l’intubation sont le plus souvent l’agitation, la présence d’un réflexe nauséeux, le traumatisme du rachis.
Le traumatisme crânien, le traumatisme du rachis : la contrainte du respect de l’alignement tête-cou-tronc lors de la phase d’intubation, ne permet pas de positionner la tête du patient dans la position amendée de Jackson entraînent des laryngoscopies difficiles. Wood et al.ont étudié le rapport entre plusieurs manœuvres d’immobilisation du rachis cervical et la difficulté de laryngoscopie. Lorsque le rachis était immobilisé par un collier cervical, la laryngoscopie était mauvaise (cordes vocales non vues) dans 64 % des cas ; lorsqu’il y avait une stabilisation manuelle du rachis, l’exposition difficile avait une incidence de 22 % [16].
Le traumatisme facial, hémoptysie, saignement ORL : peuvent provoquer de diverses
manières des difficultés à l’intubation : distorsion de l’axe laryngotrachéal, présence de sang,
de corps étrangers, immobilisation de la tête, modifications anatomiques générées par le
traumatisme maxillo-facial, limitation mécanique de l’ouverture buccale en cas de fracture, glossoptose, luxation dentaire.
Les anomalies morphologiques qui empêchent l’alignement des 3 axes physiologiques (bucco-pharyngo-laryngé) nécessaire à l’exposition de la glotte lors de la laryngoscopie : anomalie de l’articulé mandibulaire, pro ou rétrognathie des maxillaires, macro-glossie.
Les brûlés, pendus, strangulés, épiglottite, lésions cricothyroïdienne : toutes ces pathologies sont à risques d’intubation difficile majorée du fait d’un œdème laryngé.
L’inhalation, l’obstruction des voies aériennes par un corps étranger.
L’arrêt cardiorespiratoire ne semble pas être une pathologie majorant le risque d’intubation difficile. Mais au contraire, plusieurs études ont prouvées que le geste est facilité [17].
Nature de la sédation.
Le rôle de la sédation a été mis en évidence - indirectement - par une enquête prospective sur l’intubation préhospitalière de patients en coma toxique.
Dans ce travail, les auteurs retrouvèrent une corrélation significative entre l’état de conscience mesuré par la valeur du score de Glasgow (GCS) et la difficulté de l’intubation (trois tentatives). Il existait une difficulté supplémentaire pour les valeurs de GCS comprises entre 7 et 9 (figure 3 page suivante) [10]. Cette difficulté était attribuée à une sédation inadéquate.
Les patients avec un GCS supérieur à 9 bénéficiaient d’une anesthésie générale procurant de
bonnes conditions d’intubation alors que les patients intermédiaires (7<GCS<9) avaient le
plus souvent une sédation à base de benzodiazépines seules qui se révélait insuffisante pour
obtenir de bonnes conditions d’intubation.
Corrélation entre l’intubation difficile et le score de Glasgow parmi 394 patients intubés pour une intoxication en phase préhospitalière. D’après [10] (Adnet F, Borron SW, Finot MA, Lapandry C, Baud FJ. Intubation difficulty in poisoned patients: association with the initial Glasgow Coma Scale score. Acad Emerg Med 1998 ; 5 123-7).
Plusieurs études ont évalué l’apport d’une sédation comprenant une curarisation de courte durée associée à un hypnotique d’action rapide, crash induction, ou induction en séquence rapide (ISR), dans la facilité de l’intubation.
Une sédation de type ISR peut être considérée comme étant fortement associée à la facilité de l’intubation trachéale en urgence. Ce type de sédation est considéré comme le gold standard dans les pays anglo-saxons aussi bien en milieu préhospitalier que dans les services d’urgence ou de réanimation. En France, un protocole de ce type a été proposé en utilisant l’association étomidate (0,3 mg/kg) associé au suxaméthonium (1 mg/kg). Ce type de séquence est préconisé lors d’une conférence de consensus nationale sur l’abord trachéale en urgence [6].
14,315,8 20
12,9 34,6
39,4 33,3
11,8
0 25
0 14,3
0 0
5 10 15 20 25 30 35 40
Pourcentage d'intubation difficile
1
Score de glasgow
Corrélation entre l'intubation difficile et le score de Glasgow en préhospitalier.
3 4 5 6 7 8 9 10 11 12 13 14 15