"Jlr
i:1,.1 r1i-+Jl
ry''Ji
llf
de
Ia
r6gion
de
Taher,
Jijel.
Soutenu
Le
0610712019devant
lejury:
M'Boudjerda
A.
M-"N4OHDEB
R.
M*:BOUNAR
H.
M'SEBTI
M.
a-'i,?,ta'
'''-r
1rY;,
.,al.l
ttJ')
,"{
tJ4fri\ffiit6
Mohammed
Seddik Ben
Yahia
-
Jijel
Facult6
des Sciences
Exactes
et
Informatique
D6partement
de
Chimie
M6moire
Pr6sent6
pour obtenir le dipl6me
deMaster
en
Chimie
Option
Chimie pharmaceutique
R6alis6
par
Kehili
Zineb
&
Zadi Yasmina
Thdme du
m6moire:
Effets antibact6rien
et
antifo
des
huiles
essentielles
d'Inula
wscosa
aPr6sident
Encadrant
Examinatrice
Invit6
Professeur
MCB
MCB
MCB
*ffiXi
4/aa;se1't
1j:10
--"*o'l,fj
fr:*-
";
RE,I
ERCIE,I
ENT
Avont
tout
nous remercions Dieu <<ALLAH>Ietout
puissont de nous ovoir occordd, lof
orce,le
courageet
fo potience pourterminer ce trovqif .Je
tiens dremercier toutes
les personnes qui ont porticip€, deprls
ou de loin d lordolisotion de ce mdmoire, en espdront n'ovoir oublid personne;
Tout d'obord, ce
trovcil
nesereit
pos aussi rieheet
n'qurcit pos pu ovoir lejour
sonsl'oide prdcieuse de
filme IIOHDEB
Rimo,Moitre de
Confdrences, nous lo remercions pour lo guolitd de son encadrement exceptionnel, pour so potience, so rigueuret
sodisponibilitd duront
notre
prdporotion de ce mdmoire.A
iime
BOUNARH.,l4aitre
de Confdrencesdqui
nous exprimonstoute notre
grofitude
pour ovoir rdpondu fovoroblement dnotre
invitotion def
oireportie
dujury,
de soutenonce en guolitd, d'examinotrice.
A
ltlr
BOUDJERDAA.,
Professeur dEnsergnenenfSupdrieur,dqui
nous exprimonslgolement
toute
notre
grotitude
pourovoir
occept6, d'|valuer ce mdmoireat
d'enprdsider la
jury
de soutenonce.A
lrlr
SEBTI
li.,
tl4aifre de Confdrences d gui nous exprimonstoute notre
grotitude
pourcvoir
acceptdnotre
invitotion. Merci, Monsieur, pour tous vos consails, rdponseset
documentotiontrds
utiles.Une
portie
del'extroction
des HE a 6ard rdalisde ousein
du Loborotoire de lofocultd
des Sciences de lo Vie
et
de lo Noture. Nous remercions la responsableprincipald{tme
BOUHAIJ
5.
pour so gdndrositdet
tous lesoutres
ingdnieurs des laboratoirespddogogiques.
Notre
pfus grond merci s'odressed
Monsieur BOUKROUCHEO.,
Direcfeur
et
Propridfaire
du Ldboratoire des Analysesl4ddicales,
oi
lo plus importonteportie
de cetrqvoif
a6td
rdalis6e:l'$s1.^ent,
lq purif icofionet
laculture
des souches clinigues desge?m?-s utilisds, l'ontibiogromme
et
l'oromotogromme.Merci Monsieur,
pounvotre
modestie, gdndrositi,, pour vos conseils
et
surtout
pourvotre
potienceinditerminde
pour ton accueil ou sein duLoborotoire
en nousmettont
donsd'excellentes conditions de
trovoil.
Sons oublier
li"ll"Bourooui F.C.,
ingdnieur d lo conservation desfordts,
Nous vousremercions €normdment pour l'aide gue vous nous ovez opportde,
surtout
pour le choixdes espi,ces v 6gdt ales.
Enfin
ontient
d remerciertoutes
les personnesguiont
porticipd de prds ou de loin dD64teaoe
J'ai
l'honneur
de
dedie
ce
modeste
travail
d
mes chers
parents
Moarad
et
Zolikha
A
mes chdres
s&urs
Wafa,
Soumia,
Selma
et
ma
nidce Nada
A
mes
chers
frdres
Oussama
et
Mohamed Islem
A mon fiancd
Mohamed, qui
a
su de
loin m'encourAger
et me
soutenir.
A
toute
ma
famille,
mes
ancles, tantes,
cousins et cousines,
petit
et
grand,
sans exception.
A
ma
chdre
binime
Yasmina
avec
qui
j'ai
partage
se
modeste
travail
A
toutes
mes
copines
A
tous
mes
colldgues,
A
toute
Ia
promotion Master
II
chimie
pharmaceutique
2019.
A
tous
ceux
qui
me
sont
chdrcs
A
tous ceux
qui
m'aiment
A
tous ceux
que
j'aime.
Ie
d6die
ce
travail.
tu€dGc&ne
J'ai
L'honneur de
dddier
cemodeste
travail
d
:L'homme
dema
vie,
mon
exemple 6ternel,
mon
soutien
moral
etsource
dejoie
etde
bonheur, celui
qui
s'est toujours
sacrffid
pour
me
voir rdussir,
que
dieu
tegarde dans
son vasteparadis, d
toi
papa.
A Ia lumidre de
mesjours,la
source
de
mesefforts,
Ia
flamme
demon
c@Lr,
ma
vie
etmon
bonheur
;
meman
quej'adore.
Aux
personnes
dontj'ai
bien aimd
Iaprdsence dans
cejour,
d toutes
messeurs Souhila, AmeI,
tairouz
et dma
nidce
Ryam,
je
dddie
cetravail
dont
le
grand
plaisir
leurs
revient
enpremier lieu
pour
leurs conseils, aides,
et
encouragements.
A toutes
mes cousines:
Lynda,
SoniaoLoumia
et toute
la famille Zadi.
A
mon
bindme
Zineb
et toute
Ia
famille kehili.
Auxpersonnes qui m'ont toujours aidd
et
encourag{, qui 1taient toujours
dmes
c6tds,
etqui m'ont
accompagn1
durant
mon chemin
d'6tudes,
mesaimables
amies,
collDgues
d'itude,
etseurs
deceur
:Lamia, Aida,
Lylia,
Meriem,Imen,
-Nesserin,
Rofaida,
Achwak et
Wassila,
A
tous
lesmembres
de mapromotion Master
II
Chimie Pharmaceutique
2019.
A
tous
mesenseignants depuis
mespremi,ires
anndesd'dtudes.
Atous ceuxquime
sontchers
etquej'ai
omis
deciter.
Glossaire
Antibact6rien
I Oui s'oppose au d6veloppement des bact6ries.Antibiotique
: Qui s'oppose au d6veloppement de certains micro-organismes, ou les d6truit.Antifongique:
Sedit
d'un
m6dicamentqui agit
contreles
infections provoqu6par
leschampignons ou les levures parasites.
Anti-infectieuse: une substance permettant de lutter contre
f
infection.Antiseptique:
sont des substances ayant pour d6truire les germes pathogdnes.Antiparasitaire:
on dit parasiticide un produit chimique capable de d6truire les parasites.Anti
virale:
une mol6cule destin6e d agir contre la multiplication d'un virus.Anti-inflammatoire:
qui fait d6gonfler et diminuerI'irritation.
Anti
spasmodique : un produit permettant de lutter contre les spasmes musculaires. Alcaloiide : mol6cule cyclique comportant un atome d'azote ce qui la rend basique.Aromath6rapie
:
l'utilisation
deshuiles
essentielles obtenues grOced
divers
proc6d6sd'exhaction.
Ast6rac6es : Famille de plantes dicotylddones faisant partre de I'ordre des Ast6rales.
Bronchites : Inflammation des bronches.
Coumarine : mol6cule aromatique h6t6rocyclique oxyg6n6e de formule 1-benzopyran-2-one,
isomdre
de
la
cbromons.C'est
le
squelettede
basedes
mol6culesde
la
farnille
descoumarines.
Flavonoides
:
mol6cules appartenant dla
famille
des polyph6nols (constitu6s de plusieursgroupes ph6nols).
Infusion
: action de faire mac6rer une plante aromatique dans un liquide bouillon.Liste
des
abr6viations
Liste
des
abr6viations
o/o : pourcentage.
AFNOR
: Association Frangaise de Normalisation.ATB
: Antibiotique.ATBs
: Antibiotiques.C : Concentration.
CPG : Chromatographie en Phase Gazeuse.
CPG-MS:
Chromatographieen
Phase
Gazeuse
coupl6e
d la
Spectromdtrie
deMasse.
Fig. : figure.
g:
gramme.Ho/o : T aux d'humidit6 exprim6 en pourcentage.
HE
: Huile essentielle.HEs : Huiles Essentielles.
I.
Viscosa: Inula viscosa.M:
molaire.MH
: Muller HintonMin
: minute.mI
:millilitre.
mm
:millimdte.
lVfs: Matidre v6g6tale sdche
R(%)
: Rendement (7o).Rm
: Rendement en huiles essentielles.pm:
micromdfre.Liste
des
figares
Liste
des
Figures
tr'igure 1. Fleur(A), Fruit(B) et feuilles (C)
d'Iunla
Viscosa
...
.03Figure 2. Etapes de l'obtention
d'une HE
...
... 07Figure 3. Sites d'action d'HEs
sur
lesbactdries
... 08Figure 4. Mode d'action des HEs sur les champignons
....
...09
Figure 5. Situation g6ographique du site de collecte
d'Inula
viscosa
.....
.
10Figure 6. Sdchage (A) et conservation (B) de
1'6chanti11on...
....
11Figure 7. Etapes de preparation de I'infus6 (A: pesde; B: m6lange eau chaude/poudre; C: filtration de m6lange;
D:filtrat
obtenu).
...L2
Figure 8. Principe de l'extraction des HEs par hydrodistillation...
...14
Figure
9.
Clevenger / ballon utilis6s pourI'hydrodistillation
...
14Figure 10. Principe de fonctionnement de la
CPG.
...
16Figure 11. Etapes de r6alisation
d'aromatograflrme.
18 Figure 12. Taux d'humidit6 des feuillesd'Inula
viscosa.
19 Figure 13. Chromatogramme deI'HE d'Inula
viscosa.
25 Figure 14. Composition chimiques de I'huile essentille deI'Inulaviscasa.
...26
Figure 15. Antibiogramme sur les souches cliniques
isol6es.
...
28Figure 16. Effet de
I'HE
surE
coli (A),K.
terrigena (B),P.
mirabilis (C.),S. Aureus(D)
et C.Nbicans(E)....
...28
Liste
des
tableaux
Liste
des
Tableaux
Tableau l.Caractdristiques du milieu de
r6colte...
...
..10Tableau2,Testsphyto-chimiquer6alis6ssurl'infusld'Inulaviscosa....
...
13Tableau 3. Caract6ristiques des souches utilis6s et des patients porteurs correspondants.... 17
Tableau 4. Principaux groupes chimiques composant les feuilles
d'Inula
viscosa11+++):
trds abondant; (+): pr6sent;O:
absent)
... .20Tableau 5. Composition chimique de
l'huile
essentielled'Inula
viscosa...
...24Tableau 6. Diamdtre et pourcentage d'inhibition de la croissance, des souches test6es, par
Sommaire
Sommaire
REMNRCIEMENT
GLOSSAIRE
ABREVIA,TIONS
LISTE
DES FIGURESLISTE
DESTABLEAUX
Sommaire
Introduction
I.
G6n6ra1it6...
3I.l.Caract6ristiques
d'Inula
viscosa...
3I.1.1.Nomenc1ature.
3I.l.2.Description botanique. . ..
...
3I.1.3.Syst6matique..
4I.1.4. Rdpartition gdographique et
6cologie
4I.1.5.
L'utilisationtraditionnelle...
4I. 1 .6. Activit6s biologi ques d' Inula
viscosa.
4I.1.7. Composition chimique
d'Inula
viscosa...
5I.2. Le.s huile.s
essentielles
5l.2.l.Localisation
dans laplante.
51.2.2. Composition
chimique...
5I.2.3. Propri6t6s
physico-chimiques
6I.2.4. Rdle des
FIEs...
6I.2.5.Conservation des huiles
essentielles
6I.2.6.Methodes d'extraction des
F{Es..
6Sommaire
I.3.
l.Activit6
antibact6rienne....I.3. 1 .1 .D6finition de la bact6rie. . . . .
1.3.1.2. Types de bact6ries
L3.1.3.Mode d'action des huiles essentielles sur les bact6ries
I.3.2.Activit6 antifongique ..
lI.
Mat6riel
et M6thodes...
II.l.
Echantillonnage.II.2.
D6termination du tauxd'humidit6
...
II.3.
Etude phyto-chimique (screening phytochimique).II.3.1. Prdparation de I'infusd
II.3.2. Screening chimique. . .
II.4. Extraction
del'huile
essentielle.II.5.
Analyse des huiles essentiellespar
chromatographie en phase gazeuse1 8 8 9 10 10 11 11
t2
t2
t4
15couplde
i
la spectrom6trie de masse CPG-MS..[.5.1-Principe de la
m6thode.
15tr.6.
Activit6
antibact6rienne etantifongique...
17tr.6.1. Choix des
espdces
1711.6.2. Technique
d'aromatogramme..
t7
Il.6.3.Principe...
17III.
Rdsultats etdiscussion...
19III.1.
Tauxd'humidit6
t9
III.2.
Screeningphyto-chimique.
..
19III.3.
Les huilesessentielles
23III.3.1. Le
rendement....
23Ill.3.2.Caract6ristiques
organoleptiques.
23Sommuire
III.4.
Aromatogramme
...
2j
Conclusion...,.,...
...
30R6fdrences
bibliographique...
..
32Introduction
Introduction
Les plantes aromatiques et m6dicinales repr6sentent une source in6puisable de remddes
traditionnels
et
efficaces
grdce
aux
principes
actifs qu'elles
contiennent: alcaloides, flavonoides, h6t6rosides, Saponosides, quinones, vitamines et huiles essentielles.En effet, les huiles essentielles (HEs), principes actifs issus du m6tabolisme secondaire des
plantes m6dicinales, ont 6t6 utilis6es depuis I'antiquit6 et sont largement employ6es de nos
jours, pour
leurs propri6t6s biologiques (antimicrobienne, antioxydant, analgdsique,anti-inflammatoire, anti-canc6rigdne, antiparasitaire, insecticide, etc.) et leur application dans de
multiples
et
diverses industries; alimentaire, cosmdtique, parfumerieet
pharmacie (Sall6,199L;
Lafon,1988;
f,l
abed
etKambouche,2003;
Brut,
2004;Bakkali,2008).
Inula
viscosa est une plante m6dicinale de la famille des Asteraceae, largement utilis6e enm6decine haditionnelle du bassin m6ditenan6en (Reebo 2010). De nombreuses 6tudes ont mis en 6vidence la pr6sence de m6tabolites secondaires telles que les polyph6nols et les terpdnes
dou6s de plusieurs activit6s biologiques; antioxydant, antimicrobienne, anti-inflammatoires, antidiab6tiques, antihypertenssurs, etc. (Susplugas et a1.01980;
Barbetti
et al.r 1985;Lauro
et
Rolih,
1990; Al-Dissi et aL,2001; Cafarchia et a1.,20A2; Zeggwtgh et a1.,2406l Manezet
a[.r2007; Francoet
a1.,,2008; Bssaibis eta1.,2009;Remli
8.,2013.;
Seca et a1.,2014;Chahmi
et
a1.,2015).L'activit6
antibactdrienned'Inula
viscosa a b6n6fici6 de plusieurs 6tudes en M6diterran6e(Hatim
et
al., 2017). Particulidrement, enAlg6rie, elle
a
6td 6tudi6epar
Kheyar
(2009), Boumaza (2011), Boukemaya et Messaoudi (2016)o Chaou (2017), Benomari (2018).C'est dans ce contexte que s'inscrit le prdsent travail, dont le but principal est d'6tudier la phytochimie et
l'effet
antibactdrien et antifongique desIIEs
d'LViscosa de la r6gion de Jijel,sur de diff6rentes souches bact6rierures et fongiques.
Le
premiervolet
de ce travail
comporte une recherche bibliographique, abordant unedescription botanique de l'espdce
Inula
viscosa,
et quelque notions de base sur les huilesessentielles et les activit6s antibact6rienne et fongique.
Deuxidment, nous avons envisag6 la partie exp6rimentale qui se d6roule en quatre 6tapes; d
Introduction
technique d'aromatogramme et enfin I'analyse de 1'6chantil1on par chromatographie d phase gazeuse (CPG).
Lapartie cruciale de cette 6tude concernant les r6sultats et la discussion. Les r6sultats sont
pr6sent6s, interpr6t6s et discut6s.
Finalement, nous concluons ce document par une conclusion qui valorise et r6sume tout le travail.
tt
(,
G6ndralitds
I.
G6n6ralit6sI.l.Caract6ristiques
d'Inula
viscosaI.l.l.Nomenclature
Le nom
Inula
est trds ancien.L'inule
visqueuse estl'un
des rares repr6sentants du genreInula
(Ciccarelli,
2007)Inula:
viendrait
du
grec:
<[n6o>qui
signifie
(e
purge>.(Allusion
d
une
propri6t6 th6rapeutique de la plante). (Fauron et al.o 1983)Viscosa: veut dire visqueuse : Inule visqueuse.
(Fournier,
1947). Les appellations def
inule visqueuse diffdrent d'une r6gion d une autre:/
EnAngleterre: Rock Flea-bane.(Halimi
rl997 ; Wanget
al.r2004),,/
En France: Inule visqueuse, Aun6e visqueuse (Baba Aissao 2000).{
AaMaroc: Trehla. (Zeggwagh et a1.,2006).{
En Espagne: Jolivarda, joliverda, xolivarda, olivarda./
Noms Arabes: El tibek, El tayon, El rassen, El dabik.,/
En Alg6rie:
Megremen, Safsak,Mersit
et
Hfina.
Particulidrement,au
centre de1'A1g6rie, cette espdce est appell6e Afided,Niret, Tlirine (Baba Aissar 2000).
I. L.2.Description botanique
L'inule
visqueuse est une plante sauvage vivace d racine pivotante, d'assez grande taillefiusqu'il,
50 m de hauteur). Ses tiges sont assez ramifi6es et pourvuesd'un
feuillage dense.Les
feuilles
sont
allong6es, ins6r6es directement
sur
Ia
tige,
sans
p6tioles.Avec l'0ge,
elles deviennent ligneuses et fonc6esd la
base. Les fleurs sont regroup6es encapitules,
soit d
p6tales
soud6s,
formant
des
fubes
en
jaune
orang6.Toute
la
plante
est
couverte
de
poils
qui
libdrent
une
r6sine
odorif6ranteet collante (Lecomte,2015) (Fig. 1).
Figure
l.Fleur
(A), Fruit (B) et feuilles (C)d'Inula
viscosa.tr
G6ndralitds
I.l.3.Syst6matique
La classification botanique
d'Inula
viscosa L. est la suivante:Rigne:V6g6tal
Embranchement : Spermaphyte
Sous embranchement : Angiospermes
Classe: Dicotyl6dones
Sous classe: Ast6rides
Ordre
: Ast6ralesFamille
: Ast6rac6es, compos6esGenre z Inula
Espice : Inula viscosa L.
Guignard,
(2001).I.1.4.
R6partition
g6ographique et 6cologieDans
le
bassin m6diterran6en,le
genreInula
est largement distribu6 (Quezelet
santa, 1962). En Alg6rie, elle est largement r6pandue dans le Nord (Quezel etSanta,l962),
dans lesrocailles et autant sur les terrains argileux que sableux (Benayache
et
al.,l99l;
Anonyme,20L0; Ciccarellir2007). Elle pousse dans les champs sauvages et dans les alentours du bassin,
m6diterran6en
(Brullo
2000;Parolin
et
aI., 2013).Elle
se retrouve dans les collines, leszones humides et les bords des routes, et appr6cie les sols secs et calcaires @aytop, 1984;
Wenqiao
et
a1.2004).I.1.5.
L'utilisation
traditionnelle
En Algdrie, les feuilles sont utilis6es s6ch6es en tisanes et les huiles essentielles en sont
extraites
pour
le
traitementde
diverses maladiestelles que
la
bronchite,le
diabdte, lerhumatisme, les blessures et les maladies du systdme urinaire et digestif (Reebo 2010;
Ilaoui
et aI.,20ll;
Talib et
aL,20l2).I.1.6. Activit6s biologiques
d'L
viscosaL'inule
visqueuse est consid6r6e commela
reine des plantes m6dicinales (Secaet
aL,2014;
Chahmi
et a1.,2015).Elle
est utilis6e pour toaiter divers maux grdce d ses activitdsanti-inflammatoire
@arbetti
et
flL.,
1985;
Al-Dissi
et
aL,
2001; Manez
et
flLo2007),anttdiab6tique (Zeggwagh et a1.,2006), antipyr6tique et antiseptique
(Lauro
etRolih,
l990),antifonglque
(Cafarchia
et aL,
2002;Franco
et
aL,2008;
Bssaibiset
aI.,
2009),antimicrobienne (Adam et al.r1989, Bssaibiss et al.r 2009),
ft
l,t
G6ndralitds
anti-ulc6rog6nique
,
antioxydant (Remli, 2013), antivirale, anti tumoral , activit6 curative deblessures (Susplugas et al.o l9E0), activit6 hypolipidemiante (Zeggwagh et a1,02006) .
I.1.7. Composition chimique
dolnula
viscosaCette plante est compos6e
de
flavonoideset
polyphdnols.Elle
est trdsriche
en huiles essentielles,dont
la
concentrationvarie
selonles
diff6rentes parties(feuilles,
racines etfleurs).Ses composants majoritaires sont
le
camphre, I'eucalyptol etle thymol
(Benchohraet al.o 2011).
I.2. Les huiles essentielles
Les
huiles
essentiellessont
des substances huileuses,volatiles
et
odorantesqui
sontsecr6t6es
par
les plantes aromatiques que nous extrairons par divers proc6d6s(Iserin
et a[.2007).
Parmi les
I
500 000 espdces v6g6tales, 107o seulement sont dites <<aromatiques>>,c'est-d-dire
qu'elles
synth6tisentet
s6crdtentdes infimes
quantit6s
d'essences aromatiques@runeton, 1999; Degryse et al,r 2008).
I.2.1. Localisation dans la plante
Les huiles essentielles n'existent quasiment que chez les v6g6taux sup6rieurs (Lawrence, 1995). Elles peuvent 6tre stock6es dans tous les organes v6g6taux: fleurs, feuilles, 6corces,
rhizomes,
bois,
racines,fruits
et
graines.La
compositionde
l'HE
peut varier
selon salocalisation (Svoboda, 2003).
1.2.2. Camposition chimique
Les huiles essentielles sont des compos6s de groupes Terp6noides d'une part, et de groupe des compos6s aromatiques d6riv6s
du
ph6nylpropane beaucoup moins fr6quent de I'autre(Paris et
Hurabielle,
1981; Regnault-Rogeret
a[.r2002).Selon
Bachelot
et
al.,
(2000,
les HEs
contiennentun
gtand nombre
d'6l6ments biochimiques. Les plus fr6quemment rencontr6s sont les alcools, les c6tones, les ald6hydes terp6niques, les esters, les 6thers et les terpdnes.GdndralitEs
I.2.3. Propri6t6s physico-chimiques
D'une manidre g6n6rale, les propri6t6s et les caract6ristiques d'une HE sont: les differents
indices,
pouvoir
rotatoire, viscosit6, densit6,solubilit6
dansl'alcool,
point
d'6bullition
etcong6lation
(Kanko
et a1.,2003).Toutes les HEs sont liquides volatiles, odorantes et inflammables. Leur densit6 est le plus souvent infbrieure
d
i
saufl'HE
de cannelle, deGiroflier et de
Sassafras.Elles
sont peu solubles dans l'eau, solubles dans les alcools et dans la plupart des solvants organiques. Elles sont alt6rables et trds sensibles d I'oxydation(Boughendjiouna,
2015).I.2.4. Rdle des HEs
Le
r61e deshuiles
essentiellesn'a
paspu
€tre
clairement d6montr6.En effet,
nousconsid6rons
qu'il
s'agit de produits de ddchets du m6tabolisme @elaiche, L979).Toutefois certains auteurs pensent que la plante utilise son HE pour repousser les insectes,
ou au contraire pour les attirer et favoriser la pollinisation. D'autres, la considdrent cofilme
une
ressource 6nerg6tique,facilitant
certaines r6actions chimiques.D'autre part,
ellesconservent 1'humidit6 n6cessaire d la vie des plantes expos6es
i
des climats d6sertiques.I.2.S.Conservation des huiles essentielles
Les
huiles essentielles sont trdsvolatiles et
trds fragiles,pour
cela, ellesdoivent
Otreconsery6es dans des flacons propres secs en aluminium, en acier inoxydable
ou
en veffe teint6, femr6s d bouchon scell6 et stock6es dI'abri
de la lumidre et de la chaleur (A.F.N.O.R.,2000).
I.2.6.M6thodes
d'exfraction
desffi
sLa
quantit6 d'huile essentielle contenue dans les plantes est toujours faible, parfois trdsfaible,
voire infime.
Il
faut,
quelquefois, plusieurs tonnes de plantespour
obtenirun
litred'huile essentielle
@enjilali,
2004).Difftrentes
m6thodes sont mises en Guvre pourl'extraction
des essences v6g6tales. Engln5ral,
le
choix
dela
m6thode d'extraction d6pendra dela
naturedu
mat6riel v6g6tal dtraiter, de la nature des compos6s, le rendement en huile et la fragilit6 de certains constituants
des huiles aux temp6ratures 6lev6es (Khelfane et Yousfi, 1987). Les principales m6thodes d'extraction sont:
{
Hydrodistillation{
Entrainement d la vapeur d'eaur'
Hydrodiffusion,/
Extraction par du CO2 supercritiquet
u
I
\
GdnEralitEs
,/
Extraction assist6e par micro-onde,/
L'expression d froid'/
L'extraction par solvants volatilsCependant, I'hydrodistillation reste la technique la plus ancienne et la plus convenable
pour l'extraction
desHEs
(Benjilali,
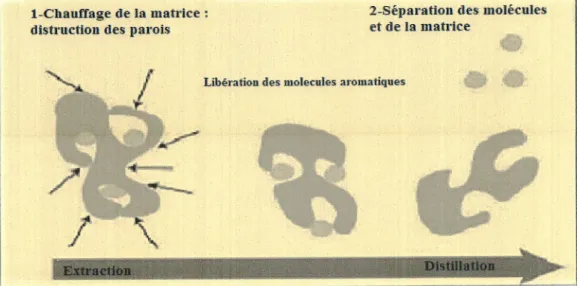
2004).Il
est n6cessaire dansun
premier temps d'extraire de la matidre v6g6tale des mol6cules aromatiques constituantI'huile
essentielle,puis dans un second temps de s6parer ces mol6cules du milieu par distillation
(tucchesi,
200s)
(Fig.2).
l-Chaufrhge de
lr
uatrice:
di$truction dt.s parois
2-$6paratioa des molGcsl€s
rt
de ta matriseLib€*elira des aolecoles arourtiques
&
Figure 2. Etapes d'obtention d'une HE (Lucchesi' 2005).
I.3.Activit6 antibactdrienne
et antifongiqueI.3.
l.Activit6
antibact6rienneI1 existe deux types d'activit6 antibact6rienne: une activit6 l6tale ou bact6ricide et une
inhibition de la croissance ou activit6 bact6riostatique. Le plus souvent, l'action des huiles
essentielles est assimil6e d un effet bact6riostatique.
Nonobstant, certains
de
leurs constituants chimiques semblent bact6ricides (Carson et Riley, 1995; Coxet
a1.r2000; Brut,2004 ).des propri6t6s
I3.1.1.D6finition
de la bact6rieUne
bactdrie
est
un
microbe
form6 d'une
seule cellule,
visible au
microscope, appartenant d une zone de transition entre le r6gne animal et le r6gne v6g6tal. Comme toute cellule, les bact6ries sont constifu6es d'un noyau, isol6 ou diffirs, un protoplasme contenantdes granulations et des vacuoles, une paroi parfois d'une capsule(Leclerc et aI.,1995 ).
avou
t
7
Gdndralit6s
I.3.1.2. Types de bact6ries
Selon leur mode de nutrition et leur comportement vis-d-vis de 1'oxyg6ne, les bact6ries sont class6es en a6robies et en ana6robies.
Cependant,
toutes
les
bact6ries
n'ont pas
la
m6me
paroi,
la
paroi
desbact6ries
d
Grampositif
contientun
trds grand nombre de saccules formant une paroi 6paisse, tandis quela paroi
des bact6riesd
Gram n6gatif contient deuxd trois
sacculesrecouvertes
d'une couche lipidique de structure proche de celle de la membrane cytoplasmique (Peber
,
200i; Baudry
et Brezellec, 2006).Ainsi ,
les bact6ries color6es enbleu'violet
seront dites d Gram positif et celles en rose d Gram n6gatif(Ileart
et Shears, 2006).I.3.1.3.Mode
d'action
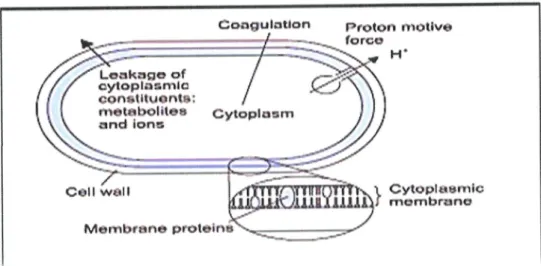
des huiles essentielles sur les bact6riesLss huiles essentielles possddent plusieurs modes d'action sur les diff6rentes souches de
bact6ries (FiS.3). Leur action antibact6rienne est due principalement d leur grande affinit6
aux lipides membranaires gr0ce d leur nature hydrophobe (Dormans et Deanso 2000).
Proton
motlvt
lotea
l.f'
Cytoplgrmle
mornbrrno
Figure 3. Sites d'action des HEs sur les bact6ries
(Burt,
2004).Lorkego of
oy{opLErml€ GOna$ruan|l:rnctabolltct
c,ytodaam
srlg lon!
J-l
-- vL,
GEn6ralitds
I.3.2.Activit6
antifongiqueL'action
antifongiquedes
huiles
essentiellesest due
d
une
augmentationde
la perm6abilit6 de la membrane plasmique suivie d'une rupture de celle-ci entrainant une fuite du contenu cytoplasmique et donc la mort de lalewre (Makhloufi,
2010).Les compos6s terp6niques des
HE
et plus pr6cis6ment leurs groupements fonctionnels ph6noliques et les ald6hydes modifient la permdabilit6 cellulaire fongique en interagissantavec les prot6ines de la membrane. Cela provoque la d6formation de la skucture cellulaire, et perturbe la fonctionnalit6 aboutissant alors d la perte des macromol6cules conduisant d
une inhibition de la croissance fongique
donc
la d6gradation de la membrane plasmatiquedes levures (Makhloufi,20101'
Pramila
et a1.,2012)(Fig'4)'
Altdration du contenu du cytopl Alt6ration de la paroi (T permeabilite) Alt6ration de I'enveloppe et du contenu de la vacuole Alt6ration de la membrane plasmique
(f
permeabilit6 membranaire) D6polarisation de la membrane mitochondrialeFigure 4. Mode d'action des HEs sur les champignons @ramila
et
a1.,2012)'D€pletion de la force proton motrice et du oool d'ATP
tl
--r
-\,
Matdriel
et
Mfithodes
II.
Mat6riel
et M6thodesII.1.
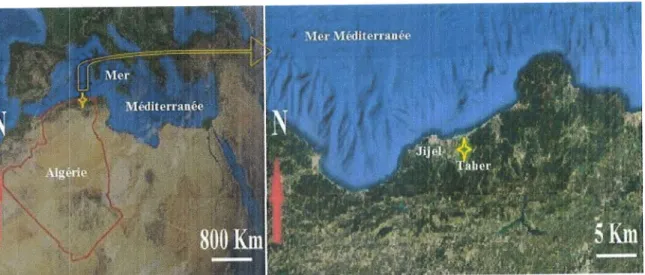
EchantillonnageAu total, 3509 de feuilles
d'Inula
viscosa ont 6t6 r6colt6s d'une manidre al6atoire durantles mois
d'avril
et mai 2019, d la r6gion de Taher, Jijel, en Est de 1'Alg6rie (Fig.s). Les caract6ristiques du lieu de r6colte sont mentionn6es dans le tableau 1.fi$rres.Sit*ation
g6ographique du site de collected'Inula
viscosa.(Google Maps ; modific ations petsonnelles)
Tableau
l.
Caractlistiques du milieu de recolte (Google Maps, 2014)R6gion
Taher
Wilaya Situation g6ographique Altitude Climat SuPerficie[,es coordonn6es g6ographiques en
DMS @egr6s, minutes, secondes)
Jijel
Est alg6rien (Nord-constantinois)
48m
Climat mdditerran6en a 6tb chaud 64,86]f|r(2
36" 46'19" Nord,
5o
53'54"
Est'/
S6ehageLe s6chage a 6t6 effectu6 d
l'air
libre, dl'abri
de la lumidre et de l'humiditd pendant quelquesjours, dans une pidce bien a6r6e (Fig. 6).Le but de cette 6tape est d'abaisser la teneur en eau, des feuilles r6colt6es, d
fin
d'6vitertoute r6action d'alt6ration et la proliferation des microorganismes.
t - t
L-t
Mathriel
et
Mfithodes
/
ConservationAfin
d,6viter tout type de contamination, les feuilles s6ch6es ont 6t6 ensuite conserv6esd
l'abri
de la lumidre, dans des flacons en velre, herm6tiquement ferm6s et couverts du papier opaque(Fig.6).
Figure6.S6chage(A)etconservation(B)de1'6chantillon.
(Photos Prises Par nous-mdmes).
II.2. D6termination
du tauxd'humidit6
Une quantit6 de 3509 de feuilles fraiches
d'L
viscosa a 6t6 pes6e avant et aprds s6chagei
I'air
libre pendant 15 jours. Le calcul de la teneur des feuilles en eau (taux d'humidit6 enpourcent) a 6t6 fait en se basant sur la formule suivante :
@ernardet'
1983)H,o=ry*
1oo;
otr:H"z: taux d'humiditd exprim6 en pourcentage M1: poids de 1'6chanti11on frais en grarnme
M2: poids de 1'6chantillon sec en gramme.
II.3.
Etude phyto-chimique (screening phytochimique)Cette 6tude a le but de d6terrniner les principes actifs contenus dans la partie foliaire
d,Inula
viscosa. pour identifierla
composition en m6tabolites secondaires pr6sents danscette plante,
un
screeningphyo-chimique
a
6t6 effectu6 surles
feuilles pr6alablementprepar6es. pr6cis6ment,
il
est recommand6 d'utiliser, soit la poudre du broyat des feuillesMatdriel
et
M6thodes
II.3.1. Pr6paration de
l'infus6
L'infus6
a
6tE prfiparf en utilisant la poudre foliaire, comme suit (Bellakhdar, 2003):-
Broyer 5 g de feuilles sdchesd'Inula
viscosa,i
l'aide d'un mixeur 6lectrique,-
Dans un b6cher, verser 100 ml d'eau distil16e chaude sur 5 g de poudre de feuilles pr6cddemment prePar6e,-
Laisser refroidir, puisfiltrer
en utilisant du papier filtre Whatman,-
Compl6ter le filtrat par I'eau distill6e, jusqu'd 100ml
(Fig. 7)Figure 7. Etapes de pr6paration de I'infus6 (A: pes6e; B:m6lange eau chaude/poudre;
C:filtration de m6lange;
D:filtrat
obtenu). (Photos effectudes par nous-mfimes)II.3.2. Screening chimique
La m6thode utilis6e dans cette 6tude est celle propos6e et confirm6e par (Trease et Evans, 1989;
Harborne,
1998).Le tableau resume et monhe les mol6cules recherch6es, leurs r6actifs de caract6risation
et les r6sultats attendus.
rt
t -t
Mathriel
et Mfithodes
Tableau 2. Tests phytochimiques r6alis6s sur
f
infus6d'L
vrscosa (Trease et Evans' 1989;Harborne,1998)
M"l6."t.a
iadmi.r
M6lange r6alis6 Rdsultat obtenus Glucosides Tanins totaux Tanins galliques Quinones libres Anthocyanes Mucilages Irridoides Coumarines Amidon Flavonoides Saponosides LeucocYanes Prot6ines ProanthocYanidolsZ g
p*Ot.
v6g6tale 1- quelques gouttes de Coloration rougebrique.
Coloration
bleunoir
intenseColoration
en bleu fonc6Coloration
rougeColoration
rouge Pr6cipit6 floconneux Coloration bleuVue
trouble
Coloration bleu violetteColoration
rouge oran96e Un pr6ciPit6 blanc Coloration rouge Coloration violetteColoration
rouge HzSO+5 mlinfus6 + quelques gouttes de FeClr
(d5%)
5m1infusd
+2
gacltate de sodium+ quelques gouttes de FeCl:'29 de poudre v6g6tale
+ zrf|.HCl
+ 20ml "f,lototo.rn". Aprds 3h,filtrer
le m6lange puis agiter avec 5ml d'ammoniaque' 5m1infus6 + quelques gouttes HCI'
lml
infus6 + 5m16thanol absolu.Agiter pendantl0min.
2ml de I'infus6
*
quelques gouttes deHCl'
Puis chauffe le m6lange
29 poudre v6g6tale + 20 ml alcool 6thylique' nouittlrpendant I 5mins puis fr1tr6'
5ml du
itlttut
*
5gouttes de KOH e 10% +quelques gouttes de
HCl
dL0%'29 poudre
*
quelques gouttes 12'5ml infus6 + 5m1HC1*
lmlalcool
iso-amylique + un coupon duMg
2ml de I'infus6 *quelquesgouttes d'acdtate de Plomb
2 g poudre + 20ml m61ange (Propanol+HCl
d
bhauffer
1 5mins dans un bain marie'1ml infus6
+
lml
NaOH {2M) +quelquesgouttes de sulfate du cuiwe'
iml
infus6+ZmlHCl.
Chauffer 5mins au bain MarieMathriel
et
M6thodes
II.4. Exfraction
deI'huile
essentielleL'extraction
des huiles
essentielles(HE)
s'effectue
par
plusieurs
m6thodes:Hydrodistillation, Exkaction
par
solvant, Hydrodiffusion,etc
(Belaiche,1979;
Chiej'
1982 ; Henrio 1993 ; Bruneton, 1999
;Benjilali'
2004).Cependant, I'hydrodistillation reste la plus convenable
(Benjilali'
2004).,/
L'hydrodistillation
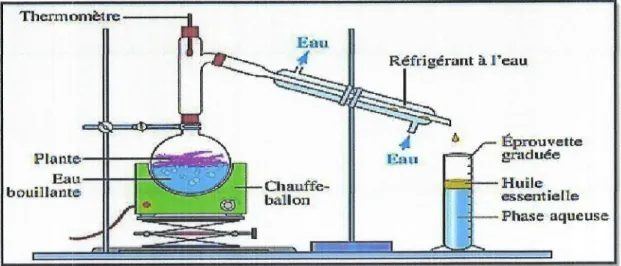
Le
principe de cette m6thode est simple: dansun
ballon,on
ported
1'6bullition unm6lange d'eau
et
dela
plante donton
souhaite extrairethuile
essentielle. Les cellules vdg6tales 6clatent et libdrent les mo16cu1es odorantes, lesquelles sont alors entrain6es par la vapeur d'eau cr66e @runeton, 1999)(Fig.8).
Thcr-:r.noptErte
R€frigfrant
illlsau
ftrrouu'ette grtdu€EI{uile
cssentielXE Fhnse:aqur:useFigure 8. Principe de I'extraction des FIEs par hydrodistillation (Lucchesi, 2005).
Figure 9. Clevenger / ballon utilis6s pour l'hydrodistillation (Photo prise par nous-m€mes)
Matdriel
et
Mdthodes
Les dtapes suivies sont:.
i0
g
de feuilles sdches a 6t6 introduit, d chaque fois, dans un ballon de2
litres,impr6gn6 d'eau distill6e
'
L'ensemble est port6i
1'6bullition pendant deux heures.
La
vapeur condens6e obtenue conduit d une phase organique (huile essentielle)qui est s6par6e de
l'hydrolatpar
diffbrence de densit6.
Aprds la r6cup6ration de I'huile, nous avons ajout6 du sulfate de sodium (Na2SO4) pour 6liminer les traces d'eau.
L'huile
essentielle a 6t6 plac6e par la suite dans un flacon en verre opaque, elle estconservde d temp6rature voisinant 6"C. Le flacon est ferm6 herm6tiquement pour le pr6server de
l'air,
de la lumidre et de la tempErature, dvitant ainsi son alt6ration par ces principaux agents de d6gradation (Fig. 9)../
Calcul du rendementLe rendement en
IIE
est le rapport entre le poids del'huile
extraite et le poids de la plante d traiter :Rnn
=
W.100;
oi:
RrD: rendement de I'extrait en pourcentage M1g: euantit6 d'essence obtenue exprimEe en g
Mr: quantit$ de matidre v6g6tale sdche utilis€e pour I'extraction, exprim6e en g.
II.5.
Analyse des huiles essentiellespar
chromatographie en phase gazeusecouplde
i
la spectrom6trie de masse CPG-MSII.5.1. Principe de
la
m6thodeLa
chromatogaphieen
phase gazeuseet
la
spechom6triede
masse possddent deslimites de sensibilitd voisines. L,eur association permet de disposer
d'un
outil
analyiquetrds performant.
Le couplage de la chromatographie en phase gazeuse d la spechomdtrie de masse
CPG-MS
est une technique d'analysequi
possdde plusieurs atouts:
le
chromatogramme en phase gazeuse permet de s6parer les constituants d'un m6lange. Le spectromdtre de masse associ6 permet d'obtenir le spectre de masse de chacun des constituants et bien souvent deles identifier.
a
_____________ ,t E
Matdriel
et
Mfithodes
Le
couplage CPG-MS en mode impact 6lectronique(SM-IE)
estla
techniquela
plus utilisde dans le domaine des HEs,i
savoirl'HE
d'L
viscosa dans notre cas.(Tranchant,
1996 ; Cavalli, 2002XFig.10).
D6bitmitre
Il€tecteur II
I
Gtz
vecteurL.!
f
I I l Earegistreuert ettraiteaalt des doas6s
Fonr
Figure 10. Principe de fonctionnement de la CPG
(Tranchantrl996).
{
Mode op6ratoireL'analyse
est
faite sur
un
appareil
Shimadzu CGMS-OP2010
qui
a
comme caract6ristique une colonne capillaire apolaire SE-30de 30 m de longueur et d'un diamdtreint6rieur de 0,25mm. Cette phase stationnaire possdde une 6paisseur de 0,25
pm
et
satemp6rature maximale est de 26A'C.
La
colonne est chauff6e de 55oC (maintenue pendant2
minutes) iL 250 oC avec une vitesse de 4oCl min.L'injecteur
et
le
d6tecteursont
respectivement programm6sd
250
et
260'C.
Les6chantillons de
I
pl sont inject6s en mode Split avec une fraction de I/20.La fragmentationest effectude par impact 6lectronique
i
70 eV'L'appareil est
reli6
dun
systdme informatique g6rant une bibliothdque de spectre demasse.
#ysteme d'iniectioa de I'echrstillon
€ffi
Mat6riel
et
M6thodes
II.
6.Activit6
antibact6rienne et antifongiqueLes activit6s antibact6rienne et antifongique de
l'HE
d'1. viscosa ont 6t6 d6termin6espar
la
m6thodede diffusion en
milieu
g6los6sur
des bact6rieset
champignons non r6sistants, pr61ev6s de diff6rentes personnes. Les caract6ristiques des germes utilis6s et despatients h6tes correspondants sont r6sum6es dans le tableau 3.
II.6.1.
Choix des esPCcesLes bact6ries choisies sont des bact6ries de forme differente
(Bacille ou
Cocci) et d gram 6galement different (Gr- et G-). Les caractdres < pathogdne D et < trds r6pandu >>, auxcas d'infections, sont les caract6ristiques communes de toutes les espdces bact6riennes et le champignon s6lectionn6s.
Tableau 3.Caructlnstiques des souches utilis6s et des patients porteurs correspondants (M:
m61e, F: femel4e, SPC: spermoculture, ECBU: itude cfiobactdriologique des utineso FCBP: 6tude
1I.6.2. Technique d' aromato gramme
C'est une technique de mesure
in
vitto
du pouvoir antibact6rien des HEs. Cet examenest 6quivalent d un antibiogramme
of
les disques d'antibiotiques sont remplac6s par desdisques des HEs, pr6alablement s6lectionn6es et reconnues.
(Girault
et Bourgeon' 197L)II.6.3.Principe
Cette m6thode consiste d
utiliser
des disques du papier impr6gn6sd'huile
essentielle,puis dispos6s d
la
surface d'une g6lose uniform6ment ensemencde avec une suspensionbact6rienne ou fongique. Aprds incubation de 18 h, les colonies se d6veloppent d la surface de la g6lose laissant des zones vierges autour des disques appel6es zones
d'inhibition'
On peut exprimer I'activit6 antimicrobienne en indiquant directement lazone d'inhibition"n*;,"_
d,
ffi
cytob actdriolo gique du Pus).
Espdce
Souche Patient porteur
Type Famille Gram Forme Sexe Age Provenance
Escherichia coli Bact6rie Enterobacteriaceae Bacille M 68 ans ECBU
Proteus mirabilis Bact6rie Enterobacteriaceae Bacille M 14 mois ECBU
Kebsiella terigena Bact6rie Enterobacteriaceae Bacille M 03 mois ECBU Staphylococcus
aufeus Bact6rie Micrococcaceae + Cocci M 33 ans
SPC
Candida albicans Champi-gnon Saccharomycetaceae F 36 ans FCBP
17
Mat$riel
et
M6thodes
millimdtre. La sensibilit6 des souches test6es est positivement proportionnelle au diamdtre
d'inhibition (Belaicheo
lg7giZaikt
ef aLo 1988)'/
Mode op6ratoireLes 6tapes suivies pour 1a r6alisation de I'aromatografirme sont r6sum6es dans
I'illustration suivante
(Fig.l
1).knpr6gner des disques steriles d'environ
lcm
de diamdtre dansI'HE
__jyry?
d{t1s_er au centre de la boite de P6hi ----1{-- -- -_ Etape 01:V6rifier la sensibilit6 des souchesRealiser un antibiogramme pour s'assurer de la sensibilit6 des souches choisies via quelques
AB:
AMX, CAA KF, GEN' AKo SXT' CT, CIP' FOS'Etape 02: Preparation de la suspension bact6rienne
1 colonie de bact6rie / champignon
+
10 ml eau physiologique sterile)Homog6n6isation Par Vortex
Etape 03:R6alisation de 1' aromatogramme
verser la suspension bact6rienne dans une boite de P6tri contenant
lemilieudeculture<<lvluellerHintoru>llaisserpendant2min
Incuber dans 1'6tuve d 3
Etape O4:Lecture des r6sultats
t
18
R6
sultats
et
cliscussion
III.
R6sultats et discussion
III.1.
Tauxd'humidit6
Le s6chage de 3509 de matidre v6g6tale foliaire fraiche, pour I'estimation du taux
d'humidit6, a donnd seulement 65n1g du poids sec, ce qui corrospond d un taux 6lev6
d'humidit6, de I'ordre de 81,47o (Frg.12).
Figure 12,Taux d'humidit6 des feuilles d'Inulaviscosa.
Le test d'humidit6 est r6alis6 dans le but d'estimer la teneur en eau de
la
plante 6tudi6e. Les analyses des feuilles d'.{. viscosa ont r6v616 un taux d'humidit6 important (8114 o/o), cequi
signifie
queplus
dela
moiti6
du poids des feuilles fraiches d7.Viscosa sont constifu6es par l'eau, le reste repr6sente la matidre sdche.
Selon
Paris
et Moyse (1965), les plantes fraiches renferment une teneur en eauallant de 600/o e
80%.
D'auhe part, la richesse en eau peut 6tre attribu6 au facteurvai6tal,
d
1'6poque
de
maturation
et
de
r6colte
et
aux
caract6ristiques p6doclimatiques.La valeur obtenue dans cette 6tude (8114 o/a) est trds proche d celles estim6es par
Remli (2013) d Oran (85
%)
et Benayache (1991) etAl-Dissi
(2001) d I'Est alg6rien.IU.2.
Screening phyto-chimiqueL'analyse phyto-chimique a permis d'identifier les diffdrents groupes chimiques
pr6sents dans I'extrait des feuilles de l'espdce
I.
viscosa (Tab.4).rr
--=
RE
sultats
et
discussion
Tableau4. Principaux groupes chimiques composant 1es feuilles d'1. viscosa ((+++):
trds abondant; (+): pr6sent; (-): absent).
Observation Prot6ines Infus6 Saponosides Irridoides Infus6 Mucilages Infus6 Coloration violette Pr6cipit6 blanc Coloration bleu Pr6cipit6 floconneux + -r
rr
t,
Rdsaltats
et
discussion
Coloration rouge
Tanins
galliques
Infus6Proanthocvanidols Flavonoides Infus6 Coumarines Bleu fonc6
+#
Coloration rouge + Rouge orang6e#
Vue troublerr
+21
1--
t
Rdsultats
et
discussion
Amidon
Leucocyanes Poudre
Glucosides Poudre
Quinones libres Poudre
Coloration bleu violette
Coloration rouge
Rouge brique
#
Coloration rouge
Les
feuillesd'inule
visqueuse sont trds richesen
flavonoides, tanins galliques,.inins
totaux et glucosides. Cependant, elles renferment des diff6rentes proportions de
coumarines, saponosides, mucilages et proanthocyanidols.
En
revanche, I'absence totale,a
6t6 marqu6e,d'amidon,
de
leucocyanes, desquinones libres, des prot6ines, des alcaloides, des irridoides et d'anthocyanes.
A
tire
comparatif avec des dtudes antdrieures, men6es surla
m€me espdce, lesresultats obtenus
sont en
accord avecceux
de Djedioui
(2010)
obtenusen
Est algdrien ori une pr€seace des flavsnoides, saponosides et tanins a 6t6 marqude, contre une absence d'alcaloides dans la partie foliaired'L
viscosa. Boumaza (2011) d Orana
aussi apergue une abondance importante des flavonoideset
saponosideset
uneabsence des quinones et leucocyanes.
Remli
(2013), d Oran, a marqu6 une existenceR6sultats
et discussion
importante en flavonoides et une pr6sence
faible
des certains m6tabolitestels
quecoumarines
les
tanins
dansla
partie
a6rienned'1.
viscosa.Nohe
r6sultata
6t66galement confirm6
par Cafarchia
et aI.,
(2002)en
ltalie, qui
ont
marqu6s une richesse des feuilles de l'espdce 6tudi6e en flavonoides, taninset
glucosides et un manque totai de l'amidon.Ces similarit6s en composition peuvent 6tre justifi6es par le climat identique des
zones de r6solte de I'espdee v6g6tale en question.
III.3.
Les huiles essentiellesIII.3.1.
Le rendementL'extraction
deshuiles
essentiellesde 350
g
des
feuilles
sdchesde
l'inule
visqueuse a dorur6 0r7 mI de
I'huile
essentielle, ce qui correspond d un rendement de0120 o/o.
L'extraction
deI'huile
essentielle dpartir
d'I.Viscosaa
aboutid un
rendement proche de celuiobtenu
par Boumaza (2011)i
oran,
qui
a indiqud un rendementcompris
entre 0124Vo
et
0,31
Vo
de
la
plante fraiche
et
sdche ordonn6ment.Benhammou (201a)
a
obtenuun
rendementde
0rlg o
,
chezla
m6me plante, r6colt6e et s6ch6e en moisd'avril
A Annaba. Des valeurs variant de 0,22 d 0,34oh ont 6t6 6galement enregistr6es chezla
plante poussant d diff6rents endroits en Alg6rie(Kheyar et al,r2014;
Madani
et
al.o20l4).Les variations l6gdres marqu6es dans les valeurs
du
rendement enHE
chez lam€me espdce, peuvent 6tre justifi6es par la nature de l'6cosystdme d'ori provierurent
les
dchantillons:plus
l'6cosystdme estferm6 (forot
densepar
exemple),plus
lacomp6tition en 6l6ment
nutritif
et en lumidre est importante et donc plus la s6cr6tiondes IIEs est consid6rable.
trI.3.2
.Caract6ristiques organoleptiquesL'huile
extraitea
de diff6rentes caract6ristiques organoleptiques.Il
s'agit
d'une huile trds dense, d aspect limpide, de couleur jaundtre et ayant une odeur attirante etd6sagrdable.
Les paramdtres organoleptiques remarqu6s sont identiques dL ceux r6pertori6s dans
les normes (AFNOR, 2000).
R6sultats
et discussion
III.3.3.
Composition chimiqueLe
temps de rdferrtiorr,la
coue.enjration traduite parla
surfape dupic
st le
nom chimique de chaque compos6, obtenus par laCPG, sont rassembl6s dans le tableau 5.Tableau 5. Composition chimique de
I'HE
d,Inula viscosa.Pic Temps de r6tention (min) Concentration (%') Compos6s I 3,410 0,84 acide 2-m6thylpropanoique (Acide iso-butyrique)
2 6,493 7,79 l -m6thy1-2- (1 -m6thy16thyle)- Benzdne
a J 6,956 0,70 1,4-cyclohexadidne, 1 -m6thy1-4- (1m6thyl6thyle) -4 23,296
tt.72
Carvacrol 5 36,750 1,22 (Z) a--bergamotEnol 6 37,526 0,72 1, 3,6-Heptatriene, 2, 5,5-tnmethyl-7 40,386 8,20 Ph6nol, 4,4'
-(I
-methylethylidene) bis[2,6-
dimethvl-8 40,396 3,26 Acide hexadOcano'ique, ester mdthylique
9 41,92r 2,00 2,7 -dim9thyloct-7-en-5 -yn-4-yl isobutyl
ester de l'acide phtalique
10 42,628 2,21 2, 8,8-t6tram6thyl, m6thyl 2H,&H-Benzo [1,2-b: acide
5-
mfithoxy-2,ester de I'acide 5-dipoxy-10 propanoique
l1 44,588 20.r7 Acide 8-Octad6c6noique, ester de m6thyl (E)
I2
44,666 26.349,12-
acide octad6cadienoique (2,Z)-,
esterm6thylique
13 44,906 3,08 Acide hetptad6canoique, 16-m6thy1- ester
de m6thvl
t4
44,969 5,65 Acide 9, 12,5-Octaddcatri6noique, ester6thylique,
(Z,Z,Z)-15 45,272 0,61 Acide
I
-adarnantanecarboxylique, ester de2-trid6cvle
l6
48,421771
Acide eicosanoique,ester m6thylique
I7
51,103 '71)
2H- Cyclohepta [b]furann e-2-one, 3,3 a, 4, 7, 8, 8a- hexahydro-7-m6thyl -3-m6thylene-6-(3-oxobutyl)-, [3aR-(3a .alpha, 7 .be
t
24
R6sultats
et discussion
la CA .F ril lT1-
c) o d -l-{ bo rl (Y) €) L bo 25R6sultats
et discussion
L'analyse chromatographique de
I'HE
d'LViscosa
a permisd'identifier
dix-septcomposds differents, qui ont donn6, aprds identification, des pics de chromatogranrme correspondant d des indices de r6tentions allant de 3,410 d 51,103
min
(Fig.13).D'aprds les r6sultats obtenus, nous constatons que la plante
I.
viscosa de la r6gion de Taher (Jtjel) est caract6ris6e par une forte teneur en monoterpdnes oxyg6n6s dans son huile essentielle. Les compos6s majoritaires sont respectivement (Fig.13etl4):
{
9,72-
acideocta 6cadienoique(Z,Z)-,ester
m6thylique (2G,34%)/
Acide 8-Octad6c6noique, ester de m6thyl (E) (20,17%){
Carvacrol(It,72%).
{4
autres
compos6s
42alo
Figure 14. Composition chimiques de
l'huile
essentilledel'Inula
viscosa.Les compos6s identifi6s sont diffdrents de ceux d6crits par
Kheyar
(2009), quirapporte
la
compositionl'HE
d'I.Viscosa commesuit:
le
thymol
(6,93%)I'iso-Dihydrocarveol (5,04%) et le carvac rol (2,27 Yo).
Berhail Q0l4)
a marqu6 que les compos6s majoritaires del'HE
de cette plante dla
r6gionde
Constantineest
principalement caractlris6epar l'acide
isocostique(25,lyo),I'acide
cosique (15,2%),
le nerolidol (9,6yo),I'acide linol6ique (9,IYo),len6o-intermedeol (7,5%o) et le fokienol (7,2%) .
Acide
8-Octad6c6noi
que,
egter
R6sultats
et discussion
Le m6me travail a 6t6 r6alis6 d la r6gion de
Jijel
aftvlIl
de diff6rents r6sultats par rapport aux notre, et que les compos6s majoritaires de leur HE extraite sont:o
2-ph6nanthr6nol,4b,
5,
6,7,8,8a,
9,10-
octahydro-4b, 8,8-trim6thyl-1-(1-m6thy6thyl)-, 4bS-trans)- (3 5,7 2%)o
Benzdne,l-m6thyl
-2- (l-m6thyl6thyl) (24,83%).
2,6-Diisopropylanisole (10,13%) (Anonyme, 2010).Ces variations en composition chimique de
I'HE
peuvent €tre attribu6es au facteur spatio-temporel, aux caractdristiques m6t6orologiques, p6dologiques, climatiques, au stade de croissance de la plante, pakimoine g6n6tique, etdla
nature de l'6cosystdmed'origine:
plus
l'6cosystdme est ferm6(for6t
densepar
exemple),plus la
plante herbac6e est stress6e et en comp6tition aux 6l6ments nutritifs et d la lumidre, et plus le taux et la composition des HEs est diff6rente par rapport aux 6cosystdmes ouvertset ensoleill6s.
III.4.
AromatogrammeLa
v6rification
de
la
sensibilit6
des
souches bact6riennesutilis6es
pour
la r6alisation de l'aromatogramme a confirmEla
sensibilitd des bactdries choisies, viales antibiotiques pr6cit6s (Fig. 15).
Cette 6tape est n6cessaire,
vue
qu'il
s'agissede
souches cliniques.Le
r6sultatobtenu confirme que
les
gennes test6sn'ont
d6velopp6 aucuneforme
r6sistancecontre les
AB,
et le r6sultat de I'aromatogramme ne risquera pas, ainsi, d'6tre faux.La
lecture de l'aromatogrammea rfv6l6
de diff6rents r6sultats, dupoint
de vuequalitatif, que quantitatif
(Fig.
16). Les espdces bact6riennesE. coli,
P.mirabilis
etK. terrigena n'ont montr6 aucune sensibilit6 vers
I'HE
6tudi6e. Cependant, la bact6rieS.
aureus
et
le
champignonC.
albicans
ont
marqu6une
croissance inhib6e, correspondantaux
diamdfresde
l3r66mm
et
17r15mm,
et
aux
pourcentagesd' inhibition 15,9 4oh et 20%orespectivement (Tab.6).
f __ I
tt
R6sultats
et discussion
Figure 15. Antibiogramme sur les souches cliniques isol6es.
Figure 16.Effet de
I'IIE
surE
coli(A),K.
terrigena(B),P.
mirabilis (C),S. Aureus(D) et C. Albicans(E). (Photos effectu1es
par
nous-m1mes)rr
Tableau 6. Diamdtre et poureentage d'inhibition de la croissanoe, des souches test6es,
Selon l'6chelle proposEe par
Mutai
etal.
Q009), ces r6sultats montrent quel'HE
d'lnula
viscosa pure possdde une activit6 antimicrobienne fortement inhibitrice de lacroissance
de
Staphylococcus Aureus(15,94
o),
et
une activit6
antifongiquemod6r6ment
inhibitrice de
la
croissance myc6liennede
Candida Albicans Q0%).Cependant, les bact6ries Escherichia
Coli,
Proteusmirabilis
et Klebsiella tenigenaont continud
i
croitre m€me en pr6sence de cette huile, ce qui signifie queI'effet
decette dernidre sur ces trois souches est minime, voire absent.
A
tire
comparatif avec des dtudes ant6rieures, men6es surla
m6me espdce, lesr6sultats obtenus sont
en
semblables avec ceuxde
Bel
kacem
et
Djazair(2016)
obtenus d l'ouest alg6rien oti les rdsultats de
HE
deI'inule
visqueuse pure possddentune activit6 antimicrobienne
forte
surS.
Aureus(27
rnrn;30 %)
et mod6r6esur
C.Nbicans (20
mm;
22,22%).
Les m6mes auteursont
enregistr6la
r6sistance deE
Coli, P" mirabilis et
K.
terrigena vial'huile
en question.Les
bact6ries ayant prdsent6 une rdsistancevers
I'Itr
6tudi6efont
partie
desbact6ries d Gram n6gatif, tandis que la bact6rie ayant pr6sent6 une sensibilit6 via cette
dernidre, est caract6ris6e par son Gram positif.
Donc, si nous pouvons g6n6raliser les r6sultats obtenus,
I'HE
d'.L viscosaa un effet antibact6rien sur les bact6ries d Gram (+) et une activit6 antifongique.par
l'HE,
et comparaison avec d'autres 6tudes.Espice
Bel kacem et
Djazairi(20f6)
Etude pr6sente Qd'inhibition
(mm) %o
d'inhibition
{
d'inhibition
(mm) 7o doinhibitionE.
coli
0 0 0 0 P.mirabilis
0 0K.
terrigena 0 0 S. aureus 27 30 13,66 15,94 C. albicans 20)) ,)
17,r5 20,00 i 29,
Conclusion
Conclusion
Les
plantes m6dicinales constituentun
groupe num6riquementvaste des
plantes6conomiquement importantes.
Elles
contiennent des composants actifsutilis6s
dans letraitement
de
diverses maladies. Outreleur utilisation
comme remddes directs.on
lesemploie aussi dans les industries pharmaceutique, alimentaire et cosm6tique.
Les huiles essentielles peuvent 0tre commercialis6es et employ6es pour leurs multiples activit6s biologiques.
Dans le but de rechercher de nouveaux agents naturels antibact6riens et antifongiques
aux int6r6ts th6rapeutiques des huiles essentielles
d'une
plante m6dicinale dela
floreAlg6rienne,
Inula
viscosaL.,
a
fait
l'objet d'une vai6t6
d'6tudes dansce
travail:phytochimie, extraction des huiles essentielles, analyse de l'essence l.Viscosapar la CPG
et
enfinla
d6termination de leur pouvoir antibact6rien et antifongiqueir
vifro
sur dessouches pathogdnes:
il
s'agit
des bact6ries Staphylococcus aureus,Klebsiella
terrigena,Proteus mirabilis, Escherichia coli et de la levure candida albicans.
Le
screening phytochimique a r6v616 la richesse des feuillesd'Inula
viscosa, de notre r6gion, en composants bioactifs suivant: flavonoides, tanins et glucosides.Les r6sultats obtenus indiquent que
l'/.
viscosapossdde une teneur importante en eau de8l,4yo.
Cette richesse hydrique est accompagn6epar
un
faible
rendementen
HE,
de0,200 . L'essence obtenue est caract6ris6e par les paramdtres organoleptiques suivants: trds dense,
i
aspect limpide, de couleurjaturdtre et ayant une odeur attirante et d6sagr6able.Les
r6sultatsde
l'analyse chimiquede
la
compositionde
l'huile Inula
viscosa par chromatographie en phase gazeuse indiquent la richesse de cette dernidre en monoterpdnes oxygdnds, domindpilr: (
9,12-
acide octad6cadienoique(2,
z)-,
ester
m6thylique >Q'6,34yo), l'acide 8-Octad6c6noique, ester de m6thyl (E) (20,17 Yo) et carvacrol (11,72%o).
L'6valuation des effets antibact6rien et antifonglque montre que la majoritd des souches
bact6riennes utilisdes
(3/4)
sont
sensiblesaux
antibiotiquesutilis6s
et
que
les
huiles essentielles sont actives sur seulement une seule souche de bact6rie (d Grampositif)
et la levure. Des zonesd'inhibition
de diamdtres variables sont observ6es. Les bact6ries Grampositif
sont plus sensibles dI'action
des huiles que les bactdries Gram n6gatives, ce qui concorde avec beaucoup d'6tudes r6alis6es dans cette optique.Cette 6tude peut 6tre consid6r6e comme une premidre source
d'information sur
lespropri6t6s phytochimiques, antibactdriennes et antifongiques des huiles essentielles
d'Inula
viscosa de
la
rdgion de Taher,Wilaya
deJijel.
Cetteplante
locale
est
une sourcet
-l
Jv
Conclusion
inestimable en divers compos6s dou6s des activit6s biologiques, ce qui t6moigne et
justifie
son utilisation en alimentation et en m6decine traditionnelle comme traitement d plusieurs
pathologies.
Cette 6tude m6rite d'6tre poursuivie et compl6t6e par des 6tudes ult6rieures, esp6rant
que
d'autresvolets soient
abord6s,toutes
les
parties
de
la
plante
soientprises
enconsiddration, non seulement les feuilles, et que l'6chantillolmage soit mensuel. Ce sujet trds important d 1'6che11e mondial, ouwe les portes dans le domaine m6dical, surtout pour
r6soudre
le
probldme
de
r6sistanceacquise
des
bact6riesvers
les
antibiotiquescommercialis6s. Les HEs, d'.[. viscosa et beaucoup d'autres plantes m6dicinales, semblent
Otre les moldcules qui remplacent les antibiotiques dans les cas de r6sistance.