© Charles-Olivier Gilbert, 2019
Développement de polymères bidimensionnels par
couplage photochimique
Mémoire
Charles-Olivier Gilbert
Maîtrise en chimie - avec mémoire
Maître ès sciences (M. Sc.)
Développement de polymères bidimensionnels par
couplage photochimique
Mémoire
Charles-Olivier Gilbert
Sous la direction de :
iii
Résumé
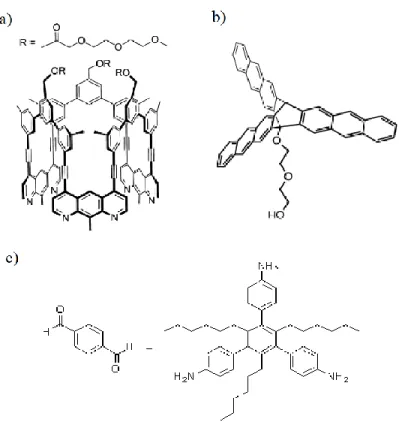
Les polymères 2D (2DP) se distinguent des polymères linéaires conventionnels par le fait qu’ils s’étendent sur deux dimensions. Bien qu’il soit possible par exfoliation d’isoler des feuilles de polymère à partir, par exemple, d’un matériau cristallin présentant des feuillets, il reste difficile d’obtenir par synthèse organique une structure 2D ordonnée dans l’espace. Il est réaliste de penser que les propriétés d’un polymère bidimensionnel soient nettement différentes de ceux ayant une structure unidimensionnelle et que ces mêmes propriétés pourraient permettre l’application des 2DP dans le domaine des semi-conducteurs, des senseurs ultra-sensibles, des matériaux optoélectroniques, de la médecine, des machines moléculaires ou même comme membrane nanoporeuse. Nos recherches ont porté sur l’élaboration d’un monomère organique capable de polymériser sur deux dimensions pour générer un polymère bidimensionnel selon la définition et les critères de Schlüter. Les objectifs de ce projet sont donc de concevoir et de synthétiser un monomère organique, de l’assembler sur deux dimensions, d’initier sa polymérisation de façon contrôlée, d’exfolier la structure d’épaisseur monomérique et de caractériser cette dernière. Trois structures sont présentées dans le cadre de ce mémoire. La première est un monomère amphiphile composé d’un fullerène (C60) hydrophobe et de chaines triéthylène glycol monométhyléther hydrophiles. Cet assemblage est orienté sur cuve Langmuir-Blodgett et polymérisé par cycloaddition [2+2] des unités fullerènes. La deuxième structure est un dérivé du poly(p-phénylènetéréphtalamide) (PPD-T). Son organisation est effectuée par filage en milieu humide en phase cristal liquide et sa polymérisation par addition 1,4 des diacétylènes. La dernière macromolécule est, elle aussi, un dérivé du PPD-T comportant de nouvelles fonctionnalités qui permettront sa mise en œuvre efficace.
iv
Table des matières
Résumé ... iii
Liste des figures ... vi
Liste des tableaux ... viii
Liste des abréviations ... ix
Remerciements ... xii
1. Introduction ... 1
1.1 Les polymères unidimensionnels ... 2
1.2 Matériaux bidimensionnels ... 5
1.3 Le cas du graphène ... 9
1.4 Les polymères 2D ... 14
1.4.1 Définition d’un 2DP ... 14
1.4.2 Les critères d’un 2DP ... 17
1.4.3 Propriétés et applications des 2DPs ... 20
1.4.4 Synthèse des 2DP ... 22
1.5 Objectifs ... 36
2. Méthodes expérimentales ... 38
2.1 Résonance magnétique nucléaire en solution (RMN) ... 38
2.2 Spectroscopie de masse haute résolution (HRMS) ... 38
2.3 Spectroscopie d’absorption ultraviolet-visible (UV-vis) ... 38
2.4 Spectroscopie Raman ... 39
2.5 Microscopie à angle de Brewster (BAM) ... 39
2.6 Analyse sur cuve Langmuir-Blodgett ... 39
2.7 Chromatographie par perméation de gel (GPC) ... 39
3. Synthèse d’un polymère bidimensionnel à l’interface air/eau via un monomère amphiphile 0D à base de fullerènes ... 41
3.1 Objectifs du chapitre ... 41
3.2 Design du monomère ... 41
3.2.1 Synthèse du monomère ... 43
v
3.3 Assemblage à l’interface air/eau ... 46
3.3.1 La cuve Langmuir-Blodgett ... 46
3.3.2 Isothermes de compression ... 47
3.3.3 Méthodes de transfert ... 49
3.4 Caractérisation ... 50
3.4.1 Microscopie à l’angle de Brewster ... 50
3.4.2 Spectroscopie ultraviolet-visible ... 52
3.4.3 Spectroscopie Raman ... 54
3.5 Conclusion du projet sur les fullerènes amphiphiles ... 57
4 Synthèse d’un polymère 2D à partir d’un dérivé du poly(p-phénylènetéréphtalamide) mis en œuvre par filage de cristaux liquides ... 59
4.1 Objectifs ... 59
4.2 Design du polymère linéaire ... 59
4.2.1 Mise en œuvre du PPD-T ... 62
4.2.2 Polymérisation des unités 1,3-butadiyne ... 65
4.2.3 Synthèse organique ... 66
4.3 Mise en œuvre par filage humide ... 68
4.4 Modification de la solubilité du polymère ... 70
4.5 Conclusion du projet sur le polymère dérivé du poly(p-phénylènetéréphtalamide) ... 71
5 Synthèse d’un polymère 2D à partir d’un dérivé du poly(p-phénylènetéréphtalamide), mis en œuvre par gélification et à l’interface air/eau .... 73
5.1 Synthèse organique ... 74
5.2 Résultats préliminaires ... 77
5.3 Conclusion du projet sur le polymère dérivé du poly(p-phénylènetéréphtalamide), 2ième génération ... 80
6 Conclusion et travaux futurs ... 81
Annexe ... 83
A.1 Procédure générale ... 83
A.2 Synthèse des produits ... 83
A.3 Spectres et illustrations supplémentaires ... 91
vi
Liste des figures
Figure 1 - Structure du caoutchouc selon la théorie d’association. ... 3
Figure 2 - Structure du caoutchouc selon la théorie macromoléculaire. ... 3
Figure 3 - Structure des bandes calculée pour MoS2 brut, quadricouche, bicouche et monocouche. 6 Figure 4 - Model tridimensionnel de la structure cristalline de MoS2, structure planaire du h-BN, design du COF-5 synthétisé par Yaghi en 2005 et structure d’un feuillet de MOF [Cu2Br(IN)2]n. .... 9
Figure 5 - Certains allotropes du carbone.... 16
Figure 6 - Vue de biais et latérale d’un hypothétique feuillet de polymère 2D en suspension. ... 18
Figure 7 - Monomère hypothétique pouvant polymériser dans deux dimensions ... 19
Figure 8 - Représentation schématique d’un 2DP possédant une série de sites actifs. ... 21
Figure 9 - Représentation idéalisée de la polymérisation du monomère 1. ... 24
Figure 10 - Couplage du monomère 1 avec une structure plus complexe, rotation des deux fragments l’un par rapport à l’autre, déformant la structure 2D... 25
Figure 11 - Structure bidimensionnelle de Zhao et de Kim. ... 28
Figure 12 - Monomère du 2DP de Häner et polymère linéaire précurseur au 2DP de Bai. ... 29
Figure 13 - Monomère de la structure de Schlüter, monomère du 2DP de King et monomères du feuillet de Zhang. ... 33
Figure 14 - Polymère 2D par Loh et monomère de Schlüter utilisés en phase cristalline. ... 36
Figure 15 - Monomère 3, fullerène amphiphile. ... 42
Figure 16 - Schéma de synthèse du fullerène amphiphile 3. ... 44
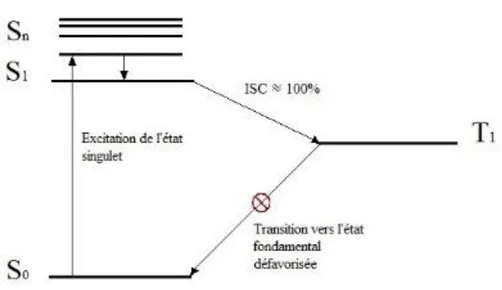
Figure 17 - Diagramme de Jablonski du fullerène à l’état solide sous photoirradiation. ... 45
Figure 18 - Isotherme de compression typique du monomère 3. ... 48
Figure 19 - Images BAM du monomère 3. L’acquisition des images est effectuée aux endroits indiqués sur l’isotherme de compression modèle du monomère amphiphile. ... 51
Figure 20 - Spectre d’absorption UV-visible d’une monocouche de monomère 3 sur une lamelle de verre après différents temps d’irradiation à 254 nm. ... 53
Figure 21 - Spectre Raman du monomère 3 déposé en «dropcast» (dépôt liquide suivi de l’évaporation du solvant) sur une lamelle de verre. ... 55
Figure 22 - Spectre Raman du monomère 3 déposé sous forme de monocouche sur une lamelle de verre... 56
Figure 23 - Spectre Raman du monomère 3 déposé sous forme de monocouche sur une lamelle de verre et irradié 1h à 254 nm sous atmosphère inerte. ... 57
Figure 24 - Stratégie de mise en œuvre du précurseur 1D avant l'étape de polymérisation. Les lignes noires schématisent l’allure des chaines de polymère alors que les rouges représentent la formation de liaisons covalentes. ... 61
Figure 25 - Polymère 10, dérivé du PPD-T. ... 61
Figure 26 - Réaction de polymérisation du polymère 10 permettant de générer un 2DP. ... 62
Figure 27 - Unité de répétition du poly(p-phénylènetéréphtalamide) (PPD-T). ... 63
Figure 28 - Schéma d’un dispositif pour le filage du PPD-T en phase cristal liquide. ... 64
Figure 29 - Projection parallèle à l’axe a de deux chaines de PPD-T liées par des liaisons hydrogène. Schéma des feuillets plissés à l’intérieur d’une fibre Kevlar. ... 65
Figure 30 - Paramètres indispensables à la synthèse topochimique de PDA. ... 66
vii
Figure 32 - Montage maison pour le filage humide du polymère 10. ... 69
Figure 33 - Illustration du polymère 22 dérivé du poly(p-phénylènetéréphtalamide), 2ième génération. ... 73
Figure 34 - Schéma de synthèse de la chaine amine 15. ... 75
Figure 35 - Schéma de synthèse de l’acide 2,5-diiodotéréphtalique 17. ... 76
Figure 36 - Schéma de synthèse du polymère 22. ... 77
viii
Liste des tableaux
Tableau 1 - Réactions effectuées pour modifier la solubilité du polymère 10 ... 71 Tableau 2 - Tests de gélification du polymère 22 dans différents solvants organiques. .. 78
ix
Liste des abréviations
1DP Polymère unidimensionnel
2DM Matériau bidimensionnel
2DP Polymère bidimensionnel
3DP Polymère tridimensionnel
AcOEt Acétate d’éthyle
AcOH Acide acétique
AFM Microscope à force atomique
ARPES Spectroscopie photoélectronique résolue en angle
BAM Microscope à angle de Brewster
CCM Chromatographie sur couche mince
CMOS Dispositifs métal-oxyde-semi-conducteur complémentaire
COF Covalent organic framework (structure organique covalente)
CVD Dépôt chimique en phase vapeur
DBU 1,8-Diazabicyclo[5.4.0]undéc-7-ène DCM Dichlorométhane DIPA Diisopropylamine DMAP 4-Diméthylaminopyridine DMSO Diméthylsulfoxyde DP Point de Dirac DMF N,N-diméthylformamide EDCl 1-Éthyl-3-(3-diméthylaminopropyl)carbodiimide eV Électron-volt
GPC Chromatographie d’exclusion stérique
h-BN Nitrure de bore hexagonal
HAP Hydrocarbure aromatique polycyclique
HMPA Hexaméthylphosphoramide
HOPG Graphite pyrolytique grandement orienté
x
ISC Conversion intersystème
J Constante de couplage (Hz)
LEED Diffraction d’électrons lents
M Molaire
MeOH Méthanol
MO Microscopie optique
MOF Metal-organic framework (structure organique-metal)
n-BuNH2 n-Butylamine
NMP N-Méthyl-2-pyrrolidone
n-PrNH2 n-Propylamine
o-DCB o-Dichlorobenzène
p-TsOH Acide paratoluènesulfonique
PDA Polydiacétylène
PEG Polyéthylène glycol
PPD-T Poly(p-phénylènetéréphtalamide)
Rhyd Rayon hydrodynamique
RMN Résonance magnétique nucléaire
SEM Microscope électronique à balayage
SLG Graphène simple-couche
STM Microscope à effet tunnel
TBAF Fluorure de tétrabutylammonium
TEA Triéthylamine
TEM Microscope électronique en transmission
THF Tétrahydrofurane
TMEDA N,N,N',N'-Tétraméthyléthylènediamine
TMD Dichalcogénure de métaux de transition
TMSA Triméthylsilyle acétylène
TsCl Chlorure de 4-toluènesulfonyle
UV-vis Ultraviolet-visible
xi
À mes premiers éducateurs, Luc et Lyne sans qui je ne serais pas allé bien loin.
« Un écureuil c’est juste un rat qui a compris la force du marketing » Olivier Niquet, La soirée est (encore) jeune
xii
Remerciements
J’aimerais d’abord remercier mon directeur de maîtrise, le professeur Jean-François Morin. Il m’a donné une chance de travailler dans son laboratoire sur un projet fascinant et m’a ouvert la porte vers un monde certes exigeant, mais aussi formateur et gratifiant. Je désire souligner sa grande disponibilité, son enthousiasme et ses capacités de pédagogues qui ont fait de mon passage dans son laboratoire une expérience positive et fort constructive. Je suis convaincu que l’approche du professeur Morin quant à la recherche scientifique en milieu universitaire fait de son laboratoire un milieu stimulant et permet de développer des scientifiques hautement compétents.
Je profite de cette section de mon mémoire de maîtrise pour remercier les membres du groupe Morin, notamment Joël Boismenu-Lavoie, Audrey Picard-Lafond, Patrick Darveau, Antoine Lafleur-Lambert et Frédéric Lirette pour leurs conseils quotidiens et la joie de vivre qu’ils dégagent. Je réserve aussi des remerciements particuliers à Maxime Daigle et Maude Desroches qui ont été des modèles d’excellence et d’assiduité. J’aimerais aussi dire merci à Sophie Morin et Guillaume Chamelot qui ont été tous deux des stagiaires exemplaires avec qui j’ai apprécié travailler. Je dois remercier particulièrement Samuel Caron qui m’a formé à mon arrivée et a littéralement posé les fondations de mes travaux de maîtrise. Finalement, un merci colossal aux différents professionnels de l’Université Laval qui m’ont aidé, c’est-à-dire Pierre Audet, Rodica Neagu Plesu et, surtout, François Paquet-Mercier.
Je termine en remerciant mes parents, Luc et Lyne, les deux personnes les plus importantes de ma vie. Ils sont mon point d’ancrage immuable qui me permet de me repérer et m’évite de tomber. Un merci particulier à mon frère Antoine et ma sœur Florence pour avoir été présents et bienveillants. Finalement, j’aimerais remercier Mélanie Légaré pour son soutien, son amour et sa patience dans les moments les plus difficiles. Tu as ensoleillé ce long périple par ta bonne humeur et ta joie contagieuse.
1
1.
Introduction
L’étude de nouveaux matériaux fait partie du quotidien de l’humanité depuis maintenant des millénaires. Que ce soit pour construire des outils, pour ériger des logements ou pour se façonner des vêtements, l’Homme a depuis longtemps expérimenté différents types d’éléments pour se protéger, s’alimenter et s’abriter. Prenons le cas des vêtements. Il a été démontré qu’il y a plus de 5000 ans, on utilisait déjà la laine de mouton en Mésopotamie pour élaborer des habits. En Égypte, dans les environs des années 3800 av. J.-C., on tissait le lin pour en faire des tenues. L’utilisation du chanvre et de la ramie comme fibres textiles date des années 2800 av. J.-C. en Asie. Même la culture de la soie remonte à 2640 av. J.-C. par le
peuple chinois qui a longtemps gardé ce savoir secret.1 Durant la période allant de la
préhistoire à la fin du 19e siècle, on exploitera exclusivement les fibres naturelles pour tisser
les habits de l’époque. Sans en être conscient, on effectuait la mise en œuvre de matériaux polymères. C’est cependant à partir des années 1860 que la science des polymères s’éveille réellement. La croissance et l’impact de ce champ d’expertise sont fulgurants et on estime qu’entre 1950 et 2015 c’est 7800 Mt de résines et de fibres qui ont été produites
synthétiquement.2 Il n’est donc pas difficile d’imaginer l’importance qu’a eu cette
technologie sur les êtres humains. Hermann Staudinger élabora d’ailleurs un modèle au début
du 20e siècle pour quantifier l’apport de la technologie à l’humanité et démontrer comment
les percées en science sont étroitement liées au changement de la société elle-même. Il avance que, sans la technologie, un individu doit se fier à lui-même et à d’autres «esclaves humains» pour accomplir des tâches. Avec l’avènement de la technologie, il peut maintenant compter sur des «esclaves techniques» pour augmenter la productivité individuelle de chacun, ce qu’il quantifie en «puissance par année». C’est à partir de ce modèle que Staudinger conclut qu’avec le support de la technologie, l’Humain n’a plus besoin de faire la guerre pour
2
1.1 Les polymères unidimensionnels
Un polymère est une molécule très étendue comprenant des centaines ou des milliers d’atomes, formée par la liaison successive d’une, deux ou plusieurs petites molécules gabarits
arrangées en chaine ou en réseau.4 On nomme les petites molécules gabarits, constituant
l’unité de répétition du polymère, des monomères. C’est à partir de ces monomères qu’on peut entreprendre des réactions de polymérisation menant aux macromolécules. Il faut remonter à l’année 1833 pour retrouver la première utilisation du terme «polymère» dans la littérature par Jons Jacob Berzelius dans son célèbre livre «Jahres-Bericht». Néanmoins, sa définition d’un polymère diffère largement de celle d’aujourd’hui, car à l’époque Berzelius reconnait que deux composés peuvent avoir la même constitution tout en différant de masse molaire, mais classe les polymères comme un nouveau type d’isomérisme sans tenir compte
de l’architecture moléculaire.5 On associait alors sous cette définition la relation entre
l’acétylène (C2H2), le benzène (C6H6) et le styrène (C8H8). La fin du 19e siècle et le début du
20e siècle ont marqué l’essor des matériaux polymères en raison de découvertes
technologiques importantes comme la vulcanisation du caoutchouc par Charles Goodyear (1839), la découverte du premier thermoplastique synthétique par Alexander Parkes (1862) et John Wesley Hyatt (1866) en utilisant du camphre comme agent plastifiant et de la nitrocellulose pour obtenir le celluloïd, et la synthèse du premier véritable polymère thermodurcissable industriel, la Bakélite, par Leo Baekeland (1907) en réalisant la
polycondensation du phénol avec le formaldéhyde.6
Malgré l’essor du domaine, la structure moléculaire des matériaux polymériques restait toujours méconnue. La théorie la plus répandue à l’époque pour expliquer le comportement de structures comme le polystyrène, la cellulose et le caoutchouc était la théorie de l’association des particules colloïdales. En se basant sur la chimie des solutions colloïdales, qui reposait largement sur les travaux de Thomas Graham à partir de 1861, on supposait que les petites molécules d’une solution s’autoassemblaient sans liaison covalente pour former
des structures micellaires.7 Ainsi, en s’appuyant sur la théorie d’association, Carl Harries
3
diméthylcyclooctadiène s’associant par des interactions non covalentes entre les alcènes,
comme représenté en Figure 1.8 Aujourd’hui, c’est plutôt la structure émergeant de la théorie
macromoléculaire, illustrée à la Figure 2, qui est acceptée pour définir le caoutchouc naturel.9
Figure 1 - Structure du caoutchouc selon la théorie d’association.
Figure 2 - Structure du caoutchouc selon la théorie macromoléculaire.
Trois éléments, selon Robert Olby, ont permis l’essor de la théorie d’association au début du
siècle dernier.10 D’une part, l’introduction des concepts de forces de valence primaires et de
forces de valence secondaires par Alfred Werner (1902) qui permettraient aux petites molécules liées de façon covalente, ou par des forces de valence primaires, de s’agréger via leurs «affinités résiduelles» pour former des complexes moléculaires en agrégat. D’autre part, les spécialistes de la cristallographie par diffraction des rayons X assuraient qu’une molécule ne pouvait pas être plus volumineuse que sa maille cristalline. Bien que cette affirmation est maintenant largement démentie, elle était alors majoritairement acceptée. Finalement, c’est l’émergence de la science des colloïdes qui joua le plus grand rôle dans l’établissement de la théorie d’association et la marginalisation du concept de longue
chaine.10
Il a fallu attendre les travaux de Hermann Staudinger, à partir de 1920, pour remettre en question la théorie d’association au profit de celle de longues chaines covalentes. La première
4
preuve expérimentale vint lorsque Staudinger et Fritschi firent l’hydrogénation du caoutchouc naturel et démontrèrent que la disparition des doubles liaisons du modèle en Figure 1 n’était pas accompagnée par la formation d’hydrocarbure volatil cyclique. En fait,
ils observèrent ce qu’ils décrivirent comme un polymère analogue au caoutchouc.11
L’avancement de l’interprétation des diffractogrammes de diffraction des rayons X, avec en chef de file Michael Polanyi, permit une analyse plus précise des polymères et contribua dès 1921 à corroborer la théorie de Staudinger. Le concept de longues chaines polymères s’étendit suite au symposium de septembre 1926 à Dusseldorf intitulé «Gesellschaft Deutscher Naturforscher und Arzte», survécut à la théorie micellaire de Meyer et Mark en
1928 et fut cimentée par les travaux de Wallace Carothers entre 1928 et 1937.12,13 Hermann
Staudinger reçu le prix Nobel de chimie en 1953 pour ces travaux sur les polymères, consolidant, par le fait même, le domaine de la chimie macromoléculaire.
Depuis, on emploie les polymères linéaires de plusieurs façons. Ils sont devenus un élément de notre quotidien et il n’est pas exagéré de dire qu’ils sont omniprésents. À preuve, en 2000,
on estimait la demande mondiale en plastique à 146 millions de tonnes.14 Bien que c’est dans
le domaine de l’emballage qu’ils sont le plus utilisés, on les exploite aussi dans le secteur des capteurs, des matériaux conducteurs, des composites biomédicales, des applications
thermoélectriques et bien plus.15 Pour ce qui est des capteurs, le faible prix des polymères,
leur facilité de fabrication, la possibilité de les déposer sur différentes surfaces et leur potentiel de fonctionnalisation font de ces structures des candidats de choix. En les mettant en œuvre, il est donc possible de façonner des capteurs mécaniques (polyimide, polyéthylène, polyacétate de vinyle), thermiques (polytétrafluoroéthylène, polyméthacrylate de méthyle), chimiques (copolymère polyfluorure de vinylidène/trifluoroéthylène), acoustiques
(polytétrafluoroéthylène, Teflon-éthylène propylène fluoré), etc.16 Les polymères
conducteurs, quant à eux, affichent évidemment des propriétés de conduction électrique, mais aussi des propriétés électroniques, magnétiques, optiques et mécaniques souvent exceptionnelles. Encore une fois, leur grande versatilité leur permet de trouver des applications en catalyses, comme dispositif de nanoélectronique (transistor à effet de champ, diode), comme dispositif de stockage d’énergie (cellule solaire, pile à combustible, batterie
5
lithium ion), etc.17 Pour terminer, les polymères trouvent également une application comme
matériaux composites dans le domaine biomédical, puisqu’ils offrent une vaste variété de structures chimiques, de propriétés et de formes. De plus, ils peuvent être façonnés en plusieurs architectures pour permettre de les utiliser comme prothèses dentaires, prothèses de ligaments ou de tendons, membres prothétiques et remplacements d’articulations
synoviales, notamment.18
1.2 Matériaux bidimensionnels
Avant de continuer sur le sujet des polymères 2D, il est primordial d’explorer le secteur des matériaux bidimensionnels (2DM) en général. Une structure assemblée en couches, où celles-ci s’étendent sur deux axes en ayant seulement de faibles interactions intercouches, peut être qualifiée de matériau 2D. Cette catégorie de matériaux possède des caractéristiques physiques, électroniques et mécaniques incomparables à celles d’autres types de structures. Ces particularités proviennent de l’épaisseur nanométrique des 2DM et permet l’apparition d’un effet de confinement quantique qui limite le déplacement des électrons du matériau sur
deux dimensions.19 En ajoutant les effets quantiques associés au confinement et en concédant
que les 2DM possèdent un ratio de surface sur volume élevé, on obtient une structure possédant éventuellement une mobilité des porteurs de charge élevée (disulfure de molybdène), une conductivité thermique appréciable (nitrure de bore hexagonal) et une bande interdite nulle en restant un semiconducteur, puisque que la bande de conduction et celle de valence se touche à un point de Dirac sans qu’il n’y ait de chevauchement (silicène). Physiquement, ces matériaux sont intrinsèquement flexibles, forts et extrêmement minces
lorsqu’isolés de la structure brute.20 Il est d’ailleurs crucial de mentionner que les propriétés
des 2DM sont modulables en fonction du nombre de couches assemblées de façon supramoléculaire les unes sur les autres. Ainsi, en s’éloignant de la structure brute et en se dirigeant vers la monocouche isolée, il est possible de modifier la structure électronique d’un matériau 2D. Le meilleur exemple pour démontrer ce phénomène est l’étude du disulfure de molybdène (MoS2). Ce dichalcogénure de métaux de transition (TMD) est assemblé selon un empilement de Bernal à l’état brut et agit comme un semiconducteur possédant une bande
6
interdite indirecte de 1,29 électron-volt (eV).21 En diminuant le nombre de couches du TMD,
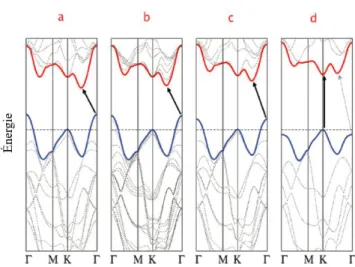
on remarque un changement dans la structure électronique du matériau qui devient photoluminescent puisque la bande interdite indirecte augmente d’environ 0,6 eV alors que la bande interdite directe située au point K (K’) de la zone de Brillouin augmente de seulement 0,1 eV. Comme indiqué à la Figure 3, le MoS2 passe donc d’un matériau possédant une bande interdite indirecte à l’état brut à une structure ayant une bande interdite
directe en monocouche.22, 23 Il s’agit d’un exemple intéressant de l’effet du confinement
quantique sur les propriétés d’un 2DM.
Figure 3 - Structure des bandes calculée pour MoS2 brut (a), quadricouche (b), bicouche (c)
et monocouche (d)22.
Les 2DM montrent aussi un caractère d’isolant topologique, des effets Hall quantiques anormaux à température ambiante, des propriétés de spintroniques intéressantes et ouvrent la
voie à une nouvelle avenue de la physique de «Fermi-Dirac».20, 24, 25
On divise habituellement en trois catégories les 2DM; solide en couches de van der Waals, solide en couches ioniques et solide non stratifiés assemblés sur support. Les solides en couches de van der Waals sont de loin les plus étudiés, car il s’agit généralement de structures
7
faciles à exfolier. Ces assemblages cristallins sont composés de feuillets neutres, d’épaisseur atomique ou polyédrique et liés de façon covalente ou ionique en deux dimensions. Les couches sont maintenues les unes aux autres par de faibles interactions de van der Waals dans le troisième axe, ce qui permet une énergie d’association d’environ 40 à 70 meV entre les feuillets. Les nanofeuillets isolés de ces structures mesurent habituellement moins de 1 nm
d’épaisseur et s’étendent sur quelques micromètres seulement.19,20 Les dichalcogénures de
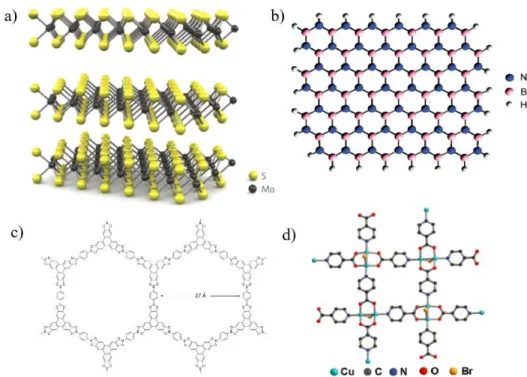
métaux de transition font partie de cette catégorie de matériaux 2D (voir Figure 4a). L’architecture des TMD est en forme de «sandwich», où un métal de transition en feuillet (Mo, W, Nb, etc.) est compris entre deux couches de chalcogènes (S, Se, Te, etc.). La structure, de nomenclature MX2, est évidemment liée fortement dans un plan par liaisons covalentes, et de faibles forces de van der Waals retiennent les couches entre elles. Deux structures cristallines peuvent être observées, la forme prismatique trigonale (2H) et la forme octaédrique (1T). La phase présente majoritairement dicte normalement les propriétés électroniques du TMD. Ces structures sont déjà envisagées comme outils optoélectroniques ou plateformes en catalyse chimique, par exemple dans des réactions de synthèse
d’hydrogène par réduction électrocatalytique ou photocatalytique de l’eau.26,27 Le nitrure de
bore hexagonal (h-BN) est une autre structure qui entre dans la catégorie des solides en couches de van der Waals (voir Figure 4b). Ce système hexagonal comprend dans sa maille des atomes de bore et d’azote s’alternant sur deux axes pour former une structure bidimensionnelle analogue au graphène. Les liaisons σ qui forment le réseau sont hybridées
sp2 et les interactions interfeuillets sont, de nouveau, de type van der Waals. Cette
organisation moléculaire confère au h-BN une conductivité thermique aussi élevée que 400
W m-1 K-1, ce qui est supérieur à la majorité des métaux et des céramiques.28
Les solides en couches ioniques sont agencés en feuillets chargés et polyédriques maintenus ensemble par l’intercalation de cations fortement électropositifs ou d’anions fortement électronégatifs entre les couches, typiquement par des ions halogénures ou hydroxydes. Les monocouches obtenues à partir de ce type de 2DM sont généralement d’une épaisseur de 0,5 à 1,0 nm et leurs dimensions latérales peuvent atteindre jusqu’à une dizaine de micromètres,
8
d’architectures composant cette classe de 2DM, mentionnons l’oxyde de pérovskite
La0.90Eu0.05Nb2O7 et l’hydroxyde de métal Eu(OH)2.5(DS)0.5.29,30
Finalement, les solides non stratifiés assemblés sur support sont la dernière catégorie de 2DM et regroupe les matériaux bidimensionnels assemblés artificiellement sur surface. Dans la plupart des cas, la synthèse s’effectue par déposition chimique en phase vapeur ou par épitaxie. Le silicène est un bon exemple de matériaux exclusivement accessible sous forme de solide non stratifié assemblable sur support. Cet allotrope du silicium est analogue au graphène par sa structure hexagonale et planaire, mais possède des liaisons covalentes qui
tendent fortement vers l’hybridation sp3, le rendant hautement actif chimiquement.31
En terminant, mentionnons qu’il existe aussi certaines structures hybrides (organiques et inorganiques) comme les MOF (Metal Organic Frameworks ou structure organique-métal) qui peuvent être assemblées sur deux dimensions par une approche exfoliatrice ou par synthèse à l’interface, permettant de catégoriser les MOF comme solide en couches de van der Waals ou comme solide non stratifié assemblé sur support (voir Figure 4d). Ces systèmes sont constitués d’ions ou d’agrégats inorganiques métalliques liés par des ligands organiques
ditopiques ou polytopiques.32 Les COF (Covalent Organic Frameworks ou structure
organique covalente), eux, sont des assemblages entièrement organiques et planaires qui peuvent être qualifiés de matériaux 2D, mais qui se placent difficilement dans les catégories énoncées précédemment, car leur synthèse s’effectue en solution par voie solvothermale, ionothermale ou par irradiation micro-onde (voir Figure 4c). Depuis les travaux de Yaghi en 2005, les COF représentent tout de même une classe de matériaux bidimensionnels intéressante grâce à leurs faibles densités, leurs porosités ajustables et leurs possibilités de
9
Figure 4 - Model tridimensionnel de la structure cristalline de MoS2 (a)27, structure
planaire du h-BN (b)28, design du COF-5 synthétisé par Yaghi en 2005 (c)33 et structure
d’un feuillet de MOF [Cu2Br(IN)2]n (d)32.
1.3 Le cas du graphène
Avant d’en venir aux polymères bidimensionnels (2DP), il est d’abord essentiel d’étudier le cas du graphène, car il s’agit de la structure primitive de tous ces polymères. Le graphène est un assemblage d’atomes de carbone liés en deux dimensions par des liaisons covalentes
hybridées sp2. Cette structure planaire forme un réseau hexagonal d’épaisseur atomique
possédant une conjugaison π étendue sur l’entièreté de son domaine. Le graphène est un matériau connu depuis bien des années. Déjà, à partir de 1947, on retrouve dans la littérature des études qui décrivent bien sa structure et qui placent les bases de l’étude de ses propriétés
électroniques.35 Néanmoins, à l’époque, c’est plutôt le graphite qui est étudié, c’est-à-dire un
empilement de feuillets de graphène que l’on retrouve abondamment dans la nature. Le graphite est donc un matériau bidimensionnel constitué de couches fortement liées sur deux
10
axes et faiblement jointes sur le troisième axe par des forces de van der Waals. On peut ainsi énoncer que le graphène est en fait du graphite qu’on aurait exfolié au maximum pour obtenir une couche unique et isolée du reste du matériau. Cette distinction entre graphène et graphite peut sembler triviale, mais le processus d’exfoliation de ce dernier permet de passer d’un matériau possédant de bonnes propriétés thermiques, électriques et mécaniques à une structure possédant des propriétés record. Ainsi, en passant du 2DM au feuillet confiné en deux dimensions, on augmente d’un facteur 100 la conductivité électrique sur un plan et par
près de deux la conductivité thermique du matériau.36,37,38 Il a fallu attendre jusqu’en 2004
les résultats des travaux de Geim et Novoselov dans Science pour finalement observer le premier feuillet de graphène isolé et commencer la caractérisation de cette architecture alors
unique.39 Ces travaux leur vaudront le prix Nobel de physique en 2010.
Trois éléments permettent d’expliquer les propriétés électroniques du graphène : sa bidimensionnalité, sa structure hexagonale et la symétrie d’inversion que possède la structure du au fait que le réseau est uniquement constitué d’atomes de carbone. Plus précisément, on peut considérer que le graphène possède deux sous-réseaux interpénétrant triangulaires où chaque atome du premier système n’est en connexion qu’avec les atomes du deuxième système. Cette particularité, lorsque traduite en structure de bande, permet d’obtenir des points de Dirac (DP) aux points K de la première zone de Brillouin. Aux DP, l’énergie d’excitation nécessaire pour permettre à un électron de passer du niveau de valence à la bande de conduction est de zéro. On constate donc un chevauchement des bandes π et π* précisément aux points K et K’ causé en grande partie par la symétrie d’inversion de la structure. En l’absence de cette dégénérescence, le graphène passerait d’un semiconducteur sans bande interdite à un isolant. L’importance de cette symétrie est évidente lorsqu’on observe la structure sœur du graphène, le h-BN. Bien que cette dernière structure soit planaire et hexagonale, elle ne possède pas de symétrie entre les deux sous-réseaux et perd le chevauchement de bandes aux DP, ce qui fait du h-BN un isolant ayant une bande interdite
d’environ 6 eV.40 Il est à noter que plusieurs autres matériaux possèdent des points de Dirac
coniques et symétriques dans leurs structures de bandes sans présenter les propriétés exceptionnelles du graphène. C’est le cas, par exemple, de certains dichalcogénures de
11
métaux de transition.41 Par contre, dans tous les cas, les propriétés électroniques des
matériaux sont dictées par d’autres états ailleurs dans la zone de Brillouin, enterrant l’effet des DP. Finalement, mentionnons que la structure de bande électronique du graphène induit dans le matériau une interconnectivité électron-trou, une suppression de la rétrodiffusion et un caractère ambipolaire, qui ajoutent au caractère singulier du matériau et qui pourraient permettre de démontrer expérimentalement certaines théories jusqu’à ce jour indémontrables comme le paradoxe de Klein, l’existence d’un indice de réfraction électronique négatif, le zitterbewegung (mouvement de tremblement) et l’effondrement atomique (atomic collapse).42,43,44
Pour ce qui est de la synthèse du graphène, plusieurs voies peuvent être utilisées. Historiquement, le premier feuillet de graphène fut isolé par la méthode du «scotch tape», c’est-à-dire par exfoliation mécanique successive d’un morceau de graphite. Avec cette méthode, on applique un ruban adhésif standard sur le graphite pour en retirer des couches qu’on ira par la suite appliquer sur un substrat. Les interactions de van der Waals sont alors
suffisantes pour retenir une monocouche de graphite lorsque le ruban est arraché.39 Cette
méthode, bien que simple et peu couteuse, reste difficilement applicable à grande échelle et génère une grande quantité de graphènes multicouches. Depuis 2006, une nouvelle méthode d’exfoliation à partir de l’oxyde de graphite permet d’obtenir des feuillets de graphène simple-couche (SLG). En oxydant le graphite par la méthode de Hummer, on obtient une structure possédant des fonctions époxydes et hydroxydes qui interagissent fortement avec
l’eau.121 Les molécules d’eau viennent donc s’intercaler entre les feuillets de carbone par
hydrophilicité pour disperser les monocouches d’oxyde de graphite qu’il est finalement
possible de réduire en SLG par traitement chimique ou par recuit.45 Les avantages de cette
méthode de synthèse sont son caractère bon marché et la possibilité de l’appliquer à grande échelle. Cependant, l’approche descendante via l’intermédiaire oxydé du graphite génère plusieurs défauts dans la structure cristalline 2D, notamment en passant d’une hybridation
sp2 à une hybridation sp3 de certains atomes de carbones pendant le processus d’oxydation.
En théorie, l’approche ascendante par synthèse organique totale permet d’obtenir des feuillets de graphène, mais en pratique c’est plutôt des molécules de la catégorie des hydrocarbures
12
aromatiques polycycliques (HAP) qui sont obtenus en raison de l’insolubilité du produit final qui limite les dimensions du réseau en formation. De plus, l’augmentation de la masse molaire entraine une augmentation des réactions secondaires, une diminution de la
dispersibilité et une diminution de la planarité.36 La dernière stratégie synthétique permettant
la synthèse ascendante du graphène est la méthode de croissance sur support qui comprend la méthode de croissance épitaxiale ainsi que le dépôt chimique en phase vapeur (CVD). La synthèse sur support permet d’obtenir de grandes quantités de graphène et il s’agit possiblement du meilleur moyen pour intégrer le matériau à une technologie CMOS (dispositifs métal-oxyde-semi-conducteur complémentaire) où les propriétés du graphène seraient intéressantes. Les défis restent le contrôle de l’épaisseur des films obtenus et la
limitation de la formation de cristaux secondaires.36,46,47
Un défi important des structures de type graphène (en particulier des SLG) est leur caractérisation. Comme il s’agit de matériaux d’épaisseur atomique et généralement insolubles, il est difficile d’observer précisément la périodicité du réseau et d’analyser les propriétés du feuillet sans adapter certains outils analytiques. Ainsi, il est possible d’observer un feuillet de graphène unique par microscopie optique (MO) en utilisant l’effet d’interférence et en modulant la source lumineuse en fonction de l’épaisseur du substrat (Si/SiO2) sur lequel repose le graphène. En utilisant une lamelle de 300 nm d’épaisseur, on obtient un contraste optimal en lumière verte et le feuillet de graphène devient invisible sous la lumière bleue. Cette technique permet de discriminer sommairement les structures
possédant peu de couches de celles en possédants plusieurs.48 Pour une analyse plus précise
de l’épaisseur des feuillets de graphène et pour confirmer l’obtention d’un SLG, on utilisera plutôt la spectroscopie Raman. Les spectres obtenus comportent généralement trois bandes ; les bandes G et G’, qui permettent d’évaluer le nombre de couches d’un flocon de graphène par analyse de leurs hauteurs relatives et leurs positions, et la bande D qui témoigne de la
pureté du feuillet.49 La méthode de caractérisation la plus populaire pour l’épaisseur du
graphène reste cependant la microscopie à sonde locale. La microscopie à force atomique (AFM) permet d’observer la topographie d’un substrat avec une résolution aussi bonne que 0,03 nm. Le graphène possède une épaisseur de 0,34 nm entre ses couches, ce qui le place
13
dans les limites de détection de l’appareil AFM. Comme il s’agit d’une technique non destructive et relativement courante, l’AFM est un outil de choix pour l’analyse des structures
2D d’épaisseur atomique.50 Dans le même ordre d’idée, la microscopie à effet tunnel est un
appareil permettant une résolution sous-atomique de la topographie de la surface du graphène et du graphite. Par cette technique, il est possible d’évaluer la cristallinité du substrat à
l’étude.51 Mentionnons finalement que plusieurs autres techniques peuvent être utilisées en
fonction des propriétés qu’on désire observer, telles que la microscopie électronique à balayage (SEM) et à transmission (TEM), la diffraction d’électrons lents (LEED), la
spectroscopie photoélectronique résolue en angle (ARPES) et bien d’autres.36,40
Quant aux propriétés du graphène, il a été dit au tout début de ce chapitre que le graphène possède des caractéristiques électroniques tout à fait phénoménales. Dans le domaine mécanique, il a été établi expérimentalement et théoriquement que le graphène possède une
rigidité de l’ordre de E = 1,0 ± 0,1 TPa, où E représente le module de Young.52 Sa résistance
à la traction mesurée à 130 GPa fait du graphène le matériau le plus résistant jamais mesuré.53
Un feuillet de graphène possède une dureté de fracture de Kc = 4,0 ± 0,6 MPa, où Kc
représente le facteur d’intensité de stress critique d’une fracture.54 Pour ce qui est des
propriétés thermiques, les fortes liaisons covalentes de la structure lui permettent d’atteindre
une conductivité thermique aussi haute que ~5000 W m-1 K-1 à température ambiante, soit
une valeur 2,5 fois plus élevée que celle du diamant et même plus élevée que la valeur
généralement acceptée pour un nanotube de carbone isolé et suspendu (~3500 W m-1 K-1).55
Terminons en mentionnant que le graphène présente aussi une sensibilité chimique extraordinaire. Il a été établi qu’un feuillet est suffisamment sensible pour détecter l’adsorption ou la désorption d’une molécule de gaz unique et cet effet s’explique par le fait que le graphène est un matériau détenant un faible bruit de fond électronique. Ce faible bruit de fond est principalement dû à la bidimensionnalité du feuillet, à sa forte conductivité électronique, à la haute cristallinité du réseau et à la possibilité d’utiliser quatre sondes sur le
14
À partir d’ici, une question s’impose. Pourquoi le cas du graphène est-il si important pour l’essor et l’épanouissement des polymères 2D? Il y a trois réponses à cette question. En premier lieu, il a longtemps été soupçonné qu’une structure 2D autoportante et planaire ne puisse exister naturellement. Ce doute originerait du théorème de Mermin-Wagner qui, interprété grossièrement, stipulerait qu’un cristal 2D est thermodynamiquement instable à
une température finie.36,40 Or, depuis l’émergence du graphène, ce scepticisme à l’endroit des
structures 2D isolées a fait place à un enthousiasme certain. En deuxième lieu, les propriétés exceptionnelles des feuillets de graphène mentionnées précédemment ont motivé la recherche d’une structure analogue qui serait équivalente ou même supérieure à cette dernière. Finalement, il va sans dire que les recherches sur le graphène ont établi les bases pour la caractérisation des structures 2D d’épaisseur atomique. Ces bases vont de la manipulation des échantillons obtenus à l’analyse des résultats, en passant par l’approche non invasive à prioriser.
1.4 Les polymères 2D
1.4.1 Définition d’un 2DP
Il est important de mentionner qu’il n’existe pas de définition sans équivoque de «polymère 2D». Le terme est souvent utilisé dans la littérature pour qualifier un polymère 1D qu’on
étend sur une surface plane, comme à l’interface air/eau d’une cuve Langmuir.57 On utilise
donc le terme «polymère 2D» pour évoquer le confinement physique des macromolécules sur un plan. Ici, c’est plutôt les polymères 2D au sens chimique qui seront étudiés, c’est-à-dire des macromolécules étendues sur un plan et contreintes par des liaisons chimiques fortes qui les obligent à garder cette conformation, peu importe le milieu où elles se trouvent. Comme il a été mentionné au chapitre 1.1, les polymères sont d’abord et avant tout constitués d’unités de répétition. Ces unités de répétition, lorsqu’isolés, sont des molécules en 0D, car ils ne se répètent dans aucune dimension. Lorsque ceux-ci s’assemblent linéairement, c’est un polymère 1D qui est synthétisé. Encore une fois, la section 1.1 mentionne cette catégorie
15
de polymères bien connue. Les polymères linéaires sont généralement solubles, aisés à mettre en œuvre et leurs méthodes de synthèse sont largement connues. Sans vouloir revenir sur le sujet, mentionnons simplement qu’il s’agit de loin des macromolécules les plus étudiées et les plus abondantes présentement. Lorsqu’un polymère 1D passe en solution, celui-ci prend une conformation «pseudo-tridimensionnelle» puisqu’il est étendu sur trois axes sur le plan physique alors que, chimiquement, il reste 1D. Ainsi, tant que le squelette principal ne réticule pas intramoléculairement ou intermoléculairement et de façon permanente, la chaine est considérée comme un polymère 1D. En établissant périodiquement des liaisons covalentes entre les chaines principales sur trois dimensions et en caractérisant ces structures pour connaitre leurs masses molaires, on pourrait considérer de telles structures comme des polymères 3D. Pour ce qui est des polymères 2D, on pourrait les définir comme des monocouches ou feuillets covalents polymériques dans lesquels l’unité de répétition est liée
périodiquement sur deux dimensions.58 Des critères plus restrictifs sont présentés plus bas
pour compléter cette définition d’un 2DP. Entre autres, ces structures doivent être cristallines dans au moins une conformation, fortement liées et elles doivent aussi être isolables si celles-ci font partie d’un système tridimensionnel étendu où plusieurs feuillets sont retenus les uns sur les autres par des forces supramoléculaires. Ces enjeux seront décrits plus précisément à la section 1.4.2. Ces quelques attributs permettent de discriminer un matériau 2D d’un polymère 2D. Ainsi, tous les polymères 2D répondent à la définition énoncée à la section 1.2 et tombent dans la catégorie des matériaux 2D, mais ce ne sont pas tous les 2DMs qui sont
capables de combler les critères d’un 2DP.59 Il s’agit d’une distinction importante à faire,
puisqu’une large partie des propriétés et des applications des 2DP dépendront de leur périodicité, de leur robustesse et de leur accessibilité. Bien que les 2DM soient intéressants et méritent d’être étudiés, ils sont passablement différents des 2DP. Pour s’en convaincre, on a qu’à observer le cas du graphite et du graphène, le premier se qualifiant comme 2DM et le second comme 2DP.
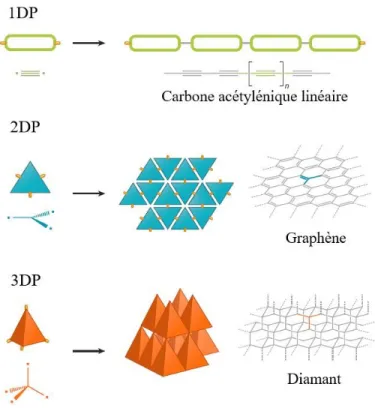
Les allotropes du carbone démontrent bien l’importance de la dimensionnalité d’un polymère. Effectivement, on reconnait que les propriétés physiques et chimiques du méthane
16
(0D) sont bien différentes de celles du carbone acétylénique linéaire (1D) elles-mêmes
différentes de celles du graphène (2D) et du diamant (3D) illustrés à la Figure 5.39,60,61
Figure 5 - Certains allotropes du carbone60.
Il est surprenant de constater que, malgré l’impact des polymères unidimensionnels sur le monde qui nous entoure, peu de résultats concluants sont disponibles dans la littérature à propos des 2DP et des 3DP. Il est vrai que l’idée de confiner des polymères sur un plan dans le but de synthétiser des feuilles de macromolécules date des années 1930 lorsque Gee polymérisa une monocouche d'un dérivé de l’anhydride maléique à l’interface air-eau, mais
aucun cas probant de polymère 2D n’a véritablement été observé avant 2012.62 C’est
d’ailleurs la conclusion à laquelle arrive Roald Hoffmann en 1993 lorsqu’il mentionne qu’une sous-culture des chimistes organiciens a appris à contrôler une dimension de l’espace moléculaire, mais que lorsqu’il est question de deux ou trois dimensions, on se retrouve en
17
1.4.2 Les critères d’un 2DP
Comme il existe plusieurs définitions d’un polymère 2D, il est nécessaire d’adopter certains critères pour discriminer les 2DP des 2DM. Évidemment, plusieurs chercheurs utilisent différentes méthodes pour qualifier un polymère 2D, certains ne considérant que la planarité du système, d’autre considérant les liaisons supramoléculaires comme suffisantes pour
générer un polymère 2D.65,67,68 Zang, lui, propose une approche plus cartésienne pour définir
un 2DP. Il mentionne que la structure 2D doit avoir une masse molaire d’au moins 10 000 Da, un «degré de bidimensionnalité» de plus de 1 000, un ratio de longueur sur largeur supérieur à 0,8 et un «ratio de bidimensionnalité» supérieur à 0,8. Le «degré de bidimensionnalité» représente l’aire du feuillet polymérique sur son épaisseur et le «ratio de bidimensionnalité» est calculé en divisant le «degré de bidimensionnalité» de la
conformation la plus stable par celui de la conformation la plus planaire.66 Toutes les
positions sont défendables mais, dans le cadre de ce mémoire, il semble essentiel de trancher et de choisir une seule définition qui s’appliquera à toutes les structures à venir. Ici, ce sont
les critères de sélections et la définition de Schlüter qui seront utilisés.59,60,64 Il s’agit, à mon
avis, des termes les plus restrictifs rencontrés dans la littérature, les mieux justifiés et les mieux élaborés. Ces derniers permettent de qualifier le graphène comme le premier polymère bidimensionnel jamais observé. Leurs caractères limitatifs permettent de disqualifier une grande quantité de structures comme les 2DM, les polymères hyperbranchés ou les assemblages supramoléculaires. Un polymère répondant à ces cinq critères présentera fort probablement les propriétés attendues pour un 2DP et sera, par le fait même, aussi susceptible d’avoir les applications espérées pour un 2DP.
Le premier critère est celui de la planarité. Les 2DPs sont donc des feuillets topologiquement planaires. La rigidité du feuillet n’a pas d’influence sur ce critère, ce qui permet au 2DP d’avoir une conformation ondulée en suspension dans un solvant. Il est d’ailleurs attendu
18
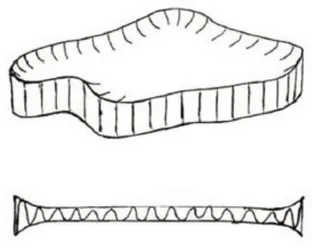
qu’en suspension la monocouche soit passablement ondulée sur tout son domaine et que cette
ondulation soit exacerbée en approchant les bords du feuillet (voir Figure 6).64
Figure 6 - Vue de biais et latérale d’un hypothétique feuillet de polymère 2D en
suspension64.
Le second critère concerne l’unité de répétition d’un 2DP. Le monomère qui le forme doit le rendre cristallin dans au moins une conformation. Ainsi, de la même manière qu’il est possible de prévoir la séquence d’atomes qui forme le polypropylène, le polystyrène ou le styrène-butadiène, un 2DP doit posséder une périodicité précise et fiable. En déposant la structure à plat sur une surface, on devrait obtenir un réseau cristallin formé par les unités de répétition. Comme illustré à la Figure 6, une fois le réseau complété, la macromolécule peut relaxer sous l’effet des degrés de liberté accessibles et adopter une conformation géométrique quelconque sans faillir à ce critère.
Le troisième critère stipule qu’un 2DP doit être formé de connexions robustes et préférablement de liaisons covalentes. De cette façon, la macromolécule obtenue est résistante aux conditions ambiantes. On discrimine donc, entre autres, les assemblages supramoléculaires, les structures synthétisées en solution tirant parti de réactions réversibles
19
autocorrectrices et les feuillets stables uniquement dans des conditions rigoureuses (sous vide, sous atmosphère inerte, à basse température, etc.).
Les 2DP se doivent d’avoir une épaisseur monomérique, c’est-à-dire de hauteur égale à l’unité de répétition qui les forme. Prenons, par exemple, un cas où l’unité de répétition serait constituée d’un segment polymérisable et d’un segment flexible comme une chaine alkyle latérale. La structure flexible possède assurément suffisamment de liberté pour effectuer des rotations avant la formation complète et irréversible du réseau périodique, ce qui empêche de prévoir où se situe le segment flexible avant la fin de l’étape de polymérisation. On obtient alors un feuillet d’épaisseur supérieure aux dimensions d’un monomère unique (Figure 7).
Figure 7 - Représentation d’un monomère hypothétique pouvant polymériser sur deux dimensions. Les points rouges représentent l’unité de couplage et les segments noirs les chaines latérales flexibles (a). Avant l’étape de couplage, les chaines peuvent se mouvoir
dans différentes positions (b). Une fois couplées, les chaines sont piégées dans cette configuration (c). Le feuillet est d’épaisseur supérieure à l’unité de répétition.
Le dernier critère est celui de la séparabilité. On devrait être en mesure d’exfolier le feuillet bidimensionnel du reste des macromolécules et d’obtenir une structure autoportante capable
20
d’exister aux conditions ambiantes. Cet assemblage isolé devrait pouvoir être modifié chimiquement. Plusieurs propriétés des 2DP découlent de l’obtention d’une monocouche unique et ce critère représente une preuve de structure d’envergure.
1.4.3 Propriétés et applications des 2DPs
L’application la plus évidente et la plus mentionnée pour les 2DP est comme membrane perméable. Effectivement, comme les 2DP sont formés d’un réseau de monomères périodique et uniforme, ils possèdent intrinsèquement une porosité monodisperse et possiblement modulable en taille s’il est possible de fonctionnaliser la structure 2D. Présentement, il n’existe aucune membrane fiable pour la séparation de mélanges gazeux composés de petites molécules de dimensions inférieures à 5 Å. À titre d’exemple, le diamètre de l’oxygène est de 3,8 Å et celui de l’azote est de 4,0 Å. Il s’agit d’une porosité plus qu’envisageable pour les structures 2D. Comme les monocouches de 2DP sont d’épaisseur monomérique, les membranes qu’elles formeraient permettraient un flux de gaz important à travers la structure, ce qui rendrait possible une séparation fort rapide. Finalement, deux mécanismes de séparation peuvent être employés en pensant à ces membranes, la diffusion de Knudsen où la dimension des pores est comparable au libre parcours moyen des molécules qui pénètrent la membrane et les effets de tamis moléculaire où la dimension des pores est beaucoup plus petite que le libre parcours moyen des éléments à isoler. Dans cette catégorie d’application, la séparation de petites molécules gazeuses est possiblement l’avenue la plus intéressante, mais il est aussi possible d’envisager d’utiliser des membranes de 2DP pour effectuer la désalinisation de l’eau ou même la filtration de
particules en suspension dans l’air.59,60,66
En synthétisant un monocristal d’empilements ultraminces de 2DP ayant les pores remplis,
il est possible de constater des effets d’optique non linéaire du second ordre.69 Cette propriété
21
nanométriques. Il serait donc possible d’élargir considérablement le domaine de longueurs
d’onde accessibles par une source de lumière cohérente.60
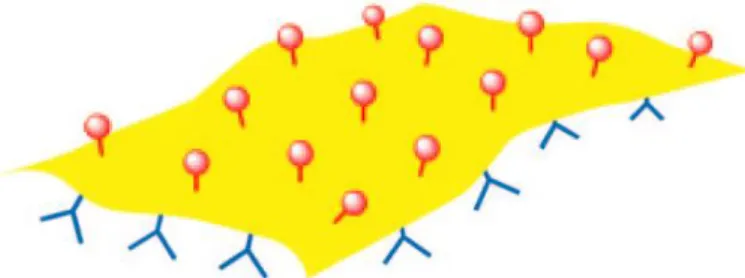
Comme la surface des 2DP est par définition périodique, il est possible d’affirmer que les groupements fonctionnels qui s’y trouvent sont nécessairement distribués uniformément sur toute la surface. La fonctionnalisation de ces groupements fonctionnels suivant l’étape de polymérisation permettrait donc d’étaler une grande population de sites actifs de façon homogène (Figure 8). À partir de ces sites actifs, il serait finalement possible d’effectuer de la catalyse hétérogène pour l’étude des relations structure-activité entre des catalyseurs et des
molécules à l’essai.60 Dans le même ordre d’idée, les sites actifs pourraient servir de point
d’ancrage pour la synthèse ascendante de structures tridimensionnelles ou pour la fabrication
de circuits électriques d’épaisseur nanométrique.70
Figure 8 - Représentation schématique d’un 2DP possédant une série de sites actifs70.
Plusieurs autres applications sont imaginables. Par exemple, en réussissant à les installer au-dessus de cavités sans endommager la structure, les 2DP pourraient agir comme capteurs de
pression ultraminces.70 En élaborant judicieusement le squelette périodique du polymère et
en introduisant une molécule appropriée dans les pores du réseau, on serait à même d’obtenir un matériau efficace pour les cellules photovoltaïques où l’un des constituants agit comme donneur et l’autre comme accepteur. Finalement, l’épaisseur monomérique et les dimensions latérales colossales des 2DP permettraient, dans plusieurs cas, l’acquisition de feuillets
22
1.4.4 Synthèse des 2DP
Il existe plusieurs stratégies pour l’élaboration synthétique de polymères 2D. Par exemple, il est possible d’opter pour une approche isotrope, où un point de nucléation (0D) polymérise en x et y simultanément pour créer le feuillet covalent. D’un autre côté, on pourrait aussi opter pour une approche anisotrope en débutant par la synthèse d’un polymère linéaire (1D)
que l’on étendrait par la suite sur une seule dimension.70 Les deux méthodes présentent des
avantages. Dans le premier cas, on évite d’assembler les monomères dans une conformation cristalline avant l’étape de polymérisation et on laisse les unités de répétitions se charger de l’assemblage 2D. Dans le second cas, on peut contrôler les dimensions latérales du polymère linéaire et on limite possiblement le nombre de défauts dans le réseau. Plusieurs considérations doivent être prises en compte lors du choix de méthode synthétique et le domaine est encore trop embryonnaire pour statuer sur la meilleure méthode, ou celle permettant les meilleurs rendements. Une chose est sûre, contrairement aux polymères unidimensionnels où le taux de conversion a un impact sur la longueur des chaines, le taux de conversion lors de la formation d’une monocouche covalente a un impact crucial sur la périodicité du réseau et, par le fait même, sur l’intégrité de la structure. Lorsque l’on considère le nombre d’évènements qui doivent avoir lieu pour qu’une macromolécule micrométrique prenne forme, il devient évident que le taux de conversion des monomères doit approcher les 100%. Ajoutons à cela que les liaisons doivent aussi se produire aux bons endroits et dans la bonne géométrie. Il est donc crucial d’élaborer des stratégies pour diriger, faciliter et assurer la formation de liens entre les monomères du feuillet organique. Ici, les trois principales stratégies synthétiques sont présentées en mentionnant leurs forces, leurs faiblesses, leurs particularités et quelques exemples de la littérature qui se sont approchés d’un polymère 2D selon la définition de Schlüter ou qui ont réussi à en obtenir un. Il s’agit de la synthèse en solution, interfaciale et via une structure cristalline.
23
1.4.4.1 Synthèse en solution
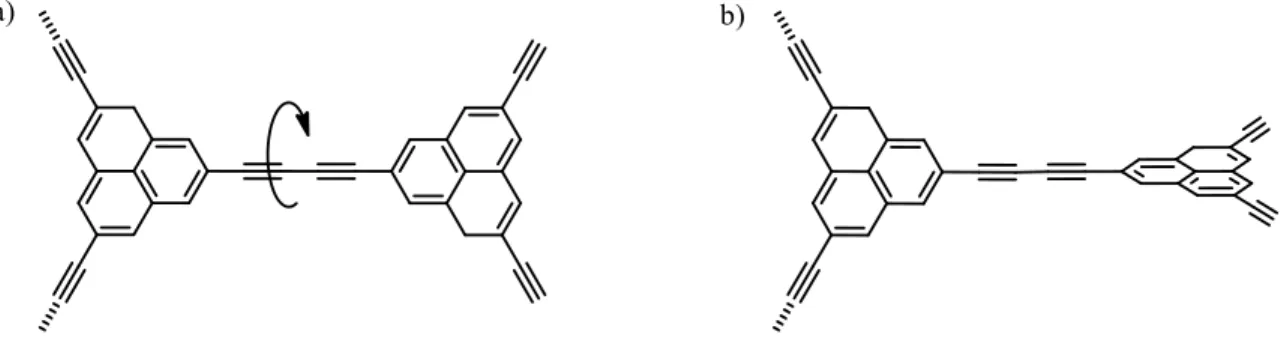
La synthèse de 2DP en solution se distingue des deux autres méthodes de synthèse par le fait que les étapes d’assemblage et de polymérisation se produisent simultanément. Comme les monomères se trouvent dans un environnement tridimensionnel dynamique, certaines stratégies doivent être employées pour assurer la bidimensionnalité du système en formation. Pour illustrer certains défis de la synthèse en solution, prenons la molécule 1 de la Figure 9 qui représente le triéthynyl-1H-phénalène déprotégé. Pour que 1 puisse polymériser sur deux dimensions, trois étapes d’homocouplage des alcynes terminaux dans les conditions de Glaser doivent se produire sur chaque monomère. La molécule résultant des trois événements d’homocouplage est représentée à la Figure 9. Il n’est pas impossible que cet intermédiaire au 2DP soit observable. Néanmoins, il est nettement plus improbable que la réaction en chaine qui suit pour permettre la synthèse de la structure 2D se produise. La faible barrière énergétique de rotation du lien qui lie les deux fragments ne restreint pas la structure sur un plan (Figure 10). Il est donc possible que, pendant un temps, l’assemblage soit bidimensionnel, mais il hautement plausible qu’à un moment, pendant la polymérisation, deux fragments se combinent avec un angle par rapport à la structure de départ et génèrent un matériau 3D aléatoire.
Un autre élément à tenir en compte est la possibilité que deux volumineux fragments se rencontrent et couplent dans une position peu optimale. Ces événements laisseraient alors des trous dans la structure avec possiblement de nombreux sites actifs non couplés au cœur du 2DP. Or, comme il a été mentionné dans la section 1.4.2, la périodicité du système est cruciale chez les 2DP. Pour éviter ces problèmes, il est important de prêter attention au design du monomère de départ. Ce dernier devrait avoir au moins trois sites actifs. Un monomère possédant quatre ou six sites fait aussi l’affaire, mais un de cinq ou sept est à éviter puisqu’il ne générera pas un réseau périodique continu. L’utilisation d’un squelette rigide et persistant restreint la formation de liaisons à, généralement, un seul site actif. Cette particularité permet de contrôler où auront lieu les événements de couplage et limite la formation de structures tridimensionnelles.
24
25
Figure 10 - Couplage du monomère 1 avec une structure plus complexe (a), rotation des deux fragments l’un par rapport à l’autre, déformant la structure 2D (b).
Dans le même ordre d’idée, l’usage d’espaceurs entre le squelette principal et les sites actifs est à éviter. Bien qu’ils permettent aux sites de formations de mieux s’orienter dans l’espace et favorisent la cinétique de réaction, ils augmentent considérablement le risque de réactions intramoléculaires et de réactions intermoléculaires sur des sites indésirables.
Pour assurer l’assemblage bidimensionnel des macromolécules, certaines stratégies synthétiques peuvent être utilisées, comme l’utilisation de réactions de polymérisation qui requièrent une coplanarité pour être effectuées. On peut penser, par exemple, à la dimérisation [4+4] des unités anthracènes, à la réaction de Diels-Alder, à la dimérisation [2+2] d’oléfines, à la photocyclo-dimérisation topochimique du 2,5-distyrylpyrazine ou, dans
certaines conditions, à la cycloaddition [2+2] des unités fullerènes.70,71,72 Cette catégorie de
réactions oblige la structure à adopter une conformation plane avant que se lient les monomères et maintient la structure en deux dimensions en limitant la rotation des parties. Une autre méthode consiste à incorporer des fonctions d’alignement pour favoriser la synthèse des polymères dans une configuration donnée ou pour limiter la synthèse dans une autre. Par exemple, il est possible d’utiliser des fonctions supramoléculaires pour favoriser l’assemblage dans un plan ou d’utiliser des fonctions volumineuses pour produire de l’encombrement stérique et défavoriser un plan lors de la polymérisation. Cette approche est toutefois laborieuse, car elle nécessite de bien connaître la cinétique d’assemblage des monomères fonctionnalisés en solution et plusieurs paramètres (pH, température, concentration, solvant, etc.) peuvent modifier le comportement de ces derniers.
26
Un autre grand défi de la synthèse des 2DP en solution est la perte rapide de solubilité des macromolécules à mesure que la polymérisation progresse. Cette perte de solubilité peut mener à la formation d’agrégats indissociables, donc peu intéressants comme 2DP. À l’instar des 1DP, il est possible de modifier les monomères de départ pour augmenter la solubilité des polymères synthétisés. La première méthode est d’introduire de longues chaines flexibles à la surface des feuillets. Le coût entropique étant de plus en plus difficile à payer à mesure que les chaines s’intercalent, une force répulsive apparaît lorsque deux macromolécules tentent de s’approcher. Ce mécanisme est d’ailleurs observable dans la nature, notamment chez les mucines, et a déjà été appliqué dans la littérature pour augmenter la solubilité, inhiber
l’adsorption de macromolécules et stabiliser des particules colloïdales en suspension.73 Une
seconde méthode consiste à installer des charges identiques à la surface des monocouches. Comme ces charges se repoussent, on devrait observer une séparation nette des macromolécules.
Au final, malgré toutes les mesures synthétiques utilisées, il est fort probable que les feuillets 2D soient polydisperses et qu’aucune des macromolécules n’ait la même forme. Il s’agit d’ailleurs d’un des désavantages de cette technique. Un autre inconvénient vient du fait qu’une fois les 2DP obtenus, il est difficile de récupérer individuellement chaque feuillet. Comme ceux-ci sont généralement en suspension dans un solvant, il est ardu de «pêcher» un polymère à la fois et c’est plutôt une masse de macromolécules qui sera récupérée. Par contre, la synthèse en solution permet d’obtenir une grande quantité de produits rapidement. Il s’agit d’ailleurs du plus grand avantage de cette technique de synthèse.
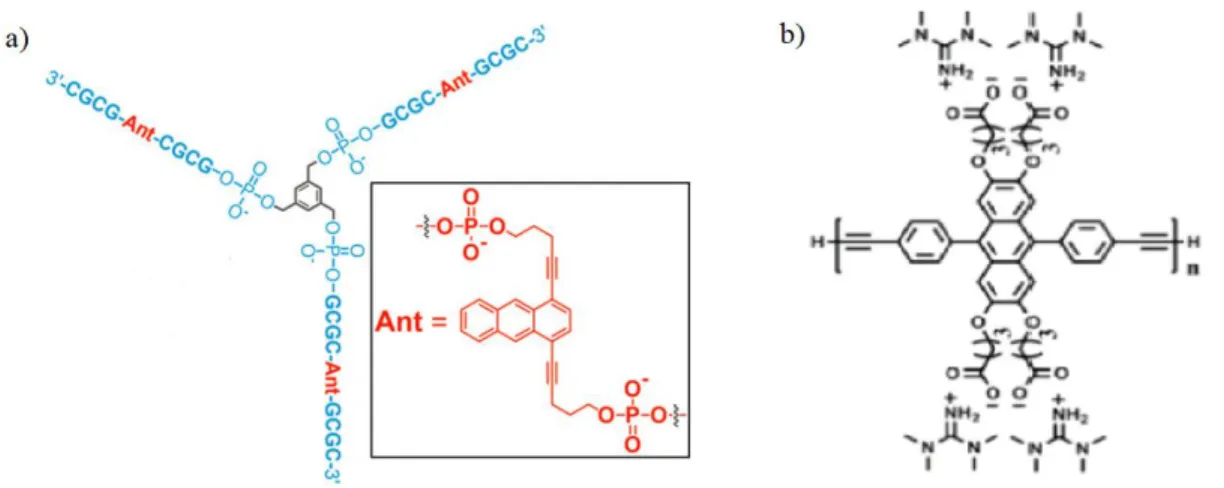
Plusieurs groupes de recherche ont tenté au fil des ans de synthétiser en solution un polymère 2D. Le groupe de Zhao a synthétisé une structure poreuse de type COF où la polycondensation d’acides boroniques avec une unité triptycène fonctionnalisée par six groupements alcools a permis la synthèse d’une monocouche (Figure 11a). Comme leur design place les fonctions aromatiques perpendiculaires au plan de la monocouche, les