Profil du pemphigus à Marrakech
Texte intégral
Figure

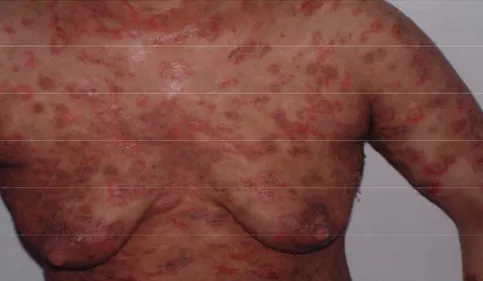
Outline
Documents relatifs
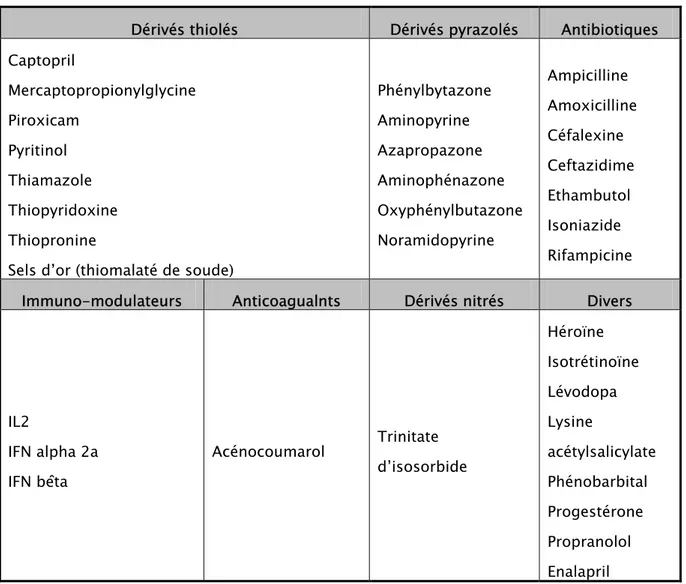
L’évolu- tion selon les modalités thérapeutiques est résumée dans le tableau II et la nature des complications iatrogènes, trouvées dans 97 cas (80 p. 100) en poussée et
L’origine difficile à expliquer et même à comprendre pour l’ensemble des protagonistes de ce système médi- cal s’articule aux manifestations symp- tomatiques parfois
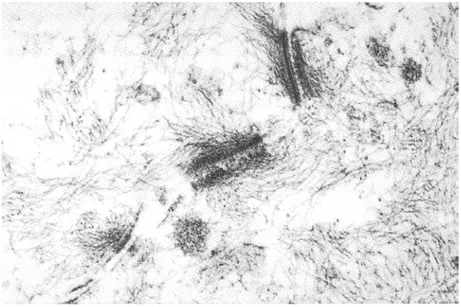
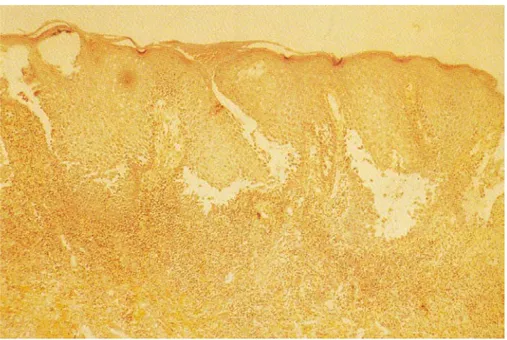
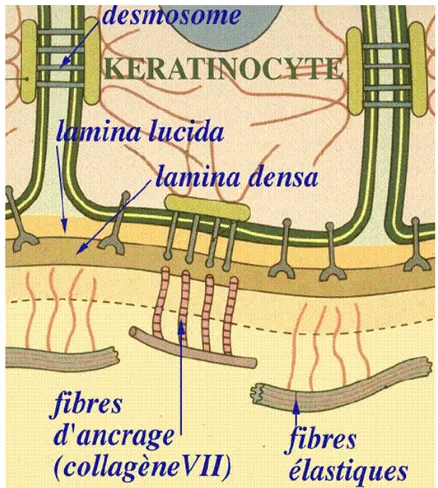
L'examen anatomo pathologique d'une biopsie de peau lésée montre un clivage intra-épider mique, plus (pemphigus foliacé) ou moins ( pemphigus vulgaire) haut dans
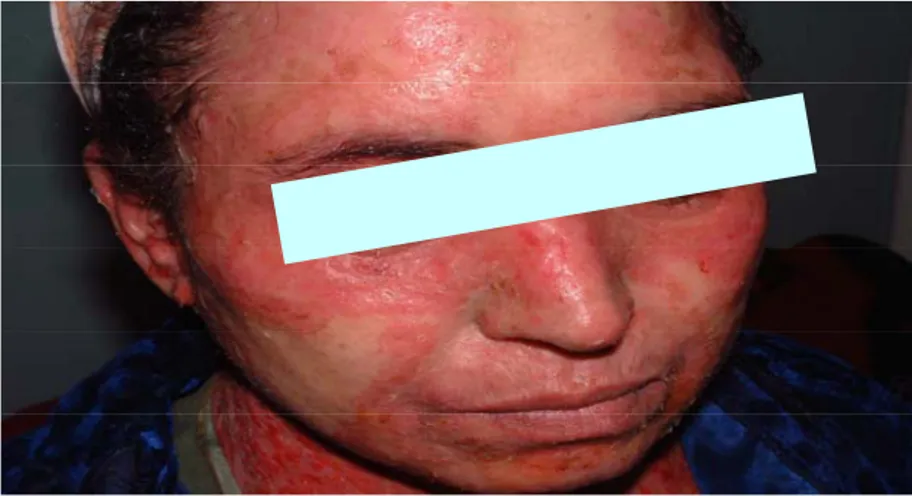
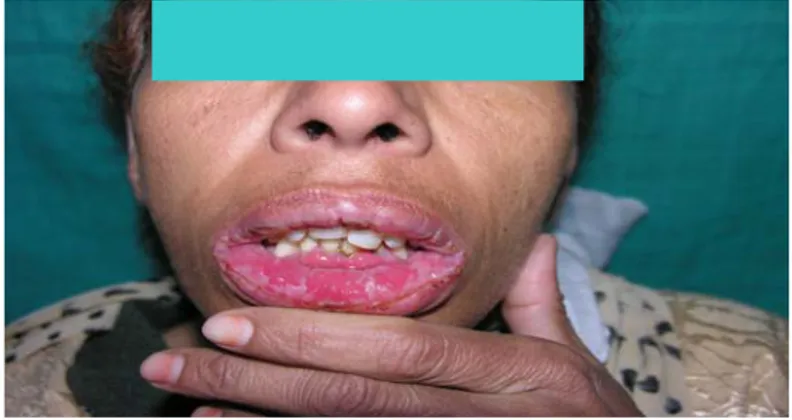
L'écartement maximum des paupières, pratiqué avec les doigts, atteint à peine un centimètre pour les deux yeux. La conjonctive palpébrale adhère à la conjonctive bulbaire
comme les mains dans leur totalité, avec deux ou trois bulles sur la face dorsale... Il n'y a rien de changé dans l'état de
Si vous êtes enceinte ou allaitante, ou que vous pensez pouvoir être enceinte ou désirez avoir un bébé, demandez conseil à votre médecin ou pharmacien avant de prendre ce
Toutefois d’autres auteurs décrivent le rôle du climat, de la pollution et de l’exposition aux rayons UV sur le risque de survenue du pemphigus. [19] Ce facteur pourrait
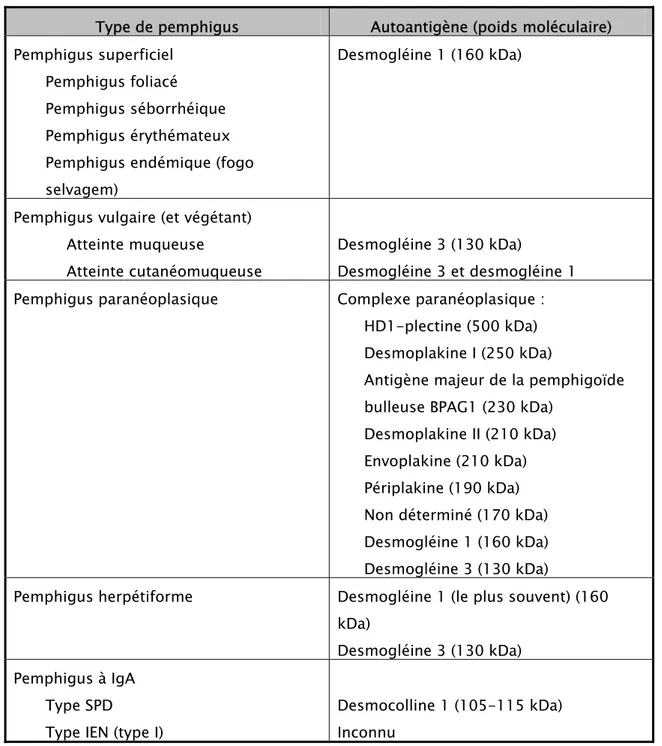
Le diagnostic du pemphigus paranéoplasique n'est pas aisé car la fréquence de la maladie est très faible et surtout les lésions cutanéo-muqueuses peuvent ressembler à