!
"# " #! $
% &
!" # " $ % && '
( ) (*+ , *" # * * " * % && '
-. +*! " / 0 # * " $ %* 1 '
* ( * " # * 0* " %* 1 '
1 0 + 0" # * 0* " %( 2 '
- 31 (*+, *"( * ( ) 4 5 " %* 1 '
(* 06 " # " $ "% 7 '
, " 8 ( " %* 1 '
# # ! $ 2
#' #' $0 0 9:;9
# (") '*" $ 1 0 + 0
0
:< ) 1$ =::;
$ ) & & 8 #
## 8 > 1 1 =:=?
Remerciements
Je tiens à remercier Monsieur Alexis Deschamps, Professeur à l’Institut National Polytechnique de Grenoble, d’avoir accepté de présider le jury lors de ma soutenance de thèse. Je remercie également Monsieur Bernard Baroux, Professeur à l’Institut National Polytechnique de Grenoble, et Monsieur David Delafosse, Professeur à l’Ecole Nationale Supérieure des Mines de Saint Etienne, qui ont accepté d’être rapporteurs de ces travaux de thèse. Mes remerciements s’adressent aussi à Monsieur Joël Alexis, Professeur à l’ENI de Tarbes pour sa participation au jury.
Je remercie Monsieur Maurice Sarfati, représentant de la DGA, pour sa participation à l’avancement des travaux et sa présence dans le jury.
Je souhaite également remercier EADS Innovation Works représenté par Madame Dominique Schuster et Monsieur Jérôme Delfosse pour l’aide financière et scientifique apportée à ce projet. Je tiens à remercier plus particulièrement Jérôme pour son implication importante au niveau du suivi de la thèse mais également pour sa gentillesse au cours de ces trois années.
Je souhaite remercier très sincèrement Madame Christine Blanc qui a dirigé cette thèse, grâce à qui j’ai pu acquérir de nombreuses connaissances en corrosion et en électrochimie qui me seront nécessaires par la suite. Au-delà de l’aspect scientifique, je tiens à vous remercier pour votre soutient, votre gentillesse, votre disponibilité, votre écoute et toutes nos discussions si enrichissantes d’un point de vue humain.
Un grand merci à Monsieur Eric Andrieu pour tout ce qu’il a pu m’apporter scientifiquement et pour ses innombrables idées d’expériences qui m’ont plus d’une fois fait « perdre la tête ».
Je tiens également à le remercier pour sa grande disponibilité malgré un emploi du temps très chargé.
Je tiens à remercier chaleureusement Monsieur Grégory Odemer qui nous a rejoint en cours de route, pour son aide si précieuse à tous égards. Merci pour ta gentillesse, ta disponibilité et ton humour qui a rendu la période de rédaction un peu plus agréable.
Merci à Monsieur Georges Mankowski d’avoir pris part à cette thèse.
Je souhaiterai également remercier toutes les personnes qui ont participé de près ou de loin à cette thèse :
- Jean-Claude Salabura et Ronan Mainguy pour la réalisation de la cellule de corrosion sous contrainte et la mise en place des essais ;
- Marie-Christine Lafont pour m’avoir permis d’approcher un peu la microscopie électronique en transmission et pour sa gentillesse ;
- Bernard Viguier pour m’avoir aidé lors des essais mécaniques de traction ;
- Dominique Poquillon pour son aide indispensable concernant la modélisation par éléments finis.
Je remercie très vivement mes collègues thésards de l’équipe CPM, Grégory et Loïc pour leur soutient et tout simplement pour leur compagnie si agréable et les bons moments partagés.
Un très grand merci à Jaime avec qui j’ai partagé le bureau pendant trois années. Merci pour ta gentillesse sans limite et pour tout ce que nous avons partagé et notamment nos longues discussions sur la vie et l’avenir. Muchas gracias amigo. Parmi les personnes qui sont passées par notre bureau, je remercie également Arfan que j’ai appris à découvrir et à apprécier.
Je tiens également à remercier les autres personnes sans qui ces années de thèses et nos soirées n’auraient pas été si agréables : Raluca, Fabienne, Aurélie, Elena, Aliou, Paul, Ronan et Nicolas.
Je remercie aussi très sincèrement mes amis qui ont fait le déplacement et qui m’ont soutenu : Cindy, Jean, Aurélie, Antoine, Valérie, Thomas, Audrey, François et Jean-Jérôme.
Evidemment, je remercie profondément mes parents pour leur soutient infaillible au cours de toutes ces années et sans qui je ne serai pas arrivée jusque là.
Enfin, merci à Paul d’avoir été toujours présent même si cela n’a pas toujours été facile. Je t’en suis infiniment reconnaissante.
TABLE DES MATIERES... 1
INTRODUCTION... 5
CHAPITRE I SYNTHESE BIBLIOGRAPHIQUE ... 9
I. ALLIAGE AA2024: MICROSTRUCTURE ET PROPRIETES MECANIQUES... 11
I.1. Les alliages d'aluminium Al-Cu... 12
I.1.1. Propriétés générales... 13
I.1.2. Durcissement structural ... 13
I.2. L'alliage d'aluminium 2024 T351 ... 14
I.2.1. Microstructure de l'alliage ... 15
I.2.2. Propriétés mécaniques... 18
II. COMPORTEMENT EN CORROSION DE L'ALLIAGE AA2024T351... 19
II.1. Corrosion des alliages d'aluminium ... 19
II.1.1. Eléments de base... 19
II.1.2. Les diverses formes de corrosion des alliages d'aluminium ... 22
II.2. La corrosion intergranulaire ... 25
II.2.1. Mécanismes de corrosion intergranulaire... 25
II.2.2. Paramètres influençant la sensibilité à la corrosion intergranulaire... 28
II.2.2.1. Espèces chimiques présentes dans le milieu ... 29
II.2.2.2. Précipitation aux joints de grains ... 31
II.2.2.3. Orientation des grains ... 32
II.2.3. Propriétés mécaniques résiduelles du matériau corrodé ... 34
II.3. La corrosion intergranulaire sous contrainte... 36
II.3.1. Mécanismes de corrosion intergranulaire sous contrainte... 37
II.3.1.1. La propagation électrochimique... 37
II.3.1.2. La fragilisation par hydrogène ... 40
II.3.2. Paramètres influençant la sensibilité à la corrosion intergranulaire sous contrainte... 40
II.3.2.1. Espèces chimiques présentes dans le milieu ... 41
II.3.2.2. Nature et niveau de contrainte ... 41
II.4. Etude des cinétiques de propagation des défauts de corrosion ... 44
II.4.1. Corrosion intergranulaire ... 44
II.4.2. Corrosion intergranulaire sous contrainte... 46
II.4.3. Modélisation des cinétiques ... 50
III. CONCLUSION... 51
CHAPITRE II METHODES ET CONDITIONS EXPERIMENTALES ... 53
I. ETUDE DU COMPORTEMENT GLOBAL EN CORROSION... 55
I.1. Caractérisation électrochimique... 55
I.2. Sensibilité à la corrosion intergranulaire : essais conventionnels d’immersion ... 57
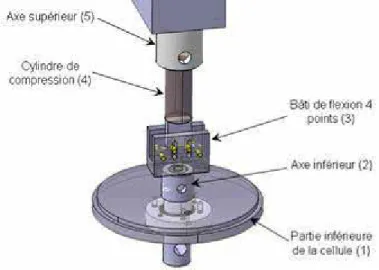
I.3. Sensibilité à la corrosion intergranulaire sous contrainte : essais de flexion 4 points .. 58
I.3.1. Principe général de l’essai ... 59
I.3.2. Protocole expérimental... 61
I.3.2.1. Essais à déplacement constant... 61
I.3.2.2. Essais à chargement constant ... 62
II. CARACTERISATION DE L’ETAT METALLURGIQUE DU MATERIAU ET CORRELATION CORROSION / ETAT METALLURGIQUE... 64
II.1. Microscopie optique... 64
II.2. Microscopie électronique à balayage (MEB) ... 65
II.3. Microscopie électronique en transmission (MET) ... 65
II.3.1. Echantillons sains... 65
II.3.2. Echantillons corrodés... 66
II.4. Spectrométrie de masse des ions secondaires (SIMS)... 66
CHAPITRE III MATERIAU DE L’ETUDE, L’ALLIAGE 2024 T351... 69
I. CARACTERISATION GLOBALE DU MATERIAU D’ETUDE... 71
I.1. Macrostructure ... 71
I.2. Propriétés mécaniques... 73
II. CARACTERISATION DE L’ETAT MICROSTRUCTURAL... 75
II.1. Précipitation intragranulaire... 75
II.2. Précipitation intergranulaire... 79
CHAPITRE IV CORROSION INTERGRANULAIRE : DESCRIPTION ET EVALUATION DU DOMMAGE ... 83
I. MISE EN EVIDENCE DE LA SENSIBILITE A LA CORROSION INTERGRANULAIRE DE L’ALLIAGE 2024 T351 ... 85
I.1. Comportement électrochimique ... 86
I.2. Mécanismes de corrosion intergranulaire ... 88
I.2.1. Observations MEB et analyses SIMS... 89
I.2.2. Observations MET ... 92
II. ESSAIS CONVENTIONNELS D’IMMERSION : CARACTERISATION DU DOMMAGE... 96
II.1. Morphologie des défauts... 96
II.2. Définition d’un critère d’évaluation des cinétiques de propagation des défauts de corrosion... 100
II.2.1. Critère d’évaluation : la longueur des défauts de corrosion intergranulaire ... 101
II.2.2. Critère d’évaluation : la densité de défauts de corrosion intergranulaire... 105
II.3. Limites de la méthode ... 106
III. LE PROTOCOLE TPC ... 107
III.1. Mise en place du protocole ... 107
III.1.1. Méthodologie expérimentale ... 107
III.1.2. Calcul de l’épaisseur de la zone endommagée par la corrosion intergranulaire... 109
III.2. Validation du protocole ... 111
III.3. Discussion sur le protocole... 115
CHAPITRE V CINETIQUES D’INITIATION ET DE PROPAGATION DE LA CORROSION INTERGRANULAIRE : IDENTIFICATION ET ANALYSE CRITIQUE DES FACTEURS DU PREMIER ORDRE ... 123
I. NATURE CHIMIQUE DU MILIEU AGRESSIF... 125
I.1. En milieu chloruré ... 126
I.1.1. Mécanismes de corrosion intergranulaire en milieu chloruré ... 127
I.1.2. Influence de la teneur en NaCl sur les cinétiques de corrosion intergranulaire ... 132
I.1.2.1. Essais conventionnels d’immersion ... 132
I.1.2.2. Protocole TpC ... 138
I.1.2.3. Comportement aux temps longs ... 141
I.2. En milieu sulfate chloruré... 146
I.2.1. Mécanismes de corrosion intergranulaire en milieu sulfate chloruré... 147
I.2.2. Influence de la teneur en Na2SO4 en milieu chloruré sur les cinétiques de corrosion intergranulaire ... 152
I.2.2.1. Essais conventionnels d’immersion ... 152
I.2.2.2. Protocole TpC ... 155
II. ETAT DE CONTRAINTE (CONTRAINTE EXTERNE) ... 157
II.1. En milieu chloruré ... 158
II.1.1. Mise en évidence de l’effet de la contrainte sur la sensibilité à la corrosion intergranulaire.... 158
II.1.2. Influence de la teneur en NaCl... 165
II.1.3. Effet du niveau de contrainte ... 169
II.2. En milieu sulfate chloruré... 170
II.2.1. Mise en évidence de l’effet de la contrainte sur la sensibilité à la corrosion intergranulaire.... 171
II.2.2. Etude du comportement en milieu NaCl 0,5M + Na2SO4 0,5M en compression ... 176
II.2.2.1. Initiation / propagation... 176
II.2.2.2. Effet du niveau de contrainte ... 180
III. CONCLUSIONS... 183
CHAPITRE VI DISCUSSION... 185
I. MECANISMES DE CORROSION INTERGRANULAIRE... 188
I.1. Initiation de la corrosion intergranulaire... 188
I.2. Propagation de la corrosion intergranulaire... 190
II. IDENTIFICATION DES FACTEURS DE PREMIER ORDRE SUR LES CINETIQUES D’INITIATION ET DE PROPAGATION DE LA CORROSION INTERGRANULAIRE... 194
II.1. Pourquoi tous les joints de grains ne sont-ils pas corrodés ?... 194
II.2. Influence de l’environnement sur la sensibilité à la corrosion intergranulaire... 199
II.3. Contrainte mécanique appliquée et sensibilité à la corrosion intergranulaire ... 201
II.3.1. Analyse des résultats obtenus en milieux contenant uniquement des ions chlorures ... 201
II.3.2. Analyse des résultats obtenus en milieux contenant des ions chlorures et des ions sulfates .... 210
III. CINETIQUES DE PROPAGATION DES DEFAUTS DE CORROSION INTERGRANULAIRE... 211
CONCLUSION GENERALE ... 219
ANNEXES ... 223
RÉFÉRENCES BIBLIOGRAPHIQUES... 237
Introduction
A l’heure où le développement et la conception d’avions dont la teneur en matériaux composites dépasse les 50% (Boeing B787 et Airbus A350) apparaissent comme des enjeux majeurs pour les industriels de l’aéronautique, il n’est pas déraisonnable de continuer à faire progresser la connaissance sur les matériaux métalliques ne serait-ce que parce qu’ils sont présents en forte proportion sur les avions des flottes actuelles. Parmi ces matériaux, les alliages d’aluminium sont très couramment employés compte tenu de leurs bonnes propriétés mécaniques et de leur légèreté. Un avion tel que l’airbus A380 est composé à 61% d’alliages d’aluminium. Cependant ces alliages sont sensibles aux phénomènes de corrosion localisée dans les environnements dans lesquels ils évoluent.
L’approche actuelle utilisée pour traiter les problèmes de corrosion qui apparaissent sur les avions en service est une approche « zéro défaut », c’est-à-dire qu’aucun défaut de corrosion n’est accepté dans la limite de détection des méthodes de contrôles non destructifs actuellement utilisées. Par conséquent, tout défaut de corrosion qui est détecté doit être réparé ou la pièce endommagée doit être remplacée. Cette approche induit des coûts de maintenance voire d’immobilisation au sol très importants. Afin de pallier cette difficulté, deux solutions sont envisagées. La première consiste à travailler sur la mise au point de méthodes de protection infaillibles. Dans la seconde approche, il ne s’agit plus de refuser tout défaut mais d’accepter l’existence des dommages de corrosion en assurant la sécurité des flottes par une parfaite maîtrise de la propagation de ces défauts. Il s’agit donc d’une approche prédictive de la corrosion dans un contexte aux enjeux économiques importants et c’est dans ce cadre-là que s’inscrivent ces travaux de thèse.
Parmi les différents types de corrosion affectant la durabilité des structures réalisées à base d’alliages d’aluminium sur avions, la corrosion intergranulaire apparaît clairement comme un processus du premier ordre. Il semble donc impératif de disposer de lois de propagation des défauts de corrosion intergranulaire pour ces matériaux. Dans le cadre de ces travaux de thèse, l’alliage étudié est l’alliage d’aluminium 2024, traditionnellement utilisé pour le fuselage des avions civils. Le succès de cette démarche repose sur une première étape
décisive qui consiste à identifier les facteurs du premier ordre contrôlant les cinétiques d’initiation et de propagation des défauts de corrosion intergranulaire. C’est cette étape là qui a fait l’objet de ce travail de thèse ; l’objectif est donc ici de répertorier les facteurs clés contrôlant ce mécanisme d’endommagement et d’analyser précisément leurs influences sur les cinétiques d’initiation et de propagation de la corrosion intergranulaire.
La démarche adoptée a d’abord consisté à caractériser de manière très détaillée les défauts de corrosion intergranulaire. On s’est ensuite interrogé sur l’influence des paramètres environnementaux sur la sensibilité de l’alliage 2024 à cette forme de corrosion. Pour cela des essais d’immersion dans différents milieux contenant des ions chlorures en concentrations variables avec ou sans ions sulfates ont été réalisés. L’étape suivante a consisté à analyser l’influence de l’état de contrainte local sur les cinétiques d’initiation et de propagation des défauts de corrosion intergranulaire en relation avec l’application d’une contrainte mécanique.
L’ensemble des résultats obtenus a permis de proposer un mécanisme pour expliquer les étapes d’initiation et de propagation de la corrosion intergranulaire. De la même façon, des lois de propagation des défauts de corrosion intergranulaire ont été écrites en milieu contenant des ions chlorures pour une structure en l’absence de tout effort appliqué.
Ainsi, ce mémoire de thèse s’articule autour de six chapitres :
- Le premier chapitre présente une synthèse bibliographique concernant l’alliage 2024 et son comportement à la corrosion intergranulaire. Une revue des mécanismes de corrosion intergranulaire de l’alliage 2024 est proposée.
Ensuite, l’influence de paramètres tels que l’état métallurgique du matériau et la composition chimique du milieu agressif sur la sensibilité à la corrosion intergranulaire est abordée. La même démarche est reprise concernant la sensibilité à la corrosion intergranulaire sous contrainte de l’alliage 2024. Un dernier paragraphe s’intéresse à la modélisation des cinétiques de corrosion intergranulaire et de corrosion intergranulaire sous contrainte.
- Le chapitre II est consacré à la description des méthodes et des conditions expérimentales mises en œuvre dans ce travail pour l’étude du comportement à la corrosion mais également pour la caractérisation de l’état métallurgique de l’alliage et la corrélation état métallurgique / corrosion.
- Une caractérisation de la macrostructure et de la microstructure du matériau est présentée dans le chapitre III. Les principales propriétés mécaniques sont également reportées.
- Le chapitre IV présente une étude de la sensibilité à la corrosion intergranulaire de l’alliage 2024 en milieu chloruré réalisée à l’aide d’essais électrochimiques et d’essais conventionnels d’immersion. Ces derniers présentant de grosses lacunes, on s’est ensuite attaché à décrire et à valider un nouveau protocole de caractérisation de la corrosion intergranulaire.
- L’influence des paramètres environnementaux (nature du milieu agressif) et de l’état de contrainte sur les cinétiques d’initiation et de propagation de la corrosion intergranulaire est analysée dans le chapitre V.
- Enfin, dans le dernier chapitre, un mécanisme est proposé à la lumière des résultats obtenus pour expliquer l’endommagement en corrosion intergranulaire et les facteurs du premier ordre sont clairement identifiés. Des lois de propagation des défauts de corrosion intergranulaire sont ensuite proposées.
I. ALLIAGE ENAW2024T351: MICROSTRUCTURE ET PROPRIETES MECANIQUES... 11
I.1. Les alliages d'aluminium Al-Cu... 12
I.1.1. Propriétés générales... 13
I.1.2. Durcissement structural ... 13
I.2. L'alliage d'aluminium 2024 T351 ... 14
I.2.1. Microstructure de l'alliage ... 15
I.2.2. Propriétés mécaniques... 18
II. COMPORTEMENT EN CORROSION DE L'ALLIAGE AA2024T351... 19
II.1. Corrosion des alliages d'aluminium ... 19
II.1.1. Eléments de base... 19
II.1.2. Les diverses formes de corrosion des alliages d'aluminium ... 22
II.2. La corrosion intergranulaire ... 25
II.2.1. Mécanismes de corrosion intergranulaire... 25
II.2.2. Paramètres influençant la sensibilité à la corrosion intergranulaire... 28
II.2.2.1. Espèces chimiques présentes dans le milieu ... 29
II.2.2.2. Précipitation aux joints de grains ... 31
II.2.2.3. Orientation des grains ... 32
II.2.3. Propriétés mécaniques résiduelles du matériau corrodé ... 34
II.3. La corrosion intergranulaire sous contrainte... 36
II.3.1. Mécanismes de corrosion intergranulaire sous contrainte... 37
II.3.1.1. La propagation électrochimique... 37
II.3.1.2. La fragilisation par hydrogène ... 40
II.3.2. Paramètres influençant la sensibilité à la corrosion intergranulaire sous contrainte... 40
II.3.2.1. Espèces chimiques présentes dans le milieu ... 41
II.3.2.2. Nature et niveau de contrainte ... 41
II.4. Etude des cinétiques de propagation des défauts de corrosion ... 44
II.4.1. Corrosion intergranulaire ... 44
II.4.2. Corrosion intergranulaire sous contrainte... 46
II.4.3. Modélisation des cinétiques ... 50
III. CONCLUSION... 51
Le but de cette étude étant de déterminer les cinétiques de propagation de la corrosion intergranulaire dans l'alliage 2024 T351, le premier chapitre vise à atteindre trois objectifs : tout d’abord, présenter les alliages d'aluminium en général et plus particulièrement le matériau de l'étude, à savoir, l'alliage 2024 T351. En effet, il apparaît important de préciser les propriétés microstructurales mais également mécaniques du matériau de manière à déterminer leur rôle dans le comportement à la corrosion et notamment à la corrosion localisée (corrosion intergranulaire et corrosion intergranulaire sous contrainte) de l'alliage. Une seconde partie est consacrée aux mécanismes de corrosion des alliages d'aluminium et aux facteurs influençant leurs cinétiques. Enfin, une dernière partie présente les moyens utilisés dans la littérature dans ce type d’étude, ainsi qu’une revue des résultats obtenus.
I. Alliage EN AW 2024 T351 : microstructure et propriétés mécaniques
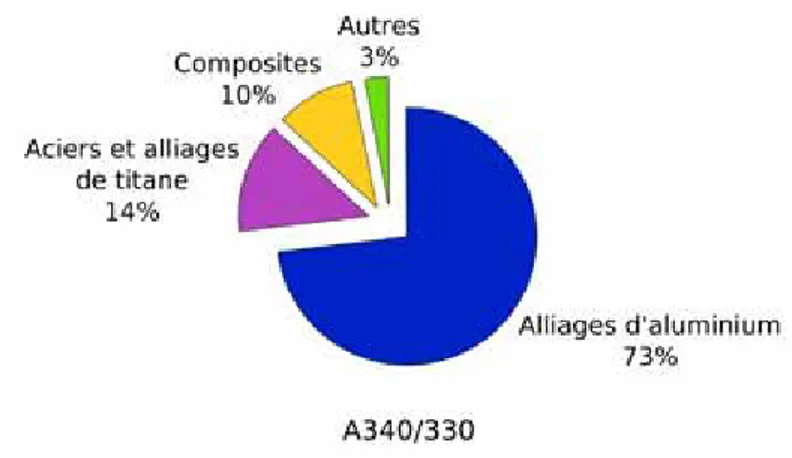
L'aluminium est le second métal le plus utilisé à travers le monde du fait notamment de sa légèreté ainsi que de sa très bonne tenue à la corrosion dans de nombreux milieux. Il fait en effet partie des matériaux les plus légers avec une masse volumique de 2700 kg.dm-3. Cette propriété fait de l'aluminium et de ses alliages des matériaux très plébiscités dans le milieu aéronautique et plus particulièrement dans la conception des avions (à hauteur de 73% sur l'A340 comme indiqué dans la Figure I-1).
Figure I-1 : Proportions des différents matériaux utilisés dans la conception des avions Airbus A340/330
Afin d'améliorer certaines propriétés comme les propriétés mécaniques, l'aptitude à la mise en forme ou la soudabilité, différents alliages d'aluminium ont été développés. La
désignation de l'alliage dépend de l'élément d'alliage principal. Les différents alliages d'aluminium de corroyage peuvent être divisés en deux groupes distincts :
− les alliages à durcissement par écrouissage qui subissent plusieurs étapes de mise en forme à chaud et éventuellement à froid, associées à des recuits intermédiaires ou finaux.
Série Eléments d’alliage
1000 Al ∼99%
3000 Al-Mn 5000 Al-Mg
8000 Al – autres éléments que Cu, Mn, Si, Mg et Zn
− les alliages à durcissement structural (traitement thermique présenté dans le paragraphe I.1.2).
Série Eléments d’alliage
2000 Al-Cu et Al-Cu-Mg
6000 Al-Mg-Si
7000 Al-Zn-Mg et Al-Zn-Mg-Cu
Il existe également des alliages de fonderie comme les alliages de la série 4000 (Al- Si).
I.1. Les alliages d'aluminium Al-Cu
L'addition de Cu en tant qu’élément d'alliage principal est liée à la recherche de meilleures propriétés mécaniques pour les alliages d'aluminium. En effet, cela permet la précipitation d'une phase durcissante améliorant ainsi les propriétés mécaniques générales de l'alliage tout en gardant un matériau relativement léger. En revanche, du fait de cette composition chimique et de la microstructure associée notamment, les alliages d'aluminium de la série 2xxx présentent traditionnellement une résistance à la corrosion relativement faible comparativement à celle de l'aluminium pur.
I.1.1. Propriétés générales
Les alliages Al-Cu de la série 2xxx peuvent être classés en plusieurs familles suivant leur utilisation. Les alliages pour déformation plastique prennent en compte les alliages possédant une bonne résistance à la corrosion, une bonne aptitude à la mise en forme par emboutissage et au soudage (ex. l'alliage 2117 2,2-3% Cu et 0,2-0,5% Mg, % en poids). Les alliages à résistance mécanique élevée qui contiennent un pourcentage de cuivre de l'ordre de 4% sont caractérisés par une bonne tenue à chaud mais une soudabilité et une tenue à la corrosion faible. Parmi ces alliages, l'alliage 2024 est utilisé dans des applications concernant les transports aéronautiques et la mécanique. La dernière famille est celle des alliages pour décolletage. Pour cette application, des additions de bismuth et/ou plomb sont effectuées pour obtenir des copeaux cassants.
I.1.2. Durcissement structural
Le durcissement structural des alliages Al-Cu permettant d'augmenter les propriétés mécaniques du matériau est obtenu par un traitement se divisant en trois étapes [Dub91]:
− dans un premier temps, l'alliage est porté à une température supérieure à la température de solvus pendant une durée suffisante pour atteindre l'équilibre thermodynamique et donc obtenir une mise en solution totale des atomes de soluté ;
− ensuite, l'opération de trempe (refroidissement rapide de l'alliage) empêche la décomposition de la solution solide avec formation de précipités d'équilibre grossiers. On obtient une solution solide sursaturée en soluté où les atomes de soluté sont positionnés de manière aléatoire aux nœuds du réseau à faces cubiques centrées de l'aluminium (on parle alors de solution solide de substitution) ;
− Après la trempe, lorsqu'un maintien en température est réalisé, un important durcissement de l'alliage est observé. Cette étape est appelée étape de revenu.
Le durcissement obtenu est fonction du temps et de la température de maintien.
C'est un phénomène de précipitation résultant de la décomposition de la solution solide sursaturée au cours du maintien isotherme qui est à l'origine du durcissement de l'alliage.
Ce traitement permet la formation de précipités appelés précipités durcissants qui se forment soit pendant la trempe à l'eau, soit lors du traitement de revenu de manière contrôlée.
Cependant, deux autres classes de particules intermétalliques peuvent être observées et distinguées en fonction de leur mode de formation, car les alliages contiennent un nombre important d'éléments d'alliages (ajoutés volontairement afin de modifier certaines propriétés du matériau) ou d'impuretés :
− les dispersoïdes qui se forment par précipitation à l'état solide. Une fois formées, ces particules ne peuvent pas être complètement dissoutes mais leur fraction volumique, leur taille ainsi que leur distribution peuvent être modifiées par des traitements thermomécaniques ;
− les particules intermétalliques grossières : les impuretés (comme le fer et le silicium) présentes dans tous les alliages commerciaux sont au départ dans la solution liquide mais elles vont se combiner avec d'autres éléments et se séparer lors de la solidification pour former des particules grossières intermétalliques. Elles peuvent être cassées lors des traitements thermiques mais ne peuvent pas être remises en solution.
I.2. L'alliage d'aluminium 2024 T351
L'alliage 2024 est un alliage dont les principaux éléments d'alliage sont le cuivre et le magnésium. Sa composition chimique est présentée dans le Tableau I.1:
% (en masse) Al Cu Mg Mn Fe Si
2024 Base 4,4 1,5 0,6 0,2 0,1
Tableau I.1 : Composition chimique (% massique) de l’alliage 2024
Le traitement thermique T351 correspond à une mise en solution à 495°C (+/- 5°C), une trempe à l’eau, des déformations plastiques (allongement par traction de l'ordre de 1 à 2
%) afin d'augmenter le nombre de germes de précipités durcissants et d'entraîner une relaxation des contraintes, et pour finir, un traitement de revenu de quatre jours à 25°C. La Figure I-2 présente l'effet d'un revenu à température ambiante (maturation) à différentes températures proches de l'ambiante sur le durcissement d'un alliage Al-Cu-Mg.
Figure I-2 : Durcissement de l’alliage Al-Cu-Mg (4% Cu) pour des températures proches de l’ambiante (maturation) [Bar97b]
Après quatre jours à température ambiante (25°C), l’alliage a quasiment atteint son maximum de durcissement.
I.2.1. Microstructure de l'alliage
Comme cela a déjà été écrit précédemment, le cuivre est ajouté à l'aluminium de manière à obtenir une phase durcissante et par conséquent de meilleures propriétés mécaniques. L'addition de magnésium à l'alliage Al-Cu entraîne également une augmentation significative des propriétés mécaniques de l'alliage lors de l'étape de maturation. L'addition de silicium et de manganèse favorise la formation de composés quaternaires. Par dispersion, ces derniers améliorent les propriétés de la matrice.
La plupart des alliages industriels Al-Cu-Mg, y compris l'alliage 2024, contiennent un excès de cuivre par rapport à la coupe quasi binaire Al-Al2CuMg (les alliages dont le rapport des teneurs en cuivre et en magnésium est de 2,2 appartiennent au système approximativement quasi binaire Al-Al2CuMg). La Figure I-3 présente une partie du diagramme ternaire Al-Cu-Mg.
Figure I-3 : Diagramme ternaire Al-Cu-Mg [ASM73]
L'alliage 2024 T351 présente donc, suite au traitement de durcissement structural, une séquence de coprécipitation mixte [Dub91] :
Les zones GP, dites de Guinier-Preston, sont composées de disques plans parallèles aux plans (100) de la matrice. La phase θ’’ est une phase cohérente avec la matrice et qui précipite sous forme de plaquettes parallèles aux plans {100} de la matrice. La phase θ’ est une phase semi- cohérente avec la matrice précipitant également sous forme de plaquettes. La phase θ est le composé d'équilibre Al2Cu, qui est totalement incohérent avec la matrice. L'alliage tend toujours vers l'état d'équilibre mais, suivant le traitement de revenu, la décomposition est plus ou moins complexe. Pour une température de revenu inférieure à 200°C, la décomposition de la solution solide sursaturée s'arrête à θ’’ ou θ’; pour des températures supérieures, on peut obtenir directement θ’. Lors d'un traitement de maturation à température ambiante, on n'obtient que les zones GP.
La présence de 1,5% de Mg dans l’alliage induit la précipitation de nouvelles phases.
Les zones GPB (Guinier-Preston-Bagaryatsky), appelées ainsi pour les différencier des zones GP, correspondent à un arrangement à courte distance d'atomes de Cu et Mg. Les phases S'' et S' sont des phases de transition respectivement cohérente et semi-cohérente avec la matrice (S'' n’est pas indiquée dans la séquence de précipitation car son existence même est sujette à
Solution Solide zones GP θ’’ θ’ θ Al2Cu zones GPB S’ S Al2CuMg alliage 2024
controverse). La phase S ou Al2CuMg est une phase à l'équilibre, incohérente avec la matrice et qui précipite sous forme de plaquettes.
Dans une étude sur les phénomènes de dissolution associés aux particules de phase S, Buchheit et al. [Buc97] mentionnent l’absence de particules de phase θ dans l'alliage 2024 T3. Il est précisé que pour les alliages ayant des compositions chimiques similaires à celles de l'alliage 2024, la formation de phase θ au cours de la solidification ou du traitement thermique est possible. En outre, le rapport des phases θ et S est très faible dans les alliages Al-Cu-Mg lorsque le rapport des concentrations Cu:Mg est compris entre 4:1 et 1,5:1 (dans le cas de l'alliage 2024, le rapport Cu:Mg est compris entre 4:1 et 2:1). Il est aussi intéressant de constater que de nombreux articles ne mentionnent pas de séquence de coprécipitation mais uniquement une séquence de précipitation Al2CuMg [Wan07, Gao07].
Compte tenu des traitements thermo-mécaniques subis par le matériau, il existe d'autres phases présentes dans l'alliage et observables à différentes échelles.
A l'échelle du microscope optique, il est possible d'observer les particules intermétalliques grossières. L'alliage 2024 contient des particules plutôt sphériques riches en Cu et en Mg qui correspondent à la phase S ou Al2CuMg. Elles ont une taille moyenne de l'ordre de 5 µm. On peut également observer des particules de forme irrégulière riches en Cu, Fe et Mn. Ces particules ont une taille moyenne de 30 µm et occupent une fraction surfacique de 2,8% alors que la fraction surfacique couverte par les particules Al2CuMg n'est que de 1%
environ [Gui98b]. Dans le cadre d'une étude de la corrosion par piqûres sur l'alliage 2024 T3 à l'aide de l'analyse "nuclear microprobe", Boag et al. [Boa05] ont confirmé la présence de particules intermétalliques du type Al-Cu-Mn-Fe avec une taille moyenne de 20 µm, et de particules de type Al2CuMg de taille inférieure aux précédentes.
De plus, les travaux réalisés par Buchheit et al. [Buc97] ont montré la présence de 61.3% de Al2CuMg (phase S), 12.3% de Al6(Cu,Fe,Mn), 5.2% de Al7Cu2Fe et 4.3% de (Al,Cu)6Mn dans l'alliage 2024 (en termes de fraction surfacique couverte par les particules intermétalliques). Cependant, 17% de phases intermétalliques restent inclassables. Cet article met également en évidence l'absence d'une zone appauvrie en Cu autour des particules de phase S.
En outre, on note la présence de dispersoïdes en plaquettes Al20Mn3Cu dont la taille moyenne est d'environ 200 nm. Ces dispersoïdes ont une distribution homogène dans la matrice et sont présents au niveau des joints de grains. Néanmoins, le voisinage des particules intermétalliques grossières est dépourvu de dispersoïdes. Cette zone sans dispersoïde est appelée « precipitate free zone » ou PFZ. Des analyses EDX ont montré que cette zone contenait 10 à 20% de Cu en moins que le reste de la matrice [Gui98b].
Dans une étude portant sur les relations existant entre la corrosion par piqûres et la corrosion intergranulaire de l'alliage 2024, Zhang et Frankel [Zha03a] ont réalisé une caractérisation microstructurale de l'alliage à l’état T3. La microscopie électronique en transmission (MET) révèle la présence de précipités durcissants de phases GP et S' dans l'alliage 2024 T3. Il révèle également la présence de particules en forme de baguettes contenant Al, Cu et Mn (probablement Al3Mn20Cu2) dans les grains. De nombreuses particules en forme de bâtonnets ont été identifiées au niveau des joints de grains. Après caractérisation EDS (spectroscopie dispersive en énergie), il s'avère que ces particules ont différentes compositions chimiques : Al2Cu (concentration en Mg très faible), Al2CuMg ou Al3Mn20Cu2 (sans Mg). Les particules riches en Cu et Mn sont introduites dans le matériau afin de contrôler la recristallisation ainsi que la croissance des grains. Quelques particules Al- Cu-Mn-Fe ont également été identifiées au niveau des joints de grains. Cependant, les auteurs n'ont pas observé de PFZ le long des joints de grains, c'est-à-dire la présence d'une zone dépourvue de précipités et appauvrie en Cu du fait de la précipitation de particules riches en Cu aux joints de grains.
I.2.2. Propriétés mécaniques
L'alliage 2024 T351 possède de meilleures propriétés mécaniques que l'aluminium pur mais nettement inférieures à celles de certains aciers. Il présente également une bonne ténacité et une bonne résistance à la propagation des criques. A l'état T351, ses principales applications concernent la construction aéronautique. Le Tableau I.2 référence les valeurs des principales propriétés mécaniques de l'alliage 2024 T351 [Dev92].
Alliage Etat Rm (MPa)
Rp0,2 (MPa)
A (%)
Dureté (HB)
2024 T351 470 325 20 120
Tableau I.2 : Propriétés mécaniques typiques de l'alliage 2024 (Rm, Rp0,2 et A sont des données obtenues à l’aide d’essais de traction)
Etant donné la présence de nombreuses particules secondaires, la rupture d’un alliage d’aluminium sain est de type ductile avec la formation de cavités [Kob00].
II. Comportement en corrosion de l'alliage AA2024 T351
Bien que largement utilisés dans le secteur aéronautique du fait de leurs bonnes propriétés mécaniques, les alliages d'aluminium des séries 2xxx et plus largement l’aluminium et ses alliages sont sensibles à différents types de corrosion généralisée et localisée. Ces phénomènes de corrosion sont dus notamment à la présence de particules riches en Cu pour ce qui concerne les alliages de la série 2xxx. La sensibilité à la corrosion d'un alliage n'est pas un critère dimensionnant mais est prédominant dans le choix du matériau.
II.1. Corrosion des alliages d'aluminium II.1.1. Eléments de base
De manière générale, la corrosion de l'aluminium en milieu aqueux se traduit par la somme d'une demi-réaction électrochimique d'oxydation et d'une demi-réaction électrochimique de réduction, telles que :
Al Al3+ + 3e- 3H+ + 3e- 3/2 H2
_________________
Al + 3H+ Al3+ + 3/2 H2
ou bien
Al + 3H2O Al(OH)3 + 3/2 H2
Le diagramme de Pourbaix de l’aluminium dans l’eau présenté sur la Figure I-4 définit les domaines de stabilité en fonction du pH et du potentiel.
Figure I-4 : Diagramme de Pourbaix E-pH de l’aluminium dans l’eau chimiquement pure à 25°C [Var04]
Ce diagramme illustre la nature amphotère de l’aluminium : il est attaqué aussi bien en milieu acide qu’en milieu basique. Pour des milieux avec un pH proche de la neutralité (de 4 à 9), l’aluminium est passif c’est-à-dire qu’un film insoluble d’oxyde ou d’hydroxyde s’est formé à sa surface. Ce dernier influence le comportement électrochimique de l’aluminium et gouverne sa résistance à la corrosion. Le paragraphe qui suit décrit la formation et la nature de ce film passif.
Il est bien connu que l'aluminium est un métal réactif qui forme facilement une couche d’alumine Al2O3 à l’air et un film d’hydroxyde lorsqu'il est exposé à un milieu aqueux à température ambiante [Mos87]. Le film d’oxyde naturel est composé de deux couches dont l’épaisseur totale est comprise entre 4 et 10 nm [Var04] (Figure I-5) :
− la première couche compacte et amorphe est appelée couche barrière à cause de ses propriétés diélectriques. Elle se forme en quelques millisecondes quelle que soit la température, à partir du moment où le métal est en contact avec le milieu oxydant ou l’air ; la température joue un rôle sur l’épaisseur finale ;
− la seconde couche croît sur la première en réagissant avec l’environnement extérieur. L’épaisseur finale de cette couche, poreuse et moins compacte que la couche barrière, ne sera pas atteinte avant des semaines voire des mois, en fonction des conditions physico-chimiques. De plus, elle réagit avec l’environnement extérieur au cours des différentes étapes de mise en forme du matériau ou pendant son service formant ainsi une couche de contamination superficielle. La composition de la surface est donc complexe.
Figure I-5 : Couches et phénomènes d’adsorption du film d’oxyde [Var04]
Lors d’un contact prolongé avec l’eau, la couche externe croît et se transforme en bayérite ou böhmite en fonction de la température du milieu. Le Tableau I.3 présente les propriétés de ces deux formes de l’oxyde d’aluminium.
Espèce Structure cristalline
Formule chimique
Température de formation (°C)
Densité
Alumine amorphe Al2O3 <50-60 3,40
Bayérite Monoclinique α-Al(OH)3 60-90 2,53
Böhmite Orthorhombique γ-AlOOH >90 3,01
Tableau I.3 : Modifications allotropiques de l’alumine [Var04]
Il convient de noter qu’en plus de l’aluminium, les alliages contiennent des impuretés et des éléments d’addition en solution solide et sous forme de composés intermétalliques. Les éléments plus nobles que l’aluminium comme le cuivre vont s’accumuler à l’interface métal/oxyde au cours de l’oxydation. Ils ne passeront dans l’oxyde qu’au-delà d’un certain seuil variable en fonction de l’élément considéré [Reb05].
En outre, en ce qui concerne le comportement à la corrosion, les hétérogénéités de la surface vont localiser l’adsorption des ions Cl- sur la surface du film [Szk99]. La présence de particules à la surface du matériau peut engendrer la formation de défauts dans le film passif lors des étapes de mise en forme pouvant faciliter sa rupture (défauts dus à la différence de ductilité entre la matrice et les particules) [Var04]. On notera également que, au vu des
différences de densité de l’alumine (3,4) avec l’aluminium sous-jacent, le film d’oxyde se trouve en compression (il peut donc supporter des déformations sans se rompre).
II.1.2. Les diverses formes de corrosion des alliages d'aluminium
Malgré son aptitude à la passivité, l’aluminium (et ses alliages) est sensible à la corrosion. Les diverses formes de corrosion localisée peuvent être classées en trois groupes selon qu’elles sont liées à des hétérogénéités intervenant au niveau :
− du milieu : un effet de couplage galvanique se produit lorsqu’il y a une variation locale de composition du milieu ;
− des conditions physico-chimiques à l’interface : corrosion par crevasse ;
− du matériau : corrosion galvanique, corrosion intergranulaire et corrosion par piqûres.
De manière générale, il n’existe pas de forme de corrosion spécifique de l’aluminium ou de ses alliages. La prépondérance d’un certain type de corrosion dépendra des propriétés du métal, du milieu et des conditions d’utilisation. Cependant, la présence d’espèces agressives spécifiques (au-delà d’une concentration limite) est nécessaire tels que les ions halogénures et plus particulièrement les ions chlorures (agressivité plus élevée que celles des bromures et des iodures).
Deux grandes formes de corrosion peuvent être distinguées : la corrosion généralisée et la corrosion localisée. La corrosion généralisée (ou uniforme) se traduit par une diminution uniforme et régulière d’épaisseur de toute la surface.
Le paragraphe suivant énumère les principales formes de corrosion localisée des alliages d’aluminium et en rappelle les principales caractéristiques. La corrosion intergranulaire ainsi que la corrosion sous contrainte seront détaillées dans les paragraphes II.2 et II.3.
La corrosion par piqûres : l’aluminium et ses alliages sont sensibles à la corrosion par piqûres dans les milieux dont le pH est proche de la neutralité (milieux naturels tels que l’eau de mer). Cette forme de corrosion se développe suivant une phase d’amorçage pendant laquelle les ions Cl- sont adsorbés dans le film d’oxyde entraînant sa rupture aux points faibles. A l’endroit des ruptures du film, il y a oxydation rapide de l’aluminium et formation
d’un complexe chloruré intermédiaire AlCl4-
. Une partie des piqûres initiées va se propager grâce à deux réactions électrochimiques d’oxydation et de réduction. La formation d’ions OH- ou la consommation d’ions H+ va modifier le pH vers un pH alcalin. En fond de piqûre, la dissolution de l’aluminium sous forme d’ions Al3+ crée un champ électrique qui déplace des ions Cl- vers le fond de la piqûre. Ces ions neutralisent chimiquement la solution et forment des chlorures d’aluminium. L’hydrolyse des chlorures d’aluminium AlCl4- provoque une acidification du fond de piqûre à pH < 3 causant l’auto-propagation de la piqûre. En diffusant vers l’ouverture de la piqûre, les ions Al3+ vont rencontrer un milieu de plus en plus alcalin et vont précipiter sous forme d’hydroxyde Al(OH)3. Les microbulles d’hydrogène produites par la réaction de réduction des ions H+ poussent l’hydroxyde vers l’ouverture de la piqûre où il se dépose. La Figure I-6 décrit les mécanismes mis en jeu lors des phénomènes de corrosion par piqûres dans les alliages d’aluminium.
Figure I-6 : Mécanismes de corrosion par piqûres des alliages d’aluminium [Var04]
L’accumulation des produits de corrosion en surface peut obstruer l’ouverture de la piqûre et ainsi ralentir ou arrêter le processus. La corrosion par piqûres peut être caractérisée par trois paramètres principaux à savoir la densité de piqûres par unité de surface, la vitesse de propagation et la probabilité de piqûres.
La corrosion galvanique se produit lorsque deux métaux différents sont en contact électrique dans le même milieu électrolytique engendrant la formation d’un couple galvanique.
La corrosion caverneuse se développe dans des interstices, des zones de recoin où le matériau est localement en contact avec un milieu corrosif confiné. La modification locale du milieu entraîne la création de piles de concentrations et de couplage galvanique entre l’extérieur et l’intérieur de la caverne.
La corrosion filiforme s’initie au niveau des défauts d’un revêtement puis se propage à l’interface métal/revêtement (peinture par exemple) en formant de fins filaments.
La corrosion intergranulaire est une forme de corrosion qui se propage dans le métal en consommant uniquement les zones associées aux joints de grains. Elle peut être liée à la structure atomique et à la composition des joints de grains en l’absence de précipitation (corrosion intergranulaire hors précipitation) ou à la décoration des joints de grains par une précipitation (corrosion intergranulaire liée à la précipitation d’une seconde phase). Les alliages de la série 2xxx sont plus particulièrement sensibles à ce dernier type de corrosion.
La corrosion exfoliante ou feuilletante est une forme de corrosion intergranulaire se propageant suivant une multitude de plans parallèles à la direction de transformation. Des feuillets de métal inattaqués très minces subsistent entre ces plans et sont repoussés par le gonflement des produits de corrosion et s’écartent de la surface du métal comme les feuilles d’un livre.
La corrosion sous contrainte : elle résulte de l'action conjuguée d'une contrainte mécanique (résiduelle ou appliquée) et d'un milieu agressif vis-à-vis du matériau, chacun de ces facteurs pris séparément n'étant pas susceptible à lui seul d'endommager la structure.
L’alliage 2024 T351 est un alliage sensible à la corrosion localisée et notamment la corrosion intergranulaire et la corrosion sous contrainte, de par sa microstructure mais également de par son histoire thermomécanique, le premier paramètre dépendant d’ailleurs étroitement du second. Les paragraphes II.2 et II.3 détaillent ces deux derniers phénomènes.
II.2. La corrosion intergranulaire
La corrosion intergranulaire consomme très peu de métal, c’est pourquoi, contrairement à la corrosion par piqûres mais surtout à la corrosion transgranulaire, l’étude de la perte de masse n’est pas un paramètre approprié pour ce type de corrosion [Var04]. La corrosion intergranulaire n’est pas observable à l’œil mais avec un microscope optique.
II.2.1. Mécanismes de corrosion intergranulaire
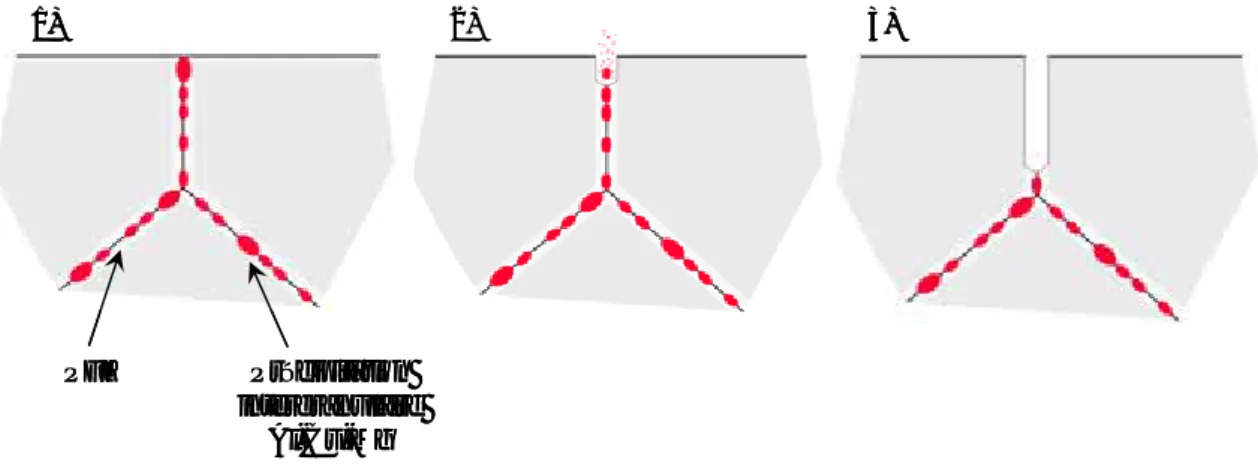
Dans la littérature, de nombreux ouvrages abordent les mécanismes de corrosion localisée et notamment de la corrosion intergranulaire sur l’alliage 2024. De manière générale, il est admis que la corrosion intergranulaire de l’alliage 2024 T351 est en partie due à la précipitation intergranulaire riche en cuivre et à la présence d’une zone appauvrie en cuivre adjacente à ces joints de grains (Figure I-7 schéma 1). Cette zone appauvrie en cuivre est anodique vis-à-vis de la matrice mais également des précipités intergranulaires Al-Cu-Mg.
Cette différence de potentiel va entraîner la dissolution de la matrice adjacente aux joints de grains ; s’en suit une dissolution préférentielle en Al et Mg des précipités intergranulaires comme le montre le schéma 2. Les précipités se trouvent donc enrichis en cuivre et sont alors cathodiques vis-à-vis de la matrice entraînant la dissolution de la matrice adjacente aux joints de grains (schéma 3). La corrosion intergranulaire se propage ensuite grâce à la présence d’un chemin anodique préférentiel.
Précipitation intergranulaire
Al-Cu-Mg PFZ
1) 2) 3)
Précipitation intergranulaire
Al-Cu-Mg PFZ
1) 2) 3)
Figure I-7 : Schémas présentant les principaux mécanismes de corrosion intergranulaire de l’alliage 2024
La suite de ce paragraphe est consacrée à une revue plus détaillée des mécanismes d’initiation et de propagation de la corrosion intergranulaire de l’alliage 2024 T351. Dans les années 1970, Galvele et DeMicheli écrivaient que l’initiation de la corrosion intergranulaire des alliages Al-Cu n’était pas due à une différence de potentiels entre les joints de grains et les grains mais à une différence de potentiels de rupture entre ces deux phases [Gal70]. Par définition, les potentiels de rupture sont reliés à la réactivité des différentes phases métalliques présentes dans l’alliage.
Par la suite, dans leurs travaux, Guillaumin et al. [Gui98a] ont étudié le comportement électrochimique de l’alliage 2024 en milieu NaCl 1M et interprété les courbes de polarisation potentiocinétique tracées dans ce milieu afin de déterminer les mécanismes de corrosion localisée (corrosion par piqûres et corrosion intergranulaire) rencontrés dans cet alliage (Figure I-8).
Figure I-8 : Courbe de polarisation potentiocinétique de l’alliage 2024 T351 dans une solution de NaCl 1M [Gui98a]
Sur cette figure, on note la présence de deux potentiels de rupture : Eb1 à -720mV (le plus actif) et Eb2 à -620mV (le plus noble).
Une dissolution de la matrice adjacente aux particules de phase S est observée pour des potentiels inférieurs à Eb1. Pour expliquer ce résultat, Guillaumin se réfère à la microstructure de l’alliage 2024. Dans ce matériau, la précipitation des dispersoïdes Al20Mn3Cu entraîne un appauvrissement en Cu de l’ensemble de la matrice. De même, quand les précipités riches en Cu de type Al2CuMg vont précipiter et croître, cela entraîne un appauvrissement en Cu localisé au niveau de la matrice adjacente au précipité. Ainsi, les dispersoïdes ne vont pas précipiter dans cette zone appauvrie en Cu et on observe alors autour
des particules Al2CuMg une zone dépourvue de dispersoïdes que l’on appelle PFZ (Precipitate Free Zone). Cette zone a un potentiel moins noble vis-à-vis de la particule S mais également du reste de la matrice. On peut donc avoir deux types de couplages galvaniques : un couplage entre les précipités S et la PFZ adjacente à ces précipités et un couplage entre la PFZ et le reste de la matrice. La PFZ adjacente aux particules S est donc très réactive du fait de ces couplages galvaniques. On observe alors une dissolution de la matrice adjacente aux particules de phase S pour un potentiel inférieur à Eb1. Les particules restent quant à elles intactes. Ces résultats sont confirmés par Zhang et Frankel [Zha03a] en milieu NaCl 1M désaéré à l’argon.
Le premier potentiel de rupture Eb1 s’explique par une réaction de dissolution des particules intermétalliques grossières Al2CuMg qui présentent alors pour certaines une structure poreuse (Figure I-9).
Figure I-9 : Particules de phase S après polarisation potentiocinétique de -900 à -690 mV/ECS, potentiel maintenu pendant 5 minutes [Gui98a]
Pour Guillaumin et al. [Gui98a], une dissolution préférentielle du Mg contenu dans les particules se produit conduisant à un enrichissement en Cu de ces particules. D’autres auteurs [Dim99, Buc97] ont émis une autre hypothèse concernant l’enrichissement en Cu : il y aurait dissolution de la particule avec redéposition du Cu au niveau de la particule et aux alentours de celle-ci. Dans tous les cas, l’enrichissement en Cu des particules S, suite à leur dissolution, accentue le couplage galvanique entre la particule et la matrice adjacente. On notera que la dissolution préférentielle de Mg des particules de phase S est un fait établi [Li05] mais que l’enrichissement en Cu de la particule et de ses alentours est un phénomène faisant l’objet de nombreux articles [Dim99]. De plus, des résultats ont montré que les différences de comportement électrochimique entre la matrice d’aluminium et les particules intermétalliques