Publisher’s version / Version de l'éditeur:
Annales du Bâtiment et des Travaux Publics, Juin 3, pp. 41-51, 2001-06-01
READ THESE TERMS AND CONDITIONS CAREFULLY BEFORE USING THIS WEBSITE. https://nrc-publications.canada.ca/eng/copyright
Vous avez des questions? Nous pouvons vous aider. Pour communiquer directement avec un auteur, consultez la première page de la revue dans laquelle son article a été publié afin de trouver ses coordonnées. Si vous n’arrivez pas à les repérer, communiquez avec nous à PublicationsArchive-ArchivesPublications@nrc-cnrc.gc.ca.
Questions? Contact the NRC Publications Archive team at
PublicationsArchive-ArchivesPublications@nrc-cnrc.gc.ca. If you wish to email the authors directly, please see the first page of the publication for their contact information.
NRC Publications Archive
Archives des publications du CNRC
This publication could be one of several versions: author’s original, accepted manuscript or the publisher’s version. / La version de cette publication peut être l’une des suivantes : la version prépublication de l’auteur, la version acceptée du manuscrit ou la version de l’éditeur.
Access and use of this website and the material on it are subject to the Terms and Conditions set forth at
Étude de la lixiviation des matériaux cimentaires avec ou sans fillers
calcaires
Catinaud, S.; Beaudoin, J. J.; Marchand, J.
https://publications-cnrc.canada.ca/fra/droits
L’accès à ce site Web et l’utilisation de son contenu sont assujettis aux conditions présentées dans le site LISEZ CES CONDITIONS ATTENTIVEMENT AVANT D’UTILISER CE SITE WEB.
NRC Publications Record / Notice d'Archives des publications de CNRC:
https://nrc-publications.canada.ca/eng/view/object/?id=6904fba8-5971-433a-b8dd-65d6a6d36862
https://publications-cnrc.canada.ca/fra/voir/objet/?id=6904fba8-5971-433a-b8dd-65d6a6d36862
http://www.nrc-cnrc.gc.ca/irc
Étude de la lixiviation des matériaux ciment aires avec ou sans fillers
calcaires
N R C C - 4 5 0 1 6
C a t i n a u d , S . ; B e a u d o i n , J . J . ; M a r c h a n d , J .
J u n e 2 0 0 1
A version of this document is published in / Une version de ce document se trouve dans:
Annales du Bâtiment et des Travaux Publics,
(3), Juin, pp. 41-51, June 01, 2001
The material in this document is covered by the provisions of the Copyright Act, by Canadian laws, policies, regulations and international agreements. Such provisions serve to identify the information source and, in specific instances, to prohibit reproduction of materials without written permission.
For more information visit http://laws.justice.gc.ca/en/showtdm/cs/C-42
Les renseignements dans ce document sont protégés par la Loi sur le droit d'auteur, par les lois, les politiques et les règlements du Canada et des accords internationaux. Ces dispositions permettent d'identifier la source de l'information et, dans certains cas, d'interdire la copie de documents sans permission écrite. Pour obtenir de plus amples renseignements : http://lois.justice.gc.ca/fr/showtdm/cs/C-42
セ
ETUDE DE LA LIXIVIATION
セ
DES MATERIAUX CIMENTAIRES
AVEC OU SANS FILLERS CALCAIRES
S. CATINAUD"', J.J. BEAUDOIN", J. MARCHAND'
I
LMSC, IUP Genie Civil et Infrastructures, Neuville-sur-Oise
2
CRIB - Departement de Genie Civil, Universire laval, Quebec (Canada)
3
Institut de Recherche en Construction, CNRC, Onawa (Conadal
INTRODUCTION
L
e tenne fillers serefere a
des particules (ajouteesa
unliant) obtenues par broyage fin ou concassage de
roches. Dans certains pays, ce type d'additions est utilise depuis des d6cennies comme remplacement d'nne partie
du ciment. Les fillers calcaires sont generalement addi-tionnes au moment de la production du ciment. Les
recherches
Menees
sur I'influence de I'utilisation de fillerscalcaires sur les proprietes des materiaux cimentaires ont
mantre que leur action est premierement due
a
un effet
'" physique [1]. Cepenrlant, I'existence de
reactions avec les
phases contenant des aluminates dans les materiaux cimen-taires a clairementetlS demontree {2]. De fines particules
[セA[Z
calcaires ont aussi ete utilisees en tant que remplacement: W:,de gypse pour les ciments Portland [3], Le fait que l'utili-';1,:',,sation de fillers calcaires puisse acceIerer l'hydratation des ·.';;:silicates de calcium anhydres presents dans Ie ciment a etc
c\tnis en evidence {4].
ZセZーオエゥャゥウ。エゥッョ de fillers calcaires conduit
a
des produits qui "5.oot des proprietes mecaniques acceptables {I, 5].セセセGオエゥャゥウ。エゥッョ
de ce type d'additions a un effet benefique surZIセウ proprietes rMologiques
[n
Les elfets positifs peuyentGセセーャゥアオ・イ pourquoi des reglementations
a
travers Ie mondeセョエ pennis son utilisation. Les norrn,es europeennes autori-Jnt entre 0 et 35 % d'additions calcaires. Des debats sur la ustification de l'utilisation de fillers calcaires dans les
IN 2001
materiaux cimentaires existent cependant dans d'autres pays comme aux Etats-Unis.
Les cas pratiquesOll les structures en beton sont au contact de solutions salines agressives sont courants. Les cot1ts considerables engendres par la maintenance et la repara-tion d'ouvrages degrades expliquent l'interet apporte
a
la durabilite des materiaux cimentaires. L'etude de l'in-fluence du contact avec des eaux moins agressives (situa-tions de stockages de dechets nucleaires) presente egalement un interet. En general lorsqu'une attaque 」ィゥセmique de la pate de ciment hydrate survient, la decalcifi-cation de la matrice se produit. Les mecanismes de decalcification induisent la dissolution des cristaux d'hy· droxyde de calcium Ca(OHh et la dissolution partielle des C-S-H (Ia phase liante) [6, 7, 8, 9, 10],
Les mecanismes de decalcification
a
la fois de l'hydroxyde de calcium et des C-S-H ont ete demierement beaucoup etudies [6, 7, 8, 9, 10]. En effet de nombreuses etudes s'in-teressent par exemple aux consequences du contact de materiaux cimentaires avec de l'eau distillee. L'eau、ゥウエゥャセlee est en effet la solution la plus simple (pas d'ions」ィャッイセ
ou sulfate) qui induise la dissolution de la matrice」ゥュ・ョセN
taire. Plusieurs techniques ont ete mises au point pour accelerer les cinetiques de degradation [6, 10, 11, 12J, Les donnees soulignent l'effet nefaste de la decalcification sur les proprietes mecaniques des materiaux cimentaires [6, 7, 8,9, 10, 11, 12, 13J,
Le cas sp6cifique de l'utilisation des fillers calcaires et son
influence sur la durabilit6 n' a pas ettS largement etudi6.
L'6valuation de I'effel
benefique
ounefaste
de l'utilisationde carbonate de calcium (Ie principal composant des fillers calcaires) sur la decalcification, et nne
reflexion
sur les、ゥヲセferents phenomenes qui surviennent semblent ponvoir apporter des elements supplementairespOUfla
comprehen-sion des attaques chimiques sur de tels
systemes.
Les resultalsde l'investigation sur l'influence de
l'utilisa-tion de fillers calcaires sur les mecamsmes de
decalcifica-tion sont presentes. Quatre principaux systemes (C3S,
C3S+C3A+CaS04.2H,O, C3S+C4AF+CaS04.2H,O et
ciment Portland) prepares avec divers pourcentages de
car-bonate de calcium (0, 5, 10 et 20
%)ont
a
cette fin ete
hydrates et testes. Cette etude fait partie d'un programme de recherche global portant sur la comprehension de la durabilite des materiaux cimentaires exposes
a
des solu-tions salines.ESSAIS EXPERIMENTAUX
Materiaux et preparation des melanges
Les surfaces specifiques des C3S, C3A, C"AF et CaC03
utilises dans cette etude valent respectivement 3000,3010, 3060 et 4600 cm2/g. L'addition calcaire utilisee, sous fonne
de calcite, contient plus de 99 % de CaC03. La composiR
エゥッセGZセ|j」ゥエョ・ョエ Portland ordinaire utilise, type 10 selon la n [ZセGmセLエLゥッョ canadienne, est donnee dans Ie tableauI.
セQセセセhーイ・セセョエ・
l"s
」。イセ」エ・イゥウエゥアオ・ウdes 16 differents
セウゥYセ|YセエセエセrXセヲBBエゥッョョ・ウN
Les pates ont ete
pre-セアセxセpbセエエセセwウッャゥ、・
de 0,5. De l'eau distillee a
HS,6e;,"L'
hydratation a eu lieu dans des cylindres deplejdglass soigneusement scelles mis en rotation conti-nl1ellependant les premieres 24 heures. Apres Ie demouR
lage, des echantillons de I nun d'epaisseur ant ete scies et places dans une eau saturee en chaux pendant au moins plusieurs semaines. Les pates hydratees des trois premiers
types de melanges (C3S, C3S+C3A+CaS04.2H20 et
ciment Portland) ont subi une cure d'au minimum six
mois. Les pates composees de C3S+C4AF+CaS04·2H,O
CaCD3sont restees quatre semaines en solution saturee en
chaux.
Caracterisatian de Vetat initial
des materiaux
•
A la fin de la periode de cure les caracteristiques micro-structurales des differents materiaux ont ete mises en 6viR
dence. Des analyses thennogravimetriques menees sur un thennogravimetre Du Pont 951 ant e16 conduites entre 20 et lOOO°C,
a
un taux de chauffage de lOoC/min aftn d'eva-luer la quantite d'eau non evaporable par unite de masse de solide initiale (autre que CaC03). Pour cela, environ 25 mg de materiau broye etseeM
SallSvide a 105°C pendant trois heures ont ete utilises.Les resultats de ces analyses sont resumes dans Ie tableau III. Les donnees presentees dans la colonne de droite correspondent a une estimation du degre d'hydrata-tion des pates en supposant que 0,25 g d'eau sont neces-saires pour hydrater completement 1 g (sans considerer Ie CaC03) de chacon des systemes anhydres et en se basant sur les quantites d'eau non evaporable mesurees.Letemps de cure r6duit pour les pates du systeme contenant du C4AF peut expliquer les valeurs mains importantes obte-nues dans ce casRlao
Des analyses de diffraction des rayons X et enthalpiques differentielles ant aussi ete conduites sur les echantillons en fin de periode de cure afin de caracteriser egalement l'etat initial avant toute degradation. Les analyses enthal-piques differentielles ant ete menees sur un systeme Du Pont en utilisant environ 20 mg de materiau seebe sous videa lO5°C pendant trois heures et broye. Un taux de chauffage de lOoC/min dans one atmosphere d'azote, jus-qu'a une temperature finale de 600°C a etc utilise pour les analyses. Un appareil Rigaku Geigerflux オエゥャゥセ⦅。ョエ des radiations au cuivre a servi aux analyses de diffracUon des rayons X. Le diametre de la majorite des particules broyees etait compris entre 3 et 6 l-tm au entre 6
a
12 !lm. L'important nombre d'analyses de diffraction des rayons X a pennis de mettre en evidence des tendances grossieresTABLEAU I : Analyse chimique et composition en terme de phases du ciment utilise.
TABLEAU II : Compo.i60n en unilll de moss. de 10 por6. sollde de. melong•• contenont C
%de CoCo.
II•• val.urs d. C
%.onl 0,5 10 ou 20),
TABLEAU III : Quann"d'eou non 'voporable de. dive" mohl,ioux el dog,' d'hydratolion corre.pondant.
TABLEAU IV : Composition des diverse5 pcites d'apres les analyses thermiques ef DRX,
au A repre.ente Co4A1203(C0310,sIOHj.l , .5H20
etBCo4A1206C03.' 1H20.
TABLEAU V: Volumetotol de pore. el volume de pore. donI Ie diom_1re est plu. potil que SOnm
!%to,5
%1.
sur les variations des quantitesde phases dans les mate-"riaux, Les mentions qui sont faites sur les intensit6s de pies
sont caracteristiques des observations. Elies ne sont pas qualitatives. La vitesse de scan choisie 6taitde 56/min. Les ,echantillons
utilises,
enlevesde la solution,etaientbroyesdans un mortier avec Ie volume minimal d'eau distillee
necessaire
a
un broyage aise. Ainsi les phenomenesd'eva-セ[juin 2001
poration et de carbonatationetaient minimises, Les
com-positions des pates des differents systemes d6duites des
resultats conjoints des analyses thenniques et de
diffrac-tion des rayons X sont synthetisees dans Ie tableau IV. La mise en evidence de CaC03 dans les echantillons de mate-riaux ne contenant pas d'addition de carbonate de calcium provient d'un phenomene de carbonatation.
43
I
"I' 1.;
ijJ
., 25 ....セ]]]]BGセ
...,..
セ
'"
....-t..
!=< 20 '.i," .セ
1 1 - - - - -_ _.
•
.." , .
•
'#.
セ
15{]]]Z]Z]]]]]Z[]B]BセBNZZBNZBNZBNZNセBNセBNセBNセBセBNセBNセ
T
..
セBN]
...
=
...
=
..=
...=
...=
...
]MセNBL
:2
10-+-
C,So
..
C,S+C,A+Gypse23
5
,.
,....
Ciment Portland
-0- cSセGゥ|AcTafKNgケーウ・ 10%deCaC0
3 20 15composition des materiaux (dissolution de phases solid apparition de complexes ou de produits bien cristall' Les procedures suivies sont les m8mes que celles dec' prec6demment, lars de la description de la caracterisatio initiale des materiaux dans leur etat de reference en fin periode de cure et avant immersion, Les analyses ont faites sur des echantillons taus d'epaisseur 1 rom, Des mesures de changement de longueur ont ete menees de petits echantillons (environ 5x25,5xlnnn). Un exlemio' metre optique de Tuckennan a servi
a
lire des variations longueur avec une precision de 2,1Q-6 mm1mm [14J, Quelques observations sur un microscope electronique balayage Cambridge Stereoscan 8250 equipe d'un metre a dispersion d' energie des rayons X ant e16 Les echantillons ont ete seches sous videa
environ 60°C pendant plusieurs heures avant d'8tre metallises avec de l'or.Dissolution de I'hydroxyde de calcium
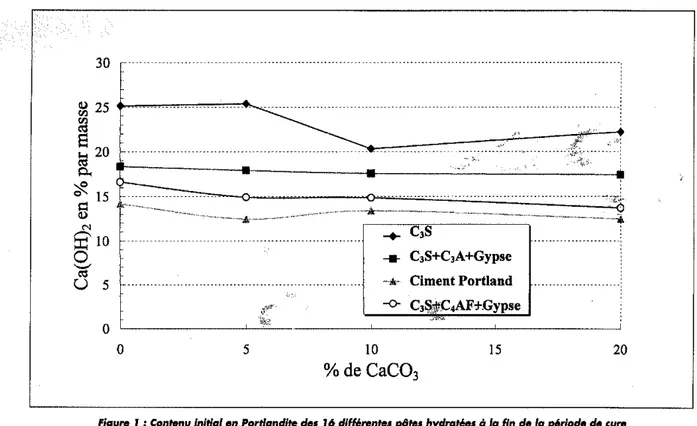
Les pourcentages massiques d'hydroxyde de calcium ini-tialement present dans les diverses pates hydratees sont presentes sur la figure 1,
Ces valeurs ont ete obtenues d'apres les analyses thenno-gravimetriques. Pour une composition donnee, Ie pourcen-tage present est fonction en partie du degre d'hydratation du materiau (voir Tableau III). Pour une masse equivalente
RESULTATS
5
o
o
30
A la fin de la periode de cure, des echantillons scies、G・ョセ
viron 1 mm d'epaisseuront ete immerges dans de I'eau dis-tillee. Des soins particuliers ont ete apportes a I'utilisation de volumes importants de solution en comparaison avec la masse d'echantillon immerge. Puisque Ie rapport volume de solution/volume de l'echantillon etait suffisamment important, les solutions n'ont pas ete renouvelees.
Immersion en eau distillee
Procedures experimentales
Afin d'obtenir les distributions en tailles des pores des dif-fe-rents mate-riaux, un porosimetre a mercure (de la compa-gnie American Instruments) a ete utilise. Les intrusions se sont faites a des pressions allant jusqu'a 387 MPa, Les echantillons etaient secMs sous vide a 105°C pendant trois heures avant la mesure. Le tableau V presente pour chacun des 16 differents materiaux la valeur de porosite totale airtsi que Ie pourcentage volumique de pores dont Ie dia-metre est plus bas que 50nm. L'addition de CaC03 contri-bue a augmenter la porosite totale, notamment par Ie biais d'une augmentation des pores dont Ie diametre est plus important que 50nm.
Les cinetiques de degradation ant ete estimees d'apres des mesures varices effectuees apres des periodes de 10, 20, 40 et 90 jours d'immersion, Des analyses de diffraction des rayons X et des analyses enthalpiques differentielles ont e16 effectuees pour determiner toute modification de la
Figure 1 : Cantenu initial enPartiandite,de. 16 dillerente. piite. hydra• •
a
10 lin de 10 periode de Cure.tovont/limmer.ian en eau di.tilliHJ.
"
de materiau initiale (solide+'eatl)" les differences des contenus en moles de calciurilpr6sentes, dependant de la nature du materiau, peuvent egaIeJrie:hi expliquer les diffcM rences observees entre les divers <systenies.
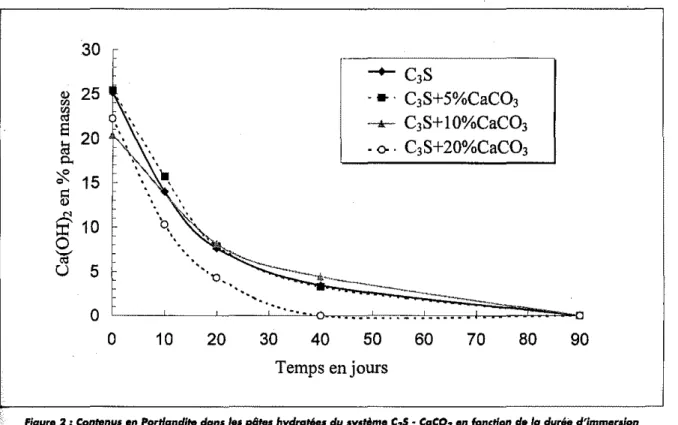
Le taux de dissolution de l'hydtoxyde de calcium dans les pates
a
base de C3S n'est pasiIlfluehce deヲ。セッョ importante par Ie contenu en CaC03 (figllre2). Ced est realise sur toute la periode qui a etc necessaire pour atteindte la dis-solution complete de tout l'hydroxyde de calcium initiale-ment present. Le tanx de dissolution de la portlandite est par contre acceIere par la presence de CaC03 pour les pates contenant du C3S, C3A et gypse. La distinction entre les pates avec ou sans addition est nette apres 10 jours d'immersion en eau distillee. Durant les 40 premiers jours d'immersion, Ie tanx initial de dissolution est similaire pour les echantillons contenant 5 ou 20 % de CaC03. Par contre apres 40 jours d'immersion, l'utilisation de 20%
d'addition a accelere deヲ。セッョ significative ce taux. Les pates preparees
a
partir du dment Portland ordinaire ont subi une dissolution de la Portlanditea
un taux en fonc-tion du temps bien mains important. Durant les 10 pre-miers jours d'immersion; la presence de carbonate de calcium ne semble pas avoir d'influence. Par la suite, Ie taux de dissolution estャ」Nセァ・イ・ュ・ョエ augmente dans Ie cas de l'utilisation de CaC03.La dissolution tatale de la Portiandite a ete observee apres une periode d'immersion de 20 jours seulement pour les pates contenant du C3S, C4AF et gypse. Ceci correspond
a
un taux de dissolution particulierement significatif. Dne parosite globalement plus importante de ces pates et des
diffusions d'ions plus rapides
a
travers elles peuvent expliM quer one part de ce constat.Les taux de dissolution durant les dix premiers jours d'im-mersion pour un materiau contenant un pourcentage donne de carhonate de calcium sont ordonnes de fat;on croissante pour les pMes de ciment, de C,S+C,A+gypse, de C,S et enfin de C,S+C4AF+gypse.
Formation additionnelle de calcite
Lecontenu en calcite a
e16
estime quaHtativement d'apres les analyses DRX. Des estimations quantitatives predses n'ont pu etre realisees puisque l'utilisation d'etalon n'a pas ete employee. Cependant Ie nombre important d'analyses ont pennis d'avoir une idee du contenu approximatif de calcite presente.Les analyses DRX conduites sur les pates avant toute immersion en eau distillee d6rnontrent une augmentation la plus significative avec Ie pourcentage de CaC03 utilise dans Ie cas des pates du systeme C3S - CaC03. L'intensit6 du pic principal de la calcite dans les echantillons des pates de C,S-CaCO, vaut ainsi 87, 197, 387 et 647 pour respec-tivement, 0, 5 10 ou 20 % de CaC03. Pour les pates des autres systemes, la difference des intensites des pics de cal-citepOUfles pates incorporant0,5ou10% d'addition est moins importante, les intensites restant dans un meme ordre de grandeur. Cette observation peut etre en partie explicable par Ie fait que ces pates contiennent des。ャオュゥセ
nates, qui peuvent reagir directement avec Ie carbonate de calcium ajoute.
2001
Figure 2 : Contenus en Portlandite dansI••p8tes hydl'Gt8es du system. C"s • CaC03 en fonction d. la dum d'immersion
en ecrudistill...
4S
90
80
70
60
-+- C
3S
- •. C
3S+5%CaC0
3 --&-C
3S+10%CaC0
3 - 0-.C
3S+20%CaC0
350
40
Temps enjours
30
",.
'.'..
20
10
30
.,
25
'"'"
oj8 20
a
Q.,'$.
15
[J
N@'
10
'<a'
u
5
0
0
Phases AFm et AFt
iセセj[ZァLセセG[ZGセセZ
pourcentage de carbonate de calciumi ies pAtes dll systeme C3S+C3A+Gypse - CaCO,
22 18
,.
29 10jours 10 22 • 18contiennent environ 2,5 fois plus de moles d'aluminate que de sulfate (sur la base d'une marne masse de solide, non hydrate, et d'eau). Dne meme caracteristique existe pour les pAtes
a
base de C3S+C4AF+Gypse - CaC03. Cependant la difference entre les contenus en aluminate et sulfate est moins importante (rapport de 1,8). Le contenu en moles de sulfate est plus important que celui des aluminates pour les pates de ciment (rapport de 1,1). La phase AFro (monosul-foaluminate de calcium hydrate) a un ratio molaire alumi-nate/sulfate plus important que celui de la phase AFt correspondante (Ettringite).Les notations A et B sur les figures 3 et 4 se referent res-pectiveroent, comme dans Ie tableau IV,
a
l'hemicarbo-aluminate de calcium hydrate et au monocarbol'hemicarbo-aluminate de calcium hydrate. Les analyses pour les pates de C3S+C,A+Gypse contenant 10 et20% de CaC03 otaient similaires. La merne remarque peut etre faite pour les pates de ciment contenant 5 et 10 % de CaC03.En presencede CaC03, la presence de
monosulfoalumi-nate de calcium hydrate n' a pas ete mise en evidence dans les pates de reference contenant du C3A, C3S et du gypse. De l'Ettringite, de l'hemicarboaluminate (en quantite faible) .et du monocarboaluminate de calcium hydrate etaient par contre presents (tableau IV). Les echantillons ne contenant pas d'addition de CaC03 ont subi de la car-bonatation (intensite accrue des pies representatifs de la presence de calcite sur les graphes des analyses DRX) durant l'immersion en eau distillee. Le roonosulfolaumi-nate de calcium hydrate non seuleroent subsiste mais sa quantite croit dans les echantillons immerges en eau distil-lee. Les formations d'hemicarboaluminate et de
monocar-,.
29 10 22 • 18,.
29ANNALES DU BATIMENT ET DES TRAVAUX PUBLICS 10
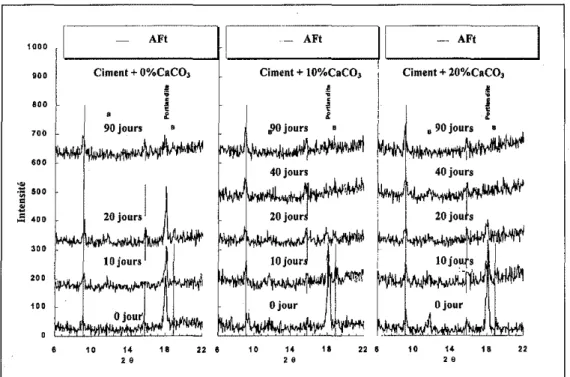
Figure3 : Analyse.DRX.surI•• pate, d.cSsKcセKァケーN・ (Ontendnt0, 5 e; 20%tI. CaC03
"pre.
diffe,.",.. periode. d'lmmer,lon en .au di,till••.L..-.-:-'
MセBa⦅Gf⦅ュ⦅N
MMMZ]M]セ
ャNNNNNZ」ZM]MZM]⦅a⦅fセエ
=:-:::::-1
L . . . I⦅セ
_ _A_F_t _ cSsKcセKgケーウ・KoEc。cPS cSsKcセKgケーウ・KUEc。cPSZ cSsKcセKgケーウ・KRPEc。cojI
700 300 800 900 600 200 100 1000'.
0-;; 500i
... 400Les pAtes du systeme C3S - CaC03 subissent les pius importantes formations de nouvelle calcite pendantl'ゥュセ
mersion en eau disti1l6e. La calcite suppIementaire apparait
principalement pendant les 20 premiersjauIsd'immersion en eau distillee. Ce systeme correspond
a
la plusimpor-tantequantitede Ca(OH)z presente qui· puissereagiravec Ie CO2 pour fonner par carbonatation de la calcite
(figure 1). L'augmentation en terme d'intensit6 de pic de
calcite des analyses DRX ne semble pas influencee de
ヲ。セッョ importante par Ie pourcentage d'addition
utilisee.
Pour les autres
pates
des autressystemes,
la formation de nouvelle calcite semble etre accrue lorsque Ie pourcentage utilise d'additionde carbonate de calcium augmente. Lesdifferences sont particulierement importantes entre les
pates ne contenant pas ou contenant 5 % d'addition. Dans Ie cas des pates des systemes C3S+C3A+gypse -CaC03 et ciment - -CaC03 la formation de nouvelle calcite intervient durant toute la periode d'immersion. Pour les pAtes du systeme C3S+C4AF+gypse - CaCO,. une aug-mentation significative intervient durant les 20 premiers jonrs d'immersion. Les taux de dissolution de la Portlandite et Ie taux de formation de nouvelle calcite pourraient donc atre eventuellement relies. Pour les pates sans addition, la presence d'aluminates dans Ie materiau peut egalement influer sur les quantites de calcite formee durant l'immersion dans de l'eau distillee.
boaluminate de」。ャ」ゥオュィケ」エイセHVゥHIGセヲVエV 6galement obser-v6es d' apres les analysesjAIャャ_Gエ」ZZセエ|・ observation suggere que !'immersion dans deイセセ|ャ、jAエuャV・ヲ。カッイゥウ・ la libera-tion de plus d'aluminate,Cela:,peut:8tre du
a
unchange-ment desolubilite des phases,:s>base'd'aluminate due en partie
a
nne diminution de<la,concentration en calciumdans la solution. En presence demonosulfoaluminate de
calcium hydrate, de l'hemkarboaluminate de calcium
hydrate se forme plutot que du monocarboaluminate de calcium hydrate. L'inverse semble se produire quand de }'Ettringite plutot que du
monosulfoaluminate
de calcium hydrat6 est present (voir tableau IV). los piltesa
base deciment et CaC03 ne subissent pas de formation significa-tive de monocarboaluminate de calcium hydrate. Le
contenu en Ettringite semble croftre Iegerement durant
l'
immersion en eau
distillee.Les piltes de C3S+C"AF+Gypse-CaC03 (dans leur etat de reference) eontlennent de I'Bttringite, dans un degnS limite. L'imrnersion en eau distillee ne modifie pas ce fait. Cependant, meme si Ie rapport aluminate/sulfate duュ。エ・セ
dan est important, une quantite significative de C4AF non hydrate subsiste (visible d'apres les analysesDRX),due
a
un degre d'hydratation limite de ces pfttes. L'hydratation du C4AF est plus lente que celle du C3A. La considerationdu rapport molaire aluminate/sulfate disponibles (pour nSagir) semble plus appropriee que celle du rapport molaire aluminate/sulfate reel comrne mentionne par Kuzel [15]. La presence de carbonate de calCiumempeche laエイ。ョウヲッイセ
mation d'Ettringite en monosulfoaluminate de calcium hydrate
a
cause de la fonnation de carboaluminates [16]. Cependant, ceci semble s' appliquer pour une certaine gamme de rapports aluminate/sulfate. Les contenus enmonosulfoaluminate et carboaluminate de calcium hydrate augmentent quand la pftte est immergee en eau distillee. Cependant, les quantites d'aluminate et de sulfate restent sensiblement identiques lors de l'utilisation de CaC03 aux divers pourcentages. II apparait done que non seulement Ie rapport molaire des ces deux especes ioniques estゥューッイセ
tant, mais qu'egalement la nature et Ie moment ou apparait une fonne de carbonate de calcium dans Ie mareriau sont importants.
La fonne que revet Ie carbonate lorsqu'un materiau cimen-taire subit de la carbonatation depend du temps ecoule depuis Ie debut de la carbonatation, du degre de」。イ「ッョ。エ。セ
tion et de la presence ou del'absence de Portlandite dans Ie mareriau [17]. Si ce produit n'est pas present, du mono-carboaluminate et de la calcite sont formes ウオ」」・ウウゥカ・セ
ment. Sinon, de I'hemicarboaluminate de calcium hydrate apparait avant Ie monocarboaluminate. L'hemicarbo-alumnate de calcium hydrate pourrait etre instable lorsque la concentration en calcium en solution diminue.
Cette hypothese expliquerait pourquoi du monocarbo-aluminate de calcium hydrate apparait dans la pftte de C3S, C3A et gypse (sans addition de CaCO,) lorsque la Portlandite a totalement disparue (figure 3). Dans Ie cas de l'addition de carbonatedecalcium, Ie contenu deュッョッセ
carboaluminate (et de I'hemicarboaluminate de calcium hydrate pour Ia pftte contenant 5 % de CaC03) augmente puis decroit des que Ia Portlandite est totalement dissoute. Le meme phenomene semble exister pour la pftte de ciment contenant20%de CaC03 (figure 4). Dans ces cas, Oll la presence d'Ettringite ne se materialise pas par des quanti-tes tres importanquanti-tes, de I'aluminate doit doucetre libere en solution. La dissolution du carboalumiuate de calcium
1 A_F_'_ _
-1
c....
-_A_F_'_ _--III
-_-_A_F' _Figure4t AnQly••• DRX ...ur I....
"a""
d. elment Portland confenant01 10.t 20%de CaC03apmdiHerentesperiod.s dlimmers10n entHlUdistille..
47
22 18"
20 10 22 •"
"
20J'O
jours 10 22 • 18"
20 90 jours Ciment+O%CaC03 10 "0 300'"
'"
,,'
100 '00 1000 セj
$00 ,5 400hydrate peut correspondre
a
la formation de nouvelle」。ャセcite, qui ne se forme pas
a
partir d'une reaction avec Ie CO2atmospherique mais qui provient d'une transformation de produit et qui ramene finalement de la calcite initialement additionnee sous sa forme originelle. Cela peut expliquer pourquoi, meme si Ie processus de carbonatation est simi· laire pour les differentes pates, I' augmentation de calcite presente dans les echantillons est d'autant plus importante lors de l'immersion dans de l'eau distillee que la pate contient plus d'addition de CaC0310rs de sa preparation.
Mesures de changements de longueur
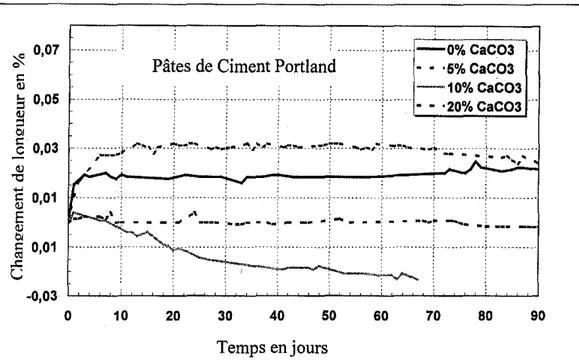
Les mesures de changements de longueur observes sur des echantillons des differentes pates immerges en eau distillee sont presentees sur les figures 5a
a
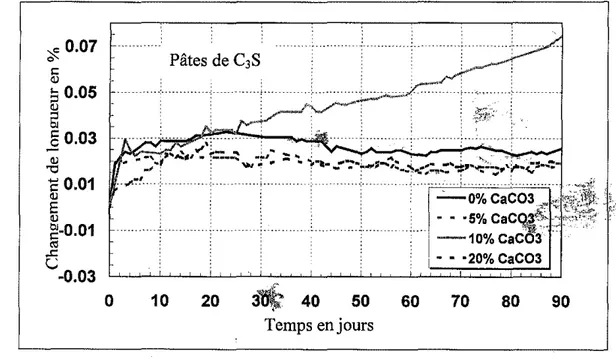
5d. Chaque figure illustre pour un type donne de pAte, l'influence deャG。、、ゥセtion de CaC03. La figure 5a montre que la superposition des phenomenes de decalcification et de carbonatation conduit
a
une expansion globale des pates decSsセc。cPSGLe processus de carbonatation n'a jamais ete associe
a
un phenomene d'expansion, La decalcification de l'hy-droxyde de calcium et des C-S-H peut cependant corresw pondre a de I'expansion. Excepte pour la pate contenant 10 % de CaC03, l'expansion est rapidement stabilisee apres environ 12 jours d'immersion. La valeur finale de l'expansion subite decroit 16gerement avec l'utilisation de CaC03 dans Ie materiau.Les pates du systeme ciment Portland.CaC03 (excepte
pour la pate contenant 10 % de CaC03) demontrent Ie meme type de comportement, 」G・ウエセ。キ、ゥイ・ une expansion initiale suivie par une stabilisation (figure 5b). La pate contenant 10 % de CaC03 subit une faible expansion lors de l'immersion a proprement parler, suivie par un retrait continuo Cependant, l'amplitude de l'expansion ァャッ「。ャ・セ
ment subie apres stabilisation depend largement du centage de CaC03 utilise dans Ie materiau,
Les changements de longueur des echantillons des pates de C,S+C,A ou C.,AF+gypse-CaCO, n'ont pas Ole enregis. tres sur des periodes d'immersion aussi importantes. Cependant, on note que Ie taux d'expansion est toujours significatif apres 40 jours d'immersion pour la pate de C,S+C,A+Gypse sans CaCO,.
Vne comparaison des courbes correspondant
a
I'utilisation de 10 % de CaCO, des figures 5aa
5c revele un compor-tement particulier. En effet, Ie taux d'expansion pOUf ces pates reste significatif durant tout Ie temps de l'immersion. Les courbes enregistrees pour les autres materiaux ne pos-sedent pas la m€me particularite. Les observations au M.E,B. sur ces 6chantillons n'ont pas revele la presence de phases expansives telles que des sulfoaluminate ou carboa-luminate de calcium hydrate.Pour les pates de C,S+C,A+Gypse-CaCO, il apparalt qu'additionner 5 % de CaC03 conduit a l'initiation d'un nouveau phenomene qui se traduit par une augmentation de l' expansion subie en comparaison avec la pate sans addition. L'utilisation de plus de CaC03 conduit par contre a une expansion plus faible. Le pOUfcentage de CaC03 requit pour induire nne diminution d'expansion du mate-riau correspond sans doute
a
un pourcentage situe entre 10 et 20%,La presence ou l'absence des phases AFro or AFt ne sem-blent pas pouvoir apporter une explication singuliereカゥウセ。キ
vis du comportement observe. Cependant, I' ordre de gran· deur des expansions subies par les echantillons des pates decSsKcTafKgケーウ・セ CaC03est plus important que celui des autres piltes. La presence de cセ pourrait done induire un comportement significativement different. La liberation d'energie provenant de la dissolution de phases solides et les perturbations des CwS-H dues aux effets du
Figure 50 : InFluence du (0(03 sur I•• changement. d. longueur d••
pate.
de(35.ANNALES DU BATIMENT ET DESTRAVAUXPUBUCS
::: .... :.
!o
It- - ' , ""'..:,.. !>;..., ..セセM '.ifA'セL '.', .. -, : -":'''"BGNセBNBZB ..."'"
, ...!
I
1
90
80
70
60
-NNLMLLL[セ[G"':"-0% CaC03 __
セL
j,i;:'!".t
- - •5%c。」ョセセセ
<.,QセNZエイイセZ
...._---.,.. セLLGBZM ..".,.... "..1-10%CaC03 ..
I - - -20% CaC03
3,*
40
50
Temps enjours
20
10
o
::s.
0.07
oセ
5
0.05
セ
§
0.03
セ
C 0.01
<1Jセ
セMPNPQ"
C
-0.03
,
j:, 11 'I i'I', I';,
.., ij: I-II
I.f
II
i"If
49
90
90
80
80
.
セ...
...' -...;-
..
70
70
-0%CaC03
•• '5% Cae03
-10%CaC03
- - '20% CaC03
60
-,..
..
....
セ60
.." セ- - - -_ セN-50
50
40
40
Temps en jours
30
3D
Temps enjours
...,
20
20
j :O"C C03
'
,
-
"
a
Pates de Ciment Portland
- •
'5% CaC03
-10%CaC03
..., _, ... • '20%Cae03
10
10
..
.... ···'···C··Figure 5b : Influence au C"C03 sur I•• chttngements de longueur de.
pate.
d. cimenf Pornand.Figure 5c :Inlluenc. duCOC03 .urIe.changementsdelongueurde.
pate.
d.cSsKcセK・[ケーN・N-0,03
o
セ
セ
0,01
セ
§
0,01
15
';f.
0.07
l:'"
!3
0.05
セ
l:0.03
c
'"
'"
+'0.01
l:'"
E
'"
-0.01
OJ§
..<:c.;
-0.03
0
2001Figure 5d : Influence du CQC03 sur les changements de longueur des pates d.cSsKcセfKgケーN・N
I
I
l
90
80
70
60
50
ANNALES DU BATIMENT ET DESTRAVAUXPUBLICS
pour reagir) semble avoir un r6le determinant dans la nature des sulfoaluminates de calcium hydrates fonnes. La presence d'hemicarboaluminate ou de monocarboalumi-nate de calcium hydrate depend respectivement de la for-mation preferentielle du monosulfoaluminate de calcium hydrate ou de l'Ettringite.
Le taux de dissolution de I'hydroxyde de calcium depend largement de la composition de la pate et de ses proprietes de transfert, lieesaux caracteristiques porosimetriques. Pour les pates contenant des aluminates, Ie taux de disso-lution de la Portlandite influence la fonnation de produits
a
base de carbonate. II apparait qui plus est que Ie mono-carboaluminate de calcium hydrate peutセエイ・ reconverti en calcite sans la fonnation additionnelle de sulfoaluminate de calcium hydrate. Durant I' immersion dans de I' eau dis-tillee, des aluminates sont done eventuellement relaches en solution.Les changements de longueur induits par les phenomenes de decalcification et de carbonatation、・ー・ョ、セLャャエ、・ la」ッュセ
position du materiau immerge. DOllze -:des;.,::-quatorze courbes presentees correspondentit.de
ᄋイ・セヲョBGsゥッョN
Cette expansion depend du pourcentage de CaC03 utilise. L'utilisation de C4AF induit des expansions plus imporMtantes. Cependant, dueit.une difference de degre d'hydra-tation de ces pates, la resistance mecanique de ces pates .etait moins developpee. Les trois autres types de pates ont demontre des expansions duュセュ・ ordre de grandeur. La complexite de l'influence du contenu en CaC03 .sur les changements de longueur des pates
a
base de ciment Portland immergees dans de I'eau distillee suggere que la stabilite volumique de ces systemes est la superposition de phenomenes varies. Le comportement des C-S-H dans ce processus doit etre important. Un comportement singulier a ete observe pOUf les pates de C3S, C3S+C3A+gypse et de40
Temps enjours
30
20
10
.-o
t
0.07
ii
a
0.05
セ
§
0.03
セ
セ
0.01
Qli·0.01
Ol..c
(.;.0.03
lessivage pourraient joner un role important sur la stabilite volumique des patesirnmergees dans de l'
eall
distil16e.Ob.ervatlons Ciu
ME8
Aセセセゥセセゥ[セセセ[セ[セbィセゥェエェ||、セs
bnl montre queGpセセセmエ|セpj_セイウN・ョ
solution d'e.u distilleeBLーセLエZエセセ「。N、ッョウ
importantes. Uoe augmentationiosH6
du' materiau
etun
changement defa micro
wstrlJc!ure des cセsm H semblent intervenir. Les diff6rentes
porosites
initiales (tableau V) induisent descaract.eris-tiques mecaniques initiales differentes. Uoe diminution des propri6tesmecaniques est done induiteparl'immersion en eall distillee puisqu' i1 semble que Ia porasite eroit. Des valeurs de resistances differentes des diverses matrices contribuent sans aucun doute aux differences de change-ments de longueur enregistrees. Une expansion plus importante n'induit pas forcement que les contraintes internes crees ontete plus importantes. Cependant, Ie com-portement des pates contenant 10
%
de CaC03 estsingu-lier alors que les caracteristiques porosimetriques ne sont pas systematiquement differentes. Ce1a suggere que la difM
ference des caracteristiques mecaniques dues
a
la presence de CaC03 ne soit pas la sourcea priorides changements de longueur. 11 est evidemment difficile de separer les effets mecaniques et chimiques (toujours interdependants) lorsque les causes des instabilites volumiques sontrecher-chees.
Le rapport molaire aluminate/sulfate introduit dans la pate (correspondant
a
des aluminates et sulfates disponiblesCONCLUSION
ciment contenant 10
%
de CaCO" La possible incorpora-tion de CaCO, au sein des phasesィケ、イ。エセウa
base de sili-cate et Ie degre de reversibilit6 de, ce processus offre unepossible explication アオ。セエ^セGLZjLGZセーセセNセセ」セGLセ・ l' addition de
CaC03 sur la stabilite カッャオュャアセセGZHLゥセウLLGュ。エ・イゥ。オク
cimen-taires inunerges en solution、G・エャNオTゥウセゥQャ・・L
Remerciements
Les auteurs sont reconnaissants au Conseil de Recherches
en Sciences Naturelles et en
Genie
du Canada et augOll-vemement de 1a province de Quebec (Fonds FCAR) pour
leur scutien financier pour ce travail. Ils souhaitent
egale-ment remercierR.E. Myers, G. Chan and G.M. Polomark
pOUf leur aide. Mme
1.
Duchesne, professeur, est aussiremercieepOUfses commentaires avises.
BIBLIOGRAPHIE
[I] Escadeillas G, (1988) Les ciments aux fillers
cal-caires : contribution ii leur optimisation par I'etude
des propriltes mecaniques et physiques des betons
jillhises, these de doctorat, Universite Paul Sabatier,
Toulouse, 144 p.
[2J Klemm W.A., Adams L.D, (1990) An investigation of
the fonnation of carboaluminates, in P. Klieger, D, Hooton (Eds.), Carbonate additions to cement,
SlP1064 ASTM.
[3] Campiteli V,C., Florindo M.e. (1990) The influence
of limestone additions on optimum sulfur trioxide content in Portland cements,in P. Klieger, D, Hooton
(Eds,), Carbonate additions to cement, STPlO64 ASTM.
[4) Ramacbandran V.S" Zhang Chun-Mei (1986)
Influence of CaCOJ on hydration and microstructural characteristics of tricaldum silicate,
n
Cementa 83,p, 139-152,
[5] Soroka L, Setter N, (1977) The effect af fillers on
strength of cement mortars, Cement and Concrete
Researcb, vol. 7, n' 4, p.449-456.
[6] Marchand J., Beaudoin JJ" Pigeon M, (1999)
Influence ofCa(OHh on the propertiesofcement sys-tems,Matenals Science of Concrete - Special Edition,
A, Ceramic, Soc" 12 (sous pressel,
[0 !UP Genie Civil et Infrastructures
Universite de Cergy-Pontoise 5 Mail Gay-Lussac n・オカゥャャ・Mウオイセoゥウ・ 95031 Cergy-Pontoise cedex 01 34256974 01 34256941 ?(Ull
[7] Faucon P, (1997) Durability of concrete:
Physico-chemistry of the degradation induced by pure water,
these de doctorat, Universite de Cergy-Pontoise,
France, 260 p.
[8] Adenot E, Buil,M. (1992) Modelling the corrosion of
the cement paste by deionized water, Cement and
Concrete Research, vol. 22, p, 489-496,
(9) Delagrave A" Gerard B" Marchand J, (1997)
Modeling calcium leaching mechanisms in hydrated cement pastes, in Mechanisms of Chemical Degradation of Cement-Based Systems, E & FN
Spon, p, 38-47.
[10] Feldman R.E, Ramachandran V.S, (1982)
Microstructure of calcium hydroxide depleted cement paste - 1 .' Density and helium flow measurements,
Cement and Concrete Research, vol. 12, p, 179-186. [11] Le Marechal J., Gerard B" Marchand J" Didry 0"
Gagnon J.P. (1998)A new accelerated leaching・クー・セ
riment - The LIFT procedure, ACI Special
Publication SP-179, p. 951-980,
[12] Carde C., Fran,ois R. (1997) Effect of the leaching of
calcium hydroxide from cement paste on the mechani-cal and physimechani-cal properties, Cement and Concrete
Research, vol. 27, p, 539-550,
[13] Bentz D.P., Garboczi E.J, (1992) Modelling the
lea-ching ofcalcium hydroxide from cement paste: Effects on pore space percolation and diffusivity, Materials
and Structures, vol. 25, p. 523-533,
[14) Feldroan R.E, SeredaP., Ramachandran V.S.(1964)A
study of length changes of compacts of Portland cement on exposure to H20, Highway Research
Board 62, p. 106-118.
[15] Kuzel H.-J. (1996) Initial hydration reactions and
mechanisms of delayed ettringite formation in Portland cements,Cement and Concrete Composites,
vol. 18, pp. 195-203,
[16] Sawlez Z" Heng 5.5, (1996) Durability of concrete
with addition of limestone powder, Magazine of
Concrete Research, vol. 48, p, 131-137,
[17] Damidot D., Stronacb 5" Kindness A" Atkins M"
Glasser F.P, (1994) Thermodynamic investigation of
the CaO-Alz0 3-CaCO,-HzO closed system at 25'C
and the influence of Na20, Cement and Concrete
Research, vol. 24, n' 3, p, 563-572,