Transplantation hépatique besoins indications et résultats
Foie;transplantation;greffeI
I. INTRODUCTION
La transplantation hépatique est une intervention chirurgicale qui permet le remplacement d’un foie défaillant, suite à l’insuffisance hépatique, par un autre foie sain.
Les indications de la greffe hépatique sont de plus en plus variées, mais largement dominées par les cirrhoses virales au stade terminal.
Depuis les premières transplantations effectuées dans les années 60 par Thomas Starzl aux USA, le taux de succès est passé de 30% à plus de 70 %. Cette amélioration est due non seulement aux techniques opératoires mais aussi aux progrès réalisés pour la conservation du foie, les critères de sélection du donneur et du receveur et l’utilisation large des immunosuppresseurs.
Le but de ce travail est de déterminer la place de la transplantation hépatique dans le traitement de l’insuffisance hépatocellulaire et le remplacement de certains foies tumoraux. Pour l’évaluation des besoins en greffe et le nombre des candidats potentiels à la transplantation dans notre contexte, nous avons pris à titre d’exemple deux échantillons de patients suivis pour une hépatopathie chronique ou un cancer du foie dans deux services appartenant au CHU Ibn Sina.
A la lumière des données de la littérature nous mettrons le point sur les principales indications de la transplantation, les critères de sélection, le choix et la préparation du donneur et du receveur. Nous rappellerons également les différentes techniques chirurgicales usuelles et les nouvelles acquisitions dans ce domaine.
N
N
o
o
t
t
r
r
e
e
é
é
t
t
u
u
d
d
e
e
II. NOTRE ETUDE:
1- patients et méthodes :
Pour l’évaluation de besoins en transplantation dans notre contexte nous avons pris deux échantillons de malades porteurs d’hépatopathies chroniques ou de cancers du foie suivis dans deux services de médecine différents appartenant au CHU Ibn Sina.
Chez ces malades, nous avons étudié les données cliniques, radiologiques, biologiques et histologiques pour le diagnostic. Nous avons adopté la classification de Child-Pugh pour la stadification des cirrhoses et les critères 5-5 pour la sélection des tumeurs.
2- Résultats :
A. Le premier échantillon :
132 patients cirrhotiques sont suivis dans un service de médecine pendant une période étalée entre 2002 et 2006.
a. Age et sexe :
L’age moyen de ces malades est de 53 ans et demi avec des extrêmes allant de 17 à 90 ans.
54,5% sont de sexe masculin. 45,5% sont de sexe féminin.
b. Types d’hépatopathie sous jacente :
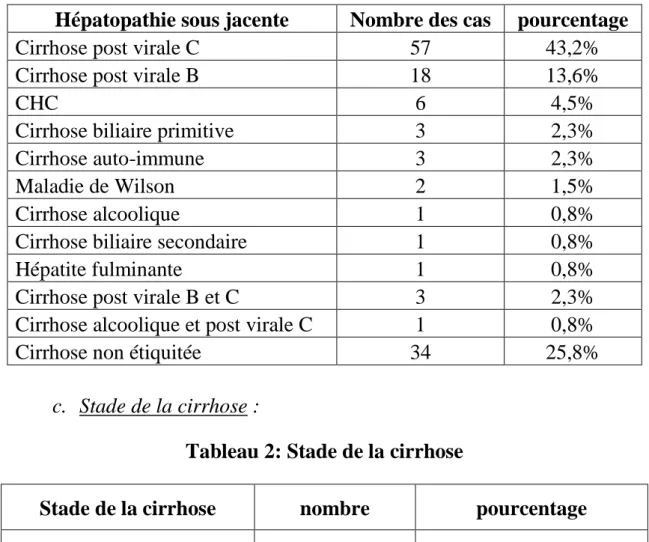
Tableau 1: Types d’hépatopathie sous jacente
Hépatopathie sous jacente Nombre des cas pourcentage
Cirrhose post virale C 57 43,2%
Cirrhose post virale B 18 13,6%
CHC 6 4,5%
Cirrhose biliaire primitive 3 2,3%
Cirrhose auto-immune 3 2,3%
Maladie de Wilson 2 1,5%
Cirrhose alcoolique 1 0,8%
Cirrhose biliaire secondaire 1 0,8%
Hépatite fulminante 1 0,8%
Cirrhose post virale B et C 3 2,3%
Cirrhose alcoolique et post virale C 1 0,8%
Cirrhose non étiquitée 34 25,8%
c. Stade de la cirrhose :
Tableau 2: Stade de la cirrhose
Stade de la cirrhose nombre pourcentage
Child A 4 3,1%
Child B 46 35,7%
Child C 63 48,8%
d. L’hémorragie digestive :
29 cas ont fait une hémorragie digestive soit dans la dernière hospitalisation ou dans les hospitalisations antérieures.
e. signes de décompensation de la cirrhose: Ascite :
L’ascite est présente dans 107 cas, dont 2 cas ont une surinfection de l’ascite.
Encéphalopathie :
38 malades sont atteints d’encéphalopathie.
f. Hypertension portale :
123 malades présentent l’hypertension portale.
g. Traitement déjà reçu :
La plupart des malades sont sous traitement symptomatique fait d’un béta bloquant, diurétique et un antibiotique.
2 patients sont sous ursolvan.
2 patients sont sous les antiviraux, dont un sous interféron et l’autre sous riveran.
1 patient sous D-penicillamine.
1 patient a reçu simultanément un traitement composé de corticoïdes, ursolvan et imurel.
Une dérivation porto-cave a été réalisée chez un seul patient. h. Les nodules de CHC :
6% des malades présentent CHC, dont ¾ ont une cirrhose post virale C et ¼ ont une cirrhose post virale B.
La découverte de CHC est faite grâce à l’échographie ou à la TDM. Dans 4 cas la taille de nodule a été entre 3 et 4 cm, alors que dans le reste la taille est comprise entre 4 et 5 cm.
B. Deuxième échantillon :
233 patients cirrhotiques sont suivis dans un autre service de même établissement pendant l’année 2002.
Stade de la cirrhose selon la classification de Child-Pugh :
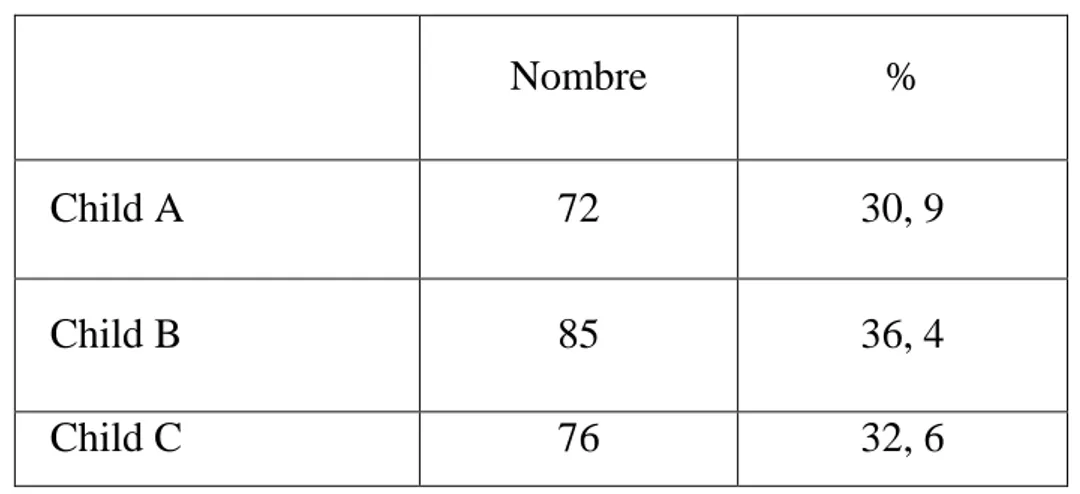
Tableau 3: Stade de la cirrhose
Nombre %
Child A 72 30, 9
Child B 85 36, 4
Child C 76 32, 6
Les indications à la transplantation dans cet échantillon sont :
- L’insuffisance hépatocellulaire associée à des degrés variables aux complications de la cirrhose.
- malades porteurs de CHC
- Cas particuliers : maladies cholestatiques chroniques :
1 cas de cirrhose biliaire primitive avec bilirubinémie >150 micromol/l
1 cas de cholangite sclérosante primitive avec des angiocholites répétés.
Ainsi parmi ces 233 patients, 99 malades sont considérés comme des candidats potentiels à la transplantation soit 42%.
Chez ces patients :
L’age : l’age moyen est de 50,5 avec des extrêmes allant de 18 ans à 83 ans
Le sexe : - 56 % sont de sexe masculin.
- 44% sont de sexe féminin.
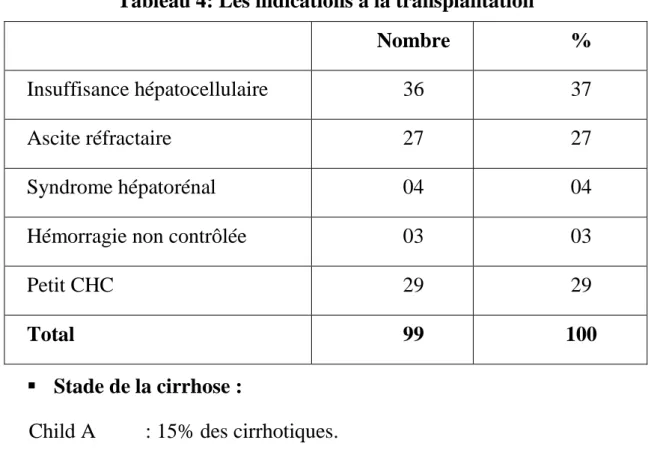
Tableau 4: Les indications à la transplantation
Nombre %
Insuffisance hépatocellulaire 36 37
Ascite réfractaire 27 27
Syndrome hépatorénal 04 04
Hémorragie non contrôlée 03 03
Petit CHC 29 29
Total 99 100
Stade de la cirrhose :
Child A : 15% des cirrhotiques. Child B : 18% des cirrhotiques. Child C : 67 % des cirrhotiques.
3. Analyse :
L’étude de ces deux échantillons, bien que peu significatifs en raison de l’effectif réduit, nous a permis de retenir les faits suivants :
Le besoin accru en transplantation dans notre pays :
La cirrhose du foie est fréquente comme le montre le deuxième échantillon où 233 patients sont suivis en une année dans un seul service.
Parmi les 365 patients suivis pour cirrhose dans les deux échantillons, 162 sont considérés comme des candidats potentiels à la transplantation, soit un taux de 44,3%.
Le recrutement des patients diffère d’un service à l’autre et par là leur prise en charge, plus que la moitié des patients (3/5) sont suivis dans un seul service durant une seule année.
L’age des patients est relativement jeune, avec une moyenne ne dépassant pas les 54 ans, sans grande différence de sexe.
La prédominance de la cirrhose post virale C et B est notée dans les deux échantillons de telle sorte qu’elles sont considérées comme l’indication la plus fréquente à la transplantation.
Les principales complications de la cirrhose pouvant conduire à
l’indication d’une transplantation sont par ordre décroissant : l’insuffisance
hépatocellulaire, l’ascite réfractaire, l’encéphalopathie et l’hémorragie digestive non contrôlable. Les autres complications, le syndrome hépatorénal, le syndrome hépatopulmonaire, hydrothorax hépatique et l’hypertension portopulmonaire sont beaucoup plus rares.
les autres types de cirrhoses, en dehors des cirrhoses post virales, ne sont représentés que par des faibles prévalences comme cela est attesté dans le premier échantillon avec des taux de 0,8% à 2,3%.
Le carcinome hépatocellulaire occupe la deuxième place dans les
indications d’une éventuelle transplantation avec un taux de 23%.
l’hépatite fulminante n’a été notée qu’une seule fois dans cette étude. Sa fréquence serait largement sous estimée car les hépatites aigues grave ne sont pas hospitalisées dans les services froids mais dans les unités de soins intensifs.
D
III. DISCUSSION :
La transplantation hépatique est en générale recommandée devant l’insuffisance hépatique terminale, engendré par des hépatopathies et certaines tumeurs.
L’analyse de notre étude nous montré le besoin accru et le caractère imminent de la transplantation hépatique dans notre contexte. L’acquisition d’une telle technique qui fait partie de la médecine de pointe nécessite un bon apprentissage des usages dans ce domaine en mettant le point sur les différentes indication, les type de transplantation à proposer aux patients, et le suivi des transplantés.
A. Indications :
Les indications de la transplantation hépatique les plus fréquentes par ordre décroissant sont :
a. Chez l’adulte :
Hépatopathie chronique :
1) Cirrhoses :
Dans notre série, la cirrhose représente la principale indication de la transplantation hépatique dont les 2 principales virale C avec un taux de 43,2% et virale B avec un taux de 13,6%. Les cirrhoses évoluent le plus souvent vers l’insuffisance hépatocellulaire, l’hypertension artérielle et peuvent dégénérer.
Le seul traitement de l’insuffisance hépatocellulaire est la transplantation hépatique .la classification de Child-Pugh permet de quantifier la gravité de la
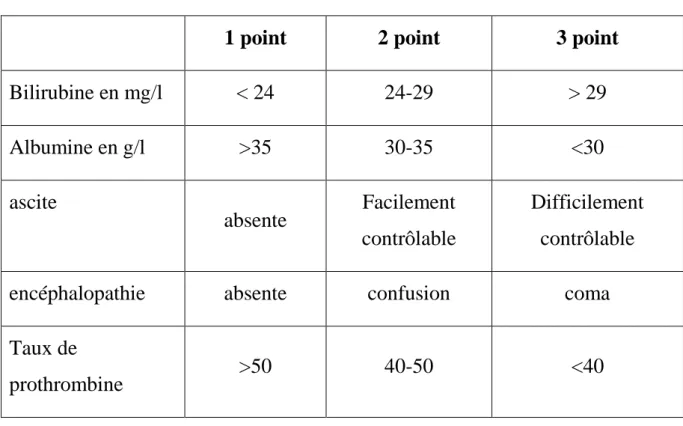
Tableau 5: classification de Child-Pugh
1 point 2 point 3 point
Bilirubine en mg/l < 24 24-29 > 29 Albumine en g/l >35 30-35 <30 ascite absente Facilement contrôlable Difficilement contrôlable
encéphalopathie absente confusion coma
Taux de
prothrombine >50 40-50 <40
Classe A : 5 à 6 points Classe B : 7 à 9 points Classe C : 10 à 15 points
Classe A correspond à la cirrhose compensée
Classe B et C correspond à la cirrhose décompensée.
Les malades parvenus au stade C présentent à des degrés divers, ascite réfractaire, ictère, encéphalopathie, dénutrition, trouble de l’hémostase, et représentent l’indication de base de la greffe.
C’est essentiellement dans ce groupe que surviennent le décès en liste d’attente .la transplantation peut être envisagée à un stade plus précoce
d’insuffisance hépatocellulaire (Child B) si certaines complications surviennent comme ascite réfractaire, plusieurs épisodes d’encéphalopathie .en absence d’insuffisance hépatocellulaire (Child A) il n’y a pas d’indication à la transplantation.
La greffe du foie n’est pas indiquée en cas d’hémorragie digestive due à l’hypertension portale avec absence d’insuffisance hépatocellulaire, elles relèvent de traitement médicamenteux et endoscopique si échec on a recours à la dérivation portosystémique.
Cirrhoses virales :
Cirrhoses dues au virus de l’hépatite C : dans cette série son taux est d’environ 43,2%.
Les cirrhoses décompensées liées à l’hépatite C constituent la première cause de transplantation hépatique aux états unis et en Europe [1]. Elles représentent une incidence de 20% en France, la survie à 5 ans après la transplantation est de l’ordre de 70-75% [2].
La récidive virale C est quasi-systématique dans les semaines qui suivent la transplantation un peu près 95-100% [2]. L’histoire naturelle de la récidive virale C est variable d’un individu à un autre .on estime à 30% la probabilité de développer une cirrhose 5 ans après la transplantation hépatique [1]. De nombreux facteurs, incluant ceux liés au virus, à l’hôte, à l’environnement et au donneur, sont vraisemblablement impliqués dans le pronostic.
Le statut immunitaire joue un rôle majeur dans la sévérité de la récidive virale C, avec une association entre d’une part une charge virale élevée et une
cadre de la transplantation hépatique, le traitement anti-viral peut être discuté avant transplantation (malade sur liste d’attente), juste après la transplantation (au moment de l’hépatite aigue sur le greffon) ou au stade d’hépatite chronique [3]. De nombreuses études avec des nombres limités des patients ont évalué la réponse virologique prolongée entre 9-30%. Les consensus ont proposé que le traitement soit instauré plus d’une année après la transplantation devant la constatation d’une fibrose avancée (> ou égale à F2 au score METAVIR) [1]. La tolérance du traitement est mauvaise avec des taux élevés d’interruption et de modification de posologie.
Cirrhose due au virus de l’hépatite B : Elle représente un peu prés 13,6% des patients de notre série.
Les patients ayant une cirrhose due au VHB représentent un groupe important des candidats potentiels à la transplantation. En effet, il s’agit de sujets jeunes avec une maladie souvent évolutive et exposés au risque de carcinome hépatocellulaire [4]. Cependant, le risque de persistance de l’infection virale et de réinfection du greffon a conduit de nombreuses équipes à restreindre cette indication. C’est pour cela qu’elle ne représente que 10 % des indications de transplantation hépatique [2].
Les critères d’indication sont les mêmes que dans la cirrhose due à l’hépatite C.
Le pronostic spontané est souvent difficile à affirmer .la cirrhose due au VHB doit le plus souvent être considérée comme une maladie évolutive. Mais le problème principal de cette maladie est le risque de réapparition de la maladie virale B après la greffe.
Pour diminuer ce risque, il a été proposé d’administrer des immunioglobuliones anti –Hbs pendant la phase d’anhépatie afin de contrôler les particules virales circulantes. Dans l’étude multicentrique européenne, la survie de patients est significativement améliorés par l’administration d’Ig anti-HBs au long cours. En Europe se dégage le consensus suivant :
Les malades n’ayant pas de réplication du VHB peuvent être transplantés s’ils reçoivent une immunoprophylaxie passive anti-HBs au long cours.
Les malade avec réplication du VHB doivent être inclus dans de protocoles de prévention de le réinfection du greffon [5].
Cirrhose due au virus de l’hépatite D et B :
Les critères d’indication de la transplantation sont les même que les cirrhoses dues au VHB. Le pronostic spontané des cirrhoses dues au VHD est assez sombre. Le risque de persistance de l’infection virale B et de l’infection virale delta sont des éléments conduisant certaines équipes à ne pas proposer la greffe chez ces malades. L’une des caractéristiques de ces malades est que la multiplication du VHB est arrêtée dans la majorité des cas lorsque les patients arrivent au stade de la transplantation. L’administration prolongée d’Ig anti-HBs permet de diminuer le risque de persistance et la réapparition de l’Ag HBs qui n’est que de 15% inférieur au taux de réinfection chez les patients transplantés pour cirrhose due au VHB [6].
A long terme, chez ces patients qui demeurent Ag HBs négatifs, l’Ag delta et l’ARN delta disparaissent dans 95% des cas du foie et du sérum [6]. la survie
c’est due au faible taux de récidive virale B et une moins grave sévérité de la réinfection B-delta par rapport à la réinfection B isolée [7].
Cirrhose alcoolique : Son taux ne dépasse pas 0,8% dans notre étude.
La cirrhose alcoolique représente la première indication de greffe pour cirrhose du foie en France [8], cependant La greffe n’est envisagée que chez moins de 5% de l’ensemble des patients atteints de cirrhose alcoolique [2].
C’est pour des raisons multiples comme l’exigence de la plupart des équipes une abstinence complète de 6 mois en dehors d’une hospitalisation, et que l’alcoolisme peut engendrer d’autre tares extrahépatiques sévères, et certains malades sont non compliants et la prise d’un traitement immunosuppresseur au long cours n’est pas possible, ainsi que la difficulté d’établir un pronostic spontané de la maladies hépatique, on peut assister même à des améliorations spectaculaires suite à un arrêt de l’alcoolisme [2] [4] [9].
L’efficacité de la transplantation hépatique dans la cirrhose alcoolique grave est certaine avec une survie identique à celle de cirrhoses non alcoolique [10]. La survie à un an est de 80% [10] et de 65% environ à 5 ans [11]. Elle est significativement supérieure à la survie théorique en absence de transplantation [11]. La greffe du foie apporte un gain moindre en cas de Child B [9].
Cirrhose biliaire primitive : présente un pourcentage de 2,3%.
Elle est apparue depuis quelques années comme une très bonne indication à la transplantation hépatique. Il s’agit principalement d’une maladie cholestatique et la cirrhose au sens histologique du terme ne se constitue que tardivement [2] [4] [10]. On estime que la cirrhose biliaire primitive évolue en 3 phases :
une première asymptomatique, révélée par une cholestase biologique ou par des manifestations extrahépatiques qui peut durer plus de 10 ans. Une seconde phase symptomatique avec prurit, ictère, et asthénie. Une troisième est dite terminale évoluent en moyenne sur 2 ans.
L’indication de transplantation doit être portée au début de cette dernière phase [4]. Les éléments font suspecter l’entrée dans cette phase sont : l’élévation sans cesse croissante de la bilirubine et l’apparition de complications de la maladie.
Le Mayo risk score permet de déterminer le pronostic et le temps de transplantation en cas de cirrhose biliaire primitive, il dépend de l’age, du taux de la bilirubine, d’albumine, de prothrombine et de la présence d’œdème [10] [12].
Mayo risk score: (0.039 × age [ans]) + (0.871 × log bilirubine [mg/dL]) − (2.53 × log albumine [g/dL]) + (2.38 × log prothrombine [secondes]) + (0.859 × œdème).
Un score égal à 7,8 représente le temps optimal pour la greffe.
La transplantation donne des bons résultats avec une survie de 88% à un an et de 85% à 8 ans [4]. .
Il est important de ne pas retarder l’indication de la greffe. Le risque de récidive de la maladie est inférieur à 10% dans un délai de 5 ans après la greffe et n’affecte pas la survie du greffon à moyen terme [4].
La cirrhose biliaire primitive reste une indication de choix de la transplantation hépatique même si c’est une maladie peu fréquente.
Cirrhose d’origine auto immune : ne représente que 2,3%.
Elles touchent surtout les jeunes femmes. Ces hépatopathies sont sensibles au traitement immunosuppresseur par azathioprine et corticoïdes [13].
La transplantation hépatique n’est indiquée que devant [4] [10] : des complications d’hypertension portale, un tableau de cirrhose décompensée, dans les formes fulminantes ou d’emblée en cas de non amélioration rapide sous traitement médical.
Le taux de survie à 3 ans est de 90%, la prévalence de récidive est faible [4].
Cirrhose biliaire secondaire : représente 0,8%.
Certaines cirrhoses peuvent être secondaires à des anomalies anatomiques des voies biliaires, à une lithiase intrahépatique ou un traumatisme opératoire de la voie biliaire. La transplantation peut être envisagée lorsqu’une intervention de dérivation des voies biliaire est impossible, ou inefficace, ou au stade de cirrhose constituée avec persistance de la cholestase clinique malgré une dérivation biliaire perméable. La transplantation est indiquée également en cas de survenue d’ascite ou de complications de l’hypertension portale. L’indication, chez ces patients qui sont souvent multiopérés, doit être envisagée à un stade précoce de la maladie. En effet, il existe souvent des adhérences très inflammatoires autour du foie et du pédicule hépatique, la phase d’hépatectomie peut devenir très hémorragique [4].
Cirrhose cryptogénétique :
Dans certains cas aucune cause n’est retrouvée à la cirrhose. L’absence d’étiologie ne modifie pas l’attitude vis-à-vis de la transplantation hépatique qui répond aux indications générales [2].
2) Les tumeurs du foie :
L’exérèse chirurgicale est le seul traitement des tumeurs du foie permettant la guérison alors que les tumeurs centrales et bi lobaires sont inextirpables par hépatectomie partielle [2] [4] [9]. De plus l’exérèse sur un foie cirrhotique est dangereuse du fait de l’insuffisance hépatocellulaire. La transplantation hépatique permet de traiter les tumeurs irrésécables et celles développées sur cirrhose. Cependant, le taux de survie a été décevant jusqu'à présent à cause de récidives tumorales intra et extra hépatique. Des progrès récents ont été obtenus grâce à une meilleure sélection des malades et l’utilisation de traitement adjuvant [14].
Carcinome hépatocellulaire :
Le carcinome hépatocellulaire est le plus fréquent des cancers primitifs du foie, dans 80% des cas il complique une cirrhose [15] son incidence est en forte augmentation [16].La transplantation hépatique est le moyen le plus efficace de traiter cette tumeur à condition qu’elle soit limitée au foie.
CHC développé sur un foie non cirrhotique est très rare et dépisté le plus souvent à un stade évolué. La présence d’une maladie extrahépatique est fréquente et interdit la greffe. Lorsque le CHC est localisé au foie, l’absence d’altération du foie sous jacente offre des possibilités d’exérèse très large et des
aller jusqu’à 80% si le diamètre de la tumeur est < à 8 cm et qu’il n’y a pas d’envahissement vasculaire macro ou microscopique [17].
La greffe s’adresse aux cancers volumineux limités au foie .la présence d’une maladie extra hépatique explique le taux de récidive inacceptable [15].
L’idée qu’il existe une relation entre la taille de CHC, la présence d’une dissémination et le risque de récidive est venue au groupe de Pittsburgh [18] en remarquant que la survie des patients transplantés pour cirrhose sans CHC est la même chez les patients transplantés pour cirrhose mais l’examen anatomopathologique a révélé la présence des petits CHC.
C’est au groupe de l’hôpital Paul [19] brousse que revient le mérite d’avoir préciser le nombre et la taille de CHC au delà desquelles le taux de décès par récidive métastatique après la greffe augmente significativement. Ils ont estimé qu’au delà de 3 nodules ou de diamètre > à 3 cm, surtout s’il existait un envahissement vasculaire le risque de récidive métastatique est très important, il rend discutable le bénéfice de traitement.
Actuellement on adopte les critères de Milan pour indiquer une transplantation hépatique en cas de carcinome hépatocellulaire (CHC) sur cirrhose [14].
Tableau 6: les critères de Milan
CHC uninodulaire Moins de 5 cm de diamètre
CHC multinodulaire Trois nodules maximums et diamètre du plus grand inférieur ou égal à 3 cm
Absence d'envahissement vasculaire macroscopique dans tous les cas
L’age, est longtemps considéré comme un critère, a perdu de son poids dans la décision de la greffe. Seul compte désormais l'âge physiologique [15].
Une étude faite à Renne [15] a montré que le sexe, le groupe sanguin, la nature de la cause de cirrhose sous jacente au CHC influencent significativement la durée de survie.
Le groupe de San Francisco (UCSF) [9] [15] [20] propose encore la transplantation pour un nodule unique de moins de 6,5 cm de diamètre ou plusieurs nodules dont le plus volumineux est inférieur à 4,5 cm à condition que la somme des diamètres n'excède pas 8 cm. Avec ces critères, ils rapportent un taux de survie à cinq ans de 50 %.
En France, il n’existe pas de restriction des indications de transplantation hépatique pour CHC [21]. L’analyse des caractéristiques tumorales des malades inscrits sur liste a permis de déterminer que la majorité d’entre eux ont au maximum 5 lésions d’un diamètre maximal de 5 cm ça ce qu’on appelle les critères 5-5 [22].
Des études menées dans 14 centres de transplantation hépatique français entre 1988 et 1998 [23] a montré que la survie à 5 ans et la probabilité de récidive ne diffèrent pas significativement entre les 2 groupes.
Le groupe répondant aux critères de milan : la survie à 5ans est de 60,9% ; le récidive est de 20%.
Le groupe hors des critères de milan mais répondent aux critères 5-5 : la survie à 5ans est de 55,1% ; le récidive est de 24%.
Les critères pronostiques essentiels dans une extension des critères de milan sont la différenciation tumorale et l’invasion vasculaire au contraire du nombre et la taille des lésions qui ne sont plus des éléments pronostiques déterminants et permettent de s’affranchir des critères de milan.
Et cela été confirmé dans une 2éme étude entre 1999 et 2001 dans 7 centres [24] avec un taux de survie et de probabilité de récidive similaire dans les 2 groupes.
Le groupe répondant aux critères de milan : taux de survie est de 79,5% ; récidive est de 9%.
Le groupe hors des critères de milan mais répondent aux critères 5-5 : taux de survie est de 77,8% ; et récidive est de 12%.
Il est possible d’identifier un sous groupe de malades hors des critères de milan pour lesquels des résultats superposables à ceux des critères de milan.
Le risque de croissance tumorale pendant la phase d'attente à la transplantation justifie pour la plupart des équipes l'intérêt d'un traitement néoadjuvant à la greffe. Trois stratégies thérapeutiques sont actuellement
proposées : la chimioembolisation lipiodolée, la destruction percutanée par radiofréquence, l'exérèse classique [10].
Les autres tumeurs :
Carcinome fibrolamellaire : est une forme histologique particulière de CHC sur foie sain touchant surtout la femme jeune. Il est caractérisé par une évolution lente. C’est une bonne indication de la transplantation hépatique lorsque l’exérèse par hépatectomie partielle n’est pas possible. Le risque de récidive n’est pas nul parce que ces patients ne sont transplantés que tardivement [4].
Hémangioendothéliome épithélioide du foie : le greffe est indiquée en cas de tumeur inextirpable et absence d’envahissement vasculaire. La survie prolongée a été rapportée après transplantation mais récidive ont été décrits [4].
Hémmangiosarcome hépatique est une contre indication absolue à la transplantation hépatique à cause des récurrences [25].
Schawnnomes hépatique : un seul patient a été transplanté pour cette pathologie mais il a décédé 3 mois et demi après la greffe [25].
Adénome hépatique : indiqué seulement en cas de multiples et des grandes adénomes ou à localisation centrale [25].
Cholangiocarcinome : la plupart des centres considèrent ce type de tumeur, une contre indication à la transplantation en raison de risque de récidive [2] [4].
Métastase hépatique : la transplantation est indiquée pour certains tumeurs carcinoïdes. En dehors de ce type de tumeur la greffe est contre
indiquée, surtout en cas de métastase colorectal et gastrique [2] [4]. Certaines équipes ont tenté la transplantation pour métastases hépatiques des tumeurs neuroendocrines. Au début, les résultats sont décevants en raison de la mauvaise sélection des patients et à la nécessité de traitements adjuvants [26]. Afin de déterminer un bon candidat à la transplantation, des auteurs, d’après des expériences multicentriques, ont précisé des critères de milan pour cette indication [26].
3) Les maladies métaboliques cirrhogénes :
La transplantation hépatique est peut être indiquée dans 3 groupes de maladies métaboliques :
Maladies dues à un trouble métabolique d’origine hépatique et dont l’organe atteint est le foie :
La greffe du foie permet d’obtenir une guérison sans risque de récidive. Les maladies qui font partie de ce groupe sont :
Maladie de Wilson :
Cette maladie se caractérise par une surcharge en cuivre dans le foie, le système nerveux, et le rein. Elle est due à un défaut d’excrétion biliaire de cuivre au niveau de l’hépatocyte.
La transplantation hépatique est indiquée [2] [4]:
- Dans les formes fulminantes de maladie de Wilson car l’évolution spontanée sous D-penicillamine est constamment mortelle.
- Dans les formes avec cirrhose décompensée parce que le traitement médical peut échouer voire être déltere.
- Dans les formes ou la maladie s’aggrave sous D-penicillamine.
- Dans les formes de poussée aigue de Wilson lorsque les patients arrêtent brutalement le traitement.
Déficit en alpha-1-antitrypsine :
Un quart des enfants ayant le phénotype Piz ont une cholestase néonatale, et 50 % d'entre eux vont développer une cirrhose. Lorsqu'il existe une cirrhose constituée, elle évolue toujours vers le décès. Ainsi dans ces cas, l'indication de transplantation hépatique est formelle. Le trouble métabolique est complètement corrigé par la transplantation sans risque de récidive [4] [10].
Autres :
Comme Tyrosinémie héréditaire, Crigler-Najjar type1, certaines glycogénoses et galactosémie, et d'autres maladies métaboliques peuvent être des indications à la transplantation hépatique [4].
Défaut métabolique d’origine en partie hépatique : Hémochromatose primitive du foie :
La principale indication de transplantation hépatique dans l'hémochromatose est représentée par l'apparition d'un carcinome hépatocellulaire dont l'exérèse par hépatectomie partielle n'est pas réalisable [4] [10].
Porphyrie érythropoïétine ou protoporphyrie :
La constitution d'une cirrhose avec insuffisance hépatique par accumulation de pigments protoporphyriques est de mauvais pronostic et doit faire envisager
Maladie de Gaucher :
Elle n’est corrigée que partiellement par la transplantation hépatique avec un risque de récidive.
Maladies dues à un trouble métabolique d’origine hépatique dont l’organe atteint n’est pas le foie :
La neuropathie amyloïde familiale due à une anomalie de la transthyrétine consiste en une atteinte essentiellement des nerfs périphériques, évoluant vers un état grabataire. L'évolution est constamment mortelle dans une médiane de 10 ans. La transplantation hépatique peut arrêter l'évolution de la maladie [4] [27].
L'hyperoxalurie primitive est due à un déficit enzymatique d'origine hépatique responsable de lithiase rénale, de néphrocalcinose, d'insuffisance rénale chronique, puis d'accumulation d'oxalate de calcium dans les tissus [2].
4) Cholangite sclérosant :
C’est une maladie atteignant les grosses voies biliaires extra- et intrahépatiques. Elle peut être secondaire ou primitive.
Cholangite sclérosante primitive :
Maladie chronique des voies biliaires, Elle atteint plus fréquemment les hommes jeunes. Biologiquement et cliniquement il existe une cholestase. La cholangiographie peut montrer des images de sténoses et de dilatations étagées sur l'ensemble de l'arbre biliaire avec raréfaction du cholangiogramme intrahépatique. À l'examen histologique, il existe une fibrose péricanalaire.
Elle peut se compliquer d'angiocholite, d’ictère, et la constitution d'une cirrhose biliaire secondaire. Il existe une possibilité de transformation maligne en carcinome cholangiocellulaire, ce risque augmente avec la durée d'évolution et devient supérieur à 30 % après 10 ans d'évolution [2] [28].
La tendance actuelle, en raison des mauvais résultats des interventions biliaires et du risque de cancer, est de proposer la greffe dès l'apparition des symptômes [28].
Il est bien sûr impératif de pratiquer une coloscopie avant la transplantation. Il faudra en revanche d'abord traiter la RCH si elle est en poussée [2] [28].
Les résultats de la transplantation hépatique pour cholangite sclérosante primitive sont aux alentours de 80 à 90 % de survie à 1 an [4]. Il n'y a pas de preuve de récidive de la cholangite sur le greffon.
Cholangite sclérosante secondaire :
La cholangite sclérosante secondaire à une chirurgie biliaire représente une entité nosologique rare mais grave pouvant relever de la transplantation hépatique après échec des thérapeutiques radio-endoscopiques. Le pronostic des ces malades après transplantation hépatique apparaît excellent [29].
5) Autres :
Le syndrome Budd -Chiari :
Les indications de transplantation hépatique pour syndrome de Budd-Chiari semblent rares ; le traitement de choix du syndrome de Budd-Chiari étant la dérivation portocave soit par anastomose mésentéricocave ou portocave, soit
plus rarement par dérivation mésoatriale lorsque la veine cave inférieure n'est pas perméable. Les indications de la transplantation hépatique sont :
le syndrome de Budd-Chiari suraigu dont le seul traitement est la greffe d’urgence.
-s’il existe une cirrhose constituée.
Lorsqu'une transplantation hépatique pour syndrome de Budd-Chiari est réalisée, il est indispensable d'identifier la maladie thromboembolique associée et de la traiter [2] [4].
Echinococcose alvéolaire, hyperplasie nodulaire régénérative, pathologie hépatique polycystique, Maladie de rendu Osler, Papillomatose multifocale des voies biliaires : sont des indications rares [25] [30] [31].
Les maladies aigues du foie :
1) Hépatite fulminante et subfulminante :
L'hépatite fulminante est la survenue au cours d'une hépatite aiguë, chez une personne n'ayant pas d’hépatopathie sous jacente connue, d'une insuffisance hépatique entraînant une encéphalopathie qui apparaît dans moins de 15 jours après le début de l'ictère. On parle d'hépatite subfulminante lorsque l'encéphalopathie survient 15 jours à 3 mois après le début de l'ictère, et d’hépatite fulminante hyperaigu si le délai entre l’encéphalopathie et l’ictère moins ou égal à 7 jours [32]. Dans tous les cas, l'apparition de l'encéphalopathie est associée à un effondrement des facteurs de coagulation. Le pronostic spontané de l'hépatite fulminante et subfulminante est mauvais puisque la mortalité globale est de 80 % principalement par décérébration [2] [4].
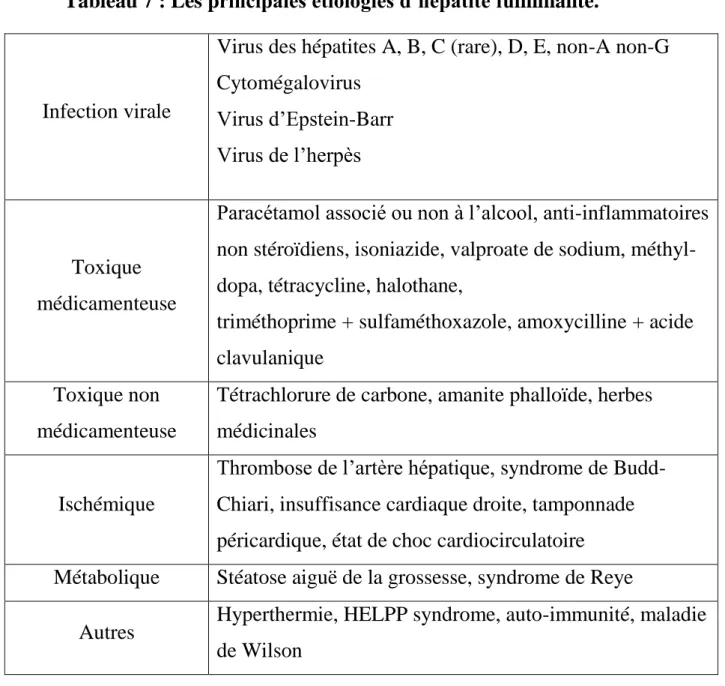
Tableau 7 : Les principales étiologies d’hépatite fulminante.
Infection virale
Virus des hépatites A, B, C (rare), D, E, non-A non-G Cytomégalovirus
Virus d’Epstein-Barr Virus de l’herpès
Toxique médicamenteuse
Paracétamol associé ou non à l’alcool, anti-inflammatoires non stéroïdiens, isoniazide, valproate de sodium, méthyl-dopa, tétracycline, halothane,
triméthoprime + sulfaméthoxazole, amoxycilline + acide clavulanique
Toxique non médicamenteuse
Tétrachlorure de carbone, amanite phalloïde, herbes médicinales
Ischémique
Thrombose de l’artère hépatique, syndrome de Budd-Chiari, insuffisance cardiaque droite, tamponnade péricardique, état de choc cardiocirculatoire Métabolique Stéatose aiguë de la grossesse, syndrome de Reye
Autres Hyperthermie, HELPP syndrome, auto-immunité, maladie de Wilson
Dans ces 20 dernières années, de nombreux traitements ont été essayés sans que l'on note une amélioration de la survie, qui reste toujours inférieure de 30%. La gravité des hépatites fulminantes et sub-fulminantes est liée à la survenue d'un oedème cérébral conduisant au décès par hypertension
intracrânienne. Pour être efficace, la transplantation hépatique doit être faite en urgence afin d'éviter la survenue de complications neurologiques irréversibles [2] [32].
La transplantation hépatique en urgence, fait passer la survie de 20 % à plus de 60 % [33].
Afin d'éviter de transplanter par excès des malades susceptibles de guérir spontanément, des critères devant conduire à la transplantation hépatique en urgence ont été établis [34]: (critères de Clichy)
Une encéphalopathie stade II (syndrome confusionnel) avec,
Un facteur V inférieur à 20 % chez les sujets de moins de 30 ans et inférieur à 30 % chez les sujets de plus de 30 ans.
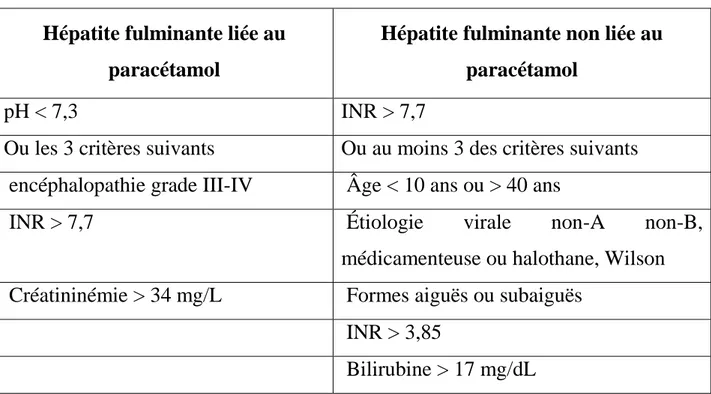
On rapporte aussi les critères du King’s Collège Hospital qui sont résumés dans le tableau suivant [35]:
Tableau 8 : les critères du King’s Collège Hospital Hépatite fulminante liée au
paracétamol
Hépatite fulminante non liée au paracétamol
pH < 7,3 INR > 7,7
Ou les 3 critères suivants Ou au moins 3 des critères suivants encéphalopathie grade III-IV Âge < 10 ans ou > 40 ans
INR > 7,7 Étiologie virale non-A non-B,
médicamenteuse ou halothane, Wilson Créatininémie > 34 mg/L Formes aiguës ou subaiguës
INR > 3,85
Bilirubine > 17 mg/dL
Une fois ces critères sont réunis, le délai pour réaliser la transplantation hépatique est de 24 à 48 heures [2].
Lorsque la cause de l'hépatite fulminante n'expose pas au risque de récidive de la maladie initiale sur le greffon, une transplantation hépatique orthotopique avec un greffon auxiliaire partiel doit être discutée [36].
Cette technique chirurgicale, développée depuis les années 90, permet en théorie de pallier l'insuffisance hépatocellulaire sévère tout en permettant la régénération des segments hépatiques natifs laissés en place. La transplantation auxiliaire peut ainsi permettre à terme l'ablation du greffon auxiliaire et l'interruption du traitement immunosuppresseur dont les conséquences délétères sont ainsi prévenues. Ce but ultime peut actuellement être réalisé dans 40 % des cas [37].
Du faite de la pénurie d’organe, 30 % à 50 % des patients décèdent au cours de l’attente de transplantation, malgré leur statut prioritaire [38]. Pour contourner ce problème, la transplantation hépatique à partir de donneur vivant a été développée. Néanmoins, elle doit être évaluée dans des essais contrôlés. Dans ce contexte, une étude faite à l’hôpital universitaire Kyushu entre octobre 1996 et mars 2007 [39], durant laquelle 252 transplantations hépatiques à donneur vivant a été réalisé. La survie du greffon à un an après la greffe est de 77,6% et de 65,5% à 10 ans. Pour les patients, elle a été de 80% et 68,2% à un an et à 10 ans respectivement. Ces résultats sont acceptable et cette technique est considérée comme un traitement de choix en cas d’hépatite fulminante mais on doit tenir en compte d’absence des donneurs cadavériques dans ce pays ce qui compromet ce type de traitement.
2) Insuffisance hépatique aigue :
Sous cette rubrique se rassemblent toutes les causes d'insuffisance hépatique [4] :
L’hépatite subaiguë grave avec apparition d'une encéphalopathie hépatique plus de 3 mois après le début des symptômes.
L’hépatite aiguë très sévère avec effondrement des facteurs de coagulation, survenue d'une ascite sans encéphalopathie.
b. particularité de la transplantation chez l’enfant :
La transplantation hépatique chez l'enfant donne classiquement de meilleurs résultats que chez l'adulte avec des survies atteignant dans certaines équipes plus de 90 % à 1 an et des courbes de survie ne s'infléchissant pas à 5 ans [40]. Souvent les enfants après la transplantation ne se sentent plus malades, et l'on note une transformation au plan psychologique avec une réintégration de l'enfant dans le groupe social.
La transplantation hépatique chez l'enfant pose des problèmes particuliers : le faible nombre de donneurs pédiatriques a rendu nécessaire la
réalisation de transplantations de foies d'adultes réduits ou partiels. un plus grand nombre de thromboses de l'artère hépatique ont été
décrites après greffe hépatique chez l'enfant.
La transplantation hépatique chez l'enfant doit être considérée pour tous les enfants avec une maladie hépatique progressive, irréversible, non contrôlée par les traitements médicaux.
Le moment de la transplantation est parfois difficile à déterminer, il est globalement préférable que l'enfant ait plus de 1 an d'âge et plus de 10 kg de poids essentiellement pour des raisons techniques [4].
Les indications de la transplantation hépatique chez l'enfant sont La cholangite sclérosante, les maladies métaboliques, les tumeurs du foie et les insuffisances hépatiques, nous insistons sur l'atrésie des voies biliaires extrahépatiques, la paucité ductulaire et la maladie de Byler.
L’atrésie des voies biliaires :
L'atrésie des voies biliaires extrahépatiques se caractérise par l'absence totale ou partielle de voie biliaire principale perméable, cette dernière étant remplacée par un tissu fibreux. Il s'agit de la principale cause de cholestase extrahépatique de l'enfant (incidence 1/8 000) et de la principale indication de transplantation hépatique chez l'enfant [41]. Le diagnostic de la maladie est porté dès les premiers mois de vie par la découverte d'un ictère cholestatique. Actuellement, tous les enfants ont une tentative de reconstruction biliaire chirurgicale par une portoentérostomie ou intervention de Kasaï [42]. Dans les autres cas il n’y a pas de rétablissement du flux biliaire et la transplantation est indiquée d’emblé.
La portoentérostomie permet d'éviter la transplantation hépatique chez 25 % des enfants et permet de retarder l'heure de la transplantation hépatique chez 40 % [4].
Paucité ductulaire :
Elle correspond à la disparition des canaux biliaires des espaces portes. Elle se présente sous deux formes : la forme syndromique et la forme non syndromique. Dans les deux cas l'évolution se fait vers une cirrhose biliaire [43].
Maladie de Byler :
Elle est caractérisée par une incapacité de l'hépatocyte à excréter la bile. Il n'y a pas d'anomalie anatomique ou histologique des voies biliaires. Le trouble basal semble être d'origine biochimique mais reste encore non élucidé. Cette maladie évolue en quelques mois vers une cirrhose biliaire secondaire et
c. Contre indication à la transplantation hépatique:
Depuis ces dernières années, le nombre des contre-indications à la transplantation hépatique s'est considérablement réduit.
Il existe un consensus actuel général sur les contre-indications suivantes [2] [10] [32] :
sepsis non contrôlé extrahépatique. tumeur maligne extrahépatique active. thrombose diffuse du système porte.
incapacité à supporter l'intervention (tare cardio-pulmonaire majeure, sauf transplantation associée).
Profil psychologique anormal.
L’acidose métabolique non corrigeable, l’hypotension réfractaire et une pression de perfusion cérébrale constamment inférieure à 40 mmHg sont considérés comme des contre indications absolues en cas d’hépatite fulminante [32].
D'autres problèmes médicaux sont considérés comme des contre-indications ou non selon les équipes de transplantation [44] [45] :
il s'agit de l'âge au-delà de 65 ans
la séropositivité au virus de l'immunodéficience humaine (VIH) sans sida.
l'alcoolisme chronique actif.
l'absence de la compliance attendue aux traitements.
la présence de l'antigène HBs dans le sérum associée à une réplication active du virus de l'hépatite B.
B. Le receveur :
a. Evaluation du candidat à la transplantation hépatique :
Elle doit permettre de caractériser la nature et la sévérité de la maladie hépatique et de rechercher des pathologies associées augmentant le risque périopératoire. Il s'agit de l'insuffisance cardiaque, de l'insuffisance coronaire, de l'insuffisance rénale et de certaines affections respiratoires ou neurologiques [46] et des variations anatomiques.
Sur le plan anesthésique [47]:
Lorsque le patient se présente pour l'intervention, la situation clinique et les paramètres biologiques importants sont réévalués. Ainsi le bilan radiologique comprend :
Une radiographie pulmonaire à la recherche d'épanchements pleuraux et d’alétéctasie, une échographie cardiaque pour évaluer la fonction ventriculaire gauche et PAPs par la quantification de la fuite tricuspide. Si l’échographie est anormale, il faut la compléter par cathétérisme cardiaque droit.
Le bilan biologique comporte :
Le dosage des Gaz du sang debout/couché à la recherche d’hypoxémie de repos et un syndrome hépatopulmonaire si PaO2>10%, un bilan d’hémostase complet (temps de Quick, TCA, facteurs de coagulation, D-diméres, produits de dégradation de fibrine, TS, temps de lyse des euglobulines), un bilan standard (NFS, ionogramme sanguin et urinaire, clairance de créatinine, calcémie et phosphorémie), le groupage ABO rhésus et recherche d’agglutinines irrégulières.
D'autre part, un contact avec le site transfusionnel est indispensable pour la préparation de 8 à 10 culots globulaires, et la réservation de quatre à huit plasmas viro-inactivés et de deux concentrés plaquettaires d'aphérèse, séronégatifs pour le cytomégalovirus (CMV) si possible.
Détermination des variations de l’anatomie vasculaire chez le
receveur :
Il est primordial de préciser les variations anatomiques vasculaires afin d’éviter les surprises et les complications au cours de la chirurgie. La TDM et l’angiographie permettent de détecter ces variétés.
1. Variantes artérielles :
Elles sont très fréquentes. Parmi les variations qui peuvent influencer sur la technique de transplantation hépatique, il y a [48]:
Artère hépatique gauche accessoire qui prend naissance de l’artère gastrique gauche ou de tronc coeliaque.
Artère hépatique droite accessoire provienne de l’artère mésentérique supérieure.
Artère hépatique propre qui surmonte l’artère mésentérique supérieure ou l’artère gastrique gauche.
Artère hépatique commune à une origine autre que l’aorte.
Artère hépatique commune donne une naissance précoce de l’artère hépatique droite ou gauche par rapport à celle de l’artère gastro-duodénale.
trifurcation de l’artère hépatique commune en artère hépatique droite, artère hépatique gauche et artère gastro-duodénale.
Origine de l’artère hépatique droite est l’artère gastro-duodénale [49]. Il faut faire attention à la présence d’anévrysme de l’artère splénique qui est très fréquent chez les patients cirrhotiques avec hypertension portale [50].
2. Variante de la veine porte : [48]
Pour la veine porte, ses variétés sont non significatives chez le receveur. Alors que la présence d’une thrombose de la veine porte dont l’incidence est élevée chez les patients cirrhotiques influence la technique chirurgicale.
Il faut faire la différence entre le thrombus blanc de la veine porte et la thrombose tumorale qui est considérée comme une contre indication à la transplantation.
Les varices du système porte peuvent provoquer une hémorragie au cours de l’hépatectomie.
3. Les veines hépatiques et la veine cave inférieure :
La présence de variétés anatomiques de ces veines est significative chez les receveurs surtout que la veine cave inférieure est préservée au cours de l’hépatectomie (technique de piggy-back) [48].
La variante la plus fréquente est la présence d’une ou de plusieurs veines hépatiques inférieures droites indépendantes de la veine cave inférieure. Rarement, on peut trouver une continuation entre la veine azygos et la veine cave inférieure [49].
Chez les patients cirrhotiques, le lobe caudé peut cerner la veine cave inférieure ce qui complique la libération du foie de la partie rétrohépatique de la veine cave inférieure pendant l’hépatectomie [48].
Détermination du pronostic et de la sévérité de la maladie
hépatique :
Il est admis que tout patient atteint d’hépatopathie chronique avec un pronostic vital menacé dans un délai de 1 à 2 ans, doit être considéré comme un candidat potentiel à la transplantation hépatique [4].
Afin de déterminer le timing de la greffe, plusieurs scores ont été établis mais le plus efficace et communément utilisé est le score de MELD [10] [51] [52] [53].
Ce score égale à :
MELD = 10 x [0,957 x log e créatinine (mg/dl) + 0,378 x log e bilirubine (mg/dl) + 1,12 x log e INR+ 0,643].
Initialement ce score est utilisé pour déterminer la mortalité chez les cirrhotique 3 mois après la mise en place de TIPS mais il s’est avéré efficace dans la détermination de la mortalité en liste d’attente et par la suite les patients prioritaires à la transplantation [54].
Ces valeurs varient de 6 à 40, plus ce score est élevé plus le patient est altéré [55]. Certains auteurs suggèrent que la transplantation serait futile si le score est entre 10 et 11 [56]. Donc le score permet de déterminer le moment de transplantation chez les patients altérés et d’éliminer ceux dont la greffe n’est pas justifiée [10]. Selon des données récentes, le score de MELD est considéré
optimal si il est compris entre 20 et 25, acceptable mais suboptimal s’il est entre 15 et 20 ou 26 et 30. En cas de score inférieur à 15 ou supérieur à 30, il faut controbalancer les bénéfices et les risques de la transplantation [57].
Cependant le score MELD comporte des limites, qui nécessitent sa réactualisation régulière. Il est mal adapté aux pathologies non cirrhotiques notamment le carcinome hépatocellulaire (CHC) développé sur une cirrhose compensée ou CHC de petite taille [10] [58].
Chez l’enfant, l’évaluation du pronostic est assurée par le score de PELD, qui correspond au score de MELD chez l’adulte [59] [60].
En somme, la détermination des candidats potentiels se base sur plusieurs arguments, notamment [52] :
seuls les patients avec une probabilité de survie à un an est supérieure ou égale à 50% après la transplantation, sont considérés des prioritaires à la greffe.
La nécessité d’une abstinence de 6 mois en cas de cirrhose alcoolique.
En cas de cirrhose post virale B, seuls les patients avec ADN-VHB indétectable seront transplantés. Si VHB persiste, un traitement antiviral est nécessaire avant la greffe.
MELD est un bon score déterminant le risque de la mortalité avant la transplantation. S’il est inférieur à 11 la transplantation n’a pas de place.
b. Préparation du malade en liste d’attente :
Prévention et traitement des complications liées à la maladie
initiale :
1. Syndrome hépatorénal :
C’est une insuffisance rénale observée uniquement chez les patients ayant à la fois une insuffisance hépatique et une hypertension portale [61]. Il existe 2 types de syndrome hépatorénal : Le type 1 est caractérisé par une augmentation en moins de 15 jours du taux de la créatinine qui peut atteindre 221umol/l ou bien une élévation de plus de 100% par rapport au chiffre initial, on parle de type 2 lorsque la dysfonction rénale est modérée. C’est la complication la plus mauvaise de la cirrhose avec une survie en cas de type 1 est de 15 jours alors celle du type 2 est de 6 mois [62]. La transplantation est le traitement idéal mais la survie est inférieure à celle des patients qui n’ont pas fait le syndrome hépatorénal avec un risque plus élevé d’évolution vers l’insuffisance rénale terminale.
2. Hydrothorax hépatique :
Il résulte du passage du liquide d’ascite vers la cavité pleurale à travers les pores micro et macroscopique du diaphragme [10]. Le traitement initial consiste à une restriction sodée et des diurétiques. En cas d’échec, on a recours au drainage répété. Un shunt péritonéo-jugulaire ou TIPS peuvent être tenté mais leur efficacité est limitée [63]. La transplantation hépatique est le seul traitement efficace au long cours [64].
3. Syndrome hépatopulmonaire :
Il est défini par l'association d'une hépatopathie avec hypertension portale, d'une hypoxémie de repos, et d'une vasodilatation intrapulmonaire [10]. Ce syndrome est présent chez 10 à 15 % des cirrhotiques graves, et la survie moyenne à partir du diagnostic est inférieure à 3 ans [65]. Certains auteurs affirment qu’à part l’administration de l’oxygène, il n’y pas de traitement spécifique. La transplantation hépatique corrige le shunt et l’hypoxémie dans la plupart des cas [66] [67].
4. Hypertension portopulmonaire :
Elle correspond à l'association d'une cirrhose, d'une PAP moyenne supérieure à 25 mmHg, et de résistances vasculaires pulmonaires élevées. C'est une complication tardive et grave de la cirrhose, et qu’il faut la chercher systématiquement [49] [68] puisque 60% des patients sont asymptomatiques. La réversibilité de cette complication après la transplantation est inconstante [68]. Il faut tenir en compte qu’une pression de l’artère pulmonaires> à 50 et une résistance vasculaire > 250 dyn s/cm5 contre indique la transplantation [69].
5. Troubles de l’hémostase :
L'altération de l'hémostase chez le cirrhotique est un facteur de gravité de la maladie, qui favorise le saignement. La baisse des facteurs de la coagulation ne résume pas toutes les anomalies de l'hémostase, et certains troubles de mécanismes complexes en partie liés à la dysfonction endothéliale sont générateurs de phénomènes thromboemboliques [70] [71]. On peut distinguer :
les anomalies de l'hémostase primaire, fréquentes et secondaires à la thrombopénie de l'hypersplénisme, à des anomalies des fonctions plaquettaires.
la fibrinolyse chronique.
Réduction du risque de récidive de la maladie initiale :
1. le cas de cirrhose virale C :
Plus de 90% des patients développent une hépatite C du greffon dans le mois qui suit la transplantation [1], responsable d'hépatites aiguë ou chronique pouvant parfois évoluer vers une cirrhose et/ou une insuffisance hépatique et nécessiter une retransplantation [9] [72].
L’évolution vers la cirrhose est accélérée dans le contexte de la transplantation. En effet 10 à 20% des greffés développent une cirrhose en 9 à 12 ans [9] [72] [73].
Un certains nombres de facteurs sont associés à la progression de la fibrose qui compromet la survie du greffon, comme :
La charge virale et le génotype [9] [74]. L’immunosuppression [75].
L’age du donneur : la réponse virologique au traitement est obtenue de façon significative quand le greffon provient d’un jeune donneur [76].
La stéatose : son rôle n’et pas encore élucidé [72].
Le donneur vivant : la survie du greffon n’était pas différente selon la provenance du foie du donneur vivant ou cadavérique [77].
L'intérêt d'un traitement de l'infection virale C avant la greffe est de diminuer ou de négativer la charge virale, elle est encore au stade d’étude. Les traitements actuels par interféron ou association interféron - ribavirine sont mal tolérés au stade de cirrhose décompensée et leur efficacité est faible [72]. L’association d’interferon pégylé et de ribavirine permet d’obtenir 20% de la réponse virologique [9].
2. Le cas de cirrhose virale B :
La réinfection par VHB est de l’ordre de 75 à 90% des cas avec une survie à 5 ans ne dépassant pas 50%. Elle peut évoluer vers une hépatite fulminante, subaigue ou chronique avec une fréquence de perte du greffon par récidive de la maladie virale B varie de 11,1% à 63,6% [78].
On a recours à l’usage des immunoglobulines afin de diminuer la récidive. Dans une étude mené à l’hôpital de Paul brousse [79] chez des patients qui ont reçu les immunoglobulines pendant la phase d’anhépatie et les 6 premiers jours et réadministration d’immunoglobulines anti Hbs si le taux sérique d’Ac anti Hbs est < 100 UI/ l a permis d’abaisser le taux de récidive à 2 ans à 29%.
La lamivudine est actuellement l'antiviral disponible le plus puissant [80]. Il permet une négativation de l'ADN du VHB chez près de 100 % des malades mais la rechute est constante à l'arrêt du traitement et par ailleurs, il existe un risque d'échappement au traitement par mutation.
3. Le cas de cirrhose alcoolique :
La fréquence de la récidive a été évaluée dans une vingtaine d'études, mais ses facteurs prédictifs restent controversés ainsi que ses conséquences. Seule la
Dans l'étude de Miguet et al [82], le taux estimé de reprise d'une consommation d'alcool est de 11 % à 12 mois et de 30 % à 24 mois. Seulement 5 % des patients, ont perdu le greffon à cause de la reprise d’alcool.
4. Le cas de CHC :
C’est la première cause de décès chez les transplantés pour CHC, et qu’il faut la rechercher systématiquement après la greffe. L’élément déterminant essentiel est la bonne sélection des candidats ainsi l’utilisation des traitements adjuvants comme la chimioembolisation, résection et l’injection intra artérielle de lipoiocis dans le but de diminuer la taille de CHC et d’éviter les récidives [72].
5. Le cas de cirrhose biliaire primitive :
La cirrhose biliaire primitive est une bonne indication à la transplantation hépatique mais la récidive histologique est estimée à 30% à 10 ans [72]. La prophylaxie se base sur l’usage de corticoïdes et les immunosuppresseurs comme ciclosporine et tacrolimus [83].
6. Le cas de cirrhose auto-immune :
La récidive de la cirrhose auto-immune existe après la transplantation, avec un taux variable selon les séries de 10% à 30% et selon la durée après la greffe. En maintenant une corticothérapie minimale, on peut réduire la récidive [72].
7. Le cas de cholangite sclérosante :
La récidive existe, et son impact à moyen terme sur la survie des patients et des greffons est pour l’instant minime mais reste à évaluer sur le long terme [72].
C. Le donneur :
a. Le donneur cadavérique :
Certains critères doivent être respectés, notamment : Les critères hémodynamiques :
1. Le donneur cadavérique dont le coeur est battant au moment du prélèvement :
Il représente 63 % des donneurs d'organes [84]. Ce donneur est déclaré « mort » sur des critères qui définissent l'arrêt du fonctionnement cérébral. Chez ce « donneur cadavérique en état de mort encéphalique », la stabilité hémodynamique est censée être un des critères importants d'acceptation des organes.
En réalité, la plupart des équipes [85] définissent plutôt les paramètres hémodynamiques à partir desquels un donneur est considéré à haut risque en cas d'utilisation :
hypotension artérielle avec une pression artérielle systolique inférieure à 80 mmHg pendant plus d'une heure.
arrêt cardiaque de plus de 10 minutes.
utilisation de doses de dopamine supérieure à 15µg/kg/min, usage de levophed, d'épinéphrine ou de norépinéphrine.
La présence de ces critères n'est pas une contre-indication formelle à l'utilisation du foie, mais le bénéfice pour le receveur doit être particulièrement discuté.
2. Le donneur à coeur arrêté :
Il constitue un cas très particulier [84]. Il s'agit de malades dont le coeur est arrêté avant le prélèvement chirurgical des organes. Le décès est défini par l'arrêt des fonctions cardio-respiratoires.
Il existe deux types de donneurs à coeur arrêté :
Le donneur à coeur arrêté « contrôlé » est un malade qui a subi des lésions cérébrales irréversibles secondaires à un traumatisme ou à un infarctus cérébral, qui est hémodynamiquement stable, et est sous ventilation mécanique. Pour ce type de donneurs, les parents ont autorisé l'arrêt de la ventilation artificielle et le prélèvement des organes dès la survenue de l'arrêt cardio-respiratoire.
Des canules sont placées dans les vaisseaux fémoraux. Après arrêt de la ventilation, dès l'arrêt cardio-respiratoire, le donneur est immédiatement refroidi via les canules vasculaires. Puis les organes sont prélevés selon les techniques classiques. Les foies provenant de ce type de donneurs sont habituellement d'excellente qualité [86].
Le donneur à coeur arrêté « non contrôlé » est un malade chez qui l'arrêt cardiaque est survenu avant l'arrêt de la ventilation artificielle, pendant le transport vers l'hôpital, aux urgences, ou aux soins intensifs. Le malade n'a pu être réanimé et est décédé d'un arrêt cardio-respiratoire.
Chez ce type de donneurs, les canules fémorales sont mises en place sur les lieux de l'arrêt cardiaque, et le refroidissement des organes est débuté le plus vite possible. Mais l'autorisation des parents, non encore obtenue, doit être sollicitée
avant d'effectuer le prélèvement. Les foies prélevés chez ce type de donneurs ne fonctionnent pas dans plus de 75 % des cas [86].
Les travaux actuels suggèrent que la durée d'ischémie chaude d'un foie à prélever ne devrait pas excéder 30 minutes entre la survenue de l'arrêt cardio-respiratoire et le début du refroidissement du foie avec la solution de conservation [87].
Critères liés aux antécédents du donneur :
Les antécédents du donneur permettent d'évaluer la fonction des organes et le risque de transmission de maladies infectieuses ou tumorales [88]:
Des antécédents de maladies neurologiques dégénératives ou démyélinisantes du système nerveux central telles que la sclérose en plaques, la démence sénile, ou la maladie d'Alzheimer, contre-indiquent le don d'organes car une origine virale est possible.
Une maladie inflammatoire de l'intestin doit faire rechercher une cholangite sclérosante dont l'effet serait désastreux sur le fonctionnement du greffon hépatique.
L'alcoolisme influence la qualité des greffons mais il ne contre-indique le prélèvement que s'il existe des signes de maladie hépatique chronique.
Les recommandations actuelles concernant l'utilisation de donneurs ayant des antécédents de tumeur maligne tiennent compte de l'ancienneté et du caractère extra ou intracérébral de la lésion.
Sérologie du donneur :
1. Ac anti Hbs + avec AgHbs – et Ac antiHbc – ou + :
Si l’anticorps antiHbc est absent, le don d’organe n’est pas contre indiqué [89]. Alors en cas de sa séropositivité, cela traduit la guérison et l'immunisation contre l'infection au virus de l'hépatite B (VHB). Cependant, malgré la guérison, le virus peut encore être présent dans le foie du donneur et se répliquer chez le receveur sous l'influence de l'immunosuppression [88].
2. Seul l’Ac antiHbc est positif :
Pour certains auteurs, un tel profil sérologique est une contre-indication au don du foie [89]. En effet, 80 % des donneurs ayant un anticorps antiHbc positif (AgHbs négatif) transmettent le virus de l'hépatite B en l'absence de traitement prophylactique du receveur.
Cependant, certaines équipes [90] n’excluent pas ces donneurs à condition que leurs foies soient utilisés selon des critères stricts.
3. Ac anti VHC :
La plupart des équipes considèrent que la présence d'un anticorps anti-VHC est une contre-indication à l'acceptation du foie [89].
Certains auteurs autorisent l’utilisation du greffon provenant des donneurs anti-VHC si les receveurs ont une cirrhose post virale C en dernier stade. Pourvu que histologiquement il n’y a pas de progression de la maladie [91].
4. Ac anti CMV :
La détection d'un anticorps anti-CMV chez le donneur ou le receveur traduit la présence latente du cytomégalovirus. Le statut anticorps CMV positif n'est pas une contre-indication au don du foie. Cependant, les statuts CMV du donneur et du receveur doivent être connus afin d'initier une prophylaxie anti-CMV chez les receveurs séronégatifs [88].
5. autres :
Le don d’organe n’est pas contre indiqué en cas de présence d’Ac anti syphilis, EBV positif ou la toxoplasmose mais certaines précautions doivent être maintenus : en cas de présence d’Ac anti syphilis, il faut traiter le receveur pendant 15 jours [89], éviter la transmission de toxoplasmose par l’administration de triméthoprime sulfaméthoxazole [88]. La séropositivité d’EBV impose une surveillance et un traitement précoce du syndrome lymphoprolifératif [89].
Critères liés à l’âge :
Quel est l'effet de l'âge sur la morphologie et la fonction du foie ? Le foie « âgé » tolère t-il les lésions liées à l'hypothermie, l'ischémie et la reperfusion ? La régénération hépatique est-elle conservée avec l'âge ? Quels risques court le receveur d'un foie « jeune » ?
Les travaux actuels [92] montrent les modifications du foie liées à l'âge se résument à une réduction de la masse, du flux sanguin, et à une capsule hépatique plus fibreuse.