ROYAUME DU MAROC UNIVERSITE MOHAMED V FACULTE DE MEDECINE ET DE PHARMACIE RABAT
Année: 2020
Infection à BK virus en transplantation rénale
:
Expérience du Centre Hospitalo-Universitaire Ibn Sina de Rabat
Présenté par :
Dr. Latifa DRIOUCH
MEMOIRE POUR L’OBTENTION DU
DIPLOME DE SPECIALITE
EN NEPHROLOGIE
Sous la direction de :
Professeur Tarik BOUATTARDOYENS HONORAIRES :
1962 – 1969: Professeur Abdelmalek FARAJ 1969 – 1974: Professeur Abdellatif BERBICH 1974 – 1981: Professeur Bachir LAZRAK 1981 – 1989: Professeur Taieb CHKILI
1989 – 1997: Professeur Mohamed Tahar ALAOUI 1997 – 2003: Professeur Abdelmajid BELMAHI 2003 - 2013: Professeur Najia HAJJAJ – HASSOUNI
ADMINISTRATION :
Doyen Professeur Mohamed ADNAOUI
Vice-Doyen chargé des Affaires Académiques et Estudiantines Professeur Brahim LEKEHAL
Vice-Doyen chargé de la Recherche et de la Coopération Professeur Toufiq DAKKA
Vice-Doyen chargé des Affaires Spécifiques à la Pharmacie Professeur Younes RAHALI
Secrétaire Général
1 - ENSEIGNANTS-CHERCHEURS MEDECINS ET PHARMACIENS PROFESSEURS DE L’ENSEIGNEMENT SUPERIEUR :
Décembre 1984
Pr. MAAOUNI Abdelaziz Médecine Interne – Clinique Royale
Pr. MAAZOUZI Ahmed Wajdi Anesthésie -Réanimation
Pr. SETTAF Abdellatif Pathologie Chirurgicale
Décembre 1989
Pr. ADNAOUI Mohamed Médecine Interne –Doyen de la FMPR
Pr. OUAZZANI Taïbi Mohamed Réda Neurologie Janvier et Novembre 1990
Pr. KHARBACH Aîcha Gynécologie -Obstétrique
Pr. TAZI Saoud Anas Anesthésie Réanimation
Février Avril Juillet et Décembre 1991
Pr. AZZOUZI Abderrahim Anesthésie Réanimation- Doyen de
FMPO
Pr. BAYAHIA Rabéa Néphrologie
Pr. BELKOUCHI Abdelkader Chirurgie Générale
Pr. BENCHEKROUN Belabbes Abdellatif Chirurgie Générale
Pr. BENSOUDA Yahia Pharmacie galénique
Pr. BERRAHO Amina Ophtalmologie
Pr. BEZAD Rachid Gynécologie Obstétrique Méd. Chef Maternité
des Orangers
Pr. CHERRAH Yahia Pharmacologie
Pr. CHOKAIRI Omar Histologie Embryologie
Pr. KHATTAB Mohamed Pédiatrie
Pr. SOULAYMANI Rachida Pharmacologie- Dir. du Centre National PV Rabat
Pr. TAOUFIK Jamal Chimie thérapeutique
Décembre 1992
Pr. AHALLAT Mohamed Chirurgie Générale Doyen de FMPT
Pr. BENSOUDA Adil Anesthésie Réanimation
Pr. CHAHED OUAZZANI Laaziza Gastro-Entérologie
Pr. CHRAIBI Chafiq Gynécologie Obstétrique
Pr. EL OUAHABI Abdessamad Neurochirurgie
Pr. FELLAT Rokaya Cardiologie
Pr. JIDDANE Mohamed Anatomie
Pr. TAGHY Ahmed Chirurgie Générale
Mars 1994
Pr. BENJAAFAR Noureddine Radiothérapie
Pr. BEN RAIS Nozha Biophysique
Pr. CAOUI Malika Biophysique
Pr. CHRAIBI Abdelmjid Endocrinologie et Maladies Métaboliques
Doyen de la FMPA
Pr. EL AMRANI Sabah Gynécologie Obstétrique
Pr. ERROUGANI Abdelkader Chirurgie Générale–Directeur du CHIS
Pr. ESSAKALI Malika Immunologie
Pr. ETTAYEBI Fouad Chirurgie Pédiatrique
Pr. IFRINE Lahssan Chirurgie Générale
Pr. RHRAB Brahim Gynécologie –Obstétrique
Pr. SENOUCI Karima Dermatologie
Mars 1994
Pr. ABBAR Mohamed* Urologie Inspecteur du SSM
Pr. BENTAHILA Abdelali Pédiatrie
Pr. BERRADA Mohamed Saleh Traumatologie – Orthopédie
Pr. CHERKAOUI Lalla Ouafae Ophtalmologie
Pr. LAKHDAR Amina Gynécologie Obstétrique
Pr. MOUANE Nezha Pédiatrie
Mars 1995
Pr. ABOUQUAL Redouane Réanimation Médicale
Pr. AMRAOUI Mohamed Chirurgie Générale
Pr. BAIDADA Abdelaziz Gynécologie Obstétrique
Pr. BARGACH Samir Gynécologie Obstétrique
Pr. EL MESNAOUI Abbes Chirurgie Générale
Pr. ESSAKALI HOUSSYNI Leila Oto-Rhino-Laryngologie
Pr. IBEN ATTYA ANDALOUSSI Ahmed Urologie
Pr. OUAZZANI CHAHDI Bahia Ophtalmologie
Pr. SEFIANI Abdelaziz Génétique
Pr. ZEGGWAGH Amine Ali Réanimation Médicale
Décembre 1996
Pr. BELKACEM Rachid Chirurgie Pédiatrie
Pr. BOULANOUAR Abdelkrim Ophtalmologie
Pr. EL ALAMI EL FARICHA EL Hassan Chirurgie Générale
Pr. GAOUZI Ahmed Pédiatrie
Pr. OUZEDDOUN Naima Néphrologie
Novembre 1997
Pr. ALAMI Mohamed Hassan Gynécologie-Obstétrique
Pr. BIROUK Nazha Neurologie
Pr. FELLAT Nadia Cardiologie
Pr. KADDOURI Noureddine Chirurgie Pédiatrique
Pr. KOUTANI Abdellatif Urologie
Pr. LAHLOU Mohamed Khalid Chirurgie Générale
Pr. MAHRAOUI CHAFIQ Pédiatrie
Pr. TOUFIQ Jallal Psychiatrie Directeur Hôp.Ar-razi Salé
Pr. YOUSFI MALKI Mounia Gynécologie Obstétrique
Novembre 1998
Pr. BENOMAR ALI Neurologie Doyen de la FMP Abulcassis
Pr. BOUGTAB Abdesslam Chirurgie Générale
Pr. ER RIHANI Hassan Oncologie Médicale
Pr. BENKIRANE Majid* Hématologie
Janvier 2000
Pr. ABID Ahmed* Pneumo-phtisiologie
Pr. AIT OUAMAR Hassan Pédiatrie
Pr. BENJELLOUN Dakhama Badr.Sououd Pédiatrie
Pr. BOURKADI Jamal-Eddine Pneumo-phtisiologie Directeur Hôp. My Youssef
Pr. CHARIF CHEFCHAOUNI Al Montacer Chirurgie Générale
Pr. ECHARRAB El Mahjoub Chirurgie Générale
Pr. EL FTOUH Mustapha Pneumo-phtisiologie
Pr. EL MOSTARCHID Brahim* Neurochirurgie
Pr. TACHINANTE Rajae Anesthésie-Réanimation
Pr. TAZI MEZALEK Zoubida Médecine Interne
Novembre 2000
Pr. AIDI Saadia Neurologie
Pr. AJANA Fatima Zohra Gastro-Entérologie
Pr. BENAMR Said Chirurgie Générale
Pr. CHERTI Mohammed Cardiologie
Pr. ECH-CHERIF EL KETTANI Selma Anesthésie-Réanimation
Pr. EL HASSANI Amine Pédiatrie -Directeur Hôp.Cheikh Zaid
Pr. EL KHADER Khalid Urologie
Pr. GHARBI Mohamed El Hassan Endocrinologie et Maladies Métaboliques
Décembre 2001
Pr. BALKHI Hicham* Anesthésie-Réanimation
Pr. BENABDELJLIL Maria Neurologie
Pr. BENAMAR Loubna Néphrologie
Pr. BENAMOR Jouda Pneumo-phtisiologie
Pr. BENELBARHDADI Imane Gastro-Entérologie
Pr. BENNANI Rajae Cardiologie
Pr. BENOUACHANE Thami Pédiatrie
Pr. BEZZA Ahmed* Rhumatologie
Pr. BOUCHIKHI IDRISSI Med Larbi Anatomie
Pr. BOUMDIN El Hassane* Radiologie
Pr. CHAT Latifa Radiologie
Pr. DAALI Mustapha* Chirurgie Générale
Pr. EL HIJRI Ahmed Anesthésie-Réanimation
Pr. EL MAAQILI Moulay Rachid Neuro-Chirurgie
Pr. EL MADHI Tarik Chirurgie-Pédiatrique
Pr. EL OUNANI Mohamed Chirurgie Générale
Pr. ETTAIR Said Pédiatrie Directeur Hôp. Univ. Cheikh
Khalifa
Pr. GAZZAZ Miloudi* Neuro-Chirurgie
Pr. HRORA Abdelmalek Chirurgie Générale Directeur Hôp Ibn Sina
Pr. KABIRI EL Hassane* Chirurgie Thoracique
Pr. LAMRANI Moulay Omar Traumatologie Orthopédie
Pr. LEKEHAL Brahim Chirurgie Vasculaire Périphérique V-D
chargé Aff Acad. Est.
Pr. MEDARHRI Jalil Chirurgie Générale
Pr. MIKDAME Mohammed* Hématologie Clinique
Pr. MOHSINE Raouf Chirurgie Générale
Pr. NOUINI Yassine Urologie
Pr. SABBAH Farid Chirurgie Générale
Pr. SEFIANI Yasser Chirurgie Vasculaire Périphérique
Pr. TAOUFIQ BENCHEKROUN Soumia Pédiatrie
Décembre 2002
Pr. AL BOUZIDI Abderrahmane* Anatomie Pathologique
Pr. AMEUR Ahmed * Urologie
Pr. AMRI Rachida Cardiologie
Pr. AOURARH Aziz* Gastro-Entérologie Dir.-Adj. HMI Mohammed V
Pr. BAMOU Youssef * Biochimie-Chimie
Pr. BELMEJDOUB Ghizlene* Endocrinologie et Maladies Métaboliques
Pr. BENZEKRI Laila Dermatologie
Pr. BENZZOUBEIR Nadia Gastro-Entérologie
Pr. CHOHO Abdelkrim * Chirurgie Générale
Pr. CHKIRATE Bouchra Pédiatrie
Pr. EL ALAMI EL Fellous Sidi Zouhair Chirurgie Pédiatrique
Pr. EL HAOURI Mohamed * Dermatologie
Pr. FILALI ADIB Abdelhai Gynécologie Obstétrique
Pr. HAJJI Zakia Ophtalmologie
Pr. JAAFAR Abdeloihab* Traumatologie Orthopédie
Pr. KRIOUILE Yamina Pédiatrie
Pr. MOUSSAOUI RAHALI Driss* Gynécologie Obstétrique
Pr. OUJILAL Abdelilah Oto-Rhino-Laryngologie
Pr. RAISS Mohamed Chirurgie Générale
Pr. SIAH Samir * Anesthésie Réanimation
Pr. THIMOU Amal Pédiatrie
Pr. ZENTAR Aziz* Chirurgie Générale
Janvier 2004
Pr. ABDELLAH El Hassan Ophtalmologie
Pr. AMRANI Mariam Anatomie Pathologique
Pr. BENBOUZID Mohammed Anas Oto-Rhino-Laryngologie
Pr. BENKIRANE Ahmed* Gastro-Entérologie
Pr. BOULAADAS Malik Stomatologie et Chirurgie Maxillo-faciale
Pr. BOURAZZA Ahmed* Neurologie
Pr. CHAGAR Belkacem* Traumatologie Orthopédie
Pr. CHERRADI Nadia Anatomie Pathologique
Pr. EL FENNI Jamal* Radiologie
Pr. EL HANCHI ZAKI Gynécologie Obstétrique
Pr. EL KHORASSANI Mohamed Pédiatrie
Pr. HACHI Hafid Chirurgie Générale
Pr. JABOUIRIK Fatima Pédiatrie
Pr. KHARMAZ Mohamed Traumatologie Orthopédie
Pr. MOUGHIL Said Chirurgie Cardio-Vasculaire
Pr. OUBAAZ Abdelbarre * Ophtalmologie
Pr. TARIB Abdelilah* Pharmacie Clinique
Pr. TIJAMI Fouad Chirurgie Générale
Pr. ZARZUR Jamila Cardiologie
Janvier 2005
Pr. ABBASSI Abdellah Chirurgie Réparatrice et Plastique
Pr. ALLALI Fadoua Rhumatologie
Pr. AMAZOUZI Abdellah Ophtalmologie
Pr. BAHIRI Rachid Rhumatologie Directeur Hôp. Al Ayachi Salé
Pr. BARKAT Amina Pédiatrie
Pr. BENYASS Aatif Cardiologie
Pr. HAJJI Leila Cardiologie (mise en disponibilité)
Pr. HESSISSEN Leila Pédiatrie
Pr. JIDAL Mohamed* Radiologie
Pr. LAAROUSSI Mohamed Chirurgie Cardio-vasculaire
Pr. LYAGOUBI Mohammed Parasitologie
Pr. SBIHI Souad Histo-Embryologie Cytogénétique
Pr. ZERAIDI Najia Gynécologie Obstétrique
AVRIL 2006
Pr. ACHEMLAL Lahsen* Rhumatologie
Pr. BELMEKKI Abdelkader* Hématologie
Pr. BENCHEIKH Razika O.R.L
Pr. BIYI Abdelhamid* Biophysique
Pr. BOUHAFS Mohamed El Amine Chirurgie - Pédiatrique
Pr. BOULAHYA Abdellatif* Chirurgie Cardio – Vasculaire. Directeur Hôpital Ibn Sina Mar
Pr. CHENGUETI ANSARI Anas Gynécologie Obstétrique
Pr. DOGHMI Nawal Cardiologie
Pr. FELLAT Ibtissam Cardiologie
Pr. FAROUDY Mamoun Anesthésie Réanimation
Pr. HARMOUCHE Hicham Médecine Interne
Pr. IDRISS LAHLOU Amine* Microbiologie
Pr. JROUNDI Laila Radiologie
Pr. KARMOUNI Tariq Urologie
Pr. KILI Amina Pédiatrie
Pr. KISRA Hassan Psychiatrie
Pr. KISRA Mounir Chirurgie – Pédiatrique
Pr. LAATIRIS Abdelkader* Pharmacie Galénique
Pr. LMIMOUNI Badreddine* Parasitologie
Pr. MANSOURI Hamid* Radiothérapie
Pr. OUANASS Abderrazzak Psychiatrie
Pr. SAFI Soumaya* Endocrinologie
Pr. SOUALHI Mouna Pneumo – Phtisiologie
Pr. TELLAL Saida* Biochimie
Pr. ZAHRAOUI Rachida Pneumo – Phtisiologie
Octobre 2007
Pr. ABIDI Khalid Réanimation médicale
Pr. ACHACHI Leila Pneumo phtisiologie
Pr. ACHOUR Abdessamad* Chirurgie générale
Pr. AIT HOUSSA Mahdi * Chirurgie cardio vasculaire
Pr. AMHAJJI Larbi * Traumatologie orthopédie
Pr. BAITE Abdelouahed * Anesthésie réanimation
Pr. BALOUCH Lhousaine * Biochimie-chimie
Pr. BENZIANE Hamid * Pharmacie clinique
Pr. BOUTIMZINE Nourdine Ophtalmologie
Pr. CHERKAOUI Naoual * Pharmacie galénique
Pr. EHIRCHIOU Abdelkader * Chirurgie générale
Pr. EL BEKKALI Youssef * Chirurgie cardio-vasculaire
Pr. EL ABSI Mohamed Chirurgie générale
Pr. EL MOUSSAOUI Rachid Anesthésie réanimation
Pr. EL OMARI Fatima Psychiatrie
Pr. GHARIB Noureddine Chirurgie plastique et réparatrice
Pr. HADADI Khalid * Radiothérapie
Pr. ICHOU Mohamed * Oncologie médicale
Pr. ISMAILI Nadia Dermatologie
Pr. KEBDANI Tayeb Radiothérapie
Pr. LOUZI Lhoussain * Microbiologie
Pr. MADANI Naoufel Réanimation médicale
Pr. MAHI Mohamed * Radiologie
Pr. MARC Karima Pneumo phtisiologie
Pr. MASRAR Azlarab Hématologie biologique
Pr. MRANI Saad * Virologie
Pr. OUZZIF Ez zohra * Biochimie-chimie
Pr. RABHI Monsef * Médecine interne
Pr. RADOUANE Bouchaib* Radiologie
Pr. SEFFAR Myriame Microbiologie
Pr. SEKHSOKH Yessine * Microbiologie
Pr. SIFAT Hassan * Radiothérapie
Pr. TABERKANET Mustafa * Chirurgie vasculaire périphérique
Pr. TACHFOUTI Samira Ophtalmologie
Pr. TAJDINE Mohammed Tariq* Chirurgie générale
Pr. TANANE Mansour * Traumatologie-orthopédie
Pr. TLIGUI Houssain Parasitologie
Pr. TOUATI Zakia Cardiologie
Mars 2009
Pr. ABOUZAHIR Ali * Médecine interne
Pr. AGADR Aomar * Pédiatrie
Pr. AIT ALI Abdelmounaim * Chirurgie Générale
Pr. AKHADDAR Ali * Neuro-chirurgie
Pr. ALLALI Nazik Radiologie
Pr. AMINE Bouchra Rhumatologie
Pr. ARKHA Yassir Neuro-chirurgie Directeur Hôp.des
Spécialités
Pr. BELYAMANI Lahcen * Anesthésie Réanimation
Pr. BOUHSAIN Sanae * Biochimie-chimie
Pr. BOUI Mohammed * Dermatologie
Pr. BOUNAIM Ahmed * Chirurgie Générale
Pr. BOUSSOUGA Mostapha * Traumatologie-orthopédie
Pr. CHTATA Hassan Toufik * Chirurgie Vasculaire Périphérique
Pr. DOGHMI Kamal * Hématologie clinique
Pr. EL MALKI Hadj Omar Chirurgie Générale
Pr. EL OUENNASS Mostapha* Microbiologie
Pr. ENNIBI Khalid * Médecine interne
Pr. FATHI Khalid Gynécologie obstétrique
Pr. HASSIKOU Hasna * Rhumatologie
Pr. KABBAJ Nawal Gastro-entérologie
Pr. KABIRI Meryem Pédiatrie
Pr. KARBOUBI Lamya Pédiatrie
Pr. LAMSAOURI Jamal * Chimie Thérapeutique
Pr. MARMADE Lahcen Chirurgie Cardio-vasculaire
Pr. MESKINI Toufik Pédiatrie
Pr. MESSAOUDI Nezha * Hématologie biologique
Pr. MSSROURI Rahal Chirurgie Générale
Pr. NASSAR Ittimade Radiologie
Pr. OUKERRAJ Latifa Cardiologie
Pr. RHORFI Ismail Abderrahmani * Pneumo-Phtisiologie Octobre 2010
Pr. ALILOU Mustapha Anesthésie réanimation
Pr. AMEZIANE Taoufiq* Médecine Interne Directeur ERSSM
Pr. BELAGUID Abdelaziz Physiologie
Pr. CHADLI Mariama* Microbiologie
Pr. CHEMSI Mohamed* Médecine Aéronautique
Pr. DAMI Abdellah* Biochimie- Chimie
Pr. DARBI Abdellatif* Radiologie
Pr. DENDANE Mohammed Anouar Chirurgie Pédiatrique
Pr. EL HAFIDI Naima Pédiatrie
Pr. EL KHARRAS Abdennasser* Radiologie
Pr. EL MAZOUZ Samir Chirurgie Plastique et Réparatrice
Pr. EL SAYEGH Hachem Urologie
Pr. ERRABIH Ikram Gastro-Entérologie
Pr. LAMALMI Najat Anatomie Pathologique
Pr. MOSADIK Ahlam Anesthésie Réanimation
Pr. MOUJAHID Mountassir* Chirurgie Générale
Pr. NAZIH Mouna* Hématologie
Decembre 2010
Pr. ZNATI Kaoutar Anatomie Pathologique
Mai 2012
Pr. AMRANI Abdelouahed Chirurgie pédiatrique
Pr. ABOUELALAA Khalil * Anesthésie Réanimation
Pr. BENCHEBBA Driss * Traumatologie-orthopédie
Pr. DRISSI Mohamed * Anesthésie Réanimation
Pr. EL ALAOUI MHAMDI Mouna Chirurgie Générale
Pr. EL OUAZZANI Hanane * Pneumophtisiologie
Pr. ER-RAJI Mounir Chirurgie Pédiatrique
Pr. JAHID Ahmed Anatomie Pathologique
Pr. RAISSOUNI Maha * Cardiologie
Février 2013
Pr. AHID Samir Pharmacologie
Pr. AIT EL CADI Mina Toxicologie
Pr. AMRANI HANCHI Laila Gastro-Entérologie
Pr. AMOR Mourad Anesthésie Réanimation
Pr. AWAB Almahdi Anesthésie Réanimation
Pr. BELAYACHI Jihane Réanimation Médicale
Pr. BELKHADIR Zakaria Houssain Anesthésie Réanimation
Pr. BENCHEKROUN Laila Biochimie-Chimie
Pr. BENKIRANE Souad Hématologie
Pr. BENNANA Ahmed* Informatique Pharmaceutique
Pr. BENSGHIR Mustapha * Anesthésie Réanimation
Pr. BENYAHIA Mohammed * Néphrologie
Pr. BOUATIA Mustapha Chimie Analytique et Bromatologie
Pr. BOUABID Ahmed Salim* Traumatologie orthopédie
Pr. BOUTARBOUCH Mahjouba Anatomie
Pr. CHAIB Ali * Cardiologie
Pr. DENDANE Tarek Réanimation Médicale
Pr. DINI Nouzha * Pédiatrie
Pr. ECH-CHERIF EL KETTANI Mohamed Ali Anesthésie Réanimation Pr. ECH-CHERIF EL KETTANI Najwa Radiologie
Pr. ELFATEMI Nizare Neuro-chirurgie
Pr. EL GUERROUJ Hasnae Médecine Nucléaire
Pr. EL HARTI Jaouad Chimie Thérapeutique
Pr. EL JAOUDI Rachid * Toxicologie
Pr. EL KABABRI Maria Pédiatrie
Pr. EL KHANNOUSSI Basma Anatomie Pathologique
Pr. EL KORAICHI Alae Anesthésie Réanimation
Pr. EN-NOUALI Hassane * Radiologie
Pr. ERRGUIG Laila Physiologie
Pr. FIKRI Meryem Radiologie
Pr. GHFIR Imade Médecine Nucléaire
Pr. IMANE Zineb Pédiatrie
Pr. IRAQI Hind Endocrinologie et maladies métaboliques
Pr. KABBAJ Hakima Microbiologie
Pr. KADIRI Mohamed * Psychiatrie
Pr. LATIB Rachida Radiologie
Pr. MAAMAR Mouna Fatima Zahra Médecine Interne
Pr. MEDDAH Bouchra Pharmacologie
Pr. MELHAOUI Adyl Neuro-chirurgie
Pr. MRABTI Hind Oncologie Médicale
Pr. NEJJARI Rachid Pharmacognosie
Pr. OUBEJJA Houda Chirugie Pédiatrique
Pr. OUKABLI Mohamed * Anatomie Pathologique
Pr. RAHALI Younes Pharmacie Galénique Vice-Doyen à la
Pharmacie
Pr. RATBI Ilham Génétique
Pr. RAHMANI Mounia Neurologie
Pr. REDA Karim * Ophtalmologie
Pr. REGRAGUI Wafa Neurologie
Pr. RKAIN Hanan Physiologie
Pr. ROSTOM Samira Rhumatologie
Pr. ROUAS Lamiaa Anatomie Pathologique
Pr. ROUIBAA Fedoua * Gastro-Entérologie
Pr SALIHOUN Mouna Gastro-Entérologie
Pr. SAYAH Rochde Chirurgie Cardio-Vasculaire
Pr. SEDDIK Hassan * Gastro-Entérologie
Pr. ZERHOUNI Hicham Chirurgie Pédiatrique
Pr. ZINE Ali * Traumatologie Orthopédie
AVRIL 2013
Pr. EL KHATIB MOHAMED KARIM * Stomatologie et Chirurgie Maxillo-faciale
MARS 2014
Pr. ACHIR Abdellah Chirurgie Thoracique
Pr. BENCHAKROUN Mohammed * Traumatologie- Orthopédie
Pr. BOUCHIKH Mohammed Chirurgie Thoracique
Pr. EL KABBAJ Driss * Néphrologie
Pr. HARDIZI Houyam Histologie- Embryologie-Cytogénétique
Pr. HASSANI Amale * Pédiatrie
Pr. HERRAK Laila Pneumologie
Pr. JANANE Abdellah * Urologie
Pr. JEAIDI Anass * Hématologie Biologique
Pr. KOUACH Jaouad* Génycologie-Obstétrique
Pr. LEMNOUER Abdelhay* Microbiologie
Pr. MAKRAM Sanaa * Pharmacologie
Pr. OULAHYANE Rachid* Chirurgie Pédiatrique
Pr. RHISSASSI Mohamed Jaafar CCV
Pr. SEKKACH Youssef* Médecine Interne
Pr. TAZI MOUKHA Zakia Génécologie-Obstétrique
DECEMBRE 2014
Pr. ABILKACEM Rachid* Pédiatrie
Pr. AIT BOUGHIMA Fadila Médecine Légale
Pr. BEKKALI Hicham * Anesthésie-Réanimation
Pr. BENAZZOU Salma Chirurgie Maxillo-Faciale
Pr. BOUABDELLAH Mounya Biochimie-Chimie
Pr. BOUCHRIK Mourad* Parasitologie
Pr. DERRAJI Soufiane* Pharmacie Clinique
Pr. DOBLALI Taoufik Microbiologie
Pr. EL AYOUBI EL IDRISSI Ali Anatomie
Pr. EL GHADBANE Abdedaim Hatim* Anesthésie-Réanimation
Pr. EL MARJANY Mohammed* Radiothérapie
Pr. FEJJAL Nawfal Chirurgie Réparatrice et Plastique
Pr. JAHIDI Mohamed* O.R.L
Pr. LAKHAL Zouhair* Cardiologie
Pr. OUDGHIRI NEZHA Anesthésie-Réanimation
Pr. RAMI Mohamed Chirurgie Pédiatrique
Pr. SABIR Maria Psychiatrie
Pr. SBAI IDRISSI Karim* Médecine préventive, santé publique et Hyg. AOUT 2015
Pr. MEZIANE Meryem Dermatologie
Pr. TAHIRI Latifa Rhumatologie
PROFESSEURS AGREGES : JANVIER 2016
Pr. BENKABBOU Amine Chirurgie Générale
Pr. EL ASRI Fouad* Ophtalmologie
Pr. ERRAMI Noureddine* O.R.L
JUIN 2017
Pr. ABBI Rachid* Microbiologie
Pr. ASFALOU Ilyasse* Cardiologie
Pr. BOUAYTI El Arbi* Médecine préventive, santé publique et Hyg.
Pr. BOUTAYEB Saber Oncologie Médicale
Pr. EL GHISSASSI Ibrahim Oncologie Médicale
Pr. HAFIDI Jawad Anatomie
Pr. OURAINI Saloua* O.R.L
Pr. RAZINE Rachid Médecine préventive, santé publique et Hyg.
Pr. ZRARA Abdelhamid* Immunologie
NOVEMBRE 2018
Pr. AMELLAL Mina Anatomie
Pr. SOULY Karim Microbiologie
Pr. TAHRI Rajae Histologie-Embryologie-Cytogénétique
NOVEMBRE 2019
Pr. AATIF Taoufiq * Néphrologie
Pr. ACHBOUK Abdelhafid * Chirurgie Réparatrice et Plastique Pr. ANDALOUSSI SAGHIR Khalid * Radiothérapie
Pr. BABA HABIB Moulay Abdellah * Gynécologie-obstétrique
Pr. BASSIR RIDA ALLAH Anatomie
Pr. BOUATTAR TARIK Néphrologie
Pr. BOUFETTAL MONSEF Anatomie
Pr. BOUCHENTOUF Sidi Mohammed * Chirurgie Générale
Pr. BOUZELMAT Hicham * Cardiologie
Pr. BOUKHRIS Jalal * Traumatologie-orthopédie
Pr. CHAFRY Bouchaib * Traumatologie-orthopédie
Pr. CHAHDI Hafsa * Anatolmie Pathologique
Pr. CHERIF EL ASRI Abad * Neurochirugie
Pr. DAMIRI Amal * Anatolmie Pathologique
Pr. DOGHMI Nawfal * Anesthésie-réanimation
Pr. ELALAOUI Sidi-Yassir Pharmacie Galénique
Pr. EL ANNAZ Hicham * Virologie
Pr. EL HASSANI Moulay EL Mehdi * Gynécologie-obstétrique
Pr. EL HJOUJI Aabderrahman * Chirurgie Générale
Pr. EL KAOUI Hakim * Chirurgie Générale
Pr. EL WALI Abderrahman * Anesthésie-réanimation
Pr. EN-NAFAA Issam * Radiologie
Pr. JIRA Mohamed * Médecine Interne
Pr. JNIENE Asmaa Physiologie
Pr. LARAQUI Hicham * Chirurgie Générale
Pr. MAHFOUD Tarik * Oncologie Médicale
Pr. MEZIANE Mohammed * Anesthésie-réanimation
Pr. MOUTAKI ALLAH Younes * Chirurgie Cardio-vasculaire
Pr. MOUZARI Yassine * Ophtalmologie
Pr. NAOUI Hafida * Parasitologie-Mycologie
Pr. OBTEL Majdouline Médecine préventive, santé publique et Hyg.
Pr. OURRAI Abdelhakim * Pédiatrie
Pr. SAOUAB Rachida * Radiologie
Pr. SBITTI Yassir * Oncologie Médicale
Pr. ZADDOUG Omar * Traumatologie Orthopédie
Pr. ZIDOUH Saad * Anesthésie-réanimation-
ENSEIGNANTS-CHERCHEURS SCIENTIFIQUES PROFESSEURS/Prs. HABILITES
Pr. ABOUDRAR Saadia Physiologie
Pr. ALAMI OUHABI Naima Biochimie-chimie
Pr. ALAOUI KATIM Pharmacologie
Pr. ALAOUI SLIMANI Lalla Naïma Histologie-Embryologie
Pr. ANSAR M’hammed Chimie Organique et Pharmacie Chimique
Pr .BARKIYOU Malika Histologie-Embryologie
Pr. BOUHOUCHE Ahmed Génétique Humaine
Pr. BOUKLOUZE Abdelaziz Applications Pharmaceutiques
Pr. CHAHED OUAZZANI Lalla Chadia Biochimie-chimie
Pr. DAKKA Taoufiq Physiologie
Pr. FAOUZI Moulay El Abbes Pharmacologie
Pr. IBRAHIMI Azeddine Biologie moléculaire/Biotechnologie
Pr. KHANFRI Jamal Eddine Biologie
Pr. OULAD BOUYAHYA IDRISSI Med Chimie Organique
Pr. REDHA Ahlam Chimie
Pr. TOUATI Driss Pharmacognosie
Pr. YAGOUBI Maamar Environnement,Eau et Hygiène
Pr. ZAHIDI Ahmed Pharmacologie
Mise à jour le 11/06/2020 KHALED Abdellah
Chef du Service des Ressources Humaines FMPR
A TOUS MES MAÎTRES
Nous vous remercions d’avoir partagé avec nous votre
passion pour la néphrologie, vous avez guidé nos pas
durant toutes ces années. Nous resterons à jamais
reconnaissants.
Table des matières :
Abréviation ………..3
Introduction……… .5
Rappels virologiques et pathogénie du BK virus……… ..7
Matériel et méthodes……… ..14
Résultats………. ..17
I. Etude descriptive
Caractéristiques initiales des patients……….… ...18Diagnostic et délai de réplication ……….20
Immunosuppression initiale et au diagnostic de l’infection BKv……… …22
Description histologique………23
Prise en charge de l’infection ………24
Négativité du BK virus …….………24
Survie du greffon ...….……….………26
II. Etude analytique
...….……….………..27Discussion Incidence et délai de survenue de la réplication ………30
Facteurs de risque de réplication de BK virus après la greffe rénale……….30
Diagnostic de l’infection à BKv ………31
Prise en charge de l’infection à BKv ……….………33
Survie et perte du greffon ……….……….35
Prévention de l’infection à BKv ………….……….………..36
Conclusion………….……….…….………..37
Références………….……….…….………..40
Liste des abréviations :
AZA : Azathioprine BK virus : Polyomavirus BK CH : cystite hémorragique CMV : Cytomegalovirus CTC : corticoïdeDFG : Débit de filtration glomérulaire DSA : Donor Specific Antigéne EME : Etat de mort encéphalique IS : immunosuppression
MDRD: Modification of Diet in Renal Disease MMF : Mycophénolate Mofétil
NBK virus : Néphropathie au polyomavirus BK PCR : Polymerase Chain Reaction
TR : transplantation rénale VP : protéine virale
Introduction :
Le développement de nouveaux protocoles de traitements immunosuppresseurs en transplantation rénale a permis ces dernières années une meilleure prévention des rejets d’allogreffe et l’amélioration de la survie à court terme du greffon. Néanmoins, la morbi-mortalité liée aux infections virales a parallèlement significativement augmenté dans ce contexte d’immunodéficience majeure.
Le polyomavirus BK (BK virus) est l’un des deux premiers polyomavirus humains identifiés. Le BK virus a été isolé pour la première fois en 1970 à partir des urines d’un patient transplanté de rein, le virus tient son nom des initiales de ce patient [1].
Le BK virus est un exemple type de virus opportuniste, dont le pouvoir pathogène s’exprime quasi-exclusivement dans un contexte d’immunosuppression. Il est responsable de dysfonction sévère du greffon rénal, voire d’une perte du greffon.
Alors que le nombre de patients greffés est en constante augmentation et que de nouveaux traitements immunosuppresseurs sont en développement, le BK virus reste un facteur de morbidité important chez ces patients. Les travaux des dix dernières années ont permis de progresser dans la compréhension des mécanismes d’interactions virus/cellule, mais il reste encore beaucoup d’inconnues dans la physiopathologie de l’infection au niveau d’un organisme, notamment en raison de l’absence de modèle animal.
Il n’existe actuellement pas de prophylaxie ni de traitement antiviral efficace. Seul un monitoring régulier de la virémie et une stratégie préemptive de réduction de l’immunosuppression s’avèrent indispensables en prévention d’une néphropathie à BK virus parfois irréversible. Le contrôle de la réplication du virus apparaît donc depuis une quinzaine d’années un défi majeur en transplantation rénale.
L’évolution à long terme de la fonction du greffon suite au diagnostic d’une infection à BK virus est rarement rapportée dans la littérature. Il en est de même des facteurs pronostiques de survie du greffon dans ce contexte.
L'objectif principal est de décrire l’épidémiologie, le diagnostic et la prise en charge et l’évolution de l'infection à BK Virus en transplantation rénale.
Rappels virologiques et pathogénie du BK virus :
I. Caractéristiques virologiques :Le BK virus appartient à la famille des Polyomaviridae, groupe des Polyomavirus.. Les polyomavirus sont des virus à ADN non enveloppés de petite taille au sein du groupe des papovavirus qui comprend également les papillomavirus. Cinq polyomavirus humains ont été identifiés : le virus BK, le virus JC, le virus KI et le virus WU, et le polyomavirus associé au carcinome des cellules de Merkel [2,3,4,5].
Le BK Virus est constitué d’un ADN bicaténaire d’environ 5000 paires de bases, entoure d’une capsule icosaédrique [5,6]. Son génome comporte 3 régions :
- la région précoce qui comporte la portion de génome transcrite, avec deux protéines de régulation, l’antigène T et l’antigène t.
- la région tardive, cette dernière codant notamment pour les protéines de capside VP1 (la protéine principale), VP2 et VP3, ainsi que la protéine non structurale Agno.
- la région régulatrice non codante (NCCR pour non coding control region), entre la région précoce et la région tardive [7].
Il ne possède pas dans sa machinerie d’ADN polymérase, ce qui implique qu’il utilise les cellules infectées pour la réplication de son ADN. (Figure 1)
Figure 1 :Représentation schématique du génome du BK virus [8] (Agno = agnoprotéine, ORI = origine de réplication, t-Ag = antigène, t, TAg= Antigène T,
II. Histoire naturelle de l’infection : 1. Tropisme viral :
Le tropisme in vivo du virus BK s’exerce vers les cellules épithéliales de diverses origines mais surtout vers les cellules tubulaires rénales avec un tropisme rénal très marqué et vers les cellules endothéliales. [9]. Le virus a également été détecté dans différents tissus (épithéliums rénaux, urothélium, prostate, glandes salivaires), même si les principales cellules cibles de la persistance semblent être les cellules épithéliales rénales. L’ADN viral a également été retrouvé dans des fractions lymphocytaires chez des sujets sains et des sujets en phase d’infection active [2,10]. La présence de récepteurs au BKv à la surface des lymphocytes avait été suggérée par la technique des rosettes [11,12].
2. Cycle de réplication du virus :
La première étape de l’infection correspond à l’attachement de VP1 aux récepteurs de la cellule infectée, au niveau de gangliosides polysialyles sur la surface membranaire. S’ensuit alors une phase d’internalisation par endocytose, puis un transport jusqu’au cytosol via le réticulum endoplasmique, probablement par la voie des microtubules [13]. Puis le génome viral est transporté dans le noyau pour être répliqué, via l’utilisation de VP2 et VP3 et de la voie d’importation utilisant des pores nucléaires [14]. Le génome viral est alors transcrit dans le noyau à l’aide de la machinerie cellulaire de la cellule hôte. Les protéines virales VP1, VP2 et VP3 sont traduites dans le cytoplasme, puis importées dans le noyau, et de nouvelles particules virales sont alors formées. On estime que les nouveaux virions apparaissent dans le noyau de la cellule hôte environ 48h après l’infection [15]. Le mode de transfert de ces nouvelles particules virales en dehors de la cellule est toutefois encore mal compris.
3. Mécanismes de transmission :
L’hypothèse la plus commune est que le BK virus entre par voie oropharyngée, en raison de l’âge précoce de séroconversion (65 à 90 % de séropositifs avant 10 ans) et de la détection d’ADN viral dans la salive et les tissus lymphoïdes de la sphère oropharyngée [16-17]. La détection du virus dans les urines ainsi que dans l’environnement peut également être compatible avec une contamination par voie orale à partir de l’environnement ou de sécrétions infectieuses d’origine humaine [18].
La détection de génome viral dans les cellules mononucléées est un argument en faveur de la possibilité d’une transmission par voie sanguine. Enfin, un cas de transmission nosocomiale au cours d’une greffe de CSH a été décrit en pédiatrie [19], ainsi que la possibilité d’une transmission verticale par voie transplacentaire [12,20].
4. Primo-infection et latence :
La primo-infection à BK virus a lieu dans l’enfance, et est le plus souvent asymptomatique. Les polyomavirus tout comme les virus Herpès sont connus pour établir des latences ou des infections persistantes. Le virus BK est capable de rester latent à l’intérieur de la cellule cible de l’épithélium rénal sous une forme non réplicative ou avec une réplication minimale, selon un mécanisme proche de celui de la famille des Herpesviridae. A l’état latent, le génome du virus BK peut rester sous forme épisomale non intégré dans les cellules cibles de l’épithélium tubulaire rénal [9].
Le site majeur de la persistance virale est l'épithélium du rein (épithéliums de transition, des tubules rénaux, de la capsule de Bowman) et du tractus urinaire [3,21]. La présence de l'ADN du BKv a également été détectée dans divers autres organes (foie, estomac, poumons, parathyroïdes, nodules lymphoïdes), et en particulier dans le cerveau et les cellules mononucléées sanguines [2,10].
5. Réactivation du BK virus :
Des phases de réactivation virales bénignes asymptomatiques peuvent avoir lieu chez les sujets immunocompétents. Par ailleurs, la détection de l’ADN de VP1 dans les cellules du sang serait plutôt associée à une réinfection ou à une réactivation [10] ; ceci s’explique en considérant que l’infection par le virus BK a lieu pendant l’enfance [5,22,23].
La réactivation du BKv chez les personnes immunocompétentes avec la présence du virus dans les urines ne s’accompagne d’aucun symptôme [49].
Le virus BK est un virus opportuniste qui affecte le greffé médullaire et le transplanté rénal. Etant donné les données séro-épidémiologiques du BK virus, ces manifestations cliniques seraient plutôt dues à une réactivation virale qu’à une nouvelle infection. Les viruries symptomatiques sont présentes en transplantation rénale et en greffe de moelle osseuse et associées à une expression clinique de type cystite hémorragique, sténose urétérale, néphrite interstitielle. Au stade SIDA, il peut y avoir des pneumopathies interstitielles à virus BK.
6. Réponse immunitaire au BK virus : 6.1 Immunité innée :
Parmi les effecteurs de la réponse immunitaire innée, les cellules Natural Killer (NK) jouent un rôle important dans le contrôle précoce des infections virales [24]. Les mécanismes qui régulent les fonctions des cellules NK impliquent notamment des récepteurs appelés KIR (Killer cell immunoglubulin-like receptors) et leurs ligands qui sont des molécules HLA de classe I. Une étude rétrospective récente chez des transplantés de rein a mis en évidence un nombre plus élevé de récepteurs KIR activateurs (KIR-DS) et notamment du récepteur KIR3DS1 dans un groupe contrôle par rapport à un groupe de patient ayant développé une néphropathie à BKv [25]. Ce rôle bénéfique de ce récepteur activateur sur le contrôle d’infection n’a pas été retrouvé dans d’autre étude [26], nécessitant une confirmation sur un plus grand nombre de patient.
Des travaux suggèrent que l’inflammation observée dans les lésions de BKv pourrait être liée à l’activation de récepteurs intracellulaires de l’immunité innée tels que TLR3 (Toll-like receptor3) et RIG-1 (Retinoic acid-inducible gene-I) [27].
Le rôle des cellules dendritiques au cours des infections à BKv a également été très peu investigué. Une seule étude, mesurant le nombre de cellules dendritiques myéloïdes dans le sang périphérique, montre des niveaux de cellules dendritiques avant greffe plus faibles chez les patients qui développeront une virémie à BKv [28].
6.2 Immunité humorale :
La réponse humorale consiste en la production d’immunoglobulines G, d’immunoglobulines M, d’immunoglobulines A incluant des anticorps neutralisants et spécifiques des sous-types dirigés contre les déterminants de la protéine majeure de capside VP1 [29].
Dans le cadre de l’allogreffe rénale, la situation est plus complexe, car le virus peut être présent chez le greffon et chez le receveur. Les infections à BKv post-greffe représentent soit des primo-infections, (donneur séropositif vers receveur séronégatif), soit des réactivations (donneur séronégatif vers receveur séropositif), soit des surinfections et/ou réactivations (donneur et receveur séropositifs).
La plupart des observations cas-cohorte sont donc cohérentes avec l’idée que l’immunité antivirale préexistante joue un rôle protecteur contre les réactivations ou surinfections par le BKv dans le cadre de l’allogreffe rénale, chez les patients adultes comme chez les enfants. [30,31,32].
Une autre façon de rechercher un effet de la réponse humorale sur la réplication virale in vivo est de suivre son évolution de façon longitudinale en parallèle de la virémie, ou de la virurie, pendant la période post-greffe. De plus, les auteurs qui ont suivi à la fois la réponse lymphocytaire T et la réponse humorale contre les antigènes du BKv ont conclu que la réponse lymphocytaire T, et non pas la réponse humorale, était associée à la résolution de l’infection [33,34].
6.3 Réponse médiée par les lymphocytes T CD4 et CD8 :
Globalement, la fréquence des lymphocytes T spécifiques du BK virus est plus faible que celle mesurée contre d’autres virus persistants responsables d’infections opportunistes comme le Cytomégalovirus ou l’Epstein-Barr virus. Cette faible fréquence de lymphocytes T fonctionnels circulants pourrait s’expliquer par une réactivation virale limitée au site de persistance du virus (le tractus réno-urinaire), avec pas ou peu de passage sanguin.
L’activité de prolifération lymphocytaire et les taux d’IgG anti-BKv étaient maximaux pour cette même tranche d’âge [35]. Au cours des premiers mois post-transplantation, la réponse T spécifique est très faible chez les patients transplantés de rein en dehors de toute réplication virale [36]. La réponse lymphocytaire T évoluerait en miroir de la virémie, la diminution de la charge virale dans le sang étant associée à une augmentation de la fréquence des lymphocytes T spécifiques [37].
III. Pouvoir pathogène du BK virus :
1. Néphropathie tubulo-interstitielle associée au BK virus (NBK virus) :
La NBK virus est une néphropathie tubulo-interstitielle qui survient quasi-exclusivement dans les 12 à 24 mois suivant une allogreffe de rein mais peut survenir dans des délais variables suivant la transplantation.
Une fois le virus réactivé, il y a une réplication virale intense et prolongée au niveau des cellules épithéliales du rein et du tractus urinaire, les virions s’accumulent dans le noyau des cellules cibles épithéliales rénales sous forme d’inclusions intra-nucléaires. En l’absence de contrôle de l’infection, la réplication virale entraîne un effet cytopathogène marqué et apparaît secondairement une nécrose des cellules infectées, responsable d’une rupture des membranes nucléaires et cytoplasmiques, de l’infiltration virale dans la lumière tubulaire, chambre urinaire avec excrétion urinaire de «decoy cells» et d’hématurie mais aussi l’interstitium, et de la propagation aux cellules environnantes et conduit au passage du virus dans le sang, par lésion de la membrane basale [38,39].
Le début de la maladie est marqué par l’infiltration tissulaire par des cellules inflammatoires, évoluant vers l’atrophie tubulaire et la fibrose interstitielle [40]. L’effet cytopathogène persiste dans 70 % des cas, et le greffon est perdu dans 45 % des cas, et même en cas de contrôle de la virémie, une fibrose séquellaire majeure se développe dans 75 % des cas [41].
2. Cystite hémorragique (CH) :
Le BK virus est un des agents infectieux associé à la survenue de cystite hémorragique, notamment dans le contexte de l’allogreffe de cellules souches hématopoïétiques. La CH est caractérisée par l’association de dysurie et douleurs avec hématurie arrivant à d’hémorragie difficilement contrôlable, et de défaillance rénale. La CH associée au BKv La pathogenèse de la CH à BK virus serait le résultat de plusieurs mécanismes concomitants : les lésions de la muqueuse urothéliale secondaires à certains traitements d’induction, la réactivation virale favorisée par l’immunosuppression et une réaction inflammatoire avec infiltrat lymphocytaire et destruction des cellules infectées [42].
3. Sténose urétérale :
Le BK virus fut initialement isolé chez un patient transplanté de rein présentant une sténose urétérale, et a depuis été régulièrement impliqué dans cette pathologie [12].
4. Oncogénicité :
L’interaction des protéines précoces avec des gènes suppresseurs de tumeur confère un pouvoir oncogène théorique au BK virus, bien que le génome viral ait pu être retrouvé dans des tumeurs, les résultats restent controversés [5,43].
Dans une étude portant sur 1135 cancers de la vessie et 982 témoins, la séroprévalence du BKv était la même dans les deux groupes, mais la séroréactivité du BK virus était significativement plus élevée dans les cancers que chez les témoins, ce qui suggère une association [44].
A ce jour, aucun argument formel ne permet de conclure que BK virus soit impliqué directement dans les processus cancéreux humains ou qu’il agirait plutôt comme cofacteur dans la pathogenèse de certains cancers. Cependant, le BKv est pour l’instant classé comme « carcinogène possible pour l’homme » par l’agence internationale de recherche contre le cancer [45].
MATERIEL ET
METHODES
MATERIEL ET METHODES
Notre étude est descriptive, non interventionnelle et monocentrique, portant sur la population des transplantés rénaux. Les données ont été recueillies d’une façon rétrospective.
Population étudiée :
La population de l’étude est constituée de patients transplantés rénaux, suivis au CHU d’Ibn Sina de Rabat, ayant bénéficié de la recherche de BK virus dans les urines et/ou dans le sang. La date de début de l’étude correspond à la date à partir de laquelle le laboratoire central de virologie a commencé la réalisation de la recherche de BK virus, soit en 2013.
La recherche du BK virus dans les urines était réalisée de manière systématique à M1, M2, M3, puis tous les 3 mois pendant les 2 premières années post-transplantation, lors d'une altération inexpliquée de la fonction du greffon et après traitement d'un rejet aigu.
L’ensemble des prélèvements ont été analysé, au Laboratoire Central de Virologie, par biologie moléculaire (PCR quantitative en temps réel). La charge virale est exprimée en Log de copies /ml.
Les transplantés présentant une charge virale urinaire et/ou plasmatique positive significative ont bénéficié d’une étude plus approfondie des facteurs de risque de l’infection, des paramètres clinico-biologiques et histologiques au cours de l’infection à BKv, ainsi que la prise en charge thérapeutique et l’évolution à court et à long terme de ces patients.
La fin de l’étude est définie au septembre 2018, afin d’avoir un recul minimal d’une année pour tous les patients.
Les patients qui n’avaient pas un suivi régulier durant les premières années post transplantation ont été exclus de l’étude.
Variables considérées :
Toutes les données ont été recueillies rétrospectivement, à partir du dossier médical du patient.
Les données épidémiologiques comprenaient l’âge et le sexe du patient, la néphropathie initiale, le type de donneur (vivant/cadavérique) ainsi que la notion de mise en dialyse préalable à la greffe étaient relevés.
Sur le plan immunologique, les compatibilités et incompatibilités HLA étaient étudiées, ainsi que l’éventuelle présence d’anticorps anti-HLA ou la survenue de rejet.
Le déroulement de la transplantation et la notion de reprise retardée du greffon étaient précisées.
Le traitement immunosuppresseur d’induction et d’entretien était évalué en précisant les taux résiduels et/ou les doses moyennes.
Les données au moment du diagnostic (circonstances du diagnostic, fonction rénale et charge virale) étaient relevées, avec les évaluations anatomo-pathologiques de la biopsie du greffon. L’action thérapeutique justifiée par la mise en évidence d’une virémie BK virus positive était détaillée, ainsi que les nouvelles modifications thérapeutiques après disparition
Le suivi avec l’évolution étaient rapportés (Débit de filtration glomérulaire, charge virale et protéinurie à 1 mois, 3 mois, 6 mois, 1 an) et notamment l’éventuelle perte du greffon (mise en dialyse), l'apparition de DSA, ou la survenue d'un rejet de greffe.
Nous avons retenu les définitions suivantes : [62]
- Virurie significative : Réplication virale urinaire par PCR de l’ADN du BKv dans les urines supérieure à 7 Log.
- Virémie significative : Réplication virale plasmatique par PCR de l’ADN du BKv dans le plasma supérieure à 500–1000copies/mL ou 4 Log.
- Néphropathie à BK Virus présomptive : virémie significative à charge virale BK Virus > 10 000 copies/ml ou > 4 Log-copies/ml, persistante plus que 3 semaines.
I. Etude descriptive
Pendant la période d’étude étalée sur 5 ans, entre début Janvier 2013 et fin Octobre 2018, 74 patients étaient transplantés et suivis à l’hôpital universitaire Ibn Sina de Rabat. Parmi ces 74 transplantés, 17 patients (soit 23%) avaient une recherche de BK virus positive urinaire et plasmatique.
1. Caractéristiques initiales des patients
L’âge moyen au diagnostic de l’infection à BKv était de 46 ans ±13 ans. Les patients sont de sexe masculin dans 11 cas et de sexe féminin dans 6 cas, soit un sex ratio homme/femme à 1,84.
Trois patients sont diabétiques avant la transplantation rénale.
La néphropathie initiale était une néphropathie indéterminée, néphrangiosclérose, néphropathie diabétique, polykystose rénale, néphrite interstitielle chronique, néphropathie de reflux respectivement dans : 53%, 17%, 12%, 6%, 6% et 6% des patients. (Figure 2).
Il s’agit d’une greffe préemptive chez un patient, tandis que 16 patients sont dialysés avant la transplantation. Il s’agit de la première greffe chez tous les patients. Le donneur était vivant chez 15 patients (88,2%). Les donneurs étaient de sexe féminin dans 9 cas et de sexe masculin dans 8 cas. L’âge moyen du donneur était de 41 ±11 ans.
Sur le plan immunologique, 24% étaient identiques tandis que 76% étaient semi-identiques. Les anticorps anti-HLA sont présents de façon préalable à la transplantation chez 8 patients mais aucun anticorps n’est dirigé contre le donneur.
Concernant l’immunosuppression initiale, le traitement d’induction est à base de Basiliximab chez un patient (5,9%) à une dose standard de 40mg, et de sérum anti-lymphocytaire chez 16 patients (94,1%) à une dose totale moyenne de 4 ± 1.5 mg/kg, associés à un bolus de méthylprednisolone chez tous les patients.
Le relais du traitement immunosuppresseur est assuré par le tacrolimus chez 15 patients (88,2%), et par la Ciclosporine chez un seul patient (5,9%). Par ailleurs, le Mycophénolate Mofétil (MMF) est prescrit chez 16 patients, et l’Azathioprine chez un patient. Les corticoïdes sont prescrits chez tous les patients systématiquement.
Les suites de la transplantation étaient marquées par une reprise retardée de fonction du greffon chez 2 patients (11,8%), l’ischémie froide était en moyenne à 186 minutes avec une médiane de 69 minutes (56 – 85minutes).
Tableau I : Tableau récapitulatif des principales données concernant le receveur, le donneur et la greffe.
Nombre
Sexe Receveur Masculin Féminin 11 6Age moyen Receveur (années) 46±13
Antécédent de diabète 3 Sexe Donneur Masculin Féminin 8 9 Type donneur Vivant EME 15 2
Age moyen donneur (années) 41±11
Immunosuppression initiale Sérum anti-lymphocytaire Basiliximab
16 1
Ischémie froide médiane (minutes) 69 Reprise retardée de fonction du greffon 2
2. Diagnostic et délai de réplication virale BK La durée moyenne de suivi
diagnostic de BK virus était posé
les urines chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus réalisée dans le cadre d’une insuffisance rénale aigue
Le délai moyen du diagnostic une PCR positive
3).
Figure
2. Diagnostic et délai de réplication virale BK La durée moyenne de suivi
diagnostic de BK virus était posé
chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus réalisée dans le cadre d’une insuffisance rénale aigue
Le délai moyen du diagnostic une PCR positive de BKv
Figure 3 : Répartition des patients selon le délai de positivité de BKv après la 2. Diagnostic et délai de réplication virale BK
La durée moyenne de suivi des patients était diagnostic de BK virus était posé suite au dépistage
chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus réalisée dans le cadre d’une insuffisance rénale aigue
Le délai moyen du diagnostic était de 7,6 BKv pendant leur
épartition des patients selon le délai de positivité de BKv après la transplantation rénale
2. Diagnostic et délai de réplication virale BK des patients était de 57.6 mois
suite au dépistage
chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus réalisée dans le cadre d’une insuffisance rénale aigue
de 7,6 ± 5.7 mois eur première année
épartition des patients selon le délai de positivité de BKv après la transplantation rénale
2. Diagnostic et délai de réplication virale BK :
57.6 mois ± 13 mois suite au dépistage systématique
chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus réalisée dans le cadre d’une insuffisance rénale aigue.
7 mois. Treize patients parmi les 17 cas première année après la transplantation rénale.
épartition des patients selon le délai de positivité de BKv après la transplantation rénale
13 mois. Pendant cette période, l systématique de la PCR de BK virus chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus
patients parmi les 17 cas la transplantation rénale.
épartition des patients selon le délai de positivité de BKv après la Pendant cette période, l de la PCR de BK virus dans chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus
patients parmi les 17 cas avaient la transplantation rénale. (Figure
épartition des patients selon le délai de positivité de BKv après la Pendant cette période, le
dans chez 15 patients (88,2% de cas), alors que chez 2 patients la PCR de BK virus était
avaient (Figure
Avant le diagnostic, le taux de créatinine sanguine moyen était de 11.2 ± 3.2 mg/l avec un débit de filtration glomérulaire estimé selon la formule MDRD à 65ml/min/1.73m².
Au diagnostic, le taux de créatinine sanguine était en moyenne de 12.5± 3.6 mg/l avec un débit de filtration glomérulaire estimé selon la formule MDRD à 54 ml/min/1.73m².
Le taux de lymphocytes sanguins était de 890 ± 412 élé/mm³.
Le reste des caractéristiques biologiques avant et après le diagnostic de positivité de BK virus sont relevées au tableau II.
La recherche de BKv était réalisée initialement dans les urines puis complétée, en cas de sa positivité, par une PCR sanguine. Chez nos patients, ont été inclus des patients ayant aussi bien une recherche urinaire que sanguine positive à la fois.
La charge virale initiale sanguine de BK virus au diagnostic était à 3.5 log en moyenne. Cette charge virale avait atteint un pic de virémie au cours du suivi de 4.2 log en moyenne.
Tableau II : Caractéristiques biologiques avant et au diagnostic de l’infection à BKv
Avant le diagnostic
n (%) Au diagnostic n (%) Protéinurie positive
Hématurie microscopique positive Leucocyturie positive
Decoy cells positive PCR CMV positive DSA positive 1 (5.9%) 1(5.9%) 0 - 0 0 1 (5.9%) 3 (17.6%) 0 1 (5.9%) 3 (17.6%) 0
3. Immunosuppression initiale et au diagnostic de l’infection BKv
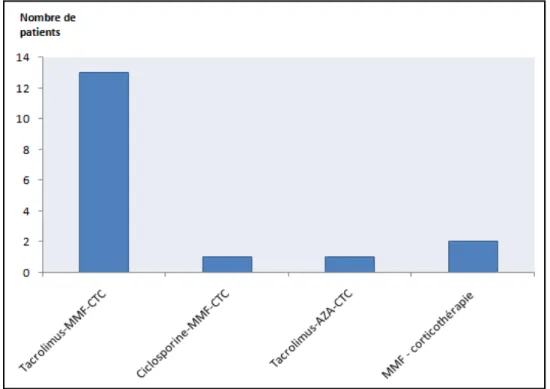
Au diagnostic, l’immunosuppression était basée sur plusieurs associations, notamment l’association Tacrolimus-MMF-corticothérapie chez 13 patients (76.5%), l’association Ciclosporine-MMF-corticothérapie était utilisée chez 1 patient, seulement 1 patient était sous Tacrolimus-Azathioprine-corticothérapie, l’association MMF – corticothérapie sans anticalcineurine était prescrite chez 2 patients. (Figure 4)
Le taux moyen résiduel de Tacrolimus au diagnostic de BK virus était de 7.4 ± 1.5 ng/ml. Un patient avait la Ciclosporine comme anticalcineurine avec un taux résiduel à 105 ng/ml. La dose moyenne du Mycophénolate Mofétil était de 1520 ±220 mg, l’aire sous la courbe n’était pas mesurée chez nos patients. La dose moyenne de corticothérapie est de 7 ±2 mg/j.
Figure 4 : Répartition des patients selon l’association des immunosuppresseurs avant l’infection BKv
(AZA= Azathioprine ; MMF= Mycophénolate Mofétil ; CTC= corticoïdes)
4. Description histologique :
Parmi les 17 patients ayant présenté une infection à BKv, seulement deux patients ont bénéficié d’une biopsie du greffon. L’indication était retenue devant la persistance de la virémie à BKv avec retentissement sur la fonction du greffon. Ces deux patients avaient une charge virale BK plasmatique persistante supérieure à 4 log/ml. La créatinine plasmatique moyenne lors de la biopsie était à 16 mg/l.
Chez le patient « X », le délai de réalisation de l’examen histologique est de 6 mois après la transplantation rénale, soit 30 jours après le diagnostic, tandis que la biopsie rénale est réalisée chez le patient « Y» 16 mois après la TR et 6 mois après le diagnostic de l’infection BKV.
Les biopsies mettent en évidence une néphropathie à BK virus définitive et contiennent un fragment médullaire. Des inclusions virales intra-nucléaires sont retrouvées sur les 2 biopsies, et la présence d’amas de « Decoy cell » dans la lumière tubulaire de la biopsie du patient « Y ». A noter, l’absence de signe de rejet aigu ou chronique sur ces biopsies.
5. Prise en charge initiale de l’infection à BKv :
Suite au diagnostic de la détection de la charge virale BK virus, le traitement immunosuppresseur est modifié chez 16 patients, soit 94% des cas. Le délai moyen de la première action thérapeutique après diagnostic positif est de 23 jours ± 12 jours. La modification de l’immunosuppression s’est basée sur la baisse de la dose des anticalcineurines, des anti-métabolites et/ou de la corticothérapie, le changement du Tacrolimus par la ciclosporine, et/ou arrêt du MMF. La baisse du MMF est de loin la première molécule modifiée, chez 12 patients (75% de cas).
Comme traitement adjuvant, les quinolones ont été prescrites chez un patient, cette thérapie est interrompue par la suite pour réaction allergique. Aucun patient n’a bénéficié de traitement par Cidofovir, Leflunomide ou de perfusion d’immunoglobulines intra-veineuses.
6. Négativité du BK virus :
Parmi les 17 patients, 16 patients ont obtenu une négativation de la charge virale BKv après un délai moyen de 121 jours avec une médiane de 70 jours [30– 180].
Avant d’obtenir cette négativation, la charge virale BK virus est restée positive dans le sang pour une durée supérieure à 3 semaines, soit la définition d’une néphropathie à BKv présomptive, chez 11 patients soit 65% des cas. Parmi ces 11 patients, seulement 2 patients avaient bénéficié de biopsie du greffon pour documenter la néphropathie à BKv.
Après l’obtention d’une charge virale négative, la créatininémie moyenne est de 12 ± 3.1 mg/l soit un débit de filtration glomérulaire moyen estimé, selon la formule MDRD, à 60 ml/min/1.73m².
L’immunosuppression ayant permis d’obtenir la négativité de la charge virale BKv chez les 16 patients est basée sur le Tacrolimus chez 8 patients (50% de cas) avec un taux résiduel à 7 ± 0.6 ng/ml, la Ciclosporine est prescrite chez 6 patients avec un taux résiduel à 100 ± 40ng/ml, soit 5 patients switché de Tacrolimus à la Ciclosporine, tandis que 2 patients ne recevaient pas d’anticalcineurine.
Le traitement par anti-métabolites est continué à base de Mycophénolate Mofétil chez 15 patients à une dose moyenne de 1204 mg/j (1000-1500 mg/j), l’Azathioprine est maintenue chez 1 patient à une dose de 150 mg/j. Le Mycophénolate Mofétil a été arrêté initialement chez 1 patient puis repris rapidement à dose faible devant le risque de rejet.
La corticothérapie est maintenue chez tous les patients à 5 mg/j.
Les données concernant l’immunosuppression initiale, au diagnostic de la BKv et après l’obtention d’une charge virale négative, sont représentées sur les figures 5 et 6.
Figure 5 : Modification de l’immunosuppression avant, au diagnostic et après négativation de BKv
(IS= immunosuppression ; MMF= Mycophénolate Mofétil)
Figure 6 : Modification de l’immunosuppression avant, au diagnostic et après négativation de BKv
7. Survie du greffon : Survenue d'une diminution de 30% du DFG estimé ou DFG<60ml/min/1.73m²
Une analyse du DFG est réalisée comparant le DFG avant l’infection BKv et après la négativation de la charge virale, avec comme critère de jugement la baisse de DFG à 30% de la valeur initiale.
Sur les 16 patients ayant négativé leur charge virale, 4 patients avait une perte de débit d’au moins 30% de leur DFG initial, dont 3 patients qui gardent un DFG entre 60 et 40 ml/min sans perte totale de la fonction du greffon et sans retour en dialyse. (Figure 7)
Figure 7 : Modification du DFG des patients avant l’infection et après la négativation du BK virus
II. Etude analytique
Analyse univariée
Les facteurs de risque présentant une association avec un p < 0,05 ont été considérés comme significatifs, afin de limiter les facteurs de confusion ou d'interaction.
L’analyse univariée avait intéressé les facteurs de risque de réplication du BKv chez les transplantés rénaux, tels que les facteurs préalables à la greffe, comme l'âge au moment de la greffe, l’antécédent de diabète, le sexe du receveur, le type de donneur ainsi que son âge et son sexe, le nombre de compatibilités HLA de groupe, une reprise retardée de fonction du greffon, et la durée d’ischémie froide. L’étude de ces facteurs n’a pas permis d’identifier un facteur de risque de réplication du BK virus statistiquement significatif.
De même, l’analyse des données liées à la greffe elle-même ou liées à la prise en charge ultérieure comme le traitement immunosuppresseur à l'induction ou d’entretien, ne semble pas distinguer un facteur de risque associé à la survenue d'une réplication virale à BKv. (Tableau III)
Tableau III : Facteurs associés à la réplication du BK virus en analyse univariée BK v + (n=17) BK v- (n= 57) p Sexe Receveur Féminin Masculin 6 11 21 36 0.9
Age receveur (an) 46±13 39±12 0.85
Diabète/receveur 2 2 0.32 Type donneur Vivant EME 15 2 48 9 0.68 Sexe donneur Féminin Receveur 9 8 32 25 0.816 Age donneur (moyenne d’années) 41±11 40±13 0.68 Compatibilité HLA (moyenne) 3.5 3.9 0.55
Durée ischémie froide (moyenne de minutes)
112±211 210±347 0.28
Reprise retardée de fonction de greffon 2 10 0.231 Induction ATG Simulect 15 2 46 8 0.59 Tacrolimus 15 47 0.66 Ciclosporine 1 5 0.69
Le développement de nouveaux agents immunosuppresseurs plus puissants a conduit à une réduction significative des taux de rejet aigu après transplantation rénale [46]. Les infections virales sont une complication bien connue de l'immunosuppression chronique notamment le BKV qui fait partie des infections opportunistes les plus courantes chez les transplantés rénaux [47,48].
I. Incidence et délai de survenue de la réplication BKv :
L’incidence de la réplication du BKv dans les greffes de rein varie entre 10.5 et 21% selon les études notamment la dernière cohorte de Schachtner ayant noté 12% de virémie BK parmi ses 862 transplantés rénaux [49,50,51,52]. Ainsi le diagnostic de réplication virale BK survient majoritairement dans la première année de la transplantation [53]. Par ailleurs dans notre série, 23% de nos patients avaient développés une virémie à BK, dont 76% ayant positivé au cours de leur première année de TR.
Le risque est l’évolution vers une néphropathie tubulo-interstitielle, dont l’incidence à 5 ans est de 6,6 % sur les données du registre américain [54].
II. Facteurs de risque de réplication de BK virus après la greffe rénale :
Les facteurs de risque d'infection par le BKV après transplantation rénale ont été largement étudiés mais les résultats restent incohérents. L'état net d'immunosuppression est actuellement considéré comme le déterminant le plus important de l'infection à BKV et de la néphropathie à BK virus [55]. Favi et al ont montré que l'origine ethnique afro-antillaise, l'inadéquation HLA donneur-receveur < 4 identités en commun, et le rejet aigu dans les trente jours suivant la transplantation sont des prédicteurs significatifs de l'infection à BKV [56].
Medeiros et al ont proposé l'absence de l'allèle HLA-C7, le donneur décédé, l'âge avancé et le sexe masculin du receveur, l'infection à CMV, le diabète sucré comme facteurs de risque de réplication de BK virus après la greffe rénale, ainsi que d’autre facteurs liés à la greffe comme le long temps d'ischémie froide et la reprise retardée de la fonction du greffon [57].
Huang et al ont démontré que l'incidence du BKv était plus faible chez les sujets qui ont reçu de la Ciclosporine en comparant au Tacrolimus [58]. Par conséquent, la charge totale des médicaments immunosuppresseurs peut être le facteur de risque le plus important [59].
Dans notre étude, on n’a pas conclu à une association significative entre la survenue de l’infection à BKv et les facteurs étudiés tels que l’âge, le sexe et l’antécédent du diabète du receveur, ainsi que le type, le sexe ou l’âge du donneur. Les paramètres liés à la greffe tel que la compatibilité HLA, la durée d’ischémie froide et la reprise retardée de fonction sont aussi étudiés, mais ne représentent pas des facteurs associés au risque de réplication de BKv. Ces résultats peuvent être expliqués par le faible échantillon dans notre étude rétrospective non randomisée.
II. Diagnostic de l’infection à BKv :
Aucun signe systémique d’une atteinte virale (fièvre, infection des voies aériennes supérieures etc.) n’est habituellement observé. Par ailleurs, plusieurs atteintes d’organes sont décrites dans la littérature exceptionnellement chez les patients en immunodépression sévère, à type de pneumonie sévère, de méningite ou encéphalite, de colite ou de vascularite [60].
1. Moyens diagnostiques : 1.1 Cytologie urinaire :
L’analyse cytologique sur urines fraîches peut mettre en évidence des decoy cells présentant de larges inclusions virales intra-nucléaires basophiles en verre dépoli. C’est une méthode sensible (100 %) et spécifique (71 %) avec une valeur prédictive négative pour la néphropathie à BKv de 100 % et la valeur prédictive positive est de 29 % mais reste encore bien moins sensible que les techniques de biologie moléculaire [61,62].
Nous n’avons effectué la recherche de Decoy cell que chez un patient, dont le résultat est positif.
1.2 Biologie moléculaire :
Le dépistage d’une réplication virale urinaire significative par PCR par quantification des copies d’ADN viral (significative au seuil de 107 copies/mL) est le témoin de l’intensité de l’infection, et la quantification de l’ARN messager de VP1 (significative à 6,5 x 105 copies/ng d’ARN total) est le meilleur reflet de la réplication virale active [62]. Dans la pratique courante, la PCR urinaire d’ADN viral est utilisée pour le dépistage de l’infection BKv due à ses avantages diagnostiques, en particulier une haute valeur prédictive négative (100%), une fenêtre de 6 à 12 semaines avant l’apparition d’une virémie puis néphropathie, un caractère non invasif et peu coûteux. Elle présente par ailleurs une clairance virale retardée par rapport à celle plasmatique, limitant son utilisation au dépistage sans intérêt au suivi de l’infection BKv.
![Figure 1 :Représentation schématique du génome du BK virus [8]](https://thumb-eu.123doks.com/thumbv2/123doknet/15058508.697958/23.810.131.685.652.984/figure-représentation-schématique-génome-bk-virus.webp)






![Tableau III : Stades histologiques de la néphropathie à BKv [63]](https://thumb-eu.123doks.com/thumbv2/123doknet/15058508.697958/50.810.77.767.168.424/tableau-iii-stades-histologiques-néphropathie-bkv.webp)
