Gefässchirurgie 2013 · 18:107–114 DOI 10.1007/s00772-013-1139-3 Online publiziert: 10. März 2013 © Springer-Verlag Berlin Heidelberg 2013 R.S. von Allmen · F. Dick Schweizer Herz- und Gefässzentrum, Klinik für Herz- und Gefässchirurgie, Universitätsspital Bern, Inselspital
Multimodale Therapie
radiogener Läsionen der
Becken-Bein-Gefäße
Ein systematischer Review
Die Strahlentherapie ist seit mehr als 100 Jahren bei vielen bösartigen und einigen gutartigen Krankheitsprozes-sen eine etablierte Behandlung, mit dem Ziel, Tumorerkrankung entwe-der vollständig zu heilen oentwe-der Symp-tome, die von der Tumorerkrankung ausgelöst werden, zu lindern oder zu vermeiden. Im Laufe der Erkran-kung ist bei vielen neu erkrankten Tumorpatienten eine Strahlenthera-pie Bestandteil der Behandlung, und bei der Hälfte aller dauerhaften Hei-lungserfolge ist diese Therapiemoda-lität integral mitbeteiligt. Neben all den erwünschten Wirkungen hat aber auch diese Therapie unerwünschte Nebenwirkungen, wie beispielsweise Strahlenschäden an Normalgewebe, unter anderem auch an großen Arte-rien.
Einleitung
Die periphere arterielle Verschlusskrank-heit (PAVK) steht üblicherweise praktisch synonym für Atherosklerose und ist als solche mit einem deutlich erhöhten kar-diovaskulären Risiko assoziiert [6]. Dane-ben existiert aber eine Reihe weiterer ok-kludierender Arteriopathien, die, weil viel seltener, in Vergessenheit zu geraten dro-hen. Dazu gehören z. B. die fibromusku-läre Dysplasie, die zystische Adventitia-Degeneration und die aktinische Gefäß-schädigung.
Radioaktive Strahlung existiert seit der Entstehung des Kosmos, aber erst die diag nostische und therapeutische Nut-zung ionisierender Strahlen hat zu einer relevanten Exposition des Menschen ge-führt [34]. Gerade in der Onkologie müs-sen so hohe Domüs-sen ionisierender Strah-lung verwendet werden, dass immer auch gesunde Gewebestrukturen exponiert werden. Dies führt unweigerlich zu ra-diogenen Schäden, die sich auch erst Jah-re nach der Behandlung manifestieJah-ren können. Man geht heute davon aus, dass bei jedem zweiten Tumorpatienten zu-mindest phasenweise eine Radiotherapie eingesetzt wird [7]. Da sich gleichzeitig die Überlebensraten der Tumorpatienten deutlich verbessert haben [3, 4, 27], wer-den die langfristigen Nebenwirkungen der Tumorbehandlung immer wichtiger.
Für den Gefäßmediziner bedeutet dies, dass er die Noxe ionisierende Strahlung und ihren Wirkmechanismus bis zur ra-diogenen Arteriopathie kennen und sich mit der optimalen Behandlung auseinan-derzusetzen muss. Ziel dieses Artikels ist es, einen groben Überblick über die all-gemeine Pathogenese und die verfügba-ren Therapieoptionen zu geben und sich danach anhand einer systematischen Li-teraturrecherche auf Schäden im Bereich der Becken-Bein-Gefäßachsen zu fokus-sieren.
Pathogenese aktinischer
Gefäßläsionen
Zur ionisierenden Strahlung zählen zwei Typen von Strahlung: die Partikelstrah-lung (α- [Helium-4-Atomkern] oder β-Strahlung [Elektronen/Positronen]) und die energiereichere Photonenstrahlung (γ-Strahlung, z. B. beim Röntgen). Die beiden Gruppen unterscheiden sich nicht nur im Strahlentyp, sondern auch in der Ionisationsdichte, die ihrerseits die Ein-dringtiefe und den biologischen Primär-schaden definiert. Während die Partikel-strahlung nur eine geringe Eindringtie-fe aufweist, hat die γ-Strahlung die Fä-higkeit, den gesamten Körper zu durch-dringen (wie z. B. beim Röntgen) [34]. In der perkutanen Radiotherapie wird heu-te v. a. ultraharheu-te Röntgenstrahlung (d. h. Photonen höherer Energie) oder Elektro-nenstrahlung verwendet. D Die biologische Wirkung wird nicht nur von der Art (und Dosis) der Strahlung beeinflusst, sondern auch von der Strahlenempfindlichkeit des Gewebes.
Diesem Faktor wird bei der Angabe der effektiven Strahlendosis Rechnung getra-gen. Während Gray (Gy, in Joule/Kilo-gramm) die absorbierte absolute Strah-lendosis misst, wird die biologisch effekti-ve Dosis (d. h. die absorbierte Dosis nach Korrektur hinsichtlich des Strahlungstyps
und der Strahlenempfindlichkeit der ein-zelnen Gewebe) in Sievert (Sv) angeben [37].
Zwei Arten von Strahlenfolgen wer-den unterschiewer-den: der deterministische Effekt und der stochastische Effekt. De-terministische Effekte treten erst ober-halb einer (individuellen) Schwellendosis auf und folgen dann einer direkten Do-sis-Wirkung-Beziehung [12]. Im Gegen-satz dazu hängen stochastische (Zell-kern-)Effekte mit strukturellen Verände-rungen der DNA und sekundären Repara-turmechanismen zusammen. Sie sind so-mit zufällig und die Schwere des Effekts dosisunabhängig [34]. Aktinische Gefäß-veränderungen werden mehrheitlich zu den deterministischen Strahlenschäden gezählt.
In Bezug auf die biologische Wirkung wird zusätzlich zwischen direkten und in-direkten Strahleneffekten unterschieden. Ein typischer direkter Strahleneffekt ent-steht, wenn ionisierende Strahlung (di-rekt) die DNA des Organismus verän-dert. Indirekte Effekte hingegen entste-hen, wenn unter der Strahlung Wasser-moleküle in Radikale zerfallen, die ihrer-seits (zufällige) Zellschäden verursachen. Solche Effekte sind viel häufiger und dar-um biologisch wichtiger.
Aktinische Gefäßschädigungen sind insbesondere für kleinere Gefäße bereits im 19. Jahrhundert entdeckt und beschrie-ben worden [13]. Bedingt durch die hohe Strahlenempfindlichkeit von Endothel-zellen weisen die kleinkalibrigsten Gefä-ße (Kapillaren) die geringste Strahlenre-sistenz auf. Bei Schäden an Arteriolen und Venolen dominieren, neben lipidhaltigen intimalen Makrophagen (Schaumzellen) und Intimafibrose, die subendotheliale und adventitielle Fibrose mit Media-Hya-linisierung sowie die inflammatorische Media- und Adventitia-Reaktion [9].
Umgekehrt gilt: je größer das Gefäß, desto geringer wird seine Strahlensensi-tivität. Venen weisen nach Bestrahlung grundsätzlich weniger strukturelle Schä-den auf als Arterien. Die großen Venen gelten sogar als sehr strahlenresistent [9]. Auf der arteriellen Seite hingegen erhöht die radiogene Makroangiopathie nach-weislich das kardio- und zerebrovasku-läre Risiko. So hatten sowohl Atombom-benüberlebende wie auch
Röntgenas-sistenten vor 1950 (also in einer Ära vor wirksamen Strahlenschutzbedingungen) ein deutlich erhöhtes Risiko für zerebro-vaskuläre Ereignisse, und zwar unabhän-gig von Strahlendosis und Expositions-dauer [19, 32]. Atombombenüberlebende waren nur einer einmaligen und hohen Strahlendosis ausgesetzt, während Rönt-genassistenten viel tiefere, dafür aber re-petitive Strahlendosen erlitten.
»
Je größer das Gefäß,
desto geringer ist seine
Strahlensensitivität
Allerdings ist der genaue Pathomecha-nismus der radiogenen Makroangiopa-thie weiterhin nicht vollständig geklärt. Es scheint, dass eine persistierende Ent-zündungsreaktion, die zur Entstehung atherosklerotischer Plaques führt, eine zentrale Rolle spielt [22]. Zudem entsteht neben der endothelialen Entzündungsre-aktion auch eine radiogene perivaskuläre Fibrose, die zu einer verminderten Gefäß-compliance führt [38]. Insgesamt nimmt man an, dass die radiogene Arteriopathie durch eine Aktivierung von atherosklero-tischen Prozessen ausgelöst wird.
Klinische (biologische) Folgen
der Gefäßbestrahlung
Der erste Fall einer aktinischen Makro-angiopathie wurde 1959 von Thomas u. Forbus bei einem Non-Hodgkin-Lym-phom-Patienten beschrieben, bei dem die Obduktion eine Nekrose der Aorten-wand erbrachte. Bei den großen Gefäßen führt die Strahlenreaktion meist zu einer Stenose oder zu einem Gefäßverschluss, aber auch Gefäßrupturen sind beschrie-ben worden [10]. In der Mikrozirkulation führen Strahlenschäden meist zu flächi-gen Gefäßverschlüssen [9].
Als Therapie haben ionisierende Strah-len auch in der kardiovaskulären Medizin einen möglichen Platz, und zwar als intra-vaskuläre Brachytherapie zur Prophylaxe von Rezidivstenosen peripherer oder ko-ronarer Gefäße. Dabei wird der Bestrah-lungskatheter in der dilatierten Stelle plat-ziert, und β- oder γ-Strahlen in einer Do-sis von 12–14 Gy appliziert, um
entzünd-lich-proliferative Restenosen zu verhin-dern [8]. Für Koronarien zeigte eine ran-domisierte Studie tatsächlich eine statis-tisch signifikante Verminderung der Re-stenoserate nach 5 Jahren [16]. Für die fe-moropopliteale Achse hingegen erbrachte die Brachytherapie in einer randomisier-ten Studie keine Verbesserung der Rezi-divstenoserate im mittelfristigen Verlauf [8].
Häufig betroffene Gefäßgebiete
Die aktinische Makroangiopathie tritt in den typischen Bestrahlungsfeldern auf, d. h. entlang der Halsgefäße, der A. sub-clavia/axillaris sowie im Bereich des Her-zens. Seltener ist die Becken-Bein-Achse betroffen. Dieses Gefäßgebiet wird später anhand einer systematischen Literaturre-cherche näher beleuchtet.A. carotis
Die Radiotherapie führt an den Halsge-fäßen nicht nur zu einer dosisabhängi-gen Verdickung der Intima-Media [15], sondern auch zu einer relevanten Steige-rung des Risikos für zerebrovaskuläre Er-eignisse [2, 36]. Die Behandlung radioge-ner Karotisstenosen folgt grundsätzlich den Richtlinien zur Behandlung athero-sklerotischer Karotiserkrankungen und wird in einem eigenen Leitthemenbeitrag gesondert beschrieben.
A. subclavia und A. axillaris
Diese Gefäße haben mit 44 Gy (median) wahrscheinlich eine höhere Strahlento-leranz als die A. carotis (median 38 Gy) [20] und sind typischerweise bei der Be-strahlung von Mammakarzinomen oder Hodgkin-Lymphomen betroffen. Ein ra-diogener Verschluss der A. subclavia wird häufig erst nach 10 bis 20 Jahren sympto-matisch. Im Gegensatz zu atherosklero-tischen Läsionen sind solche Verschlüs-se meist langstreckig und relativ schlecht kollateralisiert. Dies erklärt sich am ehes-ten dadurch, dass viele poehes-tenzielle Kolla-teralen auch ionisierender Strahlung aus-gesetzt waren [18].
Herz
Das Herz galt lange als strahlenresistent, ist aber mittlerweile als strahlensensitives Organ erkannt. Das ist insofern eine wich-tige Erkenntnis, als das Herz bei der Be-strahlung eines Hodgkin-Lymphoms oder eines Mammakarzinoms nicht selten im Strahlenfeld liegt. Faktoren, die das Risi-ko erhöhen, an einem kardiovaskulären Ereignis zu versterben, sind neben der applizierten Gesamtdosis (die Toleranz-dosis wird bei einer Fraktionierung von 2 auf ca. 40 Gy geschätzt) das bestrahlte Herzvolumen [11] und die Prognose hin-sichtlich des onkologischen Überlebens [35]. Bei jüngeren Patienten ist das Risiko eines letalen kardiovaskulären Ereignisses nach mediastinaler Strahlentherapie um das 1,5- bis 3-Fache erhöht [17]. Die The-rapie der radiogenen Herzkrankheit folgt den üblichen Richtlinien der (atheroskle-rotischen) koronaren Herzkrankheit [35] solange sie nicht auf eine konstriktive Pe-rikarditis, Myokardfibrose oder Klappen-fibrose zurückzuführen ist [27]. Des Wei-teren spielt die kardiovaskuläre Toxizität einer zusätzlichen medikamentösen The-rapie mit Chemotherapeutika eine wich-tige Rolle als nicht onkologische Todes-ursache.
Strahlenschäden der
Becken-Bein-Gefäße
Radiogene Läsionen der Gefäße im Be-cken- und Beinbereich treten typischer-weise nach Bestrahlung von Uterus-, Rektum-, Blasen-, Ovarial-, Vulva-, Zer-vix- oder Hodenkarzinomen auf. Morbus Hodgkin, Weichteilsarkome und andere infiltrierend wachsende Tumore sind wei-tere Malignome, die im Becken oder im Bereich der Beine lokal bestrahlt werden.
Methodik der systematischen
Literaturrecherche
Radiogene Läsionen der Becken-Bein-Gefäße sind das Hauptthema dieses Ar-tikels und sollen anhand einer systemati-schen Literaturrecherche erörtert werden. Die Recherche wurde im Dezember 2012 in zwei medizinischen elektronischen Datenbanken (MEDLINE und SCOPUS) durchgeführt und war auf die Sprachen
Gefässchirurgie 2013 · 18:107–114 DOI 10.1007/s00772-013-1139-3 © Springer-Verlag Berlin Heidelberg 2013
R.S. von Allmen · F. Dick
Multimodale Therapie radiogener Läsionen der
Becken-Bein-Gefäße. Ein systematischer Review
Zusammenfassung Hintergrund. Die Prognose von Karzinom-patienten hat sich nicht zuletzt durch den Einsatz der Radiotherapie deutlich verbes- sert. Entsprechend überleben Patienten ver- mehrt auch langfristig, weshalb unerwünsch-te Nebenwirkungen der Tumorbehandlung wie vaskuläre Strahlenschäden klinisch im-mer relevanter werden. Dieser systematische Review möchte einen Überblick über die Pa- thogenese und die verfügbaren Therapieop- tionen von radiogenen Läsionen der Becken-Bein-Gefäßachsen geben. Methode. Zwei elektronische Datenbanken (Medline, Scopus) wurden systematisch durchsucht. Im Zentrum der Recherche stand die optimale Therapie von radiogenen Gefäß-läsionen der Becken-Bein-Achse. Die Suche war dabei auf deutsche und englische Arti-kel beschränkt. Ergebnisse. 1573 identifizierte Abstracts wurden gescreent und 33 potenziell rele-vante ausgewählt. Von diesen wurden nach einer Volltextanalyse 16 in die Analyse einge-schlossen. Alle Studien bis auf eine wurden vor 2006 publiziert. Das Intervall zwischen der Bestrahlung und den ersten Symptomen der Durchblutungsstörung ist sehr variabel und liegt zwischen Monaten und Jahrzehn-ten. Leitsymptom ist in den meisten Fällen eine Claudicatio oder eine Beinischämie vom Acute-on-chronic-Typ. Das therapeutische Management war sehr heterogen. Die ortho-tope Revaskularisation war in 71% der Fälle die bevorzugte Wahl, sofern ein offenes chir-urgisches Verfahren gewählt worden ist. Schlussfolgerungen. Die Evidenzbasis für die Steuerung der Therapie radiogener Ge- fäßläsionen ist schwach. Das klinische Ma-nagement richtet sich darum deduktiv nach den Behandlungsrichtlinien atheroskleroti- scher Gefäßläsionen und muss auch die me- dikamentöse Sekundärprophylaxe miteinbe-ziehen. Heutzutage sollten endovaskulären Verfahren bevorzugt werden. Schlüsselwörter Radiotherapie · Aktinische Gefäßschädigung · Periphere arterielle Verschlusskrankheit · Strahlentherapie · SpätkomplikationenMultimodal therapy of radiogenic lesions of the
iliacofemoral blood vessels. A systematic review
Abstract Objective. Improvements in cancer ther- apies have increased survival following di-agnosis of a malignancy. Thus long-term side effects of treatment, such as radiogen- ic macroangiopathy have become increas- ingly more relevant to vascular surgery prac-tice. The aim of this systematic review was to give an overview of the pathogenesis and evidence-based therapeutic options for ra-diation-induced lesions of the iliacofemoral blood vessels. Methods. In this study two computer-based medical literature databases (Medline and Scopus) were searched systematically. The search was limited to German and English re- ports of clinical management of radiation-in-duced peripheral vessel lesions. Results. A total of 1,573 identified cita-tions and abstracts were screened and 33 were considered to be potentially relevant and were further scrutinized. Of these, 16 re- ports met the study criteria and were includ-ed in the analysis. All but one of the studies were published before 2006. The duration be-tween radiation and first manifestations of leg ischemia was variable and symptoms, in particular claudication or acute-on-chronic leg ischemia, can surface several months af- ter radiation up to decades later. The subse- quent therapeutic management is very het- erogeneous; however, orthotropic revascular-ization was preferred in 71% of the cases if an open surgical approach was chosen. Conclusions. Currently, there is a lack of con- vincing evidence to guide clinical decision-making; therefore physicians are advised to follow the standard treatment guidelines for atherosclerotic vascular lesions includ- ing best medical therapy. Endovascular pro- cedures should probably be preferred when-ever possible. Keywords Radiotherapy · Radiation · Actinic vessel damage · Peripheral arterial obstructive disease · Late complicationsTa b. 1 Zu sa m m en st el lu ng d er p ub liz ie rt en F äl le m it ra di og en in du zi er te n Lä si on en d er B ec ke n- u nd B ei ng ef äß e A ut or , Journal , Jahr Pa t. (n) M alignom Str ahlendo -sis (G y) A rt der G efäßläsion Sympt om -beginn (Jahr e nach B estr ah -lung) Klinisches Bild Ther apiemodalitä t Klinisches F ollo w -up N yl an de r e t a l., Ca nc er , 1 97 8 5 Ze rv ix ka rz in om (n = 3) , O va ria lk ar zi no m (n = 1) Ex te rn e un d in tr ak av itä re RT , k ei ne D os is an ga be Ke in e ge na ue n An ga be n 2– 6 (M ed ia n 6) 3 m it Cl au di ca tio , 1 m it Ru he sc hm er ze n 4-m al o rt ho to pe R ev as ku la ris a-tio n, 1 -m al e xt ra an at om isc he Re va sk ul ar isa tio n Fo llo w -u p 6 M on at e bi s 2 Ja hr e, a lle B yp äs se o ffe n H ar nb la se nk ar zi no m (n = 1) 1 m it ch ro ni sc h kr iti -sc he r I sc hä m ie Bu tle r e t a l., Br J Su rg , 1 98 0 1 Te ra to m u nd Se m in om Ke in e An ga be n Ve rs ch lu ss A . I lia ca c om m u-ni s r ec ht s 14 Sc hw er e Cl au di ca tio O ffe n-ch iru rg isc he R ek on st ru k-tio n, o rt ho to p Ke in e An ga be n La w so n et a l., J C ar di ov as c S ur g, 19 85 10 Ze rv ix ka rz in om (n = 4) En do m et riu m ka rz i-no m (n = 2) 40 –6 5 (M ed ia n 53 ) Ke in e ge na ue n An ga be n 2– 37 (M ed ia n 9) 7 m it Ru he sc hm er ze n 2 m it Cl au di ca tio 6-m al e xt ra an at om isc he R ev as -ku la ris tio n, 4 -m al o rt ho to pe Re va sk ul ar isa tio n Bl as en ka rz in om (n = 2) 1 ak ut er V er sc hl us s Fi br os ar ko m (n = 1) O st eo ge ne s F ib ro m (n = 1) Am em iy a et a l., Th e Ja pa ne se J Su rg , 1 98 7 1 N ie re nz el lk ar zi no m (T ib ia m et as ta se ) 65 Ve rs ch lu ss A . p op lit ea u nd Tr ifu rk at io n (d ie „a th er os kl e-ro tis ch “ v er än de rt en G ef äß -ab sc hn itt e w ar en a uf d as Be st ra hl un gs fe ld b es ch rä nk t) 4 In iti al C la ud ic at io , d an n Ac ut e-on -c hr on ic -Is ch äm ie Ke in e ch iru rg isc he In te rv en tio n au fg ru nd d es fo rt ge sc hr itt en en Tu m or le id en s Ke in e An ga be n Pe tt er ss on e t a l., Ac ta C hi r S ca nd , 19 90 15 Ze rv ix ka rz in om (n = 10 ) O va ria lk ar zi -no m (n = 3) E nd om et -riu m ka rz in om (n = 2) M ed ia n 36 ,3 Ve rs ch lu ss Il ia ka lg ef äß e 1– 15 (M ed ia n 6) 12 m it Cl au di ca tio , 3 m it Ru he sc hm er ze n 12 -m al o rt ho to pe R ev as ku la ri-sa tio n, 3 -m al k on se rv at iv Ke in e An ga be n Le ve nb ac k et a l., Gy ne co l O nc ol , 19 96 3 Re tr op er ito ne al es Fi br os ar ko m (n = 1) 70 Ve rs ch lu ss A . i lia ca , e in se iti g 21 Kr iti sc he Is ch äm ie (m it N ek ro se n) M aj or am pu ta tio n Fr üh p os to pe ra tiv v er -st or be n Ze rv ix ka rz in om (n = 1) 40 Ve rs ch lu ss , A . i lia ca , e in se iti g 16 Kr iti sc he Is ch äm ie (m it N ek ro se n) M aj or am pu ta tio n Ve rs to rb en n ac h 1 M on at Ze rv ix ka rz in om (n = 1) 40 M ul tip le il ia ko fe m or al e St en os en 20 Kr iti sc he Is ch äm ie (m it N ek ro se n) M aj or am pu ta tio n Pa tie nt in e nt la ss en , an so ns t k ei ne A ng ab en Sa lio u et a l., An n Va sc S ur g, 19 97 1 O st eo sa rk om 48 La ng st re ck ig e St en os e de r A. fe m or al is su pe rf ic ia lis , ei ns ei tig 13 Cl au di ca tio Pe rk ut an e An gi op la st ie , n ac h 4 M on at en fe m or op op lit ea le r (o rt ho to pe r) By pa ss b ei sy m p-to m at isc he r R es te no se U na uf fä lli ge r V er la uf b is 8 M on at e na ch B yp as s
Leitthema
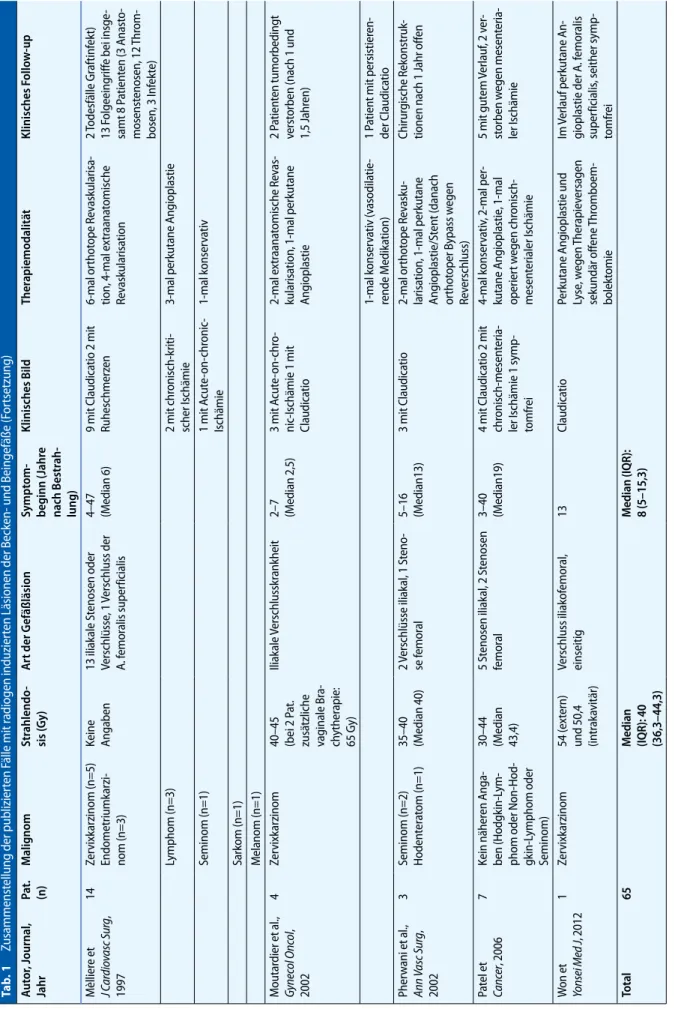
Ta b. 1 Zu sa m m en st el lu ng d er p ub liz ie rt en F äl le m it ra di og en in du zi er te n Lä si on en d er B ec ke n- u nd B ei ng ef äß e (F or ts et zu ng ) A ut or , Journal , Jahr Pa t. (n) M alignom Str ahlendo -sis (G y) A rt der G efäßläsion Sympt om -beginn (Jahr e nach B estr ah -lung) Klinisches Bild Ther apiemodalitä t Klinisches F ollo w -up M èl lie re e t J C ar di ov as c S ur g, 19 97 14 Ze rv ix ka rz in om (n = 5) En do m et riu m ka rz i-no m (n = 3) Ke in e An ga be n 13 il ia ka le S te no se n od er Ve rs ch lü ss e, 1 V er sc hl us s d er A. fe m or al is su pe rf ic ia lis 4– 47 (M ed ia n 6) 9 m it Cl au di ca tio 2 m it Ru he sc hm er ze n 6-m al o rt ho to pe R ev as ku la ris a-tio n, 4 -m al e xt ra an at om isc he Re va sk ul ar isa tio n 2 To de sf äl le G ra ft in fe kt 13 F ol ge ei ng rif fe b ei in sa m t 8 P at ie nt en (3 A na m os en st en os en , 1 2 Th bo se n, 3 In fe kt e) Ly m ph om (n = 3) 2 m it ch ro ni sc h-kr iti -sc he r I sc hä m ie 3-m al p er ku ta ne A ng io pl as tie Se m in om (n = 1) 1 m it Ac ut e-on -c hr on ic -Is ch äm ie 1-m al k on se rv at iv Sa rk om (n = 1) M el an om (n = 1) M ou ta rd ie r e t a l., Gy ne co l O nc ol , 20 02 4 Ze rv ix ka rz in om 40 –4 5 (b ei 2 P at . zu sä tz lic he va gi na le B ra -ch yt he ra pi e: 65 G y) Ili ak al e Ve rs ch lu ss kr an kh ei t 2– 7 (M ed ia n 2, 5) 3 m it Ac ut e-on -c hr o-ni c-Is ch äm ie 1 m it Cl au di ca tio 2-m al e xt ra an at om isc he R ev as -ku la ris at io n, 1 -m al p er ku ta ne An gi op la st ie 2 Pa tie nt en tu m or be di ve rs to rb en (n ac h 1 un 1, 5 Ja hr en ) 1-m al k on se rv at iv (v as od ila tie -re nd e M ed ik at io n) 1 Pa tie nt m it pe rs ist ie re de r C la ud ic at io Ph er w an i e t a l., An n Va sc S ur g, 20 02 3 Se m in om (n = 2) H od en te ra to m (n = 1) 35 –4 0 (M ed ia n 40 ) 2 Ve rs ch lü ss e ili ak al , 1 S te no -se fe m or al 5– 16 (M ed ia n1 3) 3 m it Cl au di ca tio 2-m al o rt ho to pe R ev as ku -la ris at io n, 1 -m al p er ku ta ne An gi op la st ie /S te nt (d an ac h or th ot op er B yp as s w eg en Re ve rs ch lu ss ) Ch iru rg isc he R ek on st ru tio ne n na ch 1 Ja hr o ffe Pa te l e t Ca nc er , 2 00 6 7 Ke in n äh er en A ng a-be n (H od gk in -L ym -ph om o de r N on -H od -gk in -L ym ph om o de r Se m in om ) 30 –4 4 (M ed ia n 43 ,4 ) 5 St en os en il ia ka l, 2 St en os en fe m or al 3– 40 (M ed ia n1 9) 4 m it Cl au di ca tio 2 m it ch ro ni sc h-m es en te ria -le r I sc hä m ie 1 sy m p-to m fre i 4-m al k on se rv at iv , 2 -m al p er -ku ta ne A ng io pl as tie , 1 -m al op er ie rt w eg en c hr on isc h- m es en te ria le r I sc hä m ie 5 m it gu te m V er la uf , 2 st or be n w eg en m es en le r I sc hä m ie W on e t Yo ns ei M ed J, 2 01 2 1 Ze rv ix ka rz in om 54 (e xt er n) un d 50 ,4 (in tr ak av itä r) Ve rs ch lu ss il ia ko fe m or al , ei ns ei tig 13 Cl au di ca tio Pe rk ut an e An gi op la st ie u nd Ly se , w eg en T he ra pi ev er sa ge n se ku nd är o ffe ne T hr om bo em -bo le kt om ie Im V er la uf p er ku ta ne A gi op la st ie d er A . f em or su pe rf ic ia lis , s ei th er sy to m fre i To ta l 65 M ed ia n (IQ R) : 4 0 (3 6, 3– 44 ,3 ) M ed ia n (IQ R) : 8 (5 –1 5, 3)
Deutsch und Englisch beschränkt, nicht aber auf das Erscheinungsdatum. Die fol-genden Suchbegriffe wurden in verschie-denen Kombinationen sinngemäß kom-biniert: „radiation“, „radiation-induced“, „radiotherapy“, „radiosensitivity“ und „cancer survivor“ mit „vasculopathy“, „vessel lesion“, „large vessels“, „peripheral arterial disease“, „arterial/venous occlusi-ve disease“. Dabei standen Effekte einer Radiotherapie auf die Becken- und Bein-gefäße sowie deren optimale Therapie im Zentrum. Studien wurden demnach nur eingeschlossen, wenn mindestens 2 der folgenden 4 Parameter beschrieben wur-den: applizierte Strahlendosis,
bestrahl-tes (Gefäß-)Gebiet, klinisch-chirurgi-sches Management und/oder das Behand-lungsergebnis. Gesucht wurden demzu-folge nach aktuellem Stand des Wissens valide Erkenntnisse über Symptome, kli-nische Entscheidungen, Behandlung und patientenrelevante Outcomes.
Resultate
Die initiale Literaturrecherche ergab 1573 Publikationen, wovon anhand des Abstracts aber nur 33 als potenziell the-menrelevant eingestuft wurden. Von diesen waren nach einer Volltextanaly-se noch 16 für die Fragestellung relevant und wurden in die Analyse eingeschlos-sen (. Abb. 1).
Interessanterweise gibt es bisher keine metaanalytische Zusammenfassung der bekannten Evidenz. Alle erfassten Pub-likationen beschreiben unkontrollier-te Fallserien, sodass die Evidenz zur handlung radiogener Läsionen der Be-cken-Bein-Gefäße den niedrigsten Evi-denzgrad aufweist.
»
Alle Publikationen basieren
auf Fallserien und weisen den
niedrigsten Evidenzgrad auf
Insgesamt wurden zwischen 1979 und 2012 65 Fälle von radiogenen iliakofemo-ralen Gefäßläsionen beschrieben, wobei bis auf einen alle Fallberichte vor 2006pub liziert worden waren [1, 5, 23-26, 28- 31, 33, 39].
Praktisch alle Berichte beziehen sich auf arterielle Läsionen, da die großen Ve-nen, wie bereits erwähnt, als strahlenre-sistent gelten. Arterielle Strahlenschäden manifestieren sich auch in der Becken-Bein-Achse meist als PAVK. Berichte von radiogenen Aneurysmen und Gefäßrup-turen sind eine Rarität.
Alle erfassten Fälle sind in . Tab. 1 zusammengefasst. Durchschnittlich er-hielt diese Patientenkohorte eine media-ne Strahlendosis von 40 Gy (Interquartil-sabstand (IQR) 36,3–44,3 Gy). Das me-diane Intervall zwischen Bestrahlung und erstem Auftreten von Symptomen lag bei 8 Jahren (IQR 5–15,3 Jahre).
In den meisten Fällen war das Leit-symptom entweder eine Claudicatio oder eine Beinischämie vom Acute-on-chro-nic-Typ. Eine chirurgische Revaskularisa-tion wurde in 42 der beschriebenen Fäl-le (65%) durchgeführt. In 6 FälFäl-len erfolg-te eine endovaskuläre Therapie. In wei-teren 3 Fällen wurde initial ein endovas-kulärer Therapieversuch unternommen, aber sekundär zu einem offen-chirur-gischen Verfahren wegen Reverschluss oder Komplikationen konvertiert. Weite-re 3 Patienten wurden primär amputiert. Bei den restlichen 11 Patienten (17%) wur-de eine konservative Therapie eingeleitet. Bei der chirurgisch revaskularisierten Patientengruppe (n=45) wurde nur in 13 Fällen (29%) eine extraanatomische Ge-fäßführung gewählt. Die übrigen Gefäß-rekonstruktionen wurden orthotop an-gelegt. Die Beschreibung der Nachsorge war derart unterschiedlich und mangel-haft, dass hinsichtlich der Reoperations-rate und des Beinerhalts keine Aussage gemacht werden kann. Insgesamt ist die existierende Evidenz bezüglich Behand-lung radiogener Becken-/Beinarterienlä-sionen also sehr armselig.
Diskussion
Radiogene Läsionen der Becken-Bein-Gefäße wurden bisher sehr selten be-schrieben und scheinen hauptsächlich die Arterien zu betreffen. Entsprechend schwach ist demnach die wissenschaftli-che Abstützung von Managementempfeh-lungen, die allesamt auf unkontrollierten Datenbank-Recherche
(Suche in Medline und Scopus) Letzte Suche am 29. Dezember 2012
Primär identifizierte Studien n=1573
Gescreent nach Titel und Abstract
Selektionierte Studien n=33 Volltextscreening
Eingeschlossene Studien N=16
Ausgeschlossen (Volltext nicht relevant)
n=17
Ausgeschlossen (Titel und/oder Abstract nicht relevant)
n=1540 Abb. 1 8 Flow-Chart der Studienauswahl Abb. 2 8 Angiographiebild einer 62-jährigen Patientin mit symptomatischen Beckengefäß-verschlüssen 5 Jahre nach adjuvanter Radio- und Chemotherapie wegen Endometriumkar-zinom
Leitthema
weise auf die bestrahlten Gefäßabschnit-te beschränkt und ähneln häufig einer vorzeitigen Atherosklerose (. Abb. 2). Eine Strahlengesamtdosis von über 40 Gy scheint zu einem Anstieg der Spätkompli-kationsrate zu führen, wobei das Intervall zwischen der Bestrahlung und dem Auf-treten der ersten Symptome sehr varia-bel ist und mehrere Monate bis viele Jahre betragen kann. Faktoren, die dieses Inter-vall verkürzen, sind insbesondere die Ge-samtdosis, dichte Bestrahlungsintervalle, eine ungenügende Fraktionierung sowie Zweitbestrahlungen. Außerdem treten vaskuläre Strahlenkomplikationen v. a. bei Patienten mit zusätzlichen kardiovaskulä-ren Risikofaktokardiovaskulä-ren auf [21].
Bei Patienten mit radiogener Gefäß-schädigung spielt nicht nur das Ausmaß der Ischämie eine Rolle, sondern auch dasjenige weiterer Strahlungsschäden wie z. B. eine Fibrose der umgebenden Weich-teile. Solche Zusatzschäden vermindern die Compliance der verbleibenden Ge-fäße und verhindern die Ausbildung ad-äquater Kollateralen.
Die Bestrahlung interagiert offenbar mit den üblichen sonstigen atherogenen Faktoren. Deshalb scheint es ratsam, sol-che Interaktionen bereits bei der Bestrah-lungsplanung zu antizipieren. Bisher wird bei geplanter Radiotherapie hinsichtlich des Gefäßstatus weder eine systematische Vorabklärung noch eine konsequente Verlaufsbeobachtung empfohlen und wä-re auch nicht evidenzbasiert. Es scheint je-doch auf jeden Fall empfehlenswert, Pa-tienten bereits bei geringen Anzeichen einer eingeschränkten Ruhedurchblutung eingehend abzuklären und einer medika-mentösen Sekundärprophylaxe zuzufüh-ren. Statine sollten aufgrund ihrer addi-tiven antiinflammatorischen und anti-thrombotischen Effekte im Zentrum einer solchen Behandlung stehen [14].
Wenn eine invasive Revaskularisierung notwendig wird, muss bei der Therapie-planung nicht nur die lokale Gefäßsitua-tion in Betracht gezogen werden, sondern auch weitere Faktoren wie die umgeben-den Weichteilverhältnisse und der Allge-meinzustand des Patienten. Obwohl in den verfügbaren Fallberichten bevorzugt offen-chirurgische
Behandlungsmetho-ten heute primär endovaskuläre Metho-den in Betracht gezogen werMetho-den [21]. Die endovaskulären Möglichkeiten haben in den letzten Jahren deutliche Fortschritte erzielt, sodass die erfassten Publikationen hier wohl etwas überholt sind. Wenn aller-dings ein chirurgisches Verfahren gewählt wird, ist nicht nur die Rekonstruktionsart, sondern auch das gewählte Graftmaterial von entscheidender Bedeutung. Das Risi-ko einer Graftinfektion ist in bestrahltem Gewebe auch Jahre nach Revaskularisa-tion noch deutlich erhöht, weshalb bio-logisches Material (wenn möglich auto-loge Vene) unbedingt bevorzugt verwen-det werden sollte [21]. Letztlich scheinen die Resultate einer orthotopen Graftfüh-rung zufriedenstellend. Darum sollte ein extraanatomisches Verfahren nur bei kri-tischen Weichteilverhältnissen in Betracht gezogen werden.
Fazit für die Praxis
F Die radiogene iliakofemorale Gefäß- krankheit ähnelt einer beschleunig-ten Atherosklerose und tritt vor allem nach Strahlengesamtdosen von mehr als 40 Gy auf. F Das Intervall zwischen Bestrahlung und ersten Symptomen ist sehr varia-bel und liegt zwischen Monaten und Jahrzehnten. Darum sollten Bestrah- lungspatienten auch noch nach Jah-ren bei den geringsten Anzeichen einer Minderperfusion spezialärzt-lich untersucht und mit aggressiver Sekundärprophylaxe, inklusive Stati-nen, behandelt werden. F Wenn schließlich doch eine Interven-tion an den Gefäßen notwendig wird, so sollte heute primär an eine endo-vaskuläre Therapiemodalität gedacht werden, da Weichteilschäden im ehe-maligen Bestrahlungsfeld eine offene Operation komplizieren können. F Prinzipiell gelten für radiogene Läsio- nen der Becken-Bein-Gefäße die glei-chen Behandlungsrichtlinien wie für die atherosklerotische Verschluss-krankheit. PD Dr.F. Dick Schweizer Herz- und Gefässzentrum, Klinik für Herz- und Gefässchirurgie, Universitätsspital Bern, Inselspital Freiburgstrasse, 3010 Bern Schweiz florian.dick@insel.ch
Compliance
with Ethics Guidelines
Conflict of Interest. R.S von Allmen and F. Dick decla-re that they have no conflict of interest. This article does not contain any studies with human or animal subjects.
Literatur
1. Amemiya A, Yamaguchi A, Sakurai K (1987) Radia-tion-induced occlusion of the artery in the distal lower extremity – a case report. Jpn J Surg 17:178– 181 2. Bowers DC, McNeil DE, Liu Y et al (2005) Stroke as a late treatment effect of Hodgkin’s disease: a report from the Childhood Cancer Survivor Study. J Clin Oncol 23:6508–6515 3. Brenner H (2002) Long-term survival rates of can- cer patients achieved by the end of the 20th cen-tury: a period analysis. Lancet 360:1131–1135 4. Brenner H, Hakulinen T (2006) Up-to-date estima-tes of cancer patient survival even with common latency in cancer registration. Cancer Epidemiol Biomarkers Prev 15:1727–1732 5. Butler MJ, Lane RH, Webster JH (1980) Irradiation injury to large arteries. Br J Surg 67:341–343 6. Caprie Steering Committee (1996) A randomised, blinded, trial of clopidogrel versus aspirin in pati-ents at risk of ischaemic events (CAPRIE). Lancet 348:1329–1339 7. Delaney G, Jacob S, Featherstone C, Barton M (2005) The role of radiotherapy in cancer treat- ment: estimating optimal utilization from a re-view of evidence-based clinical guidelines. Cancer 104:1129–1137 8. Diehm N, Silvestro A, Do DD et al (2005) Endova- scular brachytherapy after femoropopliteal bal- loon angioplasty fails to show robust clinical bene-fit over time. J Endovasc Ther 12:723–730 9. Fajardo LF (2005) The pathology of ionizing radia- tion as defined by morphologic patterns. Acta On-col 44:13–22 10. Fajardo LF, Lee A (1975) Rupture of major vessels after radiation. Cancer 36:904–913 11. Filopei J, Frishman W (2012) Radiation-induced he-art disease. Cardiol Rev 20:184–188 12. Fry RJ (2001) Deterministic effects. Health Phys 80:338–343 13. Gassmann A (1899) Zur Histologie des Roentge-nulcer. Fortschr Geb Roentgenstr 2:199–211Herzkranke Diabetespatienten:
Längere Überlebenszeit durch
Bypass
Laut einer neuen internationalen Studie überleben Diabetespatienten mit mehr-fach verengten Herzkranzgefäßen nach einer Bypass-OP länger als solche mit einer Gefäßstütze. Für die Studie wurden insgesamt 1900 Patienten mit einem Durchschnittsalter von 63 Jahren nach dem Zufallsprinzip in zwei Behandlungsgruppen eingeteilt. Einer Gruppe legten Chirurgen Bypässe, die zweite Gruppe unterzog sich einer perkutanen Koronarintervention mit Medikamenten freisetzenden Stents. Nach einer Bypass-Operation traten inner-halb von fünf Jahren sowohl Todesfälle als auch Herzinfarkte deutlich seltener auf. Während innerhalb von fünf Jahren 10,9% der Patienten mit Bypass verstarben, waren es in der Stent-Gruppe 16,3%. Einen Herz-infarkt erlitten 6% der Bypass-Patienten, dagegen waren es bei den Stent-Patienten 13,9%. Lediglich Schlaganfälle traten in der Bypass-Gruppe häufiger auf: Nur 2,4% der Patienten mit Stent erlitten einen Schlag-anfall, bei den Bypass-Patienten waren es 5,2%. Bei einer koronaren Katheterunter- suchung folgt auf die Diagnostik der Herz-kranzgefäße häufig sofort der Einsatz von Stents, da beides in einer Sitzung erfolgen kann. Dies gilt als einer der Gründe, warum in Deutschland diese Behandlung immer öfter gewählt wird, die Zahl der Bypass- Operationen hingegen abnimmt. Die vor-liegenden Studienergebnisse lassen jedoch den Schluss zu, dass dies nicht immer die optimale Behandlungsoption ist. Herzkran-ke Diabetespatienten sollten daher bereits frühzeitig umfassend informiert werden, damit sie eine Entscheidung für Bypass oder Stent treffen können.Literatur: Farkouh M, Domanski M, Sleeper L et al. (2012) Strategies for Multives-sel Revascularization in Patients with Diabetes. N Engl J Med, 367:2375-2384, DOI: 10.1056/NEJMoa1211585