ROYAUME DU MAROC Université Mohammed V - Rabat Faculté de Médecine et de Pharmacie
RABAT
R
R
é
é
a
a
l
l
i
i
s
s
é
é
p
p
a
a
r
r
Docteur Hind IDRISSI
Résidente en radiologie
Mémoire de fin d’études
Pour L’obtention du Diplôme National de Spécialité
en
IMAGERIE MEDICALE
Intitulé
Transplantation rénale : Place de l’imagerie
Expérience de l’HMIMV de Rabat
Sommaire
INTRODUCTION ...1
BILAN PRE-GREFFE ...4
1 / Chez le receveur ...5
2/ Bilan pré-greffe chez le donneur vivant ...7
RAPPEL SUR LA TECHNIQUE CHIRURGICALE ... 15
BILAN POST GREFFE ... 18
MOYENS D’IMAGERIE ... 19
1 / L’Echo-Doppler ... 19
2/ LE SCANNER ... 23
3) L’IRM ... 24
4 / L’angiographie ... 26
5 /La Radiologie interventionnelle ... 26
MATERIELS ET METHODES... 27
RESULTATS ... 29
A- Analyse épidémiologique ... 30
1. Receveurs ... 30
1.1. Age des receveurs ... 30
2.2. Sexe des receveurs ... 30
2. Donneurs ... 30
2.1. Age des donneurs ... 30
2.2 Sexe des donneurs ... 31
1. Échographie couplée au doppler ... 34
2. Scanner ... 34
3.IRM ... 34
D/ Les complications ... 35
1. Complications vasculaires ... 35
2. Complications urologiques et collections péri-rénales ... 40
3. Complications parenchymateuses ... 44
DISCUSSION ... 45
A/Complications vasculaires ... 49
1.Les complications vasculaires précoces ... 49
2.Les complications vasculaires tardives ... 51
B/Collections rénales et péri rénales ... 54
1. La lymphocèle ... 54
2. Les hématomes ... 54
3. L'abcès péri rénal ... 55
C/Complications urologiques ... 55
1 -Uropathie obstructive ... 55
2. Les fistules urinaires ... 56
3. Reflux vésico-urétéral ... 57
D /Complications néoplasiques ... 57
L’activité médicale de transplantation rénale est née dans les années 1950.
Elle constitue actuellement le traitement de choix de l’insuffisance rénale
terminale. Ses résultats sont parmi les plus satisfaisants de toutes les
transplantations d’organes solides, aussi bien sur le plan fonctionnel qu’en
gain de qualité de vie.
L’amélioration
des
résultats
des
transplantations
rénales
est
considérablement facilitée par les progrès de l’imagerie qui joue un rôle majeur
dans l’évaluation du greffon potentiel chez le donneur à la recherche d’une
contre-indication et pour la cartographie vasculaire chez le donneur vivant.
Après la greffe, l’imagerie joue un rôle essentiel dans le diagnostic des
complications vasculaires et urologiques.
Les complications post-transplantation rénale peuvent être divisées en
complications précoces (jusqu’à 28 jours après la transplantation) et tardives, et
en complications vasculaires et non vasculaires. Quant aux complications
médicales propres au rein transplanté, les résultats de l’imagerie sont peu
informatifs.
L’échographie-doppler couleur est la méthode d’imagerie de première
intention dans la majorité des cas. L’imagerie par résonance magnétique (IRM)
occupe aujourd’hui une place très importante dans la stratégie diagnostique
Les objectifs de ce travail sont :
- Rappeler la place de l’imagerie dans les différentes phases de la
transplantation rénale.
- Rapporter l’expérience de l’hôpital militaire en insistant sur les
complications post- greffe.
1 / chez le receveur :
Le bilan doit être réalisé avant l’inscription sur la liste d’attente dans le but de
rechercher les contre-indications à la transplantation et de réaliser un bilan morphologique précis. Ce dernier permet d’estimer la faisabilité du geste chirurgical et
détecter des pathologies associées qui pourraient affecter la survie du greffon.
Certaines procédures radiologiques sont effectuées en routine : Radiographies standard (radiographie de thorax ; des sinus ; panoramique dentaire), échographie cardiaque, échographie Doppler des carotides et des membres inférieurs avec un bilan cardiovasculaire systématique et la mammographie chez la femme de plus de 40ans.
Le scanner est l’examen de référence qui permet, en un seul temps et de façon non invasive, d’effectuer le bilan vasculaire complet et celui de la cavité abdominale.
Technique du scanner :
Le protocole dépend du statut de dialyse du patient :1,2
pour les patients non dialysés ou avec Dialyse péritonéale : la fonction rénale résiduelle peut être altérée par l’injection d’un produit de contraste. Une acquisition sans
injection doit être faite sur l’abdomen et le pelvis voir même le thorax avec un complément
d’écho-doppler.
pour les patients dialysés, l’examen est effectué sans et avec injection de produit de contraste sur l’abdomen et le pelvis. L’acquisition avec injection se fait en deux phases :
• phase artérielle : L’acquisition peut être effectuée avec un bolus tracking dans l’aorte abdominale ou entre 20 et 30 secondes après l’injection
• phase veineuse : à 70 s du début de l’injection Résultats :
L’acquisition sans injection : permet l’analyse des calcifications vasculaires aorto-iliaques, des lithiases urinaires et d’évaluer la liberté de la fosse iliaque en particulier chez les patients porteurs de reins polykystiques et chez les femmes (recherche d’éventuelle masse annexielle).
Analyse des plaques d’athérome : Localisation antérieure ou postérieure, l’étendue et le degré de sténose de la lumière vasculaire. Le chirurgien peut être amené à choisir le côté le moins atteint, ou décider de réaliser une anastomose termino-terminale sur l’artère iliaque interne lorsque celle-ci est indemne de calcifications. La phase veineuse : permet d’étudier les reins natifs (obstruction, lithiase, infection ou tumeur) et permet la recherche de néoplasie vésicale ou autre.
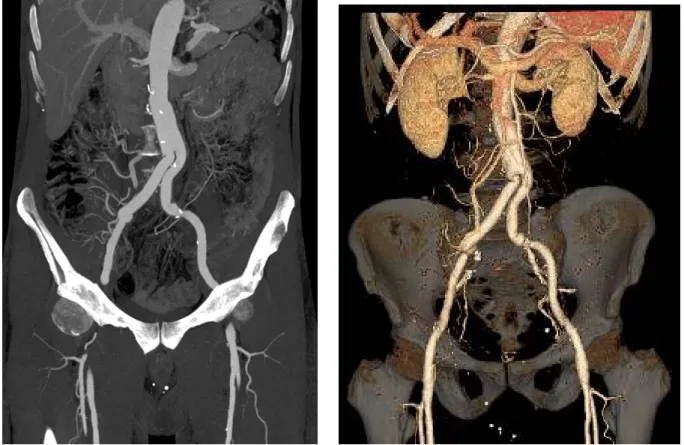
Figure 1et 2 : Bilan du receveur. Analyse artérielle de l’axe iliaque externe en reconstruction MIP et VRT.
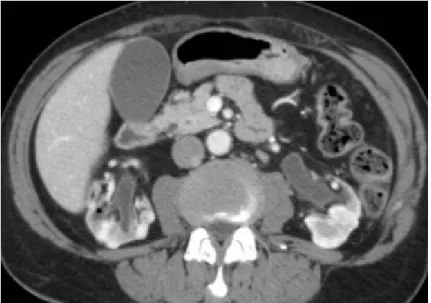
Figure 3 : syndrome obstructif urinaire bilatéral des reins natifs avec lithiase calicielle gauche.
L’IRM :
Examen de seconde intention pour évaluer les reins natifs, notamment multi- ou polykystiques à la recherche d’un processus tumoral. Il faut éviter l’injection de gadolinium si clairance inférieure à 30 ml/mn
2/ Bilan pré-greffe chez le donneur vivant :
3 types de prélèvements peuvent être réalisés à partir d’un : Donneur décédé en état de mort encéphalique (DDME) ; Donneur décédé à cœur arrêté (DDCA) ou Donneur vivant.
L’imagerie préopératoire du donneur vivant doit préciser les données anatomiques et fonctionnelles pour la sélection du donneur et la planification chirurgicale. La
cartographie vasculaire est un enjeu majeur du bilan préopératoire. Une évaluation complète
du réseau artériel et veineux est indispensable pour éviter les complications vasculaires chez le donneur et le receveur et pour le choix du rein le plus approprié au prélèvement.
D’une manière générale, le rein gauche est choisi de préférence, en raison de la longueur de la veine et de la plus grande facilité de dissection de l’artère.
Les contre-indications chirurgicales absolues à la néphrectomie sont les suivantes : tumeur, maladie polykystique, rein en fer à cheval, rein ectopique, duplication urétérale,
Le scanner multibarrettes (TDM) permet un balayage multiphasique, avec une collimation fine et une excellente résolution spatiale. Il permet une étude morphologique rénale, de l’arbre urinaire (calculs, malformation, tumeur, etc.) et de l’ensemble de la cavité abdominale.
Technique de l’ANGIO-URO-TDM 1
La technique d’acquisition n’est pas standardisée avec un nombre de passage variable (2 à 4 passages), dont l’objectif est une bonne analyse vasculaire artérielle et veineuse. On injecte 125 à 150 ml de produit de contraste non ionique à 350 mg, à un débit de 4 à 5 ml/sec (injecteur automatique). L’exploration de la voie excrétrice peut être réalisée par une spirale tardive avec injection de Lasilix. Le protocole d’acquisition le plus couramment admis comporte 4 phases.
Protocole à quatre phases :
• Phase I : sans injection, centrée sur les reins ;
• Phase II : phase artérielle, l’acquisition se fait avec un « bolus tracking » ou avec un temps empirique de 25 à 30 s, elle va permettre une meilleure analyse artérielle et veineuse,
• Phase III : phase veineuse, à 70 secondes après injection, pour une meilleure analyse veineuse, en particulier gonadique et lombaire.
• Phase IV : phase excrétoire, à environ six minutes après le début de l’injection pour l’analyse de l’anatomie de l’arbre urinaire.
Le protocole à une phase combine la phase artérielle et de la phase excrétoire avec un fractionnement du produit de contraste mais présente comme limite l’analyse veineuse qui peut être insuffisante, notamment pour les veines lombaires et gonadiques.
L’anatomie artérielle:
• Deux tiers des personnes ont des artères rénales uniques
( figures 5 et 6)
. Parmi les variantes, on retrouve : les artères rénales multiples (trajet en partie hilaire), les artèrespolaires surnuméraires (trajet trans-cortical polaire) (figure7) et la division pré-hilaire (15
à 20 mm de l’origine de l’artère) (figure 8) .
• Pour chaque artère, il faut préciser le trajet, le calibre et d’éventuelles anomalies
Figure 7 : Reconstruction coronale MIP d’une TDM avec injection de PC au temps artériel chez un donneur vivant : Artères surnuméraires polaires.
Figure8 : Reconstruction axial MIP d’une TDM avec injection au temps artériel . chez un donneur du service : division précoce de l’artère rénale gauche .
L’anatomie veineuse :
La veine rénale gauche est plus longue ; elle est rejointe par les veines gonadique, surrénalienne gauches, et lombaires.
Les veines rénales peuvent être multiples dans 15 à 30% des cas.
Anomalies complexes du trajet : veines rétro aortique ; circum aortique , confluence extra hilaire ou latéro aortique gauche .
Lorsqu’il est volumineux, le tronc rénal azygolombaire (TRAL) doit être signalé et son diamètre précisé, des veines gonadiques multiples sont présentes dans 15 % des cas ; lorsqu’elles sont volumineuses, elles doivent également être signalées ;
Les voies excrétrices :
La présence d’une duplication urétérale doit être recherchée : c’est une contre-indication à la transplantation.
RESUME DU BILAN PRE GREFFE
RECEVEUR
DONNEUR
TECHNIQUE
TDM
Patients non dialysés :
acquisition sans injection
Patients dialysés :
acquisition sans et avec
injection au temps artériel
et si besoin
néphrographique
Acquisition sans injection
reins/bifurcation,
Acquisition avec injection
(artériel, néphrographique
et excrétoire).
ELEMENTS
A
PRECISER
DANS LE
COMPTE-RENDU
Analyse des vaisseaux
aorto-iliaques : Calibre,
Analyse des calcifications
vasculaires (situation,
longueur des plaques,
caractère circulaire ou
non, sténosant ou non,
épaisseur et densité),
Liberté de la fosse iliaque
droite,
Étude des reins natifs et
de l’arbre urinaire
(infection, lithiase,
obstruction, tumeurs).
Analyse du parenchyme
rénal : taille des reins,
symétrie, anomalies
kystiques, tumorales.
Analyse artérielle :
nombre, calibre et trajet
Analyse veineuse :
nombre, calibre et trajet,
variantes
gonadiques/hémiazygos/
lombaires,
Analyse de l’arbre
urinaire : recherche d’une
duplication urétérale
(contre-indication à la
transplantation), calculs,
obstruction.
RAPPEL SUR LA
TECHNIQUE
CHIRURGICALE
Le prélèvement rénal : peut être effectué à ciel ouvert ou par coelioscopie, il
consiste à réaliser l'ablation d'un rein en préservant au maximum son système vasculaire et sa voie excrétrice. Il est recommandé de prélever le rein gauche en raison de la longueur de la veine rénale, car une veine courte expose au risque de thrombose en l’absence de variantes anatomiques. 3
Le site d’implantation du greffon : se fait au niveau de la fosse iliaque permettant
des anastomoses vasculaires aisées sur les vaisseaux iliaques externes, et une proximité du bas appareil urinaire pour un drainage urinaire simple de l’uretère du greffon. La première transplantation est toujours réalisée en fosse iliaque droite, Le rein est dans une position superficielle ce qui facilite sa surveillance. La fosse iliaque gauche n’est utilisée qu’après échec d’une première tentative effectuée à droite. Ce site est moins aisé car le sigmoïde est moins facile à récliner et les vaisseaux sont plus profondément enfoncés dans le pelvis.
La technique opératoire de la transplantation rénale obéit à des règles
simples. Idéalement la première transplantation est réalisée dans la fosse iliaque droite, en position basse, rétropéritonéale. L'anastomose artérielle est faite en latéro-terminale sur l'artère iliaque externe, l'anastomose veineuse en termino-latérale sur la veine iliaque externe, l'uretère est réimplanté dans la vessie selon la technique de Lich Gregoir, intubé par une endoprothèse 4, 5.
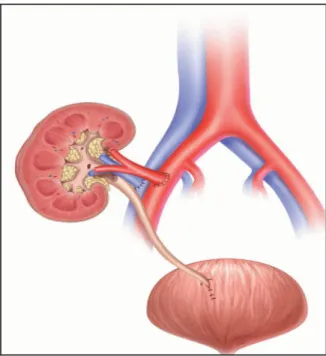
Figure 13 : Procédure chirurgicale standard de transplantation rénale
Figure 14 : L’anastomose urétéro-vésicale par voie extra-vésicale selon la Technique de Lich-Grégoire.5
MOYENS D’IMAGERIE :
Plusieurs techniques d'imagerie non invasives ont été développées et améliorées au cours des dernières années qui facilitent la détection des complications postopératoires
vasculaires et non vasculaires ainsi que le diagnostic d'autres maladies liées à l’allogreffe.
Bien que la biopsie soit généralement nécessaire pour un diagnostic définitif dans bon nombre de ces cas, il convient de noter le rôle que joue l'imagerie dans l'orientation de ces procédures.
1 / L’Echo-Doppler :
L'échographie couplée au doppler est l’examen d'imagerie de première intention permettant une analyse morphologique et hémodynamique.
C’est un examen anodin vu l’absence d’exposition aux rayonnements et la non utilisation des agents de contraste iodés potentiellement néphrotoxiques. rapide avec étude en temps réel.6
La fréquence des examens de surveillance systématique, en dehors des complications, est variable en fonction des équipes : un premier examen de référence est programmé vers
J15-20 (retour à la normale de la fonction rénale en postgreffe) ; puis un autre examen à 3 mois (pic de fréquence des sténoses de l’artère rénale) et un examen de surveillance annuel
au minimum par la suite.9
1.1 Technique :
L'évaluation de greffon est facile en raison de sa localisation dans la fosse iliaque, en avant des vaisseaux iliaques. L'évaluation comprend la taille du greffon, l'échogénécité parenchymateuse et la différenciation cortico-sinusale ainsi que le système collecteur et les tissus mous environnants.
De manière générale, une sonde barrette courbe ou sectorielle de 2 à 5 MHZ donne une bonne évaluation globale et permet la détection des collections péri-rénales ainsi que l’étude des anastomoses veineuses et artérielles.7Une sonde de haute fréquence 7à12 MHz permet de visualiser le flux au sein du cortex le plus superficiel . 8
L’étude de la vascularisation du greffon en imagerie couleur s’effectue en trois temps :9 • Etude de la vascularisation périphérique intraparenchymateuse ;
1.2 Résultats :
L'aspect général du rein transplanté est similaire à celui du rein natif normal ( fig 15) . Le greffon est généralement plus grand que le rein natif. Comme pour les reins natifs, les pyramides médullaires sont hypo-échogènes au cortex rénal et les sinus sont hyperéchogènes .10,11 les calices et le bassinet sont souvent visualisés au début de la période post-opératoire par œdème au niveau de l'anastomose vésico-urétérale en supposant que la fonction rénale est normale, afin de ne pas créer de confusion lors de l’étude échographique.7
Les vaisseaux au niveau hilaire ne doivent pas être confondu avec le bassinet et ils peuvent facilement être distingué par l'utilisation de Doppler couleur .7
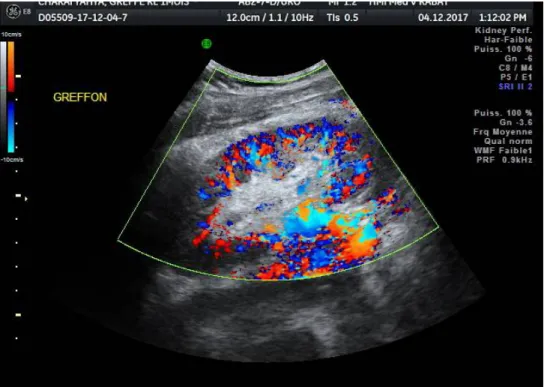
L’échographie est également utile dans l'évaluation de l'espace péri rénal , où des collections liquidiennes peuvent être présentes. L'utilisation du Doppler couleur et l'analyse spectrale améliore considérablement l'évaluation de la greffe rénale. Le doppler permet d'évaluer les principaux vaisseaux rénaux ainsi que la vascularité du parenchyme rénal. Le rein transplanté doit présenter une arborisation de perfusion vive et diffuse ( fig16 ) . L’analyse spectrale obtenue en doppler pulsé permet de vérifier les caractéristiques normales du flux artériel, avec enregistrement au niveau pédiculaire de vitesses systoliques normales voisines de 100cm, en général toujours inférieures à 190cm/s.4
Fig16 : Vascularisation riche et homogène de tout le cortex du greffon .
Figure 18 : Aspect normal d’un enregistrement spectral dans une artère périphérique avec des Index de résistance égale ou légèrement inférieur de celui de l’artère rénal ( mesuré à 0,59).
2/ LE SCANNER :
Les indications du scanner sont limitées par la néphrotoxicité des produits de contraste iodés. Il est surtout utilisé pour caractériser certaines collections postopératoires et dans le diagnostic des pyélonéphrites aiguës. L’angioscanner permet d’étudier le pédicule artériel. Il est actuellement concurrencé par l’angio-IRM qui a l’avantage d’utiliser un agent de contraste non néphrotoxique (complexe de gadolinium).9
Figure20
3) L’IRM :
Les indications de l’IRM sont orientés par l’écho doppler toujours réalisé en première intention , l’avantage de l’imagerie par résonance magnétique (IRM) comparativement au scanner réside dans l’utilisation des agents de contraste non néphrotoxiques.9 L’étude du rein transplanté se fait à l’aide d’antennes de surface. Le champ d’exploration doit être large couvrant la vessie à fin d’étudier l’anastomose utérovésicale.
Protocole :
Les séquences clés sont :
Les séquences pondérées en T1, avant et après injection IV de produit de contraste. Les séquences en écho de spin pondérées en T2, sont utiles lorsqu’il existe une
collection péri rénale.
Et les séquences d’angio-IRM, avec ou sans injection de contraste, centrées sur le pédicule rénal, permettent d’étudier l’anastomose et le tronc de l’artère rénale .12 Résultats :
L’aspect normal du rein transplanté en IRM n’est pas différent de celui des reins natifs. Les coupes obtenues après injection de gadolinium montrent un rehaussement de signal intense et homogène du parenchyme rénal et l’opacification du système excréteur sur les coupes tardives .
Figure 22
Figure 23
4 / L’angiographie :
Bien que l'angiographie conventionnelle est un examen invasif et nécessite l’administration d’un produit de contraste intra vasculaire iodé néphrotoxique, elle est la référence absolue pour l'évaluation des fistules artério-veineuses, des pseudo-anévrismes et de la sténose de l'artère rénale. En pratique, les anomalies vasculaires sont généralement détectées initialement par échographie Doppler et peuvent être confirmées par angiographie IRM. L'angiographie conventionnelle avec des techniques de soustraction numérique est réservée à la confirmation des anomalies suspectées immédiatement avant les interventions transcathéters percutanées ultérieures telles que l'angioplastie et la mise en place d'un stent dans la sténose de l'artère de transplantation ou l'embolisation d'une fistule.
5 /La Radiologie interventionnelle :
La radiologie interventionnelle est inestimable dans la prise en charge des complications vasculaires et urétérales et dans le drainage percutané des collections de fluides.
MATERIELS
ET METHODES
Notre travail a été mené au sein de l’Hôpital Militaire d’Instruction Mohamed V sur une période de onze ans allant de juin 2008 à décembre 2019, portant sur des patients transplantés rénaux. On a colligé quarante-neuf cas de transplantation rénale réalisés par l’équipe de transplantation de l’Hôpital Militaire d’Instruction Mohamed V. Nous avons étudié leurs dossiers médicaux tout au long de la période post greffe rénale ; et nous avons pu recueillir des données relatives aux aspects démographiques, paracliniques et évolutifs de ces malades.
1-Selection des patients :
Les critères d'inclusion :
Patients ayant bénéficié d’une greffe rénale au sein de l’Hôpital Militaire d’Instruction Mohamed V de Rabat.
Les critères d'exclusion :
Les patients suivis ayant été transplanté en dehors de l’Hôpital Militaire d’Instruction Mohamed V de Rabat.
Imagerie :
Tous les greffons ont été explorés en 1ére intention par échographie couplée au doppler couleur, les autres examens d’imagerie ont été réalisés en seconde intention : Scanner ( 3 cas ) et angio IRM ( 7 cas ).
Femmes 22%
Hommes 78%
Répartition selon le sexe :
A- Analyse épidémiologique :
1. Receveurs :
1.1. Age des receveurs :
La moyenne d’âge des receveurs était de 36,6±12,8 ans avec des extrêmes allant de 17 à 56 ans.
2.2. Sexe des receveurs :
On a noté une prédominance masculine, avec une répartition :38 hommes (77,5%), contre 11 Femmes (22,5%) ; avec un sexe ratio H/ F de 3,4 (Figure 1)
2. Donneurs
2.1. Age des donneurs :
L’âge des donneurs variait entre 23 et 53 ans. La moyenne d’âge était de 39.61 ± 9.81 ans.
2.2 Sexe des donneurs :
On a noté une prédominance féminine : 31 femmes, 18hommes avec un sexe ratio H/F de 0,58 (Figure2)
3. Lien de parenté
Tous nos greffes rénaux ont été prélevés à partir de donneurs vivants apparentés répartis en lien de parenté comme suit : 20 conjoints, 16 parents, 8 frères et 4 sœurs, et une tante. (Figure 3)
lithiasique 12% vasculaire 12% glomérumaire 8% nephrite tubulo interstitielle 4% polykystose rénale 6% intdeterminée 43% RVU 15%
NÉPHROPATHIE CAUSALE :
B / Néphropathies causale :
La néphropathie causale est d’origine indéterminée chez 28 patients de notre série soit 58%, alors qu'elle a pu être déterminée chez 21 patients soit 42% et répartie comme suit : (Figure4)
Lithiasique dans 6 cas, Vasculaire dans 5 cas, Glomérulaire dans 4 cas,
Par reflux vésico-urétérale dans 7 cas,
Par néphrite tubulo-interstitielle chronique dans 2 cas Polykystose rénale dans 3cas.
C /Imagerie :
1. Échographie couplée au doppler :
Réalisée de façon systématique chez tous les patients : - à J0 dans les 6 à 12h après greffe.
En urgence devant :
Une perturbation de la fonction rénale et /ou de la tension artérielle. Douleur abdominale aigue.
Syndrome hémorragique .
2. Scanner :
En complément à l’échographie, le scanner a été réalisé chez 3 patients
3. IRM :
L’IRM a été réalisé chez 7 patients sur un appareil Général électrique 1 ,5 Tesla .
Le protocole IRM utilisé est le suivant :
Séquences
Intérêt
séquences pondérées en T1,
avant et après injection IV de
produit de contraste
Collection péri rénale
Nécrose corticale
Les séquences en écho de
spin pondérées en T2
collection péri-rénale
D/ Les complications :
1. Complications vasculaires :
- Thrombose de la veine rénale post opératoire précoce : 1 cas.
- Thrombose de l’artère rénale : 1 cas
- Sténose de l’artère rénale : 2 cas.
2. Complications urologiques et collections péri-rénales :
- Hématome : 5 cas
- Lymphocèle : 3 cas.
- Sténose urétérale : 1 cas.
- Lithiase du greffon :0 cas
3. Complications parenchymateuses :
- Rejet du greffon (chronique) : 1 cas1. Complications vasculaires :
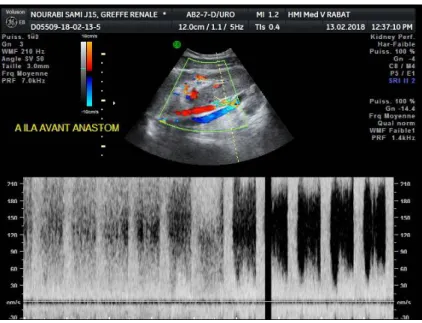
1.1. Sténose de l’artère rénale :Cas 1 : Patient de 48 ans, à j15 post greffe, altération de la fonction rénale
Figures 28et 29 : Echographie en mode doppler du greffon rénal ; montre une zone d’aliasing dans la partie proximale de l’artère rénale en pré-anastomotique .
Figure 30 : Les tracés Doppler spectraux : montrent des vitesses systoliques maximales, et des turbulences.
Cas 2 : Patient de 34ans, greffé depuis 6mois. Altération progressive de la fonction
rénale, le doppler trouve des signes directs de sténose , un complément IRM est réalisé.
Figure31 : Greffon d’aspect normal Sans dilatation des cavités excrétrices , les tracés doppler
1.2. Thrombose veine rénale :
Cas 3 : patient de 45 ans , suspicion d’une thrombose de la veine rénale sur le doppler
couleur réalisé en urgence chez un patient devant la non reprise de la diurèse .
Figure 34 Figure 35
Figures 34et 35 : Angio IRM au temps artériel et veineux: bonne opacification des artère inter lobulaires , de l’artère pédiculaire , absence d’opacification de la veine du greffon et des veines
inter lobulaires
Figure 36: IRM en coupe axial LAVA au temps veineux montrant une thrombose veineuse avec ischémie parenchymateuse.
1.3 : Thrombose de l’artère rénale :
Cas 4 : Patient présentant à trois semaines après transplantation rénale ;une ischémie
massive liée à la thrombose de l’artère rénale ,
Figures 37et 38 : IRM en coupes coronale et axiale T1 FATSAT objectivant une nécrose étendue du greffon .
2. Complications urologiques et collections péri-rénales :
2.1. Hématomes :Cas 5 : jeune fille de 23 ans, échographie réalisée à j6 après la transplantation.
Figures 39 et 40 : Greffon de taille normal , bonne différenciation cortico médullaire , avec collection de 7.5 cm hyperéchogène bien limitée entre le pôle inferieur du rein et la vessie en
Cas 6 : Patent de 35 ans , asymptomatique découverte d’une collection péri rénale à
l’IRM à 1mois après la transplantation .
Figures 41et42 : IRM en coupes sagittale T2 et coronal T1 avec FATSAT ; Collection hématique auteur des vaisseaux iliaques, en hyper signal périphérique T1 , à centre hétérogène , hyper
2.2 : Lymphocèle :
Cas7 : échographie à deux mois après transplantation rénale chez un patient
asymptomatique
Figure 44 : Collection péri rénale finement cloisonnée en faveur d’une lymphocèle.
CAS 8 : patient de 45ans , asymptomatique .
Figures 45et 46 : IRM coupes ; coronale en SP T2 FS, axiale T1 : collection péri rénale contournant le pyelon de signal hétérogène :Lymphocèle
2.3. Sténose urétérale :
Cas 9 : patient de 55 ans, ayant présenté à un 1an après la greffe, une augmentation des chiffres de la créatinémie .
3.Complications parenchymateuses :
Rejet du greffon :Cas 10 : Insuffisance rénale à 11 ans de la greffe, suspicion de rejet chronique confirmé
lors de la biopsie rénale.
Figure 50: Greffon augmenté de taille globuleux avec perte de la différentiation cortico médullaire, absence de dilatation des cavités excrétrices.
La surveillance radiologique joue un rôle principal dans le diagnostic précoce des complications chirurgicales, quant aux complications médicales les résultats de l’imagerie restent peu spécifiques et limitent le plus souvent son rôle à la surveillance évolutive.
L’enquête étiologique des complications débute par un échodoppler. Ce premier examen d’imagerie a pour objectif principal d’éliminer une complication chirurgicale vasculaire ou urologique. L’imagerie par résonance magnétique (IRM) occupe une place aujourd’hui très importante dans la stratégie diagnostique grâce à l’innocuité des agents de contraste utilisés notamment dans l’étude du pédicule vasculaire (angio-IRM) et le diagnostic des troubles de perfusion du greffon.
Les complications post-transplantation rénale peuvent être divisées en complications précoces (jusqu’à 28 jours après la transplantation) et tardives (après 28 jours de transplantation), et à des complications vasculaires et non vasculaires. Les complications les plus courantes sont : le rejet aigu, la nécrose tubulaire aigue, thrombose de l’artère rénale, thrombose veineuse rénale, collections périphériques, obstruction urinaire, sténose de l’artère rénale, anévrisme et faux anévrisme de l’artère rénale, la fistule artérioveineuse , et le rejet chronique. 13
L’hémorragie, la fuite urinaire et la pyélonéphrite peuvent également se produire. Il convient également de noter une susceptibilité accrue à développer une tumeur maligne et une surinfection
Les complications peuvent être classées en quatre grands groupes résumés dans le tableau suivant (tableau2) :
Complications
vasculaires :
Collections
rénales et péri
rénales :
Complications
urologiques
Complications
néoplasiques :
-Thrombose de
l’artère rénale ,
-Thrombose de
la veine rénale, -
Nécrose
corticale
-Sténose de
l’artère rénale
-Sténose de la
veine rénale
-FAV,
anévrisme et
faux anévrisme
-Hématome.
-Lymphocèle
-Abcès péri rénal
-Abcès rénal
-Urinome.
-Sténose urétérale
-Fistules urinaires
-RVU
- Lymphomes
- Carcinome
primitif du rein
natif .
A/Complications vasculaires :
En fonction de leur moment d’apparition après la transplantation, on distingue :
Les complications vasculaires précoces ou aigues : thrombose de l’artère rénale, thrombose de la veine rénale , nécrose corticale .
Les complications vasculaires tardives : sténose de l’artère du greffon, FAV, anévrisme et faux anévrisme,
Les complications vasculaires peuvent aussi être classées en fonction de leur caractère occlusif (sténose de l’artère, sténose et thrombose de la veine, occlusion artérielle et infarctus) ou non occlusif (anévrismes et faux anévrismes, fistule artério-veineuses post-biopsie).
1)-Les complications vasculaires précoces :
Thrombose de l’artère rénale :
La thrombose de l'artère rénale est une complication rare qui survient dans moins de 1% des cas, elle est précoce mais très grave car elle aboutit à la nécrose de l’ensemble du greffon. L’occlusion primitive de l’artère est généralement en rapport avec une malposition (torsion ou plicature) favorisée par une longueur trop importante du vaisseau ou une malfaçon de l’anastomose artérielle. La thrombose secondaire, plus rare, représente le plus souvent l’évolution finale d’un épisode de rejet très sévère, de type vasculaire, avec occlusion des artères parenchymateuses.9. Le Doppler couleur montre une absence de signaux artériels et
veineux intrarénaux, associée à la disparition de l’artère rénale circulante au niveau du
pédicule .14,15 L’IRM et le scanner avec injection de produit de contraste sont très performantes pour le diagnostic et montre typiquement une absence complète de rehaussement de signal dans la totalité du parenchyme rénal après injection de produit de contraste .
L’occlusion d’une artère polaire est une complication plus fréquente conduit à un
infarctus segmentaire. En échographie mode B, l’échostructure du cortex nécrosé se modifie
rapidement pour devenir hypoéchogène , au Doppler ça apparait comme un territoire dépourvu de signaux en imagerie couleur. Pour les infarctus de petite taille l’administration des agents de contraste est indiquée, et améliore considérablement les performances de l’écho-doppler. 7L’IRM et le scanner avec injection de produit de contraste sont très
On a noté un seul cas de thrombose artérielle dans notre étude avec nécrose massive et étendue du greffon.
Thrombose de la veine du greffon :
La thrombose de la veine rénale est également un événement rare , il se produit dans environ 4 % des cas, généralement pendant la période postopératoire immédiate.16C’est une cause fréquente de perte précoce du greffon . Elle peut être secondaire à : 17
Un problème technique peropératoire avec une ischémie chaude prolongée ; Une hypovolémie en peropératoire favorisant l’hypercoagubilité ;
Une extension d’une thrombose Ilio-fémorale préexistante
Une compression extrinsèque de la veine par une collection postopératoire ;
La greffe à partir d’un rein droit d’un donneur une veine courte et une artère longue;
Un bas débit artériel dans un greffon adulte transplanté chez un petit enfant ou un syndrome néphrotique cortico-résistant comme maladie primaire.
Ailleurs, la thrombose veineuse du greffon peut être idiopathique.
Le diagnostic de thrombose précoce en doppler doit être évoqué devant des enregistrements artériels très “résistifs” avec reflux diastolique massif (aspect de
va-et-vient) et absence de signaux veineux dans l’ensemble du greffon , associés à des
modifications de l’échostructure qui traduisent l’infarcissement du parenchyme.
Une thrombose veineuse du greffon doit être systématiquement recherchée devant la non reprise de la diurèse en post transplantation, ou devant une cassure de la diurèse après une reprise brève de trois à 72 heures.
La nécrose corticale :
La nécrose corticale est une complication également rare, mais grave, elle peut intéresser le cortex superficiel, le cortex profond ou la médullaire.
Le diagnostic est difficile, car au stade initial, les artères et veines segmentaires, voire
inter lobaires, restent perméables. L’échographie ne montre que des modifications
morphologiques, à type de gros rein globuleux, plus ou moins hétérogène. Le doppler couleur montre une raréfaction des vaisseaux au niveau du cortex et l’analyse spectrale une augmentation des résistance artérielle, avec de façon tardive une disparition complète du flux positif en diastole.4
C’est l’échographie de contraste qui objective le défaut de vascularisation d’une bande parenchymateuse sous corticale, parois étendue au cortex profond et à la médullaire. 15
Le scanner ou mieux l’IRM, permet d’évaluer avec précision l’extension de la nécrose et a une efficacité diagnostique supérieure à celle de l’écho-doppler conventionnel, surtout pour les nécroses corticales et les infarctus profonds .14 Les acquisitions en contraste T1 après injection de gadolinium, et notamment les séquences dynamiques, objectivent une absence de rehaussement de signal dans la zone nécrosée.14
2)-Les complications vasculaires tardives :
2.1 Sténose de l’artère rénale du greffon :La Sténose de l’artère rénale est la complication vasculaire la plus courante des greffes rénales avec des incidences allant de 1%à 23 % .19Le délai de découverte d’une sténose est variable, le plus souvent entre le deuxième et le quatrième mois après la greffe.9 La sténose siège le plus souvent sur le tronc de l’artère rénale .4 Le rétrécissement est en règle court et régulier , il peut intéresser l’ensemble du tronc de l’artère rénale et parfois s’étendre sur une branche de division. Les sténoses sur plicature représentent près de 30 % des sténoses de l’artère du greffon. La présentation clinique est variable est non spécifique : hypertension réfractaire, rétention d’eau, augmentation de la valeur de la créatinine sérique, œdème sont les symptômes les plus courants. Le site, la morphologie et le délai de survenue de la sténose peuvent donner une orientation sur son origine :20,16
• une courbure marquée de l’artère peut apparaître lorsque l’artère est plus longue que la veine, ce qui est le cas si, par exemple, le rein droit est greffé en fosse iliaque gauche et en cas d’artères multiples. Une courbure marquée entraîne une accélération des vitesses dans l’artère ;
• des sténoses multiples, longues, d’apparition relativement tardive, peuvent traduire des lésions endothéliales liées à un rejet et/ou à l’effet des immunosuppresseurs qui ont été suspectés d’induire des lésions.
• une sténose tardive, localisée, survenant plusieurs années après la greffe, suggère en premier lieu une atteinte athérosclérotique de l’artère rénale du greffon .
Le diagnostic initial de la sténose repose sur le doppler. Les enregistrements en doppler pulsé du pédicule artériel recherchent les signes hémodynamiques observés au niveau de la sténose (signes directs) , et signes indirects rencontrés en aval, au niveau des artères interlobaires.
Les signes directs associent, plusieurs anomalies: 4
En mode Doppler couleur : la présence d’un artefact périvasculaire. L’ajustement des PRF adapté à des vitesses élevées permet d’aborder l’analyse de l’artère elle-même, et de montrer une zone d’aliasing, traduisant l’accélération des vitesses ; Le mode pulsé montre des vitesses systoliques maximales (VSM) élevées dont le
seuil est difficile à fixer. La majorité des études s’accordent sur un seuil supérieur
à 200cm/s.
Les signes indirects ne sont observés qu’en cas de sténose très serrée. Ils
comprennent :
Un aspect amorti des tracés Doppler interlobaires : l’amortissement (est affirmé devant une augmentation du temps de montée systolique supérieur à 0,07. 21 une baisse de l’IR, qui, passant sous le seuil de 0,55 .22
Durant notre étude, nous avons eu deux cas de sténose au niveau de l'anastomose artérielle du greffon.
2.2 Les fistules artérioveineuses (FAV) :
Résulte d’un traumatisme vasculaire pendant la biopsie percutanée. Les fistules artérioveineuses se forment lorsque l’artère et la veine sont lacérées. La majorité de ces lésions sont petites, cliniquement insignifiantes et disparaissent généralement spontanément ; ainsi, la fréquence de cette complication est inconnue. 24Les FAV peuvent se manifester par une hématurie importante et persistante, une hypertension ou une insuffisance rénale (pour les FAV à haut débit). Les FAV sont facilement identifiables au Doppler couleur par un flux couleurs désorganisé en dehors du territoire vasculaire rénal normal, une apparence qui est attribuée à la transmission des vibrations dans le tissu entourant la fistule. 25L'artère nourricière et la veine drainante peuvent être visualisées avec des réglages de gain. L’angioscanner avec reconstructions 3D est une bonne alternative en cas de doute diagnostic.
Le traitement est indiqué en cas d’hématurie macroscopique ou si la taille de la fistule est supérieure à 15 mm de diamètre. L’embolisation sélective par voie fémorale percutanée sous contrôle angiographique est actuellement le traitement de choix offrant le maximum de chances de conserver un transplant fonctionnel.26
Au cours de notre étude nous n’avons rencontrés aucun cas de fistules après les PBR réalisées pour nos patients.
2.3 Le faux anévrisme de l’artère rénale (FA) :
Il s’agit d’une complication exceptionnelle < 1 % , il fait en général suite à des biopsies rénales ou à la mise en place d’une néphrostomie percutané , elle résulte d’une plaie artérielle traumatique .le FA correspond à une poche néoformée non endothelisalisée , alimentée et drainée par l’artère traumatisée avec laquelle elle communique avec un court chenal .4
Le FA se traduit par une image arrondie pseudo-kystique, le plus souvent intra-parenchymateuse , dont on peut repérer le caractère battant et pulsatile en échographie. En imagerie couleur, la poche contient un flux tourbillonnaire. L’enregistrement au niveau de l’orifice de communication montre un tracé en va-et-vient très caractéristique. 9 L’angio-IRM ou l’angioscanner sont nécessaires pour confirmer le diagnostic et obtenir une description
B/Collections rénales et péri rénales :
1. La lymphocèle :
La lymphocèle est une collection de liquide lymphatique située dans la fosse de transplantation unie ou multicompartimentée .C’est une complication assez fréquente de la greffe rénale, malgré toutes les précautions techniques prises , avec une incidence allant de 1à 20%.11 Le plus souvent la lymphocèle est de découverte fortuite, à l’occasion d’un contrôle radiologique du transplant. Il peut cependant exister différents tableaux cliniques révélateurs. Les principaux signes cliniques décrits sont : 28
La présence d’une masse abdominale palpable autour du transplant. Syndrome fébrile par complication infectieuse du lymphocèle. Dilatation des cavités pyélocalicielles par compression de l’uretère.
Œdème des membres inférieurs ou de thromboses veineuses profondes par compression des vaisseaux iliaques.
Sur le plan morphologique, une échographie du transplant couplée à un doppler est réalisée en première intention. Elle objectivera une structure anéchogène d’allure kystique, cloisonnée.29 L’abstention thérapeutique est la règle en cas découverte fortuite d’une lymphocèle asymptomatique, en cas d'une lymphocèle symptomatique, on peut procéder à : un drainage percutané simple, ou un drainage percutané, ou quasiment la chirurgie, selon les cas.
L’échographie abdominale était suffisante pour diagnostiquer 2 cas de lymphocèle
chez nos malades. Leur évolution était spontanément favorable sans avoir recours à la
ponction.
permet de localiser avec précision la collection , et fournit dans certains cas des arguments diagnostiques (densité élevée d’un hématome récent ) . En outre, il permet de guider un geste de ponction et de drainage percutané. l’IRM permet mieux de caractériser les collections hématiques.9
Nous avons recensé 5 cas d’hématome péri-rénal , et dont la résorption était spontané sans avoir recours au drainage.
3. L'abcès péri rénal :
Est une complication précoce rare de la transplantation rénale. Il se manifeste par un syndrome septique associé à des douleurs abdominales et à un syndrome inflammatoire biologique. A l'échographie Les abcès sont le plus souvent d’échostructure mixte , la présence d’échos brillants à l’intérieur d’une collection suggère la présence de bulles gazeuses à l’intérieur d’un abcès .30
La TDM et l’IRM confirment cet aspect avec une collection périrénale hétérogène à paroi épaissie rehaussée .27 L'abcès est traité par drainage percutané ou chirurgical.
C/Complications urologiques:
1 -Uropathie obstructive :
Une obstruction urétérale survient dans 2 à 10% des transplantations rénales.31
L'ischémie urétérale est la cause la plus courante d'obstruction précoce (environ 90% des
cas). L'uretère distal est particulièrement vulnérable à l'ischémie en raison de sa localisation anatomique, étant le plus éloigné de l'artère rénale.31 il peut s’agir également d’un œdème de l’anastomose urétérale, d’un granulome distal, d’une migration de caillots sanguins ou de fibrine, d’une torsion de l’uretère ou d’une compression extrinsèque par une collection (hématome, lymphocèle) ou une bride vasculaire. Les erreurs de technique chirurgicale sont également une cause reconnue. Un uretère long augmente le risque d'obstruction précoce. Plus tardivement, il pourra s’agir d’un calcul urétéral, d’une migration de caillot secondaire à une hématurie post-biopsique, d’une fibrose péri-urétérale, d’une sténose de l’anastomose urétérale, ou, exceptionnellement, d’une tumeur urothéliale. l’échographie met en évidence une dilatation pyélo-calicielle.14 A noter qu’une dilatation modérée et transitoire, dans la
jusqu’au niveau de l’obstacle fournit en échographie des informations précieuses sur l’origine de l’obstacle. La tomodensitométrie permet de mieux rechercher un calcul radiotransparent ou une cause de sténose extrinsèque avant d’envisager une urétéropyélographie et un éventuel traitement endo-urologique. Quant à l’uro-IRM, elle permet une exploration morphologique précise de et l’identification du niveau de l’obstacle. L’IRM est, par ailleurs, très performante dans le diagnostic des causes extrinsèques, grâce notamment à son pouvoir de caractérisation tissulaire. mais elle ne permet pas de caractériser avec certitude une étiologie lithiasique.9
Le drainage premier du transplant est la règle, que ce soit par une sonde double J ou une néphrostomie. En cas de sténose urétérale précoce, il est proposé de reprendre chirurgicalement l’anastomose pour sa réfection.
On a eu un seul cas de sténose retrouvée au niveau de l’uretère iliaque avec mise en place d’une sonde JJ .
2. Les fistules urinaires :
La fistule urinaire peut survenir de la première semaine jusqu’à 3 mois après la transplantation. Elle peut siéger à tous les niveaux, du parenchyme rénal à l’anastomose urétérovésicale, mais c’est au niveau de cette dernière qu’elles sont les plus fréquentes : 82 % des cas.26Ils résultent d’un défaut d’étanchéité de l’anastomose urétérale favorisée par un défaut de vascularisation de l’extrémité distale de l’uretère greffé ou par des lésions traumatiques au moment du prélèvement chez le donneur . Une fistule urinaire est suspectée devant : une cassure de la diurèse , un écoulement d’urine par le drainage, œdème cutané au niveau des organes génitaux externes . Lorsqu’elle apparaît plus tardivement et que les drains ont été retirés, la fistule urinaire se présente sous la forme d’une collection douloureuse autour du greffon, associée à une cassure de la diurèse et une augmentation de la créatinémie. En échographie, le diagnostic est suspecté devant l’apparition d’une collection mal limitée, souvent située à hauteur du pôle inférieur ou à proximité de la vessie, dont le volume tend à augmenter sur les contrôles successifs.26 Quant à L’uroscanner avec injection de produit de
3. Reflux vésico-urétéral :
L’incidence du reflux vésico-urétéral (RVU) est extrêmement variable (10 à 80%), et clairement sous-évaluée car sa recherche n’est pas systématique chez les patients transplantés rénaux. Il peut se révéler par des infections urinaires fébriles ou des bactériuries récidivantes. La cystographie rétrograde pose le diagnostic. Ces infections pouvant être délétères pour la fonction rénale, un traitement du reflux doit être proposé aux patients. De plus, en cas d'altération de la fonction rénale associée aux épisodes infectieux, le traitement du reflux peut l'améliorer ou au moins la stabiliser. 32
D /Complications néoplasiques :
L’utilisation prolongée du traitement immunosuppresseur après une transplantation rénale expose le receveur à un risque accru de développer une tumeur maligne . La prévalence moyenne de malignité rapportée chez ces patients est de 6%,33 avec principalement les cancers de la peau et lymphomes.
Le degré du traitement immunosuppresseur et sa durée sont deux facteurs importants dans le développement de la malignité. La fréquence des tumeurs urologiques telles que l'adénocarcinome prostatique et les tumeurs germinales du testicule ne semblent pas augmenter dans cette population. Cependant, la prévalence de l'adénocarcinome rénal peut être augmenté, avec 90% des tumeurs survenant sur le rein natif et 10% survenant dans le rein transplanté. Une des raisons de l'augmentation le risque d'adénocarcinome rénal est qu'environ la moitié des patients hémodialysés développent la maladie kystique rénale acquise et 9% développent des tumeurs.
Le Carcinome primitif :
le carcinome primitif ( CR) dans les reins transplantés a été rapporté sporadiquement avec une incidence d'environ 0,5%34. Le CR est plus susceptible de se développer dans les reins natifs d'un receveur et représente 5 à 16% des tumeurs malignes post-transplantation. 34 Il existe un risque plus élevé de CR dans les reins natifs que dans la population générale en raison de facteurs de risque bien définis de rein en phase terminale, de maladie rénale kystique acquise et d'hémodialyse chronique. Tous les patients subissant une transplantation rénale sont examinés par échographie annuelle pour le dépistage , et si une masse suspecte est
Les Lymphomes :
Après les cancers de la peau, les lymphomes représentent la deuxième cause des cancers primitifs chez le transplanté dont l’incidence est évaluée à 6 %. C’est une complication tardive de la transplantation, généralement dans les 9 ans après la transplantation. L’atteinte du greffon peut être primitive ou secondaire, sous la forme d’une lésion infiltrante corticale ou sinusale ou, plus rarement, d’une masse tumorale solide, unique ou multiple. La biopsie guidée sous scanner ou échographie est essentielle pour établir le diagnostic de certitude et de typer le lymphome avant de démarrer le traitement le traitement .9
E. Rejets de greffe :
L'imagerie joue un rôle plus limité dans l'évaluation des complications fonctionnelles. La spécificité est faible car les cas de rejet, de toxicité médicamenteuse, d'ischémie périopératoire et de nécrose tubulaire aiguë sont difficiles à distinguer les uns des autres par les seuls critères d'imagerie. 13
L'échographie ne joue généralement aucun rôle dans les cas de rejet suraigu puisque le diagnostic est généralement posé immédiatement après la re-perfusion de greffe en salle d'opération.
En cas de rejet aigu sévère, les résultats de l’IRM, sont peu spécifiques et d’un intérêt très limité en pratique clinique. L’échographie peut montrer des modifications morphologiques (gros rein globuleux). Le doppler couleur montre une raréfaction des
vaisseaux au sein du cortex et l’analyse spectrale à partir des artères intra-rénales, une augmentation des résistances artérielles.35 Cependant, la découverte d'un indice de résistance trop élevé est une découverte non spécifique qui peut également être observée dans le contexte de l'infection, de nécrose tubulaire aiguë, de l'ischémie périopératoire, d'hydronéphrose et de la compression extrinsèque . La différenciation de ces entités nécessite souvent une biopsie guidée par échographie. 9,13
La transplantation rénale (TR) est actuellement le traitement de choix de l’insuffisance rénale chronique terminale (IRCT). Ses résultats se sont améliorés au cours des dernières années.
Cependant elle est émaillée de nombreuses complications qui se caractérisent par la multiplicité de leurs étiologies et leur impact délétère sur le devenir du greffon. A travers notre étude, nous constatons que les complications les plus rencontrées, sont dominées essentiellement par : Les complications urologiques (64.2%) et vasculaires. Ainsi le meilleur traitement de ces complications et le moins coûteux reste la prévention par un bon contrôle post opératoire et devant le moindre signe d’appel.
1. Salah JBEN, Skalli AELA, Amraoui FEL, Chikhaoui N. AU POINT APPORT DE L ’ IMAGERIE DANS LE BILAN DE LA PRE-GREFFE RENALE. 2017;(January 2008):4-8.
2. Renard-Penna R, Ayed A, Barrou B, Grenier P. Bilan prétransplantation rénale du
receveur et du donneur. J Radiol. 2011;92(4):358-366.
doi:10.1016/j.jradio.2011.03.001
3. Delaporte V. Transplantation rénale à partir d’un donneur vivant. Prog en Urol. 2011;21(11):789-792. doi:10.1016/j.purol.2011.09.003
4. Ardelean A, Mandry D, Claudon M. Complications vasculaires de la transplantation rénale : conduite diagnostique Vascular complications following renal transplantation : Diagnostic evaluation. J Radiol. 2011;92(4):343-357. doi:10.1016/j.jradio.2011.02.018
5. Alberts VP, Idu MM, Legemate DA, Laguna Pes MP, Minnee RC. Ureterovesical anastomotic techniques for kidney transplantation: A systematic review and meta-analysis. Transpl Int. 2014;27(6):593-605. doi:10.1111/tri.12301
6. Panel E, Myles I, Nikolaidis P, et al. APPROPRIATE USE CRITERIA ACR Appropriateness Criteria â Renal Transplant Dysfunction. J Am Coll Radiol. 2017;14(5):S272-S281. doi:10.1016/j.jacr.2017.02.034
7. Baxter GM. Ultrasound of renal transplantation. Clin Radiol. 2001;56(10):802-818. doi:10.1053/crad.2001.0812
8. Grenier N, Claudon M, Trillaud H, Douws C, Levantal O. Urogenital radiology Pictorial review Noninvasive radiology of vascular complications. 1997;391:385-391.
11. Kolofousi C, Stefanidis K, Cokkinos DD, Karakitsos D, Antypa E, Piperopoulos P. Ultrasonographic Features of Kidney Transplants and Their Complications : An Imaging Review. 2013;2013.
12. Chan YL, Leung CB, Yu SCH, Yeung DKW, Li PKT. Comparison of non-breath-hold high resolution gadolinium-enhanced MRA with digital subtraction angiography in the evaluation on allograft renal artery stenosis. Clin Radiol. 2001;56(2):127-132. doi:10.1053/crad.2000.0590
13. Sjekavica I, Novosel L, Rupčić M, Smiljanić R, Muršić M, Duspara V.
RADIOLOGICAL IMAGING. 2018;57(4):694-712.
doi:10.20471/acc.2018.57.04.12
14. Correas JM, Poirée S, Anglicheau D, Legendre C, Hélénon O. & Apports du scanner et de l ’ imagerie par résonance magnétique. 2005;V:153-161.
15. Cosgrove DO, Chan KE. Renal transplants: What ultrasound can and cannot do.
Ultrasound Q. 2008;24(2):77-87. doi:10.1097/RUQ.0b013e31817c5e46
16. Granata A, Clementi S, Londrino F, et al. Renal transplant vascular complications: the role of Doppler ultrasound. J Ultrasound. 2015;18(2):101-107. doi:10.1007/s40477-014-0085-6
17. Mochtar H, Moualhil S Ben, Mohammedl C, Abdallah T Ben. Thrombose de la veine du greffon &al. Published online 2001:6-8.
18. Murphy BG, Doherty CC, Brown JH, et al. Increased renal allograft thrombosis in CAPD patients. Nephrol Dial Transplant. 1994;9(8):1166-1169. doi:10.1093/ndt/9.8.1166
19. Fananapazir G, McGahan JP, Corwin MT, et al. Screening for transplant renal artery stenosis: Ultrasound-based stenosis probability stratifcation. Am J
21. Baxter GM, Ireland H, Moss JG, et al. Colour Doppler ultrasound in renal transplant artery stenosis: Which Doppler index? Clin Radiol. 1995;50(9):618-622. doi:10.1016/S0009-9260(05)83291-X
22. Ardalan MR, Tarzamni MK, Shoja MM, et al. Black Tea Improves Endothelial Function in Renal Transplant Recipients. Transplant Proc. 2007;39(4):1139-1142. doi:10.1016/j.transproceed.2007.04.010
23. Luk SH, Chan JHM, Kwan TH, Tsui WC, Cheung YK, Yuen MK. Breath-hold 3D gadolinium-enhanced subtraction MRA in the detection of transplant renal artery stenosis. Clin Radiol. 1999;54(10):651-654. doi:10.1016/S0009-9260(99)91085-1 24. Brown ED, Michael •, Chen YM, Wolfman NT, Ott DJ, Watson NE. Complications
of Renal Transplantation: Evalu-ation with US and Ra-dionuclide Imaging 1 LEARNING OBJECTIVES FOR TEST 1. RadioGraphics. Published online 2000:607-622.
25. Middleton WD; Kellman GM; Melson GL; Madrazo. Post biopsy renal transplant arterio-venous fistulas color doppler US characteristics. Radiology.
1989;171(Apr):253–7.
26. Karam G, Maillet F, Braud G, et al. Complications chirurgicales de la transplantation rénale. Ann Urol (Paris). 2007;41(6):261-275. doi:10.1016/j.anuro.2007.08.007
27. Sebastià C, Quiroga S, Boyé R, Cantarell C, Fernandez-Planas M, Alvarez A. Helical CT in renal transplantation: Normal findings and early and late
complications. Radiographics. 2001;21(5):1103-1117.
30. Yap R, Madrazo B OH. Perirenal fluid collection after renal transplantation. Am
Surg. 1981;47:287–90.
31. Kumar S, Ameli-Renani S, Hakim A, Jeon JH, Shrivastava S, Patel U. Ureteral obstruction following renal transplantation: Causes, diagnosis and management. Br
J Radiol. 2014;87(1044). doi:10.1259/bjr.20140169
32. Bishop MC, Sherwood T, Evans DB CR. Vesicoureteric reflux after renal transplantation. Urol Radiol. 1980;(2):109–11.
33. Kyllönen L, Salmela K PE. Cancer incidence in a kidney-transplanted population.
Transpl Int. 2000;13(suppl1):S394–8.
34. Vasisth G, Kapoor A, Piercey K LS. Renal cell carcinoma in renal allograft Case series and review of literature. Urol Ann. 2018;10:229–232.
35. Evans C, Cochlin DL, Ferguson C, Griffin PJ SJ. Duplex doppler studies in acute renal transplant rejection. Transpl Proc. 1989;21:1897–901.