Prise en charge des exacerbations d'asthme
Texte intégral
Figure
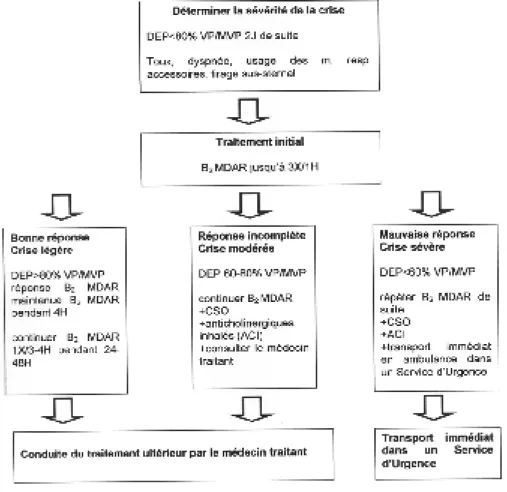
Documents relatifs
-La tolérance clinique des TDR conditionne la prise en charge et le premier traitement ainsi que le risque potentiel de complications premier traitement, ainsi que le risque
& groupe d'experts de la Société Suisse de Pneumologie Pédiatrique (SSPP) et de la Pediatric Emergency Medicine (PEM). AUGSBURGER, Florence,
L’utilisation des opioïdes doit être exceptionnelle à cause de la faible efficacité de la morphine dans les douleurs neuropathiques, de la grande fréquence des effets secondaires
Ce travail se propose d’analyser le profil épidémiologique et les modalités de prise en charge des patients asthmatiques adultes admis en exacerbation au Service
Il faut donc bien insister sur l’éducation du patient BPCO à la reconnaissance des signes d’EA BPCO pour que leur prise en charge ambulatoire soit la plus
Based upon work by Aeschbacher (1978) as well as comparative data from other ungulates, we predicted that male Alpine ibex should engage in at least 2 different mating tactics—one
At the final assessment (summer 2001/02), 66% of radio stations, both TV channels and 48% of newspapers reported UVR information in summertime weather reports.. Efforts to
c) Conversion des mesures fédérales en mesures m étriques.. Les sous-multiples sont le décimètre cube, le centimètre et le m illim ètre. Le mètre cube sert donc