HAL Id: dumas-01817520
https://dumas.ccsd.cnrs.fr/dumas-01817520
Submitted on 18 Jun 2018HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
dans le plasma par extraction en phase solide :
application à l’étude pharmacocinétique de la voie
rectale chez l’enfant
Sophie Veitl
To cite this version:
Sophie Veitl. Validation d’une méthode de dosage de la nalbuphine dans le plasma par extraction en phase solide : application à l’étude pharmacocinétique de la voie rectale chez l’enfant. Sciences pharmaceutiques. 1995. �dumas-01817520�
AVERTISSEMENT
Ce document est le fruit d'un long travail approuvé par le
jury de soutenance et mis à disposition de l'ensemble de la
communauté universitaire élargie.
Il n’a pas été réévalué depuis la date de soutenance.
Il est soumis à la propriété intellectuelle de l'auteur. Ceci
implique une obligation de citation et de référencement
lors de l’utilisation de ce document.
D’autre part, toute contrefaçon, plagiat, reproduction illicite
encourt une poursuite pénale.
Contact au SID de Grenoble :
bump-theses@univ-grenoble-alpes.fr
LIENS
LIENS
Code de la Propriété Intellectuelle. articles L 122. 4
Code de la Propriété Intellectuelle. articles L 335.2- L 335.10
http://www.cfcopies.com/juridique/droit-auteur---a
1ences Technologies MédecineU.F.R. de PHARMACIE
Domaine de la Merci - La TRONCHEANNEE: 1995
N° d'ORDRE :
1-o
'1
.9
V ALIDA TION D'UNE METHODE DE DOSAGE
DE LA NALBUPHINE DANS LE PLASMA
PAR EXTRACTION EN PHASE SOLIDE
(APPLICATION A L'ETUDE PHARMACOCINETIQUE DE LA VOIE RECTALE CHEZ L'ENFANT)
THESE
Présentée à l'Université Joseph FOURIER - GRENOBLE I pour obtenir le grade de :
DOCTEUR EN PHARMACIE
Par
Mademoiselle Sophie VEITL I
Cette thèse sera soutenue publiquement le 23 Novembre 1995 à 17h30. Devant: Monsieur le Professeur J. ROCHA T
Monsieur le Professeur G.BESSARD Madame le Docteur D. CANTIN-ESNAULT Madame le Docteur E. NICOLLE
Président du Jury Médecin Pharmacien Maître de Conférences Pharmacien Maître de Conférences [Données à caractère personnel]
UNIVERSITE Joseph FOURIER - GRENOBLE I
Sciences Technologies Médecine
U.F.R. de
PHARMACIE
Domaine de la Merci - La TRONCHEANNEE: 1995
N° d'ORDRE :
to
4
j
VALIDATION D'UNE METHODE DE DOSAGE
DE LA NALBUPHINE DANS LE PLASMA
PAR EXTRACTION EN PHASE SOLIDE
(APPLICATION A L'ETUDE PHARMACOCINETIQUE DE LA VOIE RECTALE CHEZ L'ENFANT)
THESE
Présentée à l'Université Joseph FOURIER - GRENOBLE I pour obtenir le grade de : DOCTEUR EN PHARMACIE
Par
Mademoiselle Sophie VEITL
Cette thèse sera soutenue publiquement le 23 Novembre 1995 à 17h30. Devant: Monsieur le Professeur J. ROCHA T
Monsieur le Professeur G.BESSARD Madame le Docteur D. CANTIN-ESNAULT Madame le Docteur E. NICOLLE
Président du Jury Médecin Pharmacien Maître de Conférences Pharmacien Maître de Conférences [Données à caractère personnel]
à
Monsieur J. ROCHAT, professeurà
la faculté de pharmacie de Grenoble, pour m'avoir fait l'honneur d'accepter de présider ce jury.à
Monsieur G. BESSARD, professeur à la faculté de médecine de Grenoble, chef de service du laboratoire de pharmacologie du C.H.U. de Grenoble, de m'avoir acceuillie dans son laboratoire, et d'avoir accepté de siéger dans ce jury. Qu'il trouve dans ce travail l'expression de ma reconnaisse et de mon profond respect.à
Madame D.CANTIN-ESNAUL T, maître de conférence au laboratoire de chimie analytique de la faculté de pharmacie de Grenoble, pour ces précieux conseils et pour avoir accepter de juger ce travail.à
Edwige NICOLLE, maître de conférence au laboratoire de chimie organique de la faculté de pharmacie de Grenoble, pour avoir rajouté un huitième jourà
ses semaines, afin de me diriger dans l'élaboration de cette thése. Qu'elle sache que j'ai pour elle une profonde reconnaissance et beaucoup d'amitié.à
Monsieur M.MALLARET, docteur en médecine, praticien hospitalier au laboratoire de pharmacologie du C.H.U. de Grenoble, pour sa disponibilitéà
répondreà
chacune de mes questions.à Madame F.SERRE-DEBEAUVAIS,docteur en pharmacie, praticien hospitalier au laboratoire de pharmacologie du C.H.U. de Grenoble, pour son aide dans l'elaboration de ce travail.
à
Madame J.BESSARD, attachée scientifique au laboratoire de pharmacologie du C.H.U. de Grenoble, pour les discussions très instructives que nous avons eu ensemble.à
Doriane età
Chantal, pour leur aide précieuse et leur disponibilité.à
ma soeur Anne, docteur en sciences politiques, pour s'être transformée pour l'occassion en secrétaire.à
Catherine GUIMIER, interne en pharmacie, pour avoir contribuéà
la réalisation de ce travail, avec patience et autres qualités qui ne pourront que lui servir dans la suite de ses études.
que tous ceux qui m'ont aidé et soutenu lors de la réalisation de ce travail, soit assurer de ma profonde sympathie.
à mes parents; qu'ils trouvent dans ce travail l'expression de ma reconnaissance et de l'amour que je leur porte.
à mes frères, à ma soeur et à leur famille; que l'avenir nous permette de nous voir plus souvent.
à tous mes amis, pour tous les instants de bonheur passés ensemble; qu'ils soient assurés de ma sincére et profonde amitié.
1
1
Page
[F)~A~MACOlOG~~ [))~~ MOfRi[F)~~N~QU~~
~î [))~
lA
~Al~U[F)~~N~
1s
1- STRUCTURE CHIMIQUE ET PROPRIETES
PHYSICO-CHIMIQUES DE LA NALBUPHINE 1 5 11-PHARMOCINETIQUE DE LA NALBUPHINE 18 1- Biodisponibilité 18 1-1- Définition 1 8 1-2- Biodisponibilité de la nalbuphine 19 2- Liaison protéique 19 2-1- Définition 1 9
2-2- Fixation protéique de la nalbuphine 20
3- Cinétique plasmatique 20
3-1- Temps de demi-vie 20
3-1-1- Définition 20
3-1-2- Demi-vie de la nalbuphine 21 3-1-3- Concentration plasmatique maximum 21 3-2- Clairance plasmatique 22
3-2-1- Définition 22
3-2-2- Clairance plasmatique de la nalbuphine 22
4- Distribution 23
4-1- Définition 23
4-2- Volume de distribution de la nalbuphine 23 4-3- Passage transplacentaire 23 4-4- Passage dans le lait maternel 24
5- Métabolisation 24
6- Elimination 24
Ill- LES RECEPTEURS MORPHINIQUES
26
1- Les différents types de récepteurs 27
2- Sites d'action des principaux morphiniques 30
IV- CLASSIFICATION CHIMIQUE ET PHARMACOLOGIQUE
DES MORPHINIQUES ET ANTIMORPHINIQUES 32
1- Classification chimique 32
1-1- Structure
à
cinq noyaux 321-1-1- La morphine 32
1-1-2- Les dérivés naturels et hémi-synthétiques 33 1-1-3- Les antagonistes 34 1-2- Structure à six noyaux 34 1-3- Structure
à
quatre noyaux 35 1-4- Structureà
trois noyaux 35 1-5- Structure à deux noyaux 36 1-6- Morphiniques dérivés de diamines 372- Classification pharmacologique 37
V- PROPRIETES PHARMACOLOGIQUE DES MORPHINIQUES 38
1- L'analgésie 38
1-1- Propriétés générales des morphiniques 38
1-2- Analgésie de la nalbuphine 41 1-2-1- Caractéristiques des agonistes-antagonistes 41 1-2-2- Analgésie de la nalbuphine 41
3
2- Action sur le système respiratoire 42
2-1- Propriétés générales des morphiniques 42 2-2- Propriétés de la nalbuphine 43
3- Action sur le système cardiovasculaire 45
3-1- Propriétés générales des morphiniques 45
3-2- Propriétés de la nalbuphine 45
4- Actions digestives 45
4-1- Propriétés générales des morphiniques 45
4-2- Propriétés de la nalbuphine 46
5- Actions psychoto-mimétiques 46
5-1- Propriétés générales des morphiniques 46
5-2- Propriétés de la nalbuphine 4 7
6- Somnolence et vertiges 4 7
7- Histaminolibération 47
8- Myosis 48
9- Actions hématologiques de la nalbuphine 48
10- Tolérance locale de la nalbuphine 48
VI- INDICATIONS DES MORPHINIQUES 49
1- Modalités de traitement 49
1-1- Choix de la voie d'administration 49
1-2- Intérêt de la voie rectale 50 1-3- Répartition des doses 51 1-4- Association de morphiniques 51
2- Problémes de dépendance psychologique, physique 51
et de tolérance
3-1-Douleurs post-opératoires 52 3-1-1-Propriétés générales des morphiniques 52 3-1-2-Propriétés de la nalbuphine 53 3-2-Prémédications et douleurs per-opératoires 54 3-2-1-Propriétés générales des morphiniques 54 3-2-2-Propriétés de la nalbuphine 54 3-3-Infarctus du myocarde 55 3-4-Douleurs obstréticales 56 3-5-Douleurs chroniques 57 3-6-Douleurs d'origine cancéreuse 58 3-7-Utilisation en pédiatrie 59 3-7-1-Les morphiniques 5 9 3-7-2-La nalbuphine 59
VII- CONTRE-INDICATIONS ET PRECAUTIONS D'EMPLOI DE LA NALBUPHINE
VIII- SURDOSAGE
IX- INTERACTIONS MEDICAMENTEUSES X- CONSERVATION
61
62 62 63
O AG~ ~
l
i-\
NAl~Uf)~~N~ f)ff ~ ~~î~ACî~ON
~N f)~A ~ ~Ol~ ~ ~î C~~OMAîOG~Af)~~~
l~QU~ ~ ~AUî~ f)~~ FO~MANC~
~î~Cî~ON
~l~C î~OC i N i QU ~ 64
1- TRAVAUX ANTERIEURS 11- RAPPELS TECHNIQUES
1
-L
'ex
trac
t
ion
en
phase
so
l
ide
1-1-Matériel utilisé
1-2-Les phases adsorbantes 1-3-L'interaction hydrophobe
64 67 67 67
68
68
5
1-4- L'échange d'ions 69 1-5- Avantages et inconvénients de l'extraction en phase solide 69
1-5-1- Avantages 69
1-5-2- Inconvénients
2- la chromatographie liquide haute performance
2-1- Schéma général 2-2- Le réservoir de solvant 2-3- Le système de pompage 2-4- Le solvant 2-5- Le système d'injection 2-6- La colonne
2-7- Les phases stationnaires
2-8- Les phénomènes mis en jeu dans la CLHP 2-8-1- La chromatogrrphie d'adsorption 2-8-2- La chromatographie de partage 70 70 71 71 72 72 72 73 73 73 74 75 2-8-3- La chromatographie sur gel ou d'exclusion-diffusion76 2-8-4- La chromatographie par échange d'ions 76 2-9- Les systémes de détection
2-10- Les systèmes d'enregistrement
3- l'électrochimie
3-1- Principe de la détection électrochimique 3-1-1- Les électrodes
3-1-2- Choix de la méthode de détection 3-1-3- La réaction d'oxydo-réduction 3-1-4- Choix du potentiel
3-2- Conditions particulières de l'utilisation du couplage CLHP-détection électrochimique
3-2-1- Le solvant d'extraction 3-2-2- Les systèmes de pompage
77
77
78 7879
80 81 81 83 83 84 3-3- Précautions diverses 84 3-4- Application du couplage CLHP-détection électrochimique 86 3-4-1- Groupes et structures chimiques électroactractives 86 3-4-2- Applicationsà
l'analyse de médicaments 86 3-4-3- Autres applications3-5- Intérêt de l'électrochimie
87 87
111- MISE AU POINT ET VALIDATION DE LA METHODE 88 1- Matériels et méthode 88 1-1- Matériels 88 1-2- Réactifs 8 8 1-3- Solvants 88 1-4- Solutions tampons 89 1-5- Prélèvements des échantillons 89 1-6- Préparation des solutions standard 89 1-7- Gamme d'étalonnage 90 1-8- Choix du standard interne 90
1-9- Patients 91
2- l'extraction en phase solide 94
2-1- Préparation de l'échantillon 94 2-2- Conditionnement de la colonne 94 2-3- Dépôt de l'échantillon 95 2-4- Rinçage 95 2-5- Elution 96 2-6- Evaporation 96
2-7- Reprise de l'extrait sec 96
3- La chromatographie liquide haute performance 97 3-1- Appareil de chromatographie 97 3-2- Conditions chromatographiques 97
4- L'électrochimie 98
5- Procédures de validation de la méthode 99
5-1- Spécificité 99
5-2- Linéarité et limite de linéarité 99
5-2-1- Définition 99
5-2-2- Estimation de la droite de régression linéaire 1 OO 5-2-3- Test de comparaison de l'ordonnée
à
l'origine avec0
1 OO 5-2-4- Test de l'homogénéité des variances(Test de Cochran) 101 5-2-5- Test de l'existence d'une pente significative 101
5-3- Exactitude 5-4- Fidélité 5-4-1- Définition 5-4-2- Répétabilité 5-4-3- Reproductibilité 5-5- Seuil de détection (SD) 5-5-1- Définition
7
5-5-2- Méthode de détermination 5-6- Seuil de qunatification (SQ) 5-7- Rendement 6- Résultats de la validation 6-1- Spécificité 6-2- Limite de linéarité 6-3- Exactitude 6-4- Fidélité 6-5- Seuil de détection 6-6- Seuil de quantification 6-7- Rendement6-8- Corrélations des méthodes d'extraction en phase solide et d'extraction liquide-liquide
102
102
102
103
103
103
103
104
104105
105
105107
110
111 112113
113117
119124
126Tableau 1: Principales substances dérivés par substitution de la morphine.
Tableau 2: Activités pharmacologiques de quelques morphiniques sur les récepteurs opioïdes.
Tableau 3: Comportements des morphiniques vis
à
vis des récepteurs opioïdes.Tableau 4: Activité analgésique et durée d'action de quelques morphiniques.
Tableau 5: Régies de prescription des opioïdes dans le traitement des douleurs d'origine cancéreuses.
Tableau 6: Techniques de dosage de la nalbuphine par C.L.H.P .. Tableau 7: Conditions chromatographiques utilisé par les différents
auteurs.
Tableau 8: Principaux composés electroactifs.
Tableau 9: Gamme d'étalonnage de Oà 50 ng/ml de plasma. Tableau 10: Linéarité de la méthode.
Tableau 11: Précision et exactitude de la méthode. Tableau 12: Fidélité de la méthode.
Tableau 13: Rendement d'extraction de la nalbuphine et de la naltrexone.
9
Figure 1: Structure de quelques mûrphiniques de la série des phénanthrénes.
Figure 2: Schéma de métabolisation de la nalbuphine selon LO et al .. Figure 3: Effet plafond de la buprénorphine sur la dépression
respiratoire.
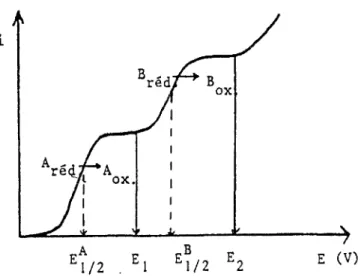
Figure 4: Schéma de principe de la détection électrochimique. Figure 5: Courbe i=f(E) de deux espéces A et B possédant des
valeurs E1/2 différentes.
Figure 6: Chromatogramme obtenu au potentiel E1. Figure 7: Chromatogramme obtenu au potentiel E2. Figure 8: Diagramme de FLEET.
Figure 9: Schéma du conditionnement des greffons de la colonne. Figure 10: Illustration du potentiel de demi-vague.
Figure 11: Plasma d'un patient traité par nalbuphine et surchargé par 40 ng/ml de naltrexone.
Figure 12: Chromatogramme d'un plasma de patient non traité. Figure 13: Chromatogramme d'un plasma surchargé par 1 O ng/ml de
naloxone (pic 1 ), 40 ng/ml de naltrexone (pic 2), 6 ng/ml de 6 monoacétylmorphine (pic 3), 1 O ng/ml de nalbuphine (pic 4). Figure 14: Rendement d'extraction de la nalbuphine
à
laFigure 15: Rendement d'extraction de la naltrexone à la concentration de 1 OO ng/ml selon le pH de dilution.
Figure
16:
Corrélation des méthodes d'extraction liquide-liquide et d'extraction en phase solide.Figure 17: Cinétique n°1
Figure 18: Cinétique n°2.
A.S.A.: American society of anesthesiologist.
C.l.H.P.: chromatographie liquide haute performance
C.l.H.P.-D.E.: C.L.H.P. couplée à la détection électrochimique Clp: clairance plasmatique
d.d.I.: degrés de liberté
D.E.: détection électrochimique D.S.: déviation standart
E: potentiel
E112: potentiel de demi-vague l.V.: intra-veineux
l.M.: intra-musculaire
l.M.A.O.: inhibiteur des mono amine oxydases
iprOH: isopropanol l.R.: intra-rectale
6 M.A.M.: 6 mono acétyl morphine Me OH: méthanol
Ks: coefficient de distribution
K's: facteur de capacité
1 1
O.M.S.: organisation mondiale de la santé S.C.: sous-cutané
S.D.: seuil de détection S.F.: soluton fille
S.I.: standart interne
S.M.: solution mère
S.P.E.: solide phase extraction (extraction en phase solide) S.Q.: seuil de quantification
T. R.: temps de rétention
1 2
La nalbuphine est un des analgésiques morphiniques qui offre le plus de sécurité, particulièrement chez l'enfant, où elle est utilisée en prémédication anesthésique (36), en anesthésie per-opératoire (31 ), et en analgésie post-opératoire (2) lors d'interventions chirurgicales. L'efficacité de la nalbuphine chez l'enfant après administration par voie intra-musculaire (IM) ou intra-veineuse (IV) a été montrée par DUVERGER et al., ainsi que par GAL Y et al. (27) (39). Plus récemment, BOYARD a montré que la voie rectale est une voie d'administration de la nalbuphine tout à fait adaptée à l'enfant (13). Toutefois, la pharmacocinétique de la nalbuphine administrée par cette voie n'a jamais été étudiée.
L'étude pharmacocinétique de la nalbuphine par voie rectale chez l'enfant nécessite le développement d'une technique analytique fiable, sensible et reproductible. La méthode de dosage adoptée devra en outre, être rapide et facile
à
utiliser, compte-tenu du nombre important d'échantillonsà
traiter au cours d'une journée.
De nombreux auteurs ont proposé des méthodes d'extraction et de dosage de la nalbuphine par chromatographie liquide haute performance (CLHP) couplée
à
une détection électrochimique ouà
la spectrophotométrie UV ou visible. Les méthodes d'extraction sont toutes des extractions liquide-liquide où de nombreux solvants plus ou moins nocifs sont utilisés. Ces techniques ne sont pas automatisables,à
l'inverse de l'extraction en phase solide, qui présente aussi d'autres avantages, tel que l'obtention d'extrait plus pur, mais qui n'a jusqu'à présent jamais été utilisée pour l'extraction de la nalbuphine.Le but de ce travail est donc de mettre au point et de valider une méthode d'extraction en phase solide de la nalbuphine qui sera ensuite dosée par CLHP couplée à une détection électrochimique. Ce travail permettra par la suite d'étudier la pharmacocinétique de la nalbuphine administrée par voie rectale, chez l'enfant.
Les résultats de la validation permettront de proposer une nouvelle technique d'extraction de la nalbuphine à partir du plasma, tout aussi performante que les techniques d'extractions liquide-liquide décrites dans la littérature, mais plus avantageuses car plus facile à réaliser.
Dans un deuxième temps, les concentrations expérimentales de nalbuphine obtenues permettront de connaître sa biodisponibilité lors de l'administration par voie rectale et donc d'ajuster au mieux la dose de nalbuphine à administrer. Cela permettra de savoir si les doses utilisées sont suffisantes pour obtenir une analgésie correcte et s'il
y
a lieu de réadministrer de la nalbuphine.Dans la première partie de ce travail, nous rappelerons les éléments de la pharmacocinétique des morphiniques, en général, et de la nalbuphine en particulier, en nous intéressant davantage à la voie rectale par rapport aux autres voies d'administration, ainsi qu'à l'utilisation de la nalbuphine en pédiatrie.
Dans une seconde partie, nous allons développer puis valider une nouvelle méthode d'extraction de la nalbuphine: extraction en phase solide. La séparation par chromatographie liquide haute performance et la détection électrochimique seront envisagées selon une technique récemment développée au laboratoire de pharmacologie du C.H.U. de Grenoble.
Dans une troisième partie, nous appliquerons cette nouvelle méthode à l'etude de la pharmacocinétique de la nalbuphine administrée par voie
1 4
rectale chez le petit enfant, qui représente une voie d'administration originale développée dans le service d'anesthésiologie et de réanimation du C.H.U. de Grenoble.
. JPIHIAJRJMLA\C(())JLO<GJIJE ]J))JES)
MOJRIPIHIJINJIQ lJJJES JET ]J))JE JLA
15
f ~~~M~COlO~~ [ ) ~ MO~f ~~~~Q~ ~
ET
[D)E lffe\
~ff ll ~f ~~~
1-STRUCTURE CHIMIQUE ET PROPRIETES PHYS ICO-CHIMIQUES DE LA NALBUPHINE(formule brute : C21 H27N04)
La nalbuphine est un morphinomimétique de type agoniste-antagoniste appartenant
à
la série des phénantrènes. Elle a été synthétisée en 1965. En 1971, ont eu lieu les premiers essais cliniques. Elle a été commercialisée en 1979 aux Etats-Unis, puis en Franceà
partir de 1988 sous le nom de NU BAIN®, antalgique injectable réservé à l'usage hospitalier, par la firme DUPONT PHARMA (16).La dénomination chimique de la nalbuphine est : chlohydrate de 17 -cyclobutyl méthyl-7,8 dihydro-14 -hydroxymorphine.
Par rapport à la morphine, la nalbuphine ne possède pas de double liaison en C7-Ca, mais possède deux groupements supplémentaires : un radical hydroxyle en C14 et un radical cyclobutylméthyle sur lachaine latérale portée par l'azote. Sa structure est proche de l'oxymorphine et de la naloxone. Les structures de quelques morphiniques sont présentées dans la figure 1, et le tableau 1 nous montre diverses structures dérivées de la morphine.
~
7
10 9
structure des phénantrènes
NALBUPHINE NALTREXONE Ho' 7 Morphine NALOXONE N-CH3 6-ACETYLMORPHINE
1 7
DCI C3 C6 Cl4 double liaison C7-C8
Morphine -OH -OH OUI
Nalbuphine -OH -OH -OH NON Naltrexone -OH =O -OH NON Naloxone -OH =O -OH NON Oxymorphine -OH =O -OH NON 6 MonoAcetylMorphine -OH -OCH3 OUI Codeine -OCH3 -OH OUI
Tableau 1: Principales substances dérivées par substitution de la morphine (17).
Le poids moléculaire de la nalbuphine est de 357. La nalbuphine est une base dont la liposolubilité est élevée. Le pH de la solution commerciale est situé entre 3,0 et 4,2. Le pKa du groupement phénol est de 9,96 et celui de l'ami ne est de 8, 71. Le pourcentage d'ionisation de la molécule au pH plasmatique (7,40) est inférieur à 10% (16).
La nalbuphine est commercialisée en ampoule injectable de 2 ml contenant 20 mg de principe actif sous forme de chlorhydrate dissout dans une solution aqueuse et acidifiée (acide citrique et acide chlorhydrique si besoin, pour obtenir un pH entre 3 et 4,2). Les conservateurs employés sont le métabisulfite de sodium et la parahydrobenzoate de méthyle et de propyle. De tels conservateurs rendent l'injection par voie péridurale ou intrathécale contre-indiquée.
11-PHARMACOCINETIQUE DE LA NALBUPHINE
La connaissance de la pharmacocinétique de la nalbuphine permet de comprendre comment celle-ci évolue dans l'organisme depuis son administration jusqu'à sa métabolisation et son élimination, et ainsi d'optimiser son utilisation.
1- Biodisponibilité (88)
1-1- Définition
La biodisponibilité (F) dépend de la fraction de la dose du médicament administré qui atteint la circulation générale et la vitesse à laquelle elle l'atteint.
Administrée par voie orale, la quantité de principe actif qui atteint la circulation générale va dépendre de la quantité absorbée par l'épithélium digestif, mais aussi de sa dégradation dans l'intestin par les sucs digestifs, de son métabolisme au niveau des entérocytes et surtout de l'effet de premier passage hépatique, correspondant au fait qu'une partie du principe actif est captée par les hépatocytes lorsque le médicament a une forte affinité pour les enzymes hépatiques.
Lorsque le captage hépatique est trop important, d'autres voies d'administration sont utilisées : la voie intra-veineuse (IV) qui amène directement le principe actif au niveau de la circulation sanguine, donnant une biodisponibilité de 100%, ou bien la voie intra-musculaire (IM) ou sous-cutanée(SC). D'autres voies non invasives sont également utilisables : la voie sublinguale, la voie transdermique par l'utilisation de patchs et la voie rectale par l'intermédiaire de suppositoires ou de lavements, qui est celle à laquelle nous nous intéresserons dans la suite de notre travail.
1 9
1-2- Biodisponibilité de la nalbuphine
Chez l'adulte jeune, la biodisponibilité par voie IM est de 80% et par voie SC de 75
à
80%. Les pics plasmatiques sont obtenus 30à
40 minutes après l'injection IM ou SC (6).Par voie orale, la biodisponibilité n'est plus que de 17%, en raison d'un effet de premier passage hépatique important (64). Mais cette biodisponibilité per os varie en fonction de l'âge du patient. JAILLON et al. ont
montré qu'elle passe de 12% chez le sujet jeune,
à
près de 46% chez le sujet de plus de 65 ans, ceci en raison d'un flux sanguin hépatique moindre chez la personne âgée. Le délai d'apparition du pic plasmatique après administration par voie orale est de 54 à 72 minutes chez l'adulte jeune et il est de 96 minutes chez le sujet âgé (50). Du fait de la mauvaise biodisponibilité par voie orale, la nalbuphine n'est pas commercialisée sous cette forme.2- Liaison protéique 2-1- Définition (88)
La fixation aux protéines plasmatiques s'exprime sous forme de fraction fixée ou pourcentage de fixation :
concentration en médicament fixé f ==
---concentration totale en médicament
La fixation aux protéines plasmatiques dépend de trois facteurs : - le nombre de sites de fixation disponibles au niveau des
proteines plasmatiques.
- la constante d'affinité Ka qui définit la force de la liaison.
En pratique, la fixation protéique n'est
à
prendre en considération que si elle est élevée, c'est-à-dire supérieure à 90%, et si le médicament a une marge thérapeutique étroite.2-2- Fixation protéigue de la nalbuphine
Elle est de 25 à 50% (6). Cette valeur de fixation protéique est considérée comme faible et n'a donc pas d'incidence sur la pharmacocinétique de la nalbuphine.
3- Cinétigue plasmatigue
3-1- Temps de demi-vie
3-1-1- Définition (88)
Le temps de demi-vie (T 112) est le temps nécessaire pour que les concentrations diminuent de moitié pendant la phase d'élimination.
On montre qu'il faut quatre demi-vies pour que 95% du médicament soit éliminés. Il faudra donc, lors de l'étude cinétique d'un médicament, effectuer des prélèvements sur une période égale à quatre demi-vies, au moins.
2 1
3-1-2- Demi-vie de la nalbuphine
Après injection IV, la nalbuphine se distribue selon un modèle bicompartimental selon JAILLON et al .. On décrit deux phases de décroissance des concentrations au cours du temps. La première est appelée : phase
a
pour laquelle on détermine un temps de demi-viea
correspondant. La deuxième phase de décroissance, plus lente, est la phase Bà
laquelle correspond le temps de demi-vie B. JAILLON et al. montrent qu'il n'existe pas de différence significative pour le T 112a
en fonction de l'âge. Ce temps de demi-viea
est de 8,4 à 12 min. Par contre le T 112 B varie selon l'âge, puisqu'il est de 54 min chez l'enfant, de 114 min chez l'adulte jeune et de 138 min chez le sujet âgé.Les temps de demi-vies
B
trouvés par JAILLON et al. sont en accord avec ceux que LO et al. avaient précédemment déterminés (50)(64).Après injection IM ou SC, la nalbuphine se distribue aussi selon un modèle bicompartimental. Ceci est également le cas lors de l'administration per os (1 ).
Récemment, le T 112 plasmatique chez le nouveau-né de mères traitées par le NUBAIN® (IM ou IV) au cours de l'accouchement a été estimé à 4,1
±
2,7 h (72).3-1-3- Concentration plasmatique maximum
Après injection IM d'une dose de 1 O mg de nalbuphine, la concentration plasmatique maximum (Cmax) est de 30 à 50 ng/ml (64).
Après administration per os d'une dose de 60 mg, la concentration plasmatique maximum est de 20 ng/ml (1 ).
3-2- Clairance plasmatique
3-2-1- Définition
La clairance plasmatique (Clp) d'un médicament est le volume de plasma totalement épuré du médicament par unité de temps. Il existe plusieurs voies d'épuration : le foie, le rein ou encore la voie pulmonaire, salivaire ou lacrymale. La valeur de la clairance plasmatique correspond à la somme des clairances de chaque organe (clairance hépatique, rénale, clairance biliaire ... ).
La valeur de la clairance plasmatique est influencée par le débit sanguin et la fixation protéique. Si la fixation protéique est faible, l'extraction par le foie ou le rein est forte, la clairance est alors limitée par le flux sanguin. A l'inverse, en cas de fixation protéique forte, l'extraction par l'organe donc la clairance du médicament va dépendre non plus du flux sanguin de l'organe, mais de la fraction non liée aux protéines.
3-2-2- Clairance plasmatique de la nalbuphine
La fixation protéique de la nalbuphine étant faible, la clairance plasmatique est proche du débit sanguin hépatique.
La valeur de la clairance de la nalbuphine diminue avec l'âge. Elle est de 2,7 l/kg/h chez l'enfant, de 1,78 l/kg/h chez l'adulte jeune et de 1,41 l/kg/h chez l'adulte âgé (50).
23
4-Distribution4-1- Définition
Le volume apparent de distribution (Vd B) est le volume qu'occuperait le fluide étudié (le plasma) si le médicament était réparti de façon homogène dans l'organisme à la fin de la phase de distribution.
Ce volume peut donc être supérieur au volume corporel total.
En effet, la quantité de médicament dans l'organisme est égale
à
la quantité de médicament dans le plasmaà
laquelle s'ajoute la quantité de médicament dans les tissus.4-2- Volume de distribution de la nalbuphine
Après injection IV, le volume de distribution est de 5 l/kg chez l'individu sain (64). Chez les malades, au cours de l'anesthésie générale, il n'est plus que de 2,5 l/kg (86). Chez l'enfant, le volume de distribution est de 3,6 l/kg et chez la femme enceinte,
à
terme, de 2 l/kg (98).La nalbuphine a une distribution tissulaire importante. On la retrouve dans le cerveau au niveau des couches profondes du cortex, de la substance grise périaqueducale, des noyaux thalamiques et de la substance gélatineuse du trijumeau et dans la substance gélatineuse spinale (23).
4-3-Passage transplacentaire
La nalbuphine passe facilement et rapidement la barrière placentaire. Le rapport foeto-maternel des concentrations plasmatiques est élevé : 0,3
à
6 (98) (21 ). Récemment, ce rapport a été évaluéà
0,74±
0,20 (72).4-4-Passage dans le lait maternel
La nalbuphine passe également dans le lait maternel, mais à de très faibles concentrations (25). WILSON et al. ont estimé que 0,01 % de la dose administrée
à
la mère se retrouve dans le lait (98).5-Métabolisme
Le métabolisme de la nalbuphine est hépatique. La nalbuphine est principalement glucuronoconjuguée soit directement, soit après hydroxylation et oxydation du groupement cyclobutyl porté par l'azote (25) (Figure 2).
Le dérivé glucuronoconjugué inactif de la nalbuphine est le métabolite principal. Les hydroxylations et les oxydations au niveau du groupe cyclobutyl aboutissent à diverses métabolites dans les proportions suivantes : 3% de M1, 8% de M2, 1 % de M3, 3% de M4, 23% de MS, 2% de M6 et 7% de M7 (6).
6-Elimination
La nalbuphine et ses métabolites sont éliminés principalement par les fèces et de façon minoritaire dans les urines.
Après extraction biliaire, l'élimination est fécale pour 93% du médicament et 7% seulement se retrouvent dans les urines (28). JASINSKI a étudié le métabolisme de la nalbuphine chez l'homme et a mis en évidence, dans les urines, de la nalbuphine inchangée ainsi que des dérivés sulfo et glucuro-conjugués (52).
NH
Noroxymorphine
0
N-(hydroxy-céto-cyclobuty l)-méthylnornalbuphine (M5))
--25
R: glucuronide, sulfateN C~
0N C~
',,
Nalbuphinel
HO Nalbuphine-N-oxydée 0 N-CH2-0
- ',
._+-rœ
-N-(hydroxy-cyclobuty l)-méthylnornalbuphine(M1. M2, M3, M4, My)
HO
N-(céto-cyclobuty l)-méthylnornalbuphine (M6)
Sept heures après administration de nalbuphine, 80
à
90 % du principe actif seront éliminés (25). Il n'existe pas de données sur l'élimination de la nalbuphine chez les sujets ayant des insuffisances rénales ou hépatiques.111-LES RECEPTEURS MORPHINIQUES
Pour provoquer leurs divers effets, souhaités ou indésirables, les morphiniques agissent par l'intermédiaire de récepteurs que nous allons étudier dans ce chapitre.
Ces récepteurs ont été mis en évidence en 1971 (43). La liaison entre le morphinique et le récepteur est une liaison :
- spécifique, stéréospécifique, - réversible,
- saturable, d'où un nombre limité de récepteurs,
- dont l'affinité est en général élevée, permettant
à
de faibles quantités de principes actifs de provoquer des effets. La puissance de l'affinité conditionne la puissance d'action des morphiniques.Ces récepteurs morphiniques sont situés dans différentes régions du système nerveux central. Ils participent
à
l'analgésie ainsi qu'aux autres actions pharmacologiques provoquées par les morphiniques (17).27
1- Les différents types de récepteurs
De nombreux auteurs ont proposé une classification des récepteurs morphiniques. Nous allons voir l'évolution de cette classification au cours du temps.
En 1976, MARTIN et al. proposent une classification en 3 types de récepteurs (chez le chien spinal):
- les récepteurs µ dont l'agoniste est la morphine,
- les récepteurs K dont les agonistes sont la nalorphine et les benzomorphanes.
- les récepteurs cr dont l'agoniste est le SKF 10047 (N-allyl-normétazocine).
La diprénorphine est un antagoniste de ces trois types de récepteurs.
A chaque type de récepteurs correspond une activité pharmacologique propre :
- les récepteurs µ entraîneraient l'analgésie, la dépression respiratoire, le myosis, l'indifférence, l'euphorie, les phénomènes de tolérance et de dépendance.
- les récepteurs K seraient responsables de l'analgésie, la sédation, la dépendance et la tolérance de façon non croisée avec celle induite par les récepteurs µ.
- les récepteurs cr produiraient les hallucinations, les dysphories, l'agitation et les réactions maniaques, correspondant aux effets psychomoteurs des morphiniques (68).
En 1977, LORD et al. isolent deux types de récepteurs sur des organes isolés et classent les morphiniques selon leur affinité pour l'un ou l'autredes récepteurs :
-les
récep
teurs
µ, situés au niveau de l'iléon de cobaye et pour lesquels les morphiniques suivants ont une forte affinité : la morphine, la 13-endorphine, la naloxone, la diprénorphine.-les
récep
teurs
~ situés au niveau du canal déférent de la souris. La13-endorphine et les enképhalines présentent une forte affinité pour ce type de récepteurs. De plus ces ~ sont antagonisés par ladiprénorphine.
-les
récep
teurs
e situés au niveau du canal déférent du rat.LORD et al. montrent dans leur étude que les récepteursµet~ se
trouvent situés également au niveau du système nerveux central (65).
En fait, en 1976, PERT et al.avaient proposé une classification en
récep
teurs
de
type
1
etrécep
teurs
de
type
Il. Cette classification recouvre celle de MARTIN et al. et celle de LORD et al. En effet pour PERT et al., les récepteurs de type1correspondent aux récepteurs µ et K de laclassificatipon de MARTIN et al., et les récepteurs de type Il correspondent aux ~ de la classification de LORD et al. et aux récepteurs cr de la
classification de MARTIN et al..
Cette classification en deux types de récepteurs semble toutefois insuffisante, certains morphiniques, tel que la brémazocine, étant agonistes sélectifs des récepteurs K, et donc difficiles à classer dans le type1puisque
29
En
1989,
CHAUVIN et al. proposent une classification en six types de récepteurs :- les récepteurs µ, situés principalement au niveau du tronc cérébral et de la moelle. Leur activation entraîne des symptômes déjà décrits par MARTIN et al., c'est-à-dire l'analgésie, le myosis, la dépression respiratoire, l'indifférence, l'euphorie, les phénomènes de tolérance et de dépendance, auxquels ARNOULD ajoute la sédation (6).
- les récepteurs K, situés principalement au niveau de la moelle, sont responsables de l'analgésie, de la sédation, du myosis, de la bradycardie et de l'hypotension.
- les récepteurs O', situés essentiellement au niveau du sytème limbique, provoquent lors de leur activation des phénomènes d'hallucination, de dysphorie, ainsi qu'une mydriase et une tachycardie.
- les récepteurs /1 qui interagissent avec les récepteurs µ pour en moduler leurs effets.
- les récepteurs
e
n'ont pas d'effets connus.-les récepteurs
y
sont des récepteurs non spécifiques des morphiniques. Leur activation entraîne des effets psychiques chez les patients (16).Pour certains de ces récepteurs, plusieurs sous-types ont été mis en évidence.
De nombreuses études ont permis de montrer qu'il existe plusieurs sous-types de récepteurs Kappa: K1, K2, K3 (101)(81). Des études plus approfondies permettent à KOSTERLITZ, en
1981,
de montrer que le récepteur K1 a comme agoniste le U 50,488H, et comme antagoniste spécifique le NORBNI (56).En 1988, ZUKIN et al. étudient le récepteur K2, sans parvenir
à
connaître clairement sa pharmacologie (105). Enfin, CLARK, en 1989, ainsi que d'autres auteurs mettent en évidence le récepteur K3, que l'on trouve dans le cerveau,
à
une concentration deux fois plus forte que les récepteursµ ou A (19).En 1990, ESCHALLIER distingue cinq classes de récepteurs, avec deux sous-classes de récepteursµ: µ1 et µ2 (29).
2- Sites d'action des principaux morphinigues
La morphine et les agonistes morphinomimétiques tels que la codéine, le dextropropoxyphène, la méthadone, l'étorphine ou encore le kétazocine sont des agonistes préférentiels des récepteurs µ. La morphine possède, en outre, une action agoniste sur les récepteurs K.
La buprénorphine est un agoniste partiel des récepteurs µ et un antagoniste K.
La nalorphine et la pentazocine sont des agonistes des récepteurs K et sont des antagonistes des récepteursµ.
La nalbuphine qui nous intéresse tout particulièrement dans ce travail a un effet antagoniste des récepteurs µ et A, et un effet agoniste K (16). Elle a une action agoniste partielle au niveau des récepteurs cr (80).
Le tableau 2 résume les activités pharmacologiques de quelques morphiniques et indique le type de récepteurs impliqués dans ces effets.
Récepteurs µ ~ K î
Légende:
+:agoniste
antagoniste
+/-:
agoniste-partiel
Actions Sites pharmacologiques principaux Analgésie tronc sédation cérébral dépression respiratoire euphorie myosis déoendancemodulent les effets dus à l'activation des récepteus µ analgésie moelle sedation bradycardie myosis hypotension système hallucinations limbique dysphorie mydriase tachycardie
Classe des Classe des Classe agonistes Agonistes- agonistes
partiels
morohine Buorénorphine Nalbuohine
+
+ /-
-+
-
+
+ /
-Tableau 2: Activités pharmacologiques de quelques morphiniques sur les récepteurs opioïdes.
des Classe des antagonistes antagonistes
Nalorphine Naloxone
-
Récemment, CHAIM et al. ont mis en évidence que parmi les 3 sous-types de récepteurs K, la nalbuphine avait non seulement une très haute affinité pour les récepteurs K1 et K2, mais que ces deux sous-types de récepteurs avaient un rôle aussi important l'un que l'autre dans la production de l'analgésie par l'intermédiaire d'intéractions complexes. Ces auteurs ont également montré que la sensibilité des récepteurs µ et K
à
l'analgésie est vraisemblablement sous la dépendance d'un facteur génétique (15).IV-CLASSIFICATION CHIMIQUE ET PHARMOCOLOGIQUE DES
MORPHINIQUES ET DES ANTIMORPHINIQUES
Les morphiniques peuvent être classés selon leur structure chimique ou selon leurs effets pharmacologiques.
1- Classification chimigue (17)
1-1- Structure à 5 noyaux
1-1-1- La morphine
Morphine
La molécule de morphine a une structure pentacyclique dont un noyau phénantrénique. Elle comporte une fonction alcool en CG, une en C3 et une
33
double liaison en C7-Ca. Certains constituants de la molécule de morphine sont indispensables pour permettre les actions sur le SNC et, en particulier, l'analgésie :
- les isomères lévogyres sont responsables d'une analgésie plus importante,
- le cycle pipéridinique est indispensable pour que l'analgésie ait lieu, - le radical phénolique a un rôle sur l'intensité des actions dépressives centrales,
- la fonction énolique intervient dans les effets de stimulation centrale de la morphine, notamment l'action émétisante,
- la suppression de la double liaison en C3-C4 renforce l'analgésie et les effets dépresseurs centraux,
- la structure a-phényl, N-méthyl pipéridine, ou une structure très proche, est indispensable
à
l'activité analgésique.1-1-2- Dérivés naturels et hémi-synthétigues
Ce sont:
- la codéine et la codéthyline : obtenues par estérification de la fonction phénol en C3,
- la thébaïne : obtenue par estérification des fonctions phénol en C3 et alcool en CG,
- l'héroïne : obtenue par acétylation des fonctions phénol en C3 et alcool en CG,
- la dihydromorphine et la dihydrocodéine : obtenues par hydrogénation de la double liaison C7-Ca de la morphine et de la codéine,
-l'oxymorphone et l'oxycodone : obtenues par hydroxylation de la dihydromorphinone et de la dihydrocodéinone en C14,
1-1-3- Les antagonistes
Par substitution de la molécule de morphine, on synthétise des molécules ayant une activité antagoniste.
La nalorphine, à activité agoniste-antagoniste, est obtenue par substitution du groupe méthyle par un groupe allyle sur l'azote de la morphine.
La nalbuphine, agoniste-antagoniste, est synthétisée
à
partir de l'oxymorphoneLa naloxone, antagoniste pur, dérive également de l'oxymorphone. 1-2- Structure
à
6 noyauxParmi les dérivés morphiniques
à
6 noyaux, on trouve :- l'étorphine et l'oripavine qui sont tous deux des agonistes dont l'activité représente 5 000
à
1 O 000 fois celle de la morphine,- la diprénorphine, molécule ayant l'activité antagoniste la plus puissante,
- la buprénorphine, à activité agoniste-antagoniste.
µ43
.
~
_ L{lHJ)J
I· 1Ho
H
OH
Structure de la buprénorphine.35
1-3- Structure à 4 noyaux
Les morphiniques ne possédant que 4 noyaux après suppression du cycle lactonique appartiennent au groupe des morphinanes dont la structure générale est la suivante :
N-H
Ce sont des produits de synthèse pure. Parmi les morphinanes, on trouve : - le lévallorphan,
- le cyclorphan, - le butorphanol,
Tous les trois ont des propriétés antagonistes.
1-4- Structure
à
3 noyauxIls appartiennent au groupe des benzomorphanes parmi lesquels on trouve:
- la phénazocine, agoniste dix fois plus puissante que la morphine, - la cyclazocine,
à
activité antagoniste.1-5- Structure
à
2 noyauxParmi les morphiniques
à
2 noyaux, on peut différencier plusieurs groupes:- le groupe des 4-phényl pipéridines dont la structure générale est la suivante :
- le groupe de la péthidine dont la formule est la suivante :
- le groupe des diphényl-propylamines alcooliques,
- le groupe des diphényl-propylamines amidiques parmi lesquels on trouve le dextromoramide.
37
1-6- Morphiniques dérivés de diamines
La structure de ces molécules différa totalement de la structure de la morphine et leur activité est très supérieure à celle de la morphine.
Le fentanyl, l'alfentanil et le sulfentanil appartiennent à ce groupe de molécules.
Structure du fentanyl 2- Classification pharmacologique
Selon leur comportement au niveau des récepteurs opioïdes, on peut classer les morphiniques en quatre groupes :
- les agonistes purs, ayant une forte affinité pour les récepteurs. Ce sont entre autres la morphine, la codéine, l'oxycodone, l'étorphine, la péthidine.
- les agonistes partiels qui possèdent une affinité plus faible et un effet plafond dans l'analgésie, l'augmentation de la dose de ces molécules n'entraînant pas une augmentation de l'analgésie. Citons la buprénorphine, le propiran, le profadol.
- les agonistes-antagonistes qui ont une activité agoniste au niveau de certains récepteurs et une activité antagoniste au niveau d'autres
récepteurs, tels que la nalbuphine, la nalorphine, la pentazocine, le butorphanol.
- les antagonistes purs qui sont des antagonistes compétitifs des récepteurs morphiniques, tels que la naloxone, la naltrexone, la diprénorphine, le lévallorphan.
Le tableau 3 présente l'activité de divers morphiniques au niveau des récepteurs opioïdes.
V-PROPRIETES PHARMACOLOGIQUES DES MORPHINIQUES
1- L'analgésie
1-1- Propriétés générales des morphiniques
Les morphiniques élèvent le seuil de perception de la douleur. Ils agissent
à
différents niveaux sur la transmission du message nociceptif. Dans le tableau 4 , on compare l'activité analgésique des différents morphiniques et la durée de l'analgésie après administration systémique (29).La puissance analgésique d'un produit correspond au rapport des doses équianalgésiques: morphine/produit. Par exemple, la puissance analgésique de la buprénorphine est de 10, ce qui correspond au fait que 10 mg de morphine et 1 mg de buprénorphine produisent la même analgésie.
Tableau N° 3 Comportement des morphiniques vis àvis des récepteurs opioïdes (29)
AGONISTES AGONISTES PARTIELS AGONISTE-ANTAGONISTES ANTAGONISTES PURS
MIXTES
Morphine Bu prénorphine Nalbuphine Naloxone
Codéine Propiran Nalorphine Naltrexone
Oxycodone Profadol Pentazocine Di prénorphine
Etorphine Bu torphanol Levallorphane
Levorphanol Ketazocine Péthidine Fentanyl Alf entanil Méthadone
Dextromoramide Dextropropoxyphène Phénopéridine
Tableau n° 4 Activité analgésique et durée d'action de quelques morphiniques (29)
OCI Nom Commercial Puissance Durée
Analgesiq ue d'action Heures
Morphine MOSCONTIN
1
4
à5
Nalbuphine NUBAIN
1
2,5
à5
Dextropropoxyphéne ANTAL VIC
1/15
à1/5
4
à6
Pethidine DO LOS AL
1/10
à1/15
2
à4
Pentazocine FORT AL
1/6
à1/3
3
à4
Dextromoramide PALFIUM
1
à2
3
à4
Methadone
1
à3
8
à12
B uprénorphine TEMGESIC
10
à30
6
à8
Fen tan y 1 FENTANYL-JANSSEN
100
à500
0,5
Alfentanyl RAPIFEN 7 fois >
fentanyl
41
1-2- Analgésie de la nalbuphine
1-2-1- Caractéristiques des agonistes-antagonistes
Les agonistes-antagonistes ont la particularité de posséder un effet plafond, ou effet plateau, qui correspond au fait que l'effet analgésique du médicament n'augmente plus même si on continue d'augmenter les doses. Par contre, d'autres effets tels que les troubles psychiques, les nausées ou les vomissements peuvent augmenter proportionnellement à la dose et ne présentent donc pas d'effet plafond (17). Cet effet plafond limite l'utilisation des agonistes-antagonistes.
D'autre part, les agonistes-antagonistes ont la propriété d'être antagonistes quand ils sont administrés après qu 'une substance agoniste ait été injectée. Cette propriété permettra d'antagoniser par exemple la dépression respiratoire induite par les agonistes morphiniques, mais elle va
aussi diminuer l'analgésie produite par ceux-ci. Aussi, la nalbuphine ne pourra être utilisée comme antagoniste morphinique. L'antagoniste morphinique classiquement utilisé en cas de dépression respiratoire est la naloxone (NARCAN®), antagoniste pur.
1-2-2- Analgésie de la nalbuphine
La puissance analgésique de la nalbuphine est égale à 1 (tableau 4). L'effet plafond apparaît à partir d'une dose de 0,3 à 0,5 mg/kg de nalbuphine, ce qui correspond à une concentration plasmatique de 20 ng/ml (37). L'analgésie apparaît en 2
à
3 min après une administration IV (37) et dure pendant 2,5à
4 heures (92)(47). Après administration en SC ou IM,l'analgésie apparaît en 15
à
20 min (37) et persiste 3à
4 heures (9). L'effet maximum est obtenu en 30 min si l'injection est intraveineuse et 60 min lorsque l'injection est SC ou IM (9).En
présence de morphiniques,
la nalbuphine lève partiellement l'analgésie et provoque une tachycardie et une augmentation de la tension artérielle mais ceci n'est pas observé dans tous les cas (10)(91 ). En effet, si la nalbuphine est administrée en présence d'un morphinique dont l'effet résiduel est inférieurà
l'effet plafond, l'analgésie est renforcée (38). Par contre, si l'effet résiduel est supérieur à l'effet plafond, l'analgésie sera diminuée.De part son activité agoniste-antagoniste, la nalbuphine comme la naloxone entraîne chez les morphinomanes, un symptôme de sevrage (76). De la même façon, on peut observer un symptôme de sevrage chez le nouveau-né pour les femmes toxicomanes.
2- Actions sur le système respiratoire
2-1- Propriétés générales des morphiniques
Les morphiniques provoquent trois types de symptômes au niveau du système respiratoire :
- la dépression respiratoire, - la rigidité thoracique, - le bronchospasme.
La
dépression respiratoire
provoquée est dose-dépendante. Elle atteint surtout la fréquence respiratoire, par augmentation de la pause43
expiratoire, sans modification du temps inspiratoire, mais avec augmentation compensatrice du volume courant (17). Au delà d'une certaine dose administrée, la bradycardie devient très importante et le volume courant diminue, jusqu'à l'apparition d'une apnée. Ce phénomène est observé avec tous les morphiniques, mis
à
part les agonistes-antagonistes tels que lanalbuphine.
La rigidité thoracique est due à une hypertonie musculaire que l'on observe uniquement à fortes doses. Elle est décrite surtout pour le fentanyl. On limitera cette rigidité musculaire en administrant lentement les morphiniques.
Le bronchospasme est en relation avec l'histaminolibération et une contraction des muscles lisses bronchiques. Ce phénomène sera à prendre en considération lors de l'utilisation de morphiniques chez l'asthmatique, en particulier, et chez tous les insuffisants respiratoires, en général.
2-2- Propriétés de la nalbuphine
Du fait de son activité agoniste-antagoniste, la dépression respiratoire observée lors de l'administration de nalbuphine présente, comme pour l'analgésie, un effet plafond à partir de 0,3
à
0,5 mg/kg (37). Cet effet plafond représente un facteur de sécurité dans l'utilisation de la nalbuphine par rapportà
un autre analgésique morphinique. La figure 3 illustre l'effet plafond sur la dépression respiratoire obtenu après administration de buprénorphine, agoniste partiel, possédant comme les agonistes-antagonistes un effet-plafond sur la dépression respiratoire. De plus, la dépression respiratoire provoquée peut au besoin être antagonisée par la naloxone (37)(85).fréquence respiratoire/min 17
~
16 151
14 13 12 11 l 10 -r-2 4 8 16 32. mg de buprénorphine Figure 3: Effet plafond de la buprénorphine sur la dépressionrespiratoire chez l'homme (95).
Si l'effet plafond représente une sécurité dans l'utilisation de la nalbuphine, cela n'est pas toujours le cas lorsque la nalbuphine est administrée chez un insuffisant respiratoire ou lors de l'association
à
un autre médicament dépresseur du système respiratoire tel qu'une benzodiazépine.En présence de morphiniques, la nalbuphine lève la dépression respiratoire induite par ceux-ci, mais son action est 40 fois moins puissante que celle de la naloxone (8). Comme pour l'analgésie, l'action de la nalbuphine sur la dépression respiratoire dépend du morphinique et de son effet résiduel. Si l'effet résiduel est inférieur
à
l'effet plafond de la nalbuphine, la dépression respiratoire est aggravée; par contre, si l'effet résiduel est supérieur à l'effet plafond, la dépression respiratoire diminue (7)(37)(38).On pourra quelquefois observer une dépression respiratoire secondaire apparaissant 30 min
à
4 heures après l'administration de la nalbuphine (104).45
3- Action sur le système cardiovasculaire
3-1- Propriétés générales des morphiniques
Les morphiniques provoquent une vasodilatation artériolaire et veineuse qui entraîne une hypotension orthostatique. Celle-ci pourra être aggravée par l'existence d'une bradycardie.
3-2- Propriétés de la nalbuphine
La nalbuphine n'entraîne quasiment pas de modifications hémodynamiques (85), même au cours d'anesthésie générale avec des doses importantes de 3 mg/kg (58)(103). La nalbuphine est de ce fait indiquée chez les malades présentant une insuffisance cardiaque ou coronarienne, ainsi que dans le traitement des douleurs de l'infarctus du myocarde, même si l'on observe une faible diminution de la fréquence cardiaque et une élévation modérée des résistances périphériques (61 ).
4- Actions digestives
4-i- Propriétés générales des morphiniques
Les morphiniques peuvent provoquer des nausées et des vomissements, par stimulation de la chemoreceptor trigger zone (CTZ) de l'area postrema. Des doses supérieures de morphiniques peuvent également inhiber nausées et vomissements (29).
Il existe aussi une action sur les fibres musculaires lisses qui seront à l'origine de l'utilisation des morphiniques comme antidiarrhéique, notamment le lopéramide et le diphénoxylate qui sont des produits de synthèse.
L'effet sur la musculature lisse peut être responsable de coliques hépatiques par action sur les voies biliaires, nécessitant l'administration de spasmolytiques en association avec la morphine (29).
4-2- Propriétés de la nalbuphine
La nalbuphine peut également provoquer des nausées et des vomissements (77). Elle agit également sur les fibres musculaires lisses, mais d'une façon moins importante que la morphine. Le transit intestinal est peu modifié par la nalbuphine et on n'observe pas d'augmentation de pression au niveau des voies biliaires (67). Sa faible action sur les musculatures lisses digestive et urinaire la rend intéressante pour le traitement des douleurs coliques hépatiques et des coliques néphrétiques (6).
5- Actions psychoto-mimétigues
5-1- Propriétés générales des morphiniques
Les morphiniques peuvent entraîner un état de dysphorie, des angoisses, une désorientation ainsi que des bourdonnements d'oreilles et des hallucinations.
47
5-2- Propriétés de la nalbuphine
Chez moins de 10% des patients, on observe des réactions psychoto-mimétiques modérées telles que: confusions, agitation et/ou hallucinations.
6- Somnolences et vertiges
A doses équiactives, les agonistes purs provoquent une sédation moins importante que les agonistes-antagonistes qui entraînent également des vertiges, une sensation ébrieuse, une difficulté à se concentrer et des sueurs (82).
La somnolence induite par la nalbuphine apparaît dès la dose de 0, 15 mg/kg (82) et elle est dépendante de la dose administrée. A partir d'une dose de 1 mg/kg, l'action de la nalbuphine est plus proche de celle d'un barbiturique que d'un morphinique (51 ).
7- Histaminolibération
Lors d'une étude chez le chien, MULDOON et al. ont montré que la nalbuphine, pour des doses de 0,3 à 3 mg/kg, ne provoque pas de libération d'histamine,
à
l'inverse de la morphine qui, pour des doses de 3 mg/kg entraîne une augmentation nette du taux plasmatique d'histamine, avec diminution de la pression artérielle moyenne (70 ).Chez l'homme, FAHMY et al. ont constaté également que l'administration de 0,3 mg/kg en IV de morphine provoque une libération d'histamine. Cet effet n'est pas observé lors de l'administration de 0,6 mg/kg en IV de nalbuphine (32).
Comme pour la morphine, la péthidine et le dextromoramide créent une histaminolibération à forte dose. A l'inverse, le fentanyl, comme la nalbuphine n'est pas histaminolibérateur (32).
8- Myosis
Les morphiniques provoquent un myosis. Le myosis induit par une dose de 8 mg/kg de nalbuphine est similaire à celui induit par 10 mg/kg de morphine (59). Le myosis apparaît dès la dose de 0, 1 mg/kg de nalbuphine.
9- Actions hématologiques de la nalbuphine
La nalbuphine ne perturbe pas la formule sanguine,
à
l'inverse de certaines classes thérapeutiques d'antalgiques (noramidopyrine, acide acétylsalicylique par exemple).La nalbuphine est dénuée d'effet anti-inflammatoire et elle ne perturbe pas les facteurs de la coagulation, n'entraînant aucun risque de saignement. L'absence de risque hémorragique permet son utilisation même en cas d'ulcère gastro-duodénal.
10- Tolérance locale de la nalbuphine
Lors d'une étude chez des volontaires sains, LASSETER a montré que l'injection IV, IM ou SC de 1 O mg de nalbuphine provoque une irritation
49
cutanée légère et fugace au site d'injection pour 4 sujets sur 37 et que l'injection de 20 mg de nalbuphine provoque le même type d'irritation cutanée chez 6 sujets sur 36. On peut donc considérer que la nalbuphine présente une bonne tolérance locale (60).
VI- INDICATIONS DES MORPHINIQUES
Les morphiniques présentent de nombreuses indications. On a recours aux morphiniques quand la douleur n'est pas calmée par les analgésiques de stade 1, c'est-à-dire les analgésiques périphériques. Les morphiniques sont classés au stade Il pour les moins puissants (codéine, dextropropoxyphène) et au stade Ill pour les plus puissants tels que la morphine, la buprénorphine, la nalbuphine, la pentazocine ou encore le dextromoramide.
1- Modalités de traitement
1-1 Choix de la voie d'administration
Dans la mesure du possible, on utilisera la voie orale sous forme de sirop ou de comprimés. Mais selon le type de morphinique, la biodisponiblité per os peut être très faible et on a recours à une autre voie d'administration : les voies sublinguale ou rectale qui sont comme la voie orale des voies non invasives, ou les voies IM, SC ou IV qui sont des voies invasives. La rapidité
d'action souhaitée du morphinique va aussi influencer le choix de la voie d'administration.
Lors de l'accouchement ou en chirurgie, on pourra utiliser la voie médullaire (péridurale ou intrathécale). De même, lors de douleurs néoplasiques intenses, la voie médullaire pourra être utilisée.
Les voies d'administration sont donc le plus souvent des voies invasives permettant de réduire les doses puisque la biodisponibilité des voies IM ou SC est meilleure que celle de la voie orale.
Si les injections doivent se répéter, on peut placer un cathéter central relié à une pompe implantée en sous-cutanée, qui permet la délivrance régulière du morphinique.
1-2-lnterêt de la voie rectale
L'administration de médicaments par l'intermédiaire de suppositoires ou de lavements est facilement réalisable et présente de nombreux avantages. Le premier avantage est que la voie rectale n'est pas une voie d'administration invasive. Elle est donc mieux accepter, surtout par l'enfant.
L'absorption du médicament n'est pas tributaire d'éventuels troubles digestifs que l'on rencontre souvent chez le malade. Les risques d'intolérance digestive dus au médicament, ainsi que les risques de dégradation enzymatiques par les enzymes digestives sont nuls. Le médicament ne subit que partiellement l'effet de premier passage hépatique, ce qui est intéréssant dans le cas de la nalbuphine pour qui cet effet de premier passage hépatique est important.
La voie rectale présente néanmoins un certain nombre d'inconvénients. L'absorption de médicaments au niveau de la muqueuse
5 1
rectale dépend de la taille des particules, du volume de la solution, ainsi que d'une variation individuelle. Le rejet du lavement parfois observé est un des inconvénients de la voie rectale, de même que l'apparition de signes d'irritation locale (83).
1-3- Répartition des doses
On tiendra compte du fait que :
- l'administration en continu à doses faibles ou à intervalles réguliers, calculés selon le temps de demi-vie du morphinique utilisé, sera toujours préférée
à
une administrationà
la demande.- pour chaque morphinique, il existe une dose efficace qui devra être respectée pour que, d'une part, l'analgésie procurée soit suffisante et que, d'autre part, les effets indérisables ne soient pas trop importants (effets dose-dépendants)
1-4- Associations de morphiniques
Ces associations ne sont pas justifiées. Par contre, l'association de morphiniques avec des analgésiques périphériques tels que l'aspirine ou le paracétamol, peut s'avérer très intéressante.
2- Problémes de dépendance psychologique. physique et de tolérance.
L'O.M.S. définit la pharmacodépendance comme un " état psychique et quelquefois également physique résultant de l'intéraction entre un organisme vivant et un médicament, se caractérisant par des modifications du